Esteroide anabólico
| Esteroides anabólicos androgénicos | |
|---|---|
| Clase de droga | |
 Estructura química del AAS natural testosterona (androst-4-en-17β-ol-3-ona). | |
| Identificadores de clase | |
| Sinónimos | Esteroides anabólicos; Andrógenos |
| Usar | Varios |
| Código ATC | A14A |
| Objetivo biológico | Receptor de andrógenos (AR) |
| Clase química | Esteroides ; Androstanos ; Estranos |
| Datos clínicos | |
| Drogas.com | Clases de drogas |
| Enlaces externos | |
| Malla | D045165 |
| Estatus legal | |
| Estatus legal | |
| En Wikidata | |
Los esteroides anabólicos , también conocidos como esteroides anabólico-androgénicos (EAA), son una clase de fármacos que están estructuralmente relacionados con la testosterona , la principal hormona sexual masculina , y producen efectos al unirse al receptor de andrógenos (AR). Los esteroides anabólicos tienen varios usos médicos, [1] pero también los usan los atletas para aumentar el tamaño muscular, la fuerza y el rendimiento.
Los riesgos para la salud pueden producirse por el uso a largo plazo o dosis excesivas de AAS. [2] [3] Estos efectos incluyen cambios nocivos en los niveles de colesterol (aumento de lipoproteínas de baja densidad y disminución de lipoproteínas de alta densidad ), acné , presión arterial alta , daño hepático (principalmente con la mayoría de los AAS orales) e hipertrofia ventricular izquierda . [4] Estos riesgos aumentan aún más cuando los atletas toman esteroides junto con otras drogas, lo que causa significativamente más daño a sus cuerpos. [5] El efecto de los esteroides anabólicos en el corazón puede causar infarto de miocardio y accidentes cerebrovasculares . [5] Las afecciones relacionadas con los desequilibrios hormonales , como la ginecomastia y la reducción del tamaño testicular, también pueden ser causadas por AAS. [6] En mujeres y niños, los AAS pueden causar masculinización irreversible . [6]
Los usos ergogénicos de los AAS en los deportes, las carreras y el culturismo como drogas para mejorar el rendimiento son controvertidos debido a sus efectos adversos y al potencial de obtener ventajas en las competiciones físicas. Su uso se conoce como dopaje y está prohibido por la mayoría de los organismos deportivos importantes. Los atletas han estado buscando drogas para mejorar sus habilidades atléticas desde que comenzaron los Juegos Olímpicos en la Antigua Grecia. [5] Durante muchos años, los AAS han sido, con mucho, las sustancias dopantes más detectadas en los laboratorios acreditados por el COI . [7] [8] Los esteroides anabólicos están clasificados como sustancias controladas de la Lista III en muchos países, [9] lo que significa que los AAS tienen un uso médico reconocido, pero también se reconoce que tienen un potencial de abuso y dependencia, lo que lleva a su regulación y control. En los países donde los AAS son sustancias controladas , a menudo existe un mercado negro en el que se venden a los usuarios medicamentos de contrabando, fabricados clandestinamente o incluso falsificados .
Usos
Médico

Desde el descubrimiento y la síntesis de la testosterona en la década de 1930, los médicos han utilizado los esteroides anabólicos para diversos fines, con distintos grados de éxito. Estos pueden agruparse en general en usos anabólicos, androgénicos y otros.
Anabólico
- Estimulación de la médula ósea : Durante décadas, los EAA fueron el pilar de la terapia para anemias hipoplásicas debidas a leucemia , insuficiencia renal o anemia aplásica . [10]
- Estimulación del crecimiento : los endocrinólogos pediátricos pueden utilizar los AAS para tratar a niños con retraso del crecimiento . [11] Sin embargo, la disponibilidad de la hormona de crecimiento sintética , que tiene menos efectos secundarios, hace que este sea un tratamiento secundario. [ cita médica necesaria ]
- Estimulación del apetito y conservación y aumento de la masa muscular : Se han administrado AAS a personas con enfermedades crónicas degenerativas como el cáncer y el SIDA . [12] [13]
- Estimulación de la masa corporal magra y prevención de la pérdida ósea en hombres de edad avanzada, como indican algunos estudios. [14] [15] [16] Sin embargo, un ensayo controlado con placebo de 2006 de suplementación con testosterona en dosis bajas en hombres de edad avanzada con niveles bajos de testosterona no encontró ningún beneficio en la composición corporal, el rendimiento físico, la sensibilidad a la insulina o la calidad de vida . [17]
- Prevención o tratamiento de la osteoporosis en mujeres posmenopáusicas . [18] [19] El decanoato de nandrolona está aprobado para este uso. [20] Aunque se han indicado para esta indicación, los AAS se han utilizado muy poco para este propósito debido a sus efectos secundarios virilizantes. [18] [21]
- Ayuda a aumentar de peso después de una cirugía o un trauma físico , durante una infección crónica o en el contexto de una pérdida de peso inexplicable . [22] [23]
- Contrarrestar el efecto catabólico de la terapia con corticosteroides a largo plazo . [22] [23]
- La oxandrolona mejora los resultados a corto y largo plazo en personas que se recuperan de quemaduras graves y está bien establecida como un tratamiento seguro para esta indicación. [24] [25]
- Tratamiento de la baja estatura idiopática , el angioedema hereditario , la hepatitis alcohólica y el hipogonadismo . [26] [27]
- La metiltestosterona se utiliza en el tratamiento de la pubertad tardía , el hipogonadismo , la criptorquidia y la disfunción eréctil en los hombres, y en dosis bajas para tratar los síntomas de la menopausia (específicamente para la osteoporosis , los sofocos y para aumentar la libido y la energía ), el dolor y la congestión mamaria posparto y el cáncer de mama en las mujeres. [28] [29] [30]
- Las hormonas de crecimiento utilizadas en medicina veterinaria (por ejemplo, acetato de trembolona ) también se utilizan en la cría intensiva de animales para obtener ganancias más rápidas de masa muscular para obtener mayores rendimientos de carne del ganado y una mayor producción de leche en la industria láctea . [31]
Androgénico
- La terapia de reemplazo de andrógenos para hombres con niveles bajos de testosterona, como los asociados con hipogonadismo de aparición tardía ; [32] también es eficaz para mejorar la libido en hombres de edad avanzada. [33] [34] [35] [36]
- Inducción de la pubertad masculina: a muchos niños que sufren un retraso extremo de la pubertad se les administran andrógenos . La testosterona es hoy en día casi el único andrógeno que se utiliza con este fin y se ha demostrado que aumenta la altura, el peso y la masa libre de grasa en niños con pubertad tardía. [37]
- Terapia hormonal masculinizante para hombres transgénero , otras personas transmasculinas y personas intersexuales , al producir características sexuales secundarias masculinas como voz más grave , aumento de la masa ósea y muscular, distribución de grasa masculina , vello facial y corporal y agrandamiento del clítoris , así como cambios mentales como alivio de la disforia de género y aumento del deseo sexual. [38] [39] [40] [41] [42]
Otro
- Tratamiento del cáncer de mama en mujeres, aunque actualmente se utilizan muy raramente con este fin debido a sus marcados efectos secundarios virilizantes. [43] [18] [44]
- En dosis bajas como componente de la terapia hormonal para mujeres posmenopáusicas y transgénero , por ejemplo para aumentar la energía , el bienestar , la libido y la calidad de vida , así como para reducir los sofocos . [45] [46] [47] [48] La testosterona se utiliza generalmente para este propósito, aunque también se utiliza metiltestosterona . [48] [49]
- Anticoncepción hormonal masculina ; actualmente experimental, pero con potencial para usarse como anticonceptivo masculino eficaz, seguro, confiable y reversible. [50]
- Auxiliar en el tratamiento del fenómeno de Raynaud y la acrocianosis periférica . La testosterona y otros anabólicos tienden a ser potentes vasodilatadores , lo que puede mejorar significativamente el flujo sanguíneo en individuos propensos a la vasoconstricción. [51]
Mejorar el rendimiento

La mayoría de los usuarios de esteroides no son deportistas. [52] En Estados Unidos, se cree que entre 1 y 3 millones de personas (1% de la población) han utilizado esteroides anabólicos. [53] Estudios realizados en Estados Unidos han demostrado que los usuarios de esteroides anabólicos tienden a ser en su mayoría hombres de clase media con una edad media de unos 25 años que son culturistas no competitivos y no deportistas y utilizan las drogas con fines cosméticos. [54] "Entre los chicos de 12 a 17 años, el uso de esteroides y drogas similares aumentó un 25 por ciento entre 1999 y 2000, y el 20 por ciento dijo que las utiliza por estética más que por deporte, según un estudio de la aseguradora Blue Cross Blue Shield". [55] Otro estudio encontró que el uso no médico de esteroides anabólicos entre los estudiantes universitarios era igual o inferior al 1%. [56] Según una encuesta reciente, el 78,4% de los usuarios de esteroides eran culturistas no competitivos y no atletas, mientras que alrededor del 13% informó prácticas de inyección inseguras, como reutilizar agujas, compartir agujas y compartir viales multidosis, [57] aunque un estudio de 2007 encontró que compartir agujas era extremadamente poco común entre las personas que usaban AAS para fines no médicos, menos del 1%. [58] Otro estudio de 2007 encontró que el 74% de los usuarios de AAS no médicos tenían títulos postsecundarios y más habían completado la universidad y menos no habían terminado la escuela secundaria de lo que se espera de la población general. [58] El mismo estudio encontró que las personas que usaban AAS para fines no médicos tenían una tasa de empleo más alta y un ingreso familiar más alto que la población general. [58] Los usuarios de AAS tienden a investigar las drogas que están tomando más que otros usuarios de sustancias controladas; [ cita requerida ] Sin embargo, las principales fuentes consultadas por los usuarios de esteroides incluyen amigos, manuales no médicos, foros en Internet, blogs y revistas de fitness, que pueden proporcionar información cuestionable o inexacta. [59]
Los usuarios de AAS tienden a estar descontentos con la representación de los AAS como mortales en los medios y en la política. [60] Según un estudio, los usuarios de AAS también desconfían de sus médicos y en la muestra el 56% no había revelado su uso de AAS a sus médicos. [61] Otro estudio de 2007 tuvo hallazgos similares, mostrando que, mientras que el 66% de las personas que usaban AAS para fines no médicos estaban dispuestas a buscar supervisión médica para su uso de esteroides, el 58% no confiaba en sus médicos, el 92% sentía que el conocimiento de la comunidad médica sobre el uso no médico de AAS era deficiente, y el 99% sentía que el público tiene una visión exagerada de los efectos secundarios del uso de AAS. [58] Un estudio reciente también ha demostrado que los usuarios de AAS a largo plazo tenían más probabilidades de tener síntomas de dismorfia muscular y también mostraron un respaldo más fuerte a los roles masculinos más convencionales. [62] Un estudio reciente en el Journal of Health Psychology mostró que muchos usuarios creían que los esteroides utilizados con moderación eran seguros. [63]
Los esteroides anabólicos han sido utilizados por hombres y mujeres en muchos tipos diferentes de deportes profesionales para lograr una ventaja competitiva o para ayudar en la recuperación de lesiones. Estos deportes incluyen el culturismo , el levantamiento de pesas , el lanzamiento de peso y otras disciplinas de atletismo , el ciclismo , el béisbol , la lucha libre , las artes marciales mixtas , el boxeo , el fútbol y el cricket . Dicho uso está prohibido por las reglas de los organismos rectores de la mayoría de los deportes. El uso de esteroides anabólicos ocurre entre adolescentes, especialmente entre aquellos que participan en deportes competitivos. Se ha sugerido que la prevalencia de uso entre estudiantes de secundaria en los EE. UU. puede ser tan alta como 2.7%. [64]
Dosis
| Medicamento | Ruta | Rango de dosis [a] | ||
|---|---|---|---|---|
| Danazol | Oral | 100–800 mg/día | ||
| Propionato de drostanolona | Inyección | 100 mg 3 veces/semana | ||
| Etilestrenol | Oral | 2–8 mg/día | ||
| Fluoximesterona | Oral | 2–40 mg/día | ||
| Mesterolona | Oral | 25–150 mg/día | ||
| Metandienona | Oral | 2,5–15 mg/día | ||
| Acetato de metenolona | Oral | 10–150 mg/día | ||
| Enantato de metenolona | Inyección | 25–100 mg/semana | ||
| Metiltestosterona | Oral | 1,5–200 mg/día | ||
| Decanoato de nandrolona | Inyección | 12,5–200 mg/semana [b] | ||
| Fenilpropionato de nandrolona | Inyección | 6,25–200 mg/semana [b] | ||
| Noretandrolona | Oral | 20–30 mg/día | ||
| Oxandrolona | Oral | 2,5–20 mg/día | ||
| Oximetolona | Oral | 1–5 mg/kg/día o 50–150 mg/día | ||
| Estanozolol | Oral | 2–6 mg/día | ||
| Inyección | 50 mg hasta cada dos semanas | |||
| Testosterona | Oral [c] | 400–800 mg/día [b] | ||
| Inyección | 25–100 mg hasta tres veces por semana | |||
| Cipionato de testosterona | Inyección | 50–400 mg cada cuatro semanas | ||
| Enantato de testosterona | Inyección | 50–400 mg cada cuatro semanas | ||
| Propionato de testosterona | Inyección | 25–50 mg hasta tres veces por semana | ||
| Undecanoato de testosterona | Oral | 80–240 mg/día [b] | ||
| Inyección | 750–1000 mg cada 10 semanas | |||
| Trenbolona HBC | Inyección | 75 mg cada 10 días | ||
Fuentes: [65] [66] [67] [68] [18] [69] [70] [71] [72] [73]
| ||||
Formularios disponibles
Los AAS que se han utilizado más comúnmente en medicina son la testosterona y sus muchos ésteres (pero más típicamente el undecanoato de testosterona , el enantato de testosterona , el cipionato de testosterona y el propionato de testosterona ), [74] los ésteres de nandrolona (típicamente el decanoato de nandrolona y el fenilpropionato de nandrolona ), el estanozolol y la metandienona (metandrostenolona). [75] Otros que también han estado disponibles y se han utilizado comúnmente pero en menor medida incluyen la metiltestosterona , la oxandrolona , la mesterolona y la oximetolona , así como el propionato de drostanolona (propionato de dromostanolona), los ésteres de metenolona (metilandrostenolona) (específicamente el acetato de metenolona y el enantato de metenolona ) y la fluoximesterona . [75] La dihidrotestosterona (DHT), conocida como androstanolona o estanolona cuando se usa con fines médicos, y sus ésteres también son notables, aunque no se usan ampliamente en medicina. [70] El undecilenato de boldenona y el acetato de trembolona se utilizan en medicina veterinaria . [75]
Los esteroides de diseño son AAS que no han sido aprobados ni comercializados para uso médico, pero se han distribuido a través del mercado negro. [76] Algunos ejemplos de esteroides de diseño notables incluyen 1-testosterona (dihidroboldenona), metasterona , enantato de trembolona , desoximetiltestosterona , tetrahidrogestrinona y metilstenbolona . [76]
Vías de administración

Existen cuatro formas comunes en las que se administran los AAS: píldoras orales; esteroides inyectables; cremas/geles para aplicación tópica; y parches cutáneos. La administración oral es la más conveniente. La testosterona administrada por vía oral se absorbe rápidamente, pero se convierte en gran parte en metabolitos inactivos, y solo alrededor de una sexta parte está disponible en forma activa. Para que sean suficientemente activos cuando se administran por vía oral, los derivados de la testosterona se alquilan en la posición 17α, por ejemplo, la metiltestosterona y la fluoximesterona . Esta modificación reduce la capacidad del hígado para descomponer estos compuestos antes de que lleguen a la circulación sistémica.
La testosterona se puede administrar por vía parenteral , pero tiene un tiempo de absorción prolongado más irregular y una mayor actividad en el músculo en forma de enantato , undecanoato o éster cipionato . Estos derivados se hidrolizan para liberar testosterona libre en el sitio de la inyección; la tasa de absorción (y, por lo tanto, el programa de inyección) varía entre diferentes ésteres, pero las inyecciones médicas normalmente se realizan en cualquier momento entre quincenalmente y una vez cada 12 semanas. Puede ser deseable un programa más frecuente para mantener un nivel más constante de hormona en el sistema. [77] Los esteroides inyectables generalmente se administran en el músculo, no en la vena, para evitar cambios repentinos en la cantidad del fármaco en el torrente sanguíneo. Además, debido a que la testosterona esterificada se disuelve en aceite, la inyección intravenosa tiene el potencial de causar una embolia peligrosa (coágulo) en el torrente sanguíneo.
También se pueden utilizar parches transdérmicos (parches adhesivos que se colocan sobre la piel) para administrar una dosis constante a través de la piel y hacia el torrente sanguíneo. También existen cremas y geles que contienen testosterona que se aplican diariamente sobre la piel, pero la absorción es ineficiente (aproximadamente el 10%, que varía de una persona a otra) y estos tratamientos tienden a ser más caros. Las personas que son especialmente activas físicamente y/o se bañan a menudo pueden no ser buenos candidatos, ya que el medicamento se puede lavar y puede tardar hasta seis horas en absorberse por completo. También existe el riesgo de que una pareja íntima o un niño entren en contacto con el lugar de aplicación y se administren la dosis inadvertidamente; los niños y las mujeres son muy sensibles a la testosterona y pueden desarrollar masculinización no deseada y efectos sobre la salud, incluso con pequeñas dosis. La inyección es el método más común utilizado por las personas que administran esteroides anabólicos con fines no médicos. [58]
Las vías tradicionales de administración no tienen efectos diferenciales sobre la eficacia del fármaco. Los estudios indican que las propiedades anabólicas de los AAS son relativamente similares a pesar de las diferencias en los principios farmacocinéticos, como el metabolismo de primer paso . Sin embargo, las formas orales de AAS pueden causar daño hepático en dosis altas. [8] [78]
Efectos adversos
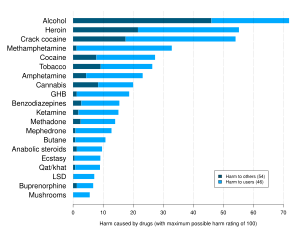
Los posibles efectos secundarios conocidos de los AAS incluyen: [6] [80] [81] [82] [83]
- Dermatológicas / tegumentales : piel grasa , acné vulgar , acné conglobata , seborrea , estrías (debido al rápido agrandamiento de los músculos ), hipertricosis (crecimiento excesivo de vello corporal), alopecia androgénica (pérdida de cabello en patrón; calvicie del cuero cabelludo), retención de líquidos / edema .
- Reproductivo / endocrino : alteraciones de la libido , infertilidad reversible , hipogonadismo hipogonadotrópico .
- Específico para varones: erecciones espontáneas , emisiones nocturnas , priapismo , disfunción eréctil , ginecomastia (en su mayoría sólo con AAS aromatizables y, por lo tanto, estrogénicos ), oligospermia / azoospermia , atrofia testicular , leiomiosarcoma intratesticular , hipertrofia de próstata , cáncer de próstata .
- Específicos de la mujer: masculinización , profundización irreversible de la voz , hirsutismo (crecimiento excesivo de vello facial y corporal), alteraciones menstruales (p. ej., anovulación , oligomenorrea , amenorrea , dismenorrea ), agrandamiento del clítoris , atrofia mamaria , atrofia uterina , teratogenicidad (en fetos femeninos ).
- Específicos de los niños: cierre epifisario prematuro y baja estatura asociada , pubertad precoz en niños, pubertad tardía y precocidad contrasexual en niñas.
- Psiquiátrico / neurológico : cambios de humor , irritabilidad , agresión , comportamiento violento , impulsividad / imprudencia , hipomanía / manía , euforia , depresión , ansiedad , disforia , suicidio , delirios , psicosis , abstinencia , dependencia , neurotoxicidad , deterioro cognitivo . [84] [85]
- Musculoesquelético : hipertrofia muscular , distensiones musculares , roturas de tendones , rabdomiólisis .
- Cardiovascular : dislipidemia (p. ej., aumento de LDLInformación sobre herramientas sobre lipoproteínas de baja densidadniveles, disminución de HDLInformación sobre herramientas sobre lipoproteínas de alta densidadniveles, apo-A1 reducidaInformación sobre herramientas sobre apolipoproteína A1niveles), aterosclerosis , hematocrito elevado , hipertensión , hipertrofia ventricular izquierda , miocardiopatía , hipertrofia miocárdica , policitemia / eritrocitosis , arritmias , trombosis (p. ej., embolia , accidente cerebrovascular ), infarto de miocardio , muerte súbita . [86] [87]
- Hepático : pruebas de función hepática elevadas ( ASTInformación sobre herramientas sobre aspartato aminotransferasa, ALTInformación sobre herramientas sobre alanina aminotransferasa, bilirrubina , LDHInformación sobre herramientas sobre la deshidrogenasa láctica, ALPInformación sobre herramientas sobre fosfatasa alcalina), hepatotoxicidad , ictericia , esteatosis hepática , adenoma hepatocelular , carcinoma hepatocelular , colestasis , peliosis hepática ; todos ellos mayoritariamente o exclusivamente con AAS 17α-alquilados. [88]
- Renal : hipertrofia renal , nefropatía , insuficiencia renal aguda (secundaria a rabdomiólisis), glomeruloesclerosis focal y segmentaria , carcinoma de células renales .
- Otros: intolerancia a la glucosa , resistencia a la insulina , disfunción inmunológica . [89]
Fisiológico
Dependiendo de la duración del uso de la droga, existe la posibilidad de que el sistema inmunológico se dañe. La mayoría de estos efectos secundarios dependen de la dosis, siendo el más común la presión arterial elevada, especialmente en aquellos con hipertensión preexistente . [90] Además de los cambios morfológicos del corazón que pueden tener un efecto adverso permanente en la eficiencia cardiovascular.
Se ha demostrado que los AAS alteran los niveles de azúcar en sangre en ayunas y las pruebas de tolerancia a la glucosa. [91] Los AAS como la testosterona también aumentan el riesgo de enfermedad cardiovascular [2] o enfermedad de la arteria coronaria . [92] [93] El acné es bastante común entre los usuarios de AAS, principalmente debido a la estimulación de las glándulas sebáceas por el aumento de los niveles de testosterona. [7] [94] La conversión de testosterona a DHT puede acelerar la tasa de calvicie prematura en los hombres genéticamente predispuestos, pero la testosterona en sí misma puede producir calvicie en las mujeres. [95]
El uso de esteroides anabólicos en adolescentes puede provocar una serie de efectos secundarios graves. Por ejemplo, los esteroides anabólicos pueden detener prematuramente el alargamiento de los huesos ( fusión epifisaria prematura a través del aumento de los niveles de metabolitos de estrógeno ), lo que da lugar a un retraso del crecimiento . Otros efectos incluyen, entre otros, la maduración ósea acelerada , el aumento de la frecuencia y duración de las erecciones y el desarrollo sexual prematuro. El uso de esteroides anabólicos en la adolescencia también se correlaciona con actitudes más pobres en relación con la salud. [96]
Cáncer
La Agencia Internacional para la Investigación sobre el Cáncer (IARC) de la Organización Mundial de la Salud incluye los AAS en el Grupo 2A : Probablemente cancerígenos para los seres humanos. [97]
Cardiovascular
Otros efectos secundarios pueden incluir alteraciones en la estructura del corazón , como agrandamiento y engrosamiento del ventrículo izquierdo , lo que altera su contracción y relajación , y por lo tanto reduce el volumen de sangre eyectada. [4] Los posibles efectos de estas alteraciones en el corazón son hipertensión, arritmias cardíacas , insuficiencia cardíaca congestiva , ataques cardíacos y muerte cardíaca súbita . [98] Estos cambios también se observan en atletas que no consumen drogas , pero el uso de esteroides puede acelerar este proceso. [99] [100] Sin embargo, tanto la conexión entre los cambios en la estructura del ventrículo izquierdo y la disminución de la función cardíaca, como la conexión con el uso de esteroides han sido cuestionadas. [101] [102]
El uso de AAS puede causar cambios perjudiciales en los niveles de colesterol : algunos esteroides causan un aumento del colesterol LDL y una disminución del colesterol HDL . [103]
Defectos de crecimiento
El uso de AAS en adolescentes acelera la maduración ósea y puede reducir la estatura adulta en dosis altas. [ cita requerida ] Se utilizan dosis bajas de AAS como la oxandrolona en el tratamiento de la baja estatura idiopática , pero esto solo puede acelerar la maduración en lugar de aumentar la estatura adulta. [104]
Feminización
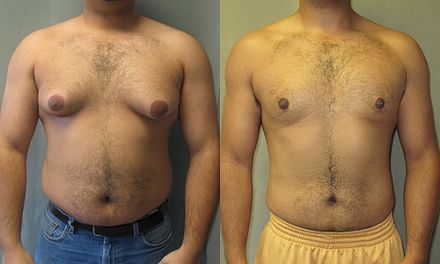
Aunque todos los esteroides anabólicos tienen efectos androgénicos , algunos de ellos paradójicamente resultan en feminización, como el tejido mamario en los hombres, una condición llamada ginecomastia . Estos efectos secundarios son causados por la conversión natural de testosterona en estrógeno y estradiol por la acción de la enzima aromatasa , codificada por el gen CYP19A1 . [105]
El uso prolongado de esteroides androgénicos-anabólicos por parte de los hombres da como resultado el cierre temporal de su producción natural de testosterona debido a una inhibición del eje hipotálamo-hipofisario-gonadal . Esto se manifiesta en atrofia testicular , inhibición de la producción de esperma , función sexual e infertilidad . [106] [107] [108] Un uso corto (1-2 meses) de esteroides androgénicos-anabólicos por parte de los hombres seguido de un ciclo de terapia para aumentar la testosterona (por ejemplo, clomifeno y gonadotropina coriónica humana ) generalmente da como resultado el retorno a la producción normal de testosterona. [109] )
Masculinización
Los efectos secundarios específicos de las mujeres incluyen aumento del vello corporal , profundización permanente de la voz, agrandamiento del clítoris y disminución temporal de los ciclos menstruales . También pueden producirse alteraciones de la fertilidad y quistes ováricos en las mujeres. [110] Cuando se toman durante el embarazo, los AAS pueden afectar el desarrollo fetal al provocar el desarrollo de características masculinas en el feto femenino y características femeninas en el feto masculino. [111]
Problemas renales
Los análisis renales revelaron que nueve de los diez usuarios de esteroides desarrollaron una afección llamada glomeruloesclerosis focal y segmentaria , un tipo de cicatrización en los riñones. El daño renal en los culturistas tiene similitudes con el que se observa en pacientes con obesidad mórbida, pero parece ser incluso más grave. [112]
Problemas de hígado
Las dosis altas de compuestos AAS orales pueden causar daño hepático . [3] La peliosis hepática se ha reconocido cada vez más con el uso de AAS.
Neurosiquiátrico

Una revisión de 2005 en CNS Drugs determinó que "síntomas psiquiátricos significativos que incluyen agresión y violencia, manía y, con menor frecuencia, psicosis y suicidio se han asociado con el abuso de esteroides . Los abusadores de esteroides a largo plazo pueden desarrollar síntomas de dependencia y abstinencia al suspender los AAS". [85] Las altas concentraciones de AAS, comparables a las que probablemente sufren muchos usuarios recreativos de AAS, producen efectos apoptóticos en las neuronas , [ cita requerida ] planteando el espectro de una posible neurotoxicidad irreversible. El uso recreativo de AAS parece estar asociado con una variedad de efectos psiquiátricos potencialmente prolongados, incluidos síndromes de dependencia, trastornos del estado de ánimo y progresión a otras formas de consumo de sustancias, pero la prevalencia y la gravedad de estos diversos efectos siguen siendo poco conocidas. [114] No hay evidencia de que la dependencia de esteroides se desarrolle a partir del uso terapéutico de AAS para tratar trastornos médicos, pero se han informado casos de dependencia de AAS entre levantadores de pesas y culturistas que administraron dosis suprafisiológicas crónicas. [115] Es probable que los trastornos del estado de ánimo (por ejemplo, depresión, [hipo]manía, características psicóticas) dependan de la dosis y del fármaco, pero la dependencia de los EAA o los efectos de abstinencia parecen ocurrir solo en un pequeño número de usuarios de EAA. [7] Actualmente no se dispone de estudios a largo plazo a gran escala sobre los efectos psiquiátricos en los usuarios de EAA. [114]
Afirmación del Manual Diagnóstico Estadístico
El DSM-IV enumera los criterios generales de diagnóstico [ ancla rota ] para un trastorno de la personalidad y establece que "el patrón no debe atribuirse mejor a una manifestación de otro trastorno mental, o a los efectos fisiológicos directos de una sustancia (por ejemplo, fármaco o medicamento) o una afección médica general (por ejemplo, traumatismo craneal)". Como resultado, los usuarios de EAA pueden recibir un diagnóstico erróneo por parte de un psiquiatra que no haya sido informado sobre su hábito. [116]
Perfiles de personalidad
Cooper, Noakes, Dunne, Lambert y Rochford identificaron que las personas que usan AAS tienen más probabilidades de obtener puntuaciones más altas en perfiles de personalidad limítrofe (4,7 veces), antisocial (3,8 veces), paranoide (3,4 veces), esquizotípica (3,1 veces), histriónica (2,9 veces), pasivo-agresiva (2,4 veces) y narcisista (1,6 veces) que los no usuarios. [117] Otros estudios han sugerido que el trastorno de personalidad antisocial es ligeramente más probable entre los usuarios de AAS que entre los no usuarios (Pope y Katz, 1994). [116] La disfunción bipolar , [118] la dependencia de sustancias y el trastorno de conducta también se han asociado con el uso de AAS. [119]
Estado de ánimo y ansiedad
Los trastornos afectivos se reconocen desde hace tiempo como una complicación del consumo de esteroides anabólicos. Los informes de casos describen tanto hipomanía como manía, junto con irritabilidad, euforia, imprudencia, pensamientos acelerados y sentimientos de poder e invencibilidad que no cumplen los criterios de manía/hipomanía. [120] De 53 culturistas que consumieron esteroides anabólicos, 27 (51%) informaron de trastornos del estado de ánimo no especificados. [121]
Agresión e hipomanía
Desde mediados de la década de 1980 en adelante, los medios de comunicación informaron que la "rabia por esteroides" era un efecto secundario de los AAS. [122] : 23
Una revisión de 2005 determinó que algunos estudios controlados aleatorios, pero no todos, han encontrado que el uso de AAS se correlaciona con la hipomanía y el aumento de la agresividad, pero señaló que los intentos de determinar si el uso de AAS desencadena el comportamiento violento han fracasado, principalmente debido a las altas tasas de no participación. [123] Un estudio de 2008 sobre una muestra representativa a nivel nacional de hombres adultos jóvenes en los Estados Unidos encontró una asociación entre el uso de AAS autodeclarado durante la vida y el año anterior y la participación en actos violentos. En comparación con las personas que no usaban esteroides, los hombres adultos jóvenes que usaban AAS informaron una mayor participación en comportamientos violentos incluso después de controlar los efectos de las variables demográficas clave, el comportamiento violento previo y el uso de múltiples drogas. [124] Una revisión de 1996 que examinó los estudios ciegos disponibles en ese momento también encontró que estos habían demostrado un vínculo entre la agresión y el uso de esteroides, pero señaló que con estimaciones de más de un millón de usuarios de esteroides pasados o actuales en los Estados Unidos en ese momento, un porcentaje extremadamente pequeño de los que usaban esteroides parecían haber experimentado trastornos mentales lo suficientemente graves como para dar lugar a tratamientos clínicos o informes de casos médicos. [125]
La relación entre el uso de AAS y la depresión no es concluyente. Una revisión de 1992 [ necesita actualización ] encontró que los AAS pueden aliviar y causar depresión, y que el cese o la disminución del uso de AAS también puede causar depresión, pero exigieron estudios adicionales debido a la disparidad de datos. [126]
Reproductivo
Los andrógenos como la testosterona , la androstenediona y la dihidrotestosterona son necesarios para el desarrollo de los órganos del sistema reproductor masculino , incluidas las vesículas seminales , el epidídimo , el conducto deferente , el pene y la próstata . [127] Los AAS son derivados de la testosterona diseñados para maximizar los efectos anabólicos de la testosterona. [75] Los AAS son consumidos por atletas de élite que compiten en deportes como el levantamiento de pesas , el culturismo y el atletismo . [128] Los atletas recreativos masculinos toman AAS para lograr una apariencia física "mejorada" . [129]
El consumo de AAS altera el eje hipotálamo-hipofisario-gonadal (eje HPG) en los hombres. [127] En el eje HPG, la hormona liberadora de gonadotropina (GnRH) se secreta desde el núcleo arqueado del hipotálamo y estimula la hipófisis anterior para secretar las dos gonadotropinas , la hormona folículo estimulante (FSH) y la hormona luteinizante (LH). [130] En los hombres adultos, la LH estimula las células de Leydig en los testículos para producir testosterona que se requiere para formar nuevos espermatozoides a través de la espermatogénesis . [127] El consumo de AAS conduce a una supresión dependiente de la dosis de la liberación de gonadotropina a través de la supresión de GnRH del hipotálamo (mecanismo de bucle largo) o de la retroalimentación negativa directa sobre la hipófisis anterior para inhibir la liberación de gonadotropina (mecanismo de bucle corto), lo que conduce al hipogonadismo inducido por AAS . [127]
Farmacología
Mecanismo de acción
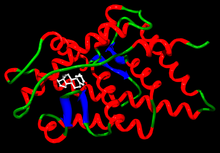
La farmacodinámica de los AAS es diferente a la de las hormonas peptídicas . Las hormonas peptídicas solubles en agua no pueden penetrar la membrana de las células grasas y solo afectan indirectamente al núcleo de las células diana a través de su interacción con los receptores de superficie de la célula . Sin embargo, como hormonas liposolubles, los AAS son permeables a la membrana e influyen en el núcleo de las células por acción directa. La acción farmacodinámica de los AAS comienza cuando la hormona exógena penetra la membrana de la célula diana y se une a un receptor de andrógenos (AR) ubicado en el citoplasma de esa célula. Desde allí, el compuesto hormona-receptor se difunde al núcleo, donde altera la expresión de genes [132] o activa procesos que envían señales a otras partes de la célula. [133] Diferentes tipos de AAS se unen al AAR con diferentes afinidades , dependiendo de su estructura química. [7]
El efecto de los AAS sobre la masa muscular se produce de al menos dos maneras: [134] primero, aumentan la producción de proteínas ; segundo, reducen el tiempo de recuperación al bloquear los efectos de la hormona del estrés cortisol sobre el tejido muscular, de modo que el catabolismo muscular se reduce en gran medida. Se ha planteado la hipótesis de que esta reducción en la degradación muscular puede ocurrir a través de la inhibición de los AAS de la acción de otras hormonas esteroides llamadas glucocorticoides que promueven la degradación de los músculos. [64] Los AAS también afectan al número de células que se convierten en células de almacenamiento de grasa, al favorecer la diferenciación celular en células musculares. [135]
Interacción molecular de los AAS con los receptores de andrógenos
Los esteroides anabólicos interactúan con los AR en varios tejidos, incluidos los músculos, los huesos y los sistemas reproductivos. [136] Al unirse al AR, los esteroides anabólicos desencadenan una translocación del complejo hormona-receptor al núcleo celular, donde alteran la expresión genética o activan las vías de señalización celular; esto da como resultado una mayor síntesis de proteínas, un mayor crecimiento muscular y una reducción del catabolismo muscular. [137]
Los esteroides anabólicos influyen en la diferenciación celular al tiempo que favorecen el desarrollo de células musculares sobre las células de almacenamiento de grasa. [138] La investigación en este campo ha demostrado que las modificaciones estructurales en los esteroides anabólicos son fundamentales para determinar su afinidad de unión a los AR y sus actividades anabólicas y androgénicas resultantes. [82] Estas modificaciones afectan la capacidad de un esteroide para influir en la expresión genética y los procesos celulares, lo que resalta las complejas interacciones biofísicas de los esteroides anabólicos a nivel celular. [136]
Efectos anabólicos y androgénicos
| Medicamento | Relación a |
|---|---|
| Testosterona | ~1:1 |
| Androstanolona ( DHT ) | ~1:1 |
| Metiltestosterona | ~1:1 |
| Metandriol | ~1:1 |
| Fluoximesterona | 1:1–1:15 |
| Metandienona | 1:1–1:8 |
| Drostanolona | 1:3–1:4 |
| Metenolona | 1:2–1:30 |
| Oximetolona | 1:2–1:9 |
| Oxandrolona | 1:3–1:13 |
| Estanozolol | 1:1–1:30 |
| Nandrolona | 1:3–1:16 |
| Etilestrenol | 1:2–1:19 |
| Noretandrolona | 1:1–1:20 |
| Notas: En roedores. Notas al pie: a = Relación entre la actividad androgénica y la anabólica. Fuentes: Ver plantilla. | |
Como sugiere su nombre, los AAS tienen dos tipos de efectos diferentes, pero superpuestos: anabólicos , lo que significa que promueven el anabolismo (crecimiento celular), y androgénicos (o virilizantes ), lo que significa que afectan el desarrollo y mantenimiento de las características masculinas.
Algunos ejemplos de los efectos anabólicos de estas hormonas son el aumento de la síntesis de proteínas a partir de aminoácidos , el aumento del apetito, el aumento de la remodelación y el crecimiento óseo y la estimulación de la médula ósea , que aumenta la producción de glóbulos rojos . A través de una serie de mecanismos, los AAS estimulan la formación de células musculares y, por lo tanto, provocan un aumento del tamaño de los músculos esqueléticos , lo que conduce a un aumento de la fuerza. [139] [12] [140]
Los efectos androgénicos de los AAS son numerosos. Dependiendo de la duración del uso, los efectos secundarios del esteroide pueden ser irreversibles. Los procesos afectados incluyen el crecimiento puberal, la producción de aceite de las glándulas sebáceas y la sexualidad (especialmente en el desarrollo fetal). Algunos ejemplos de efectos virilizantes son el crecimiento del clítoris en las mujeres y el pene en los niños varones (el tamaño del pene adulto no cambia debido a los esteroides [ cita médica requerida ] ), el aumento del tamaño de las cuerdas vocales , el aumento de la libido , la supresión de las hormonas sexuales naturales y la producción deficiente de esperma . [ 141 ] Los efectos en las mujeres incluyen la profundización de la voz, el crecimiento del vello facial y posiblemente una disminución del tamaño de los senos. Los hombres pueden desarrollar un agrandamiento del tejido mamario, conocido como ginecomastia, atrofia testicular y un recuento reducido de espermatozoides. [ cita requerida ] La relación androgénica:anabólica de un AAS es un factor importante a la hora de determinar la aplicación clínica de estos compuestos. Los compuestos con una alta proporción de efectos androgénicos y anabólicos son el fármaco de elección en la terapia de reemplazo de andrógenos (p. ej., tratamiento del hipogonadismo en hombres), mientras que los compuestos con una proporción androgénica:anabólica reducida son los preferidos para la anemia y la osteoporosis, y para revertir la pérdida de proteínas después de un traumatismo, una cirugía o una inmovilización prolongada. La determinación de la proporción androgénica:anabólica se realiza normalmente en estudios con animales, lo que ha llevado a la comercialización de algunos compuestos que se afirma que tienen actividad anabólica con efectos androgénicos débiles. Esta disociación es menos marcada en humanos, donde todos los EAA tienen efectos androgénicos significativos. [77]
Un protocolo comúnmente utilizado para determinar la relación androgénica:anabólica, que data de la década de 1950, utiliza los pesos relativos de la próstata ventral (VP) y el músculo elevador del ano (LA) de ratas macho . El peso de VP es un indicador del efecto androgénico, mientras que el peso de LA es un indicador del efecto anabólico. Se castran dos o más lotes de ratas y no se les da ningún tratamiento y respectivamente algún AAS de interés. La relación LA/VP para un AAS se calcula como la relación de las ganancias de peso LA/VP producidas por el tratamiento con ese compuesto utilizando ratas castradas pero no tratadas como línea de base: (LA c,t –LA c )/(VP c,t –VP c ). La relación de ganancia de peso LA/VP de los experimentos con ratas no es unitaria para la testosterona (normalmente 0,3–0,4), pero está normalizada para fines de presentación y se utiliza como base de comparación para otros AAS, que tienen sus proporciones androgénicas:anabólicas escaladas en consecuencia (como se muestra en la tabla anterior). [142] [143] A principios de la década de 2000, este procedimiento se estandarizó y se generalizó en toda la OCDE en lo que ahora se conoce como el ensayo de Hershberger.
Mejoras en la composición corporal y la fuerza
Los esteroides anabólicos influyen notablemente en las características de las fibras musculares, afectando tanto al tamaño como al tipo de fibras musculares. Esta alteración contribuye significativamente a mejorar la fuerza y la resistencia muscular. [144] Los esteroides anabólico-androgénicos (EAA) causan estos cambios al afectar directamente a los componentes celulares del tejido muscular. Los estudios han demostrado que estos cambios no son meramente superficiales, sino que representan una transformación profunda en las propiedades estructurales y funcionales del músculo. Esta transformación es un factor clave en la capacidad de los esteroides para mejorar el rendimiento físico y la resistencia. [145]
El peso corporal en los hombres puede aumentar de 2 a 5 kg como resultado del uso de esteroides anabólicos a corto plazo (<10 semanas), lo que puede atribuirse principalmente a un aumento de la masa magra. Los estudios en animales también encontraron que la masa grasa se redujo, pero la mayoría de los estudios en humanos no lograron dilucidar disminuciones significativas de la masa grasa. Se ha demostrado que los efectos sobre la masa corporal magra dependen de la dosis. Se ha observado tanto hipertrofia muscular como formación de nuevas fibras musculares . La hidratación de la masa magra no se ve afectada por el uso de esteroides anabólicos, aunque no se pueden descartar pequeños aumentos del volumen sanguíneo. [7]
La región superior del cuerpo (tórax, cuello, hombros y parte superior del brazo) parece ser más susceptible a los AAS que otras regiones del cuerpo debido al predominio de los AR en la parte superior del cuerpo. [ cita requerida ] La mayor diferencia en el tamaño de las fibras musculares entre los usuarios de AAS y los no usuarios se observó en las fibras musculares tipo I del vasto lateral y el músculo trapecio como resultado de la autoadministración de AAS a largo plazo. Después de la abstinencia del fármaco, los efectos desaparecen lentamente, pero pueden persistir durante más de 6 a 12 semanas después de dejar de usar AAS. [7]
Mejoras de fuerza en el rango de 5 a 20% de la fuerza inicial, dependiendo en gran medida de los fármacos y la dosis utilizados, así como del período de administración. En general, el ejercicio donde se observaron las mejoras más significativas fue el press de banca . [7] Durante casi dos décadas, se asumió que los AAS ejercían efectos significativos solo en atletas de fuerza experimentados. [146] [147] Sin embargo, un ensayo controlado aleatorio demostró que incluso en atletas novatos, un programa de entrenamiento de fuerza de 10 semanas acompañado de enantato de testosterona a 600 mg/semana puede mejorar la fuerza más que el entrenamiento solo. [7] [148] Esta dosis es suficiente para mejorar significativamente la masa muscular magra en relación con el placebo incluso en sujetos que no hicieron ejercicio en absoluto. [148] Los efectos anabólicos del enantato de testosterona fueron altamente dependientes de la dosis. [7] [149]
Disociación de efectos
Los AAS endógenos/naturales como la testosterona y la DHT y los AAS sintéticos median sus efectos uniéndose y activándose el AR. [75] Sobre la base de bioensayos animales , los efectos de estos agentes se han dividido en dos tipos parcialmente disociables: anabólicos (miotróficos) y androgénicos. [75] La disociación entre las proporciones de estos dos tipos de efectos en relación con la proporción observada con la testosterona se observa en bioensayos en ratas con varios AAS. [75] Las teorías para la disociación incluyen diferencias entre los AAS en términos de su metabolismo intracelular , selectividad funcional (reclutamiento diferencial de coactivadores ) y mecanismos no genómicos (es decir, señalización a través de receptores de andrógenos de membrana no AR , o mAR). [75] El apoyo a las dos últimas teorías es limitado y más hipotético, pero hay un buen apoyo a la teoría del metabolismo intracelular. [75]
La medición de la disociación entre los efectos anabólicos y androgénicos entre los AAS se basa en gran medida en un modelo simple pero obsoleto y poco sofisticado que utiliza bioensayos de tejido de rata. [75] Se lo ha denominado " índice miotrófico-androgénico ". [75] En este modelo, la actividad miotrófica o anabólica se mide por el cambio en el peso del músculo bulbocavernoso / elevador del ano de la rata , y la actividad androgénica se mide por el cambio en el peso de la próstata ventral de la rata (o, alternativamente, las vesículas seminales de la rata ), en respuesta a la exposición a los AAS. [75] Luego, las mediciones se comparan para formar una proporción. [75]
Metabolismo intracelular
La testosterona es metabolizada en varios tejidos por la 5α-reductasa en DHT, que es 3 a 10 veces más potente como agonista de AR, y por la aromatasa en estradiol , que es un estrógeno y carece de afinidad significativa por AR. [75] Además, la DHT es metabolizada por la 3α-hidroxiesteroide deshidrogenasa (3α-HSD) y la 3β-hidroxiesteroide deshidrogenasa (3β-HSD) en 3α-androstanodiol y 3β-androstanodiol , respectivamente, que son metabolitos con poca o ninguna afinidad por AR. [75] La 5α-reductasa se distribuye ampliamente por todo el cuerpo y se concentra en diversos grados en la piel (particularmente el cuero cabelludo, la cara y las áreas genitales), la próstata, las vesículas seminales, el hígado y el cerebro. [75] Por el contrario, la expresión de 5α-reductasa en el músculo esquelético es indetectable. [75] La aromatasa se expresa en gran medida en el tejido adiposo y el cerebro, y también se expresa significativamente en el músculo esquelético. [75] La 3α-HSD también se expresa en gran medida en el músculo esquelético. [70]
Los AAS naturales como la testosterona y la DHT y los AAS sintéticos son análogos y son muy similares estructuralmente. [75] Por esta razón, tienen la capacidad de unirse y ser metabolizados por las mismas enzimas metabolizadoras de esteroides . [75] Según la explicación del metabolismo intracelular, la relación androgénico-anabólico de un agonista de AR dado está relacionada con su capacidad de ser transformado por las enzimas mencionadas anteriormente junto con la actividad de AR de cualquier producto resultante. [75] Por ejemplo, mientras que la actividad de AR de la testosterona se potencia en gran medida por la conversión local a través de la 5α-reductasa en DHT en los tejidos donde se expresa la 5α-reductasa, un AAS que no es metabolizado por la 5α-reductasa o que ya está 5α-reducido, como la propia DHT o un derivado (como la mesterolona o la drostanolona ), no sufriría dicha potenciación en dichos tejidos. [75] Además, la nandrolona es metabolizada por la 5α-reductasa, pero a diferencia del caso de la testosterona y la DHT, el metabolito 5α-reducido de la nandrolona tiene una afinidad mucho menor por el AR que la propia nandrolona, y esto da como resultado una activación reducida del AR en los tejidos que expresan 5α-reductasa. [75] Como los llamados tejidos "androgénicos", como la piel/folículos pilosos y los tejidos reproductivos masculinos, tienen una expresión muy alta de 5α-reductasa, mientras que el músculo esquelético está prácticamente desprovisto de 5α-reductasa, esto puede explicar principalmente la alta relación miotrófica-androgénica y la disociación observada con la nandrolona, así como con varios otros EAA. [75]
Aparte de la 5α-reductasa, la aromatasa puede inactivar la señalización de testosterona en el músculo esquelético y el tejido adiposo, por lo que se podría esperar que los AAS que carecen de afinidad por la aromatasa, además de estar libres del posible efecto secundario de la ginecomastia , tengan una relación miotrófica-androgénica más alta en comparación. [75] Además, la DHT se inactiva por la alta actividad de 3α-HSD en el músculo esquelético (y el tejido cardíaco), y se podría esperar de manera similar que los AAS que carecen de afinidad por la 3α-HSD tengan una relación miotrófica-androgénica más alta (aunque quizás también mayores riesgos cardiovasculares a largo plazo). [75] De acuerdo con esto, la DHT, la mestanolona (17α-metil-DHT) y la mesterolona (1α-metil-DHT) se describen como muy poco anabólicos debido a la inactivación por 3α-HSD en el músculo esquelético, mientras que otros derivados de DHT con otras características estructurales como la metenolona , oxandrolona , oximetolona , drostanolona y estanozolol son todos sustratos pobres para 3α-HSD y se describen como anabólicos potentes. [70]
La teoría del metabolismo intracelular explica cómo y por qué puede ocurrir una notable disociación entre los efectos anabólicos y androgénicos a pesar del hecho de que estos efectos están mediados por el mismo receptor de señalización, y por qué esta disociación es invariablemente incompleta. [75] En apoyo del modelo está la rara condición de deficiencia congénita de 5α-reductasa tipo 2 , en la que la enzima 5α-reductasa tipo 2 es defectuosa, la producción de DHT está alterada y los niveles de DHT son bajos mientras que los niveles de testosterona son normales. [150] [151] Los varones con esta condición nacen con genitales ambiguos y una glándula prostática severamente subdesarrollada o incluso ausente. [150] [151] Además, en el momento de la pubertad, estos varones desarrollan una musculatura normal, voz más grave y libido, pero tienen menos vello facial, un patrón femenino de vello corporal (es decir, en gran medida restringido al triángulo púbico y las axilas), no hay incidencia de pérdida de cabello de patrón masculino y no hay agrandamiento de próstata ni incidencia de cáncer de próstata . [151] [152] [153] [154] [155] Cabe destacar que tampoco desarrollan ginecomastia como consecuencia de su condición. [153]
| Compuesto | rAR (%) | ARh (%) | ||||||
|---|---|---|---|---|---|---|---|---|
| Testosterona | 38 | 38 | ||||||
| 5α-dihidrotestosterona | 77 | 100 | ||||||
| Nandrolona | 75 | 92 | ||||||
| 5α-Dihidronandrolona | 35 | 50 | ||||||
| Etilestrenol | DAKOTA DEL NORTE | 2 | ||||||
| Noretandrolona | DAKOTA DEL NORTE | 22 | ||||||
| 5α-Dihidronoretandrolona | DAKOTA DEL NORTE | 14 | ||||||
| Metribolona | 100 | 110 | ||||||
| Fuentes: Ver plantilla. | ||||||||
Selectividad funcional
Un estudio en animales descubrió que dos tipos diferentes de elementos de respuesta a los andrógenos podrían responder de manera diferente a la testosterona y la DHT tras la activación del AR. [10] [156] Sin embargo, se desconoce si esto está involucrado en las diferencias en las proporciones del efecto anabólico a miotrófico de diferentes EAA. [10] [156] [75]
Mecanismos no genómicos
Las señales de testosterona no solo se transmiten a través del AR nuclear, sino también a través de los mAR, incluidos ZIP9 y GPRC6A . [157] [158] Se ha propuesto que la señalización diferencial a través de los mAR puede estar involucrada en la disociación de los efectos anabólicos y androgénicos de los AAS. [75] De hecho, la DHT tiene menos del 1% de la afinidad de la testosterona por ZIP9, y los AAS sintéticos metribolona y mibolerona son competidores ineficaces para el receptor de manera similar. [158] Esto indica que los AAS muestran interacciones diferenciales con el AR y los mAR. [158] Sin embargo, las mujeres con síndrome de insensibilidad completa a los andrógenos (CAIS), que tienen un genotipo 46,XY ("masculino") y testículos pero un defecto en el AR tal que no es funcional, son un desafío a esta noción. [159] Son completamente insensibles a los efectos mediados por AR de los andrógenos como la testosterona, y muestran un fenotipo perfectamente femenino a pesar de tener niveles de testosterona en el extremo superior del rango masculino normal. [159] Estas mujeres tienen poca o ninguna producción de sebo , incidencia de acné o crecimiento de vello corporal (incluso en las áreas púbica y axilar). [159] Además, las mujeres CAIS tienen una masa corporal magra que es normal para las mujeres pero, por supuesto, está muy reducida en relación con los hombres. [160] Estas observaciones sugieren que el AR es principal o exclusivamente responsable de la masculinización y miotrofia causadas por los andrógenos. [159] [160] [161] Sin embargo, se ha descubierto que los mAR están involucrados en algunos de los efectos relacionados con la salud de la testosterona, como la modulación del riesgo y la progresión del cáncer de próstata. [158] [162]
Efectos antigonadotrópicos
Los cambios en los niveles endógenos de testosterona también pueden contribuir a las diferencias en la relación miotrófica-androgénica entre la testosterona y los AAS sintéticos. [70] Los agonistas de AR son antigonadotrópicos , es decir, suprimen de forma dosis-dependiente la producción de testosterona gonadal y, por lo tanto, reducen las concentraciones sistémicas de testosterona. [70] Al suprimir los niveles endógenos de testosterona y reemplazar eficazmente la señalización de AR en el cuerpo con la de los AAS exógenos, la relación miotrófica-androgénica de un AAS determinado puede aumentar aún más, de forma dosis-dependiente, y esto, por lo tanto, puede ser un factor adicional que contribuya a las diferencias en la relación miotrófica-androgénica entre diferentes AAS. [70] Además, algunos AAS, como los derivados de la 19-nortestosterona como la nandrolona, también son progestágenos potentes , y la activación del receptor de progesterona (PR) es antigonadotrópica de manera similar a la activación del AR. [70] La combinación de una activación suficiente de AR y PR puede suprimir los niveles de testosterona circulante hasta el rango de castración en los hombres (es decir, la supresión completa de la producción de testosterona gonadal y los niveles de testosterona circulante disminuyeron en aproximadamente un 95%). [50] [163] Como tal, la actividad progestágena combinada puede servir para aumentar aún más la relación miotrófica-androgénica para un AAS determinado. [70]
GABAAmodulación del receptor
Se ha descubierto que algunos AAS, como la testosterona, la DHT, el estanozolol y la metiltestosterona, modulan el receptor GABA A de manera similar a los neuroesteroides endógenos como la alopregnanolona , el 3α-androstanodiol , el sulfato de dehidroepiandrosterona y el sulfato de pregnenolona . [75] Se ha sugerido que esto puede contribuir como un mecanismo alternativo o adicional a los efectos neurológicos y conductuales de los AAS. [75] [164] [165] [166] [167] [168] [169]
Comparación de AAS
Los AAS difieren en una variedad de formas, incluyendo en sus capacidades para ser metabolizados por enzimas esteroidogénicas como la 5α-reductasa , las 3-hidroxiesteroide deshidrogenasas y la aromatasa , en si su potencia como agonistas de AR es potenciada o disminuida por la 5α-reducción, en sus proporciones de efecto anabólico / miotrófico a androgénico , en sus actividades estrogénicas , progestágenas y neuroesteroides , en su actividad oral y en su capacidad para producir hepatotoxicidad . [70] [75] [170]
| Compuesto | Clase | 5α-R | AROM | 3-HSD | AAR | Est | Prog | Oral | HépatoInformación sobre herramientas Hepatotoxicidad |
|---|---|---|---|---|---|---|---|---|---|
| Androstanolona | DHT | – | – | + | * | – | – | – | – |
| Boldenona | yo | – | ± | – | ** | ± | – | – | – |
| Drostanolona | DHT | – | – | – | *** | – | – | – | – |
| Etilestrenol | 19-NT ; 17α-A | + ( ↓ ) | ± | – | *** | + | + | + | + |
| Fluoximesterona | T ; 17α-A | + ( ↑ ) | – | – | * | – | – | + | + |
| Mestanolona | DHT ; 17α-A | – | – | + | * | – | – | + | + |
| Mesterolona | DHT | – | – | + | * | – | – | ± | – |
| Metandienona | T ; 17α-A | – | ± | – | ** | + | – | + | + |
| Metenolona | DHT | – | – | – | ** | – | – | ± | – |
| Metiltestosterona | T ; 17α-A | + ( ↑ ) | + | – | * | + | – | + | + |
| Nandrolona | 19-NT | + ( ↓ ) | ± | – | *** | ± | + | – | – |
| Noretandrolona | 19-NT ; 17α-A | + ( ↓ ) | ± | – | *** | + | + | + | + |
| Oxandrolona | DHT ; 17α-A | – | – | – | *** | – | – | + | ± |
| Oximetolona | DHT ; 17α-A | – | – | – | *** | + | – | + | + |
| Estanozolol | DHT ; 17α-A | – | – | – | *** | – | – | + | + |
| Testosterona | yo | + ( ↑ ) | + | – | * | + | – | ± un | – |
| Trenbolona | 19-NT | – | – | – | *** | – | + | – | – |
| Clave: + = Sí. ± = Bajo. – = No. ↑ = Potenciado. ↓ = Inactivado. *** = Alto. ** = Moderado. * = Bajo. Abreviaturas: 5α-R = Metabolizado por la 5α-reductasa . AROM = Metabolizado por la aromatasa . 3-HSD = Metabolizado por la 3α-Descripción de herramienta 3α-hidroxiesteroide deshidrogenasay/o 3β-HSDDescripción de herramienta 3β-hidroxiesteroide deshidrogenasa. AAR = Relación anabólico-androgénica (cantidad de efecto anabólico ( miotrófico ) relativo al efecto androgénico ). Estr = Estrogénico . Prog = Progestágeno . Oral = Actividad oral . Hepat = Hepatotoxicidad . Notas al pie: a = Como undecanoato de testosterona . Fuentes: Ver plantilla. | |||||||||
| Esteroide | Nombre químico | Afinidades de unión relativas (%) | ||||||
|---|---|---|---|---|---|---|---|---|
| Relaciones públicasInformación sobre herramientas Receptor de progesterona | ArkansasReceptor de andrógenos | ESReceptor de estrógeno | GRAMOInformación sobre herramientas Receptor de glucocorticoides | SEÑORInformación sobre herramientas Receptor de mineralocorticoides | SHBGInformación sobre herramientas Globulina transportadora de hormonas sexuales | CBGGlobulina transportadora de corticosteroides | ||
| Androstanolona | DHT | 1.4–1.5 | 60–120 | <0,1 | <0,1–0,3 | 0,15 | 100 | 0,8 |
| Boldenona | Δ1 - T | <1 | 50–75 | ? | <1 | ? | ? | ? |
| Danazol | 2,3-Isoxazol-17α-Ety-T | 9 | 8 | ? | <0,1 a | ? | 8 | 10 |
| Dienolona | ∆ 9 -19-NT | 17 | 134 | <0,1 | 1.6 | 0.3 | ? | ? |
| Dimetildienolona | ∆ 9 -7α,17α-DiMe-19-NT | 198 | 122 | 0,1 | 6.1 | 1.7 | ? | ? |
| Dimetiltrienolona | ∆ 9,11-7α ,17α-DiMe-19-NT | 306 | 180 | 0,1 | 22 | 52 | ? | ? |
| Drostanolona | 2α-Me-DHT | ? | ? | ? | ? | ? | 39 | ? |
| Etisterona | 17α-Ety-T | 35 | 0,1 | <1.0 | <1.0 | <1.0 | 25–92 | 0.3 |
| Etilestrenol | 3-DeO-17α-Et-19-NT | ? | ? | ? | ? | ? | <1 | ? |
| Fluoximesterona | 9α-F-11β-OH-17α-Me-T | ? | ? | ? | ? | ? | ≤3 | ? |
| Gestrinona | ∆ 9,11-17α -Ety-18-Me-19-NT | 75–76 | 83–85 | <0,1–10 | 77 | 3.2 | ? | ? |
| Levonorgestrel | 17α-Ety-18-Me-19-NT | 170 | 84–87 | <0,1 | 14 | 0,6–0,9 | 14–50 | <0,1 |
| Mestanolona | 17α-Me-DHT | 5–10 | 100–125 | ? | <1 | ? | 84 | ? |
| Mesterolona | 1α-Me-DHT | ? | ? | ? | ? | ? | 82–440 | ? |
| Metandienona | ∆ 1 -17α-Me-T | ? | ? | ? | ? | ? | 2 | ? |
| Metenolona | ∆ 1 -1-Me-DHT | ? | ? | ? | ? | ? | 3 | ? |
| Metandriol | 17α-Me-A5 | ? | ? | ? | ? | ? | 40 | ? |
| Metasterona | 2α,17α-DiMe-DHT | ? | ? | ? | ? | ? | 58 | ? |
| Metildienolona | ∆9-17α -Me - 19-NT | 71 | 64 | <0,1 | 6 | 0,4 | ? | ? |
| Metiltestosterona | 17α-Me-T | 3 | 45–125 | <0,1 | 1–5 | ? | 5–64 | <0,1 |
| Metil-1-testosterona | ∆ 1 -17α-Me-DHT | ? | ? | ? | ? | ? | 69 | ? |
| Metribolona | ∆ 9,11-17α -Me-19-NT | 208–210 | 199–210 | <0,1 | 10–26 | 18 | 0,2–0,8 | ≤0,4 |
| Mibolerona | 7α,17α-DiMe-19-NT | 214 | 108 | <0,1 | 1.4 | 2.1 | 6 | ? |
| Nandrolona | 19-NT | 20 | 154–155 | <0,1 | 0,5 | 1.6 | 1–16 | 0,1 |
| Noretandrolona | 17α-Et-19-NT | ? | ? | ? | ? | ? | 3 | ? |
| Noretisterona | 17α-Ety-19-NT | 155–156 | 43–45 | <0,1 | 2.7–2.8 | 0,2 | 5–21 | 0.3 |
| Norgestrienona | ∆ 9,11-17α -Ety-19-NT | 63–65 | 70 | <0,1 | 11 | 1.8 | ? | ? |
| Normetandrona | 17α-Me-19-NT | 100 | 146 | <0,1 | 1.5 | 0.6 | 7 | ? |
| Oxandrolona | 2-Oxa-17α-Me-DHT | ? | ? | ? | ? | ? | <1 | ? |
| Oximetolona | 2-OHMeEne-17α-Me-DHT | ? | ? | ? | ? | ? | ≤3 | ? |
| RU-2309 ( 17α-Me-THG ) | ∆ 9,11-17α ,18-DiMe-19-NT | 230 | 143 | <0,1 | 155 | 36 | ? | ? |
| Estanozolol | 2,3-pirazol-17α-Me-DHT | ? | ? | ? | ? | ? | 1–36 | ? |
| Testosterona | yo | 1.0–1.2 | 100 | <0,1 | 0,17 | 0.9 | 19–82 | 3–8 |
| 1-Testosterona | ∆1 - DHT | ? | ? | ? | ? | ? | 98 | ? |
| Tibolona | 7α-Me-17α-Ety-19-N-5(10)-T | 12 | 12 | 1 | ? | ? | ? | ? |
| Δ 4 -Tibolona | 7α-Me-17α-Ety-19-NT | 180 | 70 | 1 | <1 | 2 | 1–8 | <1 |
| Trenbolona | ∆ 9,11-19 -NT | 74–75 | 190–197 | <0,1 | 2.9 | 1.33 | ? | ? |
| Trestolona | 7α-Me-19-NT | 50–75 | 100–125 | ? | <1 | ? | 12 | ? |
| Notas: Los valores son porcentajes (%). Los ligandos de referencia (100%) fueron progesterona para el PR.Información sobre herramientas sobre el receptor de progesterona, testosterona para la ARReceptor de andrógenos con información sobre herramientas, estradiol para el ERReceptor de estrógeno con información sobre herramientas, dexametasona para el GRReceptor de glucocorticoides con información sobre herramientas, aldosterona para el MRInformación sobre herramientas sobre el receptor de mineralocorticoides, dihidrotestosterona para SHBGInformación sobre herramientas sobre la globulina transportadora de hormonas sexuales, y cortisol para CBGInformación sobre herramientas sobre globulina transportadora de corticosteroidesNotas al pie: a = tiempo de incubación de 1 hora (4 horas es el tiempo estándar para este ensayo; puede afectar el valor de afinidad). Fuentes: Ver plantilla. | ||||||||
| Medicamento | Forma | Principales marcas | Duración |
|---|---|---|---|
| Testosterona | Suspensión acuosa | Andronaq, esterotato, virosterona | 2-3 días |
| Propionato de testosterona | Solución de aceite | Androteston, Perandren, Testoviron | 3-4 días |
| Fenilpropionato de testosterona | Solución de aceite | Testolent | 8 días |
| Isobutirato de testosterona | Suspensión acuosa | Depósito de agovirina, Perandren M | 14 días |
| Ésteres mixtos de testosterona a | Solución de aceite | Triolandren | 10–20 días |
| Ésteres mixtos de testosterona b | Solución de aceite | Depósito de testosterona | 14–20 días |
| Enantato de testosterona | Solución de aceite | Delatesteryl | 14–28 días |
| Cipionato de testosterona | Solución de aceite | Depovirina | 14–28 días |
| Ésteres mixtos de testosterona c | Solución de aceite | Sustanon 250 | 28 días |
| Undecanoato de testosterona | Solución de aceite | Aveed, Nebido | 100 días |
| Buciclato de testosterona d | Suspensión acuosa | 20 Aet-1, CDB-1781 y | 90–120 días |
| Fenilpropionato de nandrolona | Solución de aceite | Durabolina | 10 días |
| Decanoato de nandrolona | Solución de aceite | Deca Durabolin | 21–28 días |
| Metandriol | Suspensión acuosa | Notandron, Protandren | 8 días |
| Acetato de bisenantoilo de metandriol | Solución de aceite | Depósito de Notandron | 16 días |
| Acetato de metenolona | Solución de aceite | Primobolán | 3 días |
| Enantato de metenolona | Solución de aceite | Depósito de Primobolan | 14 días |
| Nota: Todos se administran por inyección intramuscular . Notas al pie: a = TP , TV y TUe . b = TP y TKL . c = TP , TPP , TiCa y TD . d = Estudiados, pero nunca comercializados. e = Nombres en código de desarrollo. Fuentes: Ver plantilla. | |||
| Éster de testosterona | Forma | Ruta | TmáxInformación sobre herramientas: Es hora de alcanzar los niveles máximos | mediaDescripción emergente Vida media de eliminación | metroInformación sobre herramientas Tiempo de residencia medio |
|---|---|---|---|---|---|
| Undecanoato de testosterona | Cápsulas rellenas de aceite | Oral | ? | 1,6 horas | 3,7 horas |
| Propionato de testosterona | Solución de aceite | Inyección intramuscular | ? | 0,8 días | 1,5 días |
| Enantato de testosterona | Solución de aceite de ricino | Inyección intramuscular | 10 días | 4,5 días | 8,5 días |
| Undecanoato de testosterona | Solución de aceite de semilla de té | Inyección intramuscular | 13,0 días | 20,9 días | 34,9 días |
| Undecanoato de testosterona | Solución de aceite de ricino | Inyección intramuscular | 11,4 días | 33,9 días | 36,0 días |
| Buciclato de testosterona | Suspensión acuosa | Inyección intramuscular | 25,8 días | 29,5 días | 60,0 días |
| Notas: El cipionato de testosterona tiene una farmacocinética similar a la del enantato de testosterona . Notas al pie: a = Nunca comercializado. Fuentes: Ver plantilla. | |||||
5α-reductasa y androgenicidad
La testosterona puede ser convertida robustamente por la 5α-reductasa en DHT en los llamados tejidos androgénicos como la piel , el cuero cabelludo , la próstata y las vesículas seminales , pero no en los músculos o los huesos , donde la 5α-reductasa no se expresa o solo se expresa mínimamente. [75] Como la DHT es de 3 a 10 veces más potente como agonista del AR que la testosterona, la actividad agonista del AR de la testosterona se potencia de forma marcada y selectiva en dichos tejidos. [75] A diferencia de la testosterona, la DHT y otros AAS 4,5α-dihidrogenados ya están 5α-reducidos y, por esta razón, no se pueden potenciar en los tejidos androgénicos. [75] Los derivados de 19-nortestosterona como la nandrolona pueden ser metabolizados por la 5α-reductasa de manera similar a la testosterona, pero los metabolitos 5α-reducidos de los derivados de 19-nortestosterona (por ejemplo, 5α-dihidronandrolona ) tienden a tener una actividad reducida como agonistas de AR, lo que resulta en una actividad androgénica reducida en los tejidos que expresan 5α-reductasa. [75] Además, algunos derivados de 19-nortestosterona, incluyendo trestolona (7α-metil-19-nortestosterona (MENT)), 11β-metil-19-nortestosterona (11β-MNT) y dimetandrolona (7α,11β-dimetil-19-nortestosterona), no pueden ser 5α-reducidos. [171] Por el contrario, ciertos AAS 17α-alquilados como la metiltestosterona son 5α-reducidos y potenciados en los tejidos androgénicos de manera similar a la testosterona. [75] [70] Sin embargo, los derivados de DHT 17α-alquilados no pueden ser potenciados a través de la 5α-reductasa, ya que ya están 4,5α-reducidos. [75] [70]
La capacidad de ser metabolizado por la 5α-reductasa y la actividad AR de los metabolitos resultantes parece ser uno de los principales, si no el más importante, determinante de la relación androgénico-miotrófico para un EAA determinado. [75] Los EAA que no son potenciados por la 5α-reductasa o que son debilitados por la 5α-reductasa en los tejidos androgénicos tienen un riesgo reducido de efectos secundarios androgénicos como acné , alopecia androgénica (calvicie de patrón masculino), hirsutismo (crecimiento excesivo de vello de patrón masculino), hiperplasia prostática benigna (agrandamiento de la próstata) y cáncer de próstata , mientras que la incidencia y magnitud de otros efectos como hipertrofia muscular , cambios óseos, [172] profundización de la voz y cambios en el impulso sexual no muestran diferencias. [75] [173]
Aromatasa y estrogenicidad
La testosterona puede ser metabolizada por la aromatasa en estradiol , y muchos otros AAS también pueden ser metabolizados en sus metabolitos estrogénicos correspondientes. [75] Como ejemplo, los AAS 17α-alquilados metiltestosterona y metandienona son convertidos por la aromatasa en metilestradiol . [174] Los derivados 4,5α-dihidrogenados de la testosterona como la DHT no pueden ser aromatizados, mientras que los derivados de 19-nortestosterona como la nandrolona pueden serlo, pero en un grado muy reducido. [75] [175] Algunos derivados de 19-nortestosterona, como la dimetandrolona y la 11β-MNT, no se pueden aromatizar debido al impedimento estérico proporcionado por su grupo 11β-metilo, mientras que el AAS estrechamente relacionado trestolona (7α-metil-19-nortestosterona), en relación con su falta de un grupo 11β-metilo, se puede aromatizar. [175] Los AAS que están 17α-alquilados (y no también 4,5α-reducidos o 19-desmetilados) también se aromatizan, pero en menor medida que la testosterona. [75] [176] Sin embargo, es notable que los estrógenos que están sustituidos en 17α (por ejemplo, etinilestradiol y metilestradiol) tienen una potencia estrogénica notablemente mayor debido a una estabilidad metabólica mejorada , [174] y por esta razón, los AAS 17α-alquilados en realidad pueden tener una alta estrogenicidad y efectos estrogénicos comparativamente mayores que la testosterona. [174] [70]
El principal efecto de la estrogenicidad es la ginecomastia (pechos parecidos a los de una mujer). [75] Los AAS que tienen un alto potencial de aromatización como la testosterona y particularmente la metiltestosterona muestran un alto riesgo de ginecomastia en dosis suficientemente altas, mientras que los AAS que tienen un potencial reducido de aromatización como la nandrolona muestran un riesgo mucho menor (aunque todavía potencialmente significativo en dosis altas). [75] Por el contrario, los AAS que son 4,5α-reducidos y algunos otros AAS (por ejemplo, derivados de 19-nortestosterona 11β-metilados), no tienen riesgo de ginecomastia. [75] Además de la ginecomastia, los AAS con alta estrogenicidad tienen una actividad antigonadotrópica aumentada, lo que resulta en una mayor potencia en la supresión del eje hipotálamo-hipofisario-gonadal y la producción de testosterona gonadal . [177]
Actividad progestágena
Muchos derivados de la 19-nortestosterona, incluyendo la nandrolona, la trembolona , el etilestrenol (etilnandrol), la metribolona (R-1881), la trestolona, la 11β-MNT, la dimetandrolona y otros, son potentes agonistas del receptor de progesterona (PR) y, por lo tanto, son progestágenos además de los AAS. [75] [178] De manera similar al caso de la actividad estrogénica, la actividad progestágena de estos fármacos sirve para aumentar su actividad antigonadotrópica. [178] Esto da como resultado una mayor potencia y eficacia de estos AAS como agentes antiespermatogénicos y anticonceptivos masculinos (o, dicho de otra manera, una mayor potencia y eficacia en la producción de azoospermia e infertilidad masculina reversible ). [178]
Actividad oral y hepatotoxicidad
Los derivados de testosterona no 17α-alquilados, como la propia testosterona, la DHT y la nandrolona, tienen una biodisponibilidad oral deficiente debido a un extenso metabolismo hepático de primer paso y, por lo tanto, no son activos por vía oral. [75] Una notable excepción a esto son los AAS que son precursores de andrógenos o prohormonas , entre ellos la dehidroepiandrosterona (DHEA), androstenediol , androstenediona , boldiona (androstadienediona), bolandiol (norandrostenediol), bolandiona (norandrostenediona), dienediona , mentabolan (MENT diona, trestiona) y metoxidienona (metoxigonadieno) (aunque estos son AAS relativamente débiles). [179] [180] Los AAS que no son activos por vía oral se utilizan casi exclusivamente en forma de ésteres administrados por inyección intramuscular , que actúan como depósitos y funcionan como profármacos de acción prolongada . [75] Los ejemplos incluyen testosterona, como cipionato de testosterona , enantato de testosterona y propionato de testosterona , y nandrolona, como fenilpropionato de nandrolona y decanoato de nandrolona , entre muchos otros (consulte aquí una lista completa de ésteres de testosterona y nandrolona). [75] Una excepción es el éster de cadena muy larga undecanoato de testosterona , que es activo por vía oral, aunque con una biodisponibilidad oral muy baja (aproximadamente el 3%). [181] A diferencia de la mayoría de los otros AAS, los derivados de testosterona 17α-alquilados muestran resistencia al metabolismo debido al impedimento estérico y son activos por vía oral, aunque también pueden esterificarse y administrarse mediante inyección intramuscular. [75]
Además de la actividad oral, la 17α-alquilación también confiere un alto potencial de hepatotoxicidad , y todos los AAS 17α-alquilados se han asociado, aunque de manera poco común y solo después de un uso prolongado (diferentes estimaciones entre 1 y 17%), [182] [183] con hepatotoxicidad. [75] [184] [185] Por el contrario, los ésteres de testosterona solo se han asociado de manera extremadamente rara o nunca con hepatotoxicidad, [183] y otros AAS no 17α-alquilados solo raramente, [ cita requerida ] aunque se informa que el uso a largo plazo aún puede aumentar el riesgo de cambios hepáticos (pero a una tasa mucho menor que los AAS 17α-alquilados y, según se informa, no en dosis de reemplazo). [182] [186] [74] [ cita(s) adicional(es) necesaria(s ) ] De acuerdo con esto, se ha descubierto que los glucurónidos del anillo D de la testosterona y la DHT son colestásicos. [187]
Aparte de las prohormonas y el undecanoato de testosterona, casi todos los AAS activos por vía oral están 17α-alquilados. [188] Algunos AAS que no están 17α-alquilados son activos por vía oral. [75] Algunos ejemplos incluyen los 17-éteres de testosterona cloxotestosterona , quinbolona y silandrona , [ cita requerida ] que son profármacos (a la testosterona, boldenona (Δ 1 -testosterona) y testosterona, respectivamente), los 17-éteres de DHT mepitiostano , mesabolona y prostanozol (que también son profármacos), los derivados de DHT 1-metilados mesterolona y metenolona (aunque estos son AAS relativamente débiles), [75] [74] y los derivados de 19-nortestosterona dimetandrolona y 11β-MNT, que tienen una resistencia mejorada al metabolismo hepático de primer paso debido a sus grupos 11β-metilo (en contraste con ellos, el AAS relacionado trestolona (7α-metil-19-nortestosterona) no es activo por vía oral). [75] [178] Como estos AAS no están 17α-alquilados, muestran un potencial mínimo de hepatotoxicidad. [75]
Actividad de los neuroesteroides
La DHT, a través de su metabolito 3α-androstanodiol (producido por la 3α-hidroxiesteroide deshidrogenasa (3α-HSD)), es un neurosteroide que actúa a través de la modulación alostérica positiva del receptor GABA A. [75] La testosterona, a través de la conversión en DHT , también produce 3α-androstanodiol como metabolito y, por lo tanto, tiene una actividad similar. [75] Algunos AAS que son o pueden ser reducidos en 5α, incluyendo la testosterona, la DHT, el estanozolol y la metiltestosterona, entre muchos otros, pueden o pueden modular el receptor GABA A , y esto puede contribuir como un mecanismo alternativo o adicional a sus efectos en el sistema nervioso central en términos de estado de ánimo, ansiedad, agresión y deseo sexual. [75] [164] [165] [166] [167] [168] [169]
Química
Los AAS son esteroides androstanos o estranos . Entre ellos se encuentran la testosterona (androst-4-en-17β-ol-3-ona) y derivados con diversas modificaciones estructurales como: [75] [189] [70]
- 17α-Alquilación : metiltestosterona , metandienona , fluoximesterona , oxandrolona , oximetolona , estanozolol , noretandrolona , etilestrenol
- 19-Desmetilación : nandrolona , trembolona , noretandrolona , etilestrenol , trestolona , dimetandrolona
- 5α-Reducción : androstanolona , drostanolona , mestanolona , mesterolona , metenolona , oxandrolona , oximetolona , estanozolol
- Esterificación 3β y/o 17β : enantato de testosterona , decanoato de nandrolona , propionato de drostanolona , undecilenato de boldenona , acetato de trembolona
Así como otros como 1-deshidrogenación (p. ej., metandienona , boldenona ), 1-sustitución (p. ej., mesterolona , metenolona ), 2-sustitución (p. ej., drostanolona , oximetolona , estanozolol ), 4-sustitución (p. ej., clostebol , oxabolona ) y varias otras modificaciones. [75] [189] [70]
| Clases | Andrógino | Estructura | Nombre químico | Características |
|---|---|---|---|---|
| Testosterona | 4-Hidroxiestosterona a |  | 4-Hidroxiestosterona | – |
| Androstenediol a |  | 5-Androstenediol (androst-5-eno-3β,17β-diol) | Prohormona | |
| Androstenediona a | 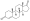 | 4-Androstenediona (androst-4-eno-3,17-diona) | Prohormona | |
| Boldenona |  | 1-Dehidrotestosterona | – | |
| Boldione una |  | 1-Dehidro-4-androstenediona | Prohormona | |
| Clostebol |  | 4-clorotestosterona | – | |
| Cloxotestosterona |  | Éter hemiacetálico de testosterona 17-cloral | Éter | |
| Prasterona |  | 5-Dehidroepiandrosterona (androst-5-en-3β-ol-17-ona) | Prohormona | |
| Quinbolona |  | 1-Dehidrotestosterona 17β-ciclopentenil enol éter | Éter | |
| Silandrona a | 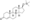 | Éter de testosterona 17β-trimetilsilílico | Éter | |
| Testosterona |  | Androst-4-en-17β-ol-3-ona | – | |
| Testosterona 17α-alquilada | Bolasterona |  | 7α,17α-Dimetiltestosterona | – |
| Calusterona |  | 7β,17α-Dimetiltestosterona | – | |
| Cloruro deshidrometilandrostenediol a | 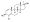 | 1-Dehidro-4-cloro-17α-metil-4-androstenediol | Prohormona | |
| Cloruro deshidrometiltestosterona |  | 1-Dehidro-4-cloro-17α-metiltestosterona | – | |
| Clorometilandrostenediol a | 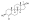 | 4-Cloro-17α-metil-4-androstenediol | – | |
| Enestebol a | 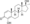 | 1-Dehidro-4-hidroxi-17α-metiltestosterona | – | |
| Etiltestosterona a |  | 17α-Etiltestosterona | – | |
| Fluoximesterona |  | 9α-Fluoro-11β-hidroxi-17α-metiltestosterona | – | |
| Formebolona |  | 1-Dehidro-2-formil-11α-hidroxi-17α-metiltestosterona | – | |
| Hidroxiestenozol a |  | 17α-Metil-2'H-androsta-2,4-dieno[3,2-c]pirazol-17β-ol | Anillo fusionado | |
| Metandienona |  | 1-Dehidro-17α-metiltestosterona | – | |
| Metandriol | 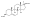 | 17α-Metil-5-androstenediol | Prohormona | |
| Metilclostebol a |  | 4-Cloro-17α-metiltestosterona | – | |
| Metiltestosterona |  | 17α-Metiltestosterona | – | |
| Éter hexílico de metiltestosterona |  | Éter enólico 3-hexílico de 17α-metiltestosterona | Éter | |
| Oximesterona |  | 4-Hidroxi-17α-metiltestosterona | – | |
| Penmesterol | 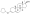 | 17α-Metiltestosterona 3-ciclopentil enol éter | Éter | |
| Tiomesterona | 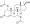 | 1α,7α-Diacetiltio-17α-metiltestosterona | – | |
| Otra testosterona 17α-sustituida | Danazol |  | 2,3-Isoxazol-17α-etiniltestosterona | Anillo fusionado |
| Dihidrotestosterona | 1-Testosterona a |  | 1-Dehidro-4,5α-dihidrotestosterona | – |
| Androstanolona | 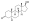 | 4,5α-dihidrotestosterona | – | |
| Bolazina |  | Dímero de azina C3 de drostanolona | Dímero | |
| Drostanolona |  | 2α-Metil-4,5α-dihidrotestosterona | – | |
| Epitiostanol |  | 2α,3α-Epitio-3-deceto-4,5α-dihidrotestosterona | Anillo fusionado | |
| Mepitiostano |  | Éter de 2α,3α-epitio-3-deceto-4,5α-dihidrotestosterona 17β-(1-metoxiciclopentano) | Anillo fusionado; éter | |
| Mesabolona a |  | Éter de 1-dehidro-4,5α-dihidrotestosterona 17β-(1-metoxiciclohexano) | Éter | |
| Mesterolona |  | 1α-Metil-4,5α-dihidrotestosterona | – | |
| Metenolona |  | 1-Dehidro-1-metil-4,5α-dihidrotestosterona | – | |
| Prostanozol a |  | Éter de 17β-tetrahidropirano y 2' H -5α-Androst-2-eno[3,2- c ]pirazol-17β-ol | Éter | |
| Estenbolona |  | 1-Dehidro-2-metil-4,5α-dihidrotestosterona | – | |
| Dihidrotestosterona 17α-alquilada | Androisoxazol |  | 17α-Metil-5α-androstano[3,2- c ]isoxazol-17β-ol | Anillo fusionado |
| Desoximetiltestosterona a |  | 2-Dehidro-3-deceto-4,5α-dihidro-17α-metiltestosterona | – | |
| Furazabol |  | 17α-Metil-5α-androstano[2,3- c ][1,2,5]oxadiazol-17β-ol | Anillo fusionado | |
| Mebolazina | 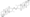 | Dímero de azina C3 de metasterona | Dímero | |
| Mestanolona |  | 4,5α-Dihidro-17α-metiltestosterona | – | |
| Metasterona a | 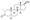 | 2α,17α-Dimetil-4,5α-dihidrotestosterona | – | |
| Metil-1-testosterona a |  | 1-Dehidro-4,5α-dihidro-17α-metiltestosterona | – | |
| Metildiazinol a | 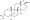 | 3-Deketo-3-azi-4,5α-dihidro-17α-metiltestosterona | – | |
| Metilepitiostanol a | 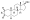 | 2α,3α-Epitio-3-deceto-4,5α-dihidro-17α-metiltestosterona | – | |
| Metilestenbolona a |  | 1-Dehidro-2,17α-dimetil-4,5α-dihidrotestosterona | – | |
| Oxandrolona |  | 2-Oxa-4,5α-dihidro-17α-metiltestosterona | – | |
| Oximetolona |  | 2-Hidroximetileno-4,5α-dihidro-17α-metiltestosterona | – | |
| Estanozolol |  | 17α-Metil-2' H -5α-androst-2-eno[3,2- c ]pirazol-17β-ol | Anillo fusionado | |
| 19-Nortestosterona | 11β-Metil-19-nortestosterona a |  | 11β-Metil-19-nortestosterona | – |
| 19-Nor-5-androstenediol a |  | 19-Nor-5-androstenediol | Prohormona | |
| 19-Nordehidroepiandrosterona a |  | 19-Nor-5-dehidroepiandrosterona | Prohormona | |
| Bolandiol a |  | 19-Nor-4-androstenediol | Prohormona | |
| Bolandiona a | 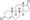 | 19-Nor-4-androstenediona | Prohormona | |
| Bolmantalato a |  | 19-Nortestosterona 17β-adamantoato | Ester | |
| Dienediona a |  | 9-Dehidro-19-nor-4-androstenediona | Prohormona | |
| Dienolona a |  | 9-Dehidro-19-nortestosterona | – | |
| Dimetandrolona a |  | 7α,11β-Dimetil-19-nortestosterona | – | |
| Metoxidienona a |  | Éter 3-metílico del 2,5(10)-didehidro-18-metil-19-norepiandrosterona | Prohormona; Éter | |
| Nandrolona |  | 19-Nortestosterona | – | |
| Norclostebol |  | 4-Cloro-19-nortestosterona | – | |
| Oxabolona |  | 4-Hidroxi-19-nortestosterona | – | |
| Trestolona a |  | 7α-Metil-19-nortestosterona | – | |
| Trenbolona |  | 9,11-Didehidro-19-nortestosterona | – | |
| Tendencia a |  | 9,11-Didehidro-19-nor-4-androstenediona | Prohormona | |
| Trestione a | 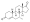 | 7α-Metil-19-nor-4-androstenediona | Prohormona | |
| 17α-19-nortestosterona alquilada | Dimetiltrienolona a |  | 7α,17α-Dimetil-9,11-didehidro-19-nortestosterona | – |
| Dimetildienolona a |  | 7α,17α-Dimetil-9-deshidro-19-nortestosterona | – | |
| Etildienolona a |  | 9-Dehidro-17α-etil-19-nortestosterona | – | |
| Etilestrenol |  | 17α-Etil-3-deceto-19-nortestosterona | – | |
| Metildienolona a |  | 9-Dehidro-17α-metil-19-nortestosterona | – | |
| Metilhidroxinandrolona a |  | 4-Hidroxi-17α-metil-19-nortestosterona | – | |
| Metribolona a |  | 9,11-Didehidro-17α-metil-19-nortestosterona | – | |
| Mibolerona |  | 7α,17α-Dimetil-19-nortestosterona | – | |
| Norboletona a |  | 17α-Etil-18-metil-19-nortestosterona | – | |
| Noretandrolona |  | 17α-Etil-19-nortestosterona | – | |
| Normetandrona |  | 17α-Metil-19-nortestosterona | – | |
| Propetandrol |  | 17α-Etil-19-nortestosterona 3-propionato | Ester | |
| RU-2309 a |  | 9,11-Didehidro-17α,18-dimetil-19-nortestosterona | – | |
| Tetrahidrogestrinona a |  | 9,11-Didehidro-17α-etil-18-metil-19-nortestosterona | – | |
| Otras 19-nortestosteronas 17α-sustituidas | Gestrinona |  | 9,11-Didehidro-17α-etinil-18-metil-19-nortestosterona | – |
| Tibolona |  | 5(10)-Dehidro-7α-metil-17α-etinil-19-nortestosterona | – | |
| Viniltestosterona a |  | 17α-Eteniltestosterona | – | |
| Notas: Los ésteres de andrógenos y esteroides anabólicos en su mayoría no están incluidos en esta tabla; consulte aquí en su lugar. Las progestinas débilmente androgénicas en su mayoría no están incluidas en esta tabla; consulte aquí en su lugar. Notas al pie: a = Nunca comercializado. | ||||
| Andrógino | Estructura | Ester | Peso molecular relativo | Contenido relativo de T b | logPc | ||||
|---|---|---|---|---|---|---|---|---|---|
| Puesto(s) | La mitad(es) | Tipo | Longitud a | ||||||
| Testosterona |  | – | – | – | – | 1.00 | 1.00 | 3,0–3,4 | |
| Propionato de testosterona |  | C17β | Ácido propanoico | Ácido graso de cadena lineal | 3 | 1.19 | 0,84 | 3.7–4.9 | |
| Isobutirato de testosterona |  | C17β | Ácido isobutírico | Ácido graso de cadena ramificada | – (~3) | 1.24 | 0,80 | 4.9–5.3 | |
| Isocaproato de testosterona |  | C17β | Ácido isohexanoico | Ácido graso de cadena ramificada | – (~5) | 1.34 | 0,75 | 4.4–6.3 | |
| Caproato de testosterona |  | C17β | Ácido hexanoico | Ácido graso de cadena lineal | 6 | 1.35 | 0,75 | 5.8–6.5 | |
| Fenilpropionato de testosterona |  | C17β | Ácido fenilpropanoico | Ácido graso aromático | – (~6) | 1.46 | 0,69 | 5.8–6.5 | |
| Cipionato de testosterona | 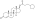 | C17β | Ácido ciclopentilpropanoico | Ácido carboxílico cíclico | – (~6) | 1.43 | 0,70 | 5.1–7.0 | |
| Enantato de testosterona |  | C17β | Ácido heptanoico | Ácido graso de cadena lineal | 7 | 1.39 | 0,72 | 3,6–7,0 | |
| Decanoato de testosterona |  | C17β | Ácido decanoico | Ácido graso de cadena lineal | 10 | 1.53 | 0,65 | 6.3–8.6 | |
| Undecanoato de testosterona |  | C17β | Ácido undecanoico | Ácido graso de cadena lineal | 11 | 1.58 | 0,63 | 6.7–9.2 | |
| Buciclato de testosterona d |  | C17β | Ácido bucíclico e | Ácido carboxílico cíclico | – (~9) | 1.58 | 0,63 | 7,9–8,5 | |
| Notas al pie: a = Longitud del éster en átomos de carbono para ácidos grasos de cadena lineal o longitud aproximada del éster en átomos de carbono para ácidos grasos aromáticos o cíclicos . b = Contenido relativo de testosterona en peso (es decir, potencia androgénica /anabólica relativa ). c = Coeficiente de reparto octanol/agua experimental o previsto (es decir, lipofilia / hidrofobicidad ). Obtenido de PubChem , ChemSpider y DrugBank . d = Nunca comercializado. e = Ácido bucíclico = ácido trans -4-butilciclohexano-1-carboxílico. Fuentes: Ver artículos individuales. | |||||||||
| Esteroide anabólico | Estructura | Ester | Peso molecular relativo | Contenido relativo de AAS b | Duración c | ||||
|---|---|---|---|---|---|---|---|---|---|
| Posición | Mitad | Tipo | Longitud a | ||||||
| Undecilenato de boldenona |  | C17β | Ácido undecilénico | Ácido graso de cadena lineal | 11 | 1.58 | 0,63 | Largo | |
| Propionato de drostanolona |  | C17β | Ácido propanoico | Ácido graso de cadena lineal | 3 | 1.18 | 0,84 | Corto | |
| Acetato de metenolona |  | C17β | Ácido etanoico | Ácido graso de cadena lineal | 2 | 1.14 | 0,88 | Corto | |
| Enantato de metenolona |  | C17β | Ácido heptanoico | Ácido graso de cadena lineal | 7 | 1.37 | 0,73 | Largo | |
| Decanoato de nandrolona |  | C17β | Ácido decanoico | Ácido graso de cadena lineal | 10 | 1.56 | 0,64 | Largo | |
| Fenilpropionato de nandrolona | 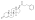 | C17β | Ácido fenilpropanoico | Ácido graso aromático | – (~6–7) | 1.48 | 0,67 | Largo | |
| Acetato de trembolona |  | C17β | Ácido etanoico | Ácido graso de cadena lineal | 2 | 1.16 | 0,87 | Corto | |
| Enantato de trembolona d | 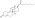 | C17β | Ácido heptanoico | Ácido graso de cadena lineal | 7 | 1.41 | 0,71 | Largo | |
| Notas al pie: a = Longitud del éster en átomos de carbono para ácidos grasos de cadena lineal o longitud aproximada del éster en átomos de carbono para ácidos grasos aromáticos . b = Contenido relativo de esteroides anabólicos/andrógenos por peso (es decir, potencia androgénica /anabólica relativa ). c = Duración por inyección intramuscular o subcutánea en solución oleosa . d = Nunca comercializado. Fuentes: Ver artículos individuales. | |||||||||
Conversiones estructurales de esteroides anabólicos
Testosterona a derivados
Conversión a DHT, [190] nandrolona, [75] metandienona (Dianabol), [191] clorodehidrometiltestosterona (Turinabol), [192] fluoximesterona (Halotestin), [193] y boldenona (Equipoise): [194]

DHT a derivados
DHT a estanozolol (Winstrol), [195] acetato de metenolona (Primobolan), [196] oximetolona (Anadrol), [197] y metasterona (Superdrol): [198]

Nandrolona y derivados
Nandrolona a trestolona, [199] trembolona, [200] norboletona, [201] y etilestrenol: [202]

Detección en fluidos corporales
La muestra fisiológica humana más comúnmente empleada para detectar el uso de esteroides anabólicos es la orina, aunque se han investigado tanto la sangre como el cabello para este propósito. Los esteroides anabólicos, ya sean de origen endógeno o exógeno, están sujetos a una biotransformación hepática extensa por una variedad de vías enzimáticas. Los metabolitos urinarios primarios pueden ser detectables hasta 30 días después del último uso, dependiendo del agente específico, la dosis y la vía de administración. Varios de los fármacos tienen vías metabólicas comunes, y sus perfiles de excreción pueden superponerse a los de los esteroides endógenos, lo que hace que la interpretación de los resultados de las pruebas sea un desafío muy importante para el químico analítico. Los métodos para la detección de las sustancias o sus productos de excreción en muestras de orina generalmente involucran cromatografía de gases-espectrometría de masas o cromatografía líquida-espectrometría de masas. [203] [204] [205] [206]
Historia
| Nombre genérico | Clase [a] | Nombre de marca | Ruta [b] | Intr. | ||
|---|---|---|---|---|---|---|
| Androstanolona [c] [d] | DHT | Andractim | PO, [e] IM, TD | 1953 | ||
| Undecilenato de boldenona [f] | Ester | Equilibrio [g] | SOY | Década de 1960 | ||
| Danazol | Alquilo | Danocrina | correos | 1971 | ||
| Propionato de drostanolona [e] | Éster de DHT | Maestro | SOY | 1961 | ||
| Etilestrenol [d] | 19-NT alquilo | Maxibolina [g] | correos | 1961 | ||
| Fluoximesterona [d] | Alquilo | Halotestin [g] | correos | 1957 | ||
| Mestanolona [e] | Alquilo DHT | Androstalona [g] | correos | Década de 1950 | ||
| Mesterolona | DHT | Provirón | correos | 1967 | ||
| Metandienona [d] | Alquilo | Dianabol | Correo electrónico, mensaje instantáneo | 1958 | ||
| Acetato de metenolona [d] | Éster de DHT | Primobolán | correos | 1961 | ||
| Enantato de metenolona [d] | Éster de DHT | Depósito de Primobolan | SOY | 1962 | ||
| Metiltestosterona [d] | Alquilo | Metandreno | correos | 1936 | ||
| Decanoato de nandrolona | Ester del NT 19 | Deca-Durabolin | SOY | 1962 | ||
| Fenilpropionato de nandrolona [d] | Ester del NT 19 | Durabolina | SOY | 1959 | ||
| Noretandrolona [d] | 19-NT alquilo | Nilevar [g] | correos | 1956 | ||
| Oxandrolona [d] | Alquilo DHT | Oxandrina [g] | correos | 1964 | ||
| Oximetolona [d] | Alquilo DHT | Anadrol [g] | correos | 1961 | ||
| Prasterona [h] | Prohormona | Intrarrosa [g] | PO, IM, vaginal | Década de 1970 | ||
| Estanozolol [e] | Alquilo DHT | Winstrol [g] | Correo electrónico, mensaje instantáneo | 1962 | ||
| Cipionato de testosterona | Ester | Depo-Testosterona | SOY | 1951 | ||
| Enantato de testosterona | Ester | Delatesteryl | SOY | 1954 | ||
| Propionato de testosterona | Ester | Testoviron | SOY | 1937 | ||
| Undecanoato de testosterona | Ester | Andriol [g] | Correo electrónico, mensaje instantáneo | Década de 1970 | ||
| Acetato de trembolona [f] | Ester del NT 19 | Finajet [g] | SOY | Década de 1970 | ||
| ||||||
Descubrimiento de los andrógenos
El uso de esteroides gonadales es anterior a su identificación y aislamiento. El uso de orina de vaca para el tratamiento de ascitis, insuficiencia cardíaca, insuficiencia renal y vitíligo ha sido descrito detalladamente en Sushruta Samhita , lo que sugiere que los antiguos indios tenían algún conocimiento de las propiedades esteroidales de la orina de vaca alrededor del siglo VI a. C. [207] La extracción de hormonas de la orina comenzó en China alrededor del año 100 a. C. [ cita requerida ] El uso médico del extracto de testículo comenzó a fines del siglo XIX, mientras aún se estudiaban sus efectos sobre la fuerza. [141] El aislamiento de esteroides gonadales se remonta a 1931, cuando Adolf Butenandt , un químico de Marburgo , purificó 15 miligramos de la hormona masculina androstenona de decenas de miles de litros de orina. Este esteroide fue sintetizado posteriormente en 1934 por Leopold Ružička , un químico de Zúrich . [208]
En la década de 1930, ya se sabía que los testículos contienen un andrógeno más potente que la androstenona , y tres grupos de científicos, financiados por compañías farmacéuticas competidoras en los Países Bajos, Alemania y Suiza, se apresuraron a aislarlo. [208] [209] Esta hormona fue identificada por primera vez por Karoly Gyula David, E. Dingemanse, J. Freud y Ernst Laqueur en un artículo de mayo de 1935 "Sobre la hormona masculina cristalina de los testículos (testosterona)". [210] Llamaron a la hormona testosterona , de las raíces de testículo y esterol , y el sufijo de cetona . La síntesis química de la testosterona se logró en agosto de ese año, cuando Butenandt y G. Hanisch publicaron un artículo que describía "Un método para preparar testosterona a partir del colesterol". [211] Sólo una semana después, el tercer grupo, Ruzicka y A. Wettstein, anunciaron una solicitud de patente en un artículo "Sobre la preparación artificial de la hormona testicular testosterona (Androsten-3-ona-17-ol)". [212] A Ruzicka y Butenandt se les ofreció el Premio Nobel de Química de 1939 por su trabajo, pero el gobierno nazi obligó a Butenandt a rechazar el honor, aunque aceptó el premio después del final de la Segunda Guerra Mundial. [208] [209]
Los ensayos clínicos en humanos, que involucraban dosis orales de metiltestosterona o inyecciones de propionato de testosterona , comenzaron ya en 1937. [208] A menudo hay rumores de que a los soldados alemanes se les administró AAS durante la Segunda Guerra Mundial, con el objetivo de aumentar su agresividad y resistencia, pero estos, hasta ahora, no están probados. [122] : 6 El propio Adolf Hitler , según su médico, fue inyectado con derivados de testosterona para tratar varias dolencias. [213] Los AAS se utilizaron en experimentos realizados por los nazis en reclusos de campos de concentración, [213] y más tarde por los aliados que intentaban tratar a las víctimas desnutridas que sobrevivieron a los campos nazis. [122] : 6 Al presidente John F. Kennedy se le administraron esteroides tanto antes como durante su presidencia. [214]
Desarrollo de AAS sintéticos
El desarrollo de las propiedades de la testosterona para el desarrollo muscular se llevó a cabo en la década de 1940, en la Unión Soviética y en los países del Bloque del Este , como Alemania del Este, donde se utilizaron programas de esteroides para mejorar el rendimiento de los levantadores de pesas olímpicos y otros levantadores de pesas aficionados . En respuesta al éxito de los levantadores de pesas rusos, el médico del equipo olímpico de EE. UU., John Ziegler, trabajó con químicos sintéticos para desarrollar un AAS con efectos androgénicos reducidos. [215] El trabajo de Ziegler resultó en la producción de metandrostenolona , que Ciba Pharmaceuticals comercializó como Dianabol. El nuevo esteroide fue aprobado para su uso en los EE. UU. Por la Administración de Alimentos y Medicamentos (FDA) en 1958. Se administraba con mayor frecuencia a víctimas de quemaduras y ancianos. Los usuarios fuera de etiqueta del fármaco eran principalmente culturistas y levantadores de pesas. Aunque Ziegler prescribía solo pequeñas dosis a los atletas, pronto descubrió que aquellos que habían usado Dianabol desarrollaban próstatas agrandadas y testículos atrofiados. [216] Los AAS fueron incluidos en la lista de sustancias prohibidas del Comité Olímpico Internacional (COI) en 1976, y una década más tarde, el comité introdujo pruebas de dopaje "fuera de competición" porque muchos atletas usaban AAS en su período de entrenamiento en lugar de durante la competición. [7]
Tres ideas principales gobernaron las modificaciones de la testosterona en una multitud de AAS: la alquilación en la posición C17α con un grupo metilo o etilo creó compuestos activos de polioxietilo porque retarda la degradación del fármaco por el hígado; la esterificación de testosterona y nortestosterona en la posición C17β permite que la sustancia se administre por vía parenteral y aumenta la duración de la eficacia porque los agentes solubles en líquidos aceitosos pueden estar presentes en el cuerpo durante varios meses; y se aplicaron alteraciones de la estructura del anillo tanto para agentes de polioxietilo como parenterales con el fin de obtener diferentes proporciones de efectos anabólicos a androgénicos. [7]
Sociedad y cultura
Etimología
Los andrógenos se descubrieron en la década de 1930 y se caracterizaron por tener efectos descritos como androgénicos (es decir, virilizantes) y anabólicos (por ejemplo, miotróficos, renotróficos). [70] [75] El término esteroide anabólico se remonta al menos a mediados de la década de 1940, cuando se utilizó para describir el concepto hipotético de ese momento de un esteroide derivado de la testosterona con efectos anabólicos pero con efectos androgénicos mínimos o nulos. [217] Este concepto se formuló con base en la observación de que los esteroides tenían proporciones de potencia renotrófica a androgénica que diferían significativamente, lo que sugería que los efectos anabólicos y androgénicos podrían ser disociables. [217]
En 1953, un esteroide derivado de la testosterona conocido como noretandrolona (17α-etil-19-nortestosterona) se sintetizó en GD Searle & Company y se estudió como progestina , pero no se comercializó. [218] Posteriormente, en 1955, se volvió a examinar para determinar su actividad similar a la de la testosterona en animales y se descubrió que tenía una actividad anabólica similar a la testosterona, pero solo un dieciseisavo de su potencia androgénica. [218] [219] Fue el primer esteroide con una marcada y favorable separación de efecto anabólico y androgénico que se descubrió y, en consecuencia, se lo ha descrito como el "primer esteroide anabólico". [220] [221] La noretandrolona se introdujo para uso médico en 1956, y rápidamente fue seguida por numerosos esteroides similares, por ejemplo, el fenilpropionato de nandrolona en 1959 y el estanozolol en 1962. [220] [221] [222] [223] Con estos desarrollos, el esteroide anabólico se convirtió en el término preferido para referirse a dichos esteroides (por encima de "andrógeno"), y entró en uso generalizado.
Aunque originalmente el término esteroide anabólico se concibió para describir específicamente los esteroides derivados de la testosterona con una marcada disociación del efecto anabólico y androgénico, hoy en día se aplica indiscriminadamente a todos los esteroides con efectos anabólicos basados en el agonismo AR, independientemente de su potencia androgénica, incluidos incluso los esteroides no sintéticos y no preferentemente anabólicos como la testosterona. [70] [75] [218] Si bien muchos esteroides anabólicos tienen una potencia androgénica disminuida en comparación con la potencia anabólica, no existe ningún esteroide anabólico que sea exclusivamente anabólico y, por lo tanto, todos los esteroides anabólicos conservan al menos algún grado de androgenicidad. [70] [75] [218] (Asimismo, todos los "andrógenos" son inherentemente anabólicos). [70] [75] [218] De hecho, probablemente no sea posible disociar completamente los efectos anabólicos de los efectos androgénicos, ya que ambos tipos de efectos están mediados por el mismo receptor de señalización, el AR. [75] Como tal, la distinción entre los términos esteroide anabólico y andrógeno es cuestionable, y esta es la base para el término revisado y más reciente esteroide anabólico-androgénico ( EAA ). [70] [75] [218]
David Handelsman ha criticado la terminología y la comprensión que rodea a los AAS en muchas publicaciones. [224] [225] [226 ] [227] [ 228] [229] [230] [231] Según Handelsman, la industria farmacéutica intentó disociar los llamados efectos "androgénicos" y "anabólicos" de los AAS a mediados del siglo XX para crear agentes anabólicos no masculinizantes que fueran más adecuados para su uso en mujeres y niños. [224] Sin embargo, este esfuerzo fracasó estrepitosamente y fue abandonado en la década de 1970. [224] [225] Este fracaso se debió al descubrimiento posterior de un receptor de andrógenos singular (AR) que media los efectos de los AAS tanto en el tejido muscular como en el reproductivo, junto con la mala interpretación de bioensayos de andrógenos animales defectuosos empleados para distinguir entre efectos androgénicos o virilizantes y efectos anabólicos o miotróficos (es decir, el ensayo de Hershberger que involucra al músculo elevador del ano no representativo). [224] [225] En realidad, todos los AAS tienen efectos mediados por AR esencialmente similares, [231] incluso si algunos pueden diferir en potencia hasta cierto punto en ciertos tejidos (por ejemplo, piel, folículos pilosos, glándula prostática) en función de la susceptibilidad a la reducción de 5α y la amplificación o inactivación metabólica asociada o la falta de ella. [231] [8] Según Handelsman, los términos "esteroide anabólico" y "esteroide anabólico-androgénico" son obsoletos, sin sentido y distinguen falsamente a estos agentes de los andrógenos cuando no hay una base fisiológica para tal distinción. [224] [225] De hecho, se ha observado que el uso y la distinción de los conceptos "anabólico" y "androgénico", así como el término "esteroide anabólico-androgénico" son oxímoron, ya que anabólico se refiere al desarrollo muscular, mientras que androgénico se refiere a la inducción y mantenimiento de las características sexuales secundarias masculinas (que en principio incluirían efectos anabólicos o de desarrollo muscular). [224] [225] [232] Handelsman ha argumentado que estos términos deberían descartarse y, en su lugar, todos los AAS deberían simplemente denominarse "andrógenos", y él utiliza este término exclusivamente para referirse a estos agentes en sus publicaciones. [224] [225] Aunque el término "esteroide anabólico-androgénico" es técnicamente válido para describir dos tipos de acciones de estos agentes, Handelsman considera que el término es innecesario y redundante y lo compara con términos hipotéticos nunca utilizados como "progestinas lúteas-gestacionales" o "estrógenos mamarios-uterinos".[224] Handelsman también señala que los "esteroides anabólicos" se confunden fácil e innecesariamente con los corticosteroides . [224]Además de los AAS, Handelsman ha criticado el término " modulador selectivo del receptor de andrógenos (SARM)" y las afirmaciones sobre estos agentes también. [226] [224] [225] [230]
Estatus legal
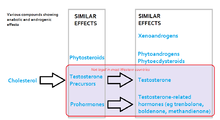
El estatus legal de los AAS varía de un país a otro: algunos tienen controles más estrictos sobre su uso o prescripción que otros, aunque en muchos países no son ilegales. En los EE. UU., los AAS están actualmente listados como sustancias controladas de la Lista III bajo la Ley de Sustancias Controladas , que hace que la simple posesión de tales sustancias sin receta sea un delito federal punible con hasta un año de prisión por la primera infracción. La distribución ilegal o posesión con intención de distribuir AAS como primera infracción se castiga con hasta diez años de prisión. [233] En Canadá, los AAS y sus derivados son parte de la Ley de Sustancias y Drogas Controladas y son sustancias de la Lista IV , lo que significa que es ilegal obtenerlos o venderlos sin receta; sin embargo, la posesión no es punible, una consecuencia reservada para las sustancias de las listas I, II o III. Los culpables de comprar o vender AAS en Canadá pueden ser encarcelados por hasta 18 meses. [234] La importación y exportación también conllevan sanciones similares.
En Canadá, los investigadores han llegado a la conclusión de que el uso de esteroides entre los deportistas estudiantes está muy extendido. Un estudio realizado en 1993 por el Centro Canadiense para un Deporte Libre de Drogas descubrió que casi 83.000 canadienses de entre 11 y 18 años consumen esteroides. [235] Los esteroides anabólicos también son ilegales sin receta en Australia, [236] Argentina, [ cita requerida ] Brasil, [ cita requerida ] y Portugal, [ cita requerida ] y están catalogados como Drogas Controladas de Clase C en el Reino Unido. Los esteroides anabólicos están fácilmente disponibles sin receta en algunos países como México y Tailandia.
| Sustancia | Ejemplo | Clasificadas como sustancias hormonales | Efectos anabólicos y androgénicos | Medicamentos de venta libre que se venden legalmente |
|---|---|---|---|---|
| Testosterona natural | testosterona | hormonal | Sí | no legal |
| Esteroides anabólicos creados artificialmente | trembolona, oxandrolona | hormonal | Sí | no legal |
| Prohormonas | 4-androstenediona | hormonal | solo indirecto | no legal |
| Fitoandrógenos | daidzeína, triterpenoides de gutapercha | No | Sí | legal |
| Fitoesteroides | campesterol, beta-sitosterol, estigmasterol | No | solo indirecto | legal |
| Xenoandrógenos | tocoferoles modificados, nicotinamida modificada | No | Sí | legal |
| Fitoecdisteroides | (25S)-20, 22-O-(R-etiliden)inokosterona | No | Sí | legal |
| Moduladores selectivos del receptor de andrógenos | ostarina | anabólico [237] | no apto para consumo humano [238] [239] |
Estados Unidos

La historia de la legislación estadounidense sobre los esteroides anabólicos se remonta a finales de la década de 1980, cuando el Congreso de Estados Unidos consideró colocar los esteroides anabólicos bajo la Ley de Sustancias Controladas tras la controversia sobre la victoria de Ben Johnson en los Juegos Olímpicos de Verano de 1988 en Seúl . Los esteroides anabólicos se agregaron al Anexo III de la Ley de Sustancias Controladas en la Ley de Control de Esteroides Anabólicos de 1990. [240]
La misma ley también introdujo controles más estrictos con sanciones penales más altas para los delitos que involucraran la distribución ilegal de AAS y hormona de crecimiento humano. A principios de la década de 1990, después de que los AAS se programaran en los EE. UU., varias compañías farmacéuticas dejaron de fabricar o comercializar los productos en los EE. UU., incluidas Ciba , Searle , Syntex y otras. En la Ley de Sustancias Controladas, los AAS se definen como cualquier fármaco o sustancia hormonal química y farmacológicamente relacionada con la testosterona (excepto estrógenos , progestinas y corticosteroides ) que promueven el crecimiento muscular. La ley fue enmendada por la Ley de Control de Esteroides Anabólicos de 2004, que agregó prohormonas a la lista de sustancias controladas , con efecto a partir del 20 de enero de 2005. [241]
Si bien todavía pueden ser recetados por un médico en los EE. UU., el uso de esteroides anabólicos para la recuperación de lesiones ha sido un tema tabú, incluso entre la mayoría de los médicos deportivos y endocrinólogos.
Reino Unido
En el Reino Unido, los AAS se clasifican como medicamentos de clase C, lo que los coloca en la misma clase que las benzodiazepinas . Los AAS están en la Lista 4, que se divide en 2 partes: la Parte 1 contiene la mayoría de las benzodiazepinas y la Parte 2 contiene los AAS.
Los medicamentos de la Parte 1 están sujetos a controles completos de importación y exportación, y su posesión constituye un delito sin una receta médica adecuada. No hay restricciones a la posesión cuando forma parte de un medicamento. Los medicamentos de la Parte 2 requieren una licencia del Ministerio del Interior para su importación y exportación, a menos que la sustancia se presente en forma de medicamento y esté destinada a la autoadministración por una persona. [242]
Estatus en el deporte
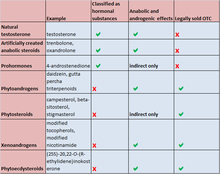
Los AAS están prohibidos por todos los organismos deportivos importantes, incluyendo la Asociación de Profesionales del Tenis , las Grandes Ligas de Béisbol , la Federación Internacional de Fútbol Asociación , [243] los Juegos Olímpicos , [244] la Asociación Nacional de Baloncesto , [245] la Liga Nacional de Hockey , [246] la World Wrestling Entertainment y la Liga Nacional de Fútbol . [247] La Agencia Mundial Antidopaje (AMA) mantiene la lista de sustancias para mejorar el rendimiento utilizadas por muchos organismos deportivos importantes e incluye todos los agentes anabólicos, que incluyen todos los AAS y precursores, así como todas las hormonas y sustancias relacionadas. [248] [249]
Uso
Aplicación de la ley
Los funcionarios encargados de hacer cumplir la ley federal de los Estados Unidos han expresado su preocupación por el uso de esteroides anabólicos por parte de los agentes de policía. "Es un gran problema y, a juzgar por la cantidad de casos, es algo que no deberíamos ignorar. No es que nos propusiéramos atacar a los policías, pero cuando estamos en medio de una investigación activa sobre esteroides , ha habido bastantes casos que han llevado a los agentes de policía", dice Lawrence Payne, portavoz de la Administración de Control de Drogas de los Estados Unidos . [250] El Boletín de Aplicación de la Ley del FBI afirmó que "el abuso de esteroides anabólicos por parte de los agentes de policía es un problema grave que merece una mayor concienciación por parte de los departamentos de todo el país". [251] También se cree que los agentes de policía de todo el Reino Unido "están utilizando a los delincuentes para comprar esteroides", lo que, según afirma, es un factor de riesgo importante para la corrupción policial .
Lucha libre profesional
Tras el doble asesinato y suicidio de Chris Benoit en 2007, el Comité de Supervisión y Reforma Gubernamental investigó el uso de esteroides en la industria de la lucha libre. [252] El Comité investigó a la WWE y a la Total Nonstop Action Wrestling (ahora conocida como Impact Wrestling ), pidiendo documentación de las políticas de drogas de sus empresas. El director ejecutivo y presidente de la WWE, Linda y Vince McMahon respectivamente, ambos testificaron. Los documentos indicaron que 75 luchadores, aproximadamente el 40 por ciento, habían dado positivo por consumo de drogas desde 2006, más comúnmente por esteroides. [253] [254]
Ciencias económicas

Los esteroides anabólicos se producen frecuentemente en laboratorios farmacéuticos, pero en países donde existen leyes más estrictas, también se producen en pequeños laboratorios clandestinos caseros, generalmente a partir de materias primas importadas del extranjero. [255] En estos países, la mayoría de los esteroides se obtienen ilegalmente a través del mercado negro . [256] [257] Estos esteroides generalmente se fabrican en otros países y, por lo tanto, deben contrabandearlos a través de las fronteras internacionales. Como en la mayoría de las operaciones de contrabando importantes, está involucrado el crimen organizado . [258]
A finales de la década de 2000, el comercio mundial de AAS ilícitos aumentó significativamente y las autoridades anunciaron incautaciones récord en tres continentes. En 2006, las autoridades finlandesas anunciaron una incautación récord de 11,8 millones de tabletas de AAS. Un año después, la DEA incautó 11,4 millones de unidades de AAS en la mayor incautación jamás realizada en Estados Unidos. En los primeros tres meses de 2008, las aduanas australianas informaron de una cifra récord de 300 incautaciones de cargamentos de AAS. [114]
En los Estados Unidos, Canadá y Europa, los esteroides ilegales a veces se compran como cualquier otra droga ilegal, a través de distribuidores que pueden obtenerlos de varias fuentes. Los esteroides anabólicos ilegales a veces se venden en gimnasios y competiciones, y por correo, pero también se pueden obtener a través de farmacias, veterinarios y médicos. [259] Además, una cantidad significativa de productos falsificados se venden como esteroides anabólicos, en particular a través de pedidos por correo desde sitios web que se hacen pasar por farmacias extranjeras. En los Estados Unidos, la importación en el mercado negro continúa desde México, Tailandia y otros países donde los esteroides están más fácilmente disponibles, ya que son legales. [260]
Investigación
Los AAS, solos y en combinación con progestágenos , se han estudiado como posibles anticonceptivos hormonales masculinos . [50] Los AAS duales y las progestinas como la trestolona y el undecanoato de dimetandrolona también se han estudiado como anticonceptivos masculinos, y este último se encuentra bajo investigación activa a partir de 2018. [261] [178] [262]
Los andrógenos tópicos se han utilizado y estudiado en el tratamiento de la celulitis en mujeres. [263] Se ha descubierto que la androstanolona tópica en el abdomen disminuye significativamente la grasa abdominal subcutánea en las mujeres y, por lo tanto, puede ser útil para mejorar la silueta corporal. [263] Sin embargo, los hombres y las mujeres hiperandrogénicas tienen mayores cantidades de grasa abdominal que las mujeres sanas, y se ha descubierto que los andrógenos aumentan la grasa abdominal también en mujeres posmenopáusicas y hombres transgénero . [264]
Véase también
Referencias
- ^ Ganesan K, Rahman S, Zito PM (2023). "Esteroides anabólicos". StatPearls . StatPearls Publishing. PMID 29494025.
Los esteroides anabólicos endógenos, como la testosterona y la dihidrotestosterona, y los esteroides anabólicos sintéticos median sus efectos uniéndose a los receptores de andrógenos y activándolos.
- ^ ab Barrett-Connor EL (junio de 1995). "Testosterona y factores de riesgo de enfermedad cardiovascular en hombres". Diabète & Métabolisme . 21 (3): 156–161. PMID 7556805.
- ^ ab Yamamoto Y, Moore R, Hess HA, Guo GL, Gonzalez FJ, Korach KS, et al. (junio de 2006). "El receptor de estrógeno alfa media el 17alfa-etinilestradiol causando hepatotoxicidad". The Journal of Biological Chemistry . 281 (24): 16625–16631. doi : 10.1074/jbc.M602723200 . PMID 16606610. S2CID 83319949.
- ^ ab De Piccoli B, Giada F, Benettin A, Sartori F, Piccolo E (agosto de 1991). "Uso de esteroides anabólicos en culturistas: un estudio ecocardiográfico de la morfología y función del ventrículo izquierdo". Revista internacional de medicina deportiva . 12 (4): 408–412. doi :10.1055/s-2007-1024703. PMID 1917226. S2CID 19425569.
- ^ abc Green GA (septiembre de 2009). "Uso de fármacos que mejoran el rendimiento". Ortopedia . 32 (9): 647–649. doi :10.3928/01477447-20090728-39. PMID 19751025.
- ^ abc Turillazzi E, Perilli G, Di Paolo M, Neri M, Riezzo I, Fineschi V (mayo de 2011). "Efectos secundarios del abuso de EAA: una descripción general". Mini Reseñas en Química Medicinal . 11 (5): 374–389. doi :10.2174/138955711795445925. hdl : 11392/2357154 . PMID 21443513.
- ^ abcdefghijk Hartgens F, Kuipers H (2004). "Efectos de los esteroides anabólicos androgénicos en atletas". Medicina deportiva . 34 (8): 513–554. doi :10.2165/00007256-200434080-00003. PMID 15248788. S2CID 15234016.
- ^ abc Kicman AT, Gower DB (julio de 2003). "Esteroides anabólicos en el deporte: perspectivas bioquímicas, clínicas y analíticas". Anales de bioquímica clínica . 40 (parte 4): 321–356. doi :10.1258/000456303766476977. PMID 12880534. S2CID 24339701.

- ^ Powers M (2011). "Fármacos que mejoran el rendimiento". En Houglum J, Harrelson GL (eds.). Principios de farmacología para entrenadores deportivos (2.ª ed.). SLACK Incorporated. pág. 345. ISBN 978-1-55642-901-9Archivado desde el original el 22 de diciembre de 2016 . Consultado el 17 de octubre de 2016 .
- ^ abc Basaria S, Wahlstrom JT, Dobs AS (noviembre de 2001). "Revisión clínica 138: Terapia con esteroides anabólicos-androgénicos en el tratamiento de enfermedades crónicas". The Journal of Clinical Endocrinology and Metabolism . 86 (11): 5108–5117. doi : 10.1210/jcem.86.11.7983 . PMID 11701661.
[...] en un estudio reciente en animales, Hsiao et al. (10) encontraron dos tipos diferentes de elementos de respuesta a los andrógenos que podrían responder de manera diferencial a T y DHT. Por lo tanto, es posible que una secuencia selectiva de elementos de respuesta a los andrógenos pueda desempeñar un papel en la transactivación diferencial de AR T vs. DHT.
- ^ Ranke MB, Bierich JR (agosto de 1986). "Tratamiento de la deficiencia de la hormona del crecimiento". Clinics in Endocrinology and Metabolism . 15 (3): 495–510. doi :10.1016/S0300-595X(86)80008-1. PMID 2429792.
- ^ ab Grunfeld C, Kotler DP, Dobs A, Glesby M, Bhasin S (marzo de 2006). "Oxandrolona en el tratamiento de la pérdida de peso asociada al VIH en hombres: un estudio aleatorizado, doble ciego, controlado con placebo". Journal of Acquired Immune Deficiency Syndromes . 41 (3): 304–314. doi : 10.1097/01.qai.0000197546.56131.40 . PMID 16540931. S2CID 25911263.
- ^ Berger JR, Pall L, Hall CD, Simpson DM, Berry PS, Dudley R (diciembre de 1996). "Oxandrolona en la miopatía debilitante por SIDA". AIDS . 10 (14): 1657–1662. doi :10.1097/00002030-199612000-00010. PMID 8970686. S2CID 9832782.
- ^ Kenny AM, Prestwood KM, Gruman CA, Marcello KM, Raisz LG (mayo de 2001). "Efectos de la testosterona transdérmica sobre los huesos y músculos en hombres mayores con niveles bajos de testosterona biodisponible". The Journals of Gerontology. Serie A, Ciencias biológicas y ciencias médicas . 56 (5): M266–M272. doi : 10.1093/gerona/56.5.M266 . PMID 11320105.
- ^ Baum NH, Crespi CA (septiembre de 2007). "Reemplazo de testosterona en hombres de edad avanzada". Geriatría . 62 (9): 15–18. PMID 17824721.
- ^ Francis RM (octubre de 2001). "Reemplazo de andrógenos en hombres que envejecen". Calcified Tissue International . 69 (4): 235–238. doi :10.1007/s00223-001-1051-9. PMID 11730258. S2CID 24170276.
- ^ Nair KS, Rizza RA, O'Brien P, Dhatariya K, Short KR, Nehra A, et al. (octubre de 2006). "DHEA en mujeres mayores y DHEA o testosterona en hombres mayores". La Revista de Medicina de Nueva Inglaterra . 355 (16): 1647–1659. doi : 10.1056/NEJMoa054629 . hdl : 11577/2443403 . PMID 17050889. S2CID 42844580.
- ^ abcd Mangus BC, Miller MG (11 de enero de 2005). "Agentes para el desarrollo muscular utilizados en el deporte". Aplicación de la farmacología en el entrenamiento atlético . FA Davis. págs. 151–. ISBN 978-0-8036-2027-8Archivado del original el 14 de abril de 2021 . Consultado el 25 de junio de 2017 .
- ^ Real Colegio de Médicos de Londres (1999). Osteoporosis: pautas clínicas para la prevención y el tratamiento. Real Colegio de Médicos. pp. 51–. ISBN 978-1-86016-079-0Archivado del original el 14 de abril de 2021 . Consultado el 25 de junio de 2017 .
- ^ Davis SR (1999). "El uso terapéutico de los andrógenos en mujeres". Revista de bioquímica de esteroides y biología molecular . 69 (1–6): 177–184. doi :10.1016/s0960-0760(99)00054-0. PMID 10418991. S2CID 23520067.
- ^ Taylor WN (16 de enero de 2002). "Usos médicos actuales y futuros de los esteroides anabólicos". Esteroides anabólicos y el atleta (2.ª ed.). McFarland. pp. 193–. ISBN 978-0-7864-1128-3Archivado del original el 14 de abril de 2021 . Consultado el 25 de junio de 2017 .
- ^ ab "Comprimidos de oxandrolona, USP – Solo con receta" (PDF) . Drugs@FDA . Administración de Alimentos y Medicamentos de los Estados Unidos. 1 de diciembre de 2006. Archivado (PDF) del original el 26 de agosto de 2016 . Consultado el 21 de junio de 2016 .
- ^ ab "Oxandrin (comprimidos de oxandrolona, USP)" (PDF) . Drugs@FDA . BTG Pharmaceuticals, Administración de Alimentos y Medicamentos de los Estados Unidos. 21 de abril de 2003. Archivado (PDF) del original el 1 de marzo de 2017 . Consultado el 21 de junio de 2016 .
- ^ Li H, Guo Y, Yang Z, Roy M, Guo Q (junio de 2016). "La eficacia y seguridad del tratamiento con oxandrolona para pacientes con quemaduras graves: una revisión sistemática y un metanálisis". Burns . 42 (4): 717–727. doi :10.1016/j.burns.2015.08.023. PMID 26454425. S2CID 24139354.
- ^ Rojas Y, Finnerty CC, Radhakrishnan RS, Herndon DN (diciembre de 2012). "Quemaduras: una actualización sobre la farmacoterapia actual". Opinión de expertos sobre farmacoterapia . 13 (17): 2485–2494. doi :10.1517/14656566.2012.738195. PMC 3576016. PMID 23121414 .
- ^ Bork K (agosto de 2012). "Opciones de tratamiento actuales para el angioedema hereditario". Current Allergy and Asthma Reports . 12 (4): 273–280. doi :10.1007/s11882-012-0273-4. PMID 22729959. S2CID 207323793.
- ^ Choi G, Runyon BA (mayo de 2012). "Hepatitis alcohólica: guía para el médico". Clinics in Liver Disease . 16 (2): 371–385. doi :10.1016/j.cld.2012.03.015. PMID 22541704.
- ^ Ebadi M (31 de octubre de 2007). "Metiltestosterona". Referencia de farmacología clínica (segunda edición). CRC Press. pp. 434–. ISBN 978-1-4200-4744-8Archivado del original el 14 de abril de 2021 . Consultado el 27 de julio de 2018 .
- ^ Mariotti A (19 de marzo de 2010). "Hormonas esteroides de la reproducción y el desarrollo sexual". En Yagiela JA, Dowd FJ, Johnson B, Mariotti A, Neidle EA (eds.). Farmacología y terapéutica para odontología – Libro electrónico . Elsevier Health Sciences. págs. 569–. ISBN 978-0-323-07824-5Archivado del original el 14 de abril de 2021 . Consultado el 27 de julio de 2018 .
- ^ "Android® C-III Label" (PDF) . Archivado (PDF) del original el 10 de febrero de 2017 . Consultado el 27 de julio de 2018 .
- ^ ""El uso de hormonas esteroides para estimular el crecimiento en animales destinados a la producción de alimentos"". Administración de Alimentos y Medicamentos . Archivado desde el original el 8 de abril de 2005. Consultado el 14 de mayo de 2024 .
{{cite web}}: CS1 maint: bot: original URL status unknown (link) - ^ Snyder P (diciembre de 2022). «Tratamiento con testosterona del hipogonadismo de aparición tardía: beneficios y riesgos». Rev Endocr Metab Disord . 23 (6): 1151–1157. doi :10.1007/s11154-022-09712-1. PMID 35266057.
- ^ Shah K, Montoya C, Persons RK (abril de 2007). "Investigaciones clínicas. ¿Las inyecciones de testosterona aumentan la libido en pacientes hipogonadales de edad avanzada?". The Journal of Family Practice . 56 (4): 301–303. PMID 17403329.
- ^ Yassin AA, Saad F (marzo de 2007). "Mejora de la función sexual en hombres con hipogonadismo de aparición tardía tratados solo con testosterona". The Journal of Sexual Medicine . 4 (2): 497–501. doi :10.1111/j.1743-6109.2007.00442.x. PMID 17367445.
- ^ Arver S, Dobs AS, Meikle AW, Caramelli KE, Rajaram L, Sanders SW, Mazer NA (diciembre de 1997). "Eficacia y seguridad a largo plazo de un sistema transdérmico de testosterona con permeación mejorada en hombres hipogonadales". Endocrinología clínica . 47 (6): 727–737. doi :10.1046/j.1365-2265.1997.3071113.x. PMID 9497881. S2CID 31976796.
- ^ Nieschlag E, Büchter D, Von Eckardstein S, Abshagen K, Simoni M, Behre HM (diciembre de 1999). "Inyecciones intramusculares repetidas de undecanoato de testosterona para terapia de sustitución en hombres hipogonadales". Endocrinología clínica . 51 (6): 757–763. doi :10.1046/j.1365-2265.1999.00881.x. PMID 10619981. S2CID 19174381.
- ^ Arslanian S, Suprasongsin C (octubre de 1997). "Tratamiento con testosterona en adolescentes con pubertad tardía: cambios en la composición corporal, proteínas, grasas y metabolismo de la glucosa". The Journal of Clinical Endocrinology and Metabolism . 82 (10): 3213–3220. doi : 10.1210/jcem.82.10.4293 . PMID 9329341. S2CID 5031396.
- ^ Moore E, Wisniewski A, Dobs A (agosto de 2003). "Tratamiento endocrino de personas transexuales: una revisión de los regímenes de tratamiento, los resultados y los efectos adversos". The Journal of Clinical Endocrinology and Metabolism . 88 (8): 3467–3473. doi : 10.1210/jc.2002-021967 . PMID 12915619.
- ^ Notaro K (24 de octubre de 2013). «Genderqueer, Pansexual, LGBTQ: ¿Existirá el género dentro de 100 años? – Reiniciado». Instituto de Ética y Tecnologías Emergentes (IEET) . Archivado desde el original el 9 de diciembre de 2014. Consultado el 17 de noviembre de 2014 .
- ^ Leigh S (12 de febrero de 2014). «Jóvenes que exploran roles de género no binarios». SF Gate . Archivado desde el original el 8 de diciembre de 2014. Consultado el 17 de noviembre de 2014 .
- ^ Warne GL, Grover S, Zajac JD (2005). "Terapias hormonales para personas con condiciones intersexuales: protocolo de uso". Tratamientos en endocrinología . 4 (1): 19–29. doi :10.2165/00024677-200504010-00003. PMID 15649098. S2CID 71737774.
- ^ "¿Qué es la intersexualidad? Preguntas frecuentes sobre la intersexualidad, por Inter/Act". Inter/Act Youth . 12 de septiembre de 2014. Archivado desde el original el 7 de diciembre de 2014. Consultado el 5 de diciembre de 2014 .
{{cite web}}: CS1 maint: unfit URL (link) - ^ Kardinal CG, Bobba RK, Cole JT (30 de julio de 2012). "Cáncer de mama". En Perry MC, Doll DC, Freter CE (eds.). Perry's The Chemotherapy Source Book . Lippincott Williams & Wilkins. págs. 409–. ISBN 978-1-4698-0343-2Archivado del original el 14 de abril de 2021 . Consultado el 25 de junio de 2017 .
- ^ Allegra JC, Bertino J, Bonomi P, Byrne P, Carpenter J, Catalano R, et al. (diciembre de 1985). "Cáncer de mama metastásico: resultados preliminares con terapia hormonal oral". Seminars in Oncology . 12 (4 Suppl 6): 61–64. PMID 3909420.
- ^ Bachmann GA (marzo de 1999). "Coterapia con andrógenos en la menopausia: evolución de los beneficios y desafíos". American Journal of Obstetrics and Gynecology . 180 (3 Pt 2): S308–S311. doi :10.1016/S0002-9378(99)70724-6. PMID 10076169.
- ^ Kotz K, Alexander JL, Dennerstein L (octubre de 2006). "Terapia hormonal con estrógenos y andrógenos y bienestar en mujeres posmenopáusicas quirúrgicas". Journal of Women's Health . 15 (8): 898–908. doi :10.1089/jwh.2006.15.898. PMID 17087613.
- ^ Garefalakis M, Hickey M (2008). "El papel de los andrógenos, progestinas y tibolona en el tratamiento de los síntomas de la menopausia: una revisión de la evidencia clínica". Intervenciones clínicas en el envejecimiento . 3 (1): 1–8. doi : 10.2147/CIA.S1043 . PMC 2544356 . PMID 18488873.
- ^ ab Somboonporn W (agosto de 2006). "Andrógenos y menopausia". Current Opinion in Obstetrics & Gynecology . 18 (4): 427–432. doi :10.1097/01.gco.0000233938.36554.37. PMID 16794424. S2CID 8030248.
- ^ Davis S (marzo de 2001). "Deficiencia de testosterona en mujeres". The Journal of Reproductive Medicine . 46 (3 Suppl): 291–296. PMID 11304877.
- ^ abc Nieschlag E (noviembre de 2010). «Ensayos clínicos en anticoncepción hormonal masculina» (PDF) . Anticoncepción . 82 (5): 457–470. doi :10.1016/j.contraception.2010.03.020. PMID 20933120. Archivado (PDF) del original el 5 de diciembre de 2020. Consultado el 18 de agosto de 2019 .
- ^ Baalmann J (19 de junio de 2017). "La testosterona puede ser parte de su plan de tratamiento para la enfermedad de Raynaud". BioBalance Health . Consultado el 9 de junio de 2023 .
- ^ "La mayoría de los usuarios de esteroides no son deportistas, según un estudio". Reuters . Reuters. 21 de noviembre de 2007. Archivado desde el original el 25 de enero de 2016 . Consultado el 3 de enero de 2014 .
- ^ Sjöqvist F, Garle M, Rane A (mayo de 2008). "Uso de agentes dopantes, en particular esteroides anabólicos, en el deporte y la sociedad". Lancet . 371 (9627): 1872–1882. doi :10.1016/S0140-6736(08)60801-6. PMID 18514731. S2CID 10762429.
- ^ Yesalis CE, Kennedy NJ, Kopstein AN, Bahrke MS (septiembre de 1993). "Uso de esteroides anabólicos androgénicos en los Estados Unidos". JAMA . 270 (10): 1217–1221. doi :10.1001/jama.270.10.1217. PMID 8355384.
- ^ Koley S (19 de noviembre de 2020). Fisiología del ejercicio. Friends Publications (India). ISBN 978-81-947997-5-7.
- ^ McCabe SE, Brower KJ, West BT, Nelson TF, Wechsler H (octubre de 2007). "Tendencias en el uso no médico de esteroides anabólicos por parte de estudiantes universitarios estadounidenses: resultados de cuatro encuestas nacionales". Dependencia de drogas y alcohol . 90 (2–3): 243–251. doi :10.1016/j.drugalcdep.2007.04.004. PMC 2383927. PMID 17512138 .
- ^ Parkinson AB, Evans NA (abril de 2006). "Esteroides anabólicos androgénicos: una encuesta a 500 usuarios". Medicina y ciencia en deportes y ejercicio . 38 (4): 644–651. doi : 10.1249/01.mss.0000210194.56834.5d . PMID 16679978.
- ^ abcde Cohen J, Collins R, Darkes J, Gwartney D (octubre de 2007). "Una liga propia: demografía, motivaciones y patrones de uso de 1.955 usuarios adultos masculinos de esteroides anabólicos no médicos en los Estados Unidos". Revista de la Sociedad Internacional de Nutrición Deportiva . 4 : 12. doi : 10.1186/1550-2783-4-12 . PMC 2131752 . PMID 17931410.
- ^ Copeland J, Peters R, Dillon P (marzo de 1998). "Un estudio de 100 usuarios de esteroides anabólicos androgénicos". The Medical Journal of Australia . 168 (6): 311–312. doi :10.5694/j.1326-5377.1998.tb140177.x. PMID 9549549. S2CID 8699231.
- ^ Eastley T (18 de enero de 2006). «Estudio sobre esteroides desacredita estereotipos de usuarios». ABC . Archivado desde el original el 16 de julio de 2014. Consultado el 3 de enero de 2014 .
- ^ Pope HG, Kanayama G, Ionescu-Pioggia M, Hudson JI (septiembre de 2004). "Actitudes de los usuarios de esteroides anabólicos hacia los médicos". Adicción . 99 (9): 1189–1194. doi :10.1111/j.1360-0443.2004.00781.x. PMID 15317640.
- ^ Kanayama G, Barry S, Hudson JI, Pope HG (abril de 2006). "Imagen corporal y actitudes hacia los roles masculinos en usuarios de esteroides anabólicos androgénicos". The American Journal of Psychiatry . 163 (4): 697–703. doi :10.1176/appi.ajp.163.4.697. PMID 16585446. S2CID 38738640.
- ^ Grogan S, Shepherd S, Evans R, Wright S, Hunter G (noviembre de 2006). "Experiencias del uso de esteroides anabólicos: entrevistas en profundidad con hombres y mujeres culturistas". Revista de Psicología de la Salud . 11 (6): 845–856. doi :10.1177/1359105306069080. PMID 17035257. S2CID 5794238.
- ^ ab Hickson RC, Czerwinski SM, Falduto MT, Young AP (junio de 1990). "Antagonismo de los glucocorticoides por el ejercicio y los esteroides anabólicos androgénicos". Medicina y ciencia en deportes y ejercicio . 22 (3): 331–340. doi :10.1249/00005768-199006000-00010. PMID 2199753.
- ^ "Drugs@FDA: Productos farmacéuticos aprobados por la FDA". Administración de Alimentos y Medicamentos de los Estados Unidos. Archivado desde el original el 16 de noviembre de 2016. Consultado el 1 de diciembre de 2019 .
- ^ Hamilton RJ, Duffy NA, Stone D (2014). "Andrógenos/esteroides anabólicos". Farmacopea de Tarascon . Jones & Bartlett Publishers. págs. 174–. ISBN 978-1-284-05671-6Archivado del original el 13 de febrero de 2021 . Consultado el 13 de septiembre de 2020 .
- ^ Ford SM, Roach SS (2010). Farmacología clínica introductoria de Roach. Lippincott Williams & Wilkins. pp. 499–. ISBN 978-1-60547-633-9Archivado del original el 14 de abril de 2021 . Consultado el 13 de septiembre de 2020 .
- ^ Lemke TL, Williams DA (24 de enero de 2012). Principios de química medicinal de Foye. Lippincott Williams & Wilkins. pp. 1358–. ISBN 978-1-60913-345-0Archivado del original el 14 de abril de 2021 . Consultado el 13 de septiembre de 2020 .
- ^ Colby HD, Longhurst PA (6 de diciembre de 2012). "Esteroides anabólicos en el cuerpo". En Thomas JA (ed.). Drogas, atletas y rendimiento físico . Springer Science & Business Media. págs. 20–. ISBN 978-1-4684-5499-4Archivado del original el 14 de abril de 2021 . Consultado el 13 de septiembre de 2020 .
- ^ abcdefghijklmnopqrst William Llewellyn (2011). Anabólicos. Molecular Nutrition Llc. ISBN 978-0-9828280-1-4Archivado del original el 14 de abril de 2021 . Consultado el 2 de diciembre de 2016 .
- ^ Burkett LN, Falduto MT (1984). "Uso de esteroides por parte de atletas en un área metropolitana". El médico y la medicina deportiva . 12 (8): 69–74. doi :10.1080/00913847.1984.11701923. ISSN 0091-3847.
- ^ Bain J, Schill WB, Schwarzstein L (6 de diciembre de 2012). Tratamiento de la infertilidad masculina. Springer Science & Business Media. pp. 176–177. ISBN 978-3-642-68223-0Archivado del original el 13 de febrero de 2021 . Consultado el 13 de septiembre de 2020 .
- ^ Snyder PJ (1984). "Uso clínico de andrógenos". Revista Anual de Medicina . 35 (1): 207–217. doi :10.1146/annurev.me.35.020184.001231. PMID 6372655.
- ^ abc Matsumoto AM (2001). "Uso clínico y abuso de andrógenos y antiandrógenos". En Becker KL (ed.). Principios y práctica de endocrinología y metabolismo . Lippincott Williams & Wilkins. págs. 1185–1186. ISBN 978-0-7817-1750-2Archivado del original el 17 de mayo de 2020 . Consultado el 17 de octubre de 2016 .
- ^ abcdefghijklmnopqrstu vwxyz aa ab ac ad ae af ag ah ai aj ak al am an ao ap aq ar as at au av aw ax ay az ba bb bc bd be bf bg bh bi bj bk bl bm bn bo bp Kicman AT (junio de 2008). "Farmacología de los esteroides anabólicos". British Journal of Pharmacology . 154 (3): 502–521. doi :10.1038/bjp.2008.165. PMC 2439524 . PMID 18500378.
- ^ ab Rahnema CD, Crosnoe LE, Kim ED (marzo de 2015). "Esteroides de diseño: suplementos de venta libre y su componente androgénico: revisión de un problema creciente". Andrology . 3 (2): 150–155. doi : 10.1111/andr.307 . PMID 25684733. S2CID 6999218.
- ^ ab Katzung BG, Chrousos GP, eds. (2012). "Las hormonas gonadales y sus inhibidores". Farmacología básica y clínica . Nueva York Londres: McGraw-Hill Medical Distribuidor de McGraw-Hill. ISBN 978-0-07-176401-8.
- ^ Mutzebaugh C (diciembre de 1998). "¿Realmente marca la diferencia la elección de alfa-AAS?". HIV Hotline . 8 (5–6): 10–11. PMID 11366379.
- ^ Nutt DJ, King LA, Phillips LD (noviembre de 2010). "Daños de las drogas en el Reino Unido: un análisis de decisiones multicriterio". Lancet . 376 (9752): 1558–1565. CiteSeerX 10.1.1.690.1283 . doi :10.1016/S0140-6736(10)61462-6. PMID 21036393. S2CID 5667719.
- ^ Casavant MJ, Blake K, Griffith J, Yates A, Copley LM (agosto de 2007). "Consecuencias del uso de esteroides anabólicos androgénicos". Clínicas pediátricas de Norteamérica . 54 (4): 677–90, x. doi :10.1016/j.pcl.2007.04.001. PMID 17723870.
- ^ Pope HG, Wood RI, Rogol A, Nyberg F, Bowers L, Bhasin S (junio de 2014). "Consecuencias adversas para la salud de las drogas que mejoran el rendimiento: una declaración científica de la Endocrine Society". Endocrine Reviews . 35 (3): 341–375. doi :10.1210/er.2013-1058. PMC 4026349 . PMID 24423981.
- ^ ab Fragkaki AG, Angelis YS, Koupparis M, Tsantili-Kakoulidou A, Kokotos G, Georgakopoulos C (febrero de 2009). "Características estructurales de los esteroides anabólicos androgénicos que contribuyen a la unión al receptor de andrógenos y a sus actividades anabólicas y androgénicas. Modificaciones aplicadas en la estructura esteroidal". Esteroides . 74 (2): 172–197. doi :10.1016/j.steroids.2008.10.016. PMID 19028512. S2CID 41356223.
- ^ Nieschlag E, Vorona E (agosto de 2015). "MECANISMOS EN ENDOCRINOLOGÍA: consecuencias médicas del dopaje con esteroides anabólicos androgénicos: efectos sobre las funciones reproductivas". Revista Europea de Endocrinología . 173 (2): R47–R58. doi : 10.1530/EJE-15-0080 . PMID 25805894.
- ^ Hall RC, Hall RC, Chapman MJ (2005). "Complicaciones psiquiátricas del abuso de esteroides anabólicos". Psychosomatics . 46 (4): 285–290. doi : 10.1176/appi.psy.46.4.285 . PMID 16000671.
- ^ ab Trenton AJ, Currier GW (2005). "Manifestaciones conductuales del uso de esteroides anabólicos". Fármacos para el SNC . 19 (7): 571–595. doi :10.2165/00023210-200519070-00002. PMID 15984895. S2CID 32243658.
- ^ Vanberg P, Atar D (2009). "Abuso de esteroides anabólicos androgénicos y el sistema cardiovascular". Dopaje en el deporte . Manual de farmacología experimental. Vol. 195. Springer. págs. 411–57. doi :10.1007/978-3-540-79088-4_18. ISBN . 978-3-540-79087-7.PMID20020375 .
- ^ Achar S, Rostamian A, Narayan SM (septiembre de 2010). "Efectos cardíacos y metabólicos del abuso de esteroides anabólicos androgénicos sobre los lípidos, la presión arterial, las dimensiones del ventrículo izquierdo y el ritmo". The American Journal of Cardiology . 106 (6): 893–901. doi :10.1016/j.amjcard.2010.05.013. PMC 4111565 . PMID 20816133.
- ^ Solimini R, Rotolo MC, Mastrobattista L, Mortali C, Minutillo A, Pichini S, et al. (marzo de 2017). "Hepatotoxicidad asociada con el uso ilícito de esteroides anabólicos androgénicos en el dopaje". Revista Europea de Ciencias Médicas y Farmacológicas . 21 (1 Suppl): 7–16. PMID 28379599.
- ^ Brenu EW, McNaughton L, Marshall-Gradisnik SM (mayo de 2011). "¿Existe una posible disfunción inmunológica con el uso de esteroides anabólicos androgénicos?: una revisión". Mini Reviews in Medicinal Chemistry . 11 (5): 438–445. doi :10.2174/138955711795445907. PMID 21443507.
- ^ Grace F, Sculthorpe N, Baker J, Davies B (septiembre de 2003). "Respuesta del producto presión arterial y frecuencia cardíaca en hombres que usan esteroides anabólicos androgénicos (EAA) en dosis altas". Journal of Science and Medicine in Sport . 6 (3): 307–312. doi :10.1016/S1440-2440(03)80024-5. PMID 14609147.
- ^ "DailyMed: Acerca de DailyMed". Dailymed.nlm.nih.gov. Archivado desde el original el 12 de mayo de 2009. Consultado el 3 de noviembre de 2008 .
- ^ Bagatell CJ, Knopp RH, Vale WW, Rivier JE, Bremner WJ (junio de 1992). "Los niveles fisiológicos de testosterona en hombres normales suprimen los niveles de colesterol de lipoproteínas de alta densidad". Anales de Medicina Interna . 116 (12 Pt 1): 967–973. doi :10.7326/0003-4819-116-12-967. PMID 1586105.
- ^ Mewis C, Spyridopoulos I, Kühlkamp V, Seipel L (febrero de 1996). "Manifestación de enfermedad coronaria grave tras el abuso de fármacos anabólicos". Cardiología clínica . 19 (2): 153–155. doi :10.1002/clc.4960190216. PMID 8821428. S2CID 37024092.
- ^ Melnik B, Jansen T, Grabbe S (febrero de 2007). "Abuso de esteroides anabolizantes androgénicos y acné culturismo: un problema de salud subestimado". Journal der Deutschen Dermatologischen Gesellschaft = Revista de la Sociedad Alemana de Dermatología . 5 (2): 110-117. doi :10.1111/j.1610-0387.2007.06176.x. PMID 17274777. S2CID 13382470.
- ^ Vierhapper H, Maier H, Nowotny P, Waldhäusl W (julio de 2003). "Tasas de producción de testosterona y de dihidrotestosterona en la pérdida de cabello de patrón femenino". Metabolism . 52 (7): 927–929. doi :10.1016/S0026-0495(03)00060-X. PMID 12870172.
- ^ Irving LM, Wall M, Neumark-Sztainer D, Story M (abril de 2002). "Uso de esteroides entre adolescentes: hallazgos del Proyecto EAT". The Journal of Adolescent Health . 30 (4): 243–252. doi :10.1016/S1054-139X(01)00414-1. PMID 11927236.
- ^ "Carcinógenos humanos conocidos y probables". Sociedad Estadounidense del Cáncer. 29 de junio de 2011. Archivado desde el original el 17 de noviembre de 2014. Consultado el 17 de noviembre de 2014 .
- ^ Sullivan ML, Martinez CM, Gallagher EJ (1999). "Fibrilación auricular y esteroides anabólicos". Revista de Medicina de Urgencias . 17 (5): 851–857. doi :10.1016/S0736-4679(99)00095-5. PMID 10499702.
- ^ Dickerman RD, Schaller F, McConathy WJ (octubre de 1998). "El engrosamiento de la pared del ventrículo izquierdo se produce en atletas de élite con o sin uso de esteroides anabólicos". Cardiología . 90 (2): 145–148. doi :10.1159/000006834. PMID 9778553. S2CID 22123696.
- ^ George KP, Wolfe LA, Burggraf GW (mayo de 1991). "El 'síndrome del corazón atlético'. Una revisión crítica". Medicina deportiva . 11 (5): 300–330. doi :10.2165/00007256-199111050-00003. PMID 1829849. S2CID 45280834.
- ^ Dickerman RD, Schaller F, Zachariah NY, McConathy WJ (abril de 1997). "Tamaño y función del ventrículo izquierdo en culturistas de élite que utilizan esteroides anabólicos". Revista clínica de medicina deportiva . 7 (2): 90–93. doi :10.1097/00042752-199704000-00003. PMID 9113423. S2CID 42891343.
- ^ Salke RC, Rowland TW, Burke EJ (diciembre de 1985). "Tamaño y función del ventrículo izquierdo en culturistas que usan esteroides anabólicos". Medicina y ciencia en deportes y ejercicio . 17 (6): 701–704. doi : 10.1249/00005768-198512000-00014 . PMID 4079743.
- ^ Tokar S (febrero de 2006). "Daño hepático y aumento del riesgo de ataque cardíaco causado por el uso de esteroides anabólicos". Universidad de California – San Francisco. Archivado desde el original el 14 de junio de 2011. Consultado el 24 de abril de 2007 .
- ^ Wit JM, Oostdijk W (junio de 2015). "Nuevos enfoques para la terapia de la baja estatura". Mejores prácticas e investigación. Endocrinología clínica y metabolismo . 29 (3): 353–366. doi :10.1016/j.beem.2015.01.003. PMID 26051296.
- ^ Marcus R, Korenman SG (1976). "Estrógenos y el varón humano". Revista Anual de Medicina . 27 : 357–370. doi :10.1146/annurev.me.27.020176.002041. PMID 779604.
- ^ Matsumoto AM (enero de 1990). "Efectos de la administración crónica de testosterona en hombres normales: seguridad y eficacia de la testosterona en dosis altas y supresión paralela dependiente de la dosis de la hormona luteinizante, la hormona folículo estimulante y la producción de esperma". The Journal of Clinical Endocrinology and Metabolism . 70 (1): 282–287. doi :10.1210/jcem-70-1-282. PMID 2104626.
- ^ Hoffman JR, Ratamess NA (1 de junio de 2006). "Cuestiones médicas asociadas con el uso de esteroides anabólicos: ¿son exageradas?" (PDF) . Revista de ciencia y medicina del deporte . Archivado (PDF) desde el original el 20 de junio de 2007. Consultado el 8 de mayo de 2007 .
- ^ Meriggiola MC, Costantino A, Bremner WJ, Morselli-Labate AM (2002). "Una dosis más alta de testosterona afecta la supresión de esperma inducida por un régimen combinado de andrógenos y progestinas". Journal of Andrology . 23 (5): 684–690. doi :10.1002/j.1939-4640.2002.tb02311.x. hdl : 1773/4474 . PMID 12185103. S2CID 2400041.
- ^ Alén M, Reinilä M, Vihko R (junio de 1985). "Respuesta de las hormonas séricas a la administración de andrógenos en atletas de potencia". Medicina y ciencia en deportes y ejercicio . 17 (3): 354–359. doi :10.1249/00005768-198506000-00009. PMID 2991700.
- ^ Franke WW, Berendonk B (julio de 1997). "Dopaje hormonal y androgenización de deportistas: un programa secreto del gobierno de la República Democrática Alemana". Química clínica . 43 (7): 1262–1279. doi : 10.1093/clinchem/43.7.1262 . PMID 9216474.
- ^ Manikkam M, Crespi EJ, Doop DD, Herkimer C, Lee JS, Yu S, et al. (febrero de 2004). "Programación fetal: el exceso de testosterona prenatal conduce a un retraso del crecimiento fetal y al crecimiento de recuperación postnatal en ovejas". Endocrinología . 145 (2): 790–798. doi : 10.1210/en.2003-0478 . PMID 14576190.
- ^ Herlitz LC, Markowitz GS, Farris AB, Schwimmer JA, Stokes MB, Kunis C, et al. (29 de octubre de 2009). Desarrollo de FSGS después del uso de esteroides anabólicos en culturistas (PDF) . 42.ª Reunión Anual y Exposición Científica de la Sociedad Estadounidense de Nefrología. Archivado (PDF) del original el 7 de octubre de 2018. Consultado el 17 de noviembre de 2014 .
- ^ Nutt D, King LA, Saulsbury W, Blakemore C (marzo de 2007). "Desarrollo de una escala racional para evaluar el daño de las drogas de posible uso indebido". Lancet . 369 (9566): 1047–1053. doi :10.1016/S0140-6736(07)60464-4. PMID 17382831. S2CID 5903121.
- ^ abc Kanayama G, Hudson JI, Pope HG (noviembre de 2008). "Consecuencias psiquiátricas y médicas a largo plazo del abuso de esteroides anabólicos androgénicos: ¿un problema inminente de salud pública?". Dependencia de drogas y alcohol . 98 (1–2): 1–12. doi :10.1016/j.drugalcdep.2008.05.004. PMC 2646607. PMID 18599224 .
- ^ Brower KJ (octubre de 2002). "Abuso y dependencia de esteroides anabólicos". Current Psychiatry Reports . 4 (5): 377–387. doi :10.1007/s11920-002-0086-6. PMID 12230967. S2CID 25684227.
- ^ ab Rashid H, Ormerod S, Day E (2007). "Esteroides anabólicos androgénicos: lo que el psiquiatra necesita saber". Avances en el tratamiento psiquiátrico . 13 (3): 203–211. doi : 10.1192/apt.bp.105.000935 .
- ^ Cooper CJ, Noakes TD, Dunne T, Lambert MI, Rochford K (septiembre de 1996). "Una alta prevalencia de rasgos de personalidad anormales en usuarios crónicos de esteroides anabólicos androgénicos". British Journal of Sports Medicine . 30 (3): 246–250. doi :10.1136/bjsm.30.3.246. PMC 1332342 . PMID 8889121.
- ^ "Dr. Ritchi Morris". Vitalquests.org. Archivado desde el original el 3 de diciembre de 2013. Consultado el 1 de diciembre de 2013 .
- ^ Kanayama G, Brower KJ, Wood RI, Hudson JI, Pope HG (diciembre de 2009). "Dependencia de esteroides anabólicos-androgénicos: un trastorno emergente". Adicción . 104 (12): 1966–1978. doi :10.1111/j.1360-0443.2009.02734.x. PMC 2780436 . PMID 19922565.
- ^ Eisenberg ER, Galloway GP (1992). "Esteroides anabólicos androgénicos". En Lowinson JH, Ruiz P, Millman RB (eds.). Abuso de sustancias: un libro de texto completo . Lippincott Williams & Wilkins. ISBN 978-0-683-05211-4.
- ^ Lindström M, Nilsson AL, Katzman PL, Janzon L, Dymling JF (junio de 1990). "Uso de esteroides anabólicos androgénicos entre culturistas: frecuencia y actitudes". Journal of Internal Medicine . 227 (6): 407–411. doi :10.1111/j.1365-2796.1990.tb00179.x. PMID 2351927. S2CID 22121959.
- ^ abc Lenahan P (2003). Esteroides anabólicos y otras drogas que mejoran el rendimiento . Londres: Taylor & Francis. ISBN 0-415-28030-3.
- ^ Thiblin I, Petersson A (febrero de 2005). "Farmacoepidemiología de los esteroides anabólicos androgénicos: una revisión". Farmacología fundamental y clínica . 19 (1): 27–44. doi :10.1111/j.1472-8206.2004.00298.x. PMID 15660958. S2CID 2009549.
- ^ Beaver KM, Vaughn MG, Delisi M, Wright JP (diciembre de 2008). "Uso de esteroides anabólicos androgénicos y participación en conductas violentas en una muestra representativa a nivel nacional de varones adultos jóvenes en los Estados Unidos". American Journal of Public Health . 98 (12): 2185–2187. doi :10.2105/AJPH.2008.137018. PMC 2636528 . PMID 18923108.
- ^ Bahrke MS, Yesalis CE, Wright JE (diciembre de 1996). "Efectos psicológicos y conductuales de la testosterona endógena y los esteroides anabólicos androgénicos. Una actualización". Medicina deportiva . 22 (6): 367–390. doi :10.2165/00007256-199622060-00005. PMID 8969015. S2CID 23846419.
- ^ Uzych L (febrero de 1992). "Esteroides anabólico-androgénicos y efectos psiquiátricos relacionados: una revisión". Revista Canadiense de Psiquiatría. Revue Canadienne de Psychiatrie . 37 (1): 23–28. doi :10.1177/070674379203700106. PMID 1551042. S2CID 22571743.
- ^ abcd El Osta R, Almont T, Diligent C, Hubert N, Eschwège P, Hubert J (2016). "Abuso de esteroides anabólicos e infertilidad masculina". Andrología básica y clínica . 26 (2): 2. doi : 10.1186/s12610-016-0029-4 . PMC 4744441 . PMID 26855782.
- ^ Stromme SB, Meen HD, Aakvaag A (1974). "Efectos de un esteroide anabólico androgénico en el desarrollo de la fuerza y los niveles plasmáticos de testosterona en varones normales". Medicina y ciencia en el deporte . 6 (3): 203–208. PMID 4437350.
- ^ Sagoe D, Molde H, Andreassen CS, Torsheim T, Pallesen S (mayo de 2014). "La epidemiología global del uso de esteroides anabólicos androgénicos: un metaanálisis y un análisis de metarregresión". Anales de Epidemiología . 24 (5): 383–398. doi :10.1007/s40279-017-0709-z. PMID 24582699. S2CID 42489596.
- ^ Christou MA, Christou PA, Markozannes G, Tsatsoulis A, Mastorakos G, Tigas S (septiembre de 2017). "Efectos de los esteroides anabólicos androgénicos en el sistema reproductivo de atletas y usuarios recreativos: una revisión sistemática y un metaanálisis". Medicina deportiva . 47 (9): 1869–1883. doi :10.1007/s40279-017-0709-z. PMID 28258581. S2CID 42489596.
- ^ Pereira de Jésus-Tran K, Côté PL, Cantin L, Blanchet J, Labrie F, Breton R (mayo de 2006). "La comparación de las estructuras cristalinas del dominio de unión del ligando del receptor de andrógenos humano en complejos con varios agonistas revela los determinantes moleculares responsables de la afinidad de unión". Protein Science . 15 (5): 987–999. doi :10.1110/ps.051905906. PMC 2242507 . PMID 16641486.
- ^ Lavery DN, McEwan IJ (noviembre de 2005). "Estructura y función de los dominios de transactivación del receptor de esteroides AF1: inducción de conformaciones activas". The Biochemical Journal . 391 (Pt 3): 449–464. doi :10.1042/BJ20050872. PMC 1276946 . PMID 16238547.
- ^ Cheskis BJ (septiembre de 2004). "Regulación de las cascadas de señalización celular por hormonas esteroides". Journal of Cellular Biochemistry . 93 (1): 20–27. doi :10.1002/jcb.20180. PMID 15352158. S2CID 43430651.
- ^ Brodsky IG, Balagopal P, Nair KS (October 1996). "Effects of testosterone replacement on muscle mass and muscle protein synthesis in hypogonadal men—a clinical research center study". The Journal of Clinical Endocrinology and Metabolism. 81 (10): 3469–3475. doi:10.1210/jcem.81.10.8855787. PMID 8855787.
- ^ Singh R, Artaza JN, Taylor WE, Gonzalez-Cadavid NF, Bhasin S (November 2003). "Androgens stimulate myogenic differentiation and inhibit adipogenesis in C3H 10T1/2 pluripotent cells through an androgen receptor-mediated pathway". Endocrinology. 144 (11): 5081–5088. doi:10.1210/en.2003-0741. PMID 12960001.
- ^ a b Heinlein CA, Chang C (April 2004). "Androgen receptor in prostate cancer". Endocrine Reviews. 25 (2): 276–308. doi:10.1210/er.2002-0032. PMID 15082523. S2CID 24665772.
- ^ Riggs BL, Khosla S, Melton LJ (June 2002). "Sex steroids and the construction and conservation of the adult skeleton". Endocrine Reviews. 23 (3): 279–302. doi:10.1210/edrv.23.3.0465. PMID 12050121. S2CID 28160750.
- ^ Azziz R, Carmina E, Dewailly D, Diamanti-Kandarakis E, Escobar-Morreale HF, Futterweit W, et al. (February 2009). "The Androgen Excess and PCOS Society criteria for the polycystic ovary syndrome: the complete task force report". Fertility and Sterility. 91 (2): 456–488. doi:10.1016/j.fertnstert.2008.06.035. PMID 18950759.
- ^ Schroeder ET, Vallejo AF, Zheng L, Stewart Y, Flores C, Nakao S, et al. (December 2005). "Six-week improvements in muscle mass and strength during androgen therapy in older men". The Journals of Gerontology. Series A, Biological Sciences and Medical Sciences. 60 (12): 1586–1592. doi:10.1093/gerona/60.12.1586. PMID 16424293.
- ^ Giorgi A, Weatherby RP, Murphy PW (December 1999). "Muscular strength, body composition and health responses to the use of testosterone enanthate: a double blind study". Journal of Science and Medicine in Sport. 2 (4): 341–355. doi:10.1016/S1440-2440(99)80007-3. PMID 10710012.
- ^ ab Kuhn CM (2002). "Esteroides anabólicos". Avances recientes en la investigación hormonal . 57 : 411–434. doi : 10.1210/rp.57.1.411 . PMID 12017555.
- ^ Roselli CE (mayo de 1998). "El efecto de los esteroides anabólicos androgénicos sobre la actividad de la aromatasa y la unión al receptor de andrógenos en el área preóptica de la rata". Brain Research . 792 (2): 271–276. doi :10.1016/S0006-8993(98)00148-6. PMID 9593936. S2CID 29441013.
- ^ Hershberger LG, Shipley EG, Meyer RK (mayo de 1953). "Actividad miotrófica de la 19-nortestosterona y otros esteroides determinada por el método modificado del músculo elevador del ano". Actas de la Sociedad de Biología y Medicina Experimental . 83 (1): 175–180. doi :10.3181/00379727-83-20301. PMID 13064212. S2CID 2628925.
- ^ Eriksson A, Kadi F, Malm C, Thornell LE (agosto de 2005). "Morfología del músculo esquelético en levantadores de pesas con y sin esteroides anabólicos". Histoquímica y biología celular . 124 (2): 167–175. doi :10.1007/s00418-005-0029-5. PMID 16059740. S2CID 1887613.
- ^ Reyes-Vallejo L (junio de 2020). "Uso y abuso actual de esteroides anabólicos". Actas Urologicas Espanolas . 44 (5): 309–313. doi :10.1016/j.acuroe.2019.10.007. PMID 32113828. S2CID 229152974.
- ^ Hervey GR, Hutchinson I, Knibbs AV, Burkinshaw L, Jones PR, Norgan NG, Levell MJ (octubre de 1976). "Efectos "anabólicos" de la methandienone en hombres sometidos a entrenamiento atlético". Lancet . 2 (7988): 699–702. doi :10.1016/S0140-6736(76)90001-5. PMID 61389. S2CID 22417506. Archivado desde el original el 29 de noviembre de 2014 . Consultado el 17 de noviembre de 2014 .

- ^ Hervey GR, Knibbs AV, Burkinshaw L, Morgan DB, Jones PR, Chettle DR, Vartsky D (abril de 1981). "Efectos de la metandienona en el rendimiento y la composición corporal de hombres sometidos a entrenamiento atlético". Clinical Science . 60 (4): 457–461. doi :10.1042/cs0600457. PMID 7018798. S2CID 30590287.
- ^ ab Bhasin S, Storer TW, Berman N, Callegari C, Clevenger B, Phillips J, et al. (julio de 1996). "Los efectos de dosis suprafisiológicas de testosterona en el tamaño y la fuerza muscular en hombres normales". The New England Journal of Medicine . 335 (1): 1–7. doi : 10.1056/NEJM199607043350101 . PMID 8637535. S2CID 73721690.
- ^ Bhasin S, Woodhouse L, Casaburi R, Singh AB, Bhasin D, Berman N, et al. (diciembre de 2001). "Relaciones dosis-respuesta de testosterona en hombres jóvenes sanos". Revista estadounidense de fisiología. Endocrinología y metabolismo . 281 (6): E1172–E1181. doi :10.1152/ajpendo.2001.281.6.E1172. PMID 11701431. S2CID 2344757.
- ^ ab Imperato-McGinley J, Peterson RE, Gautier T, Sturla E (mayo de 1979). "Andrógenos y la evolución de la identidad de género masculino entre pseudohermafroditas masculinos con deficiencia de 5alfa-reductasa". The New England Journal of Medicine . 300 (22): 1233–1237. doi :10.1056/NEJM197905313002201. PMID 431680.
- ^ abc Marks LS (2004). "5alfa-reductasa: historia e importancia clínica". Reviews in Urology . 6 (Supl 9): S11–S21. PMC 1472916 . PMID 16985920.
- ^ Sloane E (2002). Biología de la mujer. Cengage Learning. pp. 160–. ISBN 0-7668-1142-5Archivado desde el original el 19 de agosto de 2020 . Consultado el 17 de octubre de 2016 .
- ^ ab Hanno PM, Guzzi TJ, Malkowicz SB, J Wein A (26 de enero de 2014). Manual clínico de urología de Penn. Elsevier Health Sciences. págs. 782–. ISBN 978-0-323-24466-4Archivado desde el original el 19 de agosto de 2020 . Consultado el 17 de octubre de 2016 .
- ^ Saleem M, Siddiqui IA, Mukhtar H (2006). "La bebida de té en la quimioprevención del cáncer de próstata". En Jain NK, Siddiqi M, Weisburger JH (eds.). Efectos protectores del té en la salud humana . CABI. págs. 95–. ISBN 978-1-84593-113-1Archivado desde el original el 22 de diciembre de 2016 . Consultado el 17 de octubre de 2016 .
- ^ Harper C (1 de agosto de 2007). Intersex. Berg. pp. 123–. ISBN 978-1-84788-339-1Archivado desde el original el 19 de agosto de 2020 . Consultado el 17 de octubre de 2016 .
- ^ ab Basaria S, Dobs AS (mayo de 2001). "Hipogonadismo y terapia de reemplazo de andrógenos en hombres mayores". The American Journal of Medicine . 110 (7): 563–572. doi :10.1016/s0002-9343(01)00663-5. PMID 11343670.
Aunque tanto la testosterona como la dihidrotestosterona activan el mismo receptor de andrógenos, las diferencias en la secuencia de elementos de respuesta a los andrógenos son responsables de la regulación diferencial de estas hormonas (21).
- ^ Wang C, Liu Y, Cao JM (septiembre de 2014). "Receptores acoplados a proteína G: mediadores extranucleares para las acciones no genómicas de los esteroides". Revista internacional de ciencias moleculares . 15 (9): 15412–15425. doi : 10.3390/ijms150915412 . PMC 4200746 . PMID 25257522.
- ^ abcd Thomas P, Converse A, Berg HA (febrero de 2018). "ZIP9, un nuevo receptor de andrógenos de membrana y proteína transportadora de zinc". Endocrinología general y comparada . 257 : 130–136. doi :10.1016/j.ygcen.2017.04.016. PMID 28479083.
- ^ abcd Mongan NP, Tadokoro-Cuccaro R, Bunch T, Hughes IA (agosto de 2015). "Síndrome de insensibilidad a los andrógenos". Mejores prácticas e investigación. Endocrinología clínica y metabolismo . 29 (4): 569–580. doi :10.1016/j.beem.2015.04.005. PMID 26303084.
- ^ ab Baroncelli GI, Bertelloni S (30 de noviembre de 2009). "Los efectos de los esteroides sexuales en el crecimiento óseo". En Orwoll ES, Bilezikian JP, Vanderschueren D (eds.). Osteoporosis en hombres: los efectos del género en la salud ósea . Academic Press. págs. 114–. ISBN 978-0-08-092346-8Archivado del original el 14 de abril de 2021 . Consultado el 21 de diciembre de 2017 .
- ^ Rahwan RG (1988). "La farmacología de los andrógenos y los esteroides anabólicos". Revista estadounidense de educación farmacéutica . 52 (2): 167–177. doi :10.1016/S0002-9459(24)03012-2.
- ^ Pi M, Quarles LD (marzo de 2012). "GPRC6A regula la progresión del cáncer de próstata". The Prostate . 72 (4): 399–409. doi :10.1002/pros.21442. PMC 3183291 . PMID 21681779.
- ^ Wu FC, Balasubramanian R, Mulders TM, Coelingh-Bennink HJ (enero de 1999). "Progestágeno oral combinado con testosterona como un posible anticonceptivo masculino: efectos aditivos entre el desogestrel y el enantato de testosterona en la supresión de la espermatogénesis, el eje pituitario-testicular y el metabolismo lipídico". The Journal of Clinical Endocrinology and Metabolism . 84 (1): 112–122. doi : 10.1210/jcem.84.1.5412 . PMID 9920070.
- ^ ab Bitran D, Kellogg CK, Hilvers RJ (diciembre de 1993). "El tratamiento con un esteroide anabólico-androgénico afecta la conducta relacionada con la ansiedad y altera la sensibilidad de los receptores corticales GABAA en la rata". Hormones and Behavior . 27 (4): 568–583. doi :10.1006/hbeh.1993.1041. PMID 8294123. S2CID 29134676.
- ^ ab Masonis AE, McCarthy MP (abril de 1995). "Efectos directos de los esteroides anabólicos/androgénicos, estanozolol y 17 alfa-metiltestosterona, sobre la unión de las benzodiazepinas al receptor del ácido gamma-aminobutírico(a)". Neuroscience Letters . 189 (1): 35–38. doi :10.1016/0304-3940(95)11445-3. PMID 7603620. S2CID 54394931.
- ^ ab Masonis AE, McCarthy MP (octubre de 1996). "Efectos del esteroide androgénico/anabólico estanozolol en la función del receptor GABAA: entrada de 36Cl- estimulada por GABA y unión de [35S] TBPS". The Journal of Pharmacology and Experimental Therapeutics . 279 (1): 186–193. PMID 8858992.
- ^ ab Rivera-Arce JC, Morales-Crespo L, Vargas-Pinto N, Velázquez KT, Jorge JC (junio de 2006). "Efectos centrales del esteroide anabólico 17alfa metiltestosterona en la ansiedad femenina". Farmacología, bioquímica y comportamiento . 84 (2): 275–281. doi :10.1016/j.pbb.2006.05.009. PMID 16814373. S2CID 31725431.
- ^ ab Henderson LP (junio de 2007). "Modulación de la transmisión mediada por el receptor GABAA por esteroides en el hipotálamo: efectos sobre la función reproductiva". Neurofarmacología . 52 (7): 1439–1453. doi :10.1016/j.neuropharm.2007.01.022. PMC 1985867 . PMID 17433821.
- ^ ab Schwartzer JJ, Ricci LA, Melloni RH (octubre de 2009). "Interacciones entre los sistemas neuronales dopaminérgicos y GABAérgicos en el hipotálamo anterior lateral de hámsteres agresivos tratados con AAS". Behavioural Brain Research . 203 (1): 15–22. doi :10.1016/j.bbr.2009.04.007. PMID 19376158. S2CID 26938839.
- ^ Schänzer W (julio de 1996). «Metabolismo de los esteroides anabólicos androgénicos» (PDF) . Química clínica . 42 (7): 1001–1020. doi :10.1093/clinchem/42.7.1001. PMID 8674183. Archivado (PDF) del original el 23 de agosto de 2017. Consultado el 1 de abril de 2019 .
- ^ Attardi BJ, Hild SA, Koduri S, Pham T, Pessaint L, Engbring J, et al. (octubre de 2010). "Los potentes andrógenos sintéticos, dimetandrolona (7α,11β-dimetil-19-nortestosterona) y 11β-metil-19-nortestosterona, no requieren 5α-reducción para ejercer sus efectos androgénicos máximos". The Journal of Steroid Biochemistry and Molecular Biology . 122 (4): 212–218. doi :10.1016/j.jsbmb.2010.06.009. PMC 2949447 . PMID 20599615.
- ^ Wiren KM, Orwoll ES (30 de noviembre de 2009). "Andrógenos y huesos: aspectos básicos". En Orwoll ES, Bilezikian JP, Vanderschueren D (eds.). Osteoporosis en hombres: los efectos del género en la salud esquelética . Academic Press. págs. 296–. ISBN 978-0-08-092346-8.
- ^ Brinton RD (10 de mayo de 2010). "Neuroendocrinología del envejecimiento". En Fillit HM, Rockwood K, Woodhouse K (eds.). Brocklehurst's Textbook of Geriatric Medicine and Gerontology . Elsevier Health Sciences. págs. 166-167. ISBN 978-1-4377-2075-4Archivado desde el original el 9 de enero de 2020 . Consultado el 2 de diciembre de 2016 .
- ^ abc Büttner A, Thieme D (18 de diciembre de 2009). "Efectos secundarios de los esteroides anabólicos androgénicos: hallazgos patológicos y relaciones estructura-actividad". En Thieme D, Hemmersbach P (eds.). Dopaje en el deporte . Springer Science & Business Media. págs. 470–. ISBN 978-3-540-79088-4Archivado desde el original el 9 de enero de 2020 . Consultado el 2 de diciembre de 2016 .
- ^ ab Attardi BJ, Pham TC, Radler LC, Burgenson J, Hild SA, Reel JR (junio de 2008). "Dimetandrolona (7alfa,11beta-dimetil-19-nortestosterona) y 11beta-metil-19-nortestosterona no se convierten en productos aromáticos de anillo A en presencia de aromatasa humana recombinante". The Journal of Steroid Biochemistry and Molecular Biology . 110 (3–5): 214–222. doi :10.1016/j.jsbmb.2007.11.009. PMC 2575079 . PMID 18555683.
- ^ Llewellyn, William (2011). Anabólicos. Molecular Nutrition Llc. págs. 533–, 402–412, 460–467. ISBN 978-0-9828280-1-4Archivado del original el 17 de mayo de 2020 . Consultado el 2 de diciembre de 2016 .
- ^ Suvisaari J (2000). Farmacocinética y efectos antigonadotrópicos de la 7α-metil-19-nortestosterona (MENT) en hombres (PDF) (tesis doctoral). Helsinki: Universidad de Helsinki. pag. 14.ISBN 952-91-2950-5. Archivado desde el original (PDF) el 11 de agosto de 2017 . Consultado el 2 de diciembre de 2016 .
Los andrógenos, estrógenos y progestinas ejercen un efecto de retroalimentación negativa sobre la secreción de GnRH y LH por sus acciones sobre la hipófisis y el hipotálamo. La mayor parte del efecto de retroalimentación negativa de los andrógenos es causado por sus metabolitos estrogénicos producidos por aromatización. La 5α-reducción no parece ser necesaria para el efecto de retroalimentación negativa de la testosterona. (Rittmaster et al, 1992; Kumar et al, 1995a; Hayes et al, 2000).
- ^ abcde Attardi BJ, Hild SA, Reel JR (junio de 2006). "Undecanoato de dimetandrolona: un nuevo y potente andrógeno oralmente activo con actividad progestacional". Endocrinología . 147 (6): 3016–3026. doi : 10.1210/en.2005-1524 . PMID 16497801.
- ^ Myhal M, Lamb DR (1 de mayo de 2000). "Las hormonas como fármacos que mejoran el rendimiento". En Warren MP, Constantini NW (eds.). Endocrinología deportiva . Springer Science & Business Media. págs. 458–. ISBN 978-1-59259-016-2Archivado desde el original el 28 de septiembre de 2017 . Consultado el 2 de diciembre de 2016 .
- ^ Campbell B (23 de septiembre de 2015). "Sustancias y métodos que mejoran el rendimiento". En Haff GG, Triplett NT (eds.). Fundamentos del entrenamiento y acondicionamiento de la fuerza (4.ª ed.). Human Kinetics. págs. 233–. ISBN 978-1-4925-0162-6Archivado desde el original el 17 de febrero de 2018 . Consultado el 2 de diciembre de 2016 .
- ^ Lemke TL, Williams DA (24 de enero de 2012). "Salud masculina". Principios de química medicinal de Foye (7.ª ed.). Lippincott Williams & Wilkins. pp. 1360–. ISBN 978-1-60913-345-0.
- ^ ab Karch SB, Drummer O (26 de diciembre de 2001). "Esteroides anabólicos". Patología del abuso de drogas de Karch (tercera edición). CRC Press. pp. 489–. ISBN 978-1-4200-4211-5Archivado desde el original el 9 de enero de 2020 . Consultado el 2 de diciembre de 2016 .
- ^ ab van Amsterdam J, Opperhuizen A, Hartgens F (junio de 2010). "Efectos adversos para la salud de los esteroides anabólicos androgénicos". Toxicología y farmacología regulatorias . 57 (1): 117–123. doi :10.1016/j.yrtph.2010.02.001. PMID 20153798.
- ^ Wilson JD (mayo de 1988). "Abuso de andrógenos por parte de los atletas". Endocrine Reviews . 9 (2): 181–199. doi :10.1210/edrv-9-2-181. PMID 3042375.
- ^ Handelsman DJ (25 de febrero de 2015). "Fisiología, farmacología y abuso de los andrógenos". En Jameson JL, De Groot LJ (eds.). Endocrinología: adultos y niños . Elsevier Health Sciences. págs. 2391–. ISBN 978-0-323-32195-2Archivado desde el original el 9 de enero de 2020 . Consultado el 2 de diciembre de 2016 .
- ^ Handelsman DJ (26 de julio de 2012). "Terapia con andrógenos en enfermedades no gonadales". En Nieschlag E, Behre HM, Nieschlag S (eds.). Testosterona: acción, deficiencia, sustitución . Cambridge University Press. págs. 374–. doi :10.1017/CBO9781139003353.018. ISBN . 978-1-107-01290-5Archivado del original el 16 de mayo de 2020 . Consultado el 2 de diciembre de 2016 .
- ^ Watkins III JB, Klaassen CD (6 de diciembre de 2012). "Mecanismos de la colestasis inducida por fármacos". En Cameron R, Feuer G, de la Iglesia F (eds.). Hepatotoxicidad inducida por fármacos . Springer Science & Business Media. págs. 166–. ISBN 978-3-642-61013-4Archivado desde el original el 9 de enero de 2020 . Consultado el 2 de diciembre de 2016 .
- ^ Shahidi NT (septiembre de 2001). "Una revisión de la química, la acción biológica y las aplicaciones clínicas de los esteroides anabólicos androgénicos". Clinical Therapeutics . 23 (9): 1355–1390. doi :10.1016/s0149-2918(01)80114-4. PMID 11589254.
- ^ ab Büttner A, Thieme D (2009). "Efectos secundarios de los esteroides anabólicos androgénicos: hallazgos patológicos y relaciones estructura-actividad". Dopaje en el deporte . Manual de farmacología experimental. Vol. 195. Springer. págs. 459–84. doi :10.1007/978-3-540-79088-4_19. ISBN 978-3-540-79087-7. Número de identificación personal 20020376. Número de identificación personal 30314430.
- ^ Roddam AW, Allen NE, Appleby P, Key TJ (febrero de 2008). "Hormonas sexuales endógenas y cáncer de próstata: un análisis colaborativo de 18 estudios prospectivos". Revista del Instituto Nacional del Cáncer . 100 (3): 170–183. doi :10.1093/jnci/djm323. PMC 6126902 . PMID 18230794.
- ^ Meystre C, Frey H, Voser W, Wettstein A (enero de 1956). "Gewinnung von 1;4-Bisdehidro-3-oxo-esteroide. Über Steroide, 139. Mitteilung". Helvetica Chimica Acta . 39 (3): 734–742. doi :10.1002/hlca.19560390314. ISSN 0018-019X.
- ^ Kaufmann G, Schumann G, Hörhold C (octubre de 1986). "Influencia del doble enlace 1 y del grupo beta-hidroxi 11 en las reducciones microbianas estereoespecíficas de los 4-en-3-oxoesteroides". Journal of Steroid Biochemistry . 25 (4): 561–566. doi :10.1016/0022-4731(86)90403-6. PMID 3773526.
- ^ Stanley SM, Kent S, Rodgers JP (diciembre de 1997). "Biotransformación de esteroides 17-alquílicos en equinos: análisis por cromatografía líquida de alto rendimiento-espectrometría de masas y cromatografía de gases-espectrometría de masas de metabolitos de fluoximesterona en muestras de orina". Journal of Chromatography. B, Biomedical Sciences and Applications . 704 (1–2): 119–128. doi :10.1016/S0378-4347(97)00440-4. PMID 9518142.
- ^ Alm-Eldeen A, Tousson E (mayo de 2012). "Deterioro de la capa superficial endotelial glomerular y alteración de la función renal después de una inyección de boldenona, un promotor del crecimiento, en conejos". Human & Experimental Toxicology . 31 (5): 465–472. Bibcode :2012HETox..31..465A. doi :10.1177/0960327111420745. PMID 21878449. S2CID 206592924.
- ^ Clinton RO, Manson AJ, Stonner FW, Beyler AL, Potts GO, Arnold A (marzo de 1959). "[3, 2-c] pirazoles esteroidales". Revista de la Sociedad Química Americana . 81 (6): 1513–1514. doi :10.1021/ja01515a060. ISSN 0002-7863.
- ^ Bonnecaze AK, O'Connor T, Burns CA (julio de 2021). "Reducción de daños en pacientes varones que consumen activamente esteroides anabólicos androgénicos (EAA) y fármacos para mejorar el rendimiento (PED): una revisión". Revista de medicina interna general . 36 (7): 2055–2064. doi :10.1007/s11606-021-06751-3. PMC 8298654 . PMID 33948794.
- ^ Ringold HJ, Batres E, Halpern O, Necoechea E (enero de 1959). "Esteroides. CV. 1 Derivados de 2-metil y 2-hidroximetilen-androstano". Revista de la Sociedad Química Americana . 81 (2): 427–432. doi :10.1021/ja01511a040. ISSN 0002-7863.
- ^ De Brabanter N, Van Gansbeke W, Geldof L, Van Eenoo P (noviembre de 2012). "Un método mejorado de detección de sustancias dopantes mediante cromatografía de gases mediante espectrometría de masas de triple cuadrupolo, con énfasis en el control de calidad". Cromatografía biomédica . 26 (11): 1416–1435. doi :10.1002/bmc.2714. PMID 22362568.
- ^ Counsell RE, Klimstra PD, Colton FB (enero de 1962). "Agentes anabólicos. Derivados de 5α-Androst-1-eno". The Journal of Organic Chemistry . 27 (1): 248–253. doi :10.1021/jo01048a060. ISSN 0022-3263.
- ^ Lu FC, Rendel J, Abou Akkada AR, Organización de las Naciones Unidas para la Agricultura y la Alimentación, Organización Mundial de la Salud (1976). Agentes anabólicos en la producción animal: Simposio FAO/OMS sobre agentes anabólicos en la producción animal, Roma, marzo de 1975. Stuttgart: Thieme. ISBN 978-3-13-536101-7.
- ^ Catlin DH, Ahrens BD, Kucherova Y (5 de junio de 2002). "Detección de norboletona, un esteroide anabólico nunca comercializado, en la orina de los atletas". Comunicaciones rápidas en espectrometría de masas . 16 (13): 1273–1275. Bibcode :2002RCMS...16.1273C. doi :10.1002/rcm.722. PMID 12112254.
- ^ Camerino B, Sciaky R (1 de enero de 1975). "Estructura y efectos de los esteroides anabólicos". Farmacología y terapéutica , parte B. 1 (2): 233–275. doi :10.1016/0306-039X(75)90007-0. PMID 817322.
- ^ Mareck U, Geyer H, Opfermann G, Thevis M, Schänzer W (julio de 2008). "Factores que influyen en el perfil de esteroides en el análisis del control del dopaje". Journal of Mass Spectrometry . 43 (7): 877–891. Bibcode :2008JMSp...43..877M. doi :10.1002/jms.1457. PMID 18570179.
- ^ Fragkaki AG, Angelis YS, Tsantili-Kakoulidou A, Koupparis M, Georgakopoulos C (mayo de 2009). "Esquemas de patrones metabólicos de esteroides anabólicos androgénicos para la estimación de metabolitos de esteroides de diseño en orina humana". The Journal of Steroid Biochemistry and Molecular Biology . 115 (1–2): 44–61. doi :10.1016/j.jsbmb.2009.02.016. PMID 19429460. S2CID 10051396.
- ^ Blackledge RD (agosto de 2009). "Mala ciencia: los datos instrumentales en el caso Floyd Landis". Clinica Chimica Acta; Revista internacional de química clínica . 406 (1–2): 8–13. doi :10.1016/j.cca.2009.05.016. PMID 19465014.
- ^ Baselt RC (2008). Disposición de sustancias químicas y fármacos tóxicos en el hombre (8.ª ed.). Foster City, CA: Biomedical Publications. pp. 95, 393, 403, 649, 695, 952, 962, 1078, 1156, 1170, 1442, 1501, 1581. ISBN 978-0-9626523-7-0.
- ^ Randhawa, GK y Sharma, R. (2015). Potencial quimioterapéutico de la orina de vaca: una revisión. Revista de etnofarmacología intercultural, 4(2), 180.
- ^ abcd Hoberman JM, Yesalis CE (febrero de 1995). "La historia de la testosterona sintética". Scientific American . 272 (2): 76–81. Bibcode :1995SciAm.272b..76H. doi :10.1038/scientificamerican0295-76. PMID 7817189.
- ^ ab Freeman ER, Bloom DA, McGuire EJ (febrero de 2001). "Una breve historia de la testosterona". The Journal of Urology . 165 (2): 371–373. doi :10.1097/00005392-200102000-00004. PMID 11176375.
- ^ David K, Dingemanse E, Freud J, Laqueur L (1935). "Uber krystallinisches mannliches Hormon aus Hoden (Testosteron) wirksamer als aus harn oder aus Cholesterin bereitetes Androsteron". Z Physiol Chem de Hoppe-Seyler . 233 (5–6): 281–283. doi :10.1515/bchm2.1935.233.5-6.281.
- ^ Butenandt A, Hanisch G (1935). "Über die Umwandlung des Dehidro-androsterons in Δ4-Androsten-ol-(17)-0n-(3) (Testosteron); ein Weg zur Darstellung des Testosterons aus Cholesterin (Vorläuf. Mitteil.)" [Sobre la conversión de deshidro-androsterons Δ4-androsteno androsterona in-ol (17) 0n (3) (testosterona), una forma de representar la testosterona a partir del colesterol (Vorläuf. msgs.)]. Berichte der Deutschen Chemischen Gesellschaft (Series A y B) (en alemán). 68 (9): 1859–62. doi :10.1002/cber.19350680937.
- ^ Ruzicka L, Wettstein A (1935). "Sexualhormone VII. Uber die kunstliche Herstellung des Testikelhormons. Testosteron (Androsten-3-one-17-ol.)" [Hormonas sexuales VII Sobre la producción artificial de testosterona Testikelhormons (androstene-3-one-17-ol)]. Helvetica Chimica Acta (en alemán). 18 : 1264–75. doi :10.1002/hlca.193501801176.
- ^ ab Taylor WN (1 de enero de 2009). Esteroides anabólicos y el atleta . McFarland & Company. pág. 181. ISBN 978-0-7864-1128-3.
- ^ Suarez R, corresponsal senior, Kelman J, médico (18 de noviembre de 2002). "Los secretos de salud del presidente Kennedy". PBS NewsHour . Public Broadcasting System. Archivado desde el original el 22 de enero de 2014 . Consultado el 24 de agosto de 2017 .
- ^ Calfee R, Fadale P (marzo de 2006). "Fármacos y suplementos ergogénicos populares en atletas jóvenes". Pediatría . 117 (3): e577–e589. doi : 10.1542/peds.2005-1429 . PMID 16510635. S2CID 6559714.
- ^ Peters J (18 de febrero de 2005). "El hombre detrás del jugo". Slate . Archivado desde el original el 7 de septiembre de 2011 . Consultado el 29 de abril de 2008 .
- ^ ab Kochakian CD (1946). "Los efectos anabólicos de las hormonas esteroides sobre las proteínas". En Harris RS, Thimann KV (eds.). Vitaminas y hormonas . Vol. 4. Academic Press. págs. 255–310. doi :10.1016/S0083-6729(08)61085-7. ISBN 978-0-12-709804-3. ISSN 0083-6729.
En los últimos años, varios laboratorios (Kochakian, Albright, Wilkins) han abrigado la esperanza de encontrar un esteroide anabólico proteico sin efectos sexuales o con efectos menores. Estos estudios han recibido un impulso y un estímulo especiales a partir de la observación de Kochakian de que ciertos esteroides tienen mayores efectos renotróficos (¿anabólicos?) que androgénicos.
- ^ abcdef Potts GO, Arnold A, Beyler AL (6 de diciembre de 2012). "Disociación de las actividades androgénicas y otras actividades hormonales de los efectos anabólicos de los esteroides sobre las proteínas". En Kochakian CD (ed.). Esteroides anabólicos androgénicos . Springer Science & Business Media. págs. 370–373, 380. ISBN 978-3-642-66353-6Archivado del original el 14 de abril de 2021 . Consultado el 1 de abril de 2019 .
- ^ Sneader W (23 de junio de 2005). "Análogos hormonales". Descubrimiento de fármacos: una historia . John Wiley & Sons. págs. 206–. ISBN 978-0-471-89979-2.
- ^ ab Chast F (2 de mayo de 2011). "Una historia del descubrimiento de fármacos". En Wermuth CG (ed.). La práctica de la química medicinal . Academic Press. pp. 34–. ISBN 978-0-08-056877-5Archivado del original el 14 de abril de 2021 . Consultado el 28 de junio de 2018 .
- ^ ab Wright JE (1994). Estados alterados: el uso y abuso de esteroides anabólicos. Masters Press. pág. 33. ISBN 978-1-57028-013-9Archivado del original el 14 de abril de 2021 . Consultado el 28 de junio de 2018 .
- ^ Estados Unidos. Oficina de Patentes (1957). Boletín Oficial de la Oficina de Patentes de los Estados Unidos. Oficina de Patentes de los Estados Unidos.
- ^ von Deutsch DA, Abukhalaf IK, Socci RR (18 de septiembre de 2011). "Agentes dopantes anabólicos". En Mozayani A, Raymon L (eds.). Manual de interacciones farmacológicas: una guía clínica y forense . Springer Science & Business Media. págs. 651–. ISBN 978-1-61779-222-9Archivado del original el 14 de abril de 2021 . Consultado el 28 de junio de 2018 .
- ^ abcdefghij Handelsman DJ (mayo de 2011). "Comentario: andrógenos y "esteroides anabólicos": el Jano de una sola cabeza". Endocrinología . 152 (5): 1752–4. doi :10.1210/en.2010-1501. PMID 21511988.
- ^ abcdefg Handelsman DJ (julio de 2021). "Uso indebido y abuso de andrógenos". Endocr Rev. 42 ( 4): 457–501. doi :10.1210/endrev/bnab001. PMID 33484556.
Sin embargo, una tercera gran búsqueda, para el desarrollo de un andrógeno no virilizante ("esteroide anabólico") adecuado para su uso en mujeres y niños, basada en disociar los efectos virilizantes de los anabólicos de los andrógenos, fracasó estrepitosamente (36). Ahora se entiende que este fracaso se debe al descubrimiento de un receptor de andrógenos (AR) singular junto con la interpretación errónea de bioensayos de andrógenos inespecíficos en animales completos empleados para distinguir entre efectos anabólicos y virilizantes (37). El término "andrógeno" se utiliza aquí tanto para los andrógenos endógenos como para los sintéticos, incluidas las referencias a sustancias químicas denominadas en otros lugares como "esteroides anabólicos", "esteroides anabólico-androgénicos" o "moduladores específicos de AR" (SARM), que siguen haciendo una distinción obsoleta y oxímoron entre los efectos virilizantes y anabólicos de los andrógenos cuando no hay diferencia (36).
- ^ ab Handelsman DJ (julio de 2022). "Historia de los andrógenos y la acción de los andrógenos". Best Pract Res Clin Endocrinol Metab . 36 (4): 101629. doi :10.1016/j.beem.2022.101629. PMID 35277356.
- ^ Handelsman DJ (septiembre de 2013). "Mecanismos de acción de la testosterona: desenredando un nudo gordiano". N Engl J Med . 369 (11): 1058–9. doi :10.1056/NEJMe1305307. PMID 24024843. S2CID 44485330.
Estos hallazgos también resaltan cuán obsoleto es el término "esteroide anabólico", cuando se lo distingue falsamente de "andrógeno", una dicotomía carente de significado fisiológico y que persiste principalmente como una piñata mediática.10
- ^ Iyer R, Handelsman DJ (2017). "Uso indebido y abuso de testosterona". Testosterona . Cham: Springer International Publishing. págs. 375–402. doi :10.1007/978-3-319-46086-4_19. ISBN 978-3-319-46084-0Por definición ,
todos los andrógenos combinan propiedades anabólicas y androgénicas intrínsecas, que nunca se han separado significativamente [67], que se manifiestan a través del receptor de andrógenos, una proteína codificada por un gen de copia única. Por lo tanto, la singularidad de la acción de los andrógenos significa que los términos "esteroide anabólico" o "esteroides androgénicos-anabólicos" siguen siendo una terminología obsoleta que hace una distinción entre efectos androgénicos y anabólicos cuando no hay una diferencia real [67]. Esta terminología obsoleta pero ampliamente utilizada representa un vestigio de la búsqueda infructuosa de la industria farmacéutica para disociar las propiedades virilizantes de las anabólicas y permanece en la mente del público principalmente como una piñata mediática. El abuso de andrógenos, un término más apropiado que abarca el uso ilícito de todos los andrógenos disponibles, se utilizará en este capítulo.
- ^ Iyer R, DJ Handelsman (2016). "Andrógenos". Fronteras de la investigación hormonal . vol. 47. S. Karger AG. págs. 82-100. doi :10.1159/000445159. ISBN 978-3-318-05868-0. PMID 27347677.
Tras la pausa de la Segunda Guerra Mundial, el desarrollo de esteroides sintéticos por parte de la industria farmacéutica incluyó la búsqueda del objetivo de un andrógeno no virilizante ('esteroide anabólico') potencialmente adecuado para su uso para obtener efectos andrógenos farmacológicos en mujeres y niños. [...] la búsqueda industrial de un 'esteroide anabólico' basada en disociar los efectos virilizantes de los anabólicos de los andrógenos fracasó. Esto se entiende ahora a la luz del descubrimiento posterior del AR singular junto con las interpretaciones erróneas de bioensayos animales completos relativamente inespecíficos utilizados entonces para examinar esteroides sintéticos en busca de efectos anabólicos y virilizantes supuestamente distintos. Sin embargo, a pesar del abandono por parte de la industria de este esfuerzo infructuoso en 1980, y su reciente reencarnación bajo el disfraz de desarrollar un 'modulador selectivo de AR' (SARM) [6], el concepto vacío de un 'esteroide anabólico' persiste como una terminología científica mal definida y engañosa [7, 8]. En este artículo, se utiliza el término más preciso y claro "andrógeno" exclusivamente para los andrógenos endógenos y sintéticos, pero incluye referencias a sustancias químicas definidas vagamente en otros lugares como "esteroides anabólicos" o "esteroides anabólico-androgénicos", que confunden al hacer una distinción obsoleta donde no hay diferencia.
- ^ ab Handelsman DJ (26 de julio de 2012). "Terapia con andrógenos en enfermedades no gonadales". Testosterona . Cambridge University Press. págs. 372–407. doi :10.1017/cbo9781139003353.018. ISBN 978-1-139-00335-3El desarrollo de andrógenos no esteroides
, comercializados como "moduladores selectivos del receptor de andrógenos" (SARM), ofrece nuevas posibilidades para la terapia farmacológica adyuvante con andrógenos. A diferencia del espectro completo de efectos andrógenos de la testosterona, estos SARM serían andrógenos puros no sujetos a activación tisular específica por aromatización a un estrógeno correspondiente o a la amplificación de la potencia androgénica por reducción de 5a. En este contexto, los andrógenos puros endógenos nandrolona y DHT pueden considerarse SARM prototipo. Los SARM no son la encarnación moderna de los llamados "esteroides anabólicos", un término obsoleto que se refiere a andrógenos no virilizantes hipotéticos pero inexistentes dirigidos exclusivamente al músculo, un concepto fallido que carece de prueba biológica de principio (Handelsman 2011).
- ^ abc Feingold KR, Anawalt B, Blackman MR, Boyce A, Chrousos G, Corpas E, de Herder WW, Dhatariya K, Dungan K, Hofland J, Kalra S, Kaltsas G, Kapoor N, Koch C, Kopp P, Korbonits M , Kovacs CS, Kuohung W, Laferrère B, Levy M, McGee EA, McLachlan R, New M, Purnell J, Sahay R, Shah AS, Singer F, Sperling MA, Stratakis CA, Trence DL, Wilson DP, Handelsman DJ (5 de octubre de 2020). "Fisiología, farmacología, uso y mal uso de los andrógenos". Endotexto . PMID 25905231.
La identificación de un único gen y proteína para el receptor de andrógenos en 1988 (584-586) explica la observación fisiológica de que, en dosis equivalentes, todos los andrógenos tienen efectos esencialmente similares (587). El término "esteroide anabólico" fue inventado Durante la era dorada de la farmacología de esteroides posterior a la Segunda Guerra Mundial, se intentó definir un andrógeno idealizado que careciera de características virilizantes pero que mantuviera propiedades miotrópicas para que pudiera usarse de manera segura en niños y mujeres. Aunque esta búsqueda resultó ilusoria y se abandonó después de que todos los esfuerzos de la industria fracasaran en identificar dicho andrógeno idealizado, un andrógeno sintético hipotético, el término obsoleto "esteroide anabólico" persiste principalmente como una descripción escabrosa en los medios populares a pesar de seguir haciendo una distinción falsa donde no hay diferencia. Una mejor comprensión de la activación metabólica de los andrógenos a través de la reducción 5α y la aromatización en los tejidos diana y las propiedades agonistas/antagonistas parciales específicas de los tejidos de algunos andrógenos sintéticos pueden conducir a conceptos más fisiológicos de la acción de los andrógenos específicos de los tejidos ("modulador específico del receptor de andrógenos"). ) gobernada por los procesos fisiológicos de activación de andrógenos prerreceptores así como la interacción postreceptor con proteínas correguladoras análogas al desarrollo de agonistas parciales de estrógenos sintéticos con especificidad tisular ("modulador específico del receptor de estrógeno") (588). Aún quedan por evaluar en su totalidad las nuevas indicaciones terapéuticas clínicas de los nuevos andrógenos selectivos de tejidos en desarrollo clínico (589).
- ^ Bond P, Smit DL, de Ronde W (2022). "Esteroides anabolizantes androgénicos: ¿cómo funcionan y cuáles son los riesgos?". Front Endocrinol (Lausana) . 13 : 1059473. doi : 10.3389/fendo.2022.1059473 . PMC 9837614. PMID 36644692. Los esteroides anabolizantes androgénicos (EAA) son una clase de hormonas naturales y sintéticas que deben su nombre a su estructura química (el núcleo esteroide, ver Figura 1) y los
efectos biológicos (anabólicos y androgénicos) que inducen. Anabólico se refiere a las propiedades de desarrollo muscular esquelético de los EAA, mientras que androgénico se refiere a la inducción y mantenimiento de las características sexuales secundarias masculinas (que en principio incluye la acción anabólica, lo que convierte al término en un oxímoron (1)).
- ^ "Ley de Sustancias Controladas del Título 21 del Código de los Estados Unidos (USC)". Departamento de Justicia de los Estados Unidos. Archivado desde el original el 24 de julio de 2009. Consultado el 7 de septiembre de 2009 .
- ^ Ley de Sustancias y Drogas Controladas , SC 1996, c. 19, s. 4(7) (Ley de Sustancias y Drogas Controladas en el Departamento de Justicia)
- ^ Deacon J (2 de mayo de 1994). "Bíceps en una botella". Maclean's . 107 (18): 52–53.
- ^ "Esteroides". Instituto Australiano de Criminología. 2006. Archivado desde el original el 5 de abril de 2007. Consultado el 6 de mayo de 2007 .
- ^ Solomon ZJ, Mirabal JR, Mazur DJ, Kohn TP, Lipshultz LI, Pastuszak AW (enero de 2019). "Moduladores selectivos del receptor de andrógenos: conocimiento actual y aplicaciones clínicas". Sexual Medicine Reviews . 7 (1): 84–94. doi :10.1016/j.sxmr.2018.09.006. PMC 6326857 . PMID 30503797.
- ^ Sobolevsky T, Ahrens B (febrero de 2021). "Ensayo de espectrometría de masas en tándem con cromatografía líquida de alto rendimiento como procedimiento de prueba inicial para el análisis de la fracción urinaria total". Drug Testing and Analysis . 13 (2): 283–298. doi :10.1002/dta.2917. PMID 32852861. S2CID 221347916.
- ^ Turnock L, Gibbs N (2023). "Clic, clic, compra: El mercado de nuevas hormonas peptídicas sintéticas en las principales plataformas de comercio electrónico del Reino Unido". Mejora del rendimiento y salud . 11 (2): 100251. doi : 10.1016/j.peh.2023.100251 . ISSN 2211-2669.
- ^ HR 4658
- ^ "Noticias de la DEA, testimonio ante el Congreso, 16/03/04". Archivado desde el original el 6 de febrero de 2007. Consultado el 24 de abril de 2007 .
- ^ "Medicamentos controlados de Patient.info". Egton Medical Information Systems Limited. Archivado desde el original el 13 de junio de 2015. Consultado el 8 de agosto de 2013 .
- ^ "Reglamento antidopaje de la FIFA" (PDF) . FIFA. Archivado desde el original (PDF) el 21 de enero de 2012 . Consultado el 1 de diciembre de 2013 .
- ^ "Código antidopaje del movimiento olímpico" (PDF) . Comité Olímpico Internacional. 1999. Archivado (PDF) desde el original el 3 de octubre de 2018. Consultado el 6 de mayo de 2007 .
- ^ "El programa antidrogas de la NVA y la NBPA". Política de la NBA . findlaw.com. 1999. Archivado desde el original el 22 de noviembre de 2007 . Consultado el 6 de mayo de 2007 .
- ^ "Resumen del programa de sustancias que mejoran el rendimiento de la NHL/NHLPA". nhlpa.com. Archivado desde el original el 2 de junio de 2007. Consultado el 6 de mayo de 2007 .
- ^ "Lista de sustancias prohibidas" (PDF) . nflpa.com. 2006. Archivado desde el original (PDF) el 20 de junio de 2007 . Consultado el 6 de mayo de 2007 .
- ^ "Código mundial antidopaje" (PDF) . AMA. 2003. Archivado desde el original (PDF) el 7 de agosto de 2007. Consultado el 10 de julio de 2007 .
- ^ "Lista de sustancias prohibidas de 2005" (PDF) . AMA. 2005. Archivado desde el original (PDF) el 20 de junio de 2007. Consultado el 6 de mayo de 2007 .
- ^ Keeping J (27 de diciembre de 2010). "El abuso de esteroides entre los agentes de la ley es un problema a nivel nacional". The Ann Arbor News . Archivado desde el original el 4 de marzo de 2016. Consultado el 1 de diciembre de 2013 .
- ^ "Uso y abuso de esteroides anabólicos por parte de agentes de policía: políticas y prevención". El jefe de policía . Junio de 2008. Archivado desde el original el 3 de diciembre de 2013. Consultado el 1 de diciembre de 2013 .
- ^ Brian L (1 de marzo de 2010). «Investigación sobre esteroides en la WWE: una controversia que McMahon «no necesita»». Hora de Greenwich. Archivado desde el original el 31 de enero de 2021. Consultado el 1 de marzo de 2010 .
- ^ "Talent Wellness Program Program Summary Report 1 July 2007 31 March 2008" (PDF). World Wrestling Entertainment, Inc. Archived from the original (PDF) on 24 December 2010.
- ^ "Deposition details McMahon steroid testimony". News from southeastern Connecticut. The Day. 13 December 2007. Archived from the original on 12 June 2010. Retrieved 14 August 2010.
- ^ Assael S (24 September 2007). "'Raw Deal' busts labs across U.S., many supplied by China". ESPN The Magazine. Archived from the original on 14 October 2007. Retrieved 24 September 2007.
- ^ Yesalis C (2000). "Source of Anabolic Steroids". Anabolic Steroids in Sport and Exercise. Champaign, Ill.: Human Kinetics. ISBN 978-0-88011-786-9. Archived from the original on 14 April 2021. Retrieved 3 June 2020.
- ^ Black T (1996). "Does the Ban on Drugs in Sport Improve Societal Welfare?". International Review for the Sociology of Sport. 31 (4). Faculty of Business, Queensland University of Technology: 367–381. doi:10.1177/101269029603100402. S2CID 143442371.
- ^ Pound RW (2006). "Organized Crime". Inside dope: how drugs are the biggest threat to sports, why you should care, and what can be done about them. Mississaug, Ontario: Wiley. p. 175. ISBN 978-0-470-83733-7.
- ^ "Steroids". National Institute on Drug Abuse. GDCADA. Archived from the original on 11 September 2007. Retrieved 13 September 2007.
- ^ "The Drug Enforcement Administration's International Operations (Redacted)". Office of the Inspector General. USDOJ. February 2007. Archived from the original on 30 October 2013. Retrieved 2 January 2014.
- ^ Nieschlag E, Kumar N, Sitruk-Ware R (March 2013). "7α-methyl-19-nortestosterone (MENTR): the population council's contribution to research on male contraception and treatment of hypogonadism". Contraception. 87 (3): 288–295. doi:10.1016/j.contraception.2012.08.036. PMID 23063338.
- ^ "Dimethandrolone undecanoate shows promise as a male birth control pill". Endocrine Society. Archived from the original on 21 March 2018. Retrieved 20 March 2018.
- ^ a b Gruber CJ, Wieser F, Gruber IM, Ferlitsch K, Gruber DM, Huber JC (December 2002). "Current concepts in aesthetic endocrinology". Gynecological Endocrinology. 16 (6): 431–441. doi:10.1080/gye.16.6.431.441. PMID 12626029. S2CID 37424524.
- ^ Sam S (February 2015). "Adiposity and metabolic dysfunction in polycystic ovary syndrome". Hormone Molecular Biology and Clinical Investigation. 21 (2): 107–116. doi:10.1515/hmbci-2015-0008. PMID 25781555. S2CID 23592351.
Further reading
- Daniels RC (1 February 2003). The Anabolic Steroid Handbook. RCD Books. p. 80. ISBN 0-9548227-0-6.
- Gallaway S (15 January 1997). The Steroid Bible (3rd Sprl ed.). Belle Intl. p. 125. ISBN 1-890342-00-9.
- Llewellyn W (28 January 2007). Anabolics 2007: Anabolic Steroid Reference Manual (6th ed.). Body of Science. p. 988. ISBN 978-0-9679304-6-6.
- Roberts A, Clapp B (January 2006). Anabolic Steroids: Ultimate Research Guide. Anabolic Books, LLC. p. 394. ISBN 1-59975-100-3.
- Yesalis CE (2000). Anabolic Steroids in Sport and Exercise. Human Kinetics. ISBN 0-88011-786-9.
- Fragkaki AG, Angelis YS, Koupparis M, Tsantili-Kakoulidou A, Kokotos G, Georgakopoulos C (February 2009). "Structural characteristics of anabolic androgenic steroids contributing to binding to the androgen receptor and to their anabolic and androgenic activities. Applied modifications in the steroidal structure". Steroids. 74 (2): 172–197. doi:10.1016/j.steroids.2008.10.016. PMID 19028512. S2CID 41356223.
- McRobb L, Handelsman DJ, Kazlauskas R, Wilkinson S, McLeod MD, Heather AK (May 2008). "Structure-activity relationships of synthetic progestins in a yeast-based in vitro androgen bioassay". The Journal of Steroid Biochemistry and Molecular Biology. 110 (1–2): 39–47. doi:10.1016/j.jsbmb.2007.10.008. PMID 18395441. S2CID 5612000.
- Schänzer W (July 1996). "Metabolism of anabolic androgenic steroids". Clinical Chemistry. 42 (7): 1001–1020. doi:10.1093/clinchem/42.7.1001. PMID 8674183.
- Tygart TT (December 2009). "Steroids, the Media, and Youth". Prevention Researcher Integrated Research Services, Inc. 16 (7–9). SIRS Researcher. Archived from the original on 29 November 2014. Retrieved 24 November 2013.
- Eisenhauer L (7 November 2005). "Do I Look OK?". St. Louis, MO: St. Louis Post-Dispatch. Archived from the original on 2 December 2013. Retrieved 25 October 2010.


