Etinilestradiol
 | |
 | |
| Datos clínicos | |
|---|---|
| Pronunciación | / ˌ ɛ θ ɪ n ɪ l ˌ ɛ s t r ə ˈ d aɪ . əl / |
| Nombres comerciales | Muchos |
| Otros nombres | Etinilestradiol; Etinilestradiol; Etinilestradiol; EE; EE2; 17α-Etinilestradiol; 17α-Etinilestra-1,3,5(10)-trieno-3,17β-diol; NSC-10973 [1] |
| AHFS / Drogas.com | Nombres internacionales de medicamentos |
| MedlinePlus | a604032 |
| Vías de administración | • Por vía oral , transdérmica , vaginal. |
| Clase de droga | Estrógeno |
| Código ATC | |
| Estatus legal | |
| Estatus legal |
|
| Datos farmacocinéticos | |
| Biodisponibilidad | 38–48% [2] [3] [4] |
| Unión de proteínas | 97–98% (a albúmina ; [5] no está unida a SHBGInformación sobre herramientas sobre la globulina transportadora de hormonas sexuales) [6] |
| Metabolismo | Hígado (principalmente CYP3A4 ) [9] |
| Metabolitos | • Sulfato de etinilestradiol [7] [8] • Otros [7] [8] |
| Vida media de eliminación | 7–36 horas [9] [2] [10] [11] |
| Excreción | Heces : 62% [10] Orina : 38% [10] |
| Identificadores | |
| |
| Número CAS | |
| Identificador de centro de PubChem |
|
| Unión Internacional para la Investigación y el Desarrollo (IUPHAR)/BPS |
|
| Banco de medicamentos | |
| Araña química | |
| UNIVERSIDAD |
|
| BARRIL | |
| EBICh | |
| Química biológica | |
| Panel de control CompTox ( EPA ) |
|
| Tarjeta informativa de la ECHA | 100.000.311 |
| Datos químicos y físicos | |
| Fórmula | C20H24O2 |
| Masa molar | 296,410 g·mol −1 |
| Modelo 3D ( JSmol ) |
|
| Punto de fusión | 182 a 184 °C (360 a 363 °F) |
| |
| (verificar) | |
El etinilestradiol ( EE ) es un medicamento de estrógeno que se usa ampliamente en píldoras anticonceptivas en combinación con progestinas . [7] [8] En el pasado, el EE se usaba ampliamente para diversas indicaciones, como el tratamiento de los síntomas de la menopausia , los trastornos ginecológicos y ciertos cánceres sensibles a las hormonas . Por lo general, se toma por vía oral , pero también se usa como parche y anillo vaginal . [7] [12]
Los efectos secundarios generales de la EE incluyen dolor y agrandamiento de los senos , dolor de cabeza , retención de líquidos y náuseas , entre otros. [7] En los hombres, la EE también puede causar crecimiento de los senos , feminización en general, hipogonadismo y disfunción sexual . Los efectos secundarios raros pero graves incluyen coágulos de sangre , daño hepático y cáncer de útero . [7]
EE es un estrógeno , o un agonista de los receptores de estrógeno , el objetivo biológico de los estrógenos como el estradiol . [7] Es un derivado sintético del estradiol , un estrógeno natural , y se diferencia de él en varias formas. [7] En comparación con el estradiol, EE es más resistente al metabolismo , tiene una biodisponibilidad mucho mejor cuando se toma por vía oral y muestra efectos relativamente mayores en ciertas partes del cuerpo como el hígado y el útero . [7] Estas diferencias hacen que EE sea más favorable para su uso en píldoras anticonceptivas que el estradiol, aunque también resultan en un mayor riesgo de coágulos de sangre y ciertos otros efectos adversos raros. [7]
El EE se desarrolló en la década de 1930 y se introdujo para uso médico en 1943. [13] [14] El medicamento comenzó a usarse en píldoras anticonceptivas en la década de 1960. [15] El etinilestradiol se encuentra en casi todas las formas combinadas de píldoras anticonceptivas y es casi el estrógeno exclusivo utilizado para este propósito, lo que lo convierte en uno de los estrógenos más utilizados. [16] [17]
En 2022, la combinación con noretisterona o con acetato de noretisterona fue el 80.º medicamento más recetado en Estados Unidos, con más de 8 millones de recetas; [18] [19] la combinación con norgestimato fue el 99.º medicamento más recetado en Estados Unidos, con más de 6 millones de recetas; [18] [20] la combinación con levonorgestrel fue el 128.º medicamento más recetado en Estados Unidos, con más de 4 millones de recetas; [18] [21] la combinación con drospirenona fue el 142.º medicamento más recetado en Estados Unidos, con más de 4 millones de recetas; [18] [22] la combinación con desogestrel fue el 161.º medicamento más recetado en Estados Unidos, con más de 3 millones de recetas; [18] [23] la combinación con etonogestrel fue el medicamento número 194 más recetado en los EE. UU., con más de 2 millones de recetas; [18] [24] la combinación con norgestrel fue el medicamento número 264 más recetado en los EE. UU., con más de 1 millón de recetas; [18] [25] la combinación con drospirenona y ácido levomefólico fue el medicamento número 285 más recetado en los EE. UU., con más de 500 000 recetas; [18] [26] la combinación con etinodiol fue el medicamento número 294 más recetado en los EE. UU., con más de 400 000 recetas. [18] [27]
Usos médicos
El EE tiene muchos usos. Su uso más común es como anticonceptivo en los anticonceptivos orales combinados (AOC), también conocidos como anticonceptivos orales , para prevenir el embarazo después de las relaciones sexuales. El EE en su formulación anticonceptiva no solo se usa para prevenir el embarazo, sino que también se puede usar para tratar la ausencia de la menstruación, los síntomas durante la menstruación y el acné .
El EE también se utiliza como terapia hormonal menopáusica . [28] La razón principal para usar la THS en mujeres menopáusicas es aliviar los síntomas vasomotores comunes, como sofocos , sudores nocturnos y sofocos . Los estudios han encontrado que el reemplazo de estrógeno ayuda a mejorar estos síntomas en comparación con un placebo. [29] Otros síntomas comunes de la menopausia, como la sequedad vaginal (que puede causar dolor durante las relaciones sexuales), la picazón vaginal y el estado de ánimo deprimido, pueden beneficiarse de la THS. Además del tratamiento de los síntomas de la menopausia, el EE se ha utilizado como un componente de la terapia hormonal feminizante para mujeres transgénero . [30] Sin embargo, ya no se usa ni se recomienda comúnmente para este propósito, ya que el estradiol lo ha reemplazado en gran medida. [30]
El EE también se puede utilizar para tratar el hipogonadismo en mujeres, prevenir la osteoporosis en mujeres y se ha utilizado como cuidado paliativo para el cáncer de próstata en hombres y el cáncer de mama en mujeres. [8] [31] También se ha utilizado para reducir el deseo sexual en delincuentes sexuales . [32] [33]
El EE o cualquier estrógeno solo está contraindicado para mujeres que tienen útero debido al mayor riesgo de cáncer de endometrio ; administrar un progestágeno con un estrógeno mitiga el riesgo. [34]
Formularios disponibles
EE está disponible en combinación con una progestina en una gran cantidad de AOC. [35] También está disponible en combinación con progestinas como un parche anticonceptivo transdérmico y como un anillo vaginal anticonceptivo . [12] Además, existe una única preparación (nombre comercial FemHRT) que contiene dosis muy bajas de EE (2,5 y 5 μg) más una progestina en un comprimido oral que sigue utilizándose para la terapia hormonal menopáusica. [12] [28] EE estaba anteriormente disponible por sí solo bajo nombres comerciales como Estinyl y Lynoral en forma de comprimidos de 0,002, 0,01, 0,02, 0,025, 0,05, 0,1, 0,5 y 1,0 mg (2, 10, 20, 25, 50, 100, 500 y 1000 μg). [36] [37] [38] [39] [40]
La cantidad de EE en los AOC se ha reducido con los años. [8] Anteriormente, los AOC contenían dosis altas de EE de hasta 100 μg/día. [41] Las dosis de más de 50 μg de EE se consideran dosis altas, las dosis de 30 y 35 μg de EE se consideran dosis bajas y las dosis de 10 a 25 μg de EE se consideran dosis muy bajas. [42] Hoy en día, los AOC generalmente contienen de 10 a 50 μg de EE. [42] Las dosis más altas de EE se suspendieron debido a un alto riesgo de TEV y problemas cardiovasculares. [41]
Contraindicaciones
Se debe evitar la EE en personas con antecedentes o susceptibilidad conocida a trombosis arterial o venosa ( coágulos de sangre ), debido a un mayor riesgo de problemas cardiovasculares como tromboembolia venosa (TEV), infarto de miocardio y accidente cerebrovascular isquémico . [43] Esto incluye a mujeres con:
- Antecedentes de trombosis venosa profunda (TVP) o embolia pulmonar (EP) sin recibir anticoagulantes
- TVP/EP aguda
- Inmovilización prolongada debido a una cirugía mayor
- Diabetes mellitus avanzada con enfermedad vascular
- Migraña con aura
- Hipertensión ≥160/100
- Enfermedad vascular
- Historia y actualidad de la cardiopatía isquémica
- Múltiples factores de riesgo de enfermedad cardiovascular aterosclerótica (por ejemplo, edad avanzada, tabaquismo, diabetes, hipertensión, niveles bajos de HDL, niveles altos de LDL o niveles altos de triglicéridos)
- Edad ≥35 años y tabaquismo ≥15 cigarrillos/día
- Historia de accidente cerebrovascular
- Lupus eritematoso sistémico con anticuerpos antifosfolípidos positivos (o desconocidos)
- Enfermedad cardíaca valvular complicada
Excepto cuando se utilice para tratarlo, la EE debe evitarse en mujeres con cáncer de mama actual debido a un posible empeoramiento del pronóstico. [44]
También se debe evitar el uso de EE en mujeres que amamantan y que tienen menos de 21 días de posparto debido a un mayor riesgo de TEV. [45] El uso de EE en mujeres que amamantan y tienen al menos 21 días de posparto se debe discutir con un proveedor e incluir información sobre las ventajas, desventajas y alternativas para el uso de EE. [45]
Debido al riesgo de hepatotoxicidad colestásica , se considera ampliamente que los AOC que contienen EE deben evitarse en mujeres con antecedentes de colestasis del embarazo , tumores hepáticos , hepatitis activa y defectos familiares en la excreción biliar. [46]
Efectos secundarios
| Dosis de etinilestradiol | Número de casos de TEV | Años de mujer | Tasa de TEV | RR ajustado a |
|---|---|---|---|---|
| Bajo (<50 μg) | 53 | 127.000 | 4,2 por cada 10.000 mujeres-año | 1.0 |
| Intermedio (50 μg) | 69 | 98.000 | 7,0 en 10.000 mujeres-año | 1.5 |
| Alto (>50 μg) | 20 | 20.000 | 10,0 en 10.000 mujeres-año | 1.7 |
| Todo | 142 | 245.000 | 5,8 en 10.000 mujeres-año | – |
| Notas al pie: a = Relativo a dosis bajas (no a no uso). Notas: En píldoras anticonceptivas que contienen una progestina de primera generación , como noretisterona o levonorgestrel . Fuentes: Principal : [47] [48] Adicional : [49] | ||||
La gravedad de los efectos secundarios puede variar según la dosis y la vía de administración de EE. [50] Los efectos secundarios generales de EE son los mismos que para otros estrógenos e incluyen dolor en los senos , dolor de cabeza , retención de líquidos ( hinchazón ), náuseas , mareos y aumento de peso . [10] [46] El componente de estrógeno de los anticonceptivos orales, que casi siempre es EE, puede causar dolor y plenitud en los senos . [36] En los hombres, EE tiene efectos secundarios adicionales, que incluyen ginecomastia (desarrollo de los senos), feminización en general, hipogonadismo , infertilidad y disfunción sexual (p. ej., reducción de la libido y disfunción eréctil ). En los hombres que recibieron terapia de estrógeno en dosis altas con 200 μg/día de EE oral durante más de tres meses, se produjo ginecomastia en el 98% y disminución de la libido en el 42 a 73%. [51]
Efectos a largo plazo
Coágulos de sangre
La TEV es un coágulo de sangre en una vena e incluye la trombosis venosa profunda (TVP) y la embolia pulmonar (EP). [7] [53] [54] Se sabe que los estrógenos aumentan el riesgo de TEV debido a sus efectos sobre la síntesis hepática de factores de coagulación . [7] [53] [54] El EE conlleva un mayor riesgo de formación de coágulos de sangre y TEV que el estradiol natural , lo que se cree que se debe a diferencias estructurales entre los dos compuestos y diferentes susceptibilidades a la inactivación hepática . [7]
Un metaanálisis de 2012 estimó que el riesgo absoluto de TEV es de 2 por 10 000 mujeres en caso de no uso, 8 por 10 000 mujeres en caso de píldoras anticonceptivas que contienen EE y levonorgestrel , y de 10 a 15 por 10 000 mujeres en caso de píldoras anticonceptivas que contienen EE y una progestina de tercera o cuarta generación , como desogestrel o drospirenona . [55] A modo de comparación, el riesgo absoluto de TEV se estima generalmente en 1 a 5 por 10 000 mujeres-año en caso de no uso, de 5 a 20 por 10 000 mujeres-año en caso de embarazo, y de 40 a 65 por 10 000 mujeres-año en caso de posparto . [55] Los AOC modernos se asocian con un riesgo de TEV aproximadamente 2 a 4 veces mayor que el de no uso. [55] La vía de administración de EE no parece influir en el riesgo de TEV, ya que los anillos vaginales anticonceptivos y los parches anticonceptivos que contienen EE/progestina tienen el mismo riesgo de TEV o incluso mayor que los AOC. [55] [56] El embarazo se asocia con un aumento de aproximadamente 4,3 veces en el riesgo de TEV. [55] Se ha estimado que al menos 300 a 400 mujeres jóvenes sanas mueren cada año en los Estados Unidos debido a TEV causada por píldoras anticonceptivas que contienen EE. [57]
Los AOC modernos contienen de 10 a 35 μg de EE, pero normalmente son 20, 30 o 35 μg. [55] [58] Las formulaciones iniciales de AOC que se introdujeron en la década de 1960 contenían de 100 a 150 μg de EE. [59] [49] [58] Sin embargo, pronto se descubrió que el EE se asocia con un mayor riesgo de TEV y que el riesgo depende de la dosis. [58] Después de estos eventos, la dosis de EE se redujo en gran medida y ahora siempre es inferior a 50 μg. [60] [61] [62] Estas dosis más bajas tienen un riesgo significativamente reducido de TEV sin pérdida de eficacia anticonceptiva. [58] Gerstman et al. (1991) encontraron que los AOC que contienen más de 50 μg de EE tenían 1,7 veces y los AOC que contienen 50 μg de EE 1,5 veces más riesgo de TEV que los AOC que contienen menos de 50 μg. [47] Una revisión Cochrane de 2014 encontró que los AOC que contienen 50 μg de EE con levonorgestrel tenían de 2,1 a 2,3 veces más riesgo que los AOC que contienen 30 μg o 20 μg de EE con levonorgestrel, respectivamente. [55] Los AOC que contienen 20 μg de EE también se asocian con un riesgo significativamente menor de eventos cardiovasculares que los AOC que contienen 30 o 40 μg de EE. [63] Sin embargo, la interrupción de los AOC es más común con dosis de EE de 10 a 20 μg debido a cambios problemáticos en los patrones de sangrado. [64]
Las mujeres con trombofilia tienen un riesgo considerablemente mayor de TEV con anticonceptivos que contienen EE que las mujeres sin trombofilia. [55] [56] Dependiendo de la afección, el riesgo de TEV puede aumentar de 5 a 50 veces en relación con la falta de uso en dichas mujeres. [55] [56]
Los niveles de globulina transportadora de hormonas sexuales (SHBG) indican exposición estrogénica hepática y pueden ser un marcador sustituto de riesgo de coagulación y TEV con terapia con estrógenos, aunque este tema ha sido debatido. [65] [66] [67] Los niveles de SHBG con píldoras anticonceptivas que contienen diferentes progestinas aumentan de 1,5 a 2 veces con levonorgestrel , de 2,5 a 4 veces con desogestrel y gestodeno , de 3,5 a 4 veces con drospirenona y dienogest , y de 4 a 5 veces con acetato de ciproterona . [65] También se ha descubierto que los anillos vaginales anticonceptivos y los parches anticonceptivos aumentan los niveles de SHBG en 2,5 y 3,5 veces, respectivamente. [65] Las píldoras anticonceptivas que contienen altas dosis de etinilestradiol (>50 μg) pueden aumentar los niveles de SHBG de 5 a 10 veces, lo que es similar al aumento que ocurre durante el embarazo. [68] Por el contrario, los aumentos en los niveles de SHBG son mucho menores con estradiol , especialmente cuando se usa por vía parenteral. [69] [70] [71] [72] [73] Se ha descubierto que la terapia con fosfato de poliestradiol parenteral en dosis altas aumenta los niveles de SHBG aproximadamente 1,5 veces. [72]
| Tipo | Ruta | Medicamentos | Razón de probabilidades ( IC del 95 %)Intervalo de confianza de la información sobre herramientas) |
|---|---|---|---|
| Terapia hormonal para la menopausia | Oral | Estradiol solo ≤1 mg/día >1 mg/día | 1,27 (1,16–1,39)* 1,22 (1,09–1,37)* 1,35 (1,18–1,55)* |
| Estrógenos conjugados solos ≤0,625 mg/día >0,625 mg/día | 1,49 (1,39–1,60)* 1,40 (1,28–1,53)* 1,71 (1,51–1,93)* | ||
| Acetato de estradiol/medroxiprogesterona | 1,44 (1,09–1,89)* | ||
| Estradiol/didrogesterona ≤1 mg/día E2 >1 mg/día E2 | 1,18 (0,98–1,42) 1,12 (0,90–1,40) 1,34 (0,94–1,90) | ||
| Estradiol/noretisterona ≤1 mg/día E2 >1 mg/día E2 | 1,68 (1,57–1,80)* 1,38 (1,23–1,56)* 1,84 (1,69–2,00)* | ||
| Estradiol/norgestrel o estradiol/drospirenona | 1,42 (1,00–2,03) | ||
| Estrógenos conjugados/acetato de medroxiprogesterona | 2,10 (1,92–2,31)* | ||
| Estrógenos conjugados/norgestrel ≤0,625 mg/día de CEE >0,625 mg/día de CEE | 1,73 (1,57–1,91)* 1,53 (1,36–1,72)* 2,38 (1,99–2,85)* | ||
| Tibolona sola | 1,02 (0,90–1,15) | ||
| Raloxifeno solo | 1,49 (1,24–1,79)* | ||
| Transdérmico | Estradiol solo ≤50 μg/día >50 μg/día | 0,96 (0,88–1,04) 0,94 (0,85–1,03) 1,05 (0,88–1,24) | |
| Estradiol / progestágeno | 0,88 (0,73–1,01) | ||
| Vaginal | Estradiol solo | 0,84 (0,73–0,97) | |
| Estrógenos conjugados solos | 1,04 (0,76–1,43) | ||
| Anticoncepción combinada | Oral | Etinilestradiol/noretisterona | 2,56 (2,15–3,06)* |
| Etinilestradiol/levonorgestrel | 2,38 (2,18–2,59)* | ||
| Etinilestradiol/norgestimato | 2,53 (2,17–2,96)* | ||
| Etinilestradiol/desogestrel | 4,28 (3,66–5,01)* | ||
| Etinilestradiol/gestodeno | 3,64 (3,00–4,43)* | ||
| Etinilestradiol/drospirenona | 4,12 (3,43–4,96)* | ||
| Acetato de etinilestradiol/ciproterona | 4,27 (3,57–5,11)* | ||
| Notas: (1) Estudios de casos y controles anidados (2015, 2019) basados en datos de las bases de datos QResearch y Clinical Practice Research Datalink (CPRD). (2) No se incluyó la progesterona bioidéntica , pero se sabe que no se asocia con ningún riesgo adicional en relación con el estrógeno solo. Notas al pie: * = Estadísticamente significativo ( p < 0,01). Fuentes : Ver plantilla. | |||
Problemas cardiovasculares
Cuando se utilizan por vía oral en dosis altas, por ejemplo, como una forma de terapia de estrógeno en dosis altas en hombres con cáncer de próstata y en mujeres con cáncer de mama, los estrógenos sintéticos y no bioidénticos como EE y dietilestilbestrol se asocian con tasas bastante altas de complicaciones cardiovasculares graves como TEV, infarto de miocardio y accidente cerebrovascular . [31] [74] [75] El dietilestilbestrol se ha asociado con un riesgo de hasta un 35% de toxicidad cardiovascular y muerte y una incidencia del 15% de TEV en hombres tratados con él para el cáncer de próstata. [74] [75] El EE tiene un riesgo algo menor de complicaciones cardiovasculares que el dietilestilbestrol cuando se usa en el tratamiento del cáncer de próstata en hombres. [8] Sin embargo, tanto el EE como el dietilestilbestrol tienen efectos altamente desproporcionados en la síntesis de proteínas hepáticas , que se cree que es responsable de su toxicidad cardiovascular. [7] [75]
A diferencia de los estrógenos sintéticos orales como EE y dietilestilbestrol, no se ha encontrado que el fosfato de poliestradiol en dosis altas y el estradiol transdérmico aumenten el riesgo de mortalidad cardiovascular o tromboembolia en hombres con cáncer de próstata. [75] [76] [77] Sin embargo, se ha observado una morbilidad cardiovascular significativamente mayor con fosfato de poliestradiol en dosis altas. [75] [76] [77] En cualquier caso, se considera que estos estrógenos son mucho más seguros que los estrógenos sintéticos orales como EE y dietilestilbestrol. [75] [76] [77] Además, el sulfonato de etinilestradiol (EES), un profármaco oral pero parenteral de larga duración de EE, se utiliza en el tratamiento del cáncer de próstata y se dice que tiene un perfil considerablemente mejor de seguridad cardiovascular que EE. [8]
Debido a sus efectos desproporcionados sobre la síntesis de proteínas hepáticas y los riesgos cardiovasculares asociados, los estrógenos sintéticos como el EE y el dietilestilbestrol ya no se utilizan en la terapia hormonal menopáusica. [8] También están siendo reemplazados por formas parenterales de estradiol como el fosfato de poliestradiol y el estradiol transdérmico en el tratamiento del cáncer de próstata. [75]
Daño hepático
En las dosis más bajas que se utilizan ahora en las píldoras anticonceptivas, el EE se ha asociado raramente con hepatotoxicidad colestásica de manera similar a los andrógenos 17α-alquilados / esteroides anabólicos y las progestinas 17α-etilinadas 19-nortestosterona . [78] [79] La colestasis puede manifestarse como prurito e ictericia . [80] Los metabolitos glucurónidos del EE, a través de los efectos sobre las proteínas ABCB11 (BSEP) y MRP2 (ABCC2) y los consiguientes cambios en el flujo biliar y la excreción de sales biliares , parecen ser responsables de la colestasis. [81] Concentraciones muy altas de estradiol, a través de su metabolito glucurónido de estradiol , también están implicadas en la colestasis, por ejemplo en la colestasis del embarazo . [79] Sin embargo, la incidencia y gravedad de la hepatotoxicidad colestásica parecen ser mucho mayores con EE que con estradiol, lo que se cree que se debe a la sustitución reactiva de etinil C17α en EE, así como a su susceptibilidad muy reducida al metabolismo hepático. [46] [82] Mientras que las pruebas de función hepática (LFT) anormales normalmente se encuentran en alrededor del 1% de las mujeres que no toman píldoras anticonceptivas o que toman píldoras anticonceptivas que contienen EE en dosis más bajas, esto aumenta a más del 10% de las mujeres que toman píldoras anticonceptivas que contienen 50 μg/día de EE o más. [82] [80] Con píldoras anticonceptivas que contienen 50 μg/día de EE, los niveles de alanina aminotransferasa (ALT) aumentan en un 50%, el hematocrito en un 19% y los leucocitos en un 50%, mientras que la gamma-glutamiltransferasa (GGT) disminuye en un 30%. [82] Sin embargo, los valores suelen permanecer en el rango normal. [82] Además de las pruebas de función hepática anormales, se pueden observar cambios patológicos en las funciones hepáticas parciales y la morfología hepática en la mitad de las mujeres que toman píldoras anticonceptivas con 50 μg/día de EE. [82] Las píldoras anticonceptivas que contienen EE también se han asociado con un aumento de 25 a 50 veces en el riesgo de tumores hepáticos benignos raros y un aumento de 3 a 6 veces en el riesgo de carcinoma hepatocelular , [80] [83] [84] así como un mayor riesgo de otras complicaciones hepáticas. [85] [86] En un momento dado, se estimó que las píldoras anticonceptivas que contenían EE eran responsables del 84% de todos los daños hepáticos relacionados con medicamentos y verificados histológicamente. [82] Sin embargo, estos riesgos ahora se reducen con las píldoras anticonceptivas modernas que contienen EE en dosis más bajas, que contienen 35 μg/día de EE o menos. [80] [84]
Cáncer de útero
Las altas dosis de EE que se usaban en los primeros AOC se asociaron con un riesgo significativamente mayor de cáncer de endometrio en ciertas preparaciones, por ejemplo, las que contenían el progestágeno dimetisterona . [87] Los estrógenos sin oposición como el EE tienen efectos cancerígenos en el endometrio y los progestágenos protegen contra estos efectos, pero la dimetisterona es un progestágeno relativamente débil y no pudo antagonizar adecuadamente los efectos cancerígenos endometriales del EE, lo que a su vez resultó en un mayor riesgo de cáncer de endometrio. [87] Desde entonces, los AOC que contienen dimetisterona se han discontinuado (y se han usado en su lugar progestágenos más potentes) y las dosis de EE en los AOC en general se han reducido drásticamente, anulando el riesgo. [87] A su vez, la mayoría de los estudios de AOC modernos han encontrado una disminución del riesgo de cáncer de endometrio. [88]
Efectos ecológicos
Las aguas residuales contienen varios estrógenos, incluido EE, que no se descomponen completamente con los procedimientos de tratamiento de aguas residuales . [89] La entrada de estrógenos artificiales en los ecosistemas de agua dulce afecta a las poblaciones de peces y anfibios . La exposición crónica a niveles bajos de EE durante siete años provocó el colapso de las poblaciones de peces cabeza gorda en un lago experimental en Ontario, Canadá . [89] EE cambió la ovogénesis en peces hembra y peces macho feminizados de tal manera que produjeron una proteína asociada con la maduración de los huevos, vitelogenina , así como huevos en etapa temprana. [89] En los anfibios, la exposición a EE puede reducir el éxito de eclosión y alterar el desarrollo gonadal . [90] La exposición a hormonas puede cambiar el desarrollo gonadal de las ranas aunque esté codificado en sus genes . [90] Un estudio de ranas visón encontró más renacuajos intersexuales en aquellos expuestos experimentalmente a EE que en aquellos no expuestos a EE, y las ranas verdes mostraron tasas mucho más bajas de éxito de eclosión. [90]
Sobredosis
Los estrógenos como EE son relativamente seguros en caso de sobredosis aguda . [ cita requerida ]
Interacciones
El EE es metabolizado por ciertas isoformas del citocromo P450 , incluyendo CYP3A4 y CYP2C9 . [91] Por lo tanto, los inductores de enzimas como CYP3A4 pueden disminuir las concentraciones circulantes de EE. [46] Los ejemplos de inductores incluyen anticonvulsivos como fenitoína , primidona , etosuximida , fenobarbital y carbamazepina ; antimicóticos azólicos como fluconazol ; y antibióticos rifamicina como rifampicina ( rifampicina ). [46] Por el contrario, los inhibidores de CYP3A4 y otras enzimas del citocromo P450 pueden aumentar los niveles circulantes de EE. [46] Un ejemplo es la troleandomicina , que es un inhibidor potente y altamente selectivo de CYP3A4. [46]
Se ha descubierto que el paracetamol (acetaminofén) inhibe competitivamente la sulfatación de EE, y el pretratamiento con 1000 mg de paracetamol aumenta significativamente los niveles de AUC de EE (en un 22 %) y disminuye los niveles de AUC de sulfato de etinilestradiol (sulfato de EE) en mujeres. [46] Se ha descubierto lo mismo con el ácido ascórbico (vitamina C) y el EE, aunque la importancia de la interacción se ha considerado dudosa. [46]
A diferencia del estradiol, es poco probable que exista una interacción farmacocinética entre el tabaquismo (que induce de forma potente ciertas enzimas del citocromo P450 y aumenta notablemente la 2-hidroxilación del estradiol) y el EE. [46] Esto sugiere que el estradiol y el EE son metabolizados por diferentes enzimas del citocromo P450. [46] Sin embargo, existe un mayor riesgo de complicaciones cardiovasculares con el tabaquismo y el EE, de forma similar al caso del tabaquismo y otros estrógenos. [46]
Se sabe que EE inhibe varias enzimas del citocromo P450 , incluidas CYP1A2 , CYP2B6 , CYP2C9 , CYP2C19 y CYP3A4 , y es posiblemente un inductor de CYP2A6 . [92] Como resultado, puede afectar el metabolismo y las concentraciones de muchos otros fármacos. [92] Los ejemplos de interacciones conocidas incluyen bupropión , cafeína , mefenitoína , midazolam , nicotina , nifedipina , omeprazol , propranolol , proguanil , selegilina , teofilina y tizanidina . [92] [46] Una de las interacciones más notables es que EE aumenta fuertemente los niveles de selegilina , un sustrato de CYP2B6 y CYP2C19. [92] EE también puede inducir glucuronidación y posiblemente alterar la sulfatación . [92] Se ha descubierto que aumenta el aclaramiento y reduce las concentraciones de una variedad de fármacos que se sabe que están glucuronizados. [92] Los ejemplos incluyen clofibrato , lamotrigina , lorazepam , oxazepam y propranolol . [92]
También se sabe que las progestinas, que a menudo se usan en combinación con EE, inhiben las enzimas del citocromo P450, y esto también puede contribuir a las interacciones farmacológicas con anticonceptivos que contienen EE. [92] Los ejemplos incluyen gestodeno , desogestrel y etonogestrel , que son inhibidores de CYP3A4 y CYP2C19. [92] Además, se sabe que estas progestinas inhiben progresivamente el metabolismo y aumentan las concentraciones del propio EE. [46]
Farmacología
Farmacodinamia
EE es un estrógeno similar a los estrógenos naturales como el estradiol y los estrógenos conjugados (Premarin) y los estrógenos sintéticos como el dietilestilbestrol . Se une y activa ambas isoformas del receptor de estrógeno , ERα y ERβ . [8] En un estudio, se encontró que EE tenía 233% y 38% de la afinidad del estradiol por ERα y ERβ, respectivamente. [93] En otro estudio, se encontró que poseía 194% y 151% de la afinidad del estradiol por ERα y ERβ, respectivamente. [94] EE también parece actuar como un potente agonista del receptor de estrógeno acoplado a proteína G (GPER) (afinidad desconocida), un receptor de estrógeno de membrana , de manera similar al estradiol. [95] [96] [97] [98] Los estrógenos tienen efectos antigonadotrópicos a través de la activación del ERα. [99] Como anticonceptivo, el EE actúa en conjunto con una progestina para inhibir el aumento de mitad de ciclo de la hormona luteinizante (LH) y la hormona folículo estimulante (FSH) a través de sus efectos antigonadotrópicos, inhibiendo así la foliculogénesis y previniendo la ovulación y, por lo tanto, la posibilidad de embarazo . [100] [101]
El EE es un estrógeno de acción prolongada, con una retención nuclear de aproximadamente 24 horas. [48]
Por vía oral, el EE es del orden de 100 veces más potente en peso que los estrógenos naturales como el estradiol micronizado y los estrógenos conjugados, lo que se debe en gran medida a una resistencia sustancialmente mayor al metabolismo de primer paso . [102] [103] [104] Es específicamente en el rango de 80 a 200 veces más potente que el estropipato (sulfato de piperazina estrona), que tiene una potencia similar al estradiol micronizado, en términos de potencia estrogénica sistémica. [105] [106] Por el contrario, las potencias del EE y los estrógenos naturales son similares cuando se administran por vía intravenosa , debido a la evitación del metabolismo de primer paso. [58] En relación con su profármaco mestranol , el EE es aproximadamente 1,7 veces más potente en peso por vía oral. [103]
| Ligando | Otros nombres | Afinidades de unión relativas (RBA, %) a | Afinidades de unión absolutas (K i , nM) a | Acción | ||
|---|---|---|---|---|---|---|
| ERα | ERβ | ERα | ERβ | |||
| Estradiol | E2; 17β-estradiol | 100 | 100 | 0,115 (0,04–0,24) | 0,15 (0,10–2,08) | Estrógeno |
| Estrona | E1; 17-cetoestradiol | 16,39 (0,7–60) | 6.5 (1.36–52) | 0,445 (0,3–1,01) | 1,75 (0,35–9,24) | Estrógeno |
| Estriol | E3; 16α-OH-17β-E2 | 12,65 (4,03–56) | 26 (14,0–44,6) | 0,45 (0,35–1,4) | 0,7 (0,63–0,7) | Estrógeno |
| Estetrol | E4; 15α,16α-Di-OH-17β-E2 | 4.0 | 3.0 | 4.9 | 19 | Estrógeno |
| Alfatradiol | 17α-estradiol | 20,5 (7–80,1) | 8.195 (2–42) | 0,2–0,52 | 0,43–1,2 | Metabolito |
| 16-Epiestrol | 16β-Hidroxi-17β-estradiol | 7.795 (4.94–63) | 50 | ? | ? | Metabolito |
| 17-Epiestrol | 16α-Hidroxi-17α-estradiol | 55,45 (29–103) | 79–80 | ? | ? | Metabolito |
| 16,17-Epiestrol | 16β-Hidroxi-17α-estradiol | 1.0 | 13 | ? | ? | Metabolito |
| 2-Hidroxiestradiol | 2-OH-E2 | 22 (7–81) | 11–35 | 2.5 | 1.3 | Metabolito |
| 2-Metoxiestradiol | 2-MeO-E2 | 0,0027–2,0 | 1.0 | ? | ? | Metabolito |
| 4-Hidroxiestradiol | 4-OH-E2 | 13 (8–70) | 7–56 | 1.0 | 1.9 | Metabolito |
| 4-Metoxiestradiol | 4-MeO-E2 | 2.0 | 1.0 | ? | ? | Metabolito |
| 2-Hidroxiestrona | 2-OH-E1 | 2.0–4.0 | 0,2–0,4 | ? | ? | Metabolito |
| 2-Metoxiestrona | 2-MeO-E1 | <0,001–<1 | <1 | ? | ? | Metabolito |
| 4-Hidroxiestrona | 4-OH-E1 | 1.0–2.0 | 1.0 | ? | ? | Metabolito |
| 4-Metoxiestrona | 4-MeO-E1 | <1 | <1 | ? | ? | Metabolito |
| 16α-Hidroxiestrona | 16α-OH-E1; 17-cetoestriol | 2,0–6,5 | 35 | ? | ? | Metabolito |
| 2-Hidroxiestriol | 2-OH-E3 | 2.0 | 1.0 | ? | ? | Metabolito |
| 4-Metoxiestriol | 4-MeO-E3 | 1.0 | 1.0 | ? | ? | Metabolito |
| Sulfato de estradiol | E2S; 3-sulfato de estradiol | <1 | <1 | ? | ? | Metabolito |
| Disulfato de estradiol | 3,17β-disulfato de estradiol | 0,0004 | ? | ? | ? | Metabolito |
| 3-glucurónido de estradiol | E2-3G | 0,0079 | ? | ? | ? | Metabolito |
| 17β-glucurónido de estradiol | E2-17G | 0,0015 | ? | ? | ? | Metabolito |
| 3-gluc.17β-sulfato de estradiol | E2-3G-17S | 0,0001 | ? | ? | ? | Metabolito |
| Sulfato de estrona | E1S; 3-sulfato de estrona | <1 | <1 | >10 | >10 | Metabolito |
| Benzoato de estradiol | EB; 3-benzoato de estradiol | 10 | ? | ? | ? | Estrógeno |
| 17β-benzoato de estradiol | E2-17B | 11.3 | 32.6 | ? | ? | Estrógeno |
| Éter metílico de estrona | Éter 3-metílico de estrona | 0,145 | ? | ? | ? | Estrógeno |
| ent -Estradiol | 1-Estradiol | 1.31–12.34 | 9,44–80,07 | ? | ? | Estrógeno |
| Equilina | 7-Dehidroestrona | 13 (4,0–28,9) | 13.0–49 | 0,79 | 0,36 | Estrógeno |
| Equilenina | 6,8-Didehidroestrona | 2.0–15 | 7.0–20 | 0,64 | 0,62 | Estrógeno |
| 17β-Dihidroequilina | 7-Dehidro-17β-estradiol | 7.9–113 | 7.9–108 | 0,09 | 0,17 | Estrógeno |
| 17α-Dihidroequilina | 7-Dehidro-17α-estradiol | 18.6 (18–41) | 14–32 | 0,24 | 0,57 | Estrógeno |
| 17β-Dihidroequilenina | 6,8-Didehidro-17β-estradiol | 35–68 | 90–100 | 0,15 | 0,20 | Estrógeno |
| 17α-Dihidroequilenina | 6,8-Didehidro-17α-estradiol | 20 | 49 | 0,50 | 0,37 | Estrógeno |
| Δ8 - estradiol | 8,9-Dehidro-17β-estradiol | 68 | 72 | 0,15 | 0,25 | Estrógeno |
| Δ 8 -Estrona | 8,9-Dehidroestrona | 19 | 32 | 0,52 | 0,57 | Estrógeno |
| Etinilestradiol | EE; 17α-Etinil-17β-E2 | 120,9 (68,8–480) | 44,4 (2,0–144) | 0,02–0,05 | 0,29–0,81 | Estrógeno |
| Mestranol | EE 3-metil éter | ? | 2.5 | ? | ? | Estrógeno |
| Moxestrol | RU-2858; 11β-Metoxi-EE | 35–43 | 5–20 | 0,5 | 2.6 | Estrógeno |
| Metilestradiol | 17α-Metil-17β-estradiol | 70 | 44 | ? | ? | Estrógeno |
| Dietilestilbestrol | DES; Estilbestrol | 129,5 (89,1–468) | 219,63 (61,2–295) | 0,04 | 0,05 | Estrógeno |
| Hexestrol | Dihidrodietilestilbestrol | 153.6 (31–302) | 60–234 | 0,06 | 0,06 | Estrógeno |
| Dienestrol | Dehidrostilbestrol | 37 (20.4–223) | 56–404 | 0,05 | 0,03 | Estrógeno |
| Benzestrol (B2) | – | 114 | ? | ? | ? | Estrógeno |
| Clorotrianiseno | TACE | 1,74 | ? | 15.30 | ? | Estrógeno |
| Trifeniletileno | TPE | 0,074 | ? | ? | ? | Estrógeno |
| Trifenilbromoetileno | TPBE | 2.69 | ? | ? | ? | Estrógeno |
| Tamoxifeno | ICI-46,474 | 3 (0,1–47) | 3,33 (0,28–6) | 3,4–9,69 | 2.5 | SERM |
| Afimoxifeno | 4-Hidroxitamoxifeno; 4-OHT | 100.1 (1.7–257) | 10 (0,98–339) | 2,3 (0,1–3,61) | 0,04–4,8 | SERM |
| Toremifeno | 4-Clorotamoxifeno; 4-CT | ? | ? | 7.14–20.3 | 15.4 | SERM |
| Clomifeno | LMR-41 | 25 (19.2–37.2) | 12 | 0.9 | 1.2 | SERM |
| Ciclofenil | F-6066; Sexovid | 151–152 | 243 | ? | ? | SERM |
| Nafoxidina | U-11.000A | 30.9–44 | 16 | 0.3 | 0,8 | SERM |
| Raloxifeno | – | 41.2 (7.8–69) | 5,34 (0,54–16) | 0,188–0,52 | 20.2 | SERM |
| Arzoxifeno | LY-353,381 | ? | ? | 0,179 | ? | SERM |
| Lasofoxifeno | CP-336,156 | 10.2–166 | 19.0 | 0,229 | ? | SERM |
| Ormeloxifeno | Centcromante | ? | ? | 0,313 | ? | SERM |
| Levormeloxifeno | 6720-CDRI; NNC-460,020 | 1,55 | 1,88 | ? | ? | SERM |
| Ospemifeno | Desaminohidroxitoremifeno | 0,82–2,63 | 0,59–1,22 | ? | ? | SERM |
| Bazedoxifeno | – | ? | ? | 0,053 | ? | SERM |
| Etacstil | GW-5638 | 4.30 | 11.5 | ? | ? | SERM |
| ICI-164,384 | – | 63,5 (3,70–97,7) | 166 | 0,2 | 0,08 | Antiestrógeno |
| Fulvestrant | ICI-182,780 | 43,5 (9,4–325) | 21,65 (2,05–40,5) | 0,42 | 1.3 | Antiestrógeno |
| Propilpirazoltriol | Presentación en PowerPoint | 49 (10,0–89,1) | 0,12 | 0,40 | 92.8 | Agonista de ERα |
| 16α-LE2 | 16α-Lactona-17β-estradiol | 14.6–57 | 0,089 | 0,27 | 131 | Agonista de ERα |
| 16α-Yodo-E2 | 16α-Yodo-17β-estradiol | 30.2 | 2.30 | ? | ? | Agonista de ERα |
| Metilpiperidinopirazol | Miembro del Parlamento | 11 | 0,05 | ? | ? | Antagonista de ERα |
| Diarilpropionitrilo | DP | 0,12–0,25 | 6.6–18 | 32.4 | 1.7 | Agonista de ERβ |
| 8β-VE2 | 8β-vinil-17β-estradiol | 0,35 | 22.0–83 | 12.9 | 0,50 | Agonista de ERβ |
| Prinaberel | ERB-041; VÍA-202,041 | 0,27 | 67–72 | ? | ? | Agonista de ERβ |
| ERB-196 | VÍA-202,196 | ? | 180 | ? | ? | Agonista de ERβ |
| Erteberel | SERBA-1; LY-500,307 | ? | ? | 2.68 | 0,19 | Agonista de ERβ |
| SERBA-2 | – | ? | ? | 14.5 | 1.54 | Agonista de ERβ |
| Cumestrol | – | 9,225 (0,0117–94) | 64,125 (0,41–185) | 0,14–80,0 | 0,07–27,0 | Xenoestrógeno |
| Genisteína | – | 0,445 (0,0012–16) | 33,42 (0,86–87) | 2.6–126 | 0,3–12,8 | Xenoestrógeno |
| Equol | – | 0,2–0,287 | 0,85 (0,10–2,85) | ? | ? | Xenoestrógeno |
| Daidzeína | – | 0,07 (0,0018–9,3) | 0,7865 (0,04–17,1) | 2.0 | 85.3 | Xenoestrógeno |
| Biocanina A | – | 0,04 (0,022–0,15) | 0,6225 (0,010–1,2) | 174 | 8.9 | Xenoestrógeno |
| Kaempferol | – | 0,07 (0,029–0,10) | 2,2 (0,002–3,00) | ? | ? | Xenoestrógeno |
| Naringenina | – | 0,0054 (<0,001–0,01) | 0,15 (0,11–0,33) | ? | ? | Xenoestrógeno |
| 8-Prenilnaringenina | 8-PN | 4.4 | ? | ? | ? | Xenoestrógeno |
| Quercetina | – | <0,001–0,01 | 0,002–0,040 | ? | ? | Xenoestrógeno |
| Ipriflavona | – | <0,01 | <0,01 | ? | ? | Xenoestrógeno |
| Miroestrol | – | 0,39 | ? | ? | ? | Xenoestrógeno |
| Desoximiroestrol | – | 2.0 | ? | ? | ? | Xenoestrógeno |
| β-sitosterol | – | <0,001–0,0875 | <0,001–0,016 | ? | ? | Xenoestrógeno |
| Resveratrol | – | <0,001–0,0032 | ? | ? | ? | Xenoestrógeno |
| α-zearalenol | – | 48 (13–52,5) | ? | ? | ? | Xenoestrógeno |
| β-Zearalenol | – | 0,6 (0,032–13) | ? | ? | ? | Xenoestrógeno |
| Zeranol | α-Zearalanol | 48–111 | ? | ? | ? | Xenoestrógeno |
| Taleranol | β-Zearalanol | 16 (13–17.8) | 14 | 0,8 | 0.9 | Xenoestrógeno |
| Zearalenona | ZEN | 7,68 (2,04–28) | 9.45 (2.43–31.5) | ? | ? | Xenoestrógeno |
| Zearalanona | ZAN | 0,51 | ? | ? | ? | Xenoestrógeno |
| Bisfenol A | BPA | 0,0315 (0,008–1,0) | 0,135 (0,002–4,23) | 195 | 35 | Xenoestrógeno |
| Endosulfán | EDS | <0,001–<0,01 | <0,01 | ? | ? | Xenoestrógeno |
| Kepone | Clordecona | 0,0069–0,2 | ? | ? | ? | Xenoestrógeno |
| o,p'- DDT | – | 0,0073–0,4 | ? | ? | ? | Xenoestrógeno |
| p,p'- DDT | – | 0,03 | ? | ? | ? | Xenoestrógeno |
| Metoxicloro | p,p'- Dimetoxi-DDT | 0,01 (<0,001–0,02) | 0,01–0,13 | ? | ? | Xenoestrógeno |
| HPTE | Hidroxicloro; p,p' -OH-DDT | 1.2–1.7 | ? | ? | ? | Xenoestrógeno |
| Testosterona | T; 4-Androstenolona | <0,0001–<0,01 | <0,002–0,040 | >5000 | >5000 | Andrógino |
| Dihidrotestosterona | DHT; 5α-Androstanolona | 0,01 (<0,001–0,05) | 0,0059–0,17 | 221–>5000 | 73–1688 | Andrógino |
| Nandrolona | 19-Nortestosterona; 19-NT | 0,01 | 0,23 | 765 | 53 | Andrógino |
| Dehidroepiandrosterona | DHEA; Prasterona | 0,038 (<0,001–0,04) | 0,019–0,07 | 245–1053 | 163–515 | Andrógino |
| 5-Androstenediol | A5; Androstenediol | 6 | 17 | 3.6 | 0.9 | Andrógino |
| 4-Androstenediol | – | 0,5 | 0.6 | 23 | 19 | Andrógino |
| 4-Androstenediona | A4; Androstenediona | <0,01 | <0,01 | >10000 | >10000 | Andrógino |
| 3α-Androstanodiol | 3α-Adiol | 0,07 | 0.3 | 260 | 48 | Andrógino |
| 3β-Androstanodiol | 3β-Adiol | 3 | 7 | 6 | 2 | Andrógino |
| Androstanediona | 5α-Androstanediona | <0,01 | <0,01 | >10000 | >10000 | Andrógino |
| Etiocolandiona | 5β-Androstanediona | <0,01 | <0,01 | >10000 | >10000 | Andrógino |
| Metiltestosterona | 17α-Metiltestosterona | <0,0001 | ? | ? | ? | Andrógino |
| Etinilestradiol-3α-androstanodiol | 17α-Etinil-3α-adiol | 4.0 | <0,07 | ? | ? | Estrógeno |
| Etinilestradiol-3β-androstano | 17α-Etinil-3β-adiol | 50 | 5.6 | ? | ? | Estrógeno |
| Progesterona | P4; 4-Pregnenediona | <0,001–0,6 | <0,001–0,010 | ? | ? | Progestágeno |
| Noretisterona | NET; 17α-Etinil-19-NT | 0,085 (0,0015–<0,1) | 0,1 (0,01–0,3) | 152 | 1084 | Progestágeno |
| Noretinodrel | 5(10)-Noretisterona | 0,5 (0,3–0,7) | <0,1–0,22 | 14 | 53 | Progestágeno |
| Tibolona | 7α-Metilnoretinodrel | 0,5 (0,45–2,0) | 0,2–0,076 | ? | ? | Progestágeno |
| Δ 4 -Tibolona | 7α-Metilnoretisterona | 0,069–<0,1 | 0,027–<0,1 | ? | ? | Progestágeno |
| 3α-Hidroxitibolona | – | 2,5 (1,06–5,0) | 0,6–0,8 | ? | ? | Progestágeno |
| 3β-Hidroxitibolona | – | 1,6 (0,75–1,9) | 0,070–0,1 | ? | ? | Progestágeno |
| Notas al pie: a = (1) Los valores de afinidad de unión tienen el formato "mediana (rango)" (# (#–#)), "rango" (#–#) o "valor" (#) según los valores disponibles. Los conjuntos completos de valores dentro de los rangos se pueden encontrar en el código Wiki. (2) Las afinidades de unión se determinaron mediante estudios de desplazamiento en una variedad de sistemas in vitro con estradiol marcado y proteínas ERα y ERβ humanas (excepto los valores ERβ de Kuiper et al. (1997), que son ERβ de rata). Fuentes: Ver página de plantilla. | ||||||
| Estrógeno | Afinidades de unión relativas (%) | ||||||
|---|---|---|---|---|---|---|---|
| ESReceptor de estrógeno | ArkansasReceptor de andrógenos | Relaciones públicasInformación sobre herramientas Receptor de progesterona | GRAMOInformación sobre herramientas Receptor de glucocorticoides | SEÑORInformación sobre herramientas Receptor de mineralocorticoides | SHBGInformación sobre herramientas Globulina transportadora de hormonas sexuales | CBGGlobulina transportadora de corticosteroides | |
| Estradiol | 100 | 7.9 | 2.6 | 0.6 | 0,13 | 8.7–12 | <0,1 |
| Benzoato de estradiol | ? | ? | ? | ? | ? | <0,1–0,16 | <0,1 |
| Valerato de estradiol | 2 | ? | ? | ? | ? | ? | ? |
| Estrona | 11–35 | <1 | <1 | <1 | <1 | 2.7 | <0,1 |
| Sulfato de estrona | 2 | 2 | ? | ? | ? | ? | ? |
| Estriol | 10–15 | <1 | <1 | <1 | <1 | <0,1 | <0,1 |
| Equilina | 40 | ? | ? | ? | ? | ? | 0 |
| Alfatradiol | 15 | <1 | <1 | <1 | <1 | ? | ? |
| Epiestrol | 20 | <1 | <1 | <1 | <1 | ? | ? |
| Etinilestradiol | 100–112 | 1–3 | 15–25 | 1–3 | <1 | 0,18 | <0,1 |
| Mestranol | 1 | ? | ? | ? | ? | <0,1 | <0,1 |
| Metilestradiol | 67 | 1–3 | 3–25 | 1–3 | <1 | ? | ? |
| Moxestrol | 12 | <0,1 | 0,8 | 3.2 | <0,1 | <0,2 | <0,1 |
| Dietilestilbestrol | ? | ? | ? | ? | ? | <0,1 | <0,1 |
| Notas: Los ligandos de referencia (100%) fueron progesterona para el PR.Información sobre herramientas sobre el receptor de progesterona, testosterona para la ARReceptor de andrógenos con información sobre herramientas, estradiol para el ERReceptor de estrógeno con información sobre herramientas, dexametasona para el GRReceptor de glucocorticoides con información sobre herramientas, aldosterona para el MRInformación sobre herramientas sobre el receptor de mineralocorticoides, dihidrotestosterona para SHBGInformación sobre herramientas sobre la globulina transportadora de hormonas sexuales, y cortisol para CBGGlobulina transportadora de corticosteroides. Fuentes: Ver plantilla. | |||||||
| Estrógeno | alta frecuenciaInformación sobre herramientas Sofocos | VOYInformación sobre herramientas Epitelio vaginal | Universidad de California en CaliforniaInformación sobre herramientas Calcio urinario | hormona foliculoestimulanteInformación sobre herramientas Hormona folículo estimulante | LHInformación sobre herramientas Hormona luteinizante | HDLInformación sobre herramientas Lipoproteína de alta densidad- CInformación sobre herramientas sobre colesterol | SHBGInformación sobre herramientas Globulina transportadora de hormonas sexuales | CBGGlobulina transportadora de corticosteroides | AGTInformación sobre herramientas Angiotensinógeno | Hígado |
|---|---|---|---|---|---|---|---|---|---|---|
| Estradiol | 1.0 | 1.0 | 1.0 | 1.0 | 1.0 | 1.0 | 1.0 | 1.0 | 1.0 | 1.0 |
| Estrona | ? | ? | ? | 0.3 | 0.3 | ? | ? | ? | ? | ? |
| Estriol | 0.3 | 0.3 | 0,1 | 0.3 | 0.3 | 0,2 | ? | ? | ? | 0,67 |
| Sulfato de estrona | ? | 0.9 | 0.9 | 0,8–0,9 | 0.9 | 0,5 | 0.9 | 0,5–0,7 | 1.4–1.5 | 0,56–1,7 |
| Estrógenos conjugados | 1.2 | 1.5 | 2.0 | 1.1–1.3 | 1.0 | 1.5 | 3.0–3.2 | 1.3–1.5 | 5.0 | 1.3–4.5 |
| Sulfato de equilina | ? | ? | 1.0 | ? | ? | 6.0 | 7.5 | 6.0 | 7.5 | ? |
| Etinilestradiol | 120 | 150 | 400 | 60–150 | 100 | 400 | 500–600 | 500–600 | 350 | 2,9–5,0 |
| Dietilestilbestrol | ? | ? | ? | 2.9–3.4 | ? | ? | 26–28 | 25–37 | 20 | 5,7–7,5 |
Fuentes y notas a pie de página Notas: Los valores son proporciones, con el estradiol como estándar (es decir, 1,0). Abreviaturas: HF = Alivio clínico de los sofocos . VE = Aumento de la proliferación del epitelio vaginal . UCa = Disminución de UCa.Información sobre el calcio urinario. FSH = Supresión de FSHInformación sobre herramientas sobre la hormona folículo estimulanteniveles. LH = Supresión de LHInformación sobre herramientas sobre la hormona luteinizanteniveles. HDL - C , SHBG , CBG y AGT = Aumento de los niveles séricos de estas proteínas hepáticas . Hígado = Relación entre los efectos estrogénicos hepáticos y los efectos estrogénicos generales/sistémicos (sofocos/ gonadotropinas ). Fuentes: Ver plantilla. | ||||||||||
| Compuesto | Dosis para usos específicos (mg habitualmente) [a] | ||||||
|---|---|---|---|---|---|---|---|
| ETD [b] | Declaración de protección ambiental [b] | Enfermedad de Alzheimer [b] | Enfermedad de Alzheimer [c] | Identificador único [c] | TSD [c] | ||
| Estradiol (no micronizado) | 30 | ≥120–300 | 120 | 6 | - | - | |
| Estradiol (micronizado) | 6–12 | 60–80 | 14–42 | 1–2 | >5 | >8 | |
| Valerato de estradiol | 6–12 | 60–80 | 14–42 | 1–2 | - | >8 | |
| Benzoato de estradiol | - | 60–140 | - | - | - | - | |
| Estriol | ≥20 | 120–150 [día] | 28–126 | 1–6 | >5 | - | |
| Succinato de estriol | - | 140–150 [día] | 28–126 | 2–6 | - | - | |
| Sulfato de estrona | 12 | 60 | 42 | 2 | - | - | |
| Estrógenos conjugados | 5–12 | 60–80 | 8.4–25 | 0,625–1,25 | >3,75 | 7.5 | |
| Etinilestradiol | 200 μg | 1–2 | 280 μg | 20–40 μg | 100 μg | 100 μg | |
| Mestranol | 300 μg | 1,5–3,0 | 300–600 μg | 25–30 μg | >80 μg | - | |
| Quinestrol | 300 μg | 2–4 | 500 μg | 25–50 μg | - | - | |
| Metilestradiol | - | 2 | - | - | - | - | |
| Dietilestilbestrol | 2.5 | 20–30 | 11 | 0,5–2,0 | >5 | 3 | |
| Dipropionato de DES | - | 15–30 | - | - | - | - | |
| Dienestrol | 5 | 30–40 | 42 | 0,5–4,0 | - | - | |
| Diacetato de dienestrol | 3–5 | 30–60 | - | - | - | - | |
| Hexestrol | - | 70–110 | - | - | - | - | |
| Clorotrianiseno | - | >100 | - | - | >48 | - | |
| Metalenestril | - | 400 | - | - | - | - | |
Fuentes y notas a pie de página:
| |||||||
Efectos antiandrogénicos y antigonadotrópicos

El EE es un potente antiandrógeno funcional tanto en mujeres como en hombres. [127] Media sus efectos antiandrogénicos al 1) estimular la producción de globulina transportadora de hormonas sexuales (SHBG) en el hígado , lo que disminuye las concentraciones libres y, por lo tanto, bioactivas de testosterona en la sangre; y al 2) suprimir la secreción de la hormona luteinizante (LH) de la glándula pituitaria , lo que disminuye la producción de testosterona por las gónadas . [127] [128] [35] [129] Las píldoras anticonceptivas que contienen EE son útiles en el tratamiento de afecciones dependientes de andrógenos como el acné y el hirsutismo en virtud de sus efectos antiandrogénicos. [127] [130]
Se ha descubierto que las píldoras anticonceptivas que contienen EE en mujeres reducen los niveles totales de testosterona en un 30% en promedio, aumentan los niveles de SHBG circulante en aproximadamente 3 veces en promedio (pero variable según la progestina, rango de aumento de 1,5 a 5 veces) y reducen las concentraciones de testosterona libre en un 60% en promedio (rango de 40 a 80%). [131] [65] [132] [35] Las píldoras anticonceptivas que contienen altas dosis de EE pueden aumentar los niveles de SHBG en mujeres hasta de 5 a 10 veces. [68] Esto es similar al aumento de 5 a 10 veces en los niveles de SHBG que ocurre durante el embarazo . [68] Debido al marcado aumento en los niveles de SHBG, los niveles de testosterona libre se vuelven muy bajos durante el tratamiento con píldoras anticonceptivas que contienen EE. [10] En hombres, un estudio encontró que el tratamiento con una dosis relativamente baja de 20 μg/día de EE durante cinco semanas aumentó los niveles circulantes de SHBG en un 150% y, debido a la disminución acompañante en los niveles de testosterona libre, aumentó los niveles circulantes totales de testosterona en un 50% (a través de la regulación positiva de la producción de testosterona gonadal debido a la retroalimentación negativa reducida por los andrógenos en el eje hipotálamo-hipofisario-gonadal ). [128] La estimulación de la producción hepática de SHBG por EE es mucho más fuerte que con otros estrógenos como el estradiol, debido a la alta resistencia de EE a la inactivación en el hígado y, por lo tanto, sus efectos desproporcionados en esta parte del cuerpo. [7] [10] [133]
Los estrógenos son antigonadotropinas y pueden suprimir la secreción de LH y FSH de la glándula pituitaria y, por extensión, la producción de testosterona gonadal. [134] [135] La terapia con estrógenos en dosis altas , incluso con EE, puede suprimir los niveles de testosterona en los hombres en alrededor del 95%, o en el rango de castración/mujer. [136] [134] [135] La dosis de EE necesaria para su uso como componente de la terapia hormonal para mujeres transgénero preoperatorias es de 50 a 100 μg/día. [137] Esta dosis alta se asocia con una alta incidencia de TEV, particularmente en mayores de 40 años, y se ha dicho que no debería usarse. [137] La dosis de EE utilizada en el tratamiento del cáncer de próstata en hombres es de 150 a 1000 μg/día (0,15–1,0 mg/día). [8] [138] Se ha descubierto que una dosis de EE de 50 μg dos veces al día (100 μg/día en total) suprime los niveles de testosterona en los hombres en un grado equivalente a 3 mg/día de dietilestilbestrol oral , que es la dosis mínima de dietilestilbestrol necesaria para suprimir de forma constante los niveles de testosterona hasta el rango de castración. [139] La dosis inhibidora de la ovulación de EE por sí sola y no en combinación con una progestina en mujeres es de 100 μg/día. [140] [141] Sin embargo, se ha descubierto que tiene una eficacia de alrededor del 75 al 90 % para inhibir la ovulación con una dosis de 20 μg/día y de alrededor del 97 o 98 % con una dosis de 50 μg/día. [142] [143] [144] [145] En otro estudio, la ovulación se produjo en el 25,2% con una dosis de EE de 50 μg/día. [146]
Dosis más bajas de EE también tienen efectos antigonadotrópicos significativos. [137] Una dosis "muy baja" de 15 μg/día de EE se ha descrito como la cantidad "límite" necesaria para la supresión de los niveles de LH y testosterona en hombres, y un estudio encontró que los niveles de LH y testosterona se suprimieron "fiablemente" en hombres con una dosis de 30 μg/día de EE. [8] Sin embargo, otros estudios clínicos han encontrado que 20 μg/día de EE aumentaron los niveles de testosterona en un 50% en hombres (como se describió anteriormente) [128] y que dosis de 32 μg/día y 42 μg/día de EE suprimieron los niveles de FSH en hombres pero no afectaron significativamente los niveles de LH. [8] Se observó una supresión más fuerte de los niveles de testosterona en hombres después del tratamiento diario con un anticonceptivo oral combinado que contenía 50 μg de etinilestradiol y 0,5 mg de norgestrel durante 9 días. [8] Sin embargo, la investigación reveló que la progestina era el componente más importante responsable de la supresión de los niveles de testosterona. [8] De acuerdo con esto, el componente de progestina de los AOC es el principal responsable de la inhibición de la ovulación en las mujeres. [8] Se encontró que una combinación de 20 μg/día de EE y 10 mg/día de metiltestosterona suprimía la secreción de FSH en los hombres en un grado suficiente para detener la espermatogénesis . [8] Los estudios en mujeres han encontrado que 50 μg/día de EE suprimen los niveles de LH y FSH en aproximadamente un 70% en mujeres posmenopáusicas. [106]
Además de sus efectos antigonadotrópicos, el EE puede suprimir significativamente la producción de andrógenos por las glándulas suprarrenales en altas concentraciones. [8] [147] [148] Un estudio encontró que el tratamiento con una dosis alta de 100 μg/día de EE suprimió los niveles circulantes de andrógenos suprarrenales en un 27 a 48% en mujeres transgénero. [8] [147] [148] Esto puede contribuir adicionalmente a la supresión de los niveles de andrógenos por los estrógenos. [8] [147] [148]
Efectos sobre la síntesis de proteínas hepáticas
EE tiene efectos marcados en la síntesis de proteínas hepáticas , incluso en dosis bajas e independientemente de la vía de administración . [8] [7] Estos efectos están mediados por su actividad estrogénica. [8] [7] El medicamento aumenta de forma dosis-dependiente los niveles circulantes de SHBG, globulina transportadora de corticosteroides (CBG) y globulina transportadora de tiroxina (TBG), y también afecta a una amplia gama de otras proteínas hepáticas. [8] [7] EE afecta los niveles de triglicéridos en una dosis tan baja como 1 μg/día y los niveles de colesterol LDL y HDL en una dosis tan baja como 2,5 μg/día. [149] EE afecta varias proteínas hepáticas en una dosis tan baja como 5 μg/día. [8] En dosis superiores a 20 μg/día, los efectos incrementales de EE en la síntesis de proteínas hepáticas se vuelven continuamente más pequeños. [8]
Se ha descubierto que el EE a 5 μg/día aumenta los niveles de SHBG en un 100% en mujeres posmenopáusicas, mientras que una dosis de 20 μg/día de EE los aumentó en un 200%. [8] Los andrógenos disminuyen la producción hepática de SHBG y se ha descubierto que se oponen a los efectos del EE en los niveles de SHBG. [8] Esto es de particular relevancia cuando se considera que muchas progestinas utilizadas en AOC tienen diversos grados de actividad androgénica débil. [8] Una combinación de 20 μg/día de EE y 0,25 mg/día de levonorgestrel , una progestina con androgenicidad relativamente alta, disminuye los niveles de SHBG en un 50%; 30 μg/día de EE y 0,25 mg/día de levonorgestrel no tienen efecto sobre los niveles de SHBG; 30 μg/día de EE y 0,15 mg/día de levonorgestrel aumentan los niveles de SHBG en un 30%; y los AOC trifásicos que contienen EE y levonorgestrel aumentan los niveles de SHBG en un 100 a 150%. [8] La combinación de 30 μg/día de EE y 150 μg/día de desogestrel , una progestina con una androgenicidad relativamente débil que el levonorgestrel, aumenta los niveles de SHBG en un 200%, mientras que la combinación de 35 μg/día de EE y 2 mg/día de acetato de ciproterona , una progestina con potente actividad antiandrogénica , aumenta los niveles de SHBG en un 400%. [8] Como tal, el tipo y la dosis de progestina contenida en los AOC moderan potentemente los efectos del EE en los niveles de SHBG. [8]
Se ha descubierto que una dosis de 10 μg/día de EE aumenta los niveles de CBG en un 50%, mientras que una dosis de 20 μg/día de EE los aumenta en un 100%. [8] Las progestinas que son derivados de la progesterona no tienen efecto sobre los niveles de CBG, mientras que las progestinas androgénicas como los derivados de la 19-nortestosterona tienen solo un efecto débil sobre los niveles de CBG. [8] Los AOC pueden aumentar los niveles de CBG entre un 100 y un 150%. [8] Se ha descubierto que una dosis de 5 μg/día de EE aumenta los niveles de TBG en un 40%, mientras que una dosis de 20 μg/día de EE los aumenta en un 60%. [8] Las progestinas que son derivados de la progesterona no afectan los niveles de TBG, mientras que las progestinas con actividad androgénica pueden disminuir los niveles de TBG. [8] Se ha descubierto que una combinación de 30 μg/día de EE y 1 mg/día de noretisterona , una progestina moderadamente androgénica, aumenta los niveles de TBG entre un 50 y un 70%, mientras que la combinación de 30 μg/día de EE y 150 μg/día de desogestrel los aumenta en un 100%. [8]
Diferencias con el estradiol


El EE muestra efectos fuertes y desproporcionados sobre la síntesis de proteínas hepáticas en relación con el estradiol. [7] El hígado , así como el útero, expresan 17β-hidroxiesteroide deshidrogenasa (17β-HSD), y esta enzima sirve para inactivar el estradiol y suprimir eficazmente su potencia en estos tejidos al convertirlo reversiblemente en el estrógeno mucho menos potente estrona (que tiene aproximadamente el 4% de la actividad estrogénica del estradiol). [7] A diferencia del estradiol, el grupo 17α-etinilo del EE previene la oxidación de la posición C17β del EE por 17β-HSD, y por esta razón, el EE no se inactiva en estos tejidos y tiene una actividad estrogénica relativa mucho más fuerte en ellos. [7] [150] [11] Este es el mecanismo de los efectos desproporcionadamente fuertes del EE sobre la producción de proteínas hepáticas, [7] [150] lo que resulta en una magnitud mucho mayor del efecto sobre la TEV y los riesgos cardiovasculares en relación con el estradiol. [151]
Por otra parte, debido a la pérdida de la inactivación de EE por 17β-HSD en el endometrio (útero), el EE es relativamente más activo que el estradiol en el endometrio y, por esta razón, se asocia con una incidencia significativamente menor de sangrado vaginal y manchado en comparación. [7] Esto es particularmente así en el caso de la terapia combinada de estrógeno y progestágeno (como en los AOC o la THS menopáusica), ya que los progestágenos inducen la expresión de 17β-HSD en el endometrio. [7] El sangrado vaginal y el manchado reducidos con EE es una de las principales razones por las que se utiliza en los AOC en lugar del estradiol, [3] a pesar de su perfil de seguridad potencialmente inferior (relacionado con sus efectos adversos sobre la síntesis de proteínas hepáticas y la incidencia de TEV). [152]
Se ha descubierto que el EE tiene efectos desproporcionados en la síntesis de proteínas hepáticas y el riesgo de TEV independientemente de si la vía de administración es oral, transdérmica o vaginal, lo que indica que el uso de vías parenterales en lugar de la vía oral no da como resultado que el EE tenga acciones hepáticas proporcionales en relación con las acciones no hepáticas. [150] [8] Sin embargo, la potencia del EE en la síntesis de proteínas hepáticas se reduce en cualquier caso con la administración parenteral. [8] Se ha descubierto que una dosis de 10 μg/día de EE vaginal es equivalente a 50 μg de EE oral en términos de efectos en la síntesis de proteínas hepáticas, como la estimulación de la producción hepática de SHBG. [8] Como tal, se ha descubierto que el EE parenteral, que evita el primer paso a través del hígado que ocurre con el EE oral, tiene un impacto 5 veces menor en la síntesis de proteínas hepáticas en peso que el EE oral. [8] A diferencia del EE y del estradiol oral, el estradiol transdérmico muestra pocos o ningún efecto sobre la síntesis de proteínas hepáticas en dosis menopáusicas típicas. [7]
| Parámetros | Estradiol | Etinilestradiol |
|---|---|---|
| ESReceptor de estrógeno afinidad | 1 × 10 10 M -1 | 2–5 × 10 11 M -1 |
| Retención nuclear | 6–8 horas | 24 horas |
| Vida media de eliminación | 90 minutos | 7 horas |
| Sustrato para 17β-HSDDescripción de herramienta 17β-hidroxiesteroide deshidrogenasa? | Sí | No |
| Vinculado a SHBGInformación sobre herramientas Globulina transportadora de hormonas sexuales? | Sí | No |
| Potencia hepática oral relativa | 1 | ~500–1.500 |
| Potencia hipofisaria oral relativa | 1 | 200 |
| Fuentes: [72] | ||
Farmacocinética
Absorción
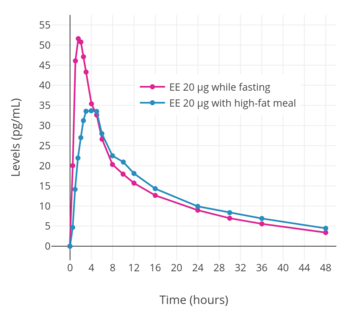
La biodisponibilidad oral de EE es del 45% en promedio, con un amplio rango de 20% a 74% (aunque más comúnmente entre 38 y 48%) que se debe a una alta variabilidad interindividual . [10] [4] Aunque relativamente baja, la biodisponibilidad oral de EE es considerablemente mayor que la del estradiol micronizado (5%). [2] [10] Después de una dosis única de 20 μg de EE en combinación con 2 mg de acetato de noretisterona en mujeres posmenopáusicas, se ha encontrado que las concentraciones de EE alcanzan un máximo de 50 pg/mL en un promedio de 1,5 horas. [7] Después de la primera dosis, los niveles medios de EE en general aumentan aún más en aproximadamente un 50% hasta que se alcanzan concentraciones en estado estacionario ; [7] [153] el estado estacionario se alcanza después de una semana de administración diaria. [8] A modo de comparación, los niveles pico medios de estradiol alcanzados con 2 mg de estradiol micronizado o valerato de estradiol son 40 pg/ml después de la primera dosis y 80 pg/ml después de tres semanas de administración. [7] Estas concentraciones máximas de estradiol están en el mismo rango que las concentraciones de EE que se producen con una dosis oral de EE que es 100 veces menor en peso, lo que concuerda con la potencia oral aproximadamente 100 veces mayor de EE en relación con el estradiol. [102] [7] De acuerdo con la alta variabilidad interindividual en la biodisponibilidad oral de EE, existe un gran grado de variación interindividual en los niveles de EE. [7] [154] Se ha descubierto que una dosis de EE de 50 μg/día alcanza un amplio rango de niveles circulantes de EE de aproximadamente 100 a 2000 pg/ml. [155] [154] Se ha descubierto que tomar EE en combinación con una comida rica en grasas reduce significativamente sus concentraciones máximas. [153] [7]
Los niveles de EE después de una dosis única de 50 μg por inyección intravenosa son varias veces más altos que los niveles de EE después de una dosis única de 50 mg administrada por vía oral. [155] Además de la diferencia en los niveles, el curso de eliminación es similar para las dos vías. [155]
Puede haber diferencias específicas de género en la farmacocinética del EE, de modo que el EE puede tener una mayor potencia oral en mujeres que en hombres. [8] Un estudio encontró que una combinación de 60 μg/día de EE y 0,25 mg/día de levonorgestrel en mujeres y hombres resultó en niveles máximos de EE de 495 pg/mL y 251 pg/mL, niveles de área bajo la curva de EE de 6,216 pg/mL/hora y 2,850 pg/mL/hora, y vidas medias de eliminación de 16,5 horas y 10,2 horas, respectivamente. [8] Se ha sugerido que este fenómeno podría representar un "mecanismo de protección" de los hombres contra la exposición al estrógeno ambiental . [8]
Distribución
La unión de EE a las proteínas plasmáticas es del 97 al 98%, y se une casi exclusivamente a la albúmina . [5] [7] [10] [156] A diferencia del estradiol, que se une con alta afinidad a la SHBG, el EE tiene una afinidad muy baja por esta proteína, aproximadamente el 2% de la del estradiol, y por lo tanto no se une a ella de manera importante. [157]
Metabolismo
Debido al alto metabolismo de primer paso en los intestinos y el hígado , solo el 1% de una dosis oral de un EE aparece en la circulación como EE en sí. [7] Durante el metabolismo de primer paso, el EE se conjuga ampliamente a través de glucuronidación y sulfatación en los glucurónidos de etinilestradiol y sulfato de etinilestradiol (sulfato de EE), hormonalmente inertes, y los niveles de sulfato de EE en circulación son entre 6 y 22 veces más altos que los de EE. [7] [4] A modo de comparación, con la administración oral de 2 mg de estradiol micronizado, los niveles de estrona y sulfato de estrona son de 4 a 6 veces y 200 veces más altos que los de estradiol, respectivamente. [7] A diferencia del estradiol, el EE, debido al impedimento estérico de su grupo etinilo C17α, no es metabolizado ni inactivado por la 17β-HSD, [11] y este es el factor principal responsable de la potencia drásticamente aumentada del EE oral en relación con el estradiol oral. [7] El EE tampoco se metaboliza en estradiol. [158]
Aparte de la conjugación con sulfato, el EE se metaboliza principalmente por hidroxilación en estrógenos catecol . [7] Esto es principalmente por 2-hidroxilación en 2-hidroxi-EE, que es catalizada principalmente por CYP3A4 . [10] También se ha informado de la hidroxilación de EE en las posiciones C4, C6α y C16β en 4-, 6α- y 16β-hidroxi-EE, pero parece contribuir a su metabolismo solo en pequeña medida. [10] El 2- y 4-metoxi-EE también se forman a través de la transformación por la catecol O-metiltransferasa de 2- y 4-hidroxi-EE. [7] A diferencia del caso del estradiol, la 16α-hidroxilación no ocurre con EE, debido al impedimento estérico por su grupo etinilo en C17α. [10] [7] La etinilación de EE es en gran medida irreversible, por lo que el EE no se metaboliza en estradiol, a diferencia de los ésteres de estradiol . [7] Una revisión encontró que el rango de la vida media de eliminación informada de EE en la literatura fue de 13,1 a 27,0 horas. [2] Otra revisión informó una vida media de eliminación de EE de 10 a 20 horas. [10] Sin embargo, otras fuentes también han informado que la vida media de eliminación de EE es tan corta como 7 horas [11] y tan larga como 36 horas. [9]
A diferencia del caso del estradiol, en el que hay un aumento rápido de sus niveles y que permanecen elevados en una curva similar a una meseta durante muchas horas, los niveles de EE caen rápidamente después de alcanzar el pico. [7] Se cree que esto se debe a que la estrona y el sulfato de estrona pueden convertirse reversiblemente de nuevo en estradiol y servir como un reservorio hormonalmente inerte para el estradiol, mientras que el reservorio de sulfato de EE para EE es mucho más pequeño en comparación. [7] [4] En cualquier caso, debido a la formación de sulfato de EE, la recirculación enterohepática está involucrada en la farmacocinética de EE de manera similar al estradiol, aunque en menor medida. [7] [159] La contribución de la recirculación enterohepática a los niveles circulantes totales de EE parece ser del 12 al 20% o menos, y no se observa de manera consistente. [8] [159] A menudo se puede observar un pico secundario en los niveles de EE de 10 a 14 horas después de la administración con EE oral. [159]
El EE, tras la formación oxidativa de un metabolito muy reactivo , inhibe irreversiblemente las enzimas del citocromo P450 implicadas en su metabolismo, y esto también puede desempeñar un papel en la mayor potencia del EE en relación con el estradiol. [7] De hecho, se dice que el EE tiene un efecto marcado en el metabolismo hepático, y esta es una de las razones, entre otras, por las que los estrógenos naturales como el estradiol pueden ser preferibles. [156] Se ha observado una acumulación de dos veces en los niveles de EE con un AOC que contiene EE después de 1 año de terapia. [159]
Eliminación
El EE se elimina en un 62% en las heces y en un 38% en la orina . [10]
Química
EE, también conocido como 17α-etinilestradiol o como 17α-etinilestra-1,3,5(10)-trieno-3,17β-diol, es un esteroide estrano sintético y un derivado del estradiol con una sustitución de etinilo en la posición C17α. [1] [160] La 17α-etinilación del estradiol para crear EE es análoga a la 17α-sustitución de testosterona para producir derivados de testosterona como progestinas 17α-etiniladas como etisterona (17α-etiniltestosterona) y noretisterona (17α-etiniltestosterona-19-nortestosterona), así como andrógenos 17α-alquilados / esteroides anabólicos como metiltestosterona (17α-metiltestosterona).
Análogos
Existen varios derivados de EE. [1] [160] Estos incluyen mestranol (EE 3-metil éter), quinestrol (EE 3-ciclopentil éter), sulfonato de etinilestradiol (EE 3-isopropilsulfonato) y moxestrol (11β-metoxi-EE). [1] [160] [8] Los tres primeros son profármacos de EE, mientras que el último no lo es. [8] Existen algunos análogos de EE con otras sustituciones en la posición C17α. [1] [160] Los ejemplos incluyen los derivados de estradiol metilestradiol (17α-metilestradiol) y etilestradiol (17α-etilestradiol), y los derivados de estriol etinilestriol (17α-etinilestriol) y nilestriol (17α-etinilestriol 3-ciclopentil éter). [1] [160] Los análogos de androstano de EE con actividad estrogénica significativa aunque débil incluyen etinilandrostenediol (17α-etinil-5-androstenediol), 17α-etinil-3β-androstanediol , 17α-etinil-3α-androstanediol y metandriol (17α-metil-5-androstenediol).
Historia
EE fue el primer estrógeno sintético activo por vía oral y fue descrito en 1938 por Hans Herloff Inhoffen y Walter Hohlweg de Schering AG en Berlín . [161] [162] [163] [164] [165] Fue aprobado por la Administración de Alimentos y Medicamentos de los Estados Unidos (FDA) en junio de 1943 y comercializado por Schering bajo la marca Estinyl. [14] La FDA retiró la aprobación de Estinyl a partir del 4 de junio de 2004 a pedido de Schering , que había descontinuado su comercialización. [166]
La EE nunca se introdujo para su uso mediante inyección intramuscular . [167]
El EE se utilizó por primera vez en AOC, como alternativa al mestranol , en 1964, y poco después reemplazó al mestranol en los AOC. [15]
Los primeros AOC contenían entre 40 y 100 μg/día de EE y entre 50 y 150 μg/día de mestranol. [168] [169]
Sociedad y cultura
Nombres genéricos
Etinilestradiol es el nombre genérico en inglés del medicamento y su DCI.Tooltip Nombre común internacional, USANDescripción emergente Nombre adoptado por Estados Unidos, PROHIBICIÓNDescripción emergente Nombre aprobado en Gran Bretaña, y ENEDescripción emergente Nombre aceptado en japonés. [170] [1] [171] [160] También se ha escrito como etinilestradiol , etinilestradiol y etinilestradiol (todos con la misma pronunciación), y este último era anteriormente su BAN .Descripción emergente Nombre aprobado en Gran Bretañapero finalmente se cambió. [170] [1] [160] Además, a menudo se incluye un espacio en el nombre de EE de modo que se escribe como etinilestradiol (así como variaciones del mismo), y esta es su USP.Información sobre herramientas de la Farmacopea de los Estados Unidosnombre. [170] [160] El nombre genérico de EE en francés y su DCFInformación sobre herramientas Denominación Comuna Francesason étinilestradiol , en español es etinilestradiol , en italiano es DCITInformación sobre herramientas Denominación Comune Italianason etinilestradiolo , y en latín es ethinylestradiolum . [170] [160]
En la literatura médica, el nombre del fármaco suele abreviarse como EE o como EE2 .
Nombres de marca
EE se ha comercializado como un fármaco oral independiente bajo las marcas Esteed , Estinyl , Feminone , Lynoral , Menolyn , Novestrol , Palonyl , Spanestrin e Ylestrol , entre otras, aunque la mayoría o todas estas formulaciones ahora están descontinuadas. [172] [173] [160] Se comercializa bajo una gran cantidad de marcas en todo el mundo en combinación con progestinas para su uso como anticonceptivo oral. [170] Además, EE se comercializa en los EE. UU. en combinación con norelgestromina bajo las marcas Ortho Evra y Xulane como parche anticonceptivo , en combinación con etonogestrel bajo la marca NuvaRing como anillo vaginal anticonceptivo y en combinación con acetato de noretisterona bajo la marca FemHRT en terapia de reemplazo hormonal oral para el tratamiento de los síntomas de la menopausia. [12]
Disponibilidad
El etinilestradiol se comercializa en todo el mundo. [170] [160] Se comercializa exclusivamente o casi exclusivamente en combinación con progestinas. [170]
Referencias
- ^ abcdefgh Elks J (14 de noviembre de 2014). Diccionario de fármacos: datos químicos: datos químicos, estructuras y bibliografías. Springer. pp. 522–. ISBN 978-1-4757-2085-3.
- ^ abcd Goldzieher JW, Brody SA (diciembre de 1990). "Farmacocinética del etinilestradiol y el mestranol". Revista estadounidense de obstetricia y ginecología . 163 (6 puntos 2): 2114–2119. doi :10.1016/0002-9378(90)90550-Q. PMID 2256522.
- ^ ab Fruzzetti F, Trémollieres F, Bitzer J (mayo de 2012). "Una visión general del desarrollo de anticonceptivos orales combinados que contienen estradiol: enfoque en valerato de estradiol/dienogest". Endocrinología ginecológica . 28 (5): 400–408. doi :10.3109/09513590.2012.662547. PMC 3399636 . PMID 22468839.
- ^ abcd Fotherby K (agosto de 1996). "Biodisponibilidad de los esteroides sexuales administrados por vía oral utilizados en la anticoncepción oral y la terapia de reemplazo hormonal". Anticoncepción . 54 (2): 59–69. doi :10.1016/0010-7824(96)00136-9. PMID 8842581.
- ^ ab Facts and Comparisons (Firm), Ovid Technologies, Inc (2005). Drug Facts and Comparisons 2005: Versión de bolsillo. Facts and Comparisons. pág. 121. ISBN 978-1-57439-179-4.
- ^ Micromedex (1 de enero de 2003). USP DI 2003: Información sobre medicamentos para profesionales de la salud. Thomson Micromedex. págs. 1253, 1258, 1266. ISBN 978-1-56363-429-1.
- ^ abcdefghijklmnopqrstu vwxyz aa ab ac ad ae af ag ah ai aj ak al am an ao ap aq ar as Kuhl H (agosto de 2005). "Farmacología de los estrógenos y progestágenos: influencia de diferentes vías de administración". Climaterio . 8 (Supl. 1): 3–63. doi :10.1080/13697130500148875. PMID 16112947. S2CID 24616324.
- ^ abcdefghijklmnopqrstu vwxyz aa ab ac ad ae af ag ah ai aj ak al am an ao ap aq ar as at au Oettel M, Schillinger E (6 de diciembre de 2012). Estrógenos y antiestrógenos II: farmacología y aplicación clínica de estrógenos y antiestrógenos. Springer Science & Business Media. págs. 4, 10, 15, 165, 247–248, 276–291, 363–408, 424, 514, 540, 543, 581. ISBN 978-3-642-60107-1La afinidad de unión del EE2 por el receptor de estrógeno es similar a la del estradiol. [...] Durante la ingesta diaria, los niveles de EE2 aumentan
hasta un estado estable que se alcanza después de aproximadamente 1 semana.
- ^ abc Hughes CL, Waters MD (23 de marzo de 2016). Toxicología traslacional: definición de una nueva disciplina terapéutica. Humana Press. pp. 73–. ISBN 978-3-319-27449-2.
- ^ abcdefghijklmn Stanczyk FZ, Archer DF, Bhavnani BR (junio de 2013). "Etinilestradiol y 17β-estradiol en anticonceptivos orales combinados: farmacocinética, farmacodinamia y evaluación de riesgos". Anticoncepción . 87 (6): 706–727. doi :10.1016/j.contraception.2012.12.011. PMID 23375353.
- ^ abcd Shellenberger TE (1986). "Farmacología de los estrógenos". El climaterio en perspectiva . págs. 393–410. doi :10.1007/978-94-009-4145-8_36. ISBN 978-94-010-8339-3
El etinilestradiol es un estrógeno sintético y relativamente potente. Como resultado de la alquilación en la posición 17-C, no es un sustrato para la 17β deshidrogenasa, una enzima que transforma el estradiol-17β natural en la estrona, menos potente, en los órganos diana
. - ^ abcd "Drugs@FDA: Productos farmacéuticos aprobados por la FDA". Administración de Alimentos y Medicamentos de los Estados Unidos (FDA) . Consultado el 22 de diciembre de 2016 .
- ^ Fischer J, Ganellin CR (2006). Descubrimiento de fármacos basado en análogos. John Wiley & Sons. pág. 482. ISBN 978-3-527-60749-5.
- ^ ab Administración de Alimentos y Medicamentos de Estados Unidos (FDA) (2007). "Historial de aprobación: Estinyl (etinilestradiol) NDA 005292".búsqueda: Estinyl
- ^ ab Gruhn JG, Kazer RR (11 de noviembre de 2013). Regulación hormonal del ciclo menstrual: la evolución de los conceptos. Springer Science & Business Media. pp. 185–. ISBN 978-1-4899-3496-3En 1964 ,
se introdujo el etinilestradiol como alternativa al mestranol como componente estrogénico, [...]
- ^ Evans G, Sutton EL (mayo de 2015). "Anticoncepción oral". Clínicas Médicas de Norteamérica . 99 (3): 479–503. doi :10.1016/j.mcna.2015.01.004. PMID 25841596.
- ^ Shoupe D, Haseltine FP (6 de diciembre de 2012). Anticoncepción. Springer Science & Business Media. pp. 112–. ISBN 978-1-4612-2730-4.
- ^ abcdefghi «Los 300 mejores del 2022». ClinCalc . Archivado desde el original el 30 de agosto de 2024 . Consultado el 30 de agosto de 2024 .
- ^ "Estadísticas de uso de etinilestradiol y noretindrona, Estados Unidos, 2013-2022". ClinCalc . Consultado el 30 de agosto de 2024 .
- ^ "Estadísticas de uso de etinilestradiol y norgestimato, Estados Unidos, 2013-2022". ClinCalc . Consultado el 30 de agosto de 2024 .
- ^ "Estadísticas de uso de etinilestradiol y levonorgestrel, Estados Unidos, 2013-2022". ClinCalc . Consultado el 30 de agosto de 2024 .
- ^ "Estadísticas de uso de drospirenona y etinilestradiol, Estados Unidos, 2013-2022". ClinCalc . Consultado el 30 de agosto de 2024 .
- ^ "Desogestrel; Estadísticas de uso de fármacos de etinilestradiol, Estados Unidos, 2013-2022". ClinCalc . Consultado el 30 de agosto de 2024 .
- ^ "Estadísticas de uso de etinilestradiol y etonogestrel, Estados Unidos, 2013-2022". ClinCalc . Consultado el 30 de agosto de 2024 .
- ^ "Estadísticas de uso de etinilestradiol y norgestrel, Estados Unidos, 2013-2022". ClinCalc . Consultado el 30 de agosto de 2024 .
- ^ "Estadísticas de uso de fármacos drospirenona, etinilestradiol y levomefolato, Estados Unidos, 2013-2022". ClinCalc . Consultado el 30 de agosto de 2024 .
- ^ "Etinilestradiol; Estadísticas de uso de etinodiol, Estados Unidos, 2013-2022". ClinCalc . Archivado desde el original el 18 de enero de 2024 . Consultado el 30 de agosto de 2024 .
- ^ ab Rowan JP, Simon JA, Speroff L, Ellman H (junio de 2006). "Efectos del acetato de noretindrona en dosis bajas más etinilestradiol (0,5 mg/2,5 microg) en mujeres con síntomas posmenopáusicos: análisis actualizado de tres ensayos controlados aleatorizados". Clinical Therapeutics . 28 (6): 921–932. doi :10.1016/j.clinthera.2006.06.013. PMID 16860174.
- ^ Hamoda H, Panay N, Arya R, Savvas M (diciembre de 2016). "Recomendaciones de 2016 de la British Menopause Society y Women's Health Concern sobre la terapia de reemplazo hormonal en mujeres menopáusicas". Salud post-reproductiva . 22 (4): 165–183. doi : 10.1177/2053369116680501 . hdl : 1983/d96e4479-2ccc-44c3-963c-d3918b1e325b .
- ^ ab Unger CA (diciembre de 2016). "Terapia hormonal para pacientes transgénero". Andrología y Urología Traslacional . 5 (6): 877–884. doi : 10.21037/tau.2016.09.04 . PMC 5182227 . PMID 28078219.
- ^ ab Coelingh Bennink HJ, Verhoeven C, Dutman AE, Thijssen J (enero de 2017). "El uso de estrógenos en dosis altas para el tratamiento del cáncer de mama". Maturitas . 95 : 11-23. doi : 10.1016/j.maturitas.2016.10.010 . PMID 27889048.
- ^ Thibaut F, De La Barra F, Gordon H, Cosyns P, Bradford JM (junio de 2010). "Directrices de la Federación Mundial de Sociedades de Psiquiatría Biológica (WFSBP) para el tratamiento biológico de las parafilias". The World Journal of Biological Psychiatry . 11 (4): 604–655. doi :10.3109/15622971003671628. PMID 20459370. S2CID 14949511.
- ^ Bancroft J, Tennent G, Loucas K, Cass J (septiembre de 1974). "El control de la conducta sexual desviada mediante fármacos. I. Cambios conductuales tras el uso de estrógenos y antiandrógenos". The British Journal of Psychiatry . 125 (586): 310–315. doi :10.1192/bjp.125.3.310. PMID 4607733. S2CID 10971754.
- ^ "Terapia hormonal para la menopausia y riesgo de cáncer". Sociedad Estadounidense del Cáncer. 13 de febrero de 2015.
- ^ abc Grupo de trabajo del IARC sobre la evaluación de los riesgos carcinógenos para los seres humanos, Organización Mundial de la Salud, Agencia Internacional para la Investigación sobre el Cáncer (2007). Anticonceptivos combinados de estrógeno y progestágeno y terapia combinada de estrógeno y progestágeno para la menopausia. Organización Mundial de la Salud. pp. 157, 433–. ISBN 978-92-832-1291-1.
- ^ abc Becker KL (2001). Principios y práctica de endocrinología y metabolismo. Lippincott Williams & Wilkins. pág. 1027. ISBN 978-0-7817-1750-2.
- ^ DIANE Publishing Company (1995). Medicamentos aprobados con evaluaciones terapéuticas. DIANE Publishing. pág. 3-122. ISBN 978-0-7881-0405-3ETINIL
ESTRADIOL: TABLETA; ORAL: ESTINYL: SCHERING: 0,02 MG; 0,05 MG; 0,5 MG
- ^ Medicamentos recetados aprobados con evaluaciones de equivalencia terapéutica. Departamento de Salud y Servicios Humanos de los EE. UU., Servicio de Salud Pública, Administración de Alimentos y Medicamentos, Oficina de Medicamentos. 1980. OCLC 7074861.
- ^ Muller (19 de junio de 1998). Índice europeo de medicamentos: Registros europeos de medicamentos, cuarta edición (4.ª ed.). CRC Press. pp. 457–. ISBN 978-3-7692-2114-5.
Etinilestradiol 0,05 mg cpr 0,05 mg etinilestradiol (G03CA01) (FR) Etinilestradiol comprimidos 50 mcg Etinilestradiol (G03CA01) (RUS) Etinilestradiol 25 μg (Jenapharm) Grageas: Etinilestradiol 25 μg (G03CA01) (DE) Etinilestradiol pch 0,002 mg cpr 0,002 mg etinilestradiol (FR) Etinilestradiol comprimido 0,05 mg etinilestradiol 0,05 mg (G03CA01) (NL) [...] Etifollin tab 0,5 mg (Nycomed pharma a/s) etinilestradiol (L02AA03) (NO) Etifollin tab 50 mcg (Nycomed pharma a/s) etinilestradiol (G03CA01) (NO)
- ^ S. Monfardini, K. Brunner, D. Crowther, S. Eckhardt, D. Olive, S. Tanneberger, A. Veronesi, JMA Whitehouse, R. Wittes, eds. (6 de diciembre de 2012). Manual de oncología médica pediátrica y para adultos. Springer Science & Business Media. págs. 78–. ISBN 978-3-642-82489-0. OCLC 1058058829.
Etinilestradiol (Lynoral, comprimidos de 0,05 mg, 0,1 mg y 1 mg)
- ^ ab Lip GY, Hall JE (28 de junio de 2007). Libro electrónico completo sobre hipertensión. Elsevier Health Sciences. págs. 865–. ISBN 978-0-323-07067-6.
- ^ ab Alldredge BK, Corelli RL, Ernst ME (1 de febrero de 2012). Koda-Kimble y Young's Applied Therapeutics: The Clinical Use of Drugs. Lippincott Williams & Wilkins. págs. 1072–. ISBN 978-1-60913-713-7.
- ^ "Recomendaciones de prácticas seleccionadas de EE. UU. para el uso de anticonceptivos, 2016" (PDF) . Recomendaciones e informes . Vol. 65, núm. 4. Centros para el Control y la Prevención de Enfermedades. 29 de julio de 2016.
- ^ "Recomendaciones de prácticas seleccionadas de EE. UU. para el uso de anticonceptivos, 2016" (PDF) . Recomendaciones e informes . Vol. 65, núm. 4. Centros para el Control y la Prevención de Enfermedades. 29 de julio de 2016.
- ^ ab "Criterios médicos de elegibilidad para el uso de anticonceptivos en Estados Unidos, 2016" (PDF) . Recomendaciones e informes . Vol. 65, núm. 3. Centros para el Control y la Prevención de Enfermedades. 29 de julio de 2016.
- ^ abcdefghijklmn Aronson JK (21 de febrero de 2009). Efectos secundarios de los fármacos endocrinos y metabólicos de Meyler. Elsevier. págs. 177, 219, 223, 224, 230, 232, 239, 242. ISBN 978-0-08-093292-7.
- ^ ab Gerstman BB, Piper JM, Tomita DK, Ferguson WJ, Stadel BV, Lundin FE (enero de 1991). "Dosis de estrógeno en anticonceptivos orales y riesgo de enfermedad tromboembólica venosa profunda". American Journal of Epidemiology . 133 (1): 32–37. doi :10.1093/oxfordjournals.aje.a115799. PMID 1983896.
- ^ ab Runnebaum B, Rabe T, eds. (17 de abril de 2013). "Contrazepción". Gynäkologische Endokrinologie und Fortpflanzungsmedizin: Banda 1: Gynäkologische Endokrinologie . Springer-Verlag. págs. 411–512. ISBN 978-3-662-07635-4.
- ^ ab Gerstman BB, Gross TP, Kennedy DL, Bennett RC, Tomita DK, Stadel BV (enero de 1991). "Tendencias en el contenido y uso de anticonceptivos orales en los Estados Unidos, 1964-88". American Journal of Public Health . 81 (1): 90–96. doi :10.2105/ajph.81.1.90. PMC 1404924 . PMID 1983923.
- ^ Gallo MF, Nanda K, Grimes DA, Lopez LM, Schulz KF (agosto de 2013). "Anticonceptivos orales combinados de estrógeno de 20 μg versus >20 μg para la anticoncepción". Base de Datos Cochrane de Revisiones Sistemáticas . 2013 (8): CD003989. doi :10.1002/14651858.CD003989.pub5. PMC 7173696. PMID 23904209 .
- ^ Pincus G (22 de octubre de 2013). Hormonas y aterosclerosis: actas de la conferencia celebrada en Brighton, Utah, del 11 al 14 de marzo de 1958. Elsevier Science. pp. 411–. ISBN 978-1-4832-7064-7.
- ^ Oettel M, Schillinger E (6 de diciembre de 2012). Estrógenos y antiestrógenos II: farmacología y aplicación clínica de estrógenos y antiestrógenos. Springer Science & Business Media. pág. 390. ISBN 978-3-642-60107-1.
- ^ ab Legato MJ (29 de octubre de 2009). Principios de la medicina específica de género. Academic Press. pp. 225–234. ISBN 978-0-08-092150-1.
- ^ ab Stein PD (5 de abril de 2016). Embolia pulmonar. Wiley. págs. 187–. ISBN 978-1-119-03909-9.
- ^ abcdefghi Pfeifer S, Butts S, Dumesic D, Fossum G, Gracia C, La Barbera A, et al. (Comité de Práctica de la Sociedad Estadounidense de Medicina Reproductiva) (enero de 2017). "Anticoncepción hormonal combinada y riesgo de tromboembolia venosa: una guía". Fertilidad y esterilidad . 107 (1): 43–51. doi : 10.1016/j.fertnstert.2016.09.027 . PMID 27793376.
- ^ abc Plu-Bureau G, Maitrot-Mantelet L, Hugon-Rodin J, Canonico M (febrero de 2013). "Anticonceptivos hormonales y tromboembolia venosa: una actualización epidemiológica". Mejores prácticas e investigación. Endocrinología clínica y metabolismo . 27 (1): 25–34. doi :10.1016/j.beem.2012.11.002. PMID 23384743.
- ^ Keenan L, Kerr T, Duane M, Van Gundy K (noviembre de 2018). "Revisión sistemática de la anticoncepción hormonal y el riesgo de trombosis venosa". The Linacre Quarterly . 85 (4): 470–477. doi :10.1177/0024363918816683. PMC 6322116 . PMID 32431379.
- ^ abcde Falcone T, Hurd WW (2007). Medicina y cirugía reproductiva clínica. Elsevier Health Sciences. págs. 388–. ISBN 978-0-323-03309-1.
- ^ Christin-Maitre S (2017). "Uso de reemplazo hormonal en mujeres con trastornos endocrinos". Investigación hormonal en pediatría . 87 (4): 215–223. doi : 10.1159/000457125 . PMID: 28376481.
- ^ Becker KL (2001). Principios y práctica de endocrinología y metabolismo. Lippincott Williams & Wilkins. págs. 1024, 1027, 1035, 2153. ISBN. 978-0-7817-1750-2Los
AOC de dosis baja contienen <50 μg de estrógeno y son la principal opción para la anticoncepción oral. Los AOC que contienen ≥50 μg de estrógeno ya no deben usarse de manera rutinaria para la anticoncepción. [...] El componente de estrógeno de los AOC puede causar sensación de llenura y dolor en los senos.
- ^ Comité sobre la relación entre los anticonceptivos orales y el cáncer de mama (1 de enero de 1991). Anticonceptivos orales y cáncer de mama. Academias Nacionales. pp. 143–. ISBN 978-0-309-04493-6. NAP:13774.
Siguiendo una recomendación de su Comité Asesor de Medicamentos para la Fertilidad y la Salud Materna, la Administración de Alimentos y Medicamentos (FDA) ordenó recientemente la retirada del mercado de todos los anticonceptivos orales con contenidos de [etinilestradiol] superiores a 50 μg.
- ^ Estudio toxicológico reproductivo multigeneracional del etinilestradiol (N.° CAS 57636) en ratas Sprague-Dawley (estudios de alimentación). DIANE Publishing. págs. 27–. ISBN 978-1-4379-4231-6Las
formulaciones anticonceptivas orales que contienen más de 50 ug de etinilestradiol fueron retiradas del mercado de los Estados Unidos en 1989, y las formulaciones comercializadas actualmente generalmente contienen entre 20 y 35 μg de etinilestradiol.
- ^ Sitruk-Ware R (noviembre de 2016). "Anticoncepción hormonal y trombosis". Fertilidad y esterilidad . 106 (6): 1289–1294. doi : 10.1016/j.fertnstert.2016.08.039 . PMID 27678035.
- ^ Gallo MF, Nanda K, Grimes DA, Lopez LM, Schulz KF (agosto de 2013). "Anticonceptivos orales combinados de estrógeno de 20 μg versus >20 μg para la anticoncepción". Base de Datos Cochrane de Revisiones Sistemáticas . 2013 (8): CD003989. doi :10.1002/14651858.CD003989.pub5. PMC 7173696. PMID 23904209 .
- ^ abcd Odlind V, Milsom I, Persson I, Victor A (junio de 2002). "¿Pueden los cambios en la globulina transportadora de hormonas sexuales predecir el riesgo de tromboembolia venosa con píldoras anticonceptivas orales combinadas?". Acta Obstetricia et Gynecologica Scandinavica . 81 (6): 482–490. PMID 12047300.
- ^ Raps M, Helmerhorst F, Fleischer K, Thomassen S, Rosendaal F, Rosing J, et al. (junio de 2012). "Globulina transportadora de hormonas sexuales como marcador del riesgo trombótico de los anticonceptivos hormonales". Journal of Thrombosis and Haemostasis . 10 (6): 992–997. doi : 10.1111/j.1538-7836.2012.04720.x . PMID 22469296. S2CID 20803995.
- ^ Stanczyk FZ, Grimes DA (septiembre de 2008). "Globulina transportadora de hormonas sexuales: no es un marcador sustituto de tromboembolia venosa en mujeres que usan anticonceptivos orales". Anticoncepción . 78 (3): 201–203. doi :10.1016/j.contraception.2008.04.004. PMID 18692609.
- ^ abc Winters SJ, Huhtaniemi IT (25 de abril de 2017). Hipogonadismo masculino: principios básicos, clínicos y terapéuticos. Humana Press. pp. 307–. ISBN 978-3-319-53298-1.
- ^ Notelovitz M (marzo de 2006). "Opinión clínica: principios biológicos y farmacológicos de la terapia con estrógenos para la menopausia sintomática". MedGenMed . 8 (1): 85. PMC 1682006 . PMID 16915215.
- ^ Goodman MP (febrero de 2012). "¿Todos los estrógenos son iguales? Una revisión de la terapia oral frente a la transdérmica". Journal of Women's Health . 21 (2): 161–169. doi :10.1089/jwh.2011.2839. PMID 22011208.
- ^ ab Stege R, Carlström K, Collste L, Eriksson A, Henriksson P, Pousette A (1988). "Terapia con fosfato de poliestradiol como fármaco único en el cáncer de próstata". American Journal of Clinical Oncology . 11 (Supl 2): S101–S103. doi :10.1097/00000421-198801102-00024. PMID 3242384. S2CID 32650111.
- ^ abcde von Schoultz B, Carlström K, Collste L, Eriksson A, Henriksson P, Pousette A, et al. (1989). "Terapia con estrógenos y función hepática: efectos metabólicos de la administración oral y parenteral". La próstata . 14 (4): 389–395. doi :10.1002/pros.2990140410. PMID 2664738. S2CID 21510744.
- ^ abc Ottosson UB, Carlström K, Johansson BG, von Schoultz B (1986). "Inducción de proteínas hepáticas y colesterol de lipoproteínas de alta densidad por estrógenos: comparación entre valerato de estradiol y etinilestradiol". Investigación ginecológica y obstétrica . 22 (4): 198–205. doi :10.1159/000298914. PMID 3817605.
- ^ ab Turo R, Smolski M, Esler R, Kujawa ML, Bromage SJ, Oakley N, et al. (febrero de 2014). "Dietilestilbestrol para el tratamiento del cáncer de próstata: pasado, presente y futuro". Revista escandinava de urología . 48 (1): 4–14. doi :10.3109/21681805.2013.861508. PMID 24256023. S2CID 34563641.[ enlace muerto ]
- ^ abcdefg Phillips I, Shah SI, Duong T, Abel P, Langley RE (2014). "Terapia de privación de andrógenos y el resurgimiento del estrógeno parenteral en el cáncer de próstata". Oncology & Hematology Review . 10 (1): 42–47. doi :10.17925/ohr.2014.10.1.42. PMC 4052190 . PMID 24932461.
- ^ abc Hong WK, Holland JK (2010). Medicina del cáncer Holland-Frei 8. PMPH-USA. págs. 753–. ISBN 978-1-60795-014-1.
- ^ abc Russell N, Cheung A, Grossmann M (agosto de 2017). "Estradiol para la mitigación de los efectos adversos de la terapia de privación de andrógenos". Cáncer relacionado con el sistema endocrino . 24 (8): R297–R313. doi : 10.1530/ERC-17-0153 . PMID 28667081.
- ^ Trauner M, Jansen PJ (2004). Patogénesis molecular de la colestasis. Springer Science & Business Media. pp. 260–. ISBN 978-0-306-48240-3.
- ^ ab Clavien PA, Baillie J (15 de abril de 2008). Enfermedades de la vesícula biliar y los conductos biliares: diagnóstico y tratamiento. John Wiley & Sons. págs. 363–. ISBN 978-0-470-98697-4.
- ^ abcd Kuhl H (1999). "Anticoncepción hormonal". Estrógenos y antiestrógenos II . Manual de farmacología experimental. Vol. 135 / 2. Springer Berlin Heidelberg. págs. 363–407. doi :10.1007/978-3-642-60107-1_18. eISSN 1865-0325. ISBN 978-3-642-64261-6. ISSN 0171-2004.
- ^ O'Brien PJ, Bruce WR (2010). Toxinas endógenas: dieta, genética, enfermedad y tratamiento. John Wiley & Sons. pp. 302–. ISBN 978-3-527-32363-0.
- ^ abcdef Kuhl H (diciembre de 1990). "[Inhibidores de la ovulación: la importancia de la dosis de estrógeno]" [Inhibidores de la ovulación: la importancia de la dosis de estrógeno]. Geburtshilfe und Frauenheilkunde (en alemán). 50 (12): 910–922. doi :10.1055/s-2008-1026392. PMID 2086334. S2CID 73398961.
- ^ Shreenath AP, Kahloon A (enero de 2022). "Adenoma hepatocelular". Adenoma hepático. EstadísticasPerlas. PMID 30020636.
- ^ ab Giannitrapani L, Soresi M, La Spada E, Cervello M, D'Alessandro N, Montalto G (noviembre de 2006). "Hormonas sexuales y riesgo de tumor hepático". Anales de la Academia de Ciencias de Nueva York . 1089 (1): 228–236. Bibcode :2006NYASA1089..228G. doi :10.1196/annals.1386.044. PMID 17261770. S2CID 7932937.
- ^ Ponnatapura J, Kielar A, Burke LM, Lockhart ME, Abualruz AR, Tappouni R, et al. (julio de 2019). "Complicaciones hepáticas de las píldoras anticonceptivas orales y el estrógeno en la resonancia magnética: controversias y actualización: adenoma y más allá". Imágenes por resonancia magnética . 60 : 110–121. doi :10.1016/j.mri.2019.04.010. PMID 31009688. S2CID 128359413.
- ^ Perarnau JM, Bacq Y (agosto de 2008). "Afectación vascular hepática relacionada con el embarazo, los anticonceptivos orales y la terapia de reemplazo de estrógenos". Seminarios sobre enfermedades hepáticas . 28 (3): 315–327. doi :10.1055/s-0028-1085099. PMID 18814084. S2CID 260318275.
- ^ abc Blaustein A (11 de noviembre de 2013). Patología del tracto genital femenino. Springer Science & Business Media. pp. 291–. ISBN 978-1-4757-1767-9.
- ^ Surwit EA, Alberts D (6 de diciembre de 2012). Cáncer de endometrio. Springer Science & Business Media. pp. 11–. ISBN 978-1-4613-0867-6.
- ^ abc Kidd KA, Blanchfield PJ, Mills KH, Palace VP, Evans RE, Lazorchak JM, et al. (mayo de 2007). "Colapso de una población de peces tras la exposición a un estrógeno sintético". Actas de la Academia Nacional de Ciencias de los Estados Unidos de América . 104 (21): 8897–8901. Bibcode :2007PNAS..104.8897K. doi : 10.1073/pnas.0609568104 . PMC 1874224 . PMID 17517636.
- ^ abc Park BJ, Kidd K (agosto de 2005). "Efectos del estrógeno sintético etinilestradiol en las primeras etapas de la vida de las ranas visón y las ranas verdes en la naturaleza y en el medio natural". Toxicología y química ambiental . 24 (8): 2027–2036. doi :10.1897/04-227R.1. PMID 16152976. S2CID 32669410.
- ^ Wang B, Sanchez RI, Franklin RB, Evans DC, Huskey SE (noviembre de 2004). "La participación de CYP3A4 y CYP2C9 en el metabolismo del 17 alfa-etinilestradiol". Metabolismo y disposición de fármacos . 32 (11): 1209–1212. doi :10.1124/dmd.104.000182. PMID 15304426. S2CID 86245855.
- ^ abcdefghi Zhang H, Cui D, Wang B, Han YH, Balimane P, Yang Z, et al. (2007). "Interacciones farmacocinéticas de fármacos que involucran 17alfa-etinilestradiol: una nueva mirada a un fármaco antiguo". Farmacocinética clínica . 46 (2): 133–157. doi :10.2165/00003088-200746020-00003. PMID 17253885. S2CID 71784426.
- ^ Escande A, Pillon A, Servant N, Cravedi JP, Larrea F, Muhn P, et al. (mayo de 2006). "Evaluación de la selectividad de ligandos utilizando líneas celulares reporteras que expresan de manera estable el receptor de estrógeno alfa o beta". Farmacología bioquímica . 71 (10): 1459–1469. doi :10.1016/j.bcp.2006.02.002. PMID 16554039.
- ^ Jeyakumar M, Carlson KE, Gunther JR, Katzenellenbogen JA (abril de 2011). "Exploración de las dimensiones de la potencia del estrógeno: análisis de las afinidades de unión del ligando y del coactivador". The Journal of Biological Chemistry . 286 (15): 12971–12982. doi : 10.1074/jbc.M110.205112 . PMC 3075970 . PMID 21321128.
- ^ Prossnitz ER, Arterburn JB (julio de 2015). "Unión Internacional de Farmacología Básica y Clínica. XCVII. Receptor de estrógeno acoplado a proteína G y sus moduladores farmacológicos". Pharmacological Reviews . 67 (3): 505–540. doi :10.1124/pr.114.009712. PMC 4485017 . PMID 26023144.
- ^ Yates MA, Li Y, Chlebeck PJ, Offner H (abril de 2010). "El GPR30, pero no el receptor de estrógeno alfa, es crucial en el tratamiento de la encefalomielitis autoinmune experimental con etinilestradiol oral". BMC Immunology . 11 : 20. doi : 10.1186/1471-2172-11-20 . PMC 2864220 . PMID 20403194.
- ^ Prossnitz ER, Barton M (agosto de 2011). "El receptor de estrógeno acoplado a proteína G GPER en la salud y la enfermedad". Nature Reviews. Endocrinology . 7 (12): 715–726. doi :10.1038/nrendo.2011.122. PMC 3474542 . PMID 21844907.
Investigaciones posteriores demostraron que el efecto terapéutico del etinilestradiol en la EAE establecida estaba mediado por GPER, pero no por ERα, y posiblemente implicaba la producción de la citocina antiinflamatoria Il‑10.115
- ^ Prossnitz ER, Barton M (mayo de 2014). "Biología del estrógeno: nuevos conocimientos sobre la función de GPER y oportunidades clínicas". Endocrinología molecular y celular . 389 (1–2): 71–83. doi :10.1016/j.mce.2014.02.002. PMC 4040308. PMID 24530924. Además
, se demostró que el efecto terapéutico del etinilestradiol en la enfermedad establecida requiere la expresión de GPER pero no de ERα, y se asoció con la producción de la citocina antiinflamatoria IL-10 (Yates et al., 2010).
- ^ Quaynor SD, Stradtman EW, Kim HG, Shen Y, Chorich LP, Schreihofer DA, et al. (julio de 2013). "Pubertad tardía y resistencia al estrógeno en una mujer con la variante α del receptor de estrógeno". The New England Journal of Medicine . 369 (2): 164–171. doi :10.1056/NEJMoa1303611. PMC 3823379 . PMID 23841731.
- ^ Craig CR, Stitzel RE (2004). Farmacología moderna con aplicaciones clínicas. Lippincott Williams & Wilkins. pp. 708–. ISBN 978-0-7817-3762-3.
- ^ Allahbadia G, Agrawal R (2007). Síndrome de ovario poliquístico. Anshan. pp. 257–. ISBN 978-1-904798-74-3.
- ^ ab Gomel V, Munro MG, Rowe TC (1990). Ginecología: un enfoque práctico. Williams & Wilkins. pág. 132,134. ISBN 978-0-683-03631-2
El estrógeno sintético, etinilestradiol, más comúnmente utilizado en los anticonceptivos orales, tiene una actividad biológica 100 veces mayor que la de las sustancias nativas y conjugadas
. - ^ ab Shoupe D (7 de noviembre de 2007). Manual de anticoncepción: una guía para el manejo práctico. Springer Science & Business Media. pp. 23–. ISBN 978-1-59745-150-5.
EE2 tiene aproximadamente 100 veces la potencia de un peso equivalente de estrógeno equino conjugado o sulfato de estrona para estimular la síntesis de proteínas hepáticas. [...] EE2 es aproximadamente 1,7 veces más potente que el mismo peso de mestranol.
- ^ McConaghy N (21 de noviembre de 2013). Conducta sexual: problemas y gestión. Springer Science & Business Media. pp. 177–. ISBN 978-1-4899-1133-9Meyer et al. descubrieron que el etinilestradiol era de 75 a 100 veces más potente que el estrógeno conjugado sobre la base de las dosis necesarias para
reducir la testosterona al rango femenino adulto, siendo necesarios 0,1 mg del primero y de 7,5 a 10 mg del segundo.
- ^ Chabner B, Longo DL (1996). Quimioterapia y bioterapia contra el cáncer: principios y práctica. Lippincott-Raven Publishers. pág. 186. ISBN 978-0-397-51418-2.
La potencia relativa de varios estrógenos se ha ensayado mediante la determinación de los efectos sobre la FSH plasmática, una medida del efecto sistémico, y por aumentos en SHBG, CBG y angiotensinógeno, todos los cuales indican el efecto hepático. El sulfato de estrona de piperazina y el estradiol micronizado fueron equipotentes con respecto a los aumentos en SHBG, mientras que los estrógenos conjugados fueron 3,2 veces más potentes, el DES fue 28,4 veces más potente y el etinilestradiol fue 600 veces más potente. Con respecto a la disminución de FSH, los estrógenos conjugados fueron 1,4 veces, el DES fue 3,8 veces y el etinilestradiol fue de 80 a 200 veces más potente que el sulfato de estrona de piperazina.
- ^ ab Mashchak CA, Lobo RA, Dozono-Takano R, Eggena P, Nakamura RM, Brenner PF, et al. (noviembre de 1982). "Comparación de las propiedades farmacodinámicas de varias formulaciones de estrógeno". Revista estadounidense de obstetricia y ginecología . 144 (5): 511–518. doi :10.1016/0002-9378(82)90218-6. PMID 6291391.
- ^ Lauritzen C (septiembre de 1990). "Uso clínico de estrógenos y progestágenos". Maturitas . 12 (3): 199–214. doi :10.1016/0378-5122(90)90004-P. PMID 2215269.
- ^ Lauritzen C (junio de 1977). "[Terapia de estrógenos en la práctica. 3. Preparaciones de estrógenos y preparaciones combinadas]" [Terapia de estrógenos en la práctica. 3. Preparaciones de estrógenos y preparaciones combinadas]. Fortschritte Der Medizin (en alemán). 95 (21): 1388–92. PMID 559617.
- ^ Wolf AS, Schneider HP (12 de marzo de 2013). Ostrogeno en Diagnostik und Therapie. Springer-Verlag. págs. 78–. ISBN 978-3-642-75101-1.
- ^ Göretzlehner G, Lauritzen C, Römer T, Rossmanith W (1 de enero de 2012). Praktische Hormontherapie in der Gynäkologie. Walter de Gruyter. págs.44–. ISBN 978-3-11-024568-4.
- ^ Knörr K, Beller FK, Lauritzen C (17 de abril de 2013). Lehrbuch der Gynäkologie. Springer-Verlag. págs. 212-213. ISBN 978-3-662-00942-0.
- ^ Horský J, Presl J (1981). "Tratamiento hormonal de los trastornos del ciclo menstrual". En Horsky J, Presl J (eds.). Función ovárica y sus trastornos: diagnóstico y terapia . Springer Science & Business Media. págs. 309–332. doi :10.1007/978-94-009-8195-9_11. ISBN 978-94-009-8195-9.
- ^ Pschyrembel W (1968). Praktische Gynäkologie: für Studierende und Ärzte. Walter de Gruyter. págs. 598–599. ISBN 978-3-11-150424-7.
- ^ Lauritzen CH (enero de 1976). "El síndrome climatérico femenino: significado, problemas, tratamiento". Acta Obstetricia Et Gynecologica Scandinavica. Suplemento . 51 : 47–61. doi :10.3109/00016347509156433. PMID 779393.
- ^ Lauritzen C (1975). "El síndrome climatérico femenino: significado, problemas, tratamiento". Acta Obstetricia et Gynecologica Scandinavica . 54 (s51): 48–61. doi :10.3109/00016347509156433. ISSN 0001-6349.
- ^ Kópera H (1991). "Hormona der Gonaden". Terapia hormonal para la mujer . Kliniktaschenbucher. págs. 59-124. doi :10.1007/978-3-642-95670-6_6. ISBN 978-3-540-54554-5. ISSN 0172-777X.
- ^ Scott WW, Menon M, Walsh PC (abril de 1980). "Terapia hormonal del cáncer de próstata". Cancer . 45 (Supl. 7): 1929–1936. doi :10.1002/cncr.1980.45.s7.1929. PMID 29603164.
- ^ Leinung MC, Feustel PJ, Joseph J (2018). "Tratamiento hormonal de mujeres transgénero con estradiol oral". Salud transgénero . 3 (1): 74–81. doi :10.1089/trgh.2017.0035. PMC 5944393 . PMID 29756046.
- ^ Ryden AB (1950). "Sustancias estrogénicas naturales y sintéticas; su eficacia relativa cuando se administran por vía oral". Acta Endocrinologica . 4 (2): 121–39. doi :10.1530/acta.0.0040121. PMID 15432047.
- ^ Ryden AB (1951). "La eficacia de las sustancias estrogénicas naturales y sintéticas en las mujeres". Acta Endocrinologica . 8 (2): 175–91. doi :10.1530/acta.0.0080175. PMID 14902290.
- ^ Kottmeier HL (1947). "Ueber blutungen in der menopause: Speziell der klinischen bedeutung eines endometriums mit zeichen hormonaler beeinflussung: Part I". Acta Obstetricia et Gynecologica Scandinavica . 27 (s6): 1–121. doi :10.3109/00016344709154486. ISSN 0001-6349.
No hay duda de que la conversión del endometrio con inyecciones de preparaciones de hormonas estrogénicas tanto sintéticas como nativas tiene éxito, pero la opinión sobre si las preparaciones nativas administradas por vía oral pueden producir una proliferación de la mucosa varía según los autores. PEDERSEN-BJERGAARD (1939) pudo demostrar que el 90% de la foliculina captada en la sangre de la vena portae se inactiva en el hígado. Ni KAUFMANN (1933, 1935), ni RAUSCHER (1939, 1942) ni HERRNBERGER (1941) lograron que un endometrio de castración proliferara utilizando grandes dosis de preparaciones de estrona o estradiol administradas por vía oral. NEUSTAEDTER (1939), LAUTERWEIN (1940) y FERIN (1941) informaron sobre otros resultados; lograron convertir un endometrio de castración atrófico en una mucosa proliferante inequívoca con 120-300 de estradiol o con 380 de estrona.
- ^ Rietbrock N, Staib AH, Loew D (11 de marzo de 2013). Farmacología clínica: Arzneitherapie. Springer-Verlag. págs. 426–. ISBN 978-3-642-57636-2.
- ^ Martinez-Manautou J, Rudel HW (1966). "Actividad antiovulatoria de varios estrógenos sintéticos y naturales". En Robert Benjamin Greenblatt (ed.). Ovulación: estimulación, supresión y detección. Lippincott. págs. 243–253.
- ^ Herr F, Revesz C, Manson AJ, Jewell JB (1970). "Propiedades biológicas de los sulfatos de estrógeno". Aspectos químicos y biológicos de la conjugación de esteroides . págs. 368–408. doi :10.1007/978-3-642-49793-3_8. ISBN . 978-3-642-49506-9.
- ^ Duncan CJ, Kistner RW, Mansell H (octubre de 1956). "Supresión de la ovulación mediante tripanisilcloroetileno (TACE)". Obstetricia y ginecología . 8 (4): 399–407. PMID 13370006.
- ^ abc Shearer RJ, Hendry WF, Sommerville IF, Fergusson JD (diciembre de 1973). "Testosterona plasmática: un monitor preciso del tratamiento hormonal en el cáncer de próstata". British Journal of Urology . 45 (6): 668–677. doi :10.1111/j.1464-410x.1973.tb12238.x. PMID 4359746.
- ^ abc Ekback MP (2017). "Hirsutismo, ¿qué hacer?" (PDF) . Revista Internacional de Endocrinología y Trastornos Metabólicos . 3 (3). doi : 10.16966/2380-548X.140 . ISSN 2380-548X.
- ^ abc Nieschlag E, Behre HM, Nieschlag S (26 de julio de 2012). Testosterona: acción, deficiencia, sustitución. Cambridge University Press. pp. 62–. ISBN 978-1-107-01290-5.
- ^ Coss CC, Jones A, Parke DN, Narayanan R, Barrett CM, Kearbey JD, et al. (marzo de 2012). "Caracterización preclínica de un nuevo agonista selectivo de ERα de difenil benzamida para la terapia hormonal en el cáncer de próstata". Endocrinología . 153 (3): 1070–1081. doi : 10.1210/en.2011-1608 . PMID 22294742.
- ^ Rich P (enero de 2008). "Anticonceptivos hormonales para el tratamiento del acné". Cutis . 81 (1 Suppl): 13–18. PMID 18338653.
- ^ Zimmerman Y, Eijkemans MJ, Coelingh Bennink HJ, Blankenstein MA, Fauser BC (2014). "El efecto de la anticoncepción oral combinada en los niveles de testosterona en mujeres sanas: una revisión sistemática y un metanálisis". Hum Reprod Update . 20 (1): 76–105. doi :10.1093/humupd/dmt038. PMC 3845679 . PMID 24082040.
- ^ Özcan Ö, den Elzen WP, Hillebrand JJ, den Heijer M, van Loendersloot LL, Fischer J, et al. (enero de 2024). "El efecto de la terapia anticonceptiva hormonal en los parámetros de laboratorio clínico: una revisión de la literatura". Clin Chem Lab Med . 62 (1): 18–40. doi : 10.1515/cclm-2023-0384 . PMID 37419659. S2CID 259361637.
- ^ Yang LP, Plosker GL (octubre de 2012). "Acetato de nomegestrol/estradiol: en anticoncepción oral". Drugs . 72 (14): 1917–1928. doi :10.2165/11208180-000000000-00000. PMID 22950535. S2CID 44335732.
- ^ ab Jacobi GH, Altwein JE, Kurth KH, Basting R, Hohenfellner R (junio de 1980). "Tratamiento del cáncer de próstata avanzado con acetato de ciproterona parenteral: un ensayo aleatorizado de fase III". British Journal of Urology . 52 (3): 208–215. doi :10.1111/j.1464-410x.1980.tb02961.x. PMID 7000222.
- ^ ab Gunnarsson PO, Norlén BJ (1988). "Farmacología clínica del fosfato de poliestradiol". La próstata . 13 (4): 299–304. doi :10.1002/pros.2990130405. PMID 3217277. S2CID 33063805.
- ^ Stahl F, Schnorr D, Bär CM, Fröhlich G, Dörner G (1989). "Supresión de los niveles plasmáticos de andrógenos con una terapia combinada de estrógeno de depósito (Turisteron) y dexametasona en pacientes con cáncer de próstata". Endocrinología experimental y clínica . 94 (3): 239–243. doi :10.1055/s-0029-1210905. PMID 2630306. S2CID 40497389.
- ^ abc Jameson JL, De Groot LJ (18 de mayo de 2010). Endocrinología - Libro electrónico: adultos y niños. Elsevier Health Sciences. pp. 2282–. ISBN 978-1-4557-1126-0.
- ^ Denis LJ, Griffiths K, Kaisary AV, Murphy GP (1 de marzo de 1999). Libro de texto sobre el cáncer de próstata: patología, diagnóstico y tratamiento: Patología, diagnóstico y tratamiento. CRC Press. págs. 297–. ISBN 978-1-85317-422-3.
- ^ Scott WW, Menon M, Walsh PC (abril de 1980). "Terapia hormonal del cáncer de próstata". Cancer . 45 (Supl 7): 1929–1936. doi : 10.1002/cncr.1980.45.s7.1929 . PMID 29603164. S2CID 4492779.
- ^ Bingel AS, Benoit PS (febrero de 1973). "Anticonceptivos orales: terapéutica frente a reacciones adversas, con una perspectiva para el futuro I". Revista de Ciencias Farmacéuticas . 62 (2): 179–200. doi :10.1002/jps.2600620202. PMID 4568621.
- ^ Rietbrock N, Staib AH, Loew D (11 de marzo de 2013). Farmacología clínica: Arzneitherapie. Springer-Verlag. págs. 426–. ISBN 978-3-642-57636-2.
- ^ Elger W (1972). "Fisiología y farmacología de la reproducción femenina bajo el aspecto del control de la fertilidad". Reseñas de fisiología, bioquímica y farmacología experimental, volumen 67. Ergebnisse der Physiologie Reseñas de fisiología. Vol. 67. págs. 69–168. doi :10.1007/BFb0036328. ISBN 3-540-05959-8. Número de identificación personal 4574573.
- ^ Bastianelli C, Farris M, Rosato E, Brosens I, Benagiano G (noviembre de 2018). "Farmacodinámica de los anticonceptivos orales combinados de estrógeno y progestina 3. Inhibición de la ovulación". Revisión experta de farmacología clínica . 11 (11): 1085–1098. doi :10.1080/17512433.2018.1536544. PMID 30325245. S2CID 53246678.
- ^ Martinez-Manautou J, Rudel HW (1966). "Actividad antiovulatoria de varios estrógenos sintéticos y naturales". En Greenblatt RB (ed.). Ovulación: estimulación, supresión y detección. Lippincott. págs. 243–253. ISBN 978-0-397-59010-0.
- ^ Herr F, Revesz C, Manson AJ, Jewell JB (1970). "Biological Properties of Estrogen Sulfates". Aspectos químicos y biológicos de la conjugación de esteroides . págs. 368–408. doi :10.1007/978-3-642-49793-3_8 (inactivo el 1 de julio de 2024). ISBN 978-3-642-49506-9.
{{cite book}}: CS1 maint: DOI inactivo a partir de julio de 2024 ( enlace ) - ^ Goldzieher JW, Pena A, Chenault CB, Woutersz TB (julio de 1975). "Estudios comparativos de los estrógenos etinílicos utilizados en anticonceptivos orales. II. Potencia antiovulatoria". American Journal of Obstetrics and Gynecology . 122 (5): 619–624. doi :10.1016/0002-9378(75)90061-7. PMID 1146927.
- ^ abc Margioris AN, Chrousos GP (20 de abril de 2001). Trastornos suprarrenales. Springer Science & Business Media. pp. 84–. ISBN 978-1-59259-101-5.
- ^ abc Polderman KH, Gooren LJ, van der Veen EA (octubre de 1995). "Efectos de los andrógenos gonadales y los estrógenos en los niveles de andrógenos suprarrenales". Endocrinología clínica . 43 (4): 415–421. doi :10.1111/j.1365-2265.1995.tb02611.x. PMID 7586614. S2CID 6815423.
- ^ Trémollieres F (febrero de 2012). "[Anticoncepción combinada oral: ¿existe alguna diferencia entre el etinilestradiol y el estradiol?]" [Anticoncepción combinada oral: ¿existe alguna diferencia entre el etinilestradiol y el estradiol?]. Gynécologie, Obstétrique & Fertilité (en francés). 40 (2): 109–115. doi :10.1016/j.gyobfe.2011.10.009. PMID 22244780.
- ^ abc Lobo RA (5 de junio de 2007). Tratamiento de la mujer posmenopáusica: aspectos básicos y clínicos. Academic Press. pp. 177, 770–771. ISBN 978-0-08-055309-2.
- ^ Shope D (10 de febrero de 2011). Anticoncepción. John Wiley e hijos. págs.79–. ISBN 978-1-4443-4263-5.
- ^ Sitruk-Ware R, Nath A (junio de 2011). "Efectos metabólicos de los esteroides anticonceptivos". Reseñas en Endocrine & Metabolic Disorders . 12 (2): 63–75. doi :10.1007/s11154-011-9182-4. PMID 21538049. S2CID 23760705.
- ^ abc Boyd RA, Zegarac EA, Eldon MA (enero de 2003). "El efecto de los alimentos en la biodisponibilidad de noretindrona y etinilestradiol de los comprimidos de acetato de noretindrona/etinilestradiol destinados a la terapia de reemplazo hormonal continua". Journal of Clinical Pharmacology . 43 (1): 52–58. doi :10.1177/0091270002239706. PMID 12520628. S2CID 27729272.
- ^ ab Dodick D, Silberstein SD (2016). Migraña. Prensa de la Universidad de Oxford. págs. 272–. ISBN 978-0-19-979361-7.
- ^ abc Orme ML, Back DJ, Breckenridge AM (1983). "Farmacocinética clínica de los esteroides anticonceptivos orales". Farmacocinética clínica . 8 (2): 95–136. doi :10.2165/00003088-198308020-00001. PMID 6342899. S2CID 43298472.
- ^ ab Notelovitz M, van Keep PA (6 de diciembre de 2012). El climaterio en perspectiva: actas del Cuarto Congreso Internacional sobre la Menopausia, celebrado en Lake Buena Vista, Florida, del 28 de octubre al 2 de noviembre de 1984. Springer Science & Business Media. pp. 395–. ISBN 978-94-009-4145-8.
- ^ Pugeat MM, Dunn JF, Nisula BC (julio de 1981). "Transporte de hormonas esteroides: interacción de 70 fármacos con globulina transportadora de testosterona y globulina transportadora de corticosteroides en plasma humano". Revista de endocrinología clínica y metabolismo . 53 (1): 69–75. doi :10.1210/jcem-53-1-69. PMID 7195405.
- ^ Backeljauw P, Klein K (marzo de 2019). "Terapia de reemplazo de hormonas sexuales para personas con síndrome de Turner". American Journal of Medical Genetics. Parte C, Seminarios en genética médica . 181 (1): 13–17. doi :10.1002/ajmg.c.31685. PMID 30809949. S2CID 73487051.
- ^ abcd Mattison DR, Karyakina N, Goodman M, LaKind JS (septiembre de 2014). "Farmacocinética y toxicocinética de estrógenos exógenos y endógenos seleccionados: una revisión de los datos e identificación de lagunas de conocimiento". Critical Reviews in Toxicology . 44 (8): 696–724. doi :10.3109/10408444.2014.930813. PMID 25099693. S2CID 11212469.
- ^ abcdefghijk Index Nominum 2000: Directorio internacional de medicamentos. Taylor y Francisco. Enero de 2000. pág. 412.ISBN 978-3-88763-075-1.
- ^ Inhoffen HH, Hohlweg W (1938). "Neue per os-wirksame weibliche Keimdrüsenhormon-Derivate: 17-Aethinyl-oestradiol und Pregnen-in-on-3-ol-17 (Nuevos derivados glandulares femeninos activos por vía oral: 17α-etinilestradiol y pregnen-in-on-3 -ol-17)". Naturwissenschaften . 26 (6): 96. Código bibliográfico : 1938NW.....26...96I. doi :10.1007/BF01681040. S2CID 46648877.
- ^ Maisel AQ (1965). La búsqueda de hormonas . Nueva York: Random House. OCLC 543168.
- ^ Petrow V (diciembre de 1970). "Los progestágenos anticonceptivos". Chemical Reviews . 70 (6): 713–726. doi :10.1021/cr60268a004. PMID 4098492.
- ^ Sneader W (2005). "Análogos hormonales". Descubrimiento de fármacos: una historia . Hoboken, NJ: John Wiley & Sons. págs. 188–225. ISBN 978-0-471-89980-8.
- ^ Djerassi C (enero de 2006). "Nacimiento químico de la píldora. 1992". Revista estadounidense de obstetricia y ginecología . 194 (1): 290–298. doi :10.1016/j.ajog.2005.06.010. PMID 16389046.
- ^ Administración de Alimentos y Medicamentos de Estados Unidos (FDA) (5 de mayo de 2004). "Schering Corp. et al.; Retirada de la aprobación de 92 solicitudes de nuevos fármacos y 49 solicitudes abreviadas de nuevos fármacos. Aviso" (PDF) . Registro Federal . 69 (87): 25124–30.
- ^ Cantor EB (septiembre de 1956). "Un estudio de los estrógenos". Medicina de posgrado . 20 (3): 224–231. doi :10.1080/00325481.1956.11691266. PMID 13359169.
- ^ Beller FK, Knörr K, Lauritzen C, Wynn RM (1974). "Planificación familiar". Ginecología . págs. 189-213. doi :10.1007/978-1-4615-7128-5_17. ISBN 978-0-387-90087-2.
- ^ Haller J (1968). "La terapia anticoncepción". Die Gestagene . págs. 1125-1178. doi :10.1007/978-3-642-99941-3_8. ISBN 978-3-642-99942-0.
- ^ abcdefg "Etinilestradiol - Drugs.com".
- ^ Morton IK, Hall JM (6 de diciembre de 2012). Diccionario conciso de agentes farmacológicos: propiedades y sinónimos. Springer Science & Business Media. pp. 115–. ISBN 978-94-011-4439-1.
- ^ Asociación Médica Estadounidense. Departamento de Medicamentos, Consejo de Medicamentos (Asociación Médica Estadounidense), Sociedad Estadounidense de Farmacología Clínica y Terapéutica (1 de febrero de 1977). "Estrógenos, progestágenos, anticonceptivos orales y agentes ovulatorios". Evaluaciones de medicamentos de la AMA. Publishing Sciences Group. págs. 540–572. ISBN 978-0-88416-175-2.
Etinilestradiol [Estinyl, Feminone, Lynoral, Novestrol, Palonyl]
- ^ Sociedad Estadounidense de Farmacéuticos Hospitalarios. Comité de Farmacia y Productos Farmacéuticos (1983). Servicio de Formularios de Medicamentos Hospitalarios Estadounidenses: Una colección de dos volúmenes de monografías de medicamentos y otra información. Sociedad Estadounidense de Farmacéuticos Hospitalarios. ISBN 978-0-930530-02-0ETINIL
ESTRADIOL USP (Esteed®, Estinyl®, Lynoral®, Menolyn®, Novestrol®, Palonyl®, Spanestrin®, Ylestrol®)
Lectura adicional
- Oettel M, Schillinger E (6 de diciembre de 2012). Estrógenos y antiestrógenos II: farmacología y aplicación clínica de estrógenos y antiestrógenos. Springer Science & Business Media. págs. 4, 10, 15, 165, 247–248, 276–291, 363–408, 424, 514, 540, 543, 581. ISBN 978-3-642-60107-1.
- Kuhl H (agosto de 2005). "Farmacología de los estrógenos y progestágenos: influencia de diferentes vías de administración". Climaterio . 8 (Supl 1): 3–63. doi :10.1080/13697130500148875. PMID 16112947. S2CID 24616324.
- Stanczyk FZ, Archer DF, Bhavnani BR (junio de 2013). "Etinilestradiol y 17β-estradiol en anticonceptivos orales combinados: farmacocinética, farmacodinamia y evaluación de riesgos". Anticoncepción . 87 (6): 706–727. doi :10.1016/j.contraception.2012.12.011. PMID 23375353.
- Mattison DR, Karyakina N, Goodman M, LaKind JS (septiembre de 2014). "Farmacocinética y toxicocinética de estrógenos exógenos y endógenos seleccionados: una revisión de los datos e identificación de lagunas de conocimiento". Critical Reviews in Toxicology . 44 (8): 696–724. doi :10.3109/10408444.2014.930813. PMID 25099693. S2CID 11212469.

