Malformación de Dandy-Walker
| Malformación de Dandy-Walker | |
|---|---|
| Otros nombres | Síndrome de Dandy-Walker (DWS), [1] Complejo de Dandy-Walker (DWC), [2] Continuo de Dandy-Walker [3] |
 | |
| Resonancia magnética sagital ponderada en T2 de la variante de Dandy-Walker (DWV) con displasia de la protuberancia y el vermis cerebeloso en un niño de 8 años | |
| Especialidad | Genética médica |
| Síntomas | Hidrocefalia: aumento del tamaño de la cabeza, vómitos, somnolencia excesiva, irritabilidad, parálisis de la mirada vertical , convulsiones [4] Condiciones genéticas asociadas: defectos cardíacos congénitos , anomalías oculares, discapacidad intelectual, agenesia del cuerpo calloso , anomalías esqueléticas, etc. [5] |
| Complicaciones | Fallo de la derivación (desplazamiento, drenaje excesivo), hematoma subdural , infección [6] |
| Tipos | Variante Dandy-Walker (DWV), [7] [6] mega cisterna magna (?) [6] [8] |
| Causas | Afecciones genéticas ciliopáticas o cromosómicas , a menudo no identificadas [5] |
| Método de diagnóstico | Resonancia magnética , ecografía prenatal o TC [6] |
| Diagnóstico diferencial | Quiste de la bolsa de Blake (BPC), [3] [8] megacisterna magna (?), [6] [8] quiste aracnoideo de la fosa posterior [6] [9] |
| Tratamiento | Derivación cistoperitoneal , derivación ventriculoperitoneal, ventriculostomía endoscópica del tercer ventrículo (VTE) [6] [10] |
| Pronóstico | 15% de riesgo de muerte, principalmente por hidrocefalia o su tratamiento [6] |
| Frecuencia | 1 en 25.000 a 1 en 50.000 [5] [11] |
La malformación de Dandy-Walker ( DWM ), también conocida como síndrome de Dandy-Walker ( DWS ), es una malformación cerebral congénita rara en la que la parte que une los dos hemisferios del cerebelo (el vermis cerebeloso ) no se forma completamente, y el cuarto ventrículo y el espacio detrás del cerebelo (la fosa posterior ) se agrandan con líquido cefalorraquídeo . La mayoría de los afectados desarrollan hidrocefalia durante el primer año de vida, [6] que puede presentarse como aumento del tamaño de la cabeza, vómitos, somnolencia excesiva, irritabilidad, desviación hacia abajo de los ojos y convulsiones . [4] Otros síntomas menos comunes generalmente se asocian con afecciones genéticas comórbidas y pueden incluir defectos cardíacos congénitos , anomalías oculares, discapacidad intelectual, tumores congénitos, otros defectos cerebrales como agenesia del cuerpo calloso , anomalías esqueléticas, encefalocele occipital o genitales o riñones subdesarrollados. [5] A veces se descubre en adolescentes o adultos debido a problemas de salud mental. [5] [6]
La hidrocefalia difusa suele estar causada por una afección genética ciliopática o cromosómica , aunque la afección causal solo se identifica en aproximadamente la mitad de los diagnosticados antes del nacimiento [6] y en un tercio de los diagnosticados después del nacimiento. [5] El mecanismo implica una migración y división celular alterada que afecta el largo período de desarrollo del vermis cerebeloso. [6] El mecanismo por el cual se produce la hidrocefalia en la hidrocefalia difusa aún no se comprende por completo. [6] La afección se diagnostica mediante resonancia magnética o, con menos frecuencia, ecografía prenatal . [6] Hay otras malformaciones que pueden parecerse mucho a la hidrocefalia difusa, y existe desacuerdo en torno a los criterios y clasificaciones utilizados para la malformación. [5] [6] [12]
El tratamiento para la mayoría de los pacientes consiste en la implantación de una derivación cerebral en la infancia. Esta suele insertarse en la fosa posterior, pero puede utilizarse una derivación en los ventrículos laterales en su lugar o en combinación. La ventriculostomía endoscópica del tercer ventriculostomía (VTE) es una opción menos invasiva para los pacientes mayores de 1 año. Las derivaciones de la fosa posterior son las más eficaces (80% de las veces), pero conllevan el mayor riesgo de complicaciones, mientras que la VTE es la menos eficaz, pero tiene el menor riesgo de complicaciones. [6] La tasa de mortalidad es de aproximadamente el 15%, principalmente debido a complicaciones de la hidrocefalia o su tratamiento, que pueden incluir hematomas subdurales o infección. [6] El pronóstico después de un tratamiento exitoso de la hidrocefalia suele ser bueno, pero depende de cualquier afección asociada y sus síntomas. [5] [6] Aquellas personas sin hidrocefalia son tratadas en función de cualquier síntoma o afección asociada. [13]
La prevalencia de DWM se estima entre 1 en 25.000 a 1 en 50.000. [5] [11] DWM es la causa de alrededor del 4,3% de los casos de hidrocefalia congénita [14] y el 2,5% de todos los casos de hidrocefalia. [6] Al menos el 21% de los que tienen DWM tienen un hermano con la malformación, y al menos el 16% tienen un padre con la malformación. [5] La malformación fue descrita por primera vez por el cirujano inglés John Bland-Sutton en 1887, [6] [15] aunque fue nombrada por el psiquiatra alemán Clemens Ernst Benda en 1954 [1] [6] en honor a los neurocirujanos estadounidenses Walter Dandy y Arthur Earl Walker , quienes la describieron en 1914 y 1942, respectivamente. [6] [16] [17]
Signos y síntomas
Hidrocefalia
Los síntomas más frecuentes y prominentes de la DWM son aquellos asociados con la hidrocefalia en el período posnatal. La hidrocefalia ocurre en un 80% estimado de los pacientes con DWM clásica. Esto suele presentarse dentro del primer año de vida (85% de las veces), con mayor frecuencia dentro de los primeros tres meses. [6] Los signos de hidrocefalia en los bebés incluyen aumento del tamaño de la cabeza, vómitos, somnolencia excesiva, irritabilidad, desviación de los ojos hacia abajo (conocida como " ojos de puesta de sol ") y convulsiones . [4] A diferencia de la DWM clásica, solo alrededor del 30% de aquellos con la variante de Dandy-Walker (DWV), en la que la fosa posterior no está agrandada, tienen hidrocefalia. [6]
Neurológico
A pesar del vermis cerebeloso hipoplásico, poco más de la mitad de los individuos con DWM (entre el 27% y el 84%) no parecen tener discapacidad intelectual significativa o retraso del desarrollo. [5] [18] Sin embargo, muchas de las condiciones genéticas asociadas con DWM pueden presentarse con retraso del desarrollo y otras anomalías cerebrales. [5] [6] Se ha encontrado agenesia del cuerpo calloso en entre el 5% y el 17% de aquellos con DWM. [10] [19] Sin embargo, esto no parece resultar en discapacidad intelectual por sí solo. [18] Otras anomalías cerebrales que se sabe que a veces se asocian con DWM incluyen heterotopia de materia gris , paquigiria (menos crestas en el cerebro), lisencefalia (crestas menos profundas), polimicrogiria , holoprosencefalia y esquizencefalia . [6] [10] Los individuos con estas características tienden a tener retraso del desarrollo o convulsiones. Las personas sin otras anomalías del sistema nervioso central tienden a tener un desarrollo intelectual normal o cercano a lo normal. [6] [18] Una revisión de 2003 encontró que la discapacidad intelectual moderada a grave y las anomalías cerebrales no relacionadas con la DWM solo estaban presentes en aquellos con las malformaciones más graves del vermis cerebeloso (menos de dos fisuras /tres lóbulos en el vermis), y estos comprendían el 16% de su muestra. La hidrocefalia también afectaba a todos estos pacientes. [12]
En la variante Dandy-Walker (DWV) y la mega cisterna magna específicamente, que son malformaciones menos graves, parece haber una mayor tasa de trastornos del espectro psicótico como esquizofrenia , trastorno bipolar , manía o catatonia . [2] [5] [20]
Anomalías asociadas
Una revisión de 2017 encontró las siguientes asociaciones en pacientes con DWS (generalmente debido a una condición o anomalía genética asociada): [5]
- El 27% de los pacientes tenía un defecto cardíaco congénito , como el conducto arterioso persistente , la coartación de la aorta , el defecto del tabique ventricular y el defecto del tabique auricular . En el 2,7% de los pacientes se informó insuficiencia cardíaca . [5]
- El 24% de los pacientes presentaba al menos una anomalía ocular, entre ellas cataratas , ojos pequeños ( microftalmia ), displasia/atrofia coriorretiniana , displasia/atrofia del nervio óptico , córnea pequeña (microcórnea) u opacidad corneal (leucoma), miopía y coloboma ( un orificio en una estructura del ojo). [5]
- El 16% de los pacientes fueron diagnosticados con un trastorno mental o conductual, y el 6,4% también tenía una discapacidad de aprendizaje. El 5,3% tenía trastorno bipolar o un trastorno del espectro psicótico , y el 2,1% tenía TDAH . Se encontraron ligeramente más de estos en la variante de Dandy-Walker (DWV) que en la DWM clásica, a pesar de que la DWV es menos común, solo en alrededor del 20% de los diagnósticos de DWS. [5]
- Alrededor del 12% de los pacientes tenían cánceres o tumores derivados de anomalías genéticas congénitas. Los más comunes fueron melanosis neurocutánea (5,9%), hemangiomas (4,8%, incluidos aquellos con síndrome PHACE ) y tumor de Wilms (4,4%). El 3,2% de los pacientes tenían nevos melanocíticos congénitos y el 2,1% tenían hamartomas linguales . Se cree que los tumores melanocíticos en estos casos se relacionan con los mismos errores genéticos en el desarrollo del tubo neural embrionario que conducen a la DWM, ya que la cresta neural embrionaria posterior da lugar a los melanocitos , entre otras células. [5]
- El 10% de los pacientes presentaba trastornos endocrinos o metabólicos y el 2,7% presentaba un crecimiento excesivo del vello ( hipertricosis ). [5]
- El 9% de los pacientes (casi todos con DWM clásica) tenían anomalías musculoesqueléticas, que incluían escoliosis o cifoescoliosis y artrogriposis . [5]
- El 5,9% de los pacientes tenían órganos reproductivos subdesarrollados, como genitales hipoplásicos o testículos no descendidos ( criptorquidia ). [5]
- El 5,3% de los pacientes tenían riñones subdesarrollados o poliquísticos. [5]
En la DWM puede producirse encefalocele occipital . [6] En general, se ha detectado en tasas del 6 al 8 %. [21] [22] [19] Se ha sugerido que se produce para compensar el aumento de presión en la fosa posterior durante la vida fetal. [6]
Ocasionalmente, la siringomielia se presenta con DWM, aunque no se sabe con certeza con qué frecuencia. [6] [23] Una revisión informó una incidencia del 4,3 % en una muestra. [7] Esto puede deberse a la herniación de la parte inferior del quiste a través del foramen magnum (un mecanismo similar a la malformación de Chiari ). Alternativamente, puede ser el resultado de la hidrocefalia, en la que se forma como un "quinto ventrículo" debido a un canal central agrandado . [6]
En raras ocasiones se ha detectado espina bífida junto con DWM. Cuando está presente, suele tratarse de espina bífida oculta. [24]
Causa

La DWM es causada por cualquier alteración del desarrollo embrionario que afecte la formación del vermis cerebeloso. Por lo general, se trata de una mutación genética que provoca una alteración de la migración y la división celular . Una gran cantidad de afecciones genéticas pueden provocar esta anomalía. En una gran parte de los casos de DWM, la afección se identifica en la persona afectada, sin embargo, en la mayoría de los casos no se identifica la causa. Al menos el 21 % de las personas con DWM tienen un hermano con la malformación y al menos el 16 % tienen un padre con la malformación. [5]
Enfermedades genéticas ciliopáticas
Se identifica una condición genética en alrededor del 33% de los diagnosticados con DWM después del nacimiento. [5] En una revisión de 2017, se encontró que el 4,3% tenía síndrome PHACE , una afección que involucra anomalías cerebrales, cardiovasculares y oculares, mientras que el 2,3% tenía síndrome de Joubert , una afección que involucra anomalías neurológicas y, a veces, oculares y renales. Entre el 21% y el 81% de las personas con síndrome PHACE tienen DWM. [25] [26] Otras afecciones genéticas comórbidas que se encontraron incluyeron el síndrome oculocerebrocutáneo , el síndrome oral-facial-digital , el síndrome de Coffin-Siris , el síndrome de Meckel-Gruber tipo 7 y el síndrome de Kallmann , entre muchos otros. [5] La DWM también se ha asociado con el síndrome 3C , el síndrome de Rubinstein-Taybi , el síndrome de Marden-Walker , el síndrome de Sheldon-Hall , el síndrome de Shah-Waardenburg , el síndrome de Fryns , [27] el síndrome de Walker-Warburg , la distrofia muscular congénita de Fukuyama , el síndrome de Ellis-Van Creveld , el síndrome de Fraser , el síndrome de Aicardi , el síndrome de Cornelia de Lange , [10] el síndrome de Klippel-Feil [28] [29] y el síndrome acrocalloso , [30] entre otros. El síndrome de craneosinostosis-malformación de Dandy-Walker-hidrocefalia también se ha descrito en un puñado de casos. Muchos de estos trastornos se clasifican como ciliopatías , trastornos genéticos que afectan a los cilios primarios celulares , proyecciones celulares delgadas hechas de microtúbulos que se cree que son cruciales en la señalización de la división y migración de células embrionarias . [31] La DWM es uno de los mayores predictores de una enfermedad genética ciliopática. [32]
Otros genes que se han relacionado con DWM incluyen ZIC1 , ZIC4 , FOXC1 , FGF17 , LAMC1 y NID1 . [5]
Anomalías cromosómicas
En aquellos a quienes se les diagnostica DWM antes del nacimiento en una ecografía , hasta la mitad tienen una anomalía cromosómica , [6] siendo la más común el síndrome de Edwards (trisomía 18), en aproximadamente el 26% de los casos de DWM prenatal. [27] El 6,5% de los diagnosticados con DWM después del nacimiento también tienen síndrome de Edwards. [5] Otras anomalías cromosómicas que pueden conducir a DWM incluyen triploidía , síndrome de Patau (trisomía 13), trisomía 9 y deleción o duplicación parcial de 3q. [5] [6] La región 3q24 contiene los genes ZIC1 y ZIC4 , que se sabe que están asociados con DWM. [6] [27]
Toxinas externas
Se sabe que el uso de warfarina durante el embarazo puede provocar defectos sistémicos en el feto , como disgenesia ocular, microcefalia , agenesia del cuerpo calloso , anomalías esqueléticas y defectos cardíacos . En 1985, también se relacionó con DWM. [33]
Fisiopatología
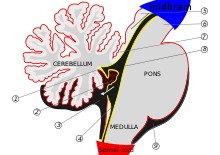
El cerebelo comienza a formarse en la quinta semana de desarrollo embrionario. Se diferencia en la parte superior del metencéfalo , mientras que el puente (en el tronco encefálico) se diferencia en la parte inferior, separado por el cuarto ventrículo . Los hemisferios cerebelosos se forman a partir de los labios rómbicos en la superficie anterior del cuarto ventrículo, que se expanden y giran para fusionarse en la línea media y formar el vermis cerebeloso en la semana 15. Si este proceso no se completa, el vermis cerebeloso no se formará por completo. Este largo período de desarrollo del vermis cerebeloso lo hace particularmente vulnerable a las interrupciones. [6]
En la DWM, el cuarto ventrículo se abre y se continúa con casi todo el espacio subaracnoideo de la fosa posterior . [6]
Fisiopatología de la hidrocefalia
La razón por la que se produce hidrocefalia en la DWM aún no se entiende completamente. Los primeros autores la habían atribuido al bloqueo o estrechamiento de los agujeros de Magendie y Luschka , las dos aberturas del cuarto ventrículo que permiten que el líquido cefalorraquídeo (LCR) escape al espacio subaracnoideo de la fosa posterior. Sin embargo, estudios posteriores encontraron que estos agujeros suelen estar abiertos en la DWM. [6] La hidrocefalia también suele estar presente (80% de las veces) al nacer en aquellos con DWM. [6]
La alteración del flujo de LCR puede estar más allá de las salidas del cuarto ventrículo. Se han propuesto teorías de desarrollo anormal o inflamación de la aracnoides en la fosa posterior. [6] La aracnoides contiene granulaciones necesarias para devolver el LCR desde los espacios subaracnoideos a las venas durales y la circulación. Las escisiones del quiste en DWM no han podido demostrar si hay una alteración de la absorción aracnoidea, ya que el espacio subaracnoideo siempre tarda días o semanas en llenarse después de la escisión. [6]
La estenosis acueductal (estrechamiento del paso entre el tercer y cuarto ventrículo) no parece ser un factor en la DWM. Generalmente es abierta y las derivaciones colocadas en el quiste de la fosa posterior casi siempre drenan todos los ventrículos superiores. Cuando está presente, puede ser el resultado de la compresión de un vermis o quiste herniado o una anomalía del desarrollo asociada. [6]
Se sabe que una vez iniciada la hidrocefalia, la compresión del quiste de la fosa posterior contra los conductos venosos de la aracnoides está implicada en el empeoramiento de la patología. [6]
Diagnóstico
La malformación de Dandy-Walker se diagnostica en base a los hallazgos característicos de neuroimagen. Puede diagnosticarse prenatalmente en ecografía ya a las 14 semanas de gestación, aunque generalmente se diagnostica postnatalmente mediante resonancia magnética . Se diagnostica dentro del primer año de vida en el 41% de los casos, normalmente debido al aumento de signos de hidrocefalia , [18] pero en el 28% de los casos se descubre en la adolescencia o la edad adulta debido a problemas de salud mental, como psicosis o trastorno del estado de ánimo . [5] [6]
Criterios y clasificación
No hay consenso sobre los criterios de diagnóstico precisos ni sobre los sistemas de clasificación de la DWM, y existe una controversia significativa sobre qué términos o criterios se deben utilizar. [5] [6] [12] Los criterios básicos de la DWM son la hipoplasia del vermis cerebeloso y un cuarto ventrículo y una fosa posterior agrandados (el espacio detrás del cerebelo), aunque no hay consenso sobre el grado específico de hipoplasia o agrandamiento quístico para el diagnóstico de la DWM. [7] Además, hay varias afecciones similares que en diversas ocasiones algunos autores han agrupado con la DWM en un continuo y otros las han separado como distintas, lo que complica aún más el diagnóstico. [6] [8]
En 1976, Harwood-Nash y Fitz propusieron el término variante de Dandy-Walker ( DWV ) para una malformación en la que la fosa posterior no está agrandada pero el vermis cerebeloso es hipoplásico. [7] [6] En 1989, Barkovich et al. propusieron el término complejo de Dandy-Walker ( DWC ) para incluir la DWM clásica y la DWV (bajo el tipo A) más una tercera malformación (bajo el tipo B) en la que el vermis cerebeloso permanece lo suficientemente grande como para ubicarse entre el cuarto ventrículo y la cisterna magna debajo de él, y en cambio es principalmente la cisterna magna la que está agrandada. En este tipo, la hipoplasia del vermis cerebeloso no llega más allá de la línea media horizontal del cuarto ventrículo, y la fosa posterior tampoco es tan grande. Los autores señalaron que esta forma anteriormente se habría clasificado simplemente como megacisterna magna . [2] [6] En 1999, Calabró et al. utilizaron por primera vez la frase " continuum de Dandy-Walker" al referirse a las propuestas de que una afección conocida como quiste de la bolsa de Blake se enmarca en el complejo de Dandy-Walker propuesto por Barkovich. [3] Autores posteriores someterían estos términos y sistemas a un intenso escrutinio y afirmarían que añadían una considerable confusión al diagnóstico de DWM. [5] [6] [12] Sin embargo, siguen utilizándose comúnmente. [5]
En 2011, Spennato et al. elaboraron un conjunto de criterios basados en Klein et al. (2003) que consideraron necesarios para el diagnóstico de DWM: [6]
- La porción inferior del vermis cerebeloso está ausente en diversos grados (tres cuartos, la mitad o un cuarto faltante).
- La fosa posterior (el espacio detrás del cerebelo) está agrandada y su flujo de líquido cefalorraquídeo es continuo con el del cuarto ventrículo.
- El resto del vermis cerebeloso es hipoplásico y está empujado hacia arriba y rotado hacia delante debido a la fosa posterior agrandada.
- Los hemisferios cerebelosos son empujados hacia delante y hacia los lados por la fosa posterior agrandada.
- El ángulo en el centro del vermis cerebeloso (que representa la ubicación del núcleo fastigial ) es grande, lo que le da una apariencia aplanada a la parte inferior del vermis, o el núcleo fastigial está completamente ausente.
- La confluencia de los senos paranasales , parte del sistema de drenaje ubicado en la parte posterior del lóbulo occipital , está elevada debido a la fosa posterior agrandada. (El tentorio cerebeloso adyacente también está elevado).
Debido a la inconsistencia de la presencia de hidrocefalia en DWM, Spennato y Klein sugirieron que no debería considerarse un criterio para DWM. [6] [12] Los criterios de Klein diferían de los de Spennato principalmente en que no requerían una hipoplasia aparente del hemisferio cerebeloso, pero también podrían haber requerido que el vermis tocara el tentorio o una ausencia de anormalidades del tronco encefálico . [12]
Métodos
La malformación de la médula espinal se puede observar prenatalmente en una ecografía a partir de las 14 semanas de gestación [5] , aunque la resonancia magnética es el método más útil para el diagnóstico. La resonancia magnética puede delinear la forma y la extensión de la malformación, así como evaluar áreas adicionales para malformaciones, como los hemisferios cerebelosos, el acueducto cerebral o el cuerpo calloso . La resonancia magnética con contraste de fase sincronizada con el corazón puede observar el flujo de líquido cefalorraquídeo (LCR) durante la sístole y la diástole del corazón. En la verdadera malformación de la médula espinal, esto encontrará un flujo desde el acueducto cerebral hasta la fosa posterior y ningún flujo entre la cisterna magna y el espacio detrás de la médula espinal cervical [6] .
También se puede utilizar la TC si no se dispone de una RMN, pero proporciona menos detalles. [6] Klein et al. (2003) sugirieron que un diagnóstico sospechado basado en una TC o una ecografía no debería confirmarse hasta que se realice una RMN, debido a la gran cantidad de afecciones que pueden presentarse de manera muy similar y confundir el diagnóstico. [12]
Diagnóstico diferencial
La DWM tiene una gran cantidad de afecciones que pueden presentarse de manera muy similar en las imágenes y confundir el diagnóstico. [6]
Quiste de la bolsa de Blake
El quiste de la bolsa de Blake (BPC), o bolsa de Blake persistente, es una afección que surge cuando la bolsa de Blake, una invaginación en el cuarto ventrículo que se rompe alrededor de los 4 meses de gestación para formar el foramen de Magendie (abertura medial), no se rompe. Esto puede provocar una dilatación del cuarto ventrículo y la consiguiente hidrocefalia de los cuatro ventrículos. [6]
En un quiste de la bolsa de Blake, a diferencia de lo que ocurre en DWM: [6]
- El cerebelo no es hipoplásico, aunque puede estar comprimido por la fosa posterior agrandada ( efecto de masa ).
- La fosa posterior no está agrandada.
- El tentorio cerebeloso/confluencia de los senos no está elevado.
- La hidrocefalia, cuando se presenta, afecta los cuatro ventrículos.
Sin embargo, algunos autores consideran que el quiste de la bolsa de Blake forma parte de un continuo con DWM (el "continuo Dandy-Walker"). [3] [8]
Mega cisterna magna
La megacisterna magna es una afección en la que la cisterna magna , la cisterna subaracnoidea que se encuentra debajo del cuarto ventrículo, está agrandada. Se ha propuesto que se debe a una ruptura tardía de la bolsa de Blake en lugar de a una ruptura fallida. [9]
En la mega cisterna magna, a diferencia de DWM: [9]
- El cerebelo no suele ser hipoplásico.
- El cuarto ventrículo tiene una forma relativamente normal.
- La hidrocefalia es poco común.
Existe un debate sobre si esta malformación es distinta de la DWM o forma parte del "continuo Dandy-Walker". [6] [8]
Quiste aracnoideo de la fosa posterior
Un quiste aracnoideo es una acumulación de líquido cefalorraquídeo (LCR) en la aracnoides . El 10% de estos se producen en la fosa posterior. [9]
En un quiste aracnoideo de fosa posterior, a diferencia de lo que ocurre en el DWM: [6] [9]
- El quiste está claramente localizado en un lugar específico separado de las salidas del cuarto ventrículo.
- El cerebelo no es hipoplásico, aunque puede estar comprimido por el quiste (efecto de masa).
- El flujo de LCR en el quiste no es continuo con el del cuarto ventrículo.
- La hidrocefalia, si se presenta, se debe a que el quiste presiona el cerebelo y comprime el acueducto cerebral o las salidas del cuarto ventrículo.
Tratamiento
El objetivo principal inmediato del tratamiento es el control de la hidrocefalia y del quiste agrandado de la fosa posterior, ya que estos pueden provocar un aumento de la presión intracraneal y daño cerebral. Una minoría de los afectados no desarrollan hidrocefalia y reciben tratamiento en función de los síntomas o la afección asociados. [13]
Hidrocefalia/quiste
En el caso de la hidrocefalia o el quiste de la fosa posterior, las derivaciones son el pilar del tratamiento. Sin embargo, los pacientes con DWM tienen una tasa más alta de complicaciones relacionadas con la derivación que otros pacientes con hidrocefalia (debido principalmente a la anatomía no convencional). [6] Una explicación de la falla de una derivación para reducir la presión intracraneal en la DWM ha sido que el quiste puede herniarse en el foramen magnum y formar una adherencia cicatricial en la unión cervical, lo que evita que se encoja nuevamente. Si esto ocurre, se puede intentar una descompresión suboccipital con duraplastia. [6]
En la DWM, no hay acuerdo sobre si se debe colocar una derivación en el cuarto ventrículo (una derivación cistoperitoneal o derivación CP), los ventrículos laterales (una derivación ventriculoperitoneal o derivación VP) o ambos, debido a estudios contradictorios sobre si el acueducto cerebral se ve afectado por la malformación. Sin embargo, una derivación CP casi siempre drena tanto el cuarto ventrículo como los laterales en la DWM, y de acuerdo con definiciones estrictas de la malformación, el acueducto debe asumirse abierto, [6] aunque las imágenes son importantes para confirmar esto. [10] Por lo tanto, muchos autores recomiendan la derivación CP como la opción lógica. Sin embargo, se asocia con una alta tasa de complicaciones, incluyendo desplazamiento y sobredrenaje. El sobredrenaje puede conducir a hematomas subdurales , una médula espinal anclada , debido a la cicatrización, o hernia descendente de los hemisferios cerebrales . Por lo tanto, Spennato et al. recomiendan una válvula reguladora de flujo o antisifón. Por otra parte, las derivaciones VP tienen una tasa de complicaciones menor que las derivaciones CP y algunos las recomiendan inicialmente. Sin embargo, son menos efectivas en la DWM y se debe considerar la posición elevada del tentorio antes de instalar una derivación VP. [6]
En pacientes mayores de un año, la ventriculostomía endoscópica del tercer ventrículo (VET) puede considerarse como el tratamiento de primera línea. Este procedimiento menos invasivo crea un orificio artificial en el tercer ventrículo para permitir que el LCR evite cualquier obstrucción. No se puede utilizar en pacientes con anomalías cerebrales como agenesia del cuerpo calloso, debido al riesgo de que el LCR se escape a otras áreas cerebrales. Sin embargo, un tronco encefálico comprimido no es una contraindicación. La VET tiene una tasa de éxito más modesta que las derivaciones, ya que el orificio a menudo se cierra. Es más probable que fracase en pacientes más jóvenes (menores de un año) y aún no se conocen sus efectos sobre el cerebro en desarrollo. [6] Los quistes posteriores al cerebelo, que se presentan en niños menores de cinco años, se han etiquetado como quistes retrocerebelosos del desarrollo según una nueva clasificación en relación con el tratamiento neuroendoscópico propuesto. [34]
Anteriormente se utilizaba la craneotomía de la fosa posterior y la escisión de la membrana quística, que a menudo no lograba prevenir la reformación del quiste y conllevaba cierto grado de mortalidad. Esta técnica todavía puede reservarse para pacientes con fallas/infecciones repetidas de la derivación. [6] [10]
Otro
Los tratamientos para cualquier otro síntoma se centran generalmente en la afección específica en cuestión y pueden incluir educación con apoyo, fisioterapia u otros servicios. Se puede ofrecer asesoramiento genético a los padres para futuras concepciones. [13]
Pronóstico
El pronóstico depende, en primer lugar, del tratamiento temprano y exitoso de la hidrocefalia, si está presente. El otro factor importante que afecta el pronóstico es la presencia de una enfermedad genética comórbida o una anomalía cerebral. [5] [6]
Las tasas de mortalidad de la DWM son aproximadamente del 15%. [6] En un estudio de la variante de Dandy-Walker (DWV), se observó una tasa de mortalidad del 12,5%. [7] La causa más común de muerte son las complicaciones de la hidrocefalia o su tratamiento. [6] [18] La hidrocefalia no tratada puede provocar un aumento de la presión intracraneal y daño cerebral. Las derivaciones utilizadas para tratar la DWM tienen una tasa de éxito moderada a buena, pero tienen una tasa de fracaso más alta que el promedio, lo que puede resultar en la imposibilidad de reducir la presión intracraneal o una infección, como la meningitis . Las complicaciones del drenaje excesivo, como los hematomas subdurales, también son posibles y pueden provocar mortalidad. [6] [35] Las derivaciones en el cuarto ventrículo (derivaciones cistoperitoneales o derivaciones CP) tienen una tasa generalmente alta de reducción exitosa del tamaño del quiste y del ventrículo, especialmente en el quiste (al menos el 80%). Con una derivación en los ventrículos laterales (derivación ventriculoperitoneal o derivación VP), los estudios generalmente han encontrado una tasa de éxito de reducción del tamaño del quiste de aproximadamente el 50 %, con una reducción exitosa del tamaño del ventrículo aproximadamente dos tercios de las veces. [6]
Otras afecciones sistémicas o genéticas a menudo están presentes con DWM, y cada una tiene su propio efecto significativo en el pronóstico. [6]
Epidemiología
La prevalencia de DWM se estima entre 1 en 25.000 a 1 en 50.000. [5] [11] La DWM es la causa de alrededor del 4,3% de los casos de hidrocefalia congénita [14] y del 2,5% de todos los casos de hidrocefalia. [6]
Una revisión de 2017 encontró que la mayoría de los pacientes (65%) fueron diagnosticados con "malformación de Dandy-Walker" o "síndrome de Dandy-Walker", mientras que el 20% fueron diagnosticados con "variante de Dandy-Walker" y el 1,1% con "mega cisterna magna". [5]
Historia
La malformación fue descrita por primera vez en 1887 por el cirujano inglés John Bland-Sutton como hipoplasia del vermis cerebeloso , una fosa posterior agrandada e hidrocefalia . [6] [15] En 1914, el neurocirujano estadounidense Walter Dandy y el pediatra estadounidense Kenneth Blackfan describieron la malformación como ausencia parcial o completa del vermis cerebeloso, un cuarto ventrículo agrandado e hidrocefalia. [6] [16] En 1942, el médico estadounidense John K. Taggart y el neurocirujano canadiense-estadounidense Arthur Earl Walker detallaron el fenómeno extensamente, atribuyendo la causa potencial como subdesarrollo de los agujeros de Luschka y Magendie , [17] que ahora ya no se cree que sean significativos. [6]
El término síndrome de Dandy-Walker (DWS) fue introducido por el psiquiatra alemán Clemens Ernst Benda en 1954; también utilizó el término malformación de Dandy-Walker una vez. [1] [6] En 1976, Harwood-Nash y Fitz propusieron el término variante de Dandy-Walker (DWV) para una malformación en la que la fosa posterior no está agrandada pero el vermis cerebeloso es hipoplásico. [7] [6] En 1989, Barkovich et al. propusieron el término complejo de Dandy-Walker (DWC) para incluir DWM y DWV clásicos (bajo el tipo A) más una tercera malformación (bajo el tipo B) en la que el vermis cerebeloso permanece lo suficientemente grande como para ubicarse entre el cuarto ventrículo y la cisterna magna , y en cambio es principalmente la cisterna magna la que está agrandada (a veces diagnosticada como "mega cisterna magna"). En 1999, Calabró et al. utilizaron por primera vez la frase "continuum de Dandy-Walker" al referirse a las propuestas de que una afección conocida como quiste de la bolsa de Blake se incluye en el complejo de Dandy-Walker propuesto por Barkovich. [3] Estos términos adicionales son en su mayoría desaconsejados por los autores modernos debido a la confusión y complejidad adicionales que implica el diagnóstico de DWM. [5] [6] [12]
Referencias
- ^ abc Benda, Clemens E. (1 de enero de 1954). "El síndrome de Dandy-Walker o la llamada atresia del foramen de Magendie". Revista de neuropatología y neurología experimental . 13 (1): 14–29. doi : 10.1093/jnen/13.1.14 . ISSN 0022-3069. PMID 13118372.
- ^ abc Barkovich, AJ; Kjos, BO; Norman, D.; Edwards, MS (diciembre de 1989). "Clasificación revisada de quistes de la fosa posterior y malformaciones similares a quistes basada en los resultados de imágenes por RM multiplanar". AJR. American Journal of Roentgenology . 153 (6): 1289–1300. doi :10.2214/ajr.153.6.1289. ISSN 0361-803X. PMID 2816648.
- ^ abcde Calabrò, F.; Arcuri, T.; Jinkins, JR (1 de abril de 2000). "Quiste de la bolsa de Blake: una entidad dentro del continuo de Dandy-Walker". Neurorradiología . 42 (4): 290–295. doi :10.1007/s002340050888. ISSN 1432-1920. PMID 10872175. S2CID 10545199.
- ^ abc "Hoja informativa sobre hidrocefalia | Instituto Nacional de Trastornos Neurológicos y Accidentes Cerebrovasculares" www.ninds.nih.gov . Consultado el 31 de diciembre de 2019 .
- ^ abcdefghijklmnopqrstu vwxyz aa ab ac ad ae af ag ah ai aj ak Stambolliu, Emelina; Ioakeim-Ioannidou, Myrsini; Kontokostas, Kimonas; Dakoutrou, Maria; Kousoulis, Antonis A. (1 de septiembre de 2017). "Las comorbilidades más comunes en pacientes con síndrome de Dandy-Walker: una revisión sistemática de informes de casos" (PDF) . Revista de neurología infantil . 32 (10): 886–902. doi :10.1177/0883073817712589. ISSN 0883-0738. PMID 28635420. S2CID 20046766.
- ^ abcdefghijklmnopqrstu vwxyz aa ab ac ad ae af ag ah ai aj ak al am an ao ap aq ar as at au av aw ax ay az ba bb bc bd be bf bg bh bi bj bk bl bm bn bo bp bq br bs bt bu bv bw bx de Spennato, Pietro; Mirón, Giuseppe; Nastro, Anna; Buonocore, María Consiglio; Ruggiero, Claudio; Trischitta, Vincenzo; Aliberti, Fernando; Cinalli, Giuseppe (octubre de 2011). "Hidrocefalia en la malformación de Dandy-Walker". El sistema nervioso del niño . 27 (10): 1665-1681. doi :10.1007/s00381-011-1544-4. ISSN 1433-0350. PMID 21928031. S2CID 25063114.
- ^ abcdef Sasaki-Adams, Deanna; Elbabaa, Samer K.; Jewells, Valerie; Carter, Lori; Campbell, Jeffrey W.; Ritter, Ann M. (septiembre de 2008). "La variante Dandy-Walker: una serie de casos de 24 pacientes pediátricos y evaluación de anomalías asociadas, incidencia de hidrocefalia y resultados del desarrollo". Revista de neurocirugía. Pediatría . 2 (3): 194–199. doi :10.3171/PED/2008/2/9/194. ISSN 1933-0707. PMID 18759601. S2CID 16364934.
- ^ abcdef Azab, Waleed A.; Shohoud, Sherien A.; Elmansoury, Tamer M.; Salaheddin, Waleed; Nasim, Khurram; Parwez, Aslam (24 de julio de 2014). "Quiste de la bolsa de Blake". Surgical Neurology International . 5 : 112. doi : 10.4103/2152-7806.137533 . ISSN 2229-5097. PMC 4123264 . PMID 25101207.
- ^ abcde Bosemani, Thangamadhan; Ormán, Gunes; Boltshauser, Eugen; Tekes, Aylín; Huisman, Thierry Asamblea General; Poretti, Andrea (1 de enero de 2015). "Anomalías congénitas de la fosa posterior". RadioGráficos . 35 (1): 200–220. doi : 10.1148/rg.351140038 . ISSN 0271-5333. PMID 25590398.
- ^ abcdef Kollias, SS; Ball, WS; Prenger, EC (noviembre de 1993). "Malformaciones quísticas de la fosa posterior: diagnóstico diferencial aclarado mediante análisis embriológico". Radiographics . 13 (6): 1211–1231. doi :10.1148/radiographics.13.6.8031352. ISSN 0271-5333. PMID 8031352.
- ^ abc "Orphanet: Malformación aislada de Dandy Walker". www.orpha.net . Consultado el 30 de diciembre de 2019 .
- ^ abcdefgh Klein, O.; Pierre-Kahn, A.; Boddaert, N.; Parisot, D.; Brunelle, F. (agosto de 2003). "Malformación de Dandy-Walker: diagnóstico prenatal y pronóstico". Sistema nervioso del niño . 19 (7–8): 484–489. doi :10.1007/s00381-003-0782-5. ISSN 0256-7040. PMID 12879343. S2CID 40944958.
- ^ abc "Malformación de Dandy Walker". NORD (Organización Nacional de Enfermedades Raras) . Consultado el 6 de enero de 2020 .
- ^ ab Lumenta, Christianto B.; Skotarczak, Ulrich (1995-03-01). "Seguimiento a largo plazo en 233 pacientes con hidrocefalia congénita". Sistema nervioso del niño . 11 (3): 173–175. doi :10.1007/BF00570260. ISSN 1433-0350. PMID 7773979. S2CID 22265554.
- ^ ab Sutton, J. Bland (1886-10-01). "Los recesos laterales del cuarto ventrículo; su relación con ciertos quistes y tumores del cerebelo y con el meningocele occipital". Cerebro . 9 (3): 352–361. doi :10.1093/brain/9.3.352. ISSN 0006-8950.
- ^ ab Dandy, Walter E.; Blackfan, Kenneth D. (1914-12-01). "UN ESTUDIO EXPERIMENTAL, CLÍNICO Y PATOLÓGICO: Parte 1.—Estudios experimentales". Revista estadounidense de enfermedades infantiles . VIII (6): 406–482. doi :10.1001/archpedi.1914.02180010416002. ISSN 0096-8994.
- ^ ab Taggart, John K.; Walker, A. Earl (1942-10-01). "Atresia congénita de los agujeros de Luschka y Magendie". Archivos de Neurología y Psiquiatría . 48 (4): 583–612. doi :10.1001/archneurpsyc.1942.02290100083008. ISSN 0096-6754.
- ^ abcde Bindal, Ajay K.; Storrs, Bruce B.; McLone, David G. (1990). "Manejo del síndrome de Dandy-Walker". Neurocirugía pediátrica . 16 (3): 163–169. doi :10.1159/000120518. ISSN 1016-2291. PMID 2134009.
- ^ ab Kumar, Raj; Jain, Manoj; Chhabra, Devendra (1 de mayo de 2001). "Síndrome de Dandy-Walker: diferentes modalidades de tratamiento y resultados en 42 casos". Sistema nervioso del niño . 17 (6): 348–352. doi :10.1007/s003810000425. ISSN 1433-0350. PMID 11417415. S2CID 23789193.
- ^ Pandurangi, Swapna; Pandurangi, Aditya; Matkar, Abhay; Shetty, Nithin; Patil, Preetam (enero de 2014). "Manifestaciones psiquiátricas asociadas a Mega Cisterna Magna". La Revista de Neuropsiquiatría y Neurociencias Clínicas . 26 (2): 169-171. doi : 10.1176/appi.neuropsych.13040097. ISSN 0895-0172. PMID 24763763.
- ^ Bindal, AK; Storrs, BB; McLone, DG (1990–1991). "Manejo del síndrome de Dandy-Walker". Neurocirugía Pediátrica . 16 (3): 163–169. doi :10.1159/000120518. ISSN 1016-2291. PMID 2134009.
- ^ Forzano, F.; Mansour, S.; Ierullo, A.; Homfray, T.; Thilaganathan, B. (2007). "Malformación de la fosa posterior en fetos: un informe de 56 casos adicionales y una revisión de la literatura". Diagnóstico prenatal . 27 (6): 495–501. doi :10.1002/pd.1722. ISSN 1097-0223. PMID 17367101. S2CID 21270692.
- ^ Hammond, Christopher J.; Chitnavis, Bhupal; Penny, Christopher C.; Strong, Anthony J. (1 de enero de 2002). "Complejo de Dandy-Walker y siringomielia en un adulto: informe de caso y discusión". Neurocirugía . 50 (1): 191–194. doi :10.1097/00006123-200201000-00028. ISSN 0148-396X. PMID 11844250. S2CID 45057003.
- ^ Golden, Jeffrey A.; Rorke, Lucy B.; Bruce, Derek A. (1987). "Síndrome de Dandy-Walker y anomalías asociadas". Neurocirugía pediátrica . 13 (1): 38–44. doi :10.1159/000120299. ISSN 1016-2291. PMID 3684814.
- ^ Metry DW, Dowd CF, Barkovich AJ, Frieden IJ (julio de 2001). "Las múltiples caras del síndrome PHACE". J. Pediatr . 139 (1): 117–23. doi :10.1067/mpd.2001.114880. PMID 11445804.
- ^ Poetke, M.; Frommeld, T.; Berlien, HP (diciembre de 2002). "Síndrome PHACE: nuevos puntos de vista sobre los criterios de diagnóstico". Revista Europea de Cirugía Pediátrica . 12 (6): 366–374. doi :10.1055/s-2002-36849. ISSN 0939-7248. PMID 12548487. S2CID 41134956.
- ^ abc Imataka, George; Yamanouchi, Hideo; Arisaka, Osamu (2007). "Síndrome de Dandy-Walker y anomalías cromosómicas". Anomalías congénitas . 47 (4): 113–118. doi : 10.1111/j.1741-4520.2007.00158.x . ISSN 1741-4520. PMID 17988252. S2CID 32024323.
- ^ Pascual-Castroviejo, I.; Vélez, A.; Pascual-Pascual, SI; Roche, MC; Villarejo, F. (1991-04-01). "Malformación de Dandy-Walker: análisis de 38 casos". Sistema nervioso del niño . 7 (2): 88–97. doi :10.1007/BF00247863. ISSN 1433-0350. PMID 1863935. S2CID 2733281.
- ^ Asai, Akio; Hoffman, Harold J.; Hendrick, Bruce; Humphreys, Robin P. (1989). "Síndrome de Dandy-Walker: experiencia en el Hospital para Niños Enfermos, Toronto". Neurocirugía Pediátrica . 15 (2): 66–73. doi :10.1159/000120445. ISSN 1423-0305. PMID 2635298.
- ^ "Entrada OMIM - # 200990 - SÍNDROME ACROCALLOSAL; ACLS" www.omim.org . Consultado el 6 de enero de 2020 .
- ^ Baker, Kate; Beales, Philip L. (2009). "Dando sentido a los cilios en la enfermedad: las ciliopatías humanas". American Journal of Medical Genetics Part C: Seminars in Medical Genetics . 151C (4): 281–295. doi : 10.1002/ajmg.c.30231 . ISSN 1552-4876. PMID 19876933. S2CID 7442991.
- ^ Badano JL, Mitsuma N, Beales PL, Katsanis N (2006). "Las ciliopatías: una clase emergente de trastornos genéticos humanos". Annu Rev Genom Hum Genet . 7 : 125–48. doi :10.1146/annurev.genom.7.080505.115610. PMID 16722803. S2CID 40223129.
- ^ Kaplan, Lawrence C. (1985). "Malformación congénita de Dandy Walker asociada con warfarina en el primer trimestre: Informe de un caso y revisión de la literatura". Teratología . 32 (3): 333–337. doi :10.1002/tera.1420320302. ISSN 1096-9926. PMID 4082063.
- ^ Dhandapani, S; Sahoo, SK (diciembre de 2019). "Quistes retrocerebelosos del desarrollo: una nueva clasificación para el tratamiento neuroendoscópico y una revisión sistemática". Neurocirugía mundial . 132 : e654–e664. doi :10.1016/j.wneu.2019.08.052. PMID 31442641. S2CID 201632112.
- ^ Yüceer N, Mertol T, Arda N (2007). "Tratamiento quirúrgico de 13 pacientes pediátricos con síndrome de Dandy-Walker". Pediatr Neurosurg . 43 (5): 358–63. doi :10.1159/000106383. PMID 17785999. S2CID 2289323.
![]() Este artículo incorpora material de dominio público de la página de información sobre el síndrome de Dandy-Walker. Instituto Nacional de Trastornos Neurológicos y Accidentes Cerebrovasculares .
Este artículo incorpora material de dominio público de la página de información sobre el síndrome de Dandy-Walker. Instituto Nacional de Trastornos Neurológicos y Accidentes Cerebrovasculares .
Lectura adicional
- Artículo de Metry Phaces en el Journal of Pediatrics, julio de 2001
- Definición de página web de medicina electrónica
- Artículo sobre la malformación de Dandy-Walker publicado en la Revista Panárabe de Neurocirugía