Antiandrógeno
| Antiandrógeno | |
|---|---|
| Clase de droga | |
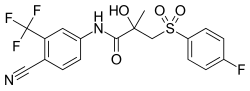 Bicalutamida , un antiandrógeno no esteroideo y el antagonista del receptor de andrógenos más utilizado en el tratamiento del cáncer de próstata . | |
| Identificadores de clase | |
| Sinónimos | Antagonistas de los andrógenos; Bloqueadores de los andrógenos; Bloqueadores de la testosterona |
| Usar | • Hombres y niños: cáncer de próstata , hiperplasia prostática benigna , pérdida de cabello del cuero cabelludo , parafilias , hipersexualidad , delincuentes sexuales , pubertad precoz , priapismo. • Mujeres y niñas: acné , seborrea , hidradenitis supurativa , hirsutismo , pérdida de cabello del cuero cabelludo , hiperandrogenismo , terapia hormonal para personas transgénero. |
| Código ATC | L02BB |
| Objetivo biológico | Receptor de andrógenos ; Receptor de progesterona ; Receptor de estrógeno ; Receptor de GnRH ; 5α-reductasa ; CYP17A1 (17α-hidroxilasa/ |
| Clase química | Esteroides ; No esteroides ; Péptidos |
| Enlaces externos | |
| Malla | D000726 |
| Estatus legal | |
| En Wikidata | |
Los antiandrógenos , también conocidos como antagonistas de los andrógenos o bloqueadores de la testosterona , son una clase de fármacos que impiden que los andrógenos como la testosterona y la dihidrotestosterona (DHT) medien sus efectos biológicos en el cuerpo. Actúan bloqueando el receptor de andrógenos (AR) y/o inhibiendo o suprimiendo la producción de andrógenos . [1] [2] Se pueden considerar como los opuestos funcionales de los agonistas de AR , por ejemplo, los andrógenos y los esteroides anabólicos (AAS) como la testosterona, la DHT y la nandrolona y los moduladores selectivos del receptor de andrógenos (SARM) como el enobosarm . Los antiandrógenos son uno de los tres tipos de antagonistas de las hormonas sexuales , los otros son los antiestrógenos y los antiprogestágenos . [3]
Los antiandrógenos se utilizan para tratar una variedad de afecciones dependientes de los andrógenos . [4] En los hombres, los antiandrógenos se utilizan en el tratamiento del cáncer de próstata , agrandamiento de próstata , pérdida de cabello del cuero cabelludo , impulso sexual excesivamente alto , impulsos sexuales inusuales y problemáticos y pubertad precoz . [4] [5] En las mujeres, los antiandrógenos se utilizan para tratar el acné , la seborrea , el crecimiento excesivo de cabello , la pérdida de cabello del cuero cabelludo y los niveles altos de andrógenos , como los que se producen en el síndrome de ovario poliquístico (SOP). [4] Los antiandrógenos también se utilizan como un componente de la terapia hormonal feminizante para mujeres transgénero y como bloqueadores de la pubertad en niñas transgénero . [4]
Los efectos secundarios de los antiandrógenos dependen del tipo de antiandrógeno y del antiandrógeno específico en cuestión. En cualquier caso, los efectos secundarios comunes de los antiandrógenos en los hombres incluyen sensibilidad en los senos , agrandamiento de los senos , feminización , sofocos , disfunción sexual , infertilidad y osteoporosis . En las mujeres, los antiandrógenos se toleran mucho mejor y los antiandrógenos que funcionan solo bloqueando directamente los andrógenos se asocian con efectos secundarios mínimos. Sin embargo, debido a que los estrógenos se fabrican a partir de los andrógenos en el cuerpo, los antiandrógenos que suprimen la producción de andrógenos pueden causar niveles bajos de estrógeno y síntomas asociados como sofocos, irregularidades menstruales y osteoporosis en mujeres premenopáusicas .
Existen varios tipos principales de antiandrógenos. [6] Estos incluyen antagonistas de AR , inhibidores de la síntesis de andrógenos y antigonadotropinas . [6] Los antagonistas de AR funcionan bloqueando directamente los efectos de los andrógenos, mientras que los inhibidores de la síntesis de andrógenos y las antigonadotropinas funcionan reduciendo los niveles de andrógenos. [6] Los antagonistas de AR se pueden dividir en antiandrógenos esteroides y antiandrógenos no esteroides ; los inhibidores de la síntesis de andrógenos se pueden dividir principalmente en inhibidores de CYP17A1 e inhibidores de la 5α-reductasa ; y las antigonadotropinas se pueden dividir en moduladores de la hormona liberadora de gonadotropina (moduladores de GnRH), progestágenos y estrógenos . [6] [7] [8]
Usos médicos
Los antiandrógenos se utilizan en el tratamiento de una variedad de afecciones dependientes de andrógenos tanto en hombres como en mujeres. [4] [9] Se utilizan para tratar a hombres con cáncer de próstata , hiperplasia prostática benigna , pérdida de cabello de patrón , hipersexualidad , parafilias y priapismo , así como a niños con pubertad precoz . [9] [10] [11] En mujeres y niñas, los antiandrógenos se utilizan para tratar el acné , la seborrea , la hidradenitis supurativa , el hirsutismo y el hiperandrogenismo . [9] [12] [13] Los antiandrógenos también se utilizan en mujeres transgénero como un componente de la terapia hormonal feminizante y como bloqueadores de la pubertad en niñas transgénero . [14] [15]
Hombres y niños
Cáncer de próstata
Los andrógenos como la testosterona y particularmente la DHT están involucrados de manera importante en el desarrollo y progresión del cáncer de próstata. [16] Actúan como factores de crecimiento en la glándula prostática , estimulando la división celular y el crecimiento tisular . [16] De acuerdo con esto, las modalidades terapéuticas que reducen la señalización de andrógenos en la glándula prostática, denominadas colectivamente como terapia de privación de andrógenos , pueden retardar significativamente el curso del cáncer de próstata y prolongar la vida en hombres con la enfermedad. [16] Aunque los antiandrógenos son efectivos para retardar la progresión del cáncer de próstata, generalmente no son curativos y, con el tiempo, la enfermedad se adapta y la terapia de privación de andrógenos eventualmente se vuelve ineficaz. [17] Cuando esto ocurre, se pueden considerar otros enfoques de tratamiento, como la quimioterapia . [17]
Los métodos más comunes de terapia de privación de andrógenos actualmente empleados para tratar el cáncer de próstata son la castración (con un modulador de GnRH u orquiectomía ), los antiandrógenos no esteroides y el inhibidor de la síntesis de andrógenos acetato de abiraterona . [16] La castración se puede utilizar sola o en combinación con uno de los otros dos tratamientos. [16] [18] Cuando la castración se combina con un antiandrógeno no esteroideo como bicalutamida , esta estrategia se conoce como bloqueo androgénico combinado (también conocido como bloqueo androgénico completo o máximo). [16] [19] La enzalutamida , la apalutamida y el acetato de abiraterona están específicamente aprobados para su uso en combinación con la castración para tratar el cáncer de próstata resistente a la castración. [16] [20] La monoterapia con el antiandrógeno no esteroide bicalutamida también se utiliza en el tratamiento del cáncer de próstata como una alternativa a la castración con una eficacia comparable pero con un perfil de efectos secundarios diferente y potencialmente ventajoso. [16] [21] [22]
El estrógeno en dosis altas fue el primer antiandrógeno funcional utilizado para tratar el cáncer de próstata. Fue ampliamente utilizado, pero en gran medida se abandonó para esta indicación a favor de agentes más nuevos con perfiles de seguridad mejorados y menos efectos secundarios feminizantes. [23] El acetato de ciproterona se desarrolló posteriormente al estrógeno en dosis altas y es el único antiandrógeno esteroide que se ha utilizado ampliamente en el tratamiento del cáncer de próstata, [24] pero ha sido reemplazado en gran medida por antiandrógenos no esteroides, que son más nuevos y tienen mayor efectividad, tolerabilidad y seguridad. [25] [26] La bicalutamida, así como la enzalutamida, han reemplazado en gran medida a los antiandrógenos no esteroides anteriores flutamida y nilutamida , que ahora se usan poco. [19] [27] [28] [29] [30] Los inhibidores anteriores de la síntesis de andrógenos, aminoglutetimida y ketoconazol, se han utilizado solo de forma limitada en el tratamiento del cáncer de próstata debido a problemas de toxicidad y han sido reemplazados por acetato de abiraterona. [31]
Además del tratamiento activo del cáncer de próstata, los antiandrógenos son eficaces como profilaxis (preventivos) para reducir el riesgo de desarrollar cáncer de próstata. [32] Los antiandrógenos solo se han evaluado de forma limitada para este propósito, pero los inhibidores de la 5α-reductasa finasterida y dutasterida y el antagonista esteroide AR espironolactona se han asociado con un riesgo significativamente reducido de cáncer de próstata. [32] [33] Además, es notable que el cáncer de próstata es extremadamente raro en mujeres transgénero que han estado en terapia hormonal feminizante durante un período prolongado de tiempo. [34] [35] [36]
Agrandamiento de la próstata
Los inhibidores de la 5α-reductasa finasterida y dutasterida se utilizan para tratar la hiperplasia prostática benigna, una afección en la que la próstata se agranda y esto produce obstrucción urinaria y malestar. [37] Son eficaces porque los andrógenos actúan como factores de crecimiento en la glándula prostática. [37] Los antiandrógenos acetato de clormadinona y oxendolona y los antiandrógenos funcionales alilestrenol y caproato de gestonorona también están aprobados en algunos países para el tratamiento de la hiperplasia prostática benigna. [38] [39]
Pérdida de cabello en el cuero cabelludo
Los inhibidores de la 5α-reductasa como la finasterida, la dutasterida y el alfatradiol y el antagonista tópico no esteroide AR topilutamida (fluridil) están aprobados para el tratamiento de la pérdida de cabello de patrón, también conocida como pérdida de cabello del cuero cabelludo o calvicie. [40] Esta afección generalmente es causada por andrógenos, por lo que los antiandrógenos pueden ralentizar o detener su progresión. [41] Los antiandrógenos sistémicos además de los inhibidores de la 5α-reductasa no se usan generalmente para tratar la pérdida de cabello del cuero cabelludo en hombres debido a riesgos como la feminización (p. ej., ginecomastia) y la disfunción sexual. [42] [43 ] [44] [45 ] [ 46] [47] [48] Sin embargo, se han evaluado y se ha informado que son efectivos para esta indicación. [42] [43] [49]
Acné
Los antiandrógenos sistémicos generalmente no se utilizan para tratar el acné en hombres debido a su alto riesgo de feminización (p. ej., ginecomastia) y disfunción sexual. [50] [51] Sin embargo, se han estudiado para el acné en hombres y se ha demostrado que son eficaces. [52] [44] [45] [53] La clascoterona , un antiandrógeno tópico, es eficaz para el acné en hombres y ha sido aprobada por la FDA en agosto de 2020. [54] [55] [56] [57]
Parafilia
Los andrógenos aumentan el deseo sexual , [58] y por esta razón, los antiandrógenos pueden reducir el deseo sexual en los hombres. [59] [60] De acuerdo con esto, los antiandrógenos se utilizan en el tratamiento de afecciones como la hipersexualidad (deseo sexual excesivamente alto) y las parafilias (intereses sexuales atípicos y a veces socialmente inaceptables) como la pedofilia (atracción sexual hacia los niños). [59] [60] Se han utilizado para disminuir el deseo sexual en delincuentes sexuales a fin de reducir la probabilidad de reincidencia (delitos repetidos). [61] Los antiandrógenos utilizados para estas indicaciones incluyen acetato de ciproterona , acetato de medroxiprogesterona y moduladores de GnRH. [62] [63]
Pubertad precoz
Los antiandrógenos se utilizan para tratar la pubertad precoz en los niños. [64] [65] [66] [67] Funcionan oponiéndose a los efectos de los andrógenos y retrasando el desarrollo de las características sexuales secundarias y la aparición de cambios en el impulso y la función sexual hasta una edad más apropiada. [64] [65] Los antiandrógenos que se han utilizado para este propósito incluyen acetato de ciproterona , acetato de medroxiprogesterona , moduladores de GnRH, espironolactona , bicalutamida y ketoconazol . [64] [67] [68] [69] [70] [71] La espironolactona y la bicalutamida requieren una combinación con un inhibidor de la aromatasa para prevenir los efectos de los estrógenos sin oposición , mientras que los otros se pueden utilizar solos. [64] [70] [71]
Erecciones duraderas
Los antiandrógenos son eficaces en el tratamiento del priapismo recurrente ( erecciones del pene potencialmente dolorosas que duran más de cuatro horas). [72] [73] [74] [75] [76]
Mujeres y niñas
Afecciones de la piel y el cabello
Los antiandrógenos se utilizan en el tratamiento de afecciones de la piel y el cabello dependientes de los andrógenos , incluyendo acné, seborrea, hidradenitis supurativa, hirsutismo y pérdida de cabello de patrón en mujeres. [12] Todas estas afecciones dependen de los andrógenos y, por esta razón, los antiandrógenos son eficaces para tratarlas. [12] Los antiandrógenos más utilizados para estas indicaciones son el acetato de ciproterona y la espironolactona . [77] La flutamida también se ha estudiado ampliamente para tales usos, pero ha caído en desgracia debido a su asociación con la hepatotoxicidad . [78] La bicalutamida , que tiene un riesgo relativamente mínimo de hepatotoxicidad, se ha evaluado para el tratamiento del hirsutismo y se ha encontrado que es eficaz de manera similar a la flutamida y puede usarse en su lugar. [79] [80] Además de los antagonistas de AR, los anticonceptivos orales que contienen etinilestradiol son eficaces para tratar estas afecciones y pueden combinarse con antagonistas de AR. [81] [82]
Niveles altos de andrógenos
El hiperandrogenismo es una afección en mujeres en la que los niveles de andrógenos son excesivamente altos y anormalmente altos. [13] Se observa comúnmente en mujeres con SOP, y también ocurre en mujeres con afecciones intersexuales como la hiperplasia suprarrenal congénita . [13] El hiperandrogenismo se asocia con la virilización , es decir, el desarrollo de características sexuales secundarias masculinas como el crecimiento de vello facial y corporal de patrón masculino (o hirsutismo), profundización de la voz , aumento de la masa y fuerza muscular y ensanchamiento de los hombros , entre otros. [13] Las afecciones de la piel y el cabello dependientes de los andrógenos, como el acné y la pérdida de cabello de patrón, también pueden ocurrir en el hiperandrogenismo, y los trastornos menstruales , como la amenorrea , se observan comúnmente. [13] Aunque los antiandrógenos no tratan la causa subyacente del hiperandrogenismo (p. ej., SOP), pueden prevenir y revertir su manifestación y efectos. [13] Al igual que en el caso de las afecciones de la piel y el cabello dependientes de los andrógenos, los antiandrógenos más utilizados en el tratamiento del hiperandrogenismo en mujeres son el acetato de ciproterona y la espironolactona. [13] Se pueden utilizar otros antiandrógenos, como la bicalutamida, como alternativa. [13]
Terapia hormonal para personas transgénero
Los antiandrógenos se utilizan para prevenir o revertir la masculinización y facilitar la feminización en mujeres transgénero que se someten a terapia hormonal y que no se han sometido a cirugía de reasignación de sexo u orquiectomía . [14] Además de los estrógenos, los principales antiandrógenos que se han utilizado para este propósito son el acetato de ciproterona, la espironolactona y los moduladores de GnRH. [14] Los antiandrógenos no esteroides como la bicalutamida también se utilizan para esta indicación. [83] [14] Además del uso en mujeres transgénero, los antiandrógenos, principalmente los moduladores de GnRH, se utilizan como bloqueadores de la pubertad para prevenir el inicio de la pubertad en las niñas transgénero hasta que sean mayores y estén listas para comenzar la terapia hormonal. [15]
Formularios disponibles
Existen varios tipos diferentes de antiandrógenos, incluidos los siguientes: [6]
- Antagonistas del receptor de andrógenos: Medicamentos que se unen directamente al AR y lo bloquean. [84] [85] Estos medicamentos incluyen los antiandrógenos esteroides acetato de ciproterona , acetato de megestrol , acetato de clormadinona , espironolactona , oxendolona y acetato de osaterona (veterinario) y los antiandrógenos no esteroides flutamida , bicalutamida , nilutamida , topilutamida , enzalutamida y apalutamida . [84] [85] [7] [8] Además del acetato de ciproterona y el acetato de clormadinona, algunas otras progestinas utilizadas en anticonceptivos orales y/o en la THS menopáusica, incluyendo dienogest , drospirenona , medrogestona , acetato de nomegestrol , promegestona y trimegestona también tienen diversos grados de actividad antagonista del AR. [86] [87] [88]
- Inhibidores de la síntesis de andrógenos: Medicamentos que inhiben directamente la biosíntesis enzimática de andrógenos como la testosterona y/o DHT. [89] [31] Los ejemplos incluyen los inhibidores de CYP17A1 ketoconazol , acetato de abiraterona y seviteronel , [89] el inhibidor de CYP11A1 (P450scc) aminoglutetimida , [89] y los inhibidores de la 5α-reductasa finasterida , dutasterida , epristerida , alfatradiol y extracto de saw palmetto ( Serenoa repens ). [90] También se sabe que varios otros antiandrógenos, incluidos el acetato de ciproterona, la espironolactona, la medrogestona, la flutamida, la nilutamida y el bifluranol , inhiben débilmente la síntesis de andrógenos.
- Antigonadotropinas: Medicamentos que suprimen la liberación inducida por la hormona liberadora de gonadotropina (GnRH) de gonadotropinas y la consiguiente activación de la producción de andrógenos gonadales . [2] [91] Los ejemplos incluyen moduladores de GnRH como leuprorelina (un agonista de GnRH ) y cetrorelix (un antagonista de GnRH ), [92] progestágenos como alilestrenol , acetato de clormadinona, acetato de ciproterona, caproato de gestonorona , caproato de hidroxiprogesterona , acetato de medroxiprogesterona , acetato de megestrol, acetato de osaterona (veterinario) y oxendolona, [93] [94] y estrógenos como estradiol , ésteres de estradiol , etinilestradiol , estrógenos conjugados y dietilestilbestrol . [2] [93]
- Varios: Medicamentos que se oponen a los efectos de los andrógenos por medios distintos a los anteriores. Los ejemplos incluyen estrógenos, especialmente orales y sintéticos (p. ej., etinilestradiol , dietilestilbestrol ), que estimulan la producción de globulina transportadora de hormonas sexuales (SHBG) en el hígado y, por lo tanto, disminuyen los niveles libres y, por lo tanto, bioactivos de testosterona y DHT; anticorticotropinas como glucocorticoides , que suprimen la producción de andrógenos suprarrenales inducida por la hormona adrenocorticotrópica (ACTH) ; e inmunógenos y vacunas contra la androstenediona como la ovandrotona albúmina y la androstenediona albúmina , que disminuyen los niveles de andrógenos a través de la generación de anticuerpos contra el andrógeno y el precursor de andrógenos androstenediona (utilizada solo en medicina veterinaria ).
Ciertos antiandrógenos combinan varios de los mecanismos anteriores. [6] [95] Un ejemplo es el antiandrógeno esteroide acetato de ciproterona, que es un potente antagonista de AR, un potente progestágeno y, por lo tanto, antigonadotropina, un glucocorticoide débil y, por lo tanto, anticorticotropina, y un inhibidor débil de la síntesis de andrógenos. [6] [95] [96] [97]
| Nombre genérico | Clase | Tipo | Nombre(s) de marca | Ruta(s) | Lanzamiento | Estado | Golpea un |
|---|---|---|---|---|---|---|---|
| Acetato de abiraterona | Esteroides | Inhibidor de la síntesis de andrógenos | Zytiga | Oral | 2011 | Disponible | 523.000 |
| Alilestrenol | Esteroides | Progestina | Gestanina, Perselina | Oral | 1961 | Disponible b | 61.800 |
| Aminoglutetimida | No esteroide | Inhibidor de la síntesis de andrógenos | Cytadren, Orimeten | Oral | 1960 | Disponible b | 222.000 |
| Apalutamida | No esteroide | Antagonista de AR | Erleada | Oral | 2018 | Disponible | 50.400 |
| Bicalutamida | No esteroide | Antagonista de AR | Casodex | Oral | 1995 | Disponible | 754.000 |
| Acetato de clormadinona | Esteroides | Progestina; antagonista de AR | Belara, Prostal | Oral | 1965 | Disponible | 220.000 |
| Acetato de ciproterona | Esteroides | Progestina; antagonista de AR | Androcur, Diana | Oral, IM | 1973 | Disponible | 461.000 |
| Acetato de delmadinona | Esteroides | Progestina; antagonista de AR | Retrasado | Veterinario | 1972 | Veterinario | 42.600 |
| Enzalutamida | No esteroide | Antagonista de AR | Xtandi | Oral | 2012 | Disponible | 328.000 |
| Flutamida | No esteroide | Antagonista de AR | Eulexina | Oral | 1983 | Disponible | 712.000 |
| Caproato de gestonorona | Esteroides | Progestina | Depósito, Primostato | SOY | 1973 | Disponible b | 119.000 |
| Caproato de hidroxiprogesterona | Esteroides | Progestina | Delalutin, Proluton | SOY | 1954 | Disponible | 108.000 |
| Ketoconazol | No esteroide | Inhibidor de la síntesis de andrógenos | Nizoral, otros | Oral, tópico | 1981 | Disponible | 3.650.000 |
| Acetato de medroxiprogesterona | Esteroides | Progestina | Provera, Depo-Provera | Oral, IM , SC | 1958 | Disponible | 1.250.000 |
| Acetato de megestrol | Esteroides | Progestina; antagonista de AR | Megace | Oral | 1963 | Disponible | 253.000 |
| Nilutamida | No esteroide | Antagonista de AR | Anandron, Nilandron | Oral | 1987 | Disponible | 132.000 |
| Acetato de osaterona | Esteroides | Progestina; antagonista de AR | Ypozane | Veterinario | 2007 | Veterinario | 87.600 |
| Oxendolona | Esteroides | Progestina; antagonista de AR | Prostetina, Roxenona | SOY | 1981 | Disponible b | 36.100 |
| Espironolactona | Esteroides | Antagonista de AR | Aldactona | Oral, tópico | 1959 | Disponible | 3.010.000 |
| Topilutamida | No esteroide | Antagonista de AR | Eucapil | Actual | 2003 | Disponible b | 36.300 |
| Notas al pie: a = Resultados = Resultados de la búsqueda de Google (a febrero de 2018). b = Disponibilidad limitada/mayormente descontinuada. Clase: Esteroideo = Antiandrógeno esteroide . No esteroide = Antiandrógeno no esteroide . Fuentes: Ver artículos individuales. | |||||||
Efectos secundarios
Los efectos secundarios de los antiandrógenos varían dependiendo del tipo de antiandrógeno –es decir, si es un antagonista selectivo de AR o reduce los niveles de andrógenos– así como de la presencia de actividad fuera del objetivo en el antiandrógeno en cuestión. [21] [98] Por ejemplo, mientras que los antiandrógenos antigonadotrópicos como los moduladores de GnRH y el acetato de ciproterona están asociados con disfunción sexual pronunciada y osteoporosis en hombres, los antagonistas selectivos de AR como la bicalutamida no están asociados con osteoporosis y han sido asociados solo con disfunción sexual mínima. [21] [99] [100] Se piensa que estas diferencias están relacionadas con el hecho de que las antigonadotropinas suprimen los niveles de andrógenos y por extensión los niveles de metabolitos bioactivos de andrógenos como estrógenos y neuroesteroides , mientras que los antagonistas selectivos de AR neutralizan de manera similar los efectos de los andrógenos pero dejan los niveles de andrógenos y por lo tanto sus metabolitos intactos (y de hecho pueden incluso aumentarlos como resultado de sus efectos progonadotrópicos ). [21] Como otro ejemplo, los antiandrógenos esteroides acetato de ciproterona y espironolactona poseen acciones fuera del objetivo que incluyen actividad progestágena , antimineralocorticoide y/o glucocorticoide además de su actividad antiandrógena, y estas actividades fuera del objetivo pueden resultar en efectos secundarios adicionales. [98]
En los hombres, los principales efectos secundarios de los antiandrógenos son la desmasculinización y la feminización . [101] Estos efectos secundarios incluyen dolor/sensibilidad en los senos y ginecomastia ( desarrollo / agrandamiento de los senos ), reducción del crecimiento/densidad del vello corporal , disminución de la masa y fuerza muscular , cambios femeninos en la masa y distribución de la grasa y reducción de la longitud del pene y del tamaño testicular . [101] Se ha descubierto que las tasas de ginecomastia en hombres con monoterapia con antagonistas selectivos de AR varían del 30 al 85%. [102] Además, los antiandrógenos pueden causar infertilidad , osteoporosis , sofocos , disfunción sexual (incluida la pérdida de la libido y la disfunción eréctil ), depresión , fatiga , anemia y disminución del volumen de semen/eyaculación en los hombres. [ verificación fallida ] [101] Por el contrario, los efectos secundarios de los antagonistas selectivos de AR en las mujeres son mínimos. [80] [103] Sin embargo, los antiandrógenos antigonadotrópicos como el acetato de ciproterona pueden producir hipoestrogenismo , amenorrea y osteoporosis en mujeres premenopáusicas, entre otros efectos secundarios. [81] [104] [105] Además, los antagonistas del receptor de andrógenos pueden producir efectos desfavorables sobre los niveles de colesterol , lo que a largo plazo puede aumentar el riesgo de enfermedad cardiovascular . [106] [107] [108] [109] [110] [111] [112]
Se ha asociado una serie de antiandrógenos con hepatotoxicidad . [113] Estos incluyen, en distintos grados, acetato de ciproterona, flutamida, nilutamida, bicalutamida, aminoglutetimida y ketoconazol. [113] Por el contrario, la espironolactona, la enzalutamida [114] y otros antiandrógenos no se asocian con tasas significativas de hepatotoxicidad. Sin embargo, aunque no plantean un riesgo de hepatotoxicidad, la espironolactona tiene un riesgo de hipercalemia y la enzalutamida tiene un riesgo de convulsiones . [ cita requerida ]
En las mujeres embarazadas , los antiandrógenos pueden interferir con la diferenciación sexual mediada por andrógenos de los genitales y el cerebro de los fetos masculinos . [115] Esto se manifiesta principalmente como genitales ambiguos , es decir, genitales subvirilizados o feminizados, que, anatómicamente, son un cruce entre un pene y una vagina , y teóricamente también como feminidad . [115] [116] Como tal, los antiandrógenos son teratógenos , y las mujeres embarazadas no deben ser tratadas con un antiandrógeno. [82] Además, a las mujeres que pueden o pueden quedar embarazadas se les recomienda encarecidamente que tomen un antiandrógeno solo en combinación con un método anticonceptivo adecuado . [82]
Sobredosis
Los antiandrógenos son relativamente seguros en caso de sobredosis aguda . [ cita requerida ]
Interacciones
Los inhibidores e inductores de las enzimas del citocromo P450 pueden interactuar con diversos antiandrógenos. [ cita requerida ]
Mecanismo de acción
Antagonistas del receptor de andrógenos
| Antiandrógeno | Afinidades de enlace relativas | ||||
|---|---|---|---|---|---|
| ArkansasReceptor de andrógenos | Relaciones públicasInformación sobre herramientas Receptor de progesterona | ESReceptor de estrógeno | GRAMOInformación sobre herramientas Receptor de glucocorticoides | SEÑORInformación sobre herramientas Receptor de mineralocorticoides | |
| Acetato de ciproterona | 8–10 | 60 | <0,1 | 5 | 1 |
| Acetato de clormadinona | 5 | 175 | <0,1 | 38 | 1 |
| Acetato de megestrol | 5 | 152 | <0,1 | 50 | 3 |
| Espironolactona | 7 | 0,4 a | <0,1 | 2 un | 182 |
| Trimetiltrienolona | 3.6 | <1 | <1 | <1 | <1 |
| Inocoterona | 0,8 | <0,1 | <0,1 | <0,1 | <0,1 |
| Acetato de inocoterona | <0,1 | <0,1 | <0,1 | <0,1 | <0,1 |
| Flutamida | <0,1 | <0,1 | <0,1 | <0,1 | <0,1 |
| Hidroxiflutamida | 0,5–0,8 | <0,1 | <0,1 | <0,1 | <0,1 |
| Nilutamida | 0,5–0,8 | <0,1 | <0,1 | <0,1 | <0,1 |
| Bicalutamida | 1.8 | <0,1 | <0,1 | <0,1 | <0,1 |
| Notas: (1): Los ligandos de referencia (100%) fueron testosterona para el ARReceptor de andrógenos con información sobre herramientas, progesterona para el PRInformación sobre herramientas sobre el receptor de progesterona, estradiol para el ERReceptor de estrógeno con información sobre herramientas, dexametasona para el GRReceptor de glucocorticoides con información sobre herramientas, y aldosterona para el MRInformación sobre herramientas sobre el receptor de mineralocorticoides(2): Los tejidos fueron próstata de rata (AR), útero de conejo (PR), útero de ratón (ER), timo de rata (GR) y riñón de rata (MR). (3): Los tiempos de incubación (0 °C) fueron 24 horas (AR, a ), 2 horas (PR, ER), 4 horas (GR) y 1 hora (MR). (4): Los métodos de ensayo fueron diferentes para bicalutamida para receptores además del AR. Fuentes: [117] [118] [119] [120] [121] [122] [123] [124] [125] [126] | |||||
| Antiandrógeno | Potencia relativa |
|---|---|
| Bicalutamida | 4.3 |
| Hidroxiflutamida | 3.5 |
| Flutamida | 3.3 |
| Acetato de ciproterona | 1.0 |
| Zanoterona | 0,4 |
| Descripción: Potencias relativas de los antiandrógenos administrados por vía oral para antagonizar 0,8 a 1,0 mg/kg scInformación sobre herramientas: inyección subcutánea Aumento del peso de la próstata ventral inducido por propionato de testosterona en ratas macho inmaduras castradas . Los valores más altos indican mayor potencia. Fuentes: Ver plantilla. | |
Los antagonistas de AR actúan uniéndose directamente y desplazando competitivamente a los andrógenos como la testosterona y la DHT del AR, evitando así que activen el receptor y medien sus efectos biológicos. [84] [85] Los antagonistas de AR se clasifican en dos tipos, según la estructura química : esteroides y no esteroides. [7] [8] [84] [85] [92] Los antagonistas de AR esteroides están estructuralmente relacionados con las hormonas esteroides como la testosterona y la progesterona , mientras que los antagonistas de AR no esteroides no son esteroides y son estructuralmente distintos. Los antagonistas de AR esteroides tienden a tener acciones hormonales fuera del objetivo debido a su similitud estructural con otras hormonas esteroides. [92] Por el contrario, los antagonistas de AR no esteroides son selectivos para el AR y no tienen actividad hormonal fuera del objetivo. [92] Por esta razón, a veces se los describe como antiandrógenos "puros". [92]
Aunque se describen como antiandrógenos y de hecho muestran solo tales efectos en general, la mayoría o todos los antagonistas esteroides del AR en realidad no son antagonistas silenciosos del AR sino más bien son agonistas parciales débiles y pueden activar el receptor en ausencia de agonistas del AR más potentes como la testosterona y la DHT. [84] [31] [127] [128] Esto puede tener implicaciones clínicas en el contexto específico del tratamiento del cáncer de próstata. [84] [127] Como ejemplo, los antagonistas esteroides del AR pueden aumentar el peso de la próstata y acelerar el crecimiento de las células del cáncer de próstata en ausencia de agonistas del AR más potentes, [84] [127] y se ha descubierto que la espironolactona acelera la progresión del cáncer de próstata en informes de casos. [129] [130] Además, mientras que el acetato de ciproterona produce genitales ambiguos a través de la feminización en fetos machos cuando se administra a animales preñados, [131] se ha descubierto que produce masculinización de los genitales de fetos hembras de animales preñados. [84] A diferencia de los antagonistas esteroides del AR, los antagonistas no esteroides del AR son antagonistas silenciosos del AR y no activan el receptor. [132] [31] [133] [127] Esta puede ser la razón por la que tienen mayor eficacia que los antagonistas esteroides del AR en el tratamiento del cáncer de próstata y es una razón importante de por qué los han reemplazado en gran medida para esta indicación en medicina. [132] [31] [133] [127]
Los antiandrógenos no esteroides tienen una afinidad relativamente baja por el AR en comparación con los ligandos esteroides del AR. [31] [133] [134] Por ejemplo, la bicalutamida tiene alrededor del 2% de la afinidad de la DHT por el AR y alrededor del 20% de la afinidad del CPA por el AR. [134] Sin embargo, a pesar de su baja afinidad por el AR, la falta de actividad agonista parcial débil de los NSAA parece mejorar su potencia en relación con los antiandrógenos esteroides. [134] [135] Por ejemplo, aunque la flutamida tiene una afinidad aproximadamente 10 veces menor por el AR que el CPA, muestra una potencia igual o ligeramente mayor que el CPA como antiandrógeno en bioensayos . [134] [135] Además, las concentraciones terapéuticas circulantes de antiandrógenos no esteroides son muy altas, del orden de miles de veces más altas que las de testosterona y DHT, y esto les permite competir eficazmente y bloquear la señalización de AR. [136]
Los antagonistas de AR pueden no unirse a los receptores de andrógenos de membrana (mAR) o bloquearlos, que son distintos del AR nuclear clásico. [137] [138] [139] Sin embargo, los mAR no parecen estar involucrados en la masculinización . Esto se evidencia por el fenotipo perfectamente femenino de las mujeres con síndrome de insensibilidad completa a los andrógenos . [140] [141] Estas mujeres tienen un cariotipo 46,XY (es decir, son genéticamente "masculinas") y altos niveles de andrógenos pero poseen un AR defectuoso y por esta razón nunca se masculinizan. [140] [141] Se las describe como altamente femeninas, tanto física como mental y conductualmente. [142] [143] [144]
Antagonistas del dominio N-terminal
Los antagonistas del dominio N-terminal del AR son un nuevo tipo de antagonista del AR que, a diferencia de todos los antagonistas del AR comercializados actualmente, se unen al dominio N-terminal (NTD) del AR en lugar del dominio de unión al ligando (LBD). [145] Mientras que los antagonistas del AR convencionales se unen al LBD del AR y desplazan competitivamente a los andrógenos, impidiendo así que activen el receptor, los antagonistas del NTD del AR se unen covalentemente al NTD del AR y previenen las interacciones proteína-proteína posteriores a la activación que se requieren para la actividad transcripcional . [145] Como tales, son antagonistas no competitivos e irreversibles del AR. [146] Los ejemplos de antagonistas del NTD del AR incluyen el éter diglicidílico de bisfenol A (BADGE) y sus derivados EPI-001 , ralaniten (EPI-002) y acetato de ralaniten (EPI-506). [145] [147] Los antagonistas de AR NTD están bajo investigación para el posible tratamiento del cáncer de próstata, y se cree que pueden tener una mayor eficacia como antiandrógenos en relación con los antagonistas de AR convencionales. [145] De acuerdo con esta noción, los antagonistas de AR NTD son activos contra las variantes de empalme del AR, lo que no ocurre con los antagonistas de AR convencionales, y los antagonistas de AR NTD son inmunes a las mutaciones de ganancia de función en el LBD de AR que convierten a los antagonistas de AR en agonistas de AR y que ocurren comúnmente en el cáncer de próstata. [145]
Degradadores del receptor de andrógenos
Los degradadores selectivos del receptor de andrógenos (SARD) son otro nuevo tipo de antiandrógeno que se ha desarrollado recientemente. [148] Funcionan mejorando la degradación del AR y son análogos a los degradadores selectivos del receptor de estrógeno (SERD) como fulvestrant (un fármaco utilizado para tratar el cáncer de mama con receptores de estrógeno positivos ). [148] De manera similar a los antagonistas del receptor de estrógeno positivo, se cree que los SARD pueden tener una mayor eficacia que los antagonistas del receptor de estrógeno convencionales y, por esta razón, se están investigando para el tratamiento del cáncer de próstata. [149] Un ejemplo de un SARD es la dimetilcurcumina (ASC-J9), que se encuentra en desarrollo como medicamento tópico para el posible tratamiento del acné. [150] Los SARD como la dimetilcurcumina se diferencian de los antagonistas del receptor de estrógeno convencionales y de los antagonistas del receptor de estrógeno positivo en que no necesariamente se unen directamente al AR. [149]
Inhibidores de la síntesis de andrógenos
Los inhibidores de la síntesis de andrógenos son inhibidores enzimáticos que impiden la biosíntesis de andrógenos. [31] Este proceso ocurre principalmente en las gónadas y las glándulas suprarrenales , pero también ocurre en otros tejidos como la glándula prostática , la piel y los folículos pilosos . Estos fármacos incluyen aminoglutetimida, ketoconazol, [151] y acetato de abiraterona. [89] [31] [152] La aminoglutetimida inhibe la enzima de escisión de la cadena lateral del colesterol, también conocida como P450scc o CYP11A1, que es responsable de la conversión de colesterol en pregnenolona y, por extensión, de la producción de todas las hormonas esteroides, incluidos los andrógenos. [89] El ketoconazol y el acetato de abiraterona son inhibidores de la enzima CYP17A1, también conocida como 17α-hidroxilasa/17,20-liasa, que es responsable de la conversión de esteroides pregnanos en andrógenos, así como de la conversión de mineralocorticoides en glucocorticoides. [89] [31] Debido a que todos estos fármacos previenen la formación de glucocorticoides además de andrógenos, deben combinarse con un glucocorticoide como la prednisona para evitar la insuficiencia suprarrenal . [152] Un fármaco más nuevo actualmente en desarrollo para el tratamiento del cáncer de próstata, el seviteronel , es selectivo para la inhibición de la funcionalidad 17,20-liasa del CYP17A1 y, por esta razón, a diferencia de los fármacos anteriores, no requiere un tratamiento concomitante con un glucocorticoide. [153]
Inhibidores de la 5α-reductasa
Los inhibidores de la 5α-reductasa, como la finasterida y la dutasterida, son inhibidores de la 5α-reductasa , una enzima responsable de la formación de DHT a partir de testosterona. [154] La DHT es entre 2,5 y 10 veces más potente que la testosterona como andrógeno [155] y se produce de manera selectiva en función del tejido en función de la expresión de la 5α-reductasa. [156] Los tejidos en los que la DHT se forma a un ritmo elevado incluyen la glándula prostática , la piel y los folículos pilosos . [41] [156] De acuerdo con esto, la DHT está implicada en la fisiopatología de la hiperplasia prostática benigna, la pérdida de cabello de patrón y el hirsutismo, y los inhibidores de la 5α-reductasa se utilizan para tratar estas afecciones. [41] [156] [157]
Antigonadotropinas
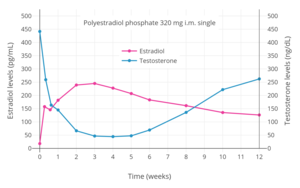

Las antigonadotropinas son fármacos que suprimen la secreción de gonadotropinas mediada por GnRH de la glándula pituitaria . [91] Las gonadotropinas incluyen la hormona luteinizante (LH) y la hormona folículo estimulante (FSH) y son hormonas peptídicas que envían señales a las gónadas para que produzcan hormonas sexuales . Al suprimir la secreción de gonadotropina, las antigonadotropinas suprimen la producción de hormonas sexuales gonadales y, por extensión, los niveles circulantes de andrógenos. [91] Los moduladores de GnRH , incluidos tanto los agonistas de GnRH como los antagonistas de GnRH , son antigonadotropinas potentes que pueden suprimir los niveles de andrógenos en un 95% en los hombres. [160] Además, los estrógenos y los progestágenos son antigonadotropinas a través del ejercicio de retroalimentación negativa en el eje hipotálamo-hipofisario-gonadal (eje HPG). [2] [93] [161] Los estrógenos en dosis altas pueden suprimir los niveles de andrógenos hasta niveles de castración en los hombres de manera similar a los moduladores de GnRH, [162] mientras que los progestágenos en dosis altas pueden suprimir los niveles de andrógenos hasta aproximadamente un 70 a 80% en los hombres. [163] [164]
Los ejemplos de agonistas de GnRH incluyen leuprorelina (leuprolida) y goserelina , mientras que un ejemplo de un antagonista de GnRH es cetrorelix . [92] Los estrógenos que se usan o se han usado como antigonadotropinas incluyen estradiol, ésteres de estradiol como valerato de estradiol , undecilato de estradiol y fosfato de poliestradiol , estrógenos conjugados, etinilestradiol, dietilestilbestrol (ya no se usa ampliamente) y bifluranol . [165] [166] Los progestágenos que se usan como antigonadotropinas incluyen acetato de clormadinona , acetato de ciproterona, caproato de gestonorona, [167] caproato de hidroxiprogesterona , acetato de medroxiprogesterona, acetato de megestrol y oxendolona. [2] [168] [169]
Misceláneas
Moduladores de globulina transportadora de hormonas sexuales
Además de sus efectos antigonadotrópicos, los estrógenos también son antiandrógenos funcionales al disminuir las concentraciones libres de andrógenos al aumentar la producción hepática de globulina transportadora de hormonas sexuales (SHBG) y, por extensión, los niveles circulantes de SHBG. [170] [171] [172] Se ha descubierto que los anticonceptivos orales combinados que contienen etinilestradiol aumentan los niveles circulantes de SHBG de 2 a 4 veces en mujeres y reducen las concentraciones de testosterona libre de 40 a 80%. [171] Sin embargo, se ha descubierto que los anticonceptivos orales combinados que contienen la progestina particularmente androgénica levonorgestrel aumentan los niveles de SHBG solo de 50 a 100%, [171] lo que probablemente se debe a que la activación del AR en el hígado tiene el efecto opuesto al estrógeno y suprime la producción de SHBG. [173] El levonorgestrel y otras progestinas 19-nortestosterona utilizadas en anticonceptivos orales combinados como la noretisterona también se unen directamente a los andrógenos de la SHBG y los desplazan, lo que puede antagonizar adicionalmente los efectos antiandrogénicos funcionales del etinilestradiol. [173] [174] En hombres, un estudio encontró que el tratamiento con una dosis relativamente baja de 20 μg/día de etinilestradiol durante 5 semanas aumentó los niveles circulantes de SHBG en un 150% y, debido a la disminución acompañante de los niveles de testosterona libre, aumentó los niveles circulantes totales de testosterona en un 50% (a través de la retroalimentación negativa reducida de los andrógenos en el eje HPG). [170]
Moduladores de globulina transportadora de corticosteroides
Los estrógenos en dosis altas pueden suprimir parcialmente la producción de andrógenos suprarrenales. [175] [176] [177] [178] [179] [180] Un estudio encontró que el tratamiento con una dosis alta de etinilestradiol (100 μg/día) redujo los niveles de los principales andrógenos suprarrenales circulantes en un 27 a 48% en mujeres transgénero . [175] [176] [177] La disminución de los andrógenos suprarrenales con estrógenos es evidente con estrógenos orales y sintéticos como el etinilestradiol y el fosfato de estramustina , pero es mínima con formas de estradiol bioidénticas parenterales como el fosfato de poliestradiol . [179] Se cree que está mediado por un mecanismo hepático , probablemente un aumento de la producción y los niveles de globulina transportadora de corticosteroides (CBG) y cambios compensatorios en la producción de esteroides suprarrenales (p. ej., derivación de la síntesis de andrógenos suprarrenales a la producción de cortisol ). [179] [180] Es notable a este respecto que los estrógenos orales y sintéticos, debido al primer paso oral y la resistencia al metabolismo hepático , tienen influencias mucho más fuertes en la síntesis de proteínas hepáticas que el estradiol parenteral. [181] La disminución de los niveles de andrógenos suprarrenales con la terapia de estrógenos en dosis altas puede ser beneficiosa en el tratamiento del cáncer de próstata . [177] [180]
Anticorticotropinas
Las anticorticotropinas como los glucocorticoides y mineralocorticoides funcionan ejerciendo retroalimentación negativa sobre el eje hipotálamo-hipofisario-suprarrenal (eje HPA), inhibiendo así la secreción de la hormona liberadora de corticotropina (CRH) y, por lo tanto, la hormona adrenocorticotrópica (ACTH; corticotropina) y, en consecuencia, suprimiendo la producción de prohormonas andrógenas como la dehidroepiandrosterona (DHEA), el sulfato de dehidroepiandrosterona (DHEA-S) y la androstenediona en la glándula suprarrenal . [182] [183] Rara vez se utilizan clínicamente como antiandrógenos funcionales, pero se utilizan como tales en el caso de hiperplasia suprarrenal congénita en niñas y mujeres, en las que hay una producción y niveles excesivos de andrógenos suprarrenales debido a la deficiencia de glucocorticoides y, por lo tanto, la hiperactividad del eje HPA. [182] [183]
Sensibilizadores de insulina
En las mujeres con resistencia a la insulina , como aquellas con síndrome de ovario poliquístico , los niveles de andrógenos suelen estar elevados. [184] La metformina , un medicamento sensibilizante a la insulina , tiene efectos antiandrogénicos indirectos en dichas mujeres, disminuyendo los niveles de testosterona hasta en un 50% debido a sus efectos beneficiosos sobre la sensibilidad a la insulina. [184] [185] [186]
Inmunógenos y vacunas
La albúmina de ovandrótono (Fecundin, Ovastim) y Androvax (albúmina de androstenediona) son inmunógenos y vacunas contra la androstenediona que se utilizan en medicina veterinaria para mejorar la fecundidad (tasa reproductiva) en ovejas (ovejas hembras adultas). [187] [188] Se cree que la generación de anticuerpos contra la androstenediona por estos agentes disminuye los niveles circulantes de androstenediona y sus metabolitos (p. ej., testosterona y estrógenos), lo que a su vez aumenta la actividad del eje HPG a través de una retroalimentación negativa reducida y aumenta la tasa de ovulación , lo que resulta en una mayor fertilidad y fecundidad. [187] [188]
Química
Los antiandrógenos se pueden dividir en varios tipos diferentes según su estructura química , incluidos los antiandrógenos esteroides , los antiandrógenos no esteroides y los péptidos . Los antiandrógenos esteroides incluyen compuestos como acetato de ciproterona , espironolactona , estradiol , acetato de abiraterona y finasterida ; los antiandrógenos no esteroides incluyen compuestos como bicalutamida , elagolix , dietilestilbestrol , aminoglutetimida y ketoconazol ; y los péptidos incluyen análogos de GnRH como leuprorelina y cetrorelix . [ cita requerida ]
Historia
Las antigonadotropinas como los estrógenos y los progestágenos se introdujeron por primera vez en la década de 1930. [189] Los efectos beneficiosos de la privación de andrógenos a través de la castración quirúrgica o la terapia de estrógenos en dosis altas sobre el cáncer de próstata se descubrieron en 1941. [31] : 56 [190] Los antagonistas de AR se descubrieron por primera vez a principios de la década de 1960. [96] El antiandrógeno esteroide acetato de ciproterona se descubrió en 1961 y se introdujo en 1973. y a menudo se describe como el primer antiandrógeno que se comercializó. [191] [62] Sin embargo, la espironolactona se introdujo en 1959., [192] [193] aunque sus efectos antiandrógenos no se reconocieron ni se aprovecharon hasta más tarde y originalmente fueron una acción no deseada fuera del objetivo del fármaco. [194] Además de la espironolactona, el acetato de clormadinona y el acetato de megestrol son antiandrógenos esteroides que son más débiles que el acetato de ciproterona, pero que también se introdujeron antes, en la década de 1960. [195] [196] [197] Otros antiandrógenos esteroides tempranos que se desarrollaron en esta época pero que nunca se comercializaron incluyen benorterona (SKF-7690; 17α-metil- B -nortestosterona), BOMT (Ro 7–2340), ciproterona (SH-80881) y trimetiltrienolona (R-2956). [198] [199]
El antiandrógeno no esteroide flutamida se informó por primera vez en 1967. [24] Se introdujo en 1983 y fue el primer antiandrógeno no esteroide comercializado. [200] [201] Otro antiandrógeno no esteroide temprano, [202] DIMP (Ro 7–8117), que está estructuralmente relacionado con la talidomida [203] y es un antiandrógeno relativamente débil, [204] [205] se describió por primera vez en 1973 y nunca se comercializó. [206] A la flutamida le siguió la nilutamida en 1989 y la bicalutamida en 1995. [207] Además de estos tres fármacos, que se han considerado antiandrógenos no esteroides de primera generación, se introdujeron los antiandrógenos no esteroides de segunda generación enzalutamida y apalutamida en 2012 y 2018. [208] [209] [210] Se diferencian de los antiandrógenos no esteroides anteriores en que son mucho más eficaces en comparación. [209]
Los inhibidores de la síntesis de andrógenos aminoglutetimida y ketoconazol se comercializaron por primera vez en 1960 y 1977, respectivamente, [211] [212] y el fármaco más nuevo, acetato de abiraterona, se introdujo en 2011. [213] Los moduladores de GnRH se introdujeron por primera vez en la década de 1980. [214] Los inhibidores de la 5α-reductasa finasterida y dutasterida se introdujeron en 1992 y 2002, respectivamente. [215] [216] Elagolix , el primer modulador de GnRH activo por vía oral que se comercializó, se introdujo en 2018. [217]
Cronología
La siguiente es una cronología de eventos en la historia de los antiandrógenos: [218]
- 1941: Hudgins y Hodges demuestran que la privación de andrógenos mediante terapia de estrógenos en dosis altas o castración quirúrgica trata el cáncer de próstata.
- 1957: Se sintetiza por primera vez el antiandrógeno esteroide espironolactona [219]
- 1960: La espironolactona se introduce por primera vez para uso médico, como antimineralocorticoide [219]
- 1961: Se sintetiza por primera vez el antiandrógeno esteroide acetato de ciproterona [220]
- 1962: Se informa por primera vez que la espironolactona produce ginecomastia en hombres [219] [221]
- 1966: La benorterona es el primer antiandrógeno conocido que se estudia clínicamente para tratar el acné y el hirsutismo en mujeres [222] [223]
- 1963: Se descubre la actividad antiandrogénica del acetato de ciproterona [48] [224]
- 1967: Se informa por primera vez que un antiandrógeno conocido, la benorterona, induce ginecomastia en hombres [222]
- 1967: Se sintetiza por primera vez el antiandrógeno no esteroide de primera generación, flutamida.
- 1967: El acetato de ciproterona se estudió clínicamente por primera vez para tratar la desviación sexual en hombres [225]
- 1969: El acetato de ciproterona se estudió por primera vez en el tratamiento del acné, el hirsutismo, la seborrea y la caída del cabello del cuero cabelludo en mujeres [226]
- 1969: Se descubre la actividad antiandrogénica de la espironolactona [227]
- 1972: Se informa por primera vez sobre la actividad antiandrogénica de la flutamida [228] [229]
- 1973: El acetato de ciproterona se introdujo por primera vez para uso médico, para tratar la desviación sexual [230]
- 1977: Se describe por primera vez el antiandrógeno de primera generación nilutamida [231]
- 1978: Se estudia por primera vez la espironolactona en el tratamiento del hirsutismo en mujeres [65] [232]
- 1979: Se estudia por primera vez el bloqueo androgénico combinado [233] [234]
- 1980: Se logra por primera vez la castración médica mediante un análogo de GnRH [ cita requerida ]
- 1982: Se describe por primera vez el antiandrógeno de primera generación bicalutamida [235]
- 1982: Se desarrolla el bloqueo androgénico combinado para el cáncer de próstata.
- 1983: Se introduce por primera vez la flutamida en Chile para uso médico, para tratar el cáncer de próstata [236] [237]
- 1987: La nilutamida se introduce por primera vez en Francia para uso médico, para tratar el cáncer de próstata [207]
- 1989: Se descubre que el bloqueo androgénico combinado a través de flutamida y un análogo de GnRH es superior a un análogo de GnRH solo para el cáncer de próstata.
- 1989: La flutamida se introduce por primera vez para uso médico en los Estados Unidos, para tratar el cáncer de próstata [238]
- 1989: Se estudia por primera vez la flutamida en el tratamiento del hirsutismo en mujeres [9]
- 1992: Se describe por primera vez el inhibidor de la síntesis de andrógenos acetato de abiraterona [239]
- 1995: Se introduce por primera vez la bicalutamida para uso médico, para tratar el cáncer de próstata [207]
- 1996: La nilutamida se introduce por primera vez para uso médico en los Estados Unidos, para tratar el cáncer de próstata [240]
- 2006: Se describe por primera vez el antiandrógeno no esteroideo de segunda generación enzalutamida [241]
- 2007: Se describe por primera vez el antiandrógeno no esteroide de segunda generación apalutamida [242]
- 2011: Se introduce por primera vez el acetato de abiraterona para uso médico, para tratar el cáncer de próstata [243]
- 2012: Se introduce por primera vez la enzalutamida para uso médico, para tratar el cáncer de próstata [244]
- 2018: Apalutamide se introduce por primera vez para uso médico, para tratar el cáncer de próstata [245]
- 2018: Elagolix es el primer antagonista de GnRH activo por vía oral que se introduce para uso médico [217]
- 2019: Relugolix es el segundo antagonista de GnRH activo por vía oral que se introduce para uso médico [246]
Sociedad y cultura
Etimología
El término antiandrógeno se utiliza generalmente para referirse específicamente a los antagonistas de AR, como lo describe Dorfman (1970): [247] [248]
Los antiandrógenos son sustancias que impiden que los andrógenos expresen su actividad en los sitios diana. Por lo tanto, el efecto inhibidor de estas sustancias debe diferenciarse de los compuestos que disminuyen la síntesis y/o liberación de factores hipotalámicos (liberadores), de las hormonas de la hipófisis anterior (gonadotropinas, en particular la hormona luteinizante) y del material que actúa directamente sobre las gónadas para inhibir la biosíntesis y/o secreción de andrógenos. [247] [248]
Sin embargo, a pesar de lo anterior, el término también puede usarse para describir antiandrógenos funcionales como inhibidores de la síntesis de andrógenos y antigonadotropinas, incluyendo incluso estrógenos y progestágenos. [2] [6] [249] Por ejemplo, el progestágeno y, por lo tanto, antigonadotropina, acetato de medroxiprogesterona, a veces se describe como un antiandrógeno esteroide, aunque no sea un antagonista del AR. [250] [249]
Investigación
Administración tópica
La precisión fáctica de esta sección puede verse comprometida debido a información desactualizada . El motivo es el siguiente: la FDA aprobó la clascoterona para el acné en agosto de 2020 y se considera muy eficaz (>= tretinoína al 0,05 %). ( abril de 2024 ) |
Ha habido mucho interés y esfuerzo en el desarrollo de antagonistas tópicos de AR para tratar afecciones dependientes de andrógenos como el acné y la pérdida de cabello de patrón en hombres. [251] Desafortunadamente, mientras que la administración sistémica de antiandrógenos es muy efectiva en el tratamiento de estas afecciones, se ha encontrado decepcionantemente que la administración tópica generalmente posee una efectividad limitada y solo modesta, incluso cuando se han empleado antagonistas esteroidales de AR de alta afinidad como el acetato de ciproterona y la espironolactona. [251] Además, en el caso específico del tratamiento del acné, se ha encontrado que los antagonistas tópicos de AR son mucho menos efectivos en comparación con los tratamientos establecidos como el peróxido de benzoilo y los antibióticos . [251]
Se han desarrollado diversos antagonistas de AR para uso tópico, pero no han completado su desarrollo y, por lo tanto, nunca se han comercializado. Estos incluyen los antagonistas de AR esteroides clascoterona , ciproterona , rosterolona y topterona y los antagonistas de AR no esteroides cioteronel , acetato de inocoterona , RU-22930 , RU-58642 y RU-58841 . Sin embargo, un antagonista de AR tópico, topilutamida (fluridil), se ha introducido en algunos países europeos para el tratamiento de la pérdida de cabello de patrón en hombres. [40] Además, un inhibidor tópico de la 5α-reductasa y estrógeno débil, alfatradiol , también se ha introducido en algunos países europeos para la misma indicación, aunque su eficacia es controvertida. [40] La espironolactona se ha comercializado en Italia en forma de crema tópica bajo la marca Spiroderm para el tratamiento del acné y el hirsutismo, pero esta formulación se suspendió y, por lo tanto, ya no está disponible. [252]
Anticoncepción masculina
Los antiandrógenos, como el acetato de ciproterona, se han estudiado para su uso potencial como anticonceptivos hormonales masculinos . [253] [254] [255] [256] [65] [257] [258] [259] Si bien son eficaces para suprimir la fertilidad masculina , su uso como monoterapias está impedido por los efectos secundarios, como la deficiencia de andrógenos (p. ej., desmasculinización , disfunción sexual , sofocos , osteoporosis ) y la feminización (p. ej., ginecomastia ). [65] [257] [258] [260] La combinación de una antigonadotropina primaria como el acetato de ciproterona para prevenir la fertilidad y un andrógeno como la testosterona para prevenir la deficiencia sistémica de andrógenos, lo que resulta en una acción antiandrogénica selectiva a nivel local en los testículos, se ha estudiado ampliamente y ha mostrado resultados prometedores, pero no ha sido aprobada para uso clínico en este momento. [258] [259] [261] [262] [260] El undecanoato de dimetandrolona (nombre en código de desarrollo CDB-4521), un AAS dual y progestágeno activo por vía oral , está bajo investigación como un posible anticonceptivo masculino y como la primera píldora anticonceptiva masculina . [263] [264]
Cáncer de mama
Los antiandrógenos como bicalutamida , enzalutamida y acetato de abiraterona están bajo investigación para el posible tratamiento del cáncer de mama , incluido el cáncer de mama triple negativo que expresa AR y otros tipos de cáncer de mama que expresan AR. [265] [266] [267] [268] [269]
Misceláneas
Los antiandrógenos pueden ser eficaces en el tratamiento del trastorno obsesivo-compulsivo . [270]
Véase también
- Síndrome de insensibilidad a los andrógenos
- Antiandrógenos en el medio ambiente
- Terapia de reemplazo de andrógenos
Referencias
- ^ Mowszowicz I (1989). "Antiandrógenos. Mecanismos y efectos paradójicos". Ann. Endocrinol . 50 (3). París: 50(3):189–99. PMID 2530930.
- ^ abcdef Brueggemeier RW (2006). "Hormonas sexuales (masculinas): análogos y antagonistas". Enciclopedia de biología celular molecular y medicina molecular . Wiley-VCH Verlag GmbH & Co. KGaA. doi :10.1002/3527600906.mcb.200500066. ISBN 3527600906.
- ^ Nath JL (2006). Uso de la terminología médica: un enfoque práctico . Lippincott Williams & Wilkins. pp. 977–. ISBN 978-0-7817-4868-1.
- ^ abcde Student S, Hejmo T, Poterała-Hejmo A, Leśniak A, Bułdak R (enero de 2020). "Terapia hormonal antiandrogénica para el cáncer y otras enfermedades". Eur. J. Pharmacol . 866 : 172783. doi : 10.1016/j.ejphar.2019.172783 . PMID 31712062.
- ^ Gillatt D (2006). "Tratamientos antiandrógenos en el cáncer de próstata localmente avanzado: ¿son todos iguales?". J Cancer Res Clin Oncol . 1 : S17-26. doi :10.1007/s00432-006-0133-5. PMID 16845534. S2CID 23888640.
- ^ abcdefgh Lieberman R (2001). "Terapia de privación de andrógenos para la quimioprevención del cáncer de próstata: estado actual y direcciones futuras para el desarrollo de agentes". Urología . 58 (2 Suppl 1): 83–90. doi :10.1016/s0090-4295(01)01247-x. PMID 11502457.
Existen varias clases de antiandrógenos, entre ellos (1) antigonadotropinas (p. ej., agonistas/antagonistas de LHRH, estrógenos sintéticos [dietilestilbestrol]); (2) antagonistas no esteroides del receptor de andrógenos (p. ej., flutamida, bicalutamida, nilutamida); (3) agentes esteroides con acciones mixtas (p. ej., acetato de ciproterona); (4) inhibidores de andrógenos suprarrenales (p. ej., ketoconazol, hidrocortisona); (5) agentes esteroides que inhiben la biosíntesis de andrógenos (por ejemplo, inhibidores de la 5α-reductasa (tipo II) e inhibidores de la 5α-reductasa de doble acción); [...]
- ^ abc Schröder FH, Radlmaier A (2009). "Antiandrógenos esteroides". En Jordan VC, Furr BA (eds.). Terapia hormonal en cáncer de mama y próstata . Humana Press. págs. 325–346. doi :10.1007/978-1-59259-152-7_15. ISBN 978-1-60761-471-5.
- ^ abc Kolvenbag GJ, Furr BJ (2009). "Antiandrógenos no esteroideos". En Jordan VC, Furr BJ (eds.). Terapia hormonal en cáncer de mama y próstata . Humana Press. págs. 347–368. doi :10.1007/978-1-59259-152-7_16. ISBN 978-1-60761-471-5.
- ^ abcd Sciarra F, Toscano V, Concolino G, Di Silverio F (noviembre de 1990). "Antiandrógenos: aplicaciones clínicas". Revista de bioquímica de esteroides y biología molecular . 37 (3): 349–362. doi :10.1016/0960-0760(90)90484-3. PMID 2147859. S2CID 20274398.
- ^ Broderick GA, Kadioglu A, Bivalacqua TJ, Ghanem H, Nehra A, Shamloul R (enero de 2010). "Priapismo: patogénesis, epidemiología y tratamiento". The Journal of Sexual Medicine . 7 (1 Pt 2): 476–500. doi :10.1111/j.1743-6109.2009.01625.x. PMID 20092449.
- ^ Steinberg MH, Forget BG, Higgs DR, Weatherall DJ (17 de agosto de 2009). Trastornos de la hemoglobina: genética, fisiopatología y tratamiento clínico. Cambridge University Press. pp. 476–. ISBN 978-1-139-48080-2.
- ^ abc Essah PA, Wickham EP, Nunley JR, Nestler JE (2006). "Dermatología de los trastornos relacionados con los andrógenos". Clinics in Dermatology . 24 (4): 289–298. doi :10.1016/j.clindermatol.2006.04.004. PMID 16828411.
- ^ abcdefgh Rabe T, Grunwald K, Feldmann K, Runnebaum B (2009). "Tratamiento del hiperandrogenismo en mujeres". Endocrinología ginecológica . 10 (sup3): 1–44. doi :10.3109/09513599609045658. ISSN 0951-3590.
- ^ abcd Bockting W, Coleman E, De Cuypere G (2011). "Atención a personas transexuales". N. Engl. J. Med . 364 (26): 2559–60, respuesta del autor 2560. doi :10.1056/NEJMc1104884. PMID 21714669.
- ^ ab Vance SR, Ehrensaft D, Rosenthal SM (2014). "Atención médica y psicológica de jóvenes no conformes con su género" (PDF) . Pediatría . 134 (6): 1184–92. doi :10.1542/peds.2014-0772. PMID 25404716. S2CID 5743822. Archivado (PDF) desde el original el 2018-05-15 . Consultado el 2018-05-14 .
- ^ abcdefgh Wadosky KM, Koochekpour S (2016). "Fundamentos terapéuticos, avances, fracasos y direcciones futuras para el cáncer de próstata avanzado". Int. J. Biol. Sci . 12 (4): 409–26. doi :10.7150/ijbs.14090. PMC 4807161. PMID 27019626 .
- ^ ab Massard C, Fizazi K (2011). "Apuntando a la señalización continua del receptor de andrógenos en el cáncer de próstata". Clin. Cancer Res . 17 (12): 3876–83. doi : 10.1158/1078-0432.CCR-10-2815 . PMID 21680543.
- ^ Msaouel P, Diamanti E, Tzanela M, Koutsilieris M (2007). "Antagonistas de la hormona liberadora de hormona luteinizante en el tratamiento del cáncer de próstata". Expert Opin Emerg Drugs . 12 (2): 285–99. doi :10.1517/14728214.12.2.285. PMID 17604502. S2CID 41988320.
- ^ ab Akaza H (enero de 2011). "Bloqueo androgénico combinado para el cáncer de próstata: revisión de eficacia, seguridad y relación coste-efectividad". Cancer Science . 102 (1): 51–6. doi : 10.1111/j.1349-7006.2010.01774.x . PMID 21091846. S2CID 38486547.
- ^ Mateo J, Smith A, Ong M, de Bono JS (2014). "Nuevos fármacos dirigidos a la vía del receptor de andrógenos en el cáncer de próstata". Cancer Metastasis Rev . 33 (2–3): 567–79. doi :10.1007/s10555-013-9472-2. PMID 24390422. S2CID 13980764.
- ^ abcd Iversen P, Melezinek I, Schmidt A (2001). "Antiandrógenos no esteroides: una opción terapéutica para pacientes con cáncer de próstata avanzado que desean conservar el interés y la función sexual". BJU Int . 87 (1): 47–56. doi : 10.1046/j.1464-410x.2001.00988.x . PMID 11121992. S2CID 28215804.
- ^ Kolvenbag GJ, Iversen P, Newling DW (agosto de 2001). "Monoterapia con antiandrógenos: una nueva forma de tratamiento para pacientes con cáncer de próstata". Urología . 58 (2 Suppl 1): 16–23. doi :10.1016/s0090-4295(01)01237-7. PMID 11502439.
- ^ Mcleod DG (2003). "Terapia hormonal: perspectiva histórica para futuras direcciones". Urología . 61 (2 Suppl 1): 3–7. doi :10.1016/s0090-4295(02)02393-2. PMID 12667881.
- ^ ab Smith HJ, Williams H (10 de octubre de 2005). Introducción a los principios del diseño y la acción de los fármacos, de Smith y Williams, cuarta edición. CRC Press. pp. 489–. ISBN 978-0-203-30415-0.
- ^ Chabner BA, Longo DL (8 de noviembre de 2010). Quimioterapia y bioterapia contra el cáncer: principios y práctica. Lippincott Williams & Wilkins. págs. 679–680. ISBN 978-1-60547-431-1. Archivado desde el original el 10 de enero de 2023 . Consultado el 27 de diciembre de 2016 .
Desde un punto de vista estructural, los antiandrógenos se clasifican como esteroides, incluida la ciproterona [acetato] (Androcur) y el megestrol [acetato], o no esteroides, incluida la flutamida (Eulexin, otros), la bicalutamida (Casodex) y la nilutamida (Nilandron). Los antiandrógenos esteroides rara vez se utilizan.
- ^ Kaliks RA, Del Giglio A (2008). "Manejo del cáncer de próstata avanzado" (PDF) . Revista de la Asociación Médica Brasileira . 54 (2): 178–82. doi : 10.1590/S0104-42302008000200025 . PMID 18506331. Archivado (PDF) desde el original el 10 de mayo de 2017 . Consultado el 27 de diciembre de 2016 .
- ^ Chang S (10 de marzo de 2010), Bicalutamide BPCA Drug Use Review in the Pediatric Population (PDF) , Departamento de Salud y Servicios Humanos de EE. UU. , archivado (PDF) del original el 24 de octubre de 2016 , consultado el 20 de julio de 2016
- ^ Gulley JL (2011). Cáncer de próstata. Demos Medical Publishing. pp. 81–. ISBN 978-1-935281-91-7.
- ^ Lutz M (1 de enero de 2008). Controversias en el tratamiento del cáncer de próstata. Karger Medical and Scientific Publishers. págs. 41-42. ISBN 978-3-8055-8524-8Archivado desde el original el 12 de enero de 2023 . Consultado el 27 de diciembre de 2016 .
- ^ Cáncer de próstata. Demos Medical Publishing. 20 de diciembre de 2011. pp. 505–. ISBN 978-1-935281-91-7.
- ^ abcdefghij Figg W, Chau CH, Small EJ (14 de septiembre de 2010). Tratamiento farmacológico del cáncer de próstata. Springer Science & Business Media. págs. 71–72, 75, 91–96. ISBN 978-1-60327-829-4.
- ^ ab Rittmaster RS (2011). "Quimioprevención del cáncer de próstata". Acta Oncol . 50 (Supl 1): 127–36. doi : 10.3109/0284186X.2010.527367 . PMID 21604953.
- ^ Mackenzie IS, Morant SV, Wei L, Thompson AM, MacDonald TM (2016). "Uso de espironolactona y riesgo de cánceres incidentales: un estudio de cohorte retrospectivo emparejado". Br J Clin Pharmacol . 83 (3): 653–663. doi :10.1111/bcp.13152. PMC 5306481 . PMID 27735065.
- ^ Hembree WC, Cohen-Kettenis P, Delemarre-van de Waal HA, Gooren LJ, Meyer WJ, Spack NP, Tangpricha V, Montori VM (2009). "Tratamiento endocrino de personas transexuales: una guía de práctica clínica de la Endocrine Society". J.Clin. Endocrinol. Metab . 94 (9): 3132–54. doi : 10.1210/jc.2009-0345 . PMID 19509099.
- ^ Gooren L, Morgentaler A (2014). "Incidencia de cáncer de próstata en personas transexuales de hombre a mujer orquidectomizadas tratadas con estrógenos". Andrologia . 46 (10): 1156–60. doi : 10.1111/and.12208 . PMID 24329588. S2CID 1445627.
- ^ Turo R, Jallad S, Prescott S, Cross WR (2013). "Cáncer de próstata metastásico en transexuales diagnosticado después de tres décadas de terapia con estrógenos". Can Urol Assoc J . 7 (7–8): E544–6. doi :10.5489/cuaj.175. PMC 3758950 . PMID 24032068.
- ^ ab Dörsam J, Altwein J (2009). "Tratamiento de enfermedades prostáticas con inhibidores de la 5alfa-reductasa: antecedentes e implicaciones prácticas". Cáncer de próstata Dis . 12 (2): 130–6. doi : 10.1038/pcan.2008.56 . PMID 19030020.
- ^ Ishizuka O, Nishizawa O, Hirao Y, Ohshima S (2002). "Metaanálisis basado en evidencia de la farmacoterapia para la hipertrofia prostática benigna". Int. J. Urol . 9 (11): 607–12. doi : 10.1046/j.1442-2042.2002.00539.x . PMID: 12534901. S2CID : 8249363.
- ^ Raspé G, Brosig W (22 de octubre de 2013). Simposio internacional sobre el tratamiento del carcinoma de próstata, Berlín, 13 al 15 de noviembre de 1969: Life Science Monographs. Elsevier. pp. 165–. ISBN 978-1-4831-8711-2.
- ^ abc Trüeb RM, Lee WS (13 de febrero de 2014). Alopecia masculina: guía para una gestión exitosa. Springer Science & Business Media. págs. 91–93. ISBN 978-3-319-03233-7.
- ^ abc Bolognia JL, Jorizzo JL, Rapini RP (2003). Dermatología. Gulf Professional Publishing. págs. 1072–. ISBN 9789997638991.
- ^ ab Simpson NB (1989). "El efecto de los fármacos en el cabello". Farmacología de la piel II . Manual de farmacología experimental. Vol. 87 / 2. Springer. págs. 495–508. doi :10.1007/978-3-642-74054-1_37. ISBN 978-3-642-74056-5. ISSN 0171-2004.
- ^ ab Unger WP (1 de febrero de 1995). "Alopecia androgenética y su tratamiento. Una visión histórica". Trasplante de cabello (tercera edición). Taylor & Francis. págs. 1–33. ISBN 978-0-8247-9363-0.
- ^ ab Rasmusson GH (1986). Capítulo 18. Control químico de la acción de los andrógenos . Informes anuales en química medicinal. Vol. 21. Academic Press. págs. 179-188. doi :10.1016/S0065-7743(08)61128-8. ISBN 9780120405213. ISSN 0065-7743.
- ^ ab Cormane RH, van der Meeren HL (1981). "Ciproteronacetato en el tratamiento del acné severo en varones". Archivos de investigación dermatológica . 271 (2): 183–187. doi :10.1007/BF00412545. ISSN 0340-3696. S2CID 12153042.
- ^ Giltay EJ, Gooren LJ (2009). "Posibles efectos secundarios del tratamiento de privación de andrógenos en delincuentes sexuales". Revista de la Academia Estadounidense de Psiquiatría y Derecho . 37 (1): 53–58. PMID 19297634.
- ^ Lam SM, Hempstead BR, Williams EF (2012). "Opciones de tratamiento médico para la pérdida del cabello". Medicina estética . Springer. págs. 529–535. doi :10.1007/978-3-642-20113-4_41. ISBN 978-3-642-20112-7.
- ^ ab Neumann F (1996). "Farmacología del acetato de ciproterona: una breve reseña". Antiandrógenos en el cáncer de próstata . págs. 31–44. doi :10.1007/978-3-642-45745-6_3. ISBN 978-3-642-45747-0.
- ^ Coskey RJ (julio de 1984). "Terapia dermatológica: diciembre de 1982 a noviembre de 1983". Revista de la Academia Estadounidense de Dermatología . 11 (1): 25–52. doi :10.1016/S0190-9622(84)80163-2. PMID 6376557.
- ^ Plewig G, Kligman AM (6 de diciembre de 2012). ACNÉ y ROSÁCEA. Springer Science & Business Media. pp. 687–. ISBN 978-3-642-59715-2.
- ^ Alldredge BK, Corelli RL, Ernst ME (1 de febrero de 2012). Koda-Kimble y Young's Applied Therapeutics: The Clinical Use of Drugs. Lippincott Williams & Wilkins. pp. 952–. ISBN 978-1-60913-713-7.
- ^ Ward A, Brogden RN, Heel RC, Speight TM, Avery GS (julio de 1984). "Isotretinoína. Una revisión de sus propiedades farmacológicas y eficacia terapéutica en el acné y otros trastornos de la piel". Drugs . 28 (1): 6–37. doi :10.2165/00003495-198428010-00002. PMID 6235105.
- ^ Misch KJ, Dolman WF, Neild V, Rhodes EL (1986). "Respuesta del acné masculino a la terapia antiandrogénica con acetato de ciproterona". Dermatologica . 173 (3): 139–142. doi :10.1159/000249236. PMID 2945742.
- ^ Kircik LH (julio de 2019). "Novedades en el tratamiento del acné vulgar". Cutis . 104 (1): 48–52. PMID 31487336. Archivado desde el original el 26 de octubre de 2020 . Consultado el 30 de marzo de 2020 .
- ^ Hassoun LA, Chahal DS, Sivamani RK, Larsen LN (junio de 2016). "El uso de agentes hormonales en el tratamiento del acné". Seminarios en Medicina y Cirugía Cutánea . 35 (2): 68–73. doi :10.12788/j.sder.2016.027 (inactivo 2024-09-01). PMID 27416311.
{{cite journal}}: CS1 maint: DOI inactivo a partir de septiembre de 2024 ( enlace ) - ^ "Cassiopea recibe la aprobación de la FDA para Winlevi® (crema de clascoterona al 1 %), el primer tratamiento tópico para el acné dirigido al receptor de andrógenos - Cassiopea". 28 de agosto de 2020. Archivado desde el original el 28 de agosto de 2020. Consultado el 15 de abril de 2024 .
- ^ "Drugs@FDA: Medicamentos aprobados por la FDA". www.accessdata.fda.gov . Consultado el 15 de abril de 2024 .
- ^ Jones RE, Lopez KH (28 de septiembre de 2013). Biología reproductiva humana. Academic Press. pp. 77–. ISBN 978-0-12-382185-0.
- ^ ab Bradford JM (2001). "La neurobiología, neurofarmacología y tratamiento farmacológico de las parafilias y la conducta sexual compulsiva". Can J Psychiatry . 46 (1): 26–34. doi : 10.1177/070674370104600104 . PMID 11221487.
- ^ ab Guay DR (2009). "Tratamiento farmacológico de los trastornos sexuales parafílicos y no parafílicos". Clin Ther . 31 (1): 1–31. doi :10.1016/j.clinthera.2009.01.009. PMID 19243704.
- ^ Marshall WL, Laws DR, Barbaree HE (21 de noviembre de 2013). Manual de agresión sexual: problemas, teorías y tratamiento del agresor. Springer Science & Business Media. pp. 297–. ISBN 978-1-4899-0915-2.
- ^ ab Stunkard AJ, Baum A (1989). Comer, dormir y sexo. Psychology Press. pp. 209–. ISBN 978-0-8058-0280-1.
- ^ Phenix A, Hoberman HM (7 de diciembre de 2015). Delito sexual: antecedentes predisponentes, evaluación y tratamiento. Springer. pp. 759–. ISBN 978-1-4939-2416-5.
- ^ abcd Brito VN, Latronico AC, Arnhold IJ, Mendonça BB (febrero de 2008). "Actualización sobre la etiología, diagnóstico y manejo terapéutico de la precocidad sexual". Arq Bras Endocrinol Metabol . 52 (1): 18–31. doi : 10.1590/S0004-27302008000100005 . PMID 18345393.
- ^ abcde Tindall DJ, Chang CH, Lobl TJ, Cunningham GR (1984). "Antagonistas de andrógenos en tejidos diana de andrógenos". Pharmacol. Ther . 24 (3): 367–400. doi :10.1016/0163-7258(84)90010-x. PMID 6205409.
- ^ Namer M (octubre de 1988). "Aplicaciones clínicas de los antiandrógenos". J. Steroid Biochem . 31 (4B): 719–29. doi :10.1016/0022-4731(88)90023-4. PMID 2462132.
- ^ ab Fraser HM, Baird DT (febrero de 1987). "Aplicaciones clínicas de los análogos de LHRH". Baillière's Clin. Endocrinol. Metab . 1 (1): 43–70. doi :10.1016/S0950-351X(87)80052-6. PMID 3109366.
- ^ Laron Z, Kauli R (julio de 2000). "Experiencia con acetato de ciproterona en el tratamiento de la pubertad precoz". J. Pediatr. Endocrinol. Metab . 13 (Supl. 1): 805–10. doi :10.1515/jpem.2000.13.s1.805. PMID 10969925. S2CID 25398066.
- ^ Neumann F, Kalmus J (1991). "Acetato de ciproterona en el tratamiento de trastornos sexuales: base farmacológica y experiencia clínica". Exp. Clin. Endocrinol . 98 (2): 71–80. doi :10.1055/s-0029-1211103. PMID 1838080.
- ^ ab Holland FJ (marzo de 1991). "Pubertad precoz independiente de gonadotropina". Endocrinol. Metab. Clin. North Am . 20 (1): 191–210. doi :10.1016/s0889-8529(18)30288-3. PMID 1903104.
- ^ ab Reiter EO, Norjavaara E (diciembre de 2005). "Testotoxicosis: punto de vista actual". Pediatr Endocrinol Rev. 3 (2): 77–86. PMID 16361981.
- ^ Levey HR, Kutlu O, Bivalacqua TJ (2012). "Manejo médico del priapismo tartamudo isquémico: una revisión contemporánea de la literatura". Revista asiática de andrología . 14 (1): 156–63. doi :10.1038/aja.2011.114. PMC 3753435 . PMID 22057380.
- ^ Broderick GA, Kadioglu A, Bivalacqua TJ, Ghanem H, Nehra A, Shamloul R (2010). "Priapismo: patogénesis, epidemiología y tratamiento". Revista de Medicina Sexual . 7 (1 Pt 2): 476–500. doi :10.1111/j.1743-6109.2009.01625.x. PMID 20092449.
- ^ Chow K, Payne S (2008). "El tratamiento farmacológico de los estados priapísmicos intermitentes". BJU International . 102 (11): 1515–21. doi : 10.1111/j.1464-410X.2008.07951.x . PMID 18793304. S2CID 35399393.
- ^ Dahm P, Rao DS, Donatucci CF (2002). "Antiandrógenos en el tratamiento del priapismo". Urología . 59 (1): 138. doi :10.1016/S0090-4295(01)01492-3. PMID 11796309.
- ^ Yuan J, Desouza R, Westney OL, Wang R (2008). "Información sobre el mecanismo del priapismo y fundamentos del tratamiento del priapismo recurrente". Revista asiática de andrología . 10 (1): 88–101. doi : 10.1111/j.1745-7262.2008.00314.x . PMID 18087648.
- ^ Baran R, Maibach HI (1 de octubre de 1998). Libro de texto de dermatología cosmética. CRC Press. pp. 388–. ISBN 978-1-85317-478-0.
- ^ Maibach HI, Gorouhi F (2011). Dermatología basada en evidencia. PMPH-USA. págs. 526–. ISBN 978-1-60795-039-4.
- ^ Williams H, Bigby M, Diepgen T, Herxheimer A, Naldi L, Rzany B (22 de enero de 2009). Dermatología basada en la evidencia. John Wiley e hijos. págs. 529–. ISBN 978-1-4443-0017-8Archivado desde el original el 10 de enero de 2023 . Consultado el 27 de diciembre de 2016 .
- ^ ab Erem C (2013). "Actualización sobre hirsutismo idiopático: diagnóstico y tratamiento". Acta Clin Belg . 68 (4): 268–74. doi :10.2143/ACB.3267. PMID 24455796. S2CID 39120534.
- ^ ab Becker KL (2001). Principios y práctica de endocrinología y metabolismo. Lippincott Williams & Wilkins. págs. 1004, 1196. ISBN 978-0-7817-1750-2.
- ^ abc Camacho PM, Gharib H, Sizemore GW (2012). Endocrinología basada en evidencia. Lippincott Williams & Wilkins. pp. 199–. ISBN 978-1-4511-1091-3.
- ^ Randolph JF (diciembre de 2018). "Terapia hormonal de afirmación de género para mujeres transgénero". Clin Obstet Gynecol . 61 (4): 705–721. doi :10.1097/GRF.0000000000000396. PMID 30256230. S2CID 52821192.
- ^ abcdefgh Singh SM, Gauthier S, Labrie F (febrero de 2000). "Antagonistas del receptor de andrógenos (antiandrógenos): relaciones estructura-actividad". Química medicinal actual . 7 (2): 211–247. doi :10.2174/0929867003375371. PMID 10637363.
- ^ abcd Shen HC, Taplin ME, Balk SP (2010). "Antagonistas del receptor de andrógenos". Tratamiento farmacológico del cáncer de próstata . Springer. págs. 71–81. doi :10.1007/978-1-60327-829-4_6. ISBN 978-1-60327-831-7.
- ^ Šauer P, Bořík A, Golovko O, Grabic R, Staňová AV, Valentová O, et al. (noviembre de 2018). "¿Las progestinas contribuyen a las actividades (anti) androgénicas en ambientes acuáticos?". Contaminación Ambiental . 242 (Parte A): 417–425. Código Bib : 2018EPoll.242..417S. doi :10.1016/j.envpol.2018.06.104. PMID 29990947. S2CID 51622914.
- ^ Raudrant D, Rabe T (2003). "Progestágenos con propiedades antiandrogénicas". Drugs . 63 (5): 463–492. doi :10.2165/00003495-200363050-00003. PMID 12600226. S2CID 28436828.
- ^ Schneider HP (noviembre de 2003). "Andrógenos y antiandrógenos". Anales de la Academia de Ciencias de Nueva York . 997 (1): 292–306. Bibcode :2003NYASA.997..292S. doi :10.1196/annals.1290.033. PMID 14644837. S2CID 8400556.
- ^ abcdef Strauss III JF, Barbieri RL (13 de septiembre de 2013). Endocrinología reproductiva de Yen y Jaffe. Ciencias de la Salud Elsevier. págs.90–. ISBN 978-1-4557-2758-2.
- ^ Aggarwal S, Thareja S, Verma A, Bhardwaj TR, Kumar M (2010). "Una descripción general de los inhibidores de la 5alfa-reductasa". Esteroides . 75 (2): 109–53. doi :10.1016/j.steroids.2009.10.005. PMID 19879888. S2CID 44363501.
- ^ abc Farmer PB, Walker JM (6 de diciembre de 2012). La base molecular del cáncer. Springer Science & Business Media. pp. 232–. ISBN 978-1-4684-7313-1.
- ^ abcdef Lemke TL, Williams DA (24 de enero de 2012). Principios de química medicinal de Foye. Lippincott Williams & Wilkins. págs. 228-231, 1371-1372. ISBN 978-1-60913-345-0.
- ^ abc de Lignières B, Silberstein S (abril de 2000). "Farmacodinamia de estrógenos y progestágenos". Cefalalgia: una revista internacional sobre dolores de cabeza . 20 (3): 200–7. doi : 10.1046/j.1468-2982.2000.00042.x . PMID 10997774. S2CID 40392817.
- ^ Ledger W, Schlaff WD, Vancaillie TG (11 de diciembre de 2014). Dolor pélvico crónico. Cambridge University Press. pp. 55–. ISBN 978-1-316-21414-5.
- ^ ab Hanna L, Crosby T, Macbeth F (19 de noviembre de 2015). Oncología clínica práctica. Cambridge University Press. pp. 37–. ISBN 978-1-107-68362-4.
- ^ ab Weber GF (22 de julio de 2015). Terapias moleculares del cáncer. Springer. pp. 314, 316. ISBN 978-3-319-13278-5.
- ^ Mahler C, Verhelst J, Denis L (mayo de 1998). "Farmacocinética clínica de los antiandrógenos y su eficacia en el cáncer de próstata". Clin Pharmacokinet . 34 (5): 405–17. doi :10.2165/00003088-199834050-00005. PMID 9592622. S2CID 25200595.
- ^ ab Thomas JA (12 de marzo de 1997). Toxicología endocrina, segunda edición. CRC Press. pp. 152–. ISBN 978-1-4398-1048-4Archivado desde el original el 11 de enero de 2023 . Consultado el 27 de diciembre de 2016 .
- ^ Anderson J (2003). "El papel de la monoterapia con antiandrógenos en el tratamiento del cáncer de próstata". BJU Int . 91 (5): 455–61. doi : 10.1046/j.1464-410x.2003.04026.x . PMID 12603397. S2CID 8639102.
- ^ Priestman T (26 de mayo de 2012). Quimioterapia contra el cáncer en la práctica clínica. Springer Science & Business Media. pp. 97–. ISBN 978-0-85729-727-3.
- ^ abc Higano CS (2003). "Efectos secundarios de la terapia de privación de andrógenos: seguimiento y minimización de la toxicidad". Urología . 61 (2 Suppl 1): 32–8. doi :10.1016/S0090-4295(02)02397-X. PMID 12667885.
- ^ Di Lorenzo G, Autorino R, Perdonà S, De Placido S (diciembre de 2005). "Manejo de la ginecomastia en pacientes con cáncer de próstata: una revisión sistemática". Lancet Oncol . 6 (12): 972–9. doi :10.1016/S1470-2045(05)70464-2. PMID 16321765.
- ^ Shapiro J (12 de noviembre de 2012). Trastornos del cabello: conceptos actuales en fisiopatología, diagnóstico y tratamiento, un número de Dermatologic Clinics. Elsevier Health Sciences. págs. 187–. ISBN 978-1-4557-7169-1.
- ^ Futterweit W (6 de diciembre de 2012). Enfermedad de ovario poliquístico. Springer Science & Business Media. pp. 282–. ISBN 978-1-4613-8289-8.
- ^ Katsambas AD, Dessinioti C (2010). "Terapia hormonal para el acné: ¿por qué no como terapia de primera línea? Hechos y controversias". Clin. Dermatol . 28 (1): 17–23. doi :10.1016/j.clindermatol.2009.03.006. PMID 20082945.
- ^ Baldani DP, Skrgatic L, Ougouag R, Kasum M (febrero de 2018). "El efecto cardiometabólico del tratamiento actual del síndrome de ovario poliquístico: estrategias de prevención y tratamiento". Gynecol Endocrinol . 34 (2): 87–91. doi :10.1080/09513590.2017.1381681. PMID 28944709. S2CID 205631980.
- ^ Nakhjavani M, Hamidi S, Esteghamati A, Abbasi M, Nosratian-Jahromi S, Pasalar P (octubre de 2009). "Efectos a corto plazo de la espironolactona en el perfil lipídico sanguíneo: un estudio de 3 meses en una cohorte de mujeres jóvenes con hirsutismo". Br J Clin Pharmacol . 68 (4): 634–7. doi :10.1111/j.1365-2125.2009.03483.x. PMC 2780289 . PMID 19843067.
- ^ Cignarella A, Mioni R, Sabbadin C, Dassie F, Parolin M, Vettor R, Barbot M, Scaroni C (diciembre de 2020). "Enfoques farmacológicos para controlar el riesgo cardiometabólico en mujeres con SOP". Int J Mol Sci . 21 (24): 9554. doi : 10.3390/ijms21249554 . PMC 7765466 . PMID 33334002.
- ^ Moretti C, Guccione L, Di Giacinto P, Simonelli I, Exacoustos C, Toscano V, Motta C, De Leo V, Petraglia F, Lenzi A (marzo de 2018). "Anticoncepción oral combinada y bicalutamida en el síndrome de ovario poliquístico y el hirsutismo severo: un ensayo controlado aleatorizado doble ciego". J. Clin. Endocrinol. Metab . 103 (3): 824–838. doi : 10.1210/jc.2017-01186 . PMID 29211888.
- ^ Coleman, E.; et al. (19 de agosto de 2022). "Estándares de atención para la salud de las personas transgénero y de género diverso, versión 8". Revista internacional de salud transgénero . 23 (Supl. 1): S1–S259. doi : 10.1080/26895269.2022.2100644 . ISSN 2689-5269. PMC 9553112 . PMID 36238954.
- ^ Godsland IF, Wynn V, Crook D, Miller NE (diciembre de 1987). "Sexo, lipoproteínas plasmáticas y aterosclerosis: suposiciones predominantes y preguntas pendientes". American Heart Journal . 114 (6): 1467–1503. doi :10.1016/0002-8703(87)90552-7. PMID 3318361.
- ^ Grundy SM, Stone NJ, Bailey AL, Beam C, Birtcher KK, Blumenthal RS, Braun LT, de Ferranti S, Faiella-Tommasino J, Forman DE, Goldberg R, Heidenreich PA, Hlatky MA, Jones DW, Lloyd-Jones D, Lopez-Pajares N, Ndumele CE, Orringer CE, Peralta CA, Saseen JJ, Smith SC, Sperling L, Virani SS, Yeboah J (junio de 2019). "Guía de 2018 de la AHA/ACC/AACVPR/AAPA/ABC/ACPM/ADA/AGS/APhA/ASPC/NLA/PCNA sobre el manejo del colesterol en sangre: un informe del grupo de trabajo sobre guías de práctica clínica del Colegio Estadounidense de Cardiología/Asociación Estadounidense del Corazón". Circulation . 139 (25): e1082–e1143. doi :10.1161/CIR.0000000000000625. PMC 7403606. PMID 30586774 .
- ^ ab Thole Z, Manso G, Salgueiro E, Revuelta P, Hidalgo A (2004). "Hepatotoxicidad inducida por antiandrógenos: una revisión de la literatura". Urol. Int . 73 (4): 289–95. doi :10.1159/000081585. PMID 15604569. S2CID 24799765.
- ^ Keating GM (marzo de 2015). "Enzalutamida: una revisión de su uso en el cáncer de próstata metastásico resistente a la castración sin quimioterapia previa". Drugs & Aging . 32 (3): 243–9. doi :10.1007/s40266-015-0248-y. PMID 25711765. S2CID 29563345.
- ^ ab Leppert PC, Peipert JF (2004). Atención primaria para mujeres. Lippincott Williams & Wilkins. pp. 277–. ISBN 978-0-7817-3790-6.
- ^ Rathus SA, Nevid JS, Fichner-Rathus L (2005). La sexualidad humana en un mundo de diversidad. Pearson Allyn y Bacon. p. 313. ISBN 978-0-205-40615-9Archivado desde el original el 26 de febrero de 2023. Consultado el 27 de diciembre de 2016 .
- ^ Moguilewsky M, Bouton MM (octubre de 1988). "Cómo el estudio de las actividades biológicas de los antiandrógenos puede orientarse hacia la clínica". Journal of Steroid Biochemistry . 31 (4B): 699–710. doi :10.1016/0022-4731(88)90021-0. PMID 3059062.
- ^ Gaillard-Moguilewsky M (1991). "Farmacología de los antiandrógenos y valor de combinar la supresión androgénica con la terapia antiandrogénica". Urología . 37 (2 Suppl): 5–12. doi :10.1016/0090-4295(91)80095-O. PMID 1992602.
- ^ Moguilewsky M, Fiet J, Tournemine C, Raynaud JP (enero de 1986). "Farmacología de un antiandrógeno, anandron, utilizado como terapia adyuvante en el tratamiento del cáncer de próstata". Journal of Steroid Biochemistry . 24 (1): 139–46. doi :10.1016/0022-4731(86)90043-9. PMID 3009970.
- ^ Teutsch G, Goubet F, Battmann T, Bonfils A, Bouchoux F, Cerede E, Gofflo D, Gaillard-Kelly M, Philibert D (enero de 1994). "Antiandrógenos no esteroideos: síntesis y perfil biológico de ligandos de alta afinidad para el receptor de andrógenos". Revista de bioquímica y biología molecular de esteroides . 48 (1): 111–9. doi :10.1016/0960-0760(94)90257-7. PMID 8136296. S2CID 31404295.
- ^ Raynaud JP, Fortin M, Hunt P, Ojasoo T, Doré JC, Surcouf E, Mornon JP (1986). "Enfoques para el desarrollo de fármacos utilizando receptores". En Gotto AM, O'Malley BW, Liliane FP (eds.). El papel de los receptores en biología y medicina: Actas del Noveno Simposio de Argenteuil. Raven Press. págs. 65–77. ISBN 978-0-88167-161-2.
- ^ Raynaud JP, Ojasoo T, Labrie F (1981). "Hormonas esteroides: agonistas y antagonistas". Mecanismos de acción de los esteroides . Macmillan Education UK. págs. 145-158. doi :10.1007/978-1-349-81345-2_11. ISBN . 978-1-349-81347-6.
- ^ Raynaud JP, Bouton MM, Moguilewsky M, Ojasoo T, Philibert D, Beck G, Labrie F, Mornon JP (enero de 1980). "Receptores de hormonas esteroides y farmacología". Journal of Steroid Biochemistry . 12 : 143–57. doi :10.1016/0022-4731(80)90264-2. PMID 7421203.
- ^ Ojasoo T, Raynaud JP (noviembre de 1978). «Unique steroid congeners for receptor studies» (Congéneres esteroides únicos para estudios de receptores). Cancer Research . 38 (11 Pt 2): 4186–98. PMID 359134. Archivado desde el original el 27 de noviembre de 2020. Consultado el 31 de octubre de 2021 .
- ^ Raynaud JP, Bonne C, Bouton MM, Moguilewsky M, Philibert D, Azadian-Boulanger G (mayo de 1975). "Detección de antihormonas mediante estudios de receptores". Journal of Steroid Biochemistry . 6 (5): 615–22. doi :10.1016/0022-4731(75)90042-4. PMID 171505.
- ^ Hanada K, Furuya K, Yamamoto N, Nejishima H, Ichikawa K, Nakamura T, Miyakawa M, Amano S, Sumita Y, Oguro N (noviembre de 2003). "Efectos anabólicos óseos de S-40503, un nuevo modulador selectivo del receptor de andrógenos no esteroides (SARM), en modelos de osteoporosis en ratas". Biol. Farmacéutica. Toro . 26 (11): 1563–9. doi : 10.1248/bpb.26.1563 . PMID 14600402.
- ^ abcde Poyet P, Labrie F (octubre de 1985). "Comparación de las actividades antiandrogénicas/androgénicas de la flutamida, el acetato de ciproterona y el acetato de megestrol". Endocrinología molecular y celular . 42 (3): 283–8. doi :10.1016/0303-7207(85)90059-0. PMID 3930312. S2CID 24746807.
- ^ Luthy IA, Begin DJ, Labrie F (1988). "Actividad androgénica de progestinas sintéticas y espironolactona en células de carcinoma mamario de ratón (Shionogi) sensibles a los andrógenos en cultivo". Journal of Steroid Biochemistry . 31 (5): 845–52. doi :10.1016/0022-4731(88)90295-6. PMID 2462135.
- ^ Sundar S, Dickinson PD (2012). "La espironolactona, un posible modulador selectivo del receptor de andrógenos, debe utilizarse con precaución en pacientes con carcinoma metastásico de próstata". BMJ Case Rep . 2012 : bcr1120115238. doi : 10.1136 /bcr.11.2011.5238. PMC 3291010. PMID 22665559.
- ^ Flynn T, Guancial EA, Kilari M, Kilari D (2016). "Informe de caso: retirada de espironolactona asociada a una respuesta drástica en un paciente con cáncer de próstata metastásico resistente a la castración". Clin Genitourin Cancer . 15 (1): e95–e97. doi :10.1016/j.clgc.2016.08.006. PMID 27641657. S2CID 38441469.
- ^ James VH, Pasqualini JR (22 de octubre de 2013). Esteroides hormonales: Actas del Sexto Congreso Internacional sobre Esteroides Hormonales. Elsevier Science. pp. 391–. ISBN 978-1-4831-9067-9.
- ^ ab Caubet JF, Tosteson TD, Dong EW, Naylon EM, Whiting GW, Ernstoff MS, Ross SD (1997). "Bloqueo máximo de andrógenos en el cáncer de próstata avanzado: un metaanálisis de ensayos controlados aleatorios publicados que utilizan antiandrógenos no esteroideos". Urología . 49 (1): 71–8. doi :10.1016/S0090-4295(96)00325-1. PMID 9000189.
Debido a que los antiandrógenos esteroideos como el acetato de ciproterona tienen una actividad androgénica intrínseca y una actividad antiandrogénica menor que los NSAA como la flutamida y la nilutamida,39–43 no es sorprendente que las dos clases de antiandrógenos puedan tener diferentes eficacias.
- ^ abc Singh SM, Gauthier S, Labrie F (febrero de 2000). "Antagonistas del receptor de andrógenos (antiandrógenos): relaciones estructura-actividad". Química medicinal actual . 7 (2): 211–47. doi :10.2174/0929867003375371. PMID 10637363.
- ^ abcd Ayub M, Levell MJ (agosto de 1989). "El efecto de los fármacos imidazólicos relacionados con el ketoconazol y los antiandrógenos sobre la unión de [3H] R 1881 al receptor de andrógenos prostáticos y la unión de [3H]5 alfa-dihidrotestosterona y [3H]cortisol a las proteínas plasmáticas". J. Steroid Biochem . 33 (2): 251–5. doi :10.1016/0022-4731(89)90301-4. PMID 2788775.
- ^ ab Yamasaki K, Sawaki M, Noda S, Muroi T, Takakura S, Mitoma H, Sakamoto S, Nakai M, Yakabe Y (2004). "Comparación del ensayo de Hershberger y el ensayo de unión al receptor de andrógenos de doce sustancias químicas". Toxicología . 195 (2–3): 177–86. Código Bib : 2004Toxgy.195..177Y. doi :10.1016/j.tox.2003.09.012. PMID 14751673.
- ^ Pratt WB (1994). Los fármacos contra el cáncer. Oxford University Press. pp. 220–. ISBN 978-0-19-506739-2En pacientes que reciben flutamida en la dosis habitual de 250 mg cada 8 horas, la concentración plasmática mínima de hidroxiflutamida es de aproximadamente 5 uM, que es 5.000 veces la concentración plasmática de testosterona (1 nM) en pacientes tratados con un
agonista de LHRH.127 Como la hidroxiflutamida es sólo un uno por ciento tan potente como la testosterona en la competencia por la unión al receptor de andrógenos,126 se requiere un nivel plasmático de 5 uM de hidroxiflutamida para asegurar una competencia efectiva.127 [...] Se ha demostrado que tanto el acetato de ciproterona como la flutamida son una terapia eficaz (aproximadamente equivalente a un estrógeno) cuando se utilizan solos en el tratamiento del carcinoma de próstata.123
- ^ Bennett NC, Gardiner RA, Hooper JD, Johnson DW, Gobe GC (2010). "Biología celular molecular de la señalización del receptor de andrógenos". Int. J. Biochem. Cell Biol . 42 (6): 813–27. doi :10.1016/j.biocel.2009.11.013. PMID 19931639.
- ^ Wang C, Liu Y, Cao JM (2014). "Receptores acoplados a proteína G: mediadores extranucleares para las acciones no genómicas de los esteroides". Int J Mol Sci . 15 (9): 15412–25. doi : 10.3390/ijms150915412 . PMC 4200746 . PMID 25257522.
- ^ Lang F, Alevizopoulos K, Stournaras C (2013). "Ataque a receptores de andrógenos de membrana en tumores". Opinión de expertos. Objetivos terapéuticos . 17 (8): 951–63. doi :10.1517/14728222.2013.806491. PMID 23746222. S2CID 23918273.
- ^ ab Pescovitz OH, Eugster EA (2004). Endocrinología pediátrica: mecanismos, manifestaciones y tratamiento. Lippincott Williams & Wilkins. págs. 248–. ISBN 978-0-7817-4059-3.
- ^ ab Buonocore G, Bracci R, Weindling M (28 de enero de 2012). Neonatología: un enfoque práctico para las enfermedades neonatales. Springer Science & Business Media. pp. 1012–. ISBN 978-88-470-1405-3.
- ^ Jordan-Young RM (7 de enero de 2011). Brain Storm. Harvard University Press. pp. 82–. ISBN 978-0-674-05879-8.
- ^ Blakemore JE, Berenbaum SA, Liben LS (13 de mayo de 2013). Gender Development. Psychology Press. pp. 115–. ISBN 978-1-135-07932-1.
- ^ Maggi M (30 de enero de 2012). Terapia hormonal para la disfunción sexual masculina. John Wiley & Sons. pp. 6–. ISBN 978-0-470-65760-7.
- ^ abcde Imamura Y, Sadar MD (agosto de 2016). "Terapias dirigidas al receptor de andrógenos en el cáncer de próstata resistente a la castración: desde el laboratorio hasta la clínica". Revista internacional de urología . 23 (8): 654–665. doi :10.1111/iju.13137. PMC 6680212 . PMID 27302572.
- ^ De Mol E, Fenwick RB, Phang CT, Buzón V, Szulc E, de la Fuente A, et al. (septiembre de 2016). "EPI-001, un compuesto activo contra el cáncer de próstata resistente a la castración, se dirige a la unidad de transactivación 5 del receptor de andrógenos". ACS Chemical Biology . 11 (9): 2499–2505. doi :10.1021/acschembio.6b00182. PMC 5027137 . PMID 27356095.
- ^ Martinez-Ariza G, Hulme C (2015). "Avances recientes en inhibidores alostéricos del receptor de andrógenos para el posible tratamiento del cáncer de próstata resistente a la castración". Pharmaceutical Patent Analyst . 4 (5): 387–402. doi :10.4155/ppa.15.20. PMID 26389532.
- ^ ab Lai AC, Crews CM (febrero de 2017). "Degradación de proteínas inducida: un paradigma emergente en el descubrimiento de fármacos". Nature Reviews. Descubrimiento de fármacos . 16 (2): 101–114. doi :10.1038/nrd.2016.211. PMC 5684876. PMID 27885283 .
- ^ ab Lai KP, Huang CK, Chang YJ, Chung CY, Yamashita S, Li L, et al. (febrero de 2013). "Nuevo enfoque terapéutico para suprimir el cáncer de próstata resistente a la castración utilizando ASC-J9 mediante la focalización del receptor de andrógenos en células de próstata selectivas". The American Journal of Pathology . 182 (2): 460–473. doi :10.1016/j.ajpath.2012.10.029. PMC 3562731 . PMID 23219429.
- ^ "ASCJ 9". AdisInsight . Springer Nature Switzerland AG. Archivado desde el original el 4 de marzo de 2018. Consultado el 24 de diciembre de 2017 .
- ^ Witjes FJ, Debruyne FM, Fernandez del Moral P, Geboers AD (mayo de 1989). "Dosis altas de ketoconazol en el tratamiento de pacientes con cáncer de próstata metastásico progresivo tratados con hormonas. Dutch South-Eastern Urological Cooperative Group". Urología . 33 (5): 411–5. doi :10.1016/0090-4295(89)90037-X. PMID 2652864.
- ^ ab Held-Warmkessel J (2006). Cuestiones contemporáneas en el cáncer de próstata: una perspectiva de enfermería. Jones & Bartlett Learning. págs. 275–. ISBN 978-0-7637-3075-8.
- ^ Bird IM, Abbott DH (2016). "La búsqueda de un inhibidor selectivo de la 17,20 liasa; lecciones aprendidas de la naturaleza". J. Steroid Biochem. Mol. Biol . 163 : 136–46. doi :10.1016/j.jsbmb.2016.04.021. PMC 5046225. PMID 27154414 .
- ^ Flores E, Bratoeff E, Cabeza M, Ramirez E, Quiroz A, Heuze I (mayo de 2003). "Inhibidores de la 5alfa-reductasa esteroide". Mini-Revisiones en Química Medicinal . 3 (3): 225–37. doi :10.2174/1389557033488196. PMID 12570838.
- ^ Mozayani A, Raymon L (18 de septiembre de 2011). Manual de interacciones farmacológicas: una guía clínica y forense. Springer Science & Business Media. pp. 656–. ISBN 978-1-61779-222-9.
- ^ abc Bhagavan NV (2002). Bioquímica médica. Academic Press. págs. 787–. ISBN 978-0-12-095440-7.
- ^ Hirshburg JM, Kelsey PA, Therrien CA, Gavino AC, Reichenberg JS (2016). "Efectos adversos y seguridad de los inhibidores de la 5-alfa reductasa (Finasterida, Dutasterida): una revisión sistemática". J Clin Aesthet Dermatol . 9 (7): 56–62. PMC 5023004 . PMID 27672412.
- ^ Stege R, Gunnarsson PO, Johansson CJ, Olsson P, Pousette A, Carlström K (1996). "Farmacocinética y supresión de testosterona de una dosis única de fosfato de poliestradiol (Estradurina) en pacientes con cáncer de próstata". Próstata . 28 (5): 307–10. doi :10.1002/(SICI)1097-0045(199605)28:5<307::AID-PROS6>3.0.CO;2-8. PMID 8610057. S2CID 33548251.
- ^ Fourcade RO, McLeod D (2015). "Tolerabilidad de los antiandrógenos en el tratamiento del cáncer de próstata". UroOncology . 4 (1): 5–13. doi :10.1080/1561095042000191655. ISSN 1561-0950.
- ^ Urotext (1 de enero de 2001). Urotext-Luts: Urología. Urotext. pp. 71–. ISBN 978-1-903737-03-3Archivado desde el original el 11 de enero de 2023. Consultado el 27 de diciembre de 2016 .
- ^ Neumann F (1978). "La acción fisiológica de la progesterona y los efectos farmacológicos de los progestágenos: una breve revisión". Revista Médica de Postgrado . 54 (Supl. 2): 11–24. PMID 368741.
- ^ Jacobi GH, Altwein JE, Kurth KH, Basting R, Hohenfellner R (1980). "Tratamiento del cáncer de próstata avanzado con acetato de ciproterona parenteral: un ensayo aleatorizado de fase III". Br J Urol . 52 (3): 208–15. doi :10.1111/j.1464-410x.1980.tb02961.x. PMID 7000222.
- ^ Wein AJ, Kavoussi LR, Novick AC, Partin AW, Peters CA (25 de agosto de 2011). Urología de Campbell-Walsh: Expert Consult Premium Edition: funciones mejoradas en línea e impresa, conjunto de 4 volúmenes. Elsevier Health Sciences. págs. 2938–. ISBN 978-1-4160-6911-9Archivado desde el original el 11 de enero de 2023 . Consultado el 27 de diciembre de 2016 .
- ^ Kjeld JM, Puah CM, Kaufman B, Loizou S, Vlotides J, Gwee HM, Kahn F, Sood R, Joplin GF (1979). "Efectos de la ingestión de norgestrel y etinilestradiol sobre los niveles séricos de hormonas sexuales y gonadotropinas en hombres". Endocrinología Clínica . 11 (5): 497–504. doi :10.1111/j.1365-2265.1979.tb03102.x. PMID 519881. S2CID 5836155.
- ^ Norman G, Dean ME, Langley RE, Hodges ZC, Ritchie G, Parmar MK, Sydes MR, Abel P, Eastwood AJ (2008). "Estrógenos parenterales en el tratamiento del cáncer de próstata: una revisión sistemática". Br. J. Cancer . 98 (4): 697–707. doi :10.1038/sj.bjc.6604230. PMC 2259178 . PMID 18268497.
- ^ Dekanski JB (1980). "Actividad antiprostática del bifluranol, un bibencilo fluorado". Br. J. Pharmacol . 71 (1): 11–6. doi :10.1111/j.1476-5381.1980.tb10903.x. PMC 2044395 . PMID 6258683.
- ^ Sander S, Nissen-Meyer R, Aakvaag A (1978). "Sobre el tratamiento con gestágenos del carcinoma prostático avanzado". Scand. J. Urol. Nephrol . 12 (2): 119–21. doi :10.3109/00365597809179977. PMID 694436.
- ^ Prentky RA, Burgess AW (31 de julio de 2000). Gestión forense de delincuentes sexuales. Springer Science & Business Media. pp. 219–. ISBN 978-0-306-46278-8.
- ^ Sudo K, Yamazaki I, Masuoka M, Nakayama R (1979). "Antiandrógeno TSAA-291. IV. Efectos del antiandrógeno TSAA-291 (16 beta-etil-17 beta-hidroxi-4-oestren-3-ona) en la secreción de gonadotropinas". Acta Endocrinol Suppl (Copenh) . 229 : 53–66. doi :10.1530/acta.0.092s053. PMID 294107.
- ^ ab Nieschlag E, Behre HM, Nieschlag S (26 de julio de 2012). Testosterona: acción, deficiencia, sustitución. Cambridge University Press. pp. 62–. ISBN 978-1-107-01290-5.
- ^ abc Grupo de trabajo del IARC sobre la evaluación de los riesgos carcinógenos para los seres humanos; Organización Mundial de la Salud; Agencia Internacional para la Investigación sobre el Cáncer (2007). Anticonceptivos combinados de estrógeno y progestágeno y terapia combinada de estrógeno y progestágeno para la menopausia. Organización Mundial de la Salud. pp. 157–. ISBN 978-92-832-1291-1.
- ^ Coss CC, Jones A, Parke DN, Narayanan R, Barrett CM, Kearbey JD, Veverka KA, Miller DD, Morton RA, Steiner MS, Dalton JT (2012). "Caracterización preclínica de un nuevo agonista selectivo de ERα de difenil benzamida para la terapia hormonal en el cáncer de próstata". Endocrinología . 153 (3): 1070–81. doi : 10.1210/en.2011-1608 . PMID 22294742.
- ^ ab Krishna UR, Sheriar NK (1 de enero de 2000). Ginecología del Adolescente (pb). Oriente Cisne Negro. págs.121–. ISBN 978-81-250-1793-6.
- ^ Filshie M, Guillebaud J (22 de octubre de 2013). Anticoncepción: ciencia y práctica. Elsevier Science. pp. 26–. ISBN 978-1-4831-6366-6.
- ^ ab Oettel M (1999). "Estrógenos y antiestrógenos en el varón". Estrógenos y antiestrógenos II . Manual de farmacología experimental. Vol. 135 / 2. Berlín, Heidelberg: Springer Berlin Heidelberg. págs. 505–571. doi :10.1007/978-3-642-60107-1_25. ISBN . 978-3-642-64261-6. ISSN 0171-2004.
- ^ ab Margioris AN, Chrousos GP (20 de abril de 2001). Trastornos suprarrenales. Springer Science & Business Media. pp. 84–. ISBN 978-1-59259-101-5.
- ^ abc Polderman KH, Gooren LJ, van der Veen EA (octubre de 1995). "Efectos de los andrógenos gonadales y los estrógenos en los niveles de andrógenos suprarrenales". Clin. Endocrinol. (Oxf) . 43 (4): 415–21. doi :10.1111/j.1365-2265.1995.tb02611.x. PMID 7586614. S2CID 6815423.
- ^ Stege R, Eriksson A, Henriksson P, Carlström K (agosto de 1987). "Orquidectomía o tratamiento con estrógenos en el cáncer de próstata: efectos sobre los niveles séricos de andrógenos suprarrenales y esteroides relacionados". Int. J. Androl . 10 (4): 581–7. doi : 10.1111/j.1365-2605.1987.tb00357.x . PMID 2958420.
- ^ abc Pousette A, Carlström K, Stege R (1989). "Andrógenos durante diferentes modos de tratamiento endocrino del cáncer de próstata". Urol. Res . 17 (2): 95–8. doi :10.1007/BF00262027. PMID 2734983. S2CID 25309877.
- ^ abc Cox RL, Crawford ED (diciembre de 1995). "Estrógenos en el tratamiento del cáncer de próstata". J. Urol . 154 (6): 1991–8. doi :10.1016/S0022-5347(01)66670-9. PMID 7500443.
- ^ von Schoultz B, Carlström K, Collste L, Eriksson A, Henriksson P, Pousette A, Stege R (1989). "Terapia con estrógenos y función hepática: efectos metabólicos de la administración oral y parenteral". Próstata . 14 (4): 389–95. doi :10.1002/pros.2990140410. PMID 2664738. S2CID 21510744.
- ^ ab Melmed S, Polonsky KS, Larsen PR, Kronenberg HM (12 de mayo de 2011). Williams Textbook of Endocrinology E-Book. Elsevier Health Sciences. págs. 753–. ISBN 978-1-4377-3600-7.
- ^ ab Kumar V, Abbas AK, Fausto N, Aster JC (10 de junio de 2009). Robbins & Cotran Pathologic Basis of Disease E-Book. Elsevier Health Sciences. págs. 1154–. ISBN 978-1-4377-2015-0.
- ^ ab Nikolakis G, Kyrgidis A, Zouboulis CC (agosto de 2019). "¿Tiene algún papel la terapia antiandrogénica en la hidradenitis supurativa? Una revisión sistemática de los datos publicados". American Journal of Clinical Dermatology . 20 (4): 503–513. doi :10.1007/s40257-019-00442-w. PMID 31073704. S2CID 149443722.
- ^ Patel R, Shah G (septiembre de 2017). "Efecto de la metformina en los resultados clínicos, metabólicos y endocrinos en mujeres con síndrome de ovario poliquístico: un metanálisis de ensayos controlados aleatorizados". Current Medical Research and Opinion . 33 (9): 1545–1557. doi :10.1080/03007995.2017.1279597. PMID 28058854. S2CID 4391302.
- ^ Guan Y, Wang D, Bu H, Zhao T, Wang H (2020). "El efecto de la metformina en el síndrome de ovario poliquístico en mujeres con sobrepeso: una revisión sistemática y un metaanálisis de ensayos controlados aleatorizados". Revista internacional de endocrinología . 2020 : 5150684. doi : 10.1155/2020/5150684 . PMC 7519180 . PMID 33014044.
- ^ ab Sreenan JM, Diskin MG (6 de diciembre de 2012). Mortalidad embrionaria en animales de granja. Springer Science & Business Media. pp. 172–. ISBN 978-94-009-5038-2.
- ^ ab Jindal SK, Sharma MC (2010). Biotecnología en la producción y salud animal. New India Publishing. pp. 77–. ISBN 978-93-80235-35-6.
- ^ Fritz MA, Speroff L (28 de marzo de 2012). Endocrinología ginecológica clínica e infertilidad. Lippincott Williams & Wilkins. págs. 750–751, 963. ISBN 978-1-4511-4847-3.
- ^ Kavoussi P, Costabile RA, Salonia A (17 de octubre de 2012). Endocrinología urológica clínica: principios para la salud masculina. Springer Science & Business Media. pp. 7–. ISBN 978-1-4471-4404-5.
- ^ Avances en la investigación de fármacos. Academic Press. 12 de agosto de 1997. pp. 34–. ISBN 978-0-08-052628-7.
- ^ Jugdutt BI (19 de febrero de 2014). Envejecimiento e insuficiencia cardíaca: mecanismos y tratamiento. Springer Science & Business Media. pp. 175–. ISBN 978-1-4939-0268-2Archivado desde el original el 11 de enero de 2023 . Consultado el 27 de diciembre de 2016 .
- ^ Wermuth CG (2 de mayo de 2011). La práctica de Murl=https://books.google.com/books?id=Qmt1_DQkCpEC&pg=PA34 . Academic Press. pp. 34–. ISBN 978-0-08-056877-5.
- ^ Azziz R (8 de noviembre de 2007). Trastornos por exceso de andrógenos en mujeres. Springer Science & Business Media. pp. 382–. ISBN 978-1-59745-179-6.
- ^ Runnebaum BC, Rabe T, Kiesel L (6 de diciembre de 2012). Anticoncepción femenina: actualización y tendencias. Springer Science & Business Media. pp. 136–. ISBN 978-3-642-73790-9.
- ^ Orfanos CE, Montagna W, Stüttgen G (6 de diciembre de 2012). Investigación capilar: situación y aspectos futuros; Actas del Primer Congreso Internacional sobre Investigación capilar, Hamburgo, 13-16 de marzo de 1979. Springer Science & Business Media. pp. 587-. ISBN 978-3-642-81650-5.
- ^ Marks L (2010). Química sexual: una historia de la píldora anticonceptiva. Yale University Press. pp. 76–78. ISBN 978-0-300-16791-7.
- ^ Horsky J, Presl J (6 de diciembre de 2012). Función ovárica y sus trastornos: diagnóstico y tratamiento. Springer Science & Business Media. pp. 112–. ISBN 978-94-009-8195-9.
- ^ Vitaminas y hormonas. Academic Press. 18 de mayo de 1976. pp. 682–. ISBN 978-0-08-086630-7.
- ^ Neal DE (6 de diciembre de 2012). Tumores en urología. Springer Science & Business Media. pp. 233–. ISBN 978-1-4471-2086-5.
- ^ Ottow E, Weinmann H (8 de septiembre de 2008). Receptores nucleares como dianas farmacológicas. John Wiley & Sons. págs. 255–. ISBN 978-3-527-62330-3.
- ^ Singhal RL, Thomas JA (1 de enero de 1976). Mecanismos celulares que modulan la acción gonadal. University Park Press. pág. 239. ISBN 978-0-8391-0776-7.
- ^ Liu B, Su L, Geng J, Liu J, Zhao G (octubre de 2010). "Desarrollos en antiandrógenos no esteroideos dirigidos al receptor de andrógenos". ChemMedChem . 5 (10): 1651–1661. doi :10.1002/cmdc.201000259. PMID 20853390. S2CID 23228778.
- ^ Heyns W, Verhoeven G, De Moor P (mayo de 1976). "Unión de andrógenos en el citosol del útero de rata. Estudio de la especificidad". Journal of Steroid Biochemistry . 7 (5): 335–343. doi :10.1016/0022-4731(76)90092-3. PMID 180344.
- ^ Informes anuales en química medicinal. Academic Press. 16 de septiembre de 1986. pp. 182–. ISBN 978-0-08-058365-5.
- ^ Boris A, Scott JW, DeMartino L, Cox DC (marzo de 1973). "Perfil endocrino de un antiandrógeno no esteroideo N-(3,5-dimetil-4-isoxazolilmetil)ftalimida (DIMP)". Acta Endocrinologica . 72 (3): 604–614. doi :10.1530/acta.0.0720604. PMID 4739363.
- ^ abc Bégué JP, Bonnet-Delpon D (2 de junio de 2008). Química bioorgánica y medicinal del flúor. John Wiley & Sons. pp. 327–. ISBN 978-0-470-28187-1Archivado desde el original el 12 de enero de 2023 . Consultado el 27 de diciembre de 2016 .
- ^ Menon MP, Higano CS (abril de 2013). "Enzalutamida, un antagonista del receptor de andrógenos de segunda generación: desarrollo y aplicaciones clínicas en el cáncer de próstata". Current Oncology Reports . 15 (2): 69–75. doi :10.1007/s11912-013-0293-9. PMID 23341368. S2CID 8725297.
- ^ ab Tran C, Ouk S, Clegg NJ, Chen Y, Watson PA, Arora V, et al. (mayo de 2009). "Desarrollo de un antiandrógeno de segunda generación para el tratamiento del cáncer de próstata avanzado". Science . 324 (5928): 787–790. Bibcode :2009Sci...324..787T. doi :10.1126/science.1168175. PMC 2981508 . PMID 19359544.
- ^ "La FDA aprueba un nuevo tratamiento para un determinado tipo de cáncer de próstata utilizando un nuevo criterio de valoración de un ensayo clínico". Administración de Alimentos y Medicamentos . 24 de marzo de 2020. Archivado desde el original el 23 de abril de 2019 . Consultado el 1 de abril de 2018 .
- ^ Sneader W (23 de junio de 2005). Descubrimiento de fármacos: una historia. John Wiley & Sons. págs. 367–. ISBN 978-0-471-89979-2.
- ^ Golan DE (2008). Principios de farmacología: la base fisiopatológica de la farmacoterapia. Lippincott Williams & Wilkins. pp. 624–. ISBN 978-0-7817-8355-2Archivado desde el original el 10 de enero de 2023. Consultado el 27 de diciembre de 2016 .
- ^ Cáncer de próstata. Demos Medical Publishing. 20 de diciembre de 2011. pp. 518–. ISBN 978-1-935281-91-7.
- ^ Bowsher W, Carter A (15 de abril de 2008). Desafíos en el cáncer de próstata. John Wiley & Sons. pp. 138–. ISBN 978-1-4051-7177-9.
- ^ Allahbadia G, Agrawal R, Merchant R (2007). Síndrome de ovario poliquístico. Anshan. págs. 184–. ISBN 978-1-904798-74-3.
- ^ Fronteras en química medicinal. Bentham Science Publishers. 2010. pp. 329–. ISBN 978-1-60805-208-0.
- ^ ab "Elagolix - Abbvie/Neurocrine Biosciences". AdisInsight . Springer Nature Switzerland AG. Archivado desde el original el 20 de septiembre de 2018. Consultado el 30 de julio de 2018 .
- ^ Crawford ED, Schellhammer PF, McLeod DG, Moul JW, Higano CS, Shore N, Denis L, Iversen P, Eisenberger MA, Labrie F (noviembre de 2018). "Tratamientos dirigidos al receptor de andrógenos para el cáncer de próstata: 35 años de progreso con antiandrógenos". J. Urol . 200 (5): 956–966. doi :10.1016/j.juro.2018.04.083. PMID 29730201. S2CID 19162538.
- ^ abc Kolkhof P, Bärfacker L (julio de 2017). "30 AÑOS DEL RECEPTOR DE MINERALOCORTICOIDES: Antagonistas del receptor de mineralocorticoides: 60 años de investigación y desarrollo". J. Endocrinol . 234 (1): T125–T140. doi :10.1530/JOE-16-0600. PMC 5488394 . PMID 28634268.
- ^ Pucci E, Petraglia F (diciembre de 1997). "Tratamiento del exceso de andrógenos en mujeres: ayer, hoy y mañana". Gynecol. Endocrinol . 11 (6): 411–33. doi :10.3109/09513599709152569. PMID 9476091.
- ^ Smith WG (1962). "Espironolactona y ginecomastia". The Lancet . 280 (7261): 886. doi :10.1016/S0140-6736(62)90668-2. ISSN 0140-6736.
- ^ ab Stewart ME, Pochi PE (abril de 1978). "Antiandrógenos y la piel". Int. J. Dermatol . 17 (3): 167–79. doi :10.1111/j.1365-4362.1978.tb06057.x. PMID 148431. S2CID 43649686.
- ^ Zarate A, Mahesh VB, Greenblatt RB (diciembre de 1966). "Efecto de un antiandrógeno, 17-alfa-metil-B-nortestosterona, sobre el acné y el hirsutismo". J. Clin. Endocrinol. Metab . 26 (12): 1394–8. doi :10.1210/jcem-26-12-1394. PMID 4225258.
- ^ Hamada H, Neumann F, Junkmann K (noviembre de 1963). "Intrauterine Antimaskuline Beeinflussung von Rattenfeten Durch ein Stark Gestagen Wirksames Steroid" [Influencia antimasculina intrauterina de fetos de rata por el nacimiento de un potente esteroide que actúa como progestágeno]. Acta Endocrinológica (en alemán). 44 (3): 380–388. doi :10.1530/acta.0.0440380. PMID 14071315.
- ^ Thibaut F, De La Barra F, Gordon H, Cosyns P, Bradford JM (junio de 2010). "Directrices de la Federación Mundial de Sociedades de Psiquiatría Biológica (WFSBP) para el tratamiento biológico de las parafilias". World J. Biol. Psychiatry . 11 (4): 604–55. doi :10.3109/15622971003671628. PMID 20459370. S2CID 14949511.
- ^ Hammerstein J, Cupceancu B (abril de 1969). "Behandlung des Hirsutismus mit Cyproteronacetat" [Manejo del hirsutismo mediante acetato de ciproterona]. Deutsche Medizinische Wochenschrift (en alemán). 94 (16): 829–34. doi :10.1055/s-0028-1111126. ISSN 0012-0472. PMID 4304873. S2CID 71214286.
- ^ Steelman SL, Brooks JR, Morgan ER, Patanelli DJ (1969). "Actividad antiandrogénica de la espironolactona". Esteroides . 14 (4): 449–50. doi :10.1016/s0039-128x(69)80007-3. PMID 5344274.
- ^ Neri R, Florance K, Koziol P, Van Cleave S (agosto de 1972). "Un perfil biológico de un antiandrógeno no esteroide, SCH 13521 (4'-nitro-3'trifluorometilisobutiranilida)". Endocrinología . 91 (2): 427–37. doi :10.1210/endo-91-2-427. PMID 4264731.
- ^ Neri RO, Monahan M (septiembre de 1972). "Efectos de un nuevo antiandrógeno no esteroideo en la hiperplasia prostática canina". Invest Urol . 10 (2): 123–30. PMID 4116667.
- ^ Neumann F (1994). "El antiandrógeno acetato de ciproterona: descubrimiento, química, farmacología básica, uso clínico y herramienta en la investigación básica". Exp. Clin. Endocrinol . 102 (1): 1–32. doi : 10.1055/s-0029-1211261 . PMID 8005205.
- ^ Raynaud JP, Bonne C, Bouton MM, Lagace L, Labrie F (1979). "Acción de un antiandrógeno no esteroide, RU 23908, en tejidos periféricos y centrales". J. Steroid Biochem . 11 (1A): 93–9. doi :10.1016/0022-4731(79)90281-4. PMID 385986.
- ^ Ober KP, Hennessy JF (1978). "Terapia con espironolactona para el hirsutismo en una mujer hiperandrogénica". Ann. Intern. Med . 89 (5 Pt 1): 643–4. doi :10.7326/0003-4819-89-5-643. PMID 717935.
- ^ Klotz L (mayo de 2006). "Bloqueo androgénico combinado: una actualización". Urol. Clin. North Am . 33 (2): 161–6, v–vi. doi :10.1016/j.ucl.2005.12.001. PMID 16631454.
- ^ Labrie F, Dupont A, Belanger A, Cusan L, Lacourciere Y, Monfette G, Laberge JG, Emond JP, Fazekas AT, Raynaud JP, Husson JM (1982). "Nueva terapia hormonal en el carcinoma prostático: tratamiento combinado con un agonista de LHRH y un antiandrógeno". Clin Invest Med . 5 (4): 267–75. PMID 6819101.
- ^ Engel J, Kleemann A, Kutscher B, Reichert D (2009). Sustancias farmacéuticas: síntesis, patentes y aplicaciones de los principios activos farmacéuticos más relevantes (5.ª ed.). Thieme. pp. 153–154. ISBN 978-3-13-179275-4.
- ^ William Andrew Publishing (22 de octubre de 2013). Pharmaceutical Manufacturing Encyclopedia, 3.ª edición. Elsevier. pp. 1695–. ISBN 978-0-8155-1856-3Archivado desde el original el 12 de enero de 2023 . Consultado el 2 de enero de 2019 .
- ^ The Irish Reports: Containing Reports of Cases Argued and Determined in the Court of Appeal, the High Court of Justice, the Court of Bankruptcy, in Ireland, and the Irish Land Commission. Incorporated Council of Law Reporting for Ireland. 1990. págs. 501–502. Archivado desde el original el 12 de enero de 2023. Consultado el 2 de enero de 2019 .
- ^ Regitz-Zagrosek V (2 de octubre de 2012). Diferencias de sexo y género en farmacología. Springer Science & Business Media. pp. 575–. ISBN 978-3-642-30725-6.
- ^ "Abiraterona: una historia de innovación científica y colaboración comercial - Instituto de Investigación del Cáncer, Londres". Archivado desde el original el 1 de enero de 2019. Consultado el 2 de enero de 2019 .
- ^ "Nilutamida". AdisInsight . Springer Nature Switzerland AG. Archivado desde el original el 5 de mayo de 2021 . Consultado el 2 de enero de 2019 .
- ^ Sawyers, C., Jung, M., Chen, C., Ouk, S., Welsbie, D., Tran, C., ... y Yoo, D. (2006). Solicitud de patente estadounidense n.º 11/433.829. https://patents.google.com/patent/US20070004753 [1]
- ^ "Espacenet - Documento original". Archivado desde el original el 4 de noviembre de 2021. Consultado el 2 de enero de 2019 .
- ^ "Acetato de abiraterona - Johnson & Johnson". AdisInsight . Springer Nature Switzerland AG. Archivado desde el original el 2019-01-03 . Consultado el 2019-01-02 .
- ^ "Enzalutamide - Astellas Pharma/Medivation". AdisInsight . Springer Nature Switzerland AG. Archivado desde el original el 17 de julio de 2018 . Consultado el 2 de enero de 2019 .
- ^ "Apalutamide - Investigación y desarrollo de Janssen". AdisInsight . Springer Nature Switzerland AG. Archivado desde el original el 2019-01-03 . Consultado el 2019-01-02 .
- ^ "Relugolix - Myovant/Takeda". AdisInsight . Springer Nature Switzerland AG. Archivado desde el original el 2021-08-19 . Consultado el 2021-08-19 .
- ^ ab Neumann F (enero de 1977). "Farmacología y uso potencial del acetato de ciproterona". Investigación hormonal y metabólica . 9 (1): 1–13. doi :10.1055/s-0028-1093574. PMID 66176. S2CID 7224893.
- ^ ab Dorfman RI (1970). "Actividad biológica de los antiandrógenos". British Journal of Dermatology . 82 (s6): 3. doi :10.1111/j.1365-2133.1970.tb07998.x. ISSN 0007-0963. S2CID 71393789.
- ^ ab Gräf KJ, Brotherton J, Neumann F (1974). "Usos clínicos de los antiandrógenos". Andrógenos II y Antiandrógenos / Andrógeno II y Antiandrógeno . Saltador. págs. 485–542. doi :10.1007/978-3-642-80859-3_7. ISBN 978-3-642-80861-6.
- ^ Vogelzang N (2006). Libro de texto completo de oncología genitourinaria. Lippincott Williams & Wilkins. págs. 316–. ISBN 978-0-7817-4984-8.
- ^ abc Helms RA, Quan DJ (2006). Libro de texto de terapéutica: manejo de fármacos y enfermedades. Lippincott Williams & Wilkins. págs. 211–. ISBN 978-0-7817-5734-8.
- ^ Farid NR, Diamanti-Kandarakis E (27 de febrero de 2009). Diagnóstico y tratamiento del síndrome de ovario poliquístico. Springer Science & Business Media. pp. 235–. ISBN 978-0-387-09718-3Archivado desde el original el 11 de enero de 2023 . Consultado el 30 de diciembre de 2016 .
- ^ Neumann F, Diallo FA, Hasan SH, Schenck B, Traore I (1976). "La influencia de los compuestos farmacéuticos en la fertilidad masculina". Andrologia . 8 (3): 203–35. doi : 10.1111/j.1439-0272.1976.tb02137.x . PMID 793446. S2CID 24859886.
- ^ Prasad MR, Rajalakshmi M (1976). "Sitios diana para la supresión de la fertilidad en el varón". Adv Sex Horm Res . 2 : 263–87. PMID 797248.
- ^ Ewing LL, Robaire B (1978). "Agentes antiespermatogénicos endógenos: perspectivas para la anticoncepción masculina". Annu. Rev. Pharmacol. Toxicol . 18 : 167–87. doi :10.1146/annurev.pa.18.040178.001123. PMID 206192.
- ^ Gombe S (abril de 1983). "Una revisión del estado actual de los estudios sobre anticoncepción masculina". East Afr Med J. 60 ( 4): 203–11. PMID 6354690.
- ^ ab Srivastava RP, Bhaduri AP (1989). "Conceptos emergentes hacia el desarrollo de agentes anticonceptivos". En Ernst Jucker (ed.). Avances en la investigación de fármacos . Avances en la investigación de medicamentos. Fortschritte der Arzneimittelforschung. Progres des Recherches Pharmaceutiques. vol. 33. Birkhäuser. págs. 267–315. doi :10.1007/978-3-0348-9146-2_9. ISBN 978-3-0348-9925-3. Número de identificación personal 2687939.
- ^ abc Wu FC (octubre de 1988). "Anticoncepción masculina: estado actual y perspectivas futuras". Clin. Endocrinol. (Oxf) . 29 (4): 443–65. doi :10.1111/j.1365-2265.1988.tb02894.x. PMID 3075164. S2CID 36608203.
- ^ ab Nieschlag E, Zitzmann M, Kamischke A (noviembre de 2003). "Uso de progestinas en la anticoncepción masculina". Esteroides . 68 (10–13): 965–72. doi :10.1016/s0039-128x(03)00135-1. PMID 14667989. S2CID 22458746.
- ^ ab Nieschlag E (2010). "Ensayos clínicos en anticoncepción hormonal masculina" (PDF) . Anticoncepción . 82 (5): 457–70. doi :10.1016/j.contraception.2010.03.020. PMID 20933120. Archivado (PDF) desde el original el 2020-12-05 . Consultado el 2019-07-08 .
- ^ Rajalakshmi M (noviembre de 2005). "Anticoncepción masculina: ampliación de la elección reproductiva". Indian J. Exp. Biol . 43 (11): 1032–41. PMID 16313066.
- ^ Chao JH, Page ST (julio de 2016). "El estado actual de la anticoncepción hormonal masculina". Pharmacol. Ther . 163 : 109–17. doi :10.1016/j.pharmthera.2016.03.012. PMID 27016468.
- ^ Attardi BJ, Hild SA, Reel JR (junio de 2006). "Undecanoato de dimetandrolona: un nuevo y potente andrógeno oralmente activo con actividad progestacional". Endocrinología . 147 (6): 3016–26. doi : 10.1210/en.2005-1524 . PMID 16497801.
- ^ Ayoub R, Page ST, Swerdloff RS, Liu PY, Amory JK, Leung A, Hull L, Blithe D, Christy A, Chao JH, Bremner WJ, Wang C (marzo de 2017). "Comparación de la farmacocinética, farmacodinámica y seguridad de dosis única de dos nuevas formulaciones orales de undecanoato de dimetandrolona (DMAU): un posible anticonceptivo oral masculino". Andrology . 5 (2): 278–285. doi :10.1111/andr.12303. PMC 5352517 . PMID 27907978.
- ^ Fioretti FM, Sita-Lumsden A, Bevan CL, Brooke GN (junio de 2014). "Revisión del papel del receptor de andrógenos en el cáncer de mama". J. Mol. Endocrinol . 52 (3): R257–65. doi : 10.1530/JME-14-0030 . PMID 24740738.
- ^ Gucalp A, Traina TA (2016). "Ataque al receptor de andrógenos en el cáncer de mama triple negativo". Curr Probl Cancer . 40 (2–4): 141–150. doi :10.1016/j.currproblcancer.2016.09.004. PMC 5580391 . PMID 27816190.
- ^ Arce-Salinas C, Riesco-Martinez MC, Hanna W, Bedard P, Warner E (febrero de 2016). "Respuesta completa del cáncer de mama metastásico con receptor de andrógenos positivo a la bicalutamida: informe de caso y revisión de la literatura". J. Clin. Oncol . 34 (4): e21–4. doi :10.1200/JCO.2013.49.8899. PMID 24888812.
- ^ Héquet D, Mzoughi S, Rouzier R, Guccione E (abril de 2017). «[Receptores de andrógenos en el cáncer de mama: expresión, valor y perspectivas terapéuticas]». Bull Cancer (en francés). 104 (4): 363–369. doi :10.1016/j.bulcan.2017.01.005. PMID 28216075.
- ^ Gerratana L, Basile D, Buono G, De Placido S, Giuliano M, Minichillo S, Coinu A, Martorana F, De Santo I, Del Mastro L, De Laurentiis M, Puglisi F, Arpino G (junio de 2018). "Receptor de andrógenos en el cáncer de mama triple negativo: un objetivo potencial para el subtipo sin objetivo". Tratamiento del cáncer. Rdo . 68 : 102-110. doi : 10.1016/j.ctrv.2018.06.005 . hdl : 11567/914067 . PMID 29940524.
- ^ Nomani H, Mohammadpour AH, Moallem SM, YazdanAbad MJ, Barreto GE, Sahebkar A (diciembre de 2019). "Fármacos antiandrógenos en el tratamiento del trastorno obsesivo-compulsivo: una revisión sistemática". Curr Med Chem . 27 (40): 6825–6836. doi :10.2174/0929867326666191209142209. PMID 31814547. S2CID 208956450.
Lectura adicional
- Neumann F, Steinbeck H (1974). "Antiandrógenos". Andrógenos II y Antiandrógenos / Andrógeno II y Antiandrógeno . Saltador. págs. 235–484. doi :10.1007/978-3-642-80859-3_6. ISBN 978-3-642-80861-6.
- Gräf KJ, Brotherton J, Neumann F (1974). "Usos clínicos de los antiandrógenos". Andrógenos II y antiandrógenos / Androgene II und Antiandrogene . Springer. págs. 485–542. doi :10.1007/978-3-642-80859-3_7. ISBN 978-3-642-80861-6.
