Oxendolona
 | |
| Datos clínicos | |
|---|---|
| Nombres comerciales | Prostetina, Roxenona |
| Otros nombres | TSAA-291; 16β-Etil-19-nortestosterona; 16β-Etilestr-4-en-17β-ol-3-ona |
| Vías de administración | Inyección intramuscular [1] [2] [3] [4] |
| Clase de droga | Antiandrógeno esteroide ; Progestágeno ; Progestina |
| Datos farmacocinéticos | |
| Biodisponibilidad | Oral : Muy baja (1% en perros) [5] |
| Vida media de eliminación | SOYInformación sobre herramientas Inyección intramuscular: 5,0–6,6 días. [4] [6] |
| Identificadores | |
| |
| Número CAS |
|
| Identificador de centro de PubChem |
|
| Araña química |
|
| UNIVERSIDAD |
|
| Panel de control CompTox ( EPA ) |
|
| Datos químicos y físicos | |
| Fórmula | C20H30O2 |
| Masa molar | 302,458 g·mol −1 |
| Modelo 3D ( JSmol ) |
|
| |
| |
La oxendolona , que se vende bajo las marcas Prostetin y Roxenone , es un medicamento antiandrógeno y progestágeno que se utiliza en Japón para el tratamiento del agrandamiento de la próstata . [7] [8] [9] [10] [11] Sin embargo, este uso es controvertido debido a las preocupaciones sobre su eficacia clínica. [11] La oxendolona no es eficaz por vía oral y debe administrarse mediante inyección en el músculo . [5] [1] [2] [3] [4]
La oxendolona es un antiandrógeno y, por lo tanto, es un antagonista del receptor de andrógenos , el objetivo biológico de los andrógenos como la testosterona y la dihidrotestosterona . [12] [13] [14] [15] [6] También es una progestina, o un progestágeno sintético , y por lo tanto es un agonista del receptor de progesterona , el objetivo biológico de los progestágenos como la progesterona . [12] [13] [14] [15] Debido a su actividad progestágena, la oxendolona tiene efectos antigonadotrópicos . [16] [17] La oxendolona no tiene otra actividad hormonal importante...
La oxendolona se introdujo para uso médico en 1981. [8] Se utiliza únicamente en Japón. [8] [11]
Usos médicos
La oxendolona se utiliza en el tratamiento de la hiperplasia prostática benigna (HPB) en Japón . [8] [11] Se ha utilizado en una dosis de 200 mg una vez cada 2 semanas mediante inyección intramuscular . [17] Aunque está aprobado para el tratamiento de la HPB en Japón, se han planteado inquietudes sobre su uso para esta afección debido a la poca eficacia observada en los ensayos clínicos . [11]
Efectos secundarios
Farmacología
Farmacodinamia
La oxendolona se une al receptor de andrógenos (K i = 320 nM) y al receptor de progesterona (K i = 20 nM) y actúa como un inhibidor débil pero clínicamente relevante de la 5α-reductasa ( IC 50Concentración inhibitoria máxima media en la descripción emergente= 1,4 μM). [12] [13] [14] [15] La afinidad de unión relativa de la oxendolona por el receptor de andrógenos es del 0,8 al 3,6% de la de la metribolona . [18] [19] La oxendolona no es un antagonista silencioso del receptor de andrógenos, sino que es predominantemente antagonista con una actividad agonista débil ; [13] por esta razón, se ha descrito como un modulador selectivo del receptor de andrógenos . [20] El medicamento tiene potentes efectos antigonadotrópicos a través de su actividad progestágena. [16] Se ha descubierto que suprime los niveles de hormona luteinizante y testosterona en un grado equivalente al alilestrenol y el acetato de clormadinona , que son dos progestinas que se utilizan de forma similar en dosis altas para tratar la HBP. [17]
Farmacocinética
La biodisponibilidad oral de la oxendolona en perros es extremadamente baja, 1% como máximo. [5] Debido a su baja biodisponibilidad oral, la oxendolona se administra por inyección intramuscular en humanos. [1] [2] [3] [4] Su vida media de eliminación por esta vía es de 5,0 a 6,6 días. [4]
Química
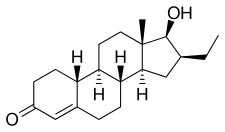
La oxendolona, también conocida como 16β-etil-19-nortestosterona o 16β-etilestr-4-en-17β-ol-3-ona, es un esteroide sintético estrano y un derivado de la testosterona y la 19-nortestosterona (nandrolona). [7] [8]
El éster de acetato de oxendolona se conoce como TSAA-328, mientras que el éster de caproato de oxendolona se conoce como TSAA-330. [21] Nunca se comercializaron. [21]
Historia
La oxendolona se comercializa en Japón por Takeda desde 1981. [8]
Sociedad y cultura
Nombres genéricos
Oxendolona es el nombre genérico del medicamento y su DCITooltip Nombre común internacional, USANDescripción emergente Nombre adoptado por Estados Unidos, y ENEDescripción emergente Nombre aceptado en japonés. [7] [22] También se le conoce por su nombre de código de desarrollo TSAA-291 . [7] [22]
Nombres de marca
La oxendolona se vende o se ha vendido bajo las marcas Prostetin y Roxenone. [7] [22]
Disponibilidad
La oxendolona se comercializa únicamente en Japón . [22]
Referencias
- ^ abc Henkler G, Klotzbach M, Koch H, Müller W, Richter J (noviembre de 1982). "[Progreso en el área del desarrollo de fármacos. 15]". Die Pharmazie (en alemán). 37 (11): 753–765. PMID 6131442.
[Oxendolona] se ha probado clínicamente en Japón (inyección intramuscular semanal de 200-400 mg) en hipertrofia prostática.
- ^ abc Hikichi Y, Yamaoka M, Kusaka M, Hara T (octubre de 2015). "Actividad moduladora selectiva del receptor de andrógenos de un antiandrógeno esteroide TSAA-291 y su perfil de reclutamiento de cofactores". Revista Europea de Farmacología . 765 : 322–331. doi :10.1016/j.ejphar.2015.08.052. PMID 26335395.
Según los datos clínicos de TSAA-291, el nivel plasmático de TSAA-291 después de la administración intramuscular semanal a 400 mg/kg durante 12 semanas es de aproximadamente 100 nM (Información del fármaco).
- ^ abc Ostri P, Swartz R, Meyhoff HH, Petersen JH, Lindgård G, Frimodt-Møller C, et al. (1989). "Tratamiento antiandrogénico de la hiperplasia prostática benigna: un ensayo controlado con placebo". Investigación urológica . 17 (1): 29–33. doi :10.1007/bf00261046. PMID 2466359. S2CID 30551043.
Treinta pacientes fueron tratados con inyecciones semanales de oxendolona 200 mg durante un período de 3 meses, y 30 pacientes fueron asignados al tratamiento con placebo.
- ^ abcde Midgley I, Fowkes AG, Darragh A, Lambe R, Chasseaud LF, Taylor T (abril de 1983). "El destino metabólico del agente antiandrogénico, oxendolona, en el hombre". Esteroides . 41 (4): 521–536. doi :10.1016/0039-128x(83)90092-2. PMID 6419414. S2CID 41224726.
Después de la administración intramuscular de 16β-etil-17β-hidroxi-4-[4-14C] estren-3-ona (14C-oxendolona; 300 mg) a 3 sujetos humanos, [...]
- ^ abc Iga K (7 de noviembre de 2002). "Sólido analgésico bucal mucoadhesivo de desintegración lenta (S-DBMP-T) y sistema de comprimidos bucales cubiertos (BCTS)". En Rathbone MJ, Hadgraft J, Roberts MS (eds.). Tecnología de administración de fármacos de liberación modificada . CRC Press. págs. 368–. ISBN 978-0-8247-0869-6.
- ^ ab Gao W, Bohl CE, Dalton JT (septiembre de 2005). "Química y biología estructural del receptor de andrógenos". Chemical Reviews . 105 (9): 3352–3370. doi :10.1021/cr020456u. PMC 2096617 . PMID 16159155.
- ^ abcde Elks J (14 de noviembre de 2014). Diccionario de fármacos: datos químicos: datos químicos, estructuras y bibliografías. Springer. pp. 914–. ISBN 978-1-4757-2085-3.
- ^ abcdef William Andrew Publishing (22 de octubre de 2013). Pharmaceutical Manufacturing Encyclopedia, 3.ª edición. Elsevier. pp. 2935–. ISBN 978-0-8155-1856-3.
- ^ Negwer M, Scharnow HG (2001). Fármacos orgánico-químicos y sus sinónimos: (una encuesta internacional). Wiley-VCH. p. 2023. ISBN 978-3-527-30247-5.
- ^ Tan MH, Li J, Xu HE, Melcher K, Yong EL (enero de 2015). "Receptor de andrógenos: estructura, función en el cáncer de próstata y descubrimiento de fármacos". Acta Pharmacologica Sinica . 36 (1): 3–23. doi :10.1038/aps.2014.18. PMC 4571323 . PMID 24909511.
- ^ abcde Ishizuka O, Nishizawa O, Hirao Y, Ohshima S (noviembre de 2002). "Metaanálisis basado en evidencia de la farmacoterapia para la hipertrofia prostática benigna". Revista Internacional de Urología . 9 (11): 607–612. doi : 10.1046/j.1442-2042.2002.00539.x . PMID 12534901.
- ^ abc Mallamo JP, Juniewicz PE (8 de septiembre de 1989). "Nuevos horizontes en el tratamiento de la enfermedad prostática proliferativa". En Johns WS (ed.). Informes anuales en química medicinal . Vol. 24. Academic Press. págs. 199–. doi :10.1016/S0065-7743(08)60543-6. ISBN 978-0-08-058368-6.
- ^ abcd Informe anual de los Laboratorios de Investigación Shionogi. 1991. págs. 76–77.
- ^ abc Kirby RS, Christmas T (1991). "El valor potencial de la inhibición de la 5-alfa-reductasa en el tratamiento de la obstrucción del flujo vesical debido a la hiperplasia prostática benigna". Revista Mundial de Urología . 9 (1). doi :10.1007/BF00184713. ISSN 0724-4983. S2CID 38790542.
- ^ abc Bashirelahi N, Ganesan S, Ekiko DB, Young JD, Shida K, Yamanaka H, Takahashi E (septiembre de 1986). "Efecto de la 16 beta-etil-17 beta-hidroxi-4-estren-3-ona (TSAA-291) en la unión de la promegestona (R5020) y la metiltrienolona (R1881) a la próstata humana hiperplásica y neoplásica". Journal of Steroid Biochemistry . 25 (3): 367–374. doi :10.1016/0022-4731(86)90249-9. PMID 2430141.
- ^ ab Sudo K, Yamazaki I, Masuoka M, Nakayama R (1979). "Antiandrógeno TSAA-291. IV. Efectos del antiandrógeno TSAA-291 (16 beta-etil-17 beta-hidroxi-4-oestren-3-ona) en la secreción de gonadotropinas". Acta Endocrinologica. Suplemento . 229 (3 Supplb): 53–66. doi :10.1530/acta.0.092S053. PMID 294107.
- ^ abc Katayama T, Umeda K, Kazama T (noviembre de 1986). "[Ambiente hormonal y tratamiento antiandrogénico en la hipertrofia prostática benigna]". Hinyokika Kiyo. Acta Urologica Japonica (en japonés). 32 (11): 1584–1589. PMID 2435122.
- ^ Dalton J, Gao W (2010). "Receptor de andrógenos". Receptores nucleares: conceptos actuales y desafíos futuros . Proteínas y regulación celular. Springer. págs. 143-182. doi :10.1007/978-90-481-3303-1_6. ISBN . 978-90-481-3302-4.
- ^ Wakeling AE, Furr BJ, Glen AT, Hughes LR (diciembre de 1981). "Unión a receptores y actividad biológica de antiandrógenos esteroides y no esteroides". Journal of Steroid Biochemistry . 15 : 355–359. doi :10.1016/0022-4731(81)90297-1. PMID 7339263.
- ^ Hikichi Y, Yamaoka M, Kusaka M, Hara T (octubre de 2015). "Actividad moduladora selectiva del receptor de andrógenos de un antiandrógeno esteroide TSAA-291 y su perfil de reclutamiento de cofactores". Revista Europea de Farmacología . 765 : 322–331. doi :10.1016/j.ejphar.2015.08.052. PMID 26335395.
- ^ ab Masuoka M, Masaki T, Yamazaki I, Hori T, Nakayama R (1979). "Antiandrógeno TSAA-291. III. Espectros hormonales del antiandrógeno TSAA-291 (16 beta-etil-17 beta-hidroxi-4-estren-3-ona) y sus derivados". Acta Endocrinológica. Suplemento . 229 : 36–52. doi :10.1530/acta.0.092s036. PMID 294106.
- ^ abcd "Usos, efectos secundarios y advertencias de la oxandrolona". Drugs.com .