Eicosanoide

Los eicosanoides son moléculas de señalización producidas por la oxidación enzimática o no enzimática del ácido araquidónico u otros ácidos grasos poliinsaturados (PUFA) que, de manera similar al ácido araquidónico , tienen alrededor de 20 unidades de carbono de longitud. Los eicosanoides son una subcategoría de las oxilipinas , es decir, ácidos grasos oxidados de diversas unidades de carbono de longitud, y se distinguen de otras oxilipinas por su abrumadora importancia como moléculas de señalización celular . Los eicosanoides funcionan en diversos sistemas fisiológicos y procesos patológicos tales como: montar o inhibir la inflamación , la alergia , la fiebre y otras respuestas inmunes ; regular el aborto del embarazo y el parto normal ; contribuir a la percepción del dolor ; regular el crecimiento celular ; controlar la presión arterial ; y modular el flujo regional de sangre a los tejidos. Al realizar estas funciones, los eicosanoides actúan con mayor frecuencia como agentes de señalización autocrinos para impactar sus células de origen o como agentes de señalización paracrinos para impactar las células en la proximidad de sus células de origen. Algunos eicosanoides, como las prostaglandinas , también pueden tener funciones endocrinas como hormonas para influir en la función de células distantes. [1] [2]
Existen múltiples subfamilias de eicosanoides, entre las que se incluyen las más destacadas prostaglandinas, tromboxanos , leucotrienos , lipoxinas , resolvinas y eoxinas . [1] Para cada subfamilia, existe el potencial de tener al menos 4 series separadas de metabolitos, dos series derivadas de los ácidos araquidónico y dihomo-gamma-linolénico ω−6, una serie derivada del ácido eicosapentaenoico ω−3 PUFA y una serie derivada del ácido mead ω−9 PUFA. Esta distinción de subfamilias es importante. Los mamíferos, incluidos los humanos, no pueden convertir ω−6 en ω−3 PUFA. En consecuencia, los niveles tisulares de los PUFA ω−6 y ω−3 y sus metabolitos eicosanoides correspondientes se vinculan directamente con la cantidad de PUFA ω−6 versus ω−3 consumidos en la dieta. [3] Dado que ciertas series de metabolitos de PUFA ω−6 y ω−3 tienen actividades fisiológicas y patológicas casi diametralmente opuestas, a menudo se ha sugerido que las consecuencias nocivas asociadas con el consumo de dietas ricas en PUFA ω−6 reflejan una producción y actividades excesivas de eicosanoides derivados de PUFA ω−6, mientras que los efectos beneficiosos asociados con el consumo de dietas ricas en PUFA ω−3 reflejan la producción y actividades excesivas de eicosanoides derivados de PUFA ω−3. [4] [5] [6] [7] Desde este punto de vista, los efectos opuestos de los eicosanoides derivados de los PUFA ω−6 y ω−3 sobre las células diana clave subyacen a los efectos perjudiciales y beneficiosos de las dietas ricas en PUFA ω−6 y ω−3 sobre la inflamación y las reacciones alérgicas , la aterosclerosis , la hipertensión , el crecimiento del cáncer y una serie de otros procesos.
Nomenclatura
Fuentes de ácidos grasos
"Eicosanoide" (del griego eicosa- 'veinte') es el término colectivo [8] para los PUFA ( ácidos grasos poliinsaturados ) de cadena lineal de 20 unidades de carbono de longitud que han sido metabolizados o convertidos de otra manera en productos que contienen oxígeno. Los precursores de PUFA de los eicosanoides incluyen:
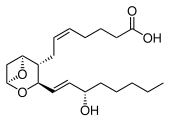
- El ácido araquidónico ( AA ), es decir, ácido 5 Z ,8 Z ,11 Z ,14 Z -eicosatetraenoico, es un ácido graso ω−6 con cuatro enlaces dobles en la configuración cis (denotado Z en la notación E–Z ), cada uno ubicado entre los carbonos 5-6, 8-9, 11-12 y 14-15 (ver numeración de carbonos ).
- El ácido adrenico ( AdA ), es decir, ácido 7Z , 10Z , 13Z , 16Z - docosatetraenoico, es un ácido graso ω−6 con cuatro enlaces dobles cis , cada uno ubicado entre los carbonos 7-8, 10-11, 13-14 y 16-17.
- El ácido eicosapentaenoico ( EPA ), es decir, 5 Z ,8 Z ,11 Z ,14 Z ,17 Z -eicosapentaenoico es un ácido graso ω−3 con cinco dobles enlaces cis , cada uno ubicado entre los carbonos 5-6, 8-9, 11-12, 14-15 y 17-18.
- El ácido dihomo-gamma-linolénico ( DGLA ), es decir, ácido 8Z , 11Z , 14Z - eicosatrienoico, es un ácido graso ω−6 con tres dobles enlaces cis , cada uno ubicado entre los carbonos 8-9, 11-12 y 14-15.
- El ácido mead , es decir, el ácido 5Z , 8Z , 11Z - eicosatrienoico, es un ácido graso ω−9 que contiene tres enlaces dobles cis , cada uno ubicado entre los carbonos 5-6, 8-9 y 11-12.
Abreviatura
Un eicosanoide particular se denota mediante una abreviatura de cuatro caracteres, compuesta por:
- su abreviatura de dos letras ( LT , EX o PG , como se describe a continuación), [9]
- una letra de secuencia ABC, [10]
- Un subíndice o un número escrito en letra simple después del nombre trivial del eicosanoide designado indica el número de sus dobles enlaces . Algunos ejemplos son:
- Los prostanoides derivados del EPA tienen tres enlaces dobles (por ejemplo, PGG 3 o PGG3), mientras que los leucotrienos derivados del EPA tienen cinco enlaces dobles (por ejemplo, LTB 5 o LTB5).
- Los prostanoides derivados de AA tienen dos enlaces dobles (por ejemplo, PGG 2 o PGG2) mientras que sus leucotrienos derivados de AA tienen cuatro enlaces dobles (por ejemplo, LTB 4 o LTB4).
- Los hidroperoxi-, hidroxi- y oxo-eicosanoides poseen un sustituyente hidroperoxi (-OOH), hidroxi (-OH) u átomo de oxígeno (=O) unido a un carbono de PUFA mediante un enlace simple (-) o doble (=). Sus nombres triviales indican el sustituyente como: Hp o HP para un residuo hidroperoxi (p. ej., ácido 5-hidroperooxi-eicosatraenoico o 5- Hp ETE o 5- HP ETE); H para un residuo hidroxi (p. ej., ácido 5-hidroxi-eicosatetraenoico o 5- H ETE); y oxo- para un residuo oxo (p. ej., ácido 5-oxo-eicosatetraenoico o 5- oxo -ETE o 5- oxo ETE). El número de sus dobles enlaces se indica por sus nombres completos y triviales: los metabolitos hidroxi derivados de AA tienen cuatro (es decir, 'tetra' o 'T') enlaces dobles (por ejemplo, ácido 5-hidroxi-eicosa tetraenoico o 5-HE T E; los metabolitos hidroxi derivados de EPA tienen cinco ('penta' o 'P') enlaces dobles (por ejemplo, ácido 5-hidroxi-eicosa pentaenoico o 5-HE P E); y los metabolitos hidroxi derivados de DGLA tienen tres ('tri' o 'Tr') enlaces dobles (por ejemplo, ácido 5-hidroxi-eicosa trienoico o 5-HE Tr E).
La estereoquímica de los productos eicosanoides formados puede diferir entre las vías. Para las prostaglandinas, esto a menudo se indica con letras griegas (p. ej., PGF 2α frente a PGF 2β ). Para los hidroperoxi e hidroxi eicosanoides, una S o R designa la quiralidad de sus sustituyentes (p. ej., el ácido 5 S -hidroxi-eicosatetraenoico [también denominado ácido 5( S )-, 5S-hidroxi- y 5(S)-hidroxi-eicosatetraenoico] recibe los nombres triviales de 5 S -HETE, 5( S )-HETE, 5S-HETE o 5(S)-HETE). Dado que las enzimas formadoras de eicosanoides comúnmente producen productos isómeros S ya sea con marcada preferencia o esencialmente de manera exclusiva, el uso de designaciones S / R a menudo se ha abandonado (p. ej., 5 S -HETE es 5-HETE). No obstante, ciertas vías de formación de eicosanoides forman isómeros R y sus productos isoméricos S versus R pueden exhibir actividades biológicas radicalmente diferentes. [11] No especificar los isómeros S / R puede ser engañoso. Aquí, todos los sustituyentes hidroperoxi e hidroxi tienen la configuración S a menos que se indique lo contrario.
Eicosanoides clásicos
El uso actual limita el término eicosanoide a:
- Eicosanoides de la serie ω−6 derivados del ácido araquidónico:
- Los ácidos hidroxieicosatetraenoicos ( HETE ) incluyen los siguientes metabolitos del ácido araquidónico:
- 5-HETE , 12-HETE , ácido 15-hidroxieicosatetraenoico (es decir, 15-HETE), ácido 20-hidroxieicosatetraenoico (es decir, 20-HETE) y 19-HETE.
- Los leucotrienos ( LT ) incluyen los siguientes metabolitos del ácido araquidónico:
- Las eoxinas ( EX ) incluyen los siguientes metabolitos del ácido araquidónico:
- Los prostanoides se dividen en varios tipos diferentes:
- Las prostaglandinas ( PG ) incluyen los siguientes metabolitos del ácido araquidónico:
- Las prostaciclinas incluyen:
- IGP 2 .
- Los tromboxanos ( TX ) incluyen los siguientes metabolitos del ácido araquidónico:
- Las prostaglandinas de ciclopentenona incluyen los siguientes metabolitos del ácido araquidónico:
- PGA 1 , PGA 2 (ver Prostanoid , PGJ 2 , Δ12-PGJ 2 y 15-desoxi-Δ12,14-PGJ 2 ). [12]
- Los ácidos hidroxieicosatetraenoicos ( HETE ) incluyen los siguientes metabolitos del ácido araquidónico:
- Eicosanoides de la serie ω−6 derivados del ácido dihomo-gamma-linolénico. Estos metabolitos son análogos de los eicosanoides derivados del ácido araquidónico, pero carecen de un doble enlace entre los carbonos 5 y 6 y, por lo tanto, tienen 1 doble enlace menos que sus análogos derivados del ácido araquidónico. Son los siguientes:
- PGA 1 , PGE 1 y TXA 1 . [13] [14]
- Eicosanoides de la serie ω−3:
- Resolvinas de la serie E ( RvE ) (las resolvinas de la serie D [RvD] son metabolitos del ácido docosahexaenoico , un ácido graso de 22 carbonos ω−3 ; véase Mediadores especializados en pro-resolución § Resolvinas derivadas de DHA ). Las RvE incluyen los siguientes metabolitos del ácido eicosapentaenoico:
- RvE1, 18S-RvE1, RvE2 y RvE3.
- Otros eicosanoides derivados del ácido eicosapentaenoico de la serie ω−3 son análogos de los metabolitos derivados del ácido graso ω−6, pero contienen un doble enlace entre el carbono 17 y 18 y, por lo tanto, tienen un doble enlace más que sus análogos derivados del ácido araquidónico. Entre ellos se incluyen (HEPE es ácido hidroxieicosapentaenoico):
- 5-HEPE, 12-HEPE, [15] 15-HEPE, [16] y 20-HETE; [17] LTA5, LTB5, LTC5, LTD5 y LTE5 (ver Araquidonato 5-lipoxigenasa § Ácido eicosapentaenoico ); [18] PGE 3 , PGD 3 , PGF 3α y Δ(17)-6-ceto PGF 1α ; [18] [19] PGI 3 (ver Interacciones de ácidos grasos esenciales § Contrarrestación ); [18] y TXA 3 y TXB 3 . [18]
- Resolvinas de la serie E ( RvE ) (las resolvinas de la serie D [RvD] son metabolitos del ácido docosahexaenoico , un ácido graso de 22 carbonos ω−3 ; véase Mediadores especializados en pro-resolución § Resolvinas derivadas de DHA ). Las RvE incluyen los siguientes metabolitos del ácido eicosapentaenoico:
- Eicosanoides de la serie ω−9
- Los hidroxi se derivan del ácido mead y se metabolizan al análogo de 5-HETE que contiene 3 dobles enlaces, es decir, 5-HETrE (ver Araquidonato 5-lipoxigenasa § Ácido mead ).
Los ácidos hidroxieicosatetraenoicos, los leucotrienos, las eoxinas y los prostanoides a veces se denominan "eicosanoides clásicos". [20] [21] [22]
Eicosanoides no clásicos
A diferencia de los eicosanoides clásicos, varias otras clases de metabolitos de PUFA se han denominado "nuevos", "similares a los eicosanoides" o " eicosanoides no clásicos ". [23] [24] [25] [26] Estos incluyen las siguientes clases:
- Los oxoeicosanoides ( oxo-ETE ) incluyen los siguientes metabolitos:
- Ácido 5-oxo-eicosatetraenoico (5-oxo-ETE), 12-oxo-ETE (ver 12-HETE § Metabolismo posterior ) y 15-oxo-ETE, que son metabolitos del ácido araquidónico (ver Ácido 15-hidroxieicosatetraenoico ) y 5-oxo-ETrE, que es un metabolito del ácido mead (ver Araquidonato 5-lipoxigenasa § Ácido mead ).
- Las hepoxilinas ( Hx ) incluyen los siguientes metabolitos del ácido araquidónico:
- HxA 3 y HxB 3 .
- Las lipoxinas ( Lx ) incluyen los siguientes metabolitos del ácido araquidónico:
- LxA 4 y LxB 4 (ver Mediadores pro-resolutivos especializados ).
- Las epilipoxinas ( epi-Lx ) incluyen los siguientes metabolitos del ácido araquidónico:
- 15-epi-LxA 4 (también denominado AT-LxA 4 ) y 15-epi-LxB 4 (también denominado AT-LxB 4 ).
- Los ácidos epoxieicosatrienoicos ( EET ) incluyen los siguientes metabolitos del ácido araquidónico:
- 5,6-EET, 8,9-EET, 11,12-EET y 14,15-EET.
- Los ácidos epoxieicosatetraenoicos ( EEQ ) incluyen los siguientes metabolitos del ácido eicosapentaenoico:
- 5,6-EEQ, 8,9-EEQ, 11,12-EEQ, 14,15-EEQ y 15,16-EEQ.
- Los isoprostanos ( isoP ) son derivados no enzimáticos de ácidos grasos poliinsaturados estudiados como marcadores de estrés oxidativo ; incluyen los siguientes isoprostanos derivados del ácido araquidónico que reciben su nombre en función de sus similitudes estructurales con los PG: [27] [28]
- D 2 -isoPs, E 2 -isoPs, A 2 -isoPs y J 2 -isoPs; y dos isoPs que contienen epóxido, 5,6-epoxiisoprostano E 2 y 5,6-epoxiisoprostano A 2 . Se ha demostrado que algunos de estos isoPs poseen actividad antiinflamatoria (ver Mediadores especializados en pro-resolución § Prostaglandinas e isoprostanos ).
- Los isofuranos son derivados de ácidos grasos poliinsaturados formados de forma no enzimática que poseen una estructura de anillo furánico ; se estudian como marcadores del estrés oxidativo. Existen 256 isómeros potencialmente diferentes que contienen anillos furánicos que pueden derivarse del ácido araquidónico. [29]
- Los endocannabinoides son ciertos glicerolípidos o dopamina que se esterifican en ácidos grasos poliinsaturados que activan los receptores cannabinoides . Entre ellos se incluyen los siguientes agentes esterificados con ácido araquidónico:
El metabolismo del ácido eicosapentaenoico a HEPE, leucotrienos, prostanoides y ácidos epoxieicosatetraenoicos, así como el metabolismo del ácido dihomo-gamma-linolénico a prostanoides y ácido mead a ácido 5(S)-hidroxi-6E,8Z,11Z-eicosatrienoico (5-HETrE), ácido 5-oxo-6,8,11-eicosatrienoico (5-oxo-ETrE), LTA 3 y LTC 3 involucran las mismas vías enzimáticas que producen sus análogos derivados del ácido araquidónico.
Biosíntesis
Los eicosanoides no suelen almacenarse en las células, sino que se sintetizan según sea necesario. Derivan de los ácidos grasos que forman la membrana celular y la membrana nuclear . Estos ácidos grasos deben liberarse de sus sitios de membrana y luego metabolizarse inicialmente en productos que, con mayor frecuencia, se metabolizan aún más a través de varias vías para formar la gran variedad de productos que reconocemos como eicosanoides bioactivos.
Movilización de ácidos grasos
La biosíntesis de eicosanoides comienza cuando una célula se activa por un trauma mecánico, isquemia , otras perturbaciones físicas, ataque de patógenos o estímulos producidos por células, tejidos o patógenos cercanos, como factores quimiotácticos , citocinas , factores de crecimiento e incluso ciertos eicosanoides. Las células activadas luego movilizan enzimas, denominadas fosfolipasas A 2 (PLA 2 ), capaces de liberar ácidos grasos ω−6 y ω−3 del almacenamiento de membrana. Estos ácidos grasos están unidos en enlace éster a la posición SN2 de los fosfolípidos de membrana ; la PLA 2 actúa como esterasa para liberar el ácido graso. Hay varias clases de PLA 2 y la PLA 2 citosólica tipo IV (cPLA 2 ) parece ser responsable de la liberación de los ácidos grasos en muchas condiciones de activación celular. La cPLA 2 actúa específicamente sobre los fosfolípidos que contienen AA, EPA o GPLA en su posición SN2. La cPLA 2 también puede liberar el lisofosfolípido que se convierte en factor activador de plaquetas . [30]
Peroxidación y especies reactivas de oxígeno
A continuación, el ácido graso libre se oxigena a través de varias vías; consulte la tabla de vías . Las vías de los eicosanoides ( a través de la lipoxigenasa o COX ) añaden oxígeno molecular (O 2 ). Aunque el ácido graso es simétrico , los eicosanoides resultantes son quirales ; las oxidaciones se producen con alta estereoselectividad (las oxidaciones enzimáticas se consideran prácticamente estereoespecíficas ).
Cuatro familias de enzimas inician o contribuyen al inicio de la catálisis de los ácidos grasos a eicosanoides:
- Ciclooxigenasas (COX): COX-1 y COX-2 inician el metabolismo del ácido araquidónico a prostanoides que contienen dos dobles enlaces, es decir, las prostaglandinas (p. ej., PGE 2 ), prostaciclinas (p. ej., PGI 2 ) y tromboxanos (p. ej., TXA 2 ). Las dos enzimas COX también inician el metabolismo de: a) Ácido eicosapentaenoico , que tiene 5 dobles enlaces en comparación con los 4 dobles enlaces del ácido araquidónico, a productos prostanoides, prostaciclinas y tromboxanos que tienen tres dobles enlaces, p. ej., PGE 3 , PGI 3 y TXA 3 y b) Ácido dihomo-γ-linolénico , que tiene tres dobles enlaces, a productos prostanoides, prostaciclinas y tromboxanos que tienen solo un doble enlace, p. ej., PGE 1 , PGI 1 y TXA 1 . [31]
- Lipooxigenasas (LOX): la 5-lipoxigenasa (5-LOX o ALOX5) inicia el metabolismo del ácido araquidónico a ácido 5-hidroperoxieicosatetraenoico (5-HpETE) que luego puede reducirse rápidamente a ácido 5-hidroxieicosatetraenoico (5-HETE) o metabolizarse aún más a leucotrienos (por ejemplo, LTB 4 y LTC 4 ); el 5-HETE puede oxidarse a ácido 5-oxo-eicosatetraenoico (5-oxo-ETE). De manera similar, la 15-lipoxigenasa (15-lipoxigenasa 1, 15-LOX, 15-LOX1 o ALOX15) inicia el metabolismo del ácido araquidónico a 15-HpETE, 15-HETE, eoxinas , ácido 8,15-dihidroxieicosatetraenoico (es decir, 8,15-DiHETE) y 15-oxo-ETE y la 12-lipoxigenasa (12-LOX o ALOX12) inicia el metabolismo del ácido araquidónico a 12-HpETE, 12-HETE, hepoxilinas y 12-oxo-ETE. Estas enzimas también inician el metabolismo de; a ) Ácido eicosapentaenoico a análogos de los metabolitos del ácido araquidónico que contienen 5 en lugar de cuatro enlaces dobles, por ejemplo, ácido 5-hidroxieicosapentaenoico (5-HEPE), LTB 5 , LTC 5 , 5-oxo-EPE, 15-HEPE y 12-HEPE; b) El ácido dihomo-γ-linolénico que contiene tres enlaces dobles a productos que contienen 3 enlaces dobles, por ejemplo, ácido 8-hidroxi-eicosatrienoico (8-HETrE), 12-HETrE y 15-HETrE (este ácido graso no se puede convertir en leucotrienos); y el ácido mead que contiene tres enlaces dobles (por ALOX5) a ácido 5-hidroperoxi-eicosatrienoico (5-HpETrE), 5-HETrE y 5-oxo-HETrE. En la vía más estudiada, ALOX5 metaboliza el ácido eicosapentaenoico a ácido 5-hidroperoxieicosapentaenoico (5-HpEPE), 5-HEPE y LTB 5 y 5-oxo-EPE, todos ellos menos activos que sus análogos del ácido araquidónico. Dado que el ácido eicosapentaenoico compite con el ácido araquidónico por ALOX5, la producción de metabolitos de eicosapentaenoato conduce a una reducción de los metabolitos de eicosatetraenoato y, por lo tanto, a una reducción de la señalización de estos últimos metabolitos. [31] [32] Los productos mono-hidroperoxi y mono-hidroxi iniciales elaborados por las lipoxigenasas mencionadas anteriormente tienen sus residuos de hidroperoxi e hidroxilo posicionados en la configuración quiral S y se denominan más apropiadamente 5 S -HpETE, 5 S -HETE, 12 S -HpETE, 12 S -HETE, 15 S -HpETE y, 15 S -HETE. ALOX12B (es decir, araquidonato 12-lipoxigenasa, tipo 12R) forma productos de quiralidad R , es decir, 12 R -HpETE y 12 R -HETE. De manera similar,ALOXE3 (lipoxigenasa 3 de tipo epidérmico o eLOX3) metaboliza el ácido araquidónico a 12 R -HpETE y 12 R -HETE; sin embargo, estos son productos menores que esta enzima forma solo bajo un conjunto limitado de condiciones. ALOXE3 metaboliza preferentemente el ácido araquidónico a hepoxilinas.
- Epoxigenasas : son enzimas del citocromo P450 que generan epóxidos eicosanoides no clásicos derivados de: a) Ácido araquidónico, a saber, ácido 5,6-epoxi-eicosatrienoico (5,6-EET), 8,9-EET, 11,12-EET y 14,15-EET (véase Ácido epoxieicosatrienoico ); b) Ácido eicosapentaenoico, a saber, ácido 5,6,-epoxi-eicosatetraenoico (5,6-EEQ), 8,9-EEQ, 11,12-EEQ, 14,15-EEQ y 17,18-EEQ (véase Ácido epoxieicosatetraenoico ); c) Ácido dihomo-γ-linolénico, a saber, ácido 8,9-epoxi-eicosadienoico (8,9-EpEDE), 11,12-EpEDE y 14,15-EpEDE; y d) Ácido adrenico, a saber, ácido 7,8-epox-eicosatrienoico (7,8-EpETrR), 10,11-EpTrE, 13,14-EpTrE y 16,17-EpETrE. Todos estos epóxidos son convertidos, a veces rápidamente, en sus metabolitos dihidroxilados por diversas células y tejidos. Por ejemplo, el 5,6-EET se convierte en ácido 5,6-dihidroxi-eicosatrienoico (5,6-DiHETrE), el 8,9-EEQ en ácido 8,9-dihidroxi-eicosatetraenoico (8,9-DiHETE), el 11,12-EpEDE en ácido 11,12-dihidroxi-eicosadienoico (11,12DiHEDE) y el 16,17-EpETrE en ácido 16,17-dihidroxi-eicosatrienoico (16,17-DiETrE). [31]
- Las ω hidroxilasas del microsoma del citocromo P450 : CYP4A11 , CYP4A22 , CYP4F2 y CYP4F3 metabolizan el ácido araquidónico principalmente a ácido 20-hidroxieicosatetraenoico (20-HETE), pero también a 16-HETE, 17-HETE, 18-HETE y 19-HETE; también metabolizan el ácido eicosapentaenoico principalmente a ácido 20-hidroxieicosapentaenoico (20-HEPE), pero también a 19-HEPE. [31]
Dos enzimas diferentes pueden actuar en serie sobre un PUFA para formar metabolitos más complejos. Por ejemplo, ALOX5 actúa con ALOX12 o COX-2 tratada con aspirina para metabolizar el ácido araquidónico a lipoxinas y con citocromo P450 monooxigenasa(s), citocromo P450 bacteriano (en tejidos infectados) o COX2 tratada con aspirina para metabolizar el ácido eicosapentaenoico a las resolvinas de la serie E (RvEs) (ver Mediadores pro-resolución especializados ). Cuando esto ocurre con enzimas ubicadas en diferentes tipos de células e implica la transferencia del producto de una enzima a una célula que usa la segunda enzima para producir el producto final, se lo denomina metabolismo transcelular o biosíntesis transcelular. [33]
La oxidación de los lípidos es peligrosa para las células, en particular cuando se encuentran cerca del núcleo. Existen mecanismos complejos para prevenir la oxidación no deseada. La COX, las lipoxigenasas y las fosfolipasas están estrechamente controladas: hay al menos ocho proteínas activadas para coordinar la generación de leucotrienos. Varias de ellas existen en múltiples isoformas . [7]
La oxidación por COX o lipoxigenasa libera especies reactivas de oxígeno (ROS) y los productos iniciales en la generación de eicosanoides son en sí mismos peróxidos altamente reactivos . LTA 4 puede formar aductos con ADN tisular . Otras reacciones de lipoxigenasas generan daño celular; modelos murinos implican a 15-lipoxigenasa en la patogénesis de la aterosclerosis . [34] [35] La oxidación en la generación de eicosanoides está compartimentada; esto limita el daño de los peróxidos. Las enzimas que son biosintéticas para eicosanoides (p. ej., glutatión-S-transferasas , epóxido hidrolasas y proteínas transportadoras ) pertenecen a familias cuyas funciones están involucradas en gran medida con la desintoxicación celular. Esto sugiere que la señalización de eicosanoides podría haber evolucionado a partir de la desintoxicación de ROS.
La célula debe obtener algún beneficio de la generación de hidroperóxidos lipídicos cerca de su núcleo. Las PG y los LT pueden señalar o regular la transcripción del ADN allí; LTB 4 es un ligando para PPARα . [5] (Ver diagrama en PPAR .)
Vías de los prostanoides
Tanto la COX1 como la COX2 (también denominadas prostaglandina-endoperóxido sintasa-1 ( PTGS1 ) y PTGS2 , respectivamente) metabolizan el ácido araquidónico añadiendo O2 molecular entre los carbonos 9 y 11 para formar un puente de endoperóxido entre estos dos carbonos, añadiendo O2 molecular al carbono 15 para producir un producto 15-hidroperoxi, creando un enlace carbono-carbono entre los carbonos 8 y 12 para crear un anillo de ciclopentano en el medio del ácido graso, y en el proceso produciendo PGG 2 , un producto que tiene dos enlaces dobles menos que el ácido araquidónico. El residuo 15-hidroperoxi de PGG 2 se reduce entonces a un residuo 15- hidroxilo formando así PGH 2. PGH 2 es el prostanoide padre de todos los demás prostanoides. Es metabolizada por (ver diagrama en Prostanoid ): a) La vía de la prostaglandina E sintasa en la que cualquiera de las tres isoenzimas , PTGES , PTGES2 o PTGES3 , convierte PGH 2 en PGE 2 (los productos posteriores de esta vía incluyen PGA 2 y PGB 2 (ver Prostanoid § Biosíntesis de prostaglandinas ); b) PGF sintasa que convierte PGH 2 en PGF 2α ; c) Prostaglandina D 2 sintasa que convierte PGH 2 en PGD 2 (los productos posteriores en esta vía incluyen 15-dPGJ 2 (ver Prostaglandina ciclopentenona ); d) Tromboxano sintasa que convierte PGH 2 en TXA 2 (los productos posteriores en esta vía incluyen TXB 2 ); y e) la sintetasa de prostaciclina , que convierte la PGH 2 en PGI 2 (los productos posteriores de esta vía incluyen 6-ceto-PGFα). [36] [37] Se ha demostrado o, en algunos casos, se ha supuesto que estas vías metabolizan el ácido eicosapentaenoico en análogos eicosanoides de los productos mencionados que tienen tres en lugar de dos enlaces dobles y, por lo tanto, contienen el número 3 en lugar de 2 adjunto a sus nombres (por ejemplo, PGE 3 en lugar de PGE 2 ). [38]
Los productos PGE 2 , PGE 1 y PGD 2 formados en las vías recién citadas pueden sufrir una reacción de deshidratación espontánea para formar PGA 2 , PGA 1 y PGJ 2 , respectivamente; PGJ 2 puede luego sufrir una isomerización espontánea seguida de una reacción de deshidratación para formar en serie Δ12-PGJ 2 y 15-desoxi-Δ12,14-PGJ 2 . [39]
La PGH 2 tiene un anillo de 5 carbonos unido por oxígeno molecular. Sus PGS derivados han perdido este puente de oxígeno y contienen un solo anillo insaturado de 5 carbonos, con excepción del tromboxano A 2 , que posee un anillo de 6 miembros que consta de un átomo de oxígeno y 5 de carbono. El anillo de 5 carbonos de la prostaciclina está unido a un segundo anillo que consta de 4 átomos de carbono y un átomo de oxígeno. Y el anillo de 5 miembros de las prostaglandinas de ciclopentenona posee un enlace insaturado en un sistema conjugado con un grupo carbonilo que hace que estas PG formen enlaces con una amplia gama de proteínas bioactivas (para obtener más información, consulte los diagramas en Prostanoid ).
Vías de los hidroxieicosatetraenoatos (HETE) y los leucotrienos (LT)
La enzima 5-lipoxigenasa (5-LO o ALOX5) convierte el ácido araquidónico en ácido 5-hidroperoxieicosatetraenoico (5-HPETE), que puede liberarse y reducirse rápidamente a ácido 5-hidroxieicosatetraenoico (5-HETE) por las peroxidasas dependientes del glutatión celulares ubicuas . [40] Alternativamente, ALOX5 usa su actividad de LTA sintasa para actuar y convertir 5-HPETE en leucotrieno A 4 (LTA 4 ). Luego, el LTA 4 se metaboliza a LTB 4 por la leucotrieno A 4 hidrolasa o al leucotrieno C 4 (LTC 4 ) por la LTC 4 sintasa o la glutatión S-transferasa microsomal 2 ( MGST2 ). Cualquiera de las dos últimas enzimas actúa para unir el azufre del grupo tio- (es decir, SH) de la cisteína en el tripéptido glutamato - cisteína - glicina al carbono 6 de LTA 4 , formando así LTC 4. Después de la liberación de su célula madre, los residuos de glutamato y glicina de LTC 4 son eliminados paso a paso por la gamma-glutamiltransferasa y una dipeptidasa para formar secuencialmente LTD 4 y LTE 4 . [41] [42] La decisión de formar LTB 4 versus LTC 4 depende del contenido relativo de LTA 4 hidrolasa versus LTC 4 sintasa (o glutatión S-transferasa en las células; los eosinófilos , mastocitos y macrófagos alveolares poseen niveles relativamente altos de LTC 4 sintasa y, en consecuencia, forman LTC 4 en lugar de o en un grado mucho mayor que LTB 4. La 5-LOX también puede funcionar en serie con las oxigenasas del citocromo P450 o la COX2 tratada con aspirina para formar resolvinas RvE1, RvE2 y 18S-RvE1 (ver Mediadores especializados en pro-resolución § Resolvinas derivadas de EPA ).
La enzima araquidonato 12-lipoxigenasa (12-LO o ALOX12) metaboliza el ácido araquidónico al estereoisómero S del ácido 12-hidroperoxieicosatetraenoico (12-HPETE), que es rápidamente reducido por las peroxidasas celulares al estereoisómero S del ácido 12-hidroxieicosatetraenoico (12-HETE) o metabolizado aún más a hepoxilinas (Hx) como HxA3 y HxB. [43] [44]
Las enzimas 15-lipoxigenasa -1 (15-LO-1 o ALOX15 ) y 15-lipoxigenasa-2 (15-LO-2, ALOX15B ) metabolizan el ácido araquidónico al estereoisómero S del ácido 15-hidroperoxieicosatetraenoico (15(S)-HPETE), que es rápidamente reducido por las peroxidasas celulares al estereoisómero S del ácido 15-hidroxieicosatetraenoico (15(S)-HETE). [45] [46] Las 15-lipoxigenasas (particularmente ALOX15) también pueden actuar en serie con la 5-lipoxigenasa, la 12-lipoxigenasa o la COX2 tratada con aspirina para formar las lipoxinas y epilipoxinas o con las oxigenasas P450 o la COX2 tratada con aspirina para formar resolvina E3 (ver Mediadores pro-resolución especializados § Resolvinas derivadas de EPA ).
Un subconjunto de ω hidroxilasas unidas al microsoma del citocromo P450 (CYP450) metabolizan el ácido araquidónico a ácido 20-hidroxieicosatetraenoico (20-HETE) y ácido 19-hidroxieicosatetraenoico mediante una reacción de oxidación omega . [47]
Vía de los epoxieicosanoides
Las epoxigenasas del citocromo P450 (CYP) humano, CYP1A1, CYP1A2, CYP2C8, CYP2C9, CYP2C18, CYP2C19, CYP2E1, CYP2J2 y CYP2S1 metabolizan el ácido araquidónico en ácidos epoxieicosatrienoicos (EET) no clásicos al convertir uno de los dobles enlaces del ácido graso en su epóxido para formar uno o más de los siguientes EET: 14,15-ETE, 11,12-EET, 8,9-ETE y 4,5-ETE. [48] [49] 14,15-EET y 11,12-EET son los principales EET producidos por los tejidos de mamíferos, incluidos los humanos. [49] [50] [51] [52] [53] Los mismos CYP, pero también CYP4A1, CYP4F8 y CYP4F12 metabolizan el ácido eicosapentaenoico a cinco ácidos epóxido epoxieicosatetraenoicos (EEQ), a saber, 17,18-EEQ, 14,15-EEQ, 11,12-EEQ, 8,9-EEQ y 5,6-EEQ. [54]
Función, farmacología y significado clínico
La siguiente tabla enumera una muestra de los principales eicosanoides que poseen una actividad biológica clínicamente relevante, los receptores celulares (ver Receptor de superficie celular ) que estimulan o, cuando se indica, antagonizan para lograr esta actividad, algunas de las principales funciones que regulan (ya sea que promuevan o inhiban) en modelos humanos y de ratón, y algunas de sus relevancias para las enfermedades humanas.
| Eicosanoide | Receptores específicos | Funciones reguladas | Relevancia clínica |
|---|---|---|---|
| PGE2 | PTGER1 , PTGER2 , PTGER3 , PTGER4 | inflamación; fiebre; percepción del dolor; alodinia ; parto | Los AINE inhiben su producción para reducir la inflamación, la fiebre y el dolor; se utilizan para promover el parto; son abortivos [37] [55] [56] |
| DGP 2 | Receptor 1 de prostaglandina DP1, receptor de prostaglandina DP2 | reacciones alérgicas ; alodinia ; crecimiento del cabello | Los AINE pueden dirigirse a él para inhibir la alodinia y la pérdida de cabello de patrón masculino [37] [57] [58] [59] [60] |
| TXA2 | Receptor de tromboxano α y β | agregación plaquetaria ; coagulación sanguínea; reacciones alérgicas | Los AINE inhiben su producción para reducir la incidencia de accidentes cerebrovasculares y ataques cardíacos [37] [61] |
| IGP 2 | Receptor de prostaciclina | Agregación plaquetaria, contracción del músculo liso vascular. | Análogos de PGI2 utilizados para tratar trastornos vasculares como hipertensión pulmonar , síndrome de Raynaud y enfermedad de Buerger [62] [63] [64] |
| 15-d-Δ12,14- PGJ2 | PPARγ , receptor de prostaglandina DP2 | Inhibe la inflamación y el crecimiento celular. | Inhibe diversas respuestas inflamatorias en modelos animales; modelo estructural para el desarrollo de agentes antiinflamatorios [12] [59] [60] |
| 20-HETE | ? | vasoconstricción, inhibe las plaquetas | mutaciones inactivadoras en la enzima formadora de 20-HETE, CYP2U1 , asociadas con la paraplejía espástica hereditaria [65] |
| 5-Oxo-ETE | Oxígeno 1 | Factor quimiotáctico y activador de los eosinófilos. | Se necesitan estudios para determinar si inhibir su producción o acción inhibe las reacciones alérgicas [32] |
| 4 de julio | LTB4R , LTB4R2 | Factor quimiotáctico y activador de los leucocitos; inflamación | Los estudios realizados hasta la fecha no han demostrado beneficios claros de los antagonistas del receptor LTB 4 para las enfermedades inflamatorias humanas [66] [67] [68] |
| LTC 4 | CYSLTR1 , CYSLTR2 , GPR17 | permeabilidad vascular; contracción del músculo liso vascular; alergia | Antagonistas de CYSLTR1 utilizados en el asma, así como en otras reacciones alérgicas y similares [69] [70] |
| Limitada 4 | CYSLTR1 , CYSLTR2 , GPR17 | permeabilidad vascular; contracción del músculo liso vascular; alergia | Antagonistas de CYSLTR1 utilizados en el asma, así como en otras reacciones alérgicas y similares [66] |
| LTE 4 | GPR99 | Aumenta la permeabilidad vascular y la secreción de mucina en las vías respiratorias. | Se cree que contribuye al asma y a otras reacciones alérgicas y similares [71] |
| LxA 4 | FPR2 | inhibe las funciones de las células proinflamatorias | Clase de mediadores pro-resolutivos especializados supresores de la reacción inflamatoria [72] [73] |
| LxB 4 | FPR2 , GPR32 y AHR | inhibe las funciones de las células proinflamatorias | Clase de mediadores pro-resolutivos especializados supresores de la reacción inflamatoria [72] [73] |
| RVE1 | CMKLR1 , inhibe BLT , TRPV1 , TRPV3 , NMDAR , TNFR | inhibe las funciones de las células proinflamatorias | Clase especializada de mediadores pro-resolutivos supresores de la reacción inflamatoria; también suprime la percepción del dolor [74] [75] [76] |
| RVE2 | CMKLR1 , antagonista del receptor BLT | inhibe las funciones de las células proinflamatorias | Clase de mediadores pro-resolutivos especializados supresores de la reacción inflamatoria [72] [73] [76] [77] |
| 14,15-EET | ? | vasodilatación , inhibe plaquetas y células proinflamatorias | Papel(es) en enfermedades humanas aún no demostrado (s) [78] [79] |
Prostanoides
Se sabe que muchos de los prostanoides median los síntomas locales de la inflamación : vasoconstricción o vasodilatación , coagulación , dolor y fiebre . La inhibición de la COX-1 y/o las isoformas inducibles de la COX-2 es el sello distintivo de los AINE (medicamentos antiinflamatorios no esteroides), como la aspirina . Los prostanoides también activan los miembros PPAR γ de la familia esteroide/tiroidea de receptores de hormonas nucleares e influyen directamente en la transcripción genética . [80] Los prostanoides tienen muchas otras relevancias para la medicina clínica como lo demuestra su uso, el uso de sus análogos farmacológicos más estables, del uso de sus antagonistas de receptores como se indica en el siguiente cuadro.
| Medicamento | Tipo | Condición médica o uso | Medicamento | Tipo | Condición médica o uso | |
|---|---|---|---|---|---|---|
| Alprostadil | PGE1 | Disfunción eréctil , mantenimiento de un conducto arterioso persistente en el feto | Beraprost | PGI 2 analógico | Hipertensión pulmonar , evitando la lesión por reperfusión | |
| Bimatoprost | Análogo de PGF 2α | Glaucoma , hipertensión ocular | Carboprost | Análogo de PGF 2α | Inducción del parto, abortivo en el embarazo temprano | |
| Dinoprostona | PGE2 | Inducción del parto | Iloprost | PGI 2 analógico | Hipertensión de la arteria pulmonar | |
| Latanoprost | Análogo de PGF 2α | Glaucoma , hipertensión ocular | Misoprostol | PGE 1 analógico | Úlceras de estómago , inducción del parto , abortivo | |
| Travoprost | Análogo de PGF 2α | Glaucoma , hipertensión ocular | U46619 | Analógico TX de mayor duración | Solo investigación |
Prostaglandinas de ciclopentenona
PGA 1 , PGA 2 , PGJ 2 , Δ12-PGJ 2 y 15-deox-Δ12,14-PGJ 2 exhiben una amplia gama de acciones antiinflamatorias y de resolución de la inflamación en diversos modelos animales. [39] Por lo tanto, parecen funcionar de manera similar a los mediadores especializados en pro-resolución, aunque uno de sus mecanismos de acción, la formación de enlaces covalentes con proteínas de señalización clave, difiere de los de los mediadores especializados en pro-resolución.
HETE y oxo-ETEs
Como se indica en sus páginas individuales de Wikipedia, el ácido 5-hidroxieicosatetraenoico (que, al igual que el ácido 5-oxo-eicosatetraenoico, actúa a través del receptor OXER1), el ácido 5-oxo-eicosatetraenoico , el ácido 12-hidroxieicosatetraenoico , el ácido 15-hidroxieicosatetraenoico y el ácido 20-hidroxieicosatetraenoico muestran numerosas actividades en células animales y humanas, así como en modelos animales, que están relacionadas, por ejemplo, con la inflamación, las reacciones alérgicas, el crecimiento de células cancerosas, el flujo sanguíneo a los tejidos y/o la presión arterial. Sin embargo, su función y relevancia para la fisiología y patología humanas aún no se han demostrado.
Leucotrienos
Los tres leucotrienos cisteinílicos, LTC 4 , LTD 4 y LTE 4 , son potentes broncoconstrictores, incrementadores de la permeabilidad vascular en las vénulas poscapilares y estimuladores de la secreción de moco que se libera del tejido pulmonar de sujetos asmáticos expuestos a alérgenos específicos. Desempeñan un papel fisiopatológico en diversos tipos de reacciones de hipersensibilidad inmediata . [81] Los fármacos que bloquean su activación del receptor CYSLTR1 , a saber, montelukast , zafirlukast y pranlukast , se utilizan clínicamente como tratamiento de mantenimiento para el asma y la rinitis inducidas por alérgenos ; asma y rinitis inducidas por fármacos antiinflamatorios no esteroides (ver enfermedad respiratoria exacerbada por aspirina ); asma inducida por ejercicio y aire frío (ver Broncoconstricción inducida por ejercicio ); y apnea del sueño infantil debido a hipertrofia adenoamigdalina (ver Miopatía no inflamatoria adquirida § Miopatía inducida por dieta y trauma ). [82] [83] [84] [85] Cuando se combinan con terapia con antihistamínicos , también parecen útiles para tratar enfermedades urticariales como la urticaria. [86]
Lipoxinas y epilipoxinas
LxA 4 , LxB 4 , 15-epi-LxA 4 y 15-epi-LXB 4 , al igual que otros miembros de la clase de mediadores pro-resolución especializados de eicosanoides, poseen actividad antiinflamatoria y de resolución de la inflamación. En un ensayo controlado aleatorizado , AT-LXA 4 y un análogo comparativamente estable de LXB 4 , 15 R/S -metil-LXB 4 , redujeron la gravedad del eczema en un estudio de 60 bebés [87] y, en otro estudio, LXA 4 inhalado disminuyó la broncoprovocación iniciada por LTC 4 en pacientes con asma. [88]
Eoxinas
Las eoxinas (EXC 4 , EXD 4 , EXE 5 ) se han descrito recientemente. Estimulan la permeabilidad vascular en un sistema modelo endotelial vascular humano ex vivo, [89] y en un pequeño estudio de 32 voluntarios, la producción de EXC 4 por eosinófilos aislados de asmáticos graves e intolerantes a la aspirina fue mayor que la de voluntarios sanos y pacientes asmáticos leves; se ha sugerido que estos hallazgos indican que las eoxinas tienen acciones proinflamatorias y, por lo tanto, están potencialmente involucradas en varias reacciones alérgicas. [90] La producción de eoxinas por células de Reed-Sternberg también ha llevado a sugerir que están involucradas en la enfermedad de Hodgkin . [91] Sin embargo, aún no se ha demostrado la importancia clínica de las eoxinas.
Metabolitos resolvínicos del ácido eicosapentaenoico
RvE1, 18S-RvE1, RvE2 y RvE3, al igual que otros miembros de la clase de mediadores pro-resolución especializados de eicosanoides, poseen actividad antiinflamatoria y de resolución de la inflamación. Un análogo sintético de RvE1 se encuentra en pruebas clínicas de fase III (ver Fases de la investigación clínica ) para el tratamiento del síndrome del ojo seco basado en la inflamación ; junto con este estudio, se están realizando otros ensayos clínicos (NCT01639846, NCT01675570, NCT00799552 y NCT02329743) que utilizan un análogo de RvE1 para tratar varias afecciones oculares. [88] RvE1 también se encuentra en estudios de desarrollo clínico para el tratamiento de enfermedades neurodegenerativas y pérdida auditiva. [92]
Otros metabolitos del ácido eicosapentaenoico
Los metabolitos del ácido eicosapentaenoico que son análogos de sus contrapartes prostanoides derivadas del ácido araquidónico, HETE y LT incluyen: los prostanoides de la serie 3 (p. ej., PGE 3 , PGD 3 , PGF 3α , PGI 3 y TXA 3 ), los ácidos hidroxieicosapentaenoicos (p. ej., 5-HEPE, 12-HEPE, 15-HEPE y 20-HEPE) y los LT de la serie 5 (p. ej., LTB 5 , LTC 5 , LTD 5 y LTE 5 ). Se ha demostrado o se piensa que muchos de los prostanoides de la serie 3, los ácidos hidroxieicosapentaenoicos y los LT de la serie 5 son estimuladores más débiles de sus células y tejidos diana que sus análogos derivados del ácido araquidónico. Se propone reducir las acciones de sus análogos derivados del araquidonato reemplazando su producción con análogos más débiles. [93] [94] No se han descrito contrapartes de las eoxinas derivadas del ácido eicosapentaenoico.
Epoxieicosanoides
Los ácidos epoxi eicosatrienoicos (o EET) -y, presumiblemente, los ácidos epoxi eicosatetraenoicos- tienen acciones vasodilatadoras en el corazón , los riñones y otros vasos sanguíneos, así como en la reabsorción de sodio y agua en los riñones, y actúan para reducir la presión arterial y las lesiones isquémicas y de otro tipo en el corazón, el cerebro y otros tejidos ; también pueden actuar para reducir la inflamación, promover el crecimiento y la metástasis de ciertos tumores , promover el crecimiento de nuevos vasos sanguíneos, en el sistema nervioso central , regular la liberación de hormonas neuropeptídicas y, en el sistema nervioso periférico, inhibir o reducir la percepción del dolor. [48] [49] [51]
Las series ω−3 y ω−6
La reducción de los eicosanoides derivados del AA y la menor actividad de los productos alternativos generados a partir de los ácidos grasos ω-3 sirven como base para explicar algunos de los efectos beneficiosos de una mayor ingesta de ω-3.
— Kevin Fritsche, Los ácidos grasos como moduladores de la respuesta inmunitaria [95]
El ácido araquidónico (AA; 20:4 ω−6) se encuentra a la cabeza de la "cascada del ácido araquidónico": más de veinte vías de señalización mediadas por eicosanoides que controlan una amplia gama de funciones celulares, especialmente aquellas que regulan la inflamación , la inmunidad y el sistema nervioso central . [6]
En la respuesta inflamatoria, otros dos grupos de ácidos grasos de la dieta forman cascadas que compiten con la cascada del ácido araquidónico y son paralelos a ella. El EPA (20:5 ω−3) constituye la cascada competidora más importante. El DGLA (20:3 ω−6) constituye una tercera cascada menos prominente. Estas dos cascadas paralelas suavizan los efectos inflamatorios del AA y sus productos. La ingesta dietética baja de estos ácidos grasos menos inflamatorios, especialmente los ω−3, se ha relacionado con varias enfermedades relacionadas con la inflamación y, tal vez, con algunas enfermedades mentales .
Los Institutos Nacionales de Salud de los Estados Unidos y la Biblioteca Nacional de Medicina afirman que hay evidencia de nivel "A" de que el aumento de ω−3 en la dieta mejora los resultados en la hipertrigliceridemia , la prevención secundaria de enfermedades cardiovasculares y la hipertensión . Hay evidencia de nivel "B" ("buena evidencia científica") de un aumento de ω−3 en la dieta en la prevención primaria de enfermedades cardiovasculares, artritis reumatoide y protección contra la toxicidad de la ciclosporina en pacientes con trasplante de órganos . También señalan evidencia más preliminar que muestra que el ω−3 en la dieta puede aliviar los síntomas en varios trastornos psiquiátricos. [96]
Además de la influencia sobre los eicosanoides, las grasas poliinsaturadas de la dieta modulan la respuesta inmunitaria a través de otros tres mecanismos moleculares. Estos (a) alteran la composición y función de la membrana , incluida la composición de las balsas lipídicas ; (b) cambian la biosíntesis de citocinas ; y (c) activan directamente la transcripción genética. [95] De estos, la acción sobre los eicosanoides es la mejor explorada.
Datos recientes de 2024 han demostrado que el tratamiento con ω−3 redujo la degradación de la integridad neuronal en los portadores de APOE*E4 , lo que sugiere que este tratamiento puede ser beneficioso para este grupo específico; los suplementos de aceite de pescado podrían ayudar a los adultos mayores a combatir la enfermedad de Alzheimer . [97] [98]
Mecanismos de acción de ω−3
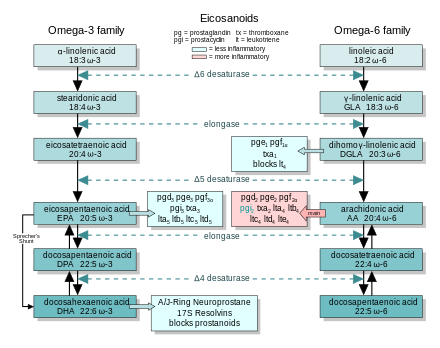
En general, los eicosanoides derivados del AA promueven la inflamación, y los del EPA y del GLA ( a través de DGLA) son menos inflamatorios, o inactivos, o incluso antiinflamatorios y pro-resolutivos .
La figura muestra las cadenas de síntesis ω−3 y −6, junto con los principales eicosanoides de AA, EPA y DGLA.
El ω−3 y el GLA de la dieta contrarrestan los efectos inflamatorios de los eicosanoides del AA de tres maneras, a lo largo de las vías de los eicosanoides:
- Desplazamiento : el ω−3 de la dieta disminuye las concentraciones de AA en los tejidos, por lo que hay menos cantidad para formar eicosanoides ω−6.
- Inhibición competitiva : el DGLA y el EPA compiten con el AA por el acceso a las enzimas ciclooxigenasa y lipoxigenasa. Por lo tanto, la presencia de DGLA y EPA en los tejidos reduce la producción de eicosanoides del AA.
- Contrarrestación : algunos eicosanoides derivados de DGLA y EPA contrarrestan sus contrapartes derivadas de AA.
Papel en la inflamación
Desde la antigüedad , los signos cardinales de la inflamación se conocen como: calor, dolor, hinchazón y rubor. Los eicosanoides están implicados en cada uno de estos signos.
Enrojecimiento : la picadura de un insecto desencadena la respuesta inflamatoria clásica. Los vasoconstrictores de acción corta (TXA 2 ) se liberan rápidamente después de la lesión. El sitio puede palidecer momentáneamente. Luego, el TXA 2 media la liberación de los vasodilatadores PGE 2 y LTB 4 . Los vasos sanguíneos se congestionan y la lesión se enrojece.
Hinchazón : el LTB 4 hace que los vasos sanguíneos sean más permeables. El plasma se filtra hacia los tejidos conectivos y estos se hinchan. El proceso también pierde citocinas proinflamatorias.
Dolor : las citocinas aumentan la actividad de la COX-2. Esto eleva los niveles de PGE 2 , sensibilizando a las neuronas del dolor.
Calor : la PGE 2 también es un potente agente pirético. La aspirina y los AINE (fármacos que bloquean las vías de la COX y detienen la síntesis de prostanoides) limitan la fiebre o el calor de la inflamación localizada.
Historia
En 1930, el ginecólogo Raphael Kurzrok y el farmacólogo Charles Leib caracterizaron la prostaglandina como un componente del semen. Entre 1929 y 1932, George y Mildred Burr demostraron que restringir la grasa de la dieta de los animales conducía a una enfermedad carencial, y describieron por primera vez los ácidos grasos esenciales . [99] En 1935, von Euler identificó la prostaglandina. En 1964, Bergström y Samuelsson vincularon estas observaciones cuando demostraron que los eicosanoides "clásicos" se derivaban del ácido araquidónico, que anteriormente se había considerado uno de los ácidos grasos esenciales. [100] En 1971, Vane demostró que la aspirina y fármacos similares inhiben la síntesis de prostaglandinas. [101] Von Euler recibió el Premio Nobel de Medicina en 1970, que Samuelsson, Vane y Bergström también recibieron en 1982. EJ Corey lo recibió en Química en 1990, principalmente por su síntesis de prostaglandinas.
Véase también
Referencias
- ^ ab "Síntesis y metabolismo de eicosanoides: prostaglandinas, tromboxanos, leucotrienos, lipoxinas". The Medical Biochemistry Page. 2024. Consultado el 9 de abril de 2024 .
- ^ "15.2C: Química de las hormonas". Medicine LibreTexts . 2018-07-21 . Consultado el 2024-04-09 .
- ^ Edwards IJ, O'Flaherty JT (2008). "Ácidos grasos omega-3 y PPARgamma en el cáncer". PPAR Research . 2008 : 358052. doi : 10.1155/2008/358052 . PMC 2526161 . PMID 18769551.
- ^ DeCaterina, R; Basta, G (junio de 2001). "Ácidos grasos n-3 y respuesta inflamatoria: antecedentes biológicos". Suplementos de European Heart Journal . 3, Supl D: D42–D49. doi : 10.1016/S1520-765X(01)90118-X . S2CID 22691568.
- ^ ab Funk, Colin D. (30 de noviembre de 2001). "Prostaglandinas y leucotrienos: avances en la biología de los eicosanoides". Science . 294 (5548): 1871–1875. Bibcode :2001Sci...294.1871F. doi :10.1126/science.294.5548.1871. PMID 11729303.
- ^ ab Piomelli, Daniele (2000). "Ácido araquidónico". Neuropsicofarmacología: la quinta generación del progreso . Archivado desde el original el 15 de julio de 2006. Consultado el 3 de marzo de 2006 .
- ^ ab Soberman, Roy J.; Christmas, Peter (2003). "La organización y las consecuencias de la señalización de eicosanoides". J. Clin. Invest . 111 (8): 1107–1113. doi :10.1172/JCI18338. PMC 152944 . PMID 12697726.
- ^ Beare-Rogers (2001). "IUPAC Lexicon of Lipid Nutrition" (PDF) . Consultado el 1 de junio de 2006 .
- ^ La prostaciclina (PGI) se clasificaba anteriormente como prostaglandina y conserva su antiguo identificador PGI2 .
- ^ Los eicosanoides con letras diferentes tienen la ubicación de los dobles enlaces y diferentes grupos funcionales unidos al esqueleto molecular. Las letras indican aproximadamente el orden en que se describieron por primera vez los eicosanoides en la literatura. Para ver los diagramas de PG [A–H], consulte Cyberlipid Center. "Prostanoides". Archivado desde el original el 8 de febrero de 2007. Consultado el 5 de febrero de 2007 .
- ^ Rossi AG, Thomas MJ, O'Flaherty JT (1988). "Acciones estereoespecíficas del 5-hidroxieicosatetraenoato". FEBS Letters . 240 (1–2): 163–166. doi : 10.1016/0014-5793(88)80360-0 . PMID 3191990. S2CID 43027447.
- ^ ab Straus DS, Glass CK (2001). "Prostaglandinas de ciclopentenona: nuevos conocimientos sobre actividades biológicas y objetivos celulares". Medicinal Research Reviews . 21 (3): 185–210. doi :10.1002/med.1006.abs. PMID 11301410.
- ^ Prasad KN, Hovland AR, Cole WC, Prasad KC, Nahreini P, Edwards-Prasad J, Andreatta CP (2000). "Antioxidantes múltiples en la prevención y el tratamiento de la enfermedad de Alzheimer: análisis de la justificación biológica". Neurofarmacología clínica . 23 (1): 2–13. doi :10.1097/00002826-200001000-00002. PMID 10682224.
- ^ Xu Y, Qian SY (2014). "Actividades anticancerígenas de los ácidos grasos poliinsaturados ω-6". Revista biomédica . 37 (3): 112–119. doi : 10.4103/2319-4170.131378 . PMC 4166599 . PMID 24923568.
- ^ Gomolka B, Siegert E, Blossey K, Schunck WH, Rothe M, Weylandt KH (2011). "Análisis de la formación de metabolitos lipídicos derivados de ácidos grasos omega-3 y omega-6 en muestras de sangre humana y de ratón". Prostaglandinas y otros mediadores lipídicos . 94 (3–4): 81–87. doi :10.1016/j.prostaglandins.2010.12.006. PMID 21236358.
- ^ Zulfakar MH, Edwards M, Heard CM (2007). "¿Tiene alguna utilidad el ácido eicosapentaenoico administrado por vía tópica en el tratamiento de la psoriasis?". Revista Europea de Dermatología . 17 (4): 284–291. doi :10.1684/ejd.2007.0201 (inactivo 2024-09-12). PMID 17540633.
{{cite journal}}: CS1 maint: DOI inactivo a partir de septiembre de 2024 ( enlace ) - ^ Caramia G (2012). "[Ácidos grasos esenciales y mediadores lipídicos. Endocannabinoides]". La Pediatria Medica e Chirurgica: Pediatría médica y quirúrgica (en italiano). 34 (2): 65–72. doi : 10.4081/pmc.2012.2 . PMID 22730630.
- ^ abcd Wiktorowska-Owczarek A, Berezińska M, Nowak JZ (2015). «AGPI: estructuras, metabolismo y funciones». Avances en medicina clínica y experimental . 24 (6): 931–941. doi : 10.17219/acem/31243 . PMID: 26771963.
- ^ Tanaka N, Yamaguchi H, Furugen A, Ogura J, Kobayashi M, Yamada T, Mano N, Iseki K (2014). "Cuantificación de prostanoides intracelulares y extracelulares derivados del ácido eicosapentaenoico de la serie 3 mediante cromatografía líquida/espectrometría de masas en tándem con ionización por electrospray". Prostaglandinas, leucotrienos y ácidos grasos esenciales . 91 (3): 61–71. doi :10.1016/j.plefa.2014.04.005. PMID 24996760.
- ^ Van Dyke TE, Serhan CN (2003). "Resolución de la inflamación: un nuevo paradigma para la patogénesis de las enfermedades periodontales". J. Dent. Res . 82 (2): 82–90. doi :10.1177/154405910308200202. PMID 12562878. S2CID 40812937.
- ^ Serhan CN, Gotlinger K, Hong S, Arita M (2004). "Resolvinas, docosatrienos y neuroprotectinas, nuevos mediadores derivados de omega-3 y sus epímeros endógenos activados por aspirina: una descripción general de sus funciones protectoras en la catabasis". Prostaglandinas y otros mediadores lipídicos . 73 (3–4): 155–172. doi :10.1016/j.prostaglandins.2004.03.005. PMID 15290791.
- ^ Anderle P, Farmer P, Berger A, Roberts MA (2004). "Enfoque nutrigenómico para comprender los mecanismos por los cuales los ácidos grasos de cadena larga de la dieta inducen señales genéticas y controlan los mecanismos involucrados en la carcinogénesis". Nutrition (Burbank, Condado de Los Ángeles, California) . 20 (1): 103–108. doi :10.1016/j.nut.2003.09.018. PMID 14698023.
- ^ Evans AR, Junger H, Southall MD, et al. (2000). "Isoprostanos, nuevos eicosanoides que producen nocicepción y sensibilizan las neuronas sensoriales de ratas". J. Pharmacol. Exp. Ther . 293 (3): 912–920. PMID 10869392.
- ^ O'Brien WF, Krammer J, O'Leary TD, Mastrogiannis DS (1993). "El efecto del paracetamol en la producción de prostaciclina en mujeres embarazadas". Am. J. Obstet. Gynecol . 168 (4): 1164–1169. doi :10.1016/0002-9378(93)90362-m. PMID 8475962.
- ^ Behrendt H, Kasche A, Ebner von Eschenbach C, Risse U, Huss-Marp J, Ring J (2001). "La secreción de sustancias proinflamatorias similares a los eicosanoides precede a la liberación de alérgenos de los granos de polen en el inicio de la sensibilización alérgica" (PDF) . Int. Arch. Allergy Immunol . 124 (1–3): 121–125. doi :10.1159/000053688. PMID 11306946. S2CID 53331.
- ^ Sarau HM, Foley JJ, Schmidt DB, et al. (1999). "Caracterización farmacológica in vitro e in vivo de SB 201993, un antagonista del receptor LTB4 similar a los eicosanoides con actividad antiinflamatoria". Prostaglandinas Leukot. Essent. Ácidos grasos . 61 (1): 55–64. doi :10.1054/plef.1999.0074. PMID 10477044.
- ^ Czerska M, Zieliński M, Gromadzińska J (2016). "Isoprostanos: un nuevo grupo importante de marcadores de estrés oxidativo". Revista internacional de medicina ocupacional y salud ambiental . 29 (2): 179–190. doi : 10.13075/ijomeh.1896.00596 . PMID 26670350.
- ^ Friedli O, Freigang S (2016). "Fosfolípidos oxidados que contienen ciclopentenona y sus isoprostanos como mediadores pro-resolutivos de la inflamación". Biochimica et Biophysica Acta (BBA) - Biología molecular y celular de los lípidos . 1862 (4): 382–392. doi : 10.1016/j.bbalip.2016.07.006 . PMID 27422370.
- ^ Cuyamendous C, de la Torre A, Lee YY, Leung KS, Guy A, Bultel-Poncé V, Galano JM, Lee JC, Oger C, Durand T (2016). "La novedad de los fitofuranos, isofuranos, dihomo-isofuranos y neurofuranos: descubrimiento, síntesis y aplicación potencial" (PDF) . Biochimie . 130 : 49–62. doi :10.1016/j.biochi.2016.08.002. PMID 27519299. S2CID 1504539.
- ^ University of Kansas Medical Center (2004). "Eicosanoides e inflamación" (PDF) . Archivado desde el original (PDF) el 2005-05-16 . Consultado el 2007-01-05 .
- ^ abcd Gabbs M, Leng S, Devassy JG, Monirujjaman M, Aukema HM (2015). "Avances en nuestra comprensión de las oxilipinas derivadas de los PUFA dietéticos". Avances en nutrición . 6 (5): 513–540. doi :10.3945/an.114.007732. PMC 4561827 . PMID 26374175.
- ^ ab Powell WS, Rokach J (2015). "Biosíntesis, efectos biológicos y receptores de ácidos hidroxieicosatetraenoicos (HETE) y ácidos oxoeicosatetraenoicos (oxo-ETEs) derivados del ácido araquidónico". Biochimica et Biophysica Acta (BBA) - Biología molecular y celular de los lípidos . 1851 (4): 340–355. doi :10.1016/j.bbalip.2014.10.008. PMC 5710736. PMID 25449650 .
- ^ Capra V, Rovati GE, Mangano P, Buccellati C, Murphy RC, Sala A (2015). "Biosíntesis transcelular de mediadores lipídicos eicosanoides". Biochimica et Biophysica Acta (BBA) - Biología molecular y celular de los lípidos . 1851 (4): 377–382. doi :10.1016/j.bbalip.2014.09.002. PMID 25218301.
- ^ Cyrus, Tillmann; Witztum, Joseph L.; Rader, Daniel J.; Tangirala, Rajendra; Fazio, Sergio; Linton, Macrae F.; Funk, Colin D. (junio de 1999). "La interrupción del gen de la 12/15-lipoxigenasa disminuye la aterosclerosis en ratones deficientes en apo E". J Clin Invest . 103 (11): 1597–1604n. doi :10.1172/JCI5897. PMC 408369 . PMID 10359569.
- ^ Schewe T. (marzo-abril de 2002). "15-lipoxigenasa-1: una enzima prooxidante". Biol. Chem . 383 (3-4): 365-374. doi :10.1515/BC.2002.041. PMID 12033428. S2CID 7487557.
- ^ Korbecki J, Baranowska-Bosiacka I, Gutowska I, Chlubek D (2014). "Vías de la ciclooxigenasa". Acta Biochimica Polonica . 61 (4): 639–649. doi : 10.18388/abp.2014_1825 . PMID 25343148.
- ^ abcd Claar D, Hartert TV, Peebles RS (2015). "El papel de las prostaglandinas en la inflamación pulmonar alérgica y el asma". Expert Review of Respiratory Medicine . 9 (1): 55–72. doi :10.1586/17476348.2015.992783. PMC 4380345 . PMID 25541289.
- ^ Simopoulos AP (2010). "Variantes genéticas en el metabolismo de los ácidos grasos omega-6 y omega-3: su papel en la determinación de los requerimientos nutricionales y el riesgo de enfermedades crónicas". Experimental Biology and Medicine . 235 (7): 785–795. doi :10.1258/ebm.2010.009298. PMID 20558833. S2CID 207195131.
- ^ ab Surh YJ, Na HK, Park JM, Lee HN, Kim W, Yoon IS, Kim DD (2011). "15-Deoxy-Δ¹²,¹⁴-prostaglandina J₂, un mediador lipídico electrofílico de la señalización antiinflamatoria y pro-resolución". Farmacología bioquímica . 82 (10): 1335–1351. doi :10.1016/j.bcp.2011.07.100. PMID 21843512.
- ^ Powell, WS; Rokach, J (2013). "El quimioatrayente de eosinófilos 5-oxo-ETE y el receptor OXE". Progreso en la investigación de lípidos . 52 (4): 651–665. doi :10.1016/j.plipres.2013.09.001. PMC 5710732. PMID 24056189 .
- ^ Rådmark O, Werz O, Steinhilber D, Samuelsson B (2015). "5-Lipoxigenasa, una enzima clave para la biosíntesis de leucotrienos en la salud y la enfermedad". Biochimica et Biophysica Acta (BBA) - Biología molecular y celular de los lípidos . 1851 (4): 331–339. doi :10.1016/j.bbalip.2014.08.012. PMID 25152163.
- ^ Ahmad S, Thulasingam M, Palombo I, Daley DO, Johnson KA, Morgenstern R, Haeggström JZ, Rinaldo-Matthis A (2015). "La glutatión transferasa 2 microsomal trimérica muestra un tercio de la reactividad de los sitios". Biochimica et Biophysica Acta (BBA) - Proteínas y proteómica . 1854 (10 Pt A): 1365–1371. doi :10.1016/j.bbapap.2015.06.003. PMID 26066610.
- ^ Pace-Asciak, CR (2009). "Las hepoxilinas y algunos análogos: una revisión de su biología". British Journal of Pharmacology . 158 (4): 972–981. doi :10.1111/j.1476-5381.2009.00168.x. PMC 2785520 . PMID 19422397.
- ^ Dobrian, AD; Lieb, DC; Cole, BK; Taylor-Fishwick, DA; Chakrabarti, SK; Nadler, JL (2011). "Funciones funcionales y patológicas de las 12- y 15-lipoxigenasas". Progreso en la investigación de lípidos . 50 (1): 115–131. doi :10.1016/j.plipres.2010.10.005. PMC 3012140. PMID 20970452 .
- ^ Ivanov, I; Kuhn, H; Heydeck, D (2015). "Biología estructural y funcional de la 15-lipoxigenasa-1 del ácido araquidónico (ALOX15)". Gene . 573 (1): 1–32. doi :10.1016/j.gene.2015.07.073. PMC 6728142 . PMID 26216303.
- ^ Wittwer, J; Hersberger, M (2007). "Las dos caras de la 15-lipoxigenasa en la aterosclerosis". Prostaglandinas, leucotrienos y ácidos grasos esenciales . 77 (2): 67–77. doi :10.1016/j.plefa.2007.08.001. PMID 17869078.
- ^ Kroetz DL, Xu F (2005). "Regulación e inhibición de las omega-hidroxilasas del ácido araquidónico y la formación de 20-HETE". Revisión anual de farmacología y toxicología . 45 : 413–438. doi :10.1146/annurev.pharmtox.45.120403.100045. PMID 15822183.
- ^ ab Yang, L; Mäki-Petäjä, K; Cheriyan, J; McEniery, C; Wilkinson, IB (2015). "El papel de los ácidos epoxieicosatrienoicos en el sistema cardiovascular". British Journal of Clinical Pharmacology . 80 (1): 28–44. doi :10.1111/bcp.12603. PMC 4500322 . PMID 25655310.
- ^ abc Spector, AA; Kim, HY (2015). "Vía de la citocromo P450 epoxigenasa del metabolismo de los ácidos grasos poliinsaturados". Biochimica et Biophysica Acta (BBA) - Biología molecular y celular de los lípidos . 1851 (4): 356–365. doi :10.1016/j.bbalip.2014.07.020. PMC 4314516. PMID 25093613 .
- ^ Fer, M; Dréano, Y; Lucas, D; Corcos, L; Salaün, JP; Berthou, F; Amet, Y (2008). "Metabolismo de los ácidos eicosapentaenoico y docosahexaenoico por citocromos humanos recombinantes P450". Archivos de bioquímica y biofísica . 471 (2): 116–125. doi :10.1016/j.abb.2008.01.002. PMID 18206980.
- ^ ab Shahabi, P; Siest, G; Meyer, UA; Visvikis-Siest, S (2014). "Epoxigenasas del citocromo P450 humano: variabilidad en la expresión y función en trastornos relacionados con la inflamación". Farmacología y terapéutica . 144 (2): 134–161. doi :10.1016/j.pharmthera.2014.05.011. PMID 24882266.
- ^ Frömel, T; Kohlstedt, K; Popp, R; Yin, X; Awwad, K; Barbosa-Sicard, E; Thomas, AC; Lieberz, R; Mayr, M; Fleming, I (2013). "Citocromo P4502S1: una nueva epoxigenasa de ácidos grasos de monocitos/macrófagos en placas ateroscleróticas humanas". Investigación básica en cardiología . 108 (1): 319. doi :10.1007/s00395-012-0319-8. PMID 23224081. S2CID 9158244.
- ^ Fleming, I (2014). "La farmacología del eje citocromo P450 epoxigenasa/epóxido hidrolasa soluble en la vasculatura y la enfermedad cardiovascular". Pharmacological Reviews . 66 (4): 1106–1140. doi :10.1124/pr.113.007781. PMID 25244930. S2CID 39465144.
- ^ Westphal, C; Konkel, A; Schunck, WH (2011). "CYP-eicosanoides: ¿un nuevo vínculo entre los ácidos grasos omega-3 y la enfermedad cardíaca?". Prostaglandinas y otros mediadores lipídicos . 96 (1–4): 99–108. doi :10.1016/j.prostaglandins.2011.09.001. PMID 21945326.
- ^ Matsuoka T, Narumiya S (2007). "Señalización del receptor de prostaglandina en la enfermedad". TheScientificWorldJournal . 7 : 1329–1347. doi : 10.1100/tsw.2007.182 . PMC 5901339 . PMID 17767353.
- ^ Thomas J, Fairclough A, Kavanagh J, Kelly AJ (2014). "Prostaglandina vaginal (PGE2 y PGF2a) para la inducción del parto a término". Base de datos Cochrane de revisiones sistemáticas . 2014 (6): CD003101. doi :10.1002/14651858.CD003101.pub3. PMC 7138281. PMID 24941907 .
- ^ Rossi A, Anzalone A, Fortuna MC, Caro G, Garelli V, Pranteda G, Carlesimo M (2016). "Multiterapias en alopecia androgenética: revisión y experiencias clínicas". Dermatologic Therapy . 29 (6): 424–432. doi :10.1111/dth.12390. hdl : 11573/877469 . PMID 27424565. S2CID 45963890.
- ^ Garza LA, Liu Y, Yang Z, Alagesan B, Lawson JA, Norberg SM, Loy DE, Zhao T, Blatt HB, Stanton DC, Carrasco L, Ahluwalia G, Fischer SM, FitzGerald GA, Cotsarelis G (2012). "La prostaglandina D2 inhibe el crecimiento del cabello y se encuentra elevada en el cuero cabelludo calvo de hombres con alopecia androgénica". Science Translational Medicine . 4 (126): 126ra34. doi :10.1126/scitranslmed.3003122. PMC 3319975 . PMID 22440736.
- ^ ab Hata AN, Breyer RM (2004). "Farmacología y señalización de los receptores de prostaglandinas: múltiples funciones en la inflamación y la modulación inmunitaria". Farmacología y terapéutica . 103 (2): 147–166. doi :10.1016/j.pharmthera.2004.06.003. PMID 15369681.
- ^ ab Figueiredo-Pereira ME, Corwin C, Babich J (2016). "Prostaglandina J2: un objetivo potencial para detener la neurodegeneración inducida por la inflamación". Anales de la Academia de Ciencias de Nueva York . 1363 (1): 125–137. Bibcode :2016NYASA1363..125F. doi :10.1111/nyas.12987. PMC 4801700 . PMID 26748744.
- ^ Hoxha M, Buccellati C, Capra V, Garella D, Cena C, Rolando B, Fruttero R, Carnevali S, Sala A, Rovati GE, Bertinaria M (2016). "Evaluación farmacológica in vitro de agentes multiobjetivo para el antagonismo del receptor de prostanoides tromboxano y la inhibición de COX-2" (PDF) . Investigación farmacológica . 103 : 132–143. doi :10.1016/j.phrs.2015.11.012. hdl :2318/1551575. PMID 26621246. S2CID 12881002.
- ^ Cruz JE, Ward A, Anthony S, Chang S, Bae HB, Hermes-DeSantis ER (2016). "Evidencia del uso de epoprostenol para tratar el fenómeno de Raynaud con o sin úlceras digitales: una revisión de la literatura". Anales de farmacoterapia . 50 (12): 1060–1067. doi :10.1177/1060028016660324. PMID 27465880. S2CID 38333954.
- ^ O'Connell C, Amar D, Boucly A, Savale L, Jaïs X, Chaumais MC, Montani D, Humbert M, Simonneau G, Sitbon O (2016). "Seguridad y tolerabilidad comparativas de las prostaciclinas en la hipertensión pulmonar". Drug Safety . 39 (4): 287–294. doi :10.1007/s40264-015-0365-x. PMID 26748508. S2CID 24852012.
- ^ Cacione, Daniel G.; Macedo, Cristiane R.; do Carmo Novaes, Frederico; Baptista-Silva, Jose Cc (4 de mayo de 2020). "Tratamiento farmacológico de la enfermedad de Buerger". Base de Datos Cochrane de Revisiones Sistemáticas . 5 (5): CD011033. doi :10.1002/14651858.CD011033.pub4. ISSN 1469-493X. PMC 7197514 . PMID 32364620.
- ^ Citterio A, Arnoldi A, Panzeri E, D'Angelo MG, Filosto M, Dilena R, Arrigoni F, Castelli M, Maghini C, Germiniasi C, Menni F, Martinuzzi A, Bresolin N, Bassi MT (2014). "Las mutaciones en los genes CYP2U1, DDHD2 y GBA2 son causas raras de formas complicadas de paraparesia espástica hereditaria" (PDF) . Revista de Neurología . 261 (2): 373–381. doi :10.1007/s00415-013-7206-6. hdl :2434/421160. PMID 24337409. S2CID 19189811.
- ^ ab Liu M, Yokomizo T (2015). "El papel de los leucotrienos en las enfermedades alérgicas". Allergology International . 64 (1): 17–26. doi : 10.1016/j.alit.2014.09.001 . PMID 25572555.
- ^ Bäck M, Dahlén SE, Drazen JM, Evans JF, Serhan CN, Shimizu T, Yokomizo T, Rovati GE (2011). "Unión Internacional de Farmacología Básica y Clínica. LXXXIV: nomenclatura, distribución y funciones fisiopatológicas de los receptores de leucotrienos". Pharmacological Reviews . 63 (3): 539–584. doi : 10.1124/pr.110.004184 . PMID 21771892. S2CID 5563700.
- ^ Bäck M, Powell WS, Dahlén SE, Drazen JM, Evans JF, Serhan CN, Shimizu T, Yokomizo T, Rovati GE (2014). "Actualización sobre los receptores de leucotrienos, lipoxinas y oxoeicosanoides: Revisión IUPHAR 7". British Journal of Pharmacology . 171 (15): 3551–3574. doi :10.1111/bph.12665. PMC 4128057 . PMID 24588652.
- ^ Cingi C, Muluk NB, Ipci K, Şahin E (2015). "Antileucotrienos en enfermedades inflamatorias de las vías respiratorias superiores". Current Allergy and Asthma Reports . 15 (11): 64. doi :10.1007/s11882-015-0564-7. PMID 26385352. S2CID 38854822.
- ^ Nettis E, D'Erasmo M, Di Leo E, Calogiuri G, Montinaro V, Ferrannini A, Vacca A (2010). "El empleo de antagonistas de leucotrienos en enfermedades cutáneas pertenecientes al campo alergológico". Mediadores de la inflamación . 2010 : 1–6. doi : 10.1155/2010/628171 . PMC 2945673 . PMID 20886028.
- ^ Kanaoka Y, Maekawa A, Austen KF (2013). "Identificación de la proteína GPR99 como un tercer receptor potencial de cisteinil leucotrieno con preferencia por el ligando de leucotrieno E4". The Journal of Biological Chemistry . 288 (16): 10967–10972. doi : 10.1074/jbc.C113.453704 . PMC 3630866 . PMID 23504326.
- ^ abc Romano M, Cianci E, Simiele F, Recchiuti A (2015). "Lipoxinas y lipoxinas activadas por aspirina en la resolución de la inflamación". Revista Europea de Farmacología . 760 : 49–63. doi :10.1016/j.ejphar.2015.03.083. PMID 25895638.
- ^ abc Chiang N, Serhan CN, Dahlén SE, Drazen JM, Hay DW, Rovati GE, Shimizu T, Yokomizo T, Brink C (2006). "El receptor de lipoxina ALX: potentes acciones estereoselectivas y específicas del ligando in vivo". Pharmacological Reviews . 58 (3): 463–487. doi :10.1124/pr.58.3.4. PMID 16968948. S2CID 6496181.
- ^ Qu Q, Xuan W, Fan GH (2015). "Funciones de las resolvinas en la resolución de la inflamación aguda". Cell Biology International . 39 (1): 3–22. doi :10.1002/cbin.10345. PMID 25052386. S2CID 10160642.
- ^ Lim JY, Park CK, Hwang SW (2015). "Funciones biológicas de las resolvinas y sustancias relacionadas en la resolución del dolor". BioMed Research International . 2015 : 830930. doi : 10.1155/2015/830930 . PMC 4538417. PMID 26339646 .
- ^ ab Serhan CN, Chiang N, Dalli J, Levy BD (2015). "Mediadores lipídicos en la resolución de la inflamación". Cold Spring Harbor Perspectives in Biology . 7 (2): a016311. doi :10.1101/cshperspect.a016311. PMC 4315926 . PMID 25359497.
- ^ Serhan CN, Chiang N (2013). "Mediadores lipídicos de la inflamación en fase de resolución: agonistas de la resolución". Current Opinion in Pharmacology . 13 (4): 632–640. doi :10.1016/j.coph.2013.05.012. PMC 3732499 . PMID 23747022.
- ^ Yang L, Mäki-Petäjä K, Cheriyan J, McEniery C, Wilkinson IB (2015). "El papel de los ácidos epoxieicosatrienoicos en el sistema cardiovascular". British Journal of Clinical Pharmacology . 80 (1): 28–44. doi :10.1111/bcp.12603. PMC 4500322 . PMID 25655310.
- ^ Número de ensayo clínico NCT00847899 para "Evaluación del inhibidor de la epóxido hidrolasa soluble (s-EH) en pacientes con hipertensión leve a moderada y tolerancia a la glucosa deteriorada" en ClinicalTrials.gov
- ^ Bos C, Richel D, Ritsema T, Peppelenbosch M, Versteeg H (2004). "Prostanoides y receptores de prostanoides en la transducción de señales". Int J Biochem Cell Biol . 36 (7): 1187-1205. doi :10.1016/j.biocel.2003.08.006. PMID 15109566.
- ^ Samuelsson B (mayo de 1983). "Leucotrienos: mediadores de las reacciones de hipersensibilidad inmediata y de la inflamación". Science . 220 (4597): 568–575. Bibcode :1983Sci...220..568S. doi :10.1126/science.6301011. PMID 6301011.
- ^ Haeggström JZ, Funk CD (2011). "Vías de la lipooxigenasa y los leucotrienos: bioquímica, biología y funciones en la enfermedad". Chemical Reviews . 111 (10): 5866–5898. doi :10.1021/cr200246d. PMID 21936577.[ enlace muerto permanente ]
- ^ Anwar Y, Sabir JS, Qureshi MI, Saini KS (2014). "5-lipoxigenasa: un prometedor objetivo farmacológico contra enfermedades inflamatorias: regulación bioquímica y farmacológica". Current Drug Targets . 15 (4): 410–422. doi :10.2174/1389450114666131209110745. PMID 24313690.
- ^ Kar M, Altıntoprak N, Muluk NB, Ulusoy S, Bafaqeeh SA, Cingi C (marzo de 2016). "Antileucotrienos en la hipertrofia adenoamigdalina: una revisión de la literatura". Archivos europeos de otorrinolaringología . 273 (12): 4111–4117. doi :10.1007/s00405-016-3983-8. PMID 26980339. S2CID 31311115.
- ^ Oussalah A, Mayorga C, Blanca M, Barbaud A, Nakonechna A, Cernadas J, Gotua M, Brockow K, Caubet JC, Bircher A, Atanaskovic M, Demoly P, K Tanno L, Terreehorst I, Laguna JJ, Romano A, Guéant JL (abril de 2016). "Variantes genéticas asociadas con reacciones de hipersensibilidad inmediata inducidas por fármacos: una revisión sistemática compatible con PRISMA". Alergia . 71 (4): 443–462. doi : 10.1111/todos.12821 . PMID 26678823. S2CID 13352894.
- ^ Mitchell S, Balp MM, Samuel M, McBride D, Maurer M (2015). "Revisión sistemática de los tratamientos para la urticaria crónica espontánea con respuesta inadecuada a los tratamientos de primera línea autorizados". Revista Internacional de Dermatología . 54 (9): 1088–1104. doi :10.1111/ijd.12727. PMID 25515967. S2CID 23250789.
- ^ Wu SH, Chen XQ, Liu B, Wu HJ, Dong L (2013). "Eficacia y seguridad de la 15(R/S)-metil-lipoxina A(4) en el tratamiento tópico del eczema infantil". The British Journal of Dermatology . 168 (1): 172–178. doi :10.1111/j.1365-2133.2012.11177.x. PMID 22834636. S2CID 31721094.
- ^ ab Basil MC, Levy BD (2016). "Mediadores pro-resolución especializados: reguladores endógenos de la infección y la inflamación". Nature Reviews. Inmunología . 16 (1): 51–67. doi :10.1038/nri.2015.4. PMC 5242505 . PMID 26688348.
- ^ Feltenmark S, Gautam N, Brunnström A, Griffiths W, Backman L, Edenius C, Lindbom L, Björkholm M, Claesson HE (enero de 2008). "Las eoxinas son metabolitos proinflamatorios del ácido araquidónico producidos a través de la vía de la 15-lipoxigenasa-1 en los eosinófilos y mastocitos humanos". Proc. Natl. Sci. EE. UU . . 105 (2): 680–685. Bibcode :2008PNAS..105..680F. doi : 10.1073/pnas.0710127105 . PMC 2206596 . PMID 18184802.
- ^ James A, Daham K, Backman L, Brunnström A, Tingvall T, Kumlin M, Edenius C, Dahlén SE, Dahlén B, Claesson HE (2013). "La influencia de la aspirina en la liberación de eoxina C4, leucotrieno C4 y 15-HETE, en granulocitos eosinofílicos aislados de pacientes con asma". Int. Arch. Allergy Immunol . 162 (2): 135–142. doi :10.1159/000351422. PMID 23921438. S2CID 29180895.
- ^ Claesson HE (2009). "Sobre la biosíntesis y el papel biológico de las eoxinas y la 15-lipoxigenasa-1 en la inflamación de las vías respiratorias y el linfoma de Hodgkin". Prostaglandinas y otros mediadores lipídicos . 89 (3–4): 120–125. doi :10.1016/j.prostaglandins.2008.12.003. PMID 19130894.
- ^ Serhan CN, Chiang N, Dalli J (2015). "El código de resolución de la inflamación aguda: nuevos mediadores lipídicos pro-resolutivos en la resolución". Seminarios en Inmunología . 27 (3): 200–215. doi :10.1016/j.smim.2015.03.004. PMC 4515371 . PMID 25857211.
- ^ Guichardant M, Calzada C, Bernoud-Hubac N, Lagarde M, Véricel E (2015). "Ácidos grasos poliinsaturados omega-3 y metabolismo oxigenado en la aterotrombosis". Biochimica et Biophysica Acta (BBA) - Biología molecular y celular de los lípidos . 1851 (4): 485–495. doi :10.1016/j.bbalip.2014.09.013. PMID 25263947.
- ^ Calder PC (2014). "Biomarcadores de inmunidad e inflamación para su uso en intervenciones nutricionales: trabajo de la rama europea del Instituto Internacional de Ciencias de la Vida sobre criterios de selección e interpretación". Objetivos farmacológicos para trastornos endocrinos, metabólicos e inmunológicos . 14 (4): 236–244. doi :10.2174/1871530314666140709091650. PMID 25008763.
- ^ ab Fritsche, Kevin (agosto de 2006). "Ácidos grasos como moduladores de la respuesta inmunitaria". Revista anual de nutrición . 26 : 45–73. doi :10.1146/annurev.nutr.25.050304.092610. PMID 16848700.
- ^ Instituto Nacional de Salud (1 de agosto de 2005). «Ácidos grasos omega-3, aceite de pescado, ácido alfa-linolénico». Archivado desde el original el 3 de mayo de 2006. Consultado el 26 de marzo de 2006 .
- ^ Thompson, Dennis (2 de agosto de 2024). "El aceite de pescado podría ayudar a los adultos mayores con alto riesgo a evitar el Alzheimer". www.healthday.com . Consultado el 6 de agosto de 2024 .
- ^ Shinto, Lynne H.; Murchison, Charles F.; Silbert, Lisa C.; Dodge, Hiroko H.; Lahna, David; Rooney, William; Kaye, Jeffrey; Quinn, Joseph F.; Bowman, Gene L. (1 de agosto de 2024). "ω-3 PUFA para la prevención secundaria de lesiones de la sustancia blanca y deterioro de la integridad neuronal en adultos mayores: un ensayo clínico aleatorizado". JAMA Network Open . 7 (8): e2426872. doi :10.1001/jamanetworkopen.2024.26872. ISSN 2574-3805. PMC 11294966 . PMID 39088212.
- ^ Burr, GO; Burr, MM (1930). "Sobre la naturaleza y el papel de los ácidos grasos esenciales en la nutrición". J. Biol. Chem . 86 (587): 587–621. doi : 10.1016/S0021-9258(20)78929-5 .
- ^ Bergström, S.; Danielsson, H.; Samuelsson, B. (1964). "La formación enzimática de prostaglandina E2 a partir de ácido araquidónico". Biochim. Biophys. Acta . 90 (207): 207–210. doi :10.1016/0304-4165(64)90145-x. PMID 14201168.
- ^ Vane, JR (23 de junio de 1971). "Inhibición de la síntesis de prostaglandinas como mecanismo de acción de fármacos similares a la aspirina". Nature New Biology . 231 (25): 232–235. doi :10.1038/newbio231232a0. PMID 5284360.
Enlaces externos
- Eicosanoides en los encabezados de materias médicas (MeSH) de la Biblioteca Nacional de Medicina de EE. UU.