Leucotrieno
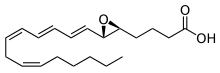




Los leucotrienos son una familia de mediadores inflamatorios eicosanoides producidos en los leucocitos por la oxidación del ácido araquidónico (AA) y del ácido graso esencial ácido eicosapentaenoico (EPA) por la enzima araquidonato 5-lipoxigenasa . [1] [2] [3]
Los leucotrienos utilizan la señalización lipídica para transmitir información a la célula que los produce ( señalización autocrina ) o a las células vecinas ( señalización paracrina ) con el fin de regular las respuestas inmunitarias. La producción de leucotrienos suele ir acompañada de la producción de histamina y prostaglandinas , que también actúan como mediadores inflamatorios. [4]
Una de sus funciones (específicamente, el leucotrieno D 4 ) es desencadenar contracciones en los músculos lisos que recubren los bronquiolos; su sobreproducción es una causa importante de inflamación en el asma y la rinitis alérgica . [5] Los antagonistas de los leucotrienos se utilizan para tratar estos trastornos al inhibir la producción o actividad de los leucotrienos. [6]
Historia y nombre
El nombre leucotrieno , introducido por el bioquímico sueco Bengt Samuelsson en 1979, proviene de las palabras leucocito y trieno (que indican los tres enlaces dobles conjugados del compuesto ). Lo que más tarde se llamaría leucotrieno C, "sustancia estimulante del músculo liso de reacción lenta" ( SRS ), fue descrito originalmente entre 1938 y 1940 por Feldberg y Kellaway. [7] [8] [9] Los investigadores aislaron la SRS del tejido pulmonar después de un período prolongado tras la exposición al veneno de serpiente y la histamina. [9]
Tipos
Leucotrienos cisteinílicos
LTC 4 , LTD 4 , LTE 4 y LTF 4 a menudo se denominan leucotrienos cisteinílicos debido a la presencia del aminoácido cisteína en su estructura. Los leucotrienos cisteinílicos constituyen la sustancia de reacción lenta de la anafilaxia (SRS-A). LTF 4 , al igual que LTD 4 , es un metabolito de LTC 4 , pero, a diferencia de LTD 4 , que carece del residuo glutámico del glutatión , LTF 4 carece del residuo de glicina del glutatión. [10]
LTB4
El LTB 4 se sintetiza in vivo a partir del LTA 4 por la enzima LTA 4 hidrolasa . Su función principal es reclutar neutrófilos a las zonas de daño tisular, aunque también ayuda a promover la producción de citocinas inflamatorias por parte de diversas células inmunitarias. Los fármacos que bloquean las acciones del LTB 4 han demostrado cierta eficacia para frenar la progresión de las enfermedades mediadas por los neutrófilos. [11]
Larga vida4
También se ha postulado la existencia de LTG 4 , un metabolito de LTE 4 en el que la fracción cisteinílica se ha oxidado a un alfa-cetoácido (es decir, la cisteína se ha reemplazado por un piruvato ). Se sabe muy poco sobre este supuesto leucotrieno. [ cita requerida ]
LTB5
Los leucotrienos originados a partir del ácido eicosapentaenoico (EPA) de la clase omega-3 han disminuido los efectos inflamatorios. En sujetos humanos cuyas dietas han sido suplementadas con ácido eicosapentaenoico, la leucotrina B5, junto con la leucotrina B4, es producida por los neutrófilos. [12] El LTB 5 induce la agregación de neutrófilos de rata , la quimiocinesis de neutrófilos polimorfonucleares humanos (PMN), la liberación de enzimas lisosomales de PMN humanos y la potenciación de la exudación plasmática inducida por bradicinina, aunque en comparación con el LTB 4 , tiene al menos 30 veces menos potencia. [13]
Bioquímica
Síntesis
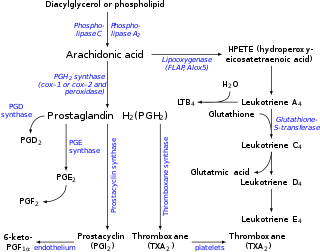
Los leucotrienos se sintetizan en la célula a partir del ácido araquidónico por acción de la enzima araquidonato 5-lipoxigenasa . El mecanismo catalítico implica la inserción de una fracción de oxígeno en una posición específica de la cadena principal del ácido araquidónico. [ cita requerida ]
La vía de la lipoxigenasa está activa en los leucocitos y otras células inmunocompetentes, incluidos los mastocitos , los eosinófilos , los neutrófilos , los monocitos y los basófilos . Cuando se activan dichas células, la fosfolipasa A2 libera ácido araquidónico de los fosfolípidos de la membrana celular y la proteína activadora de la 5-lipoxigenasa (FLAP) lo dona a la 5-lipoxigenasa. [ cita requerida ]
La 5- lipoxigenasa (5-LO) utiliza FLAP para convertir el ácido araquidónico en ácido 5-hidroperoxieicosatetraenoico (5-HPETE), que se reduce espontáneamente a ácido 5-hidroxieicosatetraenoico (5-HETE). La enzima 5-LO actúa de nuevo sobre el 5-HETE para convertirlo en leucotrieno A 4 (LTA 4 ), un epóxido inestable. El 5-HETE puede metabolizarse aún más a 5-oxo-ETE y 5-oxo-15-hidroxi-ETE, todos los cuales tienen acciones proinflamatorias similares pero no idénticas a las del LTB 4 y mediadas no por los receptores LTB 4 sino por el receptor OXE (ver ácido 5-hidroxieicosatetraenoico y ácido 5-oxo-eicosatetraenoico ). [14] [15]
En las células equipadas con LTA hidrolasa , como los neutrófilos y los monocitos, la LTA 4 se convierte en el leucotrieno dihidroxiácido LTB 4 , que es un potente quimioatrayente para los neutrófilos que actúa en los receptores BLT 1 y BLT 2 en la membrana plasmática de estas células. [ cita requerida ]
En las células que expresan la sintetasa LTC 4 , como los mastocitos y los eosinófilos, la LTA 4 se conjuga con el tripéptido glutatión para formar el primero de los cisteinil-leucotrienos, LTC 4 . Fuera de la célula, la LTC 4 puede ser convertida por enzimas ubicuas para formar sucesivamente LTD 4 y LTE 4 , que conservan la actividad biológica . [ cita requerida ]
Los cisteinil-leucotrienos actúan en sus receptores de superficie celular CysLT1 y CysLT2 en las células diana para contraer el músculo liso bronquial y vascular, aumentar la permeabilidad de los vasos sanguíneos pequeños, mejorar la secreción de moco en las vías respiratorias y el intestino y reclutar leucocitos a los sitios de inflamación. [ cita requerida ]
Tanto el LTB 4 como los cisteinil-leucotrienos (LTC 4 , LTD 4 , LTE 4 ) se degradan parcialmente en los tejidos locales y, en última instancia, se convierten en metabolitos inactivos en el hígado. [ cita requerida ]
Función
Los leucotrienos actúan principalmente sobre una subfamilia de receptores acoplados a la proteína G. También pueden actuar sobre los receptores activados por el proliferador de peroxisomas . Los leucotrienos están involucrados en reacciones alérgicas y asmáticas y actúan para mantener las reacciones inflamatorias. Varios antagonistas del receptor de leucotrienos, como el montelukast y el zafirlukast , se utilizan para tratar el asma . Investigaciones recientes apuntan a un papel de la 5-lipoxigenasa en enfermedades cardiovasculares y neuropsiquiátricas. [16]
Los leucotrienos son agentes muy importantes en la respuesta inflamatoria . Algunos, como el LTB 4, tienen un efecto quimiotáctico sobre los neutrófilos migratorios y, por lo tanto, ayudan a llevar las células necesarias al tejido. Los leucotrienos también tienen un efecto poderoso en la broncoconstricción y aumentan la permeabilidad vascular . [17]
Leucotrienos en el asma
Los leucotrienos contribuyen a la fisiopatología del asma , especialmente en pacientes con enfermedad respiratoria exacerbada por aspirina (EREA), y causan o potencian los siguientes síntomas : [18]
- Obstrucción del flujo de aire
- Aumento de la secreción de moco.
- Acumulación de mucosa
- Broncoconstricción
- Infiltración de células inflamatorias en la pared de las vías respiratorias.
Papel de los leucotrienos cisteinílicos
Los receptores de leucotrienos cisteinílicos CYSLTR1 y CYSLTR2 están presentes en los mastocitos, los eosinófilos y las células endoteliales. Durante la interacción de los leucotrienos cisteinílicos, pueden estimular actividades proinflamatorias como la adherencia de las células endoteliales y la producción de quimiocinas por los mastocitos. Además de mediar la inflamación, inducen asma y otros trastornos inflamatorios, reduciendo así el flujo de aire a los alvéolos . Se ha informado que los niveles de leucotrienos cisteinílicos, junto con 8-isoprostano , aumentan en el EBC de pacientes con asma , lo que se correlaciona con la gravedad de la enfermedad. [19] Los leucotrienos cisteinílicos también pueden desempeñar un papel en las reacciones adversas a los medicamentos en general y en las reacciones adversas inducidas por el medio de contraste en particular. [20]
En exceso, los leucotrienos cisteinílicos pueden inducir un shock anafiláctico . [21]
Leucotrienos en la demencia
En estudios con animales se ha descubierto que los leucotrienos desempeñan un papel importante en las últimas etapas de la enfermedad de Alzheimer y demencias relacionadas. En ratones transgénicos tau, que desarrollan patología tau , se ha descubierto que el " zileutón " , un fármaco que inhibe la formación de leucotrienos al bloquear la enzima 5-lipoxigenasa ", revierte la pérdida de memoria . [22]
Véase también
- Síntesis química del éster metílico del leucotrieno A
- Eoxinas (14,15-leucotrienos)
Referencias
- ^ Loick, H.; Theissen, J. (1994). "Die Eicosanoide als Mediatoren beim ARDS" [Eicosanoides como mediadores en el SDRA]. Anästhesiologie, Intensivmedizin, Notfallmedizin, Schmerztherapie (en alemán). 29 (1): 3–9. doi :10.1055/s-2007-996677. PMID 8142566.
- ^ Salmon, John A; Higgs, Gerald A (1987). "Prostaglandinas y leucotrienos como mediadores inflamatorios". British Medical Bulletin . 43 (2): 285–96. doi :10.1093/oxfordjournals.bmb.a072183. PMID 2825898.
- ^ O'Byrne, Paul M.; Israel, Elliot; Drazen, Jeffrey M. (1997). "Antileucotrienos en el tratamiento del asma". Anales de Medicina Interna . 127 (6): 472–80. doi :10.7326/0003-4819-127-6-199709150-00009. PMID 9313005. S2CID 21480605.
- ^ White, Martha (1999). "Mediadores de la inflamación y el proceso inflamatorio". The Journal of Allergy and Clinical Immunology . 103 (3 Pt 2): S378-81. doi : 10.1016/S0091-6749(99)70215-0 . PMID 10069896 . Consultado el 8 de junio de 2019 .
- ^ Nelson, David L.; Cox, Michael M. (2008). "Leucotrienos". Principios de bioquímica de Lehninger (5.ª ed.). Macmillan. pág. 359. ISBN 978-0-7167-7108-1.
- ^ Scott JP, Peters-Golden M (septiembre de 2018). "Agentes antileucotrienos para el tratamiento de la enfermedad pulmonar". Am. J. Respir. Crit. Care Med . 188 (5): 538–544. doi :10.1164/rccm.201301-0023PP. PMID 23822826.
- ^ Feldberg, W.; Kellaway, CH (1938). "Liberación de histamina y formación de sustancias similares a la lisocitina por el veneno de cobra". The Journal of Physiology . 94 (2): 187–226. doi :10.1113/jphysiol.1938.sp003674. PMC 1393616 . PMID 16995038.
- ^ Feldberg, W.; Holden, HF; Kellaway, CH (1938). "La formación de lisocitina y de una sustancia estimulante de los músculos por venenos de serpiente". The Journal of Physiology . 94 (2): 232–48. doi :10.1113/jphysiol.1938.sp003676. PMC 1393612 . PMID 16995040.
- ^ ab Kellaway, CH; Trethewie, ER (1940). "La liberación de una sustancia estimulante del músculo liso de reacción lenta en la anafilaxia". Revista trimestral de fisiología experimental y ciencias médicas afines . 30 (2): 121–145. doi : 10.1113/expphysiol.1940.sp000825 . ISSN 1469-445X.
- ^ Consultado en Internet el 24 de abril de 2012 [ cita completa necesaria ]
- ^ Crooks, SW; Stockley, RA (1998). "Leucotrieno B4". Revista internacional de bioquímica y biología celular . 30 (2): 173–8. doi :10.1016/S1357-2725(97)00123-4. PMID 9608670. S2CID 45983006.
- ^ von Schacky, C; Fahrer, C; Fischer, S (octubre de 1990). "Catabolismo del leucotrieno B5 en humanos". Journal of Lipid Research . 31 (10): 1831–1838. doi : 10.1016/S0022-2275(20)42326-0 . PMID 1964169 . Consultado el 16 de enero de 2023 .
- ^ Terano, Takashi; Salmon, John A.; Moncada, Salvador (1984). "Biosíntesis y actividad biológica del leucotrieno B5". Prostaglandinas . 27 (2): 217–32. doi :10.1016/0090-6980(84)90075-3. PMID 6326200.
- ^ O'Flaherty, Joseph T.; Taylor, Jennifer S.; Thomas, Michael J. (1998). "Receptores para la clase 5-oxo de eicosanoides en neutrófilos". The Journal of Biological Chemistry . 273 (49): 32535–41. doi : 10.1074/jbc.273.49.32535 . PMID 9829988.
- ^ Powell, William S.; Rokach, Joshua (2013). "El quimioatrayente de eosinófilos 5-oxo-ETE y el receptor OXE". Progreso en la investigación de lípidos . 52 (4): 651–65. doi :10.1016/j.plipres.2013.09.001. PMC 5710732 . PMID 24056189.
- ^ Manev, Radmila; Manev, Hari (2004). "5-lipoxigenasa como posible vínculo entre trastornos cardiovasculares y psiquiátricos". Critical Reviews in Neurobiology . 16 (1–2): 181–6. doi :10.1615/CritRevNeurobiol.v16.i12.190. PMID 15581413.
- ^ Dahlén, Sven-Erik; Bjork, Jakob; Hedqvist, Per; Arfors, Karl-E.; Hammarstrom, Sven; Lindgren, Jan-Åke; Samuelsson, Bengt (1981). "Los leucotrienos promueven la fuga de plasma y la adhesión de leucocitos en las vénulas poscapilares: efectos in vivo relevantes para la respuesta inflamatoria aguda". Actas de la Academia Nacional de Ciencias . 78 (6): 3887–91. Código bibliográfico : 1981PNAS...78.3887D. doi : 10.1073/pnas.78.6.3887 . JSTOR 10943. PMC 319678 . PID 6267608.
- ^ Berger, A. (1999). "Comentario científico: ¿Qué son los leucotrienos y cómo funcionan en el asma?". BMJ . 319 (7202): 90. doi :10.1136/bmj.319.7202.90. PMC 1116241 . PMID 10398630.
- ^ Samitas, Konstantinos; Chorianopoulos, Dimitrios; Vittorakis, Stelios; Zervas, Eleftherios; Economidou, Erasmia; Papatheodorou, George; Loukides, Stelios; Gaga, Mina (2009). "Cisteinil-leucotrienos y 8-isoprostano exhalados en pacientes con asma y su relación con la gravedad clínica". Medicina Respiratoria . 103 (5): 750–6. doi : 10.1016/j.rmed.2008.11.009 . PMID 19110408.
- ^ Böhm, Ingrid; Speck, Ulrich; Schild, Hans (2005). "Un posible papel de los cisteinil-leucotrienos en las reacciones adversas inducidas por medios de contraste no iónicos". Revista Europea de Radiología . 55 (3): 431–6. doi :10.1016/j.ejrad.2005.01.007. PMID 16129253.
- ^ Brocklehurst, WE (1960). "Liberación de histamina y formación de una sustancia de reacción lenta (SRS-A) durante el shock anafiláctico". The Journal of Physiology . 151 (3): 416–35. doi :10.1113/jphysiol.1960.sp006449. PMC 1363273 . PMID 13804592.
- ^ "Investigadores de Temple revierten el deterioro cognitivo en ratones con demencia". Eurekalart! . 8 de junio de 2018.
Lectura adicional
- Bailey, J. Martyn (1985) Prostaglandinas, leucotrienos y lipoxinas: bioquímica, mecanismo de acción y aplicaciones clínicas Plenum Press, Nueva York, ISBN 0-306-41980-7
- Lipkowitz, Myron A. y Navarra, Tova (2001) The Encyclopedia of Allergies (2.ª ed.) Facts on File, Nueva York, pág. 167, ISBN 0-8160-4404-X
- Samuelsson, Bengt (ed.) (2001) Avances en la investigación de prostaglandinas y leucotrienos: ciencia básica y nuevas aplicaciones clínicas: 11.ª Conferencia internacional sobre avances en la investigación de prostaglandinas y leucotrienos: ciencia básica y nuevas aplicaciones clínicas, Florencia, Italia, 4 al 8 de junio de 2000 Kluwer Academic Publishers, Dordrecht, ISBN 1-4020-0146-0
Enlaces externos
- Leucotrienos en los encabezados de materias médicas (MeSH) de la Biblioteca Nacional de Medicina de EE. UU.