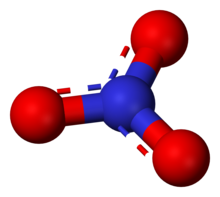
Nitrato
 | |
| Nombres | |
|---|---|
| Nombre sistemático de la IUPAC Nitrato | |
| Identificadores | |
Modelo 3D ( JSmol ) |
|
| EBICh |
|
| Araña química |
|
Identificador de centro de PubChem |
|
| UNIVERSIDAD | |
Panel de control CompTox ( EPA ) |
|
| |
| |
| Propiedades | |
| NO− 3 | |
| Masa molar | 62,004 g·mol −1 |
| Ácido conjugado | Ácido nítrico |
Salvo que se indique lo contrario, los datos se proporcionan para los materiales en su estado estándar (a 25 °C [77 °F], 100 kPa). | |
El nitrato es un ion poliatómico con la fórmula química NO−
3Las sales que contienen este ion se denominan nitratos . Los nitratos son componentes comunes de fertilizantes y explosivos. [1] Casi todos los nitratos inorgánicos son solubles en agua . Un ejemplo de nitrato insoluble es el oxinitrato de bismuto .
Estructura química

El anión nitrato es la base conjugada del ácido nítrico , que consiste en un átomo de nitrógeno central rodeado por tres átomos de oxígeno enlazados de manera idéntica en una disposición plana trigonal . El ion nitrato tiene una carga formal de −1. [ cita requerida ] Esta carga resulta de una carga formal combinada en la que cada uno de los tres oxígenos tiene una carga de − 2 ⁄ 3 , [ cita requerida ] mientras que el nitrógeno tiene una carga de +1, todas estas sumadas forman la carga formal del ion nitrato poliatómico. [ cita requerida ] Esta disposición se usa comúnmente como un ejemplo de resonancia . Al igual que el ion carbonato isoelectrónico , el ion nitrato puede representarse mediante tres estructuras de resonancia:
Propiedades químicas y bioquímicas
En el NO−3anión, el estado de oxidación del átomo de nitrógeno central es V (+5). Esto corresponde al mayor número de oxidación posible del nitrógeno. El nitrato es un oxidante potencialmente poderoso como lo demuestra su comportamiento explosivo a alta temperatura cuando se detona en nitrato de amonio ( NH 4 NO 3 ), o pólvora negra , encendida por la onda de choque de un explosivo primario . Sin embargo, en contraste con el ácido nítrico fumante rojo ( HNO 3 /N 2 O 4 ), o el ácido nítrico concentrado ( HNO 3 ), el nitrato disuelto en solución acuosa a pH neutro o alto es solo un agente oxidante débil y es estable en condiciones estériles o asépticas , en ausencia de microorganismos . Para aumentar su poder de oxidación, se necesitan condiciones ácidas y altas concentraciones, bajo las cuales el nitrato se transforma en ácido nítrico. Este comportamiento es consistente con la teoría general de reducción-oxidación (redox) en electroquímica : el poder oxidante se exacerba en condiciones ácidas mientras que el poder de los agentes reductores se refuerza en condiciones básicas. Esto se puede ilustrar mediante un diagrama de Pourbaix (diagrama E h –pH) dibujado usando la ecuación de Nernst y las reacciones redox correspondientes. Durante la reducción de oxidantes, el estado de oxidación disminuye y los iones óxido ( O 2− ) en exceso liberados en agua por la reacción se protonan más fácilmente en condiciones ácidas ( O 2− + 2 H + → H 2 O ) lo que impulsa la reacción de reducción hacia la derecha de acuerdo con el principio de Le Chatelier . Para la oxidación de agentes reductores, ocurre lo contrario: a medida que aumenta el estado de oxidación, se necesitan aniones óxido para neutralizar el exceso de cargas positivas soportadas por el átomo central. Como las condiciones básicas favorecen la producción de aniones óxido ( 2 OH − → O 2− + H 2 O ), esto impulsa el equilibrio químico de la reacción de oxidación hacia la derecha.
Mientras tanto, el nitrato se utiliza como un potente aceptor terminal de electrones por parte de las bacterias desnitrificantes para entregarles la energía que necesitan para prosperar. En condiciones anaeróbicas , el nitrato es el aceptor de electrones más fuerte que utilizan los microorganismos procariotas ( bacterias y arqueas ) para respirar. El par redox NO−3/ N 2 está en la parte superior de la escala redox para la respiración anaeróbica , justo debajo del par oxígeno ( O 2 / H 2 O ), pero por encima de los pares Mn (IV) / Mn (II), Fe (III) / Fe (II), SO2−4/ HS − , CO 2 / CH 4 . En aguas naturales, inevitablemente contaminadas por microorganismos, el nitrato es una especie química disuelta bastante inestable y lábil porque es metabolizada por bacterias desnitrificantes. Las muestras de agua para análisis de nitrato/nitrito deben conservarse a 4 °C en una cámara refrigerada y analizarse lo más rápido posible para limitar la pérdida de nitrato.
En el primer paso del proceso de desnitrificación, el nitrato disuelto ( NO−3) se reduce catalíticamente a nitrito ( NO−2) por la actividad enzimática de las bacterias. En solución acuosa, el nitrito disuelto, N(III), es un oxidante más potente que el nitrato, N(V), porque tiene que aceptar menos electrones y su reducción está menos obstaculizada cinéticamente que la del nitrato.
Durante el proceso de desnitrificación biológica, la reducción adicional de nitrito también da lugar a otro potente agente oxidante: el óxido nítrico (NO). El NO puede fijarse en la mioglobina acentuando su coloración roja. El NO es una importante molécula de señalización biológica e interviene en el proceso de vasodilatación , pero también puede producir radicales libres en los tejidos biológicos , acelerando su proceso de degradación y envejecimiento. Las especies reactivas de oxígeno (ROS) generadas por el NO contribuyen al estrés oxidativo , una condición involucrada en la disfunción vascular y la aterogénesis . [2]
Detección en análisis químicos
El anión nitrato se analiza comúnmente en agua mediante cromatografía iónica (CI) junto con otros aniones también presentes en solución. La principal ventaja de la CI es su facilidad y el análisis simultáneo de todos los aniones presentes en la muestra acuosa. Otros métodos para la detección específica de nitrato se basan en su conversión a nitrito seguida de pruebas específicas de nitrito. La reducción de nitrato a nitrito se efectúa mediante un material de cobre - cadmio . La muestra se introduce en un analizador de inyección de flujo y el efluente resultante que contiene nitrito se combina luego con un reactivo para detección colorimétrica o electroquímica. El más popular de estos ensayos es la prueba de Griess , mediante la cual el nitrito se convierte en un colorante azo de color intenso adecuado para el análisis espectroscópico UV-vis. El método explota la reactividad del ácido nitroso derivado de la acidificación del nitrito. El ácido nitroso reacciona selectivamente con aminas aromáticas para dar sales de diazonio, que a su vez se acoplan con un segundo reactivo para dar el colorante azo. El límite de detección es de 0,02 a 2 μM. [3] Estos métodos se han adaptado altamente a las muestras biológicas. [4]
Ocurrencia y producción
Las sales de nitrato se encuentran de forma natural en la Tierra en ambientes áridos en forma de grandes depósitos, particularmente de nitratina , una fuente importante de nitrato de sodio .
Los nitratos son producidos por diversas especies de bacterias nitrificantes en el medio natural utilizando amoniaco o urea como fuente de nitrógeno y fuente de energía libre. Los compuestos de nitrato para la pólvora se producían históricamente, en ausencia de fuentes minerales de nitrato, mediante diversos procesos de fermentación utilizando orina y estiércol.
Los rayos que caen en la atmósfera terrestre, rica en nitrógeno y oxígeno, producen una mezcla de óxidos de nitrógeno, que forman iones nitrosos e iones nitrato, que son arrastrados de la atmósfera por la lluvia o en deposición oculta .
Los nitratos se producen industrialmente a partir del ácido nítrico . [1]
Usos
Agricultura
El nitrato es un compuesto químico que sirve como forma primaria de nitrógeno para muchas plantas. Este nutriente esencial es utilizado por las plantas para sintetizar proteínas, ácidos nucleicos y otras moléculas orgánicas vitales. [5] La transformación del nitrógeno atmosférico en nitrato es facilitada por ciertas bacterias y rayos en el ciclo del nitrógeno, lo que ejemplifica la capacidad de la naturaleza para convertir una molécula relativamente inerte en una forma que es crucial para la productividad biológica. [6]
Los nitratos se utilizan como fertilizantes en la agricultura debido a su alta solubilidad y biodegradabilidad. Los principales fertilizantes a base de nitratos son las sales de amonio , sodio , potasio , calcio y magnesio . Se producen varios miles de millones de kilogramos al año para este propósito. [1] La importancia del nitrato se extiende más allá de su papel como nutriente, ya que actúa como una molécula de señalización en las plantas, regulando procesos como el crecimiento de las raíces, la floración y el desarrollo de las hojas. [7]
Si bien el nitrato es beneficioso para la agricultura, ya que mejora la fertilidad del suelo y el rendimiento de los cultivos, su uso excesivo puede provocar la pérdida de nutrientes, la contaminación del agua y la proliferación de zonas acuáticas muertas. [8] Por lo tanto, son necesarias prácticas agrícolas sostenibles que equilibren la productividad con el cuidado del medio ambiente. La importancia del nitrato en los ecosistemas es evidente, ya que apoya el crecimiento y el desarrollo de las plantas, contribuyendo a la biodiversidad y al equilibrio ecológico. [9]
Armas de fuego
Los nitratos se utilizan como agentes oxidantes , sobre todo en explosivos , donde la rápida oxidación de compuestos de carbono libera grandes volúmenes de gases (véase la pólvora como ejemplo).
Industrial
El nitrato de sodio se utiliza para eliminar las burbujas de aire del vidrio fundido y de algunos materiales cerámicos . Se utilizan mezclas de sales fundidas para endurecer la superficie de algunos metales. [1]
Película fotográfica
El nitrato también se utilizó como material de película a través de la nitrocelulosa . Debido a su alta combustibilidad, los estudios cinematográficos cambiaron a la película de seguridad de acetato de celulosa en 1950.
Uso medicinal y farmacéutico
En el campo médico, los ésteres orgánicos derivados del nitrato , como el trinitrato de glicerilo , el dinitrato de isosorbida y el mononitrato de isosorbida , se utilizan en la profilaxis y el tratamiento del síndrome coronario agudo , el infarto de miocardio y el edema pulmonar agudo . [10] Esta clase de fármacos, a la que también pertenece el nitrito de amilo , se conocen como nitrovasodilatadores .
Toxicidad y seguridad
Las dos áreas de preocupación sobre la toxicidad del nitrato son las siguientes:
- El nitrato reducido por la actividad microbiana de las bacterias reductoras de nitrato es el precursor del nitrito en el agua y en el tracto gastrointestinal inferior . El nitrito es un precursor de las nitrosaminas cancerígenas y;
- A través de la formación de nitrito, el nitrato está implicado en la metahemoglobinemia , un trastorno de la hemoglobina en los glóbulos rojos susceptible de afectar especialmente a bebés y niños pequeños. [11] [12]
Metahemoglobinemia
Una de las causas más comunes de metahemoglobinemia en los bebés se debe a la ingestión de nitratos y nitritos a través del agua de pozo o de los alimentos.
De hecho, los nitratos ( NO−3), a menudo presentes en concentraciones demasiado altas en el agua potable, son solo las especies químicas precursoras de los nitritos ( NO−2), los verdaderos culpables de la metahemoglobinemia. Los nitritos producidos por la reducción microbiana del nitrato (directamente en el agua de bebida, o después de la ingestión por el niño, en su sistema digestivo) son oxidantes más potentes que los nitratos y son el agente químico realmente responsable de la oxidación de Fe 2+ en Fe 3+ en el hemo tetrapirrólico de la hemoglobina . De hecho, los aniones nitrato son oxidantes demasiado débiles en solución acuosa para poder oxidar directamente, o al menos con suficiente rapidez, Fe 2+ en Fe 3+ , debido a limitaciones cinéticas .
Los lactantes menores de 4 meses tienen mayor riesgo debido a que beben más agua por peso corporal, tienen una menor actividad de la NADH - citocromo b5 reductasa y tienen un mayor nivel de hemoglobina fetal que se convierte más fácilmente en metahemoglobina . Además, los lactantes tienen mayor riesgo después de un episodio de gastroenteritis debido a la producción de nitritos por parte de las bacterias . [13]
Sin embargo, otras causas distintas a los nitratos también pueden afectar a los bebés y a las mujeres embarazadas. [14] [15] De hecho, el síndrome del bebé azul también puede ser causado por una serie de otros factores como la cardiopatía cianótica , un defecto cardíaco congénito que resulta en bajos niveles de oxígeno en la sangre, [16] o por malestar gástrico, como infección diarreica, intolerancia a las proteínas, toxicidad por metales pesados, etc. [17]
Normas de agua potable
A través de la Ley de Agua Potable Segura , la Agencia de Protección Ambiental de los Estados Unidos ha establecido un nivel máximo de contaminante de 10 mg/L o 10 ppm de nitrato en el agua potable. [18]
El Comité Mixto FAO/OMS de Expertos en Aditivos Alimentarios (JEFCA) estableció una ingesta diaria admisible (IDA) de iones de nitrato en el rango de 0 a 3,7 mg (kg de peso corporal) −1 día −1 [19] .
Toxicidad acuática

En los sistemas de agua dulce o estuarinos cercanos a la tierra, el nitrato puede alcanzar concentraciones que son letales para los peces. Si bien el nitrato es mucho menos tóxico que el amoníaco, [20] los niveles superiores a 30 ppm de nitrato pueden inhibir el crecimiento, perjudicar el sistema inmunológico y causar estrés en algunas especies acuáticas. [21] La toxicidad del nitrato sigue siendo un tema de debate. [22]
En la mayoría de los casos de concentraciones excesivas de nitrato en los sistemas acuáticos, las fuentes principales son las descargas de aguas residuales, así como la escorrentía superficial de áreas agrícolas o paisajísticas que han recibido un exceso de fertilizantes de nitrato. La eutrofización y la proliferación de algas resultantes dan lugar a anoxia y zonas muertas . En consecuencia, como el nitrato forma un componente de los sólidos disueltos totales , se utilizan ampliamente como indicador de la calidad del agua .
Impactos humanos en los ecosistemas a través de la deposición de nitratos

La deposición de nitratos en los ecosistemas ha aumentado notablemente debido a las actividades antropogénicas , en particular a la aplicación generalizada de fertilizantes ricos en nitrógeno en la agricultura y a las emisiones procedentes de la quema de combustibles fósiles . [23] Anualmente, se utilizan alrededor de 195 millones de toneladas métricas de fertilizantes nitrogenados sintéticos en todo el mundo, y los nitratos constituyen una parte importante de esta cantidad. [24] En regiones con agricultura intensiva, como partes de los EE. UU., China e India, el uso de fertilizantes nitrogenados puede superar los 200 kilogramos por hectárea. [24]
El impacto del aumento de la deposición de nitratos se extiende más allá de las comunidades vegetales y afecta a las poblaciones microbianas del suelo . [25] El cambio en la química del suelo y la dinámica de los nutrientes puede alterar los procesos naturales de fijación de nitrógeno , nitrificación y desnitrificación , lo que conduce a la alteración de las estructuras y funciones de la comunidad microbiana. Esta alteración puede afectar aún más el ciclo de nutrientes y la salud general del ecosistema . [26]
Nitrato dietético
Una fuente de nitrato en la dieta humana surge del consumo de alimentos de hojas verdes, como la espinaca y la rúcula . NO−
3Puede estar presente en el jugo de remolacha . El agua potable también representa una fuente primaria de ingesta de nitrato. [27]
La ingestión de nitratos aumenta rápidamente la concentración plasmática de nitratos en un factor de 2 a 3, y esta concentración elevada de nitratos puede mantenerse durante más de 2 semanas. El aumento de nitratos plasmáticos mejora la producción de óxido nítrico , NO. El óxido nítrico es una molécula de señalización fisiológica que interviene, entre otras cosas, en la regulación del flujo sanguíneo muscular y la respiración mitocondrial. [28]
Carnes curadas
Nitrito ( NO−2) el consumo está determinado principalmente por la cantidad de carnes procesadas consumidas y la concentración de nitratos ( NO−3) añadidos a estas carnes ( tocino , salchichas …) para su curado. Aunque los nitritos son las especies nitrogenadas más utilizadas en el curado de la carne , también se utilizan nitratos que pueden transformarse en nitrito por microorganismos, o en el proceso de digestión, empezando por su disolución en la saliva y su contacto con la microbiota de la boca. Los nitritos conducen a la formación de nitrosaminas cancerígenas . [29] La producción de nitrosaminas puede inhibirse mediante el uso de los antioxidantes vitamina C y la forma alfa-tocoferol de la vitamina E durante el curado. [30]
Muchos procesadores de carne afirman que sus carnes (por ejemplo, el tocino) no están "curadas", lo que es una afirmación de marketing sin ninguna base fáctica: no existe el tocino "sin curar" (ya que, en esencia, sería panceta de cerdo cruda cortada en lonchas). [31] [ Se necesita una mejor fuente ] La carne "sin curar" en realidad está curada con nitritos sin que prácticamente haya ninguna distinción en el proceso; la única diferencia es el requisito de etiquetado del USDA entre el nitrito de origen vegetal (como el del apio) y el nitrito de sodio "sintético". Una analogía sería la " sal marina " purificada frente al cloruro de sodio , ya que ambos son exactamente el mismo producto químico y la única diferencia esencial es el origen.
Las dietas antihipertensivas , como la dieta DASH , suelen contener altos niveles de nitratos, que primero se reducen a nitrito en la saliva , como se detecta en las pruebas de saliva , antes de formar óxido nítrico (NO). [27]
Alimentos para animales domésticos
Los síntomas de intoxicación por nitratos en animales domésticos incluyen aumento de la frecuencia cardíaca y respiratoria; en casos avanzados, la sangre y los tejidos pueden adquirir un color azul o marrón. Se pueden realizar pruebas de nitratos en los alimentos; el tratamiento consiste en complementar o sustituir los suministros existentes con material con menor contenido de nitratos. Los niveles seguros de nitratos para varios tipos de ganado son los siguientes: [32]
| Categoría | % NO3 | %NO3 - N | % KNO3 | Efectos |
|---|---|---|---|---|
| 1 | < 0,5 | < 0,12 | < 0,81 | Generalmente seguro para ganado vacuno y ovino. |
| 2 | 0,5–1,0 | 0,12–0,23 | 0,81–1,63 | Precaución: pueden aparecer algunos síntomas subclínicos en yeguas gestantes, ovejas y ganado vacuno de carne. |
| 3 | 1.0 | 0,23 | 1.63 | Problemas de altos niveles de nitratos: pueden producirse pérdidas por muerte y abortos en el ganado vacuno y ovino |
| 4 | < 1,23 | < 0,28 | < 2,00 | Nivel máximo seguro para caballos. No alimente a yeguas preñadas con forrajes con alto contenido de nitratos. |
Los valores anteriores se refieren a una base seca (sin humedad).
Sales y derivados covalentes
Formación de nitratos con elementos de la tabla periódica:
Véase también
- Amonio
- Eutrofización
- relación f en oceanografía
- Diagrama de escarcha
- Nitrificación
- Nitratina
- Nitrito , el anión NO−
2 - Óxido de nitrógeno
- Trióxido de nitrógeno , el radical neutro NO
3 - Peroxinitrato , OONO–
2 - Nitrato de sodio
Referencias
- ^ abcd Laue W, Thiemann M, Scheibler E, Wiegand KW (2006). "Nitratos y Nitritos". Enciclopedia de química industrial de Ullmann . Weinheim: Wiley-VCH. doi :10.1002/14356007.a17_265. ISBN 978-3527306732.
- ^ Lubos E, Handy DE, Loscalzo J (mayo de 2008). "El papel del estrés oxidativo y el óxido nítrico en la aterotrombosis". Frontiers in Bioscience . 13 (13). IMR Press: 5323–5344. doi :10.2741/3084. PMC 2617738 . PMID 18508590.
- ^ Moorcroft MJ, Davis J, Compton RG (junio de 2001). "Detección y determinación de nitrato y nitrito: una revisión". Talanta . 54 (5): 785–803. doi :10.1016/S0039-9140(01)00323-X. PMID 18968301.
- ^ Ellis G, Adatia I, Yazdanpanah M, Makela SK (junio de 1998). "Análisis de nitritos y nitratos: una perspectiva de bioquímica clínica". Bioquímica clínica . 31 (4): 195–220. doi :10.1016/S0009-9120(98)00015-0. PMID 9646943.
- ^ Zhang GB, Meng S, Gong JM (noviembre de 2018). "Los roles esperados e inesperados de los transportadores de nitrato en la resistencia al estrés abiótico de las plantas y su regulación". Revista internacional de ciencias moleculares . 19 (11): 3535. doi : 10.3390/ijms19113535 . PMC 6274899 . PMID 30423982.
- ^ Chuang HP (26 de noviembre de 2018). "Información sobre las vías de transformación de las especies de nitrógeno y la expresión de genes funcionales por parte de actores específicos involucrados en el ciclo del nitrógeno". Impact . 2018 (8): 58–59. doi :10.21820/23987073.2018.8.58. ISSN 2398-7073.
- ^ Liu B, Wu J, Yang S, Schiefelbein J, Gan Y (julio de 2020). Xu G (ed.). "Regulación del desarrollo de las raíces laterales y de los pelos radiculares por nitratos en plantas". Journal of Experimental Botany . 71 (15): 4405–4414. doi :10.1093/jxb/erz536. PMC 7382377 . PMID 31796961.
- ^ Bashir U, Lone FA, Bhat RA, Mir SA, Dar ZA, Dar SA (2020). "Preocupaciones y amenazas de contaminación en los ecosistemas acuáticos". En Hakeem KR, Bhat RA, Qadri H (eds.). Biorremediación y biotecnología . Cham: Springer International Publishing. págs. 1–26. doi :10.1007/978-3-030-35691-0_1. ISBN . 978-3-030-35690-3.
- ^ Kirchmann H, Johnston AE, Bergström LF (agosto de 2002). "Posibilidades de reducir la lixiviación de nitratos de tierras agrícolas". Ambio . 31 (5): 404–408. Bibcode :2002Ambio..31..404K. doi :10.1579/0044-7447-31.5.404. PMID 12374048.
- ^ Soman B, Vijayaraghavan G (abril de 2017). "El papel de los nitratos orgánicos en el tratamiento médico óptimo de la angina". Revista electrónica de práctica de cardiología (2) . Consultado el 30 de octubre de 2023 .
- ^ Powlson DS, Addiscott TM, Benjamin N, Cassman KG, de Kok TM, van Grinsven H, et al. (2008). "¿Cuándo se convierte el nitrato en un riesgo para los seres humanos?". Journal of Environmental Quality . 37 (2): 291–295. Bibcode :2008JEnvQ..37..291P. doi :10.2134/jeq2007.0177. PMID 18268290. S2CID 14097832.
- ^ "Intoxicación por nitratos y nitritos: Introducción". Manual veterinario de Merck . Consultado el 27 de diciembre de 2008 .
- ^ Smith-Whitley K, Kwiatkowski JL (2000). "Capítulo 489: Hemoglobinopatías". En Kliegman RM (ed.). Nelson Textbook of Pediatrics (21.ª ed.). Elsevier Inc., págs. 2540–2558. ISBN 978-0-323-52950-1.
- ^ Addiscott TM, Benjamin N (2006). "Nitrato y salud humana". Uso y gestión del suelo . 20 (2): 98–104. doi :10.1111/j.1475-2743.2004.tb00344.x. S2CID 96297102.
- ^ Avery AA (julio de 1999). "Metahemoglobinemia infantil: reexaminando el papel de los nitratos en el agua potable". Environmental Health Perspectives . 107 (7): 583–6. doi :10.1289/ehp.99107583. PMC 1566680 . PMID 10379005.
- ^ Enciclopedia MedlinePlus : Enfermedad cardíaca cianótica
- ^ Manassaram DM, Backer LC, Messing R, Fleming LE, Luke B, Monteilh CP (octubre de 2010). "Nitratos en el agua potable y niveles de metahemoglobina en el embarazo: un estudio longitudinal". Salud ambiental . 9 (1): 60. Bibcode :2010EnvHe...9...60M. doi : 10.1186/1476-069x-9-60 . PMC 2967503 . PMID 20946657.
- ^ "4. ¿Cuáles son las normas de la EPA sobre el agua potable en lo que respecta al nitrato?". Agua subterránea y agua potable . Consultado el 13 de noviembre de 2018 .
- ^ Bagheri H, Hajian A, Rezaei M, Shirzadmehr A (febrero de 2017). "Compuesto de nanopartículas de metal Cu-nanotubos de carbono multipared-óxido de grafeno reducido como una plataforma novedosa y de alto rendimiento del sensor electroquímico para la determinación simultánea de nitrito y nitrato". Journal of Hazardous Materials . 324 (Pt B): 762–772. Bibcode :2017JHzM..324..762B. doi :10.1016/j.jhazmat.2016.11.055. PMID 27894754.
- ^ Romano N, Zeng C (septiembre de 2007). "Toxicidad aguda del nitrato de sodio, nitrato de potasio y cloruro de potasio y sus efectos en la composición de la hemolinfa y la estructura de las branquias de los cangrejos nadadores azules juveniles tempranos (Portunus pelagicus Linnaeus, 1758) (Decapoda, Brachyura, Portunidae)". Toxicología y química ambiental . 26 (9): 1955–1962. doi :10.1897/07-144r.1. PMID 17705664. S2CID 19854591.
- ^ Sharpe, Shirlie. "Nitratos en el acuario". About.com . Archivado desde el original el 24 de julio de 2011. Consultado el 30 de octubre de 2013 .
- ^ Romano N, Zeng C (diciembre de 2007). "Efectos del potasio en las alteraciones de la osmorregulación mediadas por nitrato en cangrejos marinos". Toxicología acuática . 85 (3): 202–208. Bibcode :2007AqTox..85..202R. doi :10.1016/j.aquatox.2007.09.004. PMID 17942166.
- ^ Kanakidou M, Myriokefalitakis S, Daskalakis N, Fanourgakis G, Nenes A, Baker AR, et al. (mayo de 2016). "Deposición atmosférica de nitrógeno en el pasado, presente y futuro". Revista de ciencias atmosféricas . 73 (5): 2039–2047. Bibcode :2016JAtS...73.2039K. doi :10.1175/JAS-D-15-0278.1. PMC 7398418 . PMID 32747838.
- ^ ab "Consumo mundial de fertilizantes por nutriente 1965-2021". Statista . Consultado el 20 de abril de 2024 .
- ^ Li Y, Zou N, Liang X, Zhou X, Guo S, Wang Y, et al. (10 de enero de 2023). "Efectos del aporte de nitrógeno en la estructura de la comunidad bacteriana del suelo y el ciclo del nitrógeno del suelo en el suelo rizosfera de Lycium barbarum L". Frontiers in Microbiology . 13 : 1070817. doi : 10.3389/fmicb.2022.1070817 . PMC 9871820 . PMID 36704567.
- ^ Melillo JM (abril de 2021). "La disrupción del ciclo global del nitrógeno: un gran desafío para el siglo XXI: este artículo pertenece a la Colección del 50.º aniversario de Ambio. Tema: Eutrofización". Ambio . 50 (4): 759–763. doi :10.1007/s13280-020-01429-2. PMC 7982378 . PMID 33534057.
- ^ ab Hord NG, Tang Y, Bryan NS (julio de 2009). "Fuentes alimentarias de nitratos y nitritos: el contexto fisiológico de los posibles beneficios para la salud". The American Journal of Clinical Nutrition . 90 (1): 1–10. doi : 10.3945/ajcn.2008.27131 . PMID 19439460.
- ^ Maughan RJ (2013). Alimentación, nutrición y rendimiento deportivo III . Nueva York: Taylor & Francis. pág. 63. ISBN 978-0-415-62792-4.
- ^ Bingham SA, Hughes R, Cross AJ (noviembre de 2002). "Efecto de la carne blanca frente a la roja en la nitrosación endógena de nitrógeno en el colon humano y más pruebas de una respuesta a la dosis". The Journal of Nutrition . 132 (11 Suppl): 3522S–3525S. doi : 10.1093/jn/132.11.3522S . PMID 12421881.
- ^ Parthasarathy DK, Bryan NS (noviembre de 2012). "Nitrito de sodio: la "cura" para la insuficiencia de óxido nítrico". Meat Science . 92 (3): 274–279. doi :10.1016/j.meatsci.2012.03.001. PMID 22464105.
- ^ "¿Existe alguna diferencia entre el tocino curado y el no curado?". 9 de diciembre de 2022.
- ^ "Riesgo de nitratos en cultivos forrajeros: preguntas frecuentes". Agricultura y desarrollo rural . Gobierno de Alberta . Consultado el 30 de octubre de 2013 .
Enlaces externos
- ATSDR – Estudios de casos en medicina ambiental – Toxicidad por nitratos y nitritos (archivo)



