Trasplante de células madre hematopoyéticas
| Trasplante de células madre hematopoyéticas | |
|---|---|
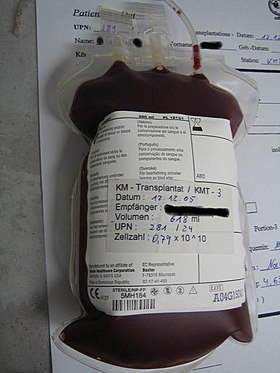 Trasplante de médula ósea | |
| CIE-9-CM | 41.0 |
| Malla | D018380 |
| MedlinePlus | 003009 |
El trasplante de células madre hematopoyéticas ( TCMH ) es el trasplante de células madre hematopoyéticas multipotentes , generalmente derivadas de la médula ósea , sangre periférica o sangre del cordón umbilical , con el fin de replicarse dentro de un paciente y producir células sanguíneas normales adicionales. [1] [2] [3] [4] [5] [6] El TPH puede ser autólogo (se utilizan las propias células madre del paciente), singénico (células madre de un gemelo idéntico ) o alogénico (células madre de un donante). [4] [5]
Se realiza con mayor frecuencia en pacientes con ciertos tipos de cáncer de la sangre o de la médula ósea, como el mieloma múltiple , la leucemia , algunos tipos de linfoma y deficiencias inmunitarias . [5] En estos casos, el sistema inmunitario del receptor suele suprimirse con radiación o quimioterapia antes del trasplante. La infección y la enfermedad de injerto contra huésped son complicaciones importantes del TPH alogénico. [5]
El trasplante de células madre hematopoyéticas sigue siendo un procedimiento peligroso con muchas complicaciones posibles; se reserva para pacientes con enfermedades potencialmente mortales. A medida que ha aumentado la supervivencia tras el procedimiento, su uso se ha ampliado más allá del cáncer a enfermedades autoinmunes [7] [8] y displasias esqueléticas hereditarias , en particular la osteopetrosis infantil maligna [9] [10] y la mucopolisacaridosis [11] .
Usos médicos

Indicaciones
Las indicaciones para el trasplante de células madre son:
Maligno (canceroso)
- Leucemia mieloide aguda
- Leucemia mieloide crónica
- Leucemia linfoblástica aguda
- Leucemia mielomonocítica juvenil
- Linfoma de Hodgkin (recidivante, refractario)
- Linfoma no Hodgkin (recidivante, refractario)
- Neuroblastoma
- Sarcoma de Ewing
- Mieloma múltiple
- Síndromes mielodisplásicos
- Gliomas , otros tumores sólidos
No maligno (no canceroso)
- Talasemia
- Anemia de células falciformes
- Anemia aplásica
- Anemia de Fanconi
- Osteopetrosis infantil maligna
- Mucopolisacaridosis
- Hemoglobinuria paroxística nocturna
- Deficiencia de piruvato quinasa
- Síndromes de inmunodeficiencia
- Enfermedades autoinmunes , [12] incluida la esclerosis múltiple [13] [14]
Muchos receptores de TPH son pacientes con mieloma múltiple [15] o leucemia [16] que no se beneficiarían de un tratamiento prolongado con quimioterapia o que ya son resistentes a ella . Los candidatos para TPH incluyen casos pediátricos en los que el paciente tiene un defecto congénito como inmunodeficiencia combinada grave o neutropenia congénita con células madre defectuosas, y también niños o adultos con anemia aplásica [17] que han perdido sus células madre después del nacimiento. Otras afecciones [18] tratadas con trasplantes de células madre incluyen la enfermedad de células falciformes , el síndrome mielodisplásico , el neuroblastoma , el linfoma , el sarcoma de Ewing , el tumor desmoplásico de células pequeñas y redondas , la enfermedad granulomatosa crónica , la enfermedad de Hodgkin y el síndrome de Wiskott-Aldrich . Se han desarrollado procedimientos no mieloablativos, denominados minitrasplantes (microtrasplantes) , que requieren dosis más pequeñas de quimioterapia preparatoria y radioterapia , lo que permite realizar el TPH en ancianos y otros pacientes que de otro modo se considerarían demasiado débiles para soportar un régimen de tratamiento convencional. [19]
Número de procedimientos
En 2006, se registraron 50.417 primeros trasplantes de células madre hematopoyéticas en todo el mundo, según una encuesta mundial realizada en 1.327 centros de 71 países por la Red Mundial de Trasplante de Sangre y Médula Ósea. De ellos, 28.901 (57%) fueron autólogos y 21.516 (43%) alogénicos (11.928 de donantes familiares y 9.588 de donantes no emparentados). Las principales indicaciones de trasplante fueron trastornos linfoproliferativos (55%) y leucemias (34%), y muchos se realizaron en Europa (48%) o en las Américas (36%). [20]
La Red Mundial de Trasplante de Sangre y Médula Ósea informó que en diciembre de 2012 se realizó el trasplante número un millón. [21]
En 2014, según la Asociación Mundial de Donantes de Médula Ósea , los productos de células madre proporcionados para trasplantes no relacionados en todo el mundo habían aumentado a 20.604 (4.149 donaciones de médula ósea, 12.506 donaciones de células madre de sangre periférica y 3.949 unidades de sangre del cordón umbilical). [22]
Tipos de injerto
Autólogo
El trasplante autólogo de células madre hematopoyéticas (HSC) requiere la extracción ( aféresis ) de células madre hematopoyéticas (HSC) del paciente y el almacenamiento de las células obtenidas en un congelador. Luego, el paciente es tratado con quimioterapia de dosis alta con o sin radioterapia con la intención de erradicar la población de células malignas del paciente a costa de una ablación parcial o completa de la médula ósea (destrucción de la capacidad de la médula ósea del paciente para generar nuevas células sanguíneas). Luego, las células madre almacenadas del propio paciente se transfunden a su torrente sanguíneo, donde reemplazan el tejido destruido y reanudan la producción normal de células sanguíneas del paciente. [2] Los trasplantes autólogos tienen la ventaja de un menor riesgo de infección durante la parte inmunodeprimida del tratamiento, ya que la recuperación de la función inmunológica es rápida. Además, la incidencia de pacientes que experimentan rechazo es muy rara (y la enfermedad de injerto contra huésped es imposible) debido a que el donante y el receptor son el mismo individuo. Estas ventajas han establecido el HSCT autólogo como uno de los tratamientos estándar de segunda línea para enfermedades como el linfoma . [23]
Sin embargo, en el caso de otros tipos de cáncer, como la leucemia mieloide aguda , la menor mortalidad del TPH autólogo en comparación con el alogénico puede verse compensada por una mayor probabilidad de recaída del cáncer y mortalidad relacionada, por lo que el tratamiento alogénico puede ser preferible para esas afecciones. [24]
Los investigadores han llevado a cabo pequeños estudios utilizando el HSCT no mieloablativo como un posible tratamiento para la diabetes tipo I (dependiente de la insulina) en niños y adultos. Los resultados han sido prometedores, pero a partir de 2019 [actualizar], especular si estos experimentos conducirán a tratamientos efectivos para la diabetes es prematuro. [25] [26] [27] El HSCT autólogo es un tratamiento eficaz contra la esclerosis múltiple agresiva. [28] El tipo de HSCT autólogo utilizado como tratamiento de la esclerosis múltiple se considera seguro y los eventos adversos graves son raros. [29]
Alogénico
El trasplante alogénico de células madre implica la participación de dos personas: el donante (sano) y el receptor (paciente). Los donantes de células madre alogénicas deben tener un tipo de tejido ( antígeno leucocitario humano , HLA) que coincida con el receptor. La compatibilidad se realiza en función de la variabilidad en tres o más loci del gen HLA, y se prefiere una coincidencia perfecta en estos loci. Incluso si existe una buena compatibilidad en estos alelos críticos , el receptor necesitará medicamentos inmunosupresores para mitigar la enfermedad de injerto contra huésped. Los donantes de trasplante alogénico pueden ser parientes (generalmente un hermano con una compatibilidad HLA cercana), singénicos (un gemelo monocigótico o idéntico del paciente, necesariamente extremadamente raro ya que pocos pacientes tienen un gemelo idéntico, pero que ofrece una fuente de células madre con una compatibilidad HLA perfecta), no emparentados (donante que no está emparentado y se descubre que tiene un grado muy cercano de compatibilidad HLA) o, como en el caso del trasplante haploidéntico, un pariente medio compatible, como un padre, un hijo o un hermano. Se pueden encontrar donantes no emparentados a través de un registro de donantes de médula ósea, como el Programa Nacional de Donantes de Médula Ósea (NMDP) en los EE. UU. Se puede seleccionar intencionalmente un " hermano salvador " mediante un diagnóstico genético preimplantacional para que coincida con un niño tanto en cuanto al tipo de HLA como a que no presente ningún trastorno hereditario obvio. Los trasplantes alogénicos también se realizan utilizando sangre del cordón umbilical como fuente de células madre. En general, al transfundir células madre sanas al torrente sanguíneo del receptor para reformar un sistema inmunológico saludable, los TPH alogénicos parecen mejorar las posibilidades de curación o remisión a largo plazo una vez que se resuelven las complicaciones inmediatas relacionadas con el trasplante. [30] [31] [32]
Un donante compatible se encuentra haciendo pruebas HLA adicionales a la sangre de los donantes potenciales. Los genes HLA se dividen en dos categorías (tipos I y II). En general, las discordancias de los genes de tipo I (es decir, HLA-A , HLA-B o HLA-C ) aumentan el riesgo de rechazo del injerto. Una discordancia de un gen HLA de tipo II (es decir, HLA-DR o HLA-DQB1 ) aumenta el riesgo de enfermedad de injerto contra huésped. Además, una discordancia genética tan pequeña como un solo par de bases de ADN es significativa, por lo que las compatibilidades perfectas requieren el conocimiento de la secuencia de ADN exacta de estos genes tanto para el donante como para el receptor. Los principales centros de trasplantes actualmente realizan pruebas para los cinco genes HLA antes de declarar que un donante y un receptor son HLA idénticos. [ cita requerida ]
Se sabe que la raza y la etnicidad desempeñan un papel importante en las campañas de reclutamiento de donantes, ya que los miembros del mismo grupo étnico tienen más probabilidades de tener genes compatibles, incluidos los genes para HLA. [33]
A partir de 2013 [actualizar], se han desarrollado al menos dos terapias celulares alogénicas comercializadas, Prochymal y Cartistem. [34] Omidubicel fue aprobado para uso médico en los Estados Unidos en abril de 2023. [35]
Fuentes y almacenamiento de células.
Para limitar los riesgos de rechazo de células madre trasplantadas o de enfermedad grave de injerto contra huésped en el TPH alogénico, el donante debe tener preferiblemente el mismo tipo de HLA que el receptor. Alrededor del 25 al 30% de los receptores de TPH alogénico tienen un hermano con HLA idéntico. Incluso los llamados "compatibles perfectos" pueden tener alelos menores no compatibles que contribuyen a la enfermedad de injerto contra huésped. Con los recientes avances en terapias de depleción de células T , como la ciclofosfamida postrasplante , los trasplantes haploidénticos (semicompletados) han permitido el trasplante exitoso de muchos pacientes que de otra manera no habrían tenido un donante. [36]
Médula ósea

En el caso de un trasplante de médula ósea, las células madre hematopoyéticas se extraen de un hueso grande del donante, normalmente la pelvis , a través de una aguja grande que llega al centro del hueso. La técnica se denomina recolección de médula ósea y se realiza bajo anestesia local o general . [37]
Células madre de sangre periférica

Las células madre de sangre periférica [38] son actualmente la fuente más común de células madre para el TPH. Se obtienen de la sangre mediante un proceso conocido como aféresis . La sangre del donante se extrae a través de una aguja estéril en un brazo y se pasa por una máquina que elimina los glóbulos blancos . Los glóbulos rojos se devuelven al donante. La producción de células madre periféricas se potencia con inyecciones subcutáneas diarias de factor estimulante de colonias de granulocitos , que sirve para movilizar las células madre de la médula ósea del donante hacia la circulación periférica. [39]
Líquido amniótico
La extracción de células madre del líquido amniótico es posible y puede tener aplicaciones para uso autólogo y heterólogo . [40]
Almacenamiento de HSC
A diferencia de otros órganos, las células de la médula ósea se pueden congelar ( criopreservar ) durante períodos prolongados sin dañar demasiadas células. Esto es una necesidad con las HSC autólogas porque las células deben recolectarse del receptor meses antes del tratamiento de trasplante. En el caso de los trasplantes alogénicos , se prefieren las HSC frescas para evitar la pérdida de células que podría ocurrir durante el proceso de congelación y descongelación. La sangre del cordón umbilical alogénica se almacena congelada en un banco de sangre del cordón umbilical porque solo se puede obtener en el momento del parto . Para criopreservar las HSC, se debe agregar un conservante, dimetilsulfóxido , y las células deben enfriarse muy lentamente en un congelador de velocidad controlada para evitar la lesión celular osmótica durante la formación de cristales de hielo. Las HSC pueden almacenarse durante años en un criocongelador, que generalmente utiliza nitrógeno líquido . [41]
Regímenes de acondicionamiento
Mieloablativo
La quimioterapia o la irradiación administrada inmediatamente antes de un trasplante se denomina régimen de acondicionamiento, cuyo propósito es ayudar a erradicar la enfermedad del paciente antes de la infusión de células madre hematopoyéticas y suprimir las reacciones inmunitarias. La médula ósea se puede extirpar (destruir) con niveles de dosis que causan un daño mínimo a otros tejidos. En los trasplantes alogénicos, se emplea convencionalmente una combinación de ciclofosfamida con irradiación corporal total . Este tratamiento también tiene un efecto inmunosupresor que previene el rechazo de las células madre hematopoyéticas por el sistema inmunitario del receptor . El pronóstico posterior al trasplante a menudo incluye enfermedad de injerto contra huésped aguda y crónica que puede poner en peligro la vida. Sin embargo, en ciertas leucemias, esto puede coincidir con la protección contra la recaída del cáncer debido al efecto de injerto contra tumor . [42] Los trasplantes autólogos también pueden utilizar regímenes de acondicionamiento similares, pero se pueden utilizar muchas otras combinaciones de quimioterapia según el tipo de enfermedad.
No mieloablativo
Un nuevo enfoque de tratamiento, el trasplante alogénico no mieloablativo, también denominado acondicionamiento de intensidad reducida (RIC), utiliza dosis de quimioterapia y radiación demasiado bajas para erradicar todas las células de la médula ósea del receptor. [43] : 320–321 En cambio, los trasplantes no mieloablativos conllevan menores riesgos de infecciones graves y mortalidad relacionada con el trasplante, al tiempo que dependen del efecto injerto contra tumor para resistir el aumento inherente del riesgo de recaída del cáncer. [44] [45] También es significativo que, si bien requieren altas dosis de agentes inmunosupresores en las primeras etapas del tratamiento, estas dosis son menores que para los trasplantes convencionales. [46] Esto conduce a un estado de quimerismo mixto poco después del trasplante, donde tanto las HSC del receptor como las del donante coexisten en el espacio de la médula ósea. [47]
La disminución de las dosis de la terapia inmunosupresora permite que las células T del donante erradiquen las células madre hematopoyéticas restantes del receptor e induzcan el efecto injerto contra tumor. Este efecto suele ir acompañado de una enfermedad injerto contra huésped leve, cuya aparición suele ser un marcador sustituto de la aparición del efecto injerto contra tumor deseado, y también sirve como señal para establecer un nivel de dosis adecuado para el tratamiento sostenido con niveles bajos de agentes inmunosupresores. [48]
Debido a que los regímenes de acondicionamiento son más suaves, estos trasplantes se asocian con un menor riesgo de mortalidad relacionada con el trasplante, por lo que permiten que los pacientes que se consideran de riesgo demasiado alto para el TPH alogénico convencional se sometan a una terapia potencialmente curativa para su enfermedad. La estrategia de acondicionamiento óptima para cada enfermedad y receptor no se ha establecido por completo, pero el RIC se puede utilizar en pacientes de edad avanzada que no son aptos para regímenes mieloablativos, para quienes un mayor riesgo de recaída del cáncer puede ser aceptable. [43] [45]
Injerto
Después de varias semanas de crecimiento en la médula ósea, la expansión de las células madre hematopoyéticas y su progenie es suficiente para normalizar el recuento de células sanguíneas y reiniciar el sistema inmunológico. Se ha documentado que la descendencia de las células madre hematopoyéticas derivadas de donantes pueblan muchos órganos diferentes del receptor, incluidos el corazón , el hígado y los músculos , y se ha sugerido que estas células tienen la capacidad de regenerar el tejido dañado en estos órganos. Sin embargo, investigaciones recientes han demostrado que dicha infidelidad de linaje no ocurre como un fenómeno normal. [ cita requerida ]
El seguimiento del quimerismo es un método para controlar el equilibrio entre las células madre del propio paciente y las nuevas células madre de un donante. En los casos en que las células madre del propio paciente aumentan en número después del tratamiento, es posible que el tratamiento no haya funcionado como se esperaba. [49]
Complicaciones
El trasplante de células madre hematopoyéticas se asocia a una alta mortalidad relacionada con el tratamiento en el receptor, lo que limita su uso a condiciones que son en sí mismas potencialmente mortales. (Se ha estimado que la tasa de supervivencia a un año es de aproximadamente el 60%, aunque esta cifra incluye muertes por la enfermedad subyacente, así como por el procedimiento de trasplante). [50] Las complicaciones principales incluyen enfermedad venooclusiva , mucositis , infecciones ( sepsis ), enfermedad de injerto contra huésped y el desarrollo de nuevas neoplasias malignas . [51]
Infección
El trasplante de médula ósea generalmente requiere que se destruya la propia médula ósea del receptor (mieloablación). Antes de la administración de nuevas células (injerto), los pacientes pueden pasar varias semanas sin una cantidad apreciable de glóbulos blancos para ayudar a combatir la infección . Esto pone al paciente en alto riesgo de infecciones, sepsis y choque séptico , a pesar de los antibióticos profilácticos . Sin embargo, los medicamentos antivirales , como el aciclovir y el valaciclovir , son bastante eficaces en la prevención del brote de infección herpética relacionado con el TPH en pacientes seropositivos . [52] Los agentes inmunosupresores empleados en trasplantes alogénicos para la prevención o el tratamiento de la enfermedad de injerto contra huésped aumentan aún más el riesgo de infección oportunista . Los medicamentos inmunosupresores se administran durante un mínimo de seis meses después de un trasplante, o mucho más tiempo si es necesario para el tratamiento de la enfermedad de injerto contra huésped. Los pacientes trasplantados pierden su inmunidad adquirida, por ejemplo, inmunidad a enfermedades infantiles como el sarampión o la polio . Por lo tanto, los pacientes trasplantados deben volver a recibir vacunas infantiles una vez que dejan de tomar medicamentos inmunosupresores. [53]
Enfermedad venooclusiva
La enfermedad venooclusiva hepática (EVO), recientemente denominada síndrome de obstrucción sinusoidal (SOS), puede producir una lesión hepática grave. [54] Los niveles elevados de bilirrubina , la hepatomegalia y la retención de líquidos son características clínicas de esta afección. Ahora es mayor la apreciación de la lesión celular generalizada y la obstrucción en los senos venosos hepáticos . Los casos graves de SOS se asocian con una alta tasa de mortalidad. Los anticoagulantes o la defibrotida pueden ser eficaces para reducir la gravedad de la EVO, pero también pueden aumentar las complicaciones hemorrágicas. Se ha demostrado que el ursodiol ayuda a prevenir la EVO, presumiblemente al facilitar el flujo de bilis .
Mucositis
La lesión de la mucosa de la boca y la garganta es una toxicidad frecuente relacionada con el régimen posterior a los tratamientos de TPH ablativo. Por lo general, no pone en peligro la vida, pero es muy dolorosa e impide comer y beber. La mucositis se trata con analgésicos más infusiones intravenosas para prevenir la deshidratación y la desnutrición. [55]
Cistitis hemorrágica
El revestimiento mucoso de la vejiga se ve afectado en aproximadamente el 5% de los niños sometidos a TPH. Esto provoca hematuria (sangre en la orina), micción frecuente, dolor abdominal y trombocitopenia . [56]
Enfermedad de injerto contra huésped
La enfermedad de injerto contra huésped (EICH) es una enfermedad inflamatoria exclusiva del trasplante alogénico. Se trata de un ataque de las células inmunitarias de la médula ósea "nueva" contra los tejidos del receptor. Esto puede ocurrir incluso si el donante y el receptor son HLA idénticos, porque el sistema inmunitario puede reconocer otras diferencias entre sus tejidos. Se denomina enfermedad de injerto contra huésped porque las células trasplantadas deben aceptar el cuerpo en lugar de que el cuerpo acepte las nuevas células. [57]
La EICH aguda ocurre típicamente en los primeros tres meses después del trasplante y puede afectar la piel , el intestino o el hígado . Los corticosteroides en dosis altas , como la prednisona , son un tratamiento estándar, pero este tratamiento inmunosupresor a menudo conduce a infecciones mortales. La EICH crónica también puede desarrollarse después del trasplante alogénico. Es la principal fuente de complicaciones tardías relacionadas con el tratamiento, aunque con menos frecuencia resulta en la muerte. Además de la inflamación, la EICH crónica puede conducir al desarrollo de fibrosis o tejido cicatricial, similar a la esclerodermia ; puede causar discapacidad funcional y requerir terapia inmunosupresora prolongada. La EICH generalmente está mediada por células T, que reaccionan a péptidos extraños presentados en el complejo principal de histocompatibilidad del huésped. [58]
Se necesitan más investigaciones para determinar si las células estromales mesenquimales se pueden utilizar para la profilaxis y el tratamiento de la EICH. [59]
Efecto injerto contra tumor
El efecto injerto contra tumor (GVT), o efecto "injerto contra leucemia", es el aspecto beneficioso del fenómeno de la EICH. Por ejemplo, los pacientes con TPH que presentan una EICH aguda o, en particular, crónica después de un trasplante alogénico tienden a tener un menor riesgo de recaída del cáncer. [60] [42] Esto se debe a una reacción inmunitaria terapéutica de los linfocitos T del donante injertados contra la médula ósea enferma del receptor. Esta menor tasa de recaída explica la mayor tasa de éxito de los trasplantes alogénicos, en comparación con los trasplantes de gemelos idénticos, e indica que el TPH alogénico es una forma de inmunoterapia. El GVT es el principal beneficio de los trasplantes que no emplean los regímenes inmunosupresores más altos.
El injerto contra tumor es principalmente beneficioso en enfermedades con progreso lento, por ejemplo leucemia crónica, linfoma de bajo grado y en algunos casos mieloma múltiple, pero es menos eficaz en leucemias agudas de rápido crecimiento. [61]
Si el cáncer recae después del TPH, se puede realizar otro trasplante, infundiendo al paciente una mayor cantidad de glóbulos blancos del donante ( infusión de linfocitos del donante ). [61]
Neoplasias malignas
Los pacientes que se someten a un TPH tienen un mayor riesgo de padecer carcinoma oral . El cáncer oral posterior al TPH puede tener un comportamiento más agresivo y un peor pronóstico, en comparación con el cáncer oral en pacientes que no se sometieron a un TPH. [62]
Un metaanálisis mostró que el riesgo de cánceres secundarios como cáncer de huesos , cáncer de cabeza y cuello y melanoma , con índices de incidencia estandarizados de 10,04 (3,48–16,61), 6,35 (4,76–7,93) y 3,52 (2,65–4,39), respectivamente, aumentó significativamente después del TPH. Por lo tanto, las pruebas de diagnóstico para estos cánceres deberían incluirse en el programa de detección de estos pacientes para la prevención y detección temprana de estos cánceres. [63]
Pronóstico
El pronóstico en el trasplante de células madre varía ampliamente según el tipo de enfermedad, el estadio, la fuente de células madre, el estado de compatibilidad HLA (para el trasplante de células madre alogénico) y el régimen de acondicionamiento. Un trasplante ofrece una posibilidad de curación o remisión a largo plazo si se puede sobrevivir a las complicaciones inherentes de la enfermedad de injerto contra huésped, los tratamientos inmunosupresores y el espectro de infecciones oportunistas. [30] [31] En los últimos años, las tasas de supervivencia han mejorado gradualmente en casi todas las poblaciones y subpoblaciones que reciben trasplantes. [64]
La mortalidad por trasplante alogénico de células madre se puede estimar utilizando el modelo de predicción creado por Sorror et al ., [65] utilizando el Índice de Comorbilidad Específico del Trasplante de Células Hematopoyéticas (HCT-CI). El HCT-CI fue derivado y validado por investigadores del Centro de Investigación del Cáncer Fred Hutchinson en los EE. UU. El HCT-CI modifica y agrega a un índice de comorbilidad bien validado, el Índice de Comorbilidad de Charlson (CCI) (Charlson, et al .) [66] El CCI se aplicó anteriormente a pacientes sometidos a HCT alogénico, pero parece proporcionar menos predicción de supervivencia y discriminación que el sistema de puntuación HCT-CI.
Se observó que los pacientes que recibieron un tratamiento exitoso con TPH e irradiación corporal total en la infancia tenían un mayor porcentaje de masa grasa, lo que condujo a una disminución significativa de la capacidad de ejercicio en la edad adulta. Esto sugiere que los pacientes que se sometieron a un tratamiento exitoso con TPH tienen una mayor predisposición a sufrir enfermedades cardiovasculares más adelante en la vida. [67]
Riesgos para el donante
Los riesgos de una complicación dependen de las características del paciente, los proveedores de atención médica, el procedimiento de aféresis y el factor estimulante de colonias utilizado ( G-CSF ). Los medicamentos G-CSF incluyen filgrastim (Neupogen, Neulasta) y lenograstim (Graslopin).
Riesgos de los medicamentos
El filgrastim se dosifica típicamente en el nivel de 10 microgramos/kg durante 4 a 5 días durante la recolección de células madre. Los efectos adversos documentados del filgrastim incluyen ruptura esplénica , síndrome de dificultad respiratoria aguda , hemorragia alveolar y reacciones alérgicas (generalmente experimentadas en los primeros 30 minutos). [68] [69] [70] Además, los niveles de plaquetas y hemoglobina disminuyen después del procedimiento y no vuelven a la normalidad hasta después de un mes. [70]
No se ha estudiado lo suficiente si los pacientes mayores de 65 años reaccionan de la misma manera que los menores. Se sabe que la inyección de G-CSF produce problemas de coagulación e inflamación de las placas ateroscleróticas. También se ha descrito que el G-CSF induce cambios genéticos en los agranulocitos de donantes normales. [69] No hay evidencia estadísticamente significativa a favor o en contra de la hipótesis de que la mielodisplasia (SMD) o la leucemia mieloide aguda (LMA) puedan ser inducidas por G-CSF en individuos susceptibles. [71]
Riesgos de acceso
En la mayoría de los pacientes, la sangre se extrae de una vena periférica, pero puede utilizarse una vía central hacia las venas yugular, subclavia y femoral. Se experimentaron reacciones adversas durante la aféresis en el 20 % de las mujeres y el 8 % de los hombres; estos eventos adversos consistieron principalmente en entumecimiento/hormigueo, múltiples intentos de inserción de la vía y náuseas. [70]
Observaciones clínicas
Un estudio que involucró a 2.408 donantes (de 18 a 60 años) indicó que el dolor óseo (principalmente de espalda y caderas) como resultado del tratamiento con filgrastim se observa en el 80% de los donantes. [70] No se recomienda la donación a quienes tienen antecedentes de dolor de espalda. [70] Otros síntomas observados en más del 40 por ciento de los donantes incluyen dolor muscular, dolor de cabeza, fatiga y dificultad para dormir. [70] Todos estos síntomas regresaron a la línea de base 1 mes después de la donación en la mayoría de los pacientes. [70]
En un metaestudio que incorporó datos de 377 donantes, el 44% de los pacientes informaron haber tenido efectos secundarios adversos después del TPH de sangre periférica. [71] Los efectos secundarios incluyeron dolor antes del procedimiento de recolección como resultado de las inyecciones de G-CSF y dolor esquelético generalizado posterior al procedimiento, fatiga y reducción de energía. [71]
Reacciones graves
Un estudio que encuestó a 2.408 donantes encontró que ocurrieron eventos adversos graves (que requirieron hospitalización prolongada) en 15 donantes (a una tasa del 0,6%), aunque ninguno de estos eventos fue fatal. [70] No se observó que los donantes tuvieran tasas más altas de lo normal de cáncer con hasta 4 a 8 años de seguimiento. [70] Un estudio basado en una encuesta de equipos médicos cubrió alrededor de 24.000 casos de TPH de sangre periférica entre 1993 y 2005, y encontró una tasa de reacciones adversas cardiovasculares graves de aproximadamente uno en 1.500. [69] Este estudio informó un riesgo de fatalidad relacionada con enfermedades cardiovasculares dentro de los primeros 30 días del TPH de aproximadamente dos en 10.000. [69]
Historia
En 1939, una mujer con anemia aplásica recibió la primera transfusión de médula ósea humana. Esta paciente recibió transfusiones de sangre periódicas y se intentó aumentar su recuento de leucocitos y plaquetas mediante una inyección intravenosa de médula ósea sin que se produjera ninguna reacción inesperada. [72]
El trasplante de células madre fue pionero utilizando células madre derivadas de la médula ósea por un equipo del Centro de Investigación del Cáncer Fred Hutchinson desde la década de 1950 hasta la de 1970 dirigido por E. Donnall Thomas , cuyo trabajo fue reconocido más tarde con un Premio Nobel de Fisiología o Medicina . El trabajo de Thomas demostró que las células de la médula ósea infundidas por vía intravenosa podían repoblar la médula ósea y producir nuevas células sanguíneas. Su trabajo también redujo la probabilidad de desarrollar una enfermedad de injerto contra huésped potencialmente mortal. [73] En colaboración con Eloise Giblett , profesora de la Universidad de Washington , descubrió marcadores genéticos que podían confirmar la compatibilidad de los donantes.
El primer médico que realizó con éxito un trasplante de médula ósea en un ser humano en una enfermedad distinta del cáncer fue Robert A. Good , de la Universidad de Minnesota, en 1968. [74] En 1975, John Kersey, también de la Universidad de Minnesota, realizó con éxito el primer trasplante de médula ósea para curar el linfoma. Su paciente, un muchacho de 16 años, es hoy el superviviente más longevo de un trasplante de linfoma. [75]
Registro y captación de donantes
A finales de 2012, 20,2 millones de personas habían registrado su voluntad de ser donantes de médula ósea en uno de los 67 registros de 49 países participantes en Bone Marrow Donors Worldwide . Alrededor de 17,9 millones de estos donantes registrados habían sido tipificados según ABDR, lo que permitió una fácil compatibilidad. Uno de los 46 bancos de sangre de cordón umbilical de 30 países participantes había recibido otras 561.000 unidades de sangre de cordón umbilical. El mayor número total de donantes de médula ósea registrados fue el de los EE. UU. (8,0 millones), y el mayor número per cápita fue el de Chipre (15,4% de la población). [76]
En Estados Unidos, los grupos de minorías raciales son los que tienen menos probabilidades de ser registrados y, por lo tanto, de encontrar un donante compatible que pueda salvarles la vida. En 1990, sólo seis afroamericanos lograron encontrar un donante compatible de médula ósea, y todos ellos tenían firmas genéticas europeas comunes. [77]
Los africanos son genéticamente más diversos que las personas de ascendencia europea, lo que significa que se necesitan más registros para encontrar una compatibilidad. Existen bancos de médula ósea y sangre del cordón umbilical en Sudáfrica , y se está iniciando un nuevo programa en Nigeria . [77] Se solicita a muchas personas pertenecientes a diferentes razas que donen, ya que existe una escasez de donantes en las comunidades africanas, mestizas, latinas, aborígenes y muchas otras.
Dos registros en los EE. UU. reclutan donantes alogénicos no emparentados: NMDP o Be the Match y el Gift of Life Marrow Registry .
Investigación
VIH
En 2007, un equipo de médicos en Berlín, Alemania, incluido Gero Hütter , realizó un trasplante de células madre para el paciente de leucemia Timothy Ray Brown , que también era VIH positivo. [78] De 60 donantes compatibles, seleccionaron un individuo homocigoto [CCR5]-Δ32 con dos copias genéticas de una variante rara de un receptor de superficie celular . Este rasgo genético confiere resistencia a la infección por VIH al bloquear la unión del VIH a la célula. Aproximadamente una de cada 1000 personas de ascendencia europea tiene esta mutación hereditaria , pero es más rara en otras poblaciones. [79] [80] El trasplante se repitió un año después después de una recaída de leucemia. Más de tres años después del trasplante inicial, y a pesar de suspender la terapia antirretroviral , los investigadores no pueden detectar el VIH en la sangre del receptor del trasplante ni en varias biopsias de sus tejidos. [81] Los niveles de anticuerpos específicos del VIH también han disminuido, lo que ha llevado a especular que el paciente puede haberse curado funcionalmente del VIH, pero los científicos enfatizan que este es un caso inusual. [82] Las complicaciones potencialmente fatales del trasplante (el "paciente de Berlín" desarrolló enfermedad de injerto contra huésped y leucoencefalopatía ) significan que el procedimiento no podría realizarse en otros con VIH, incluso si se encontrara un número suficiente de donantes adecuados. [83] [84]
En 2012, Daniel Kuritzkes informó de los resultados de dos trasplantes de células madre en pacientes con VIH. Sin embargo, no utilizaron donantes con la deleción Δ32. Después de los procedimientos de trasplante, ambos recibieron terapias antirretrovirales, durante las cuales ninguno mostró rastros de VIH en su plasma sanguíneo y se purificaron las células T CD4 + mediante un método de cultivo sensible (menos de 3 copias/ml). El virus se detectó nuevamente en ambos pacientes algún tiempo después de la interrupción de la terapia. [85]
En 2019, un hombre británico se convirtió en el segundo en quedar libre de VIH tras recibir un trasplante de médula ósea de un donante resistente al virus (Δ32). A este paciente se lo denomina "el paciente de Londres" (en referencia al famoso paciente de Berlín). [86]
Esclerosis múltiple
Desde el informe de 1997 de McAllister sobre un paciente con esclerosis múltiple (EM) que recibió un trasplante de médula ósea para leucemia mieloide crónica (LMC), [87] se han publicado más de 600 informes que describen TPH realizados principalmente para EM. [88] Se ha demostrado que estos "reducen o eliminan las recaídas clínicas en curso, detienen la progresión posterior y reducen la carga de discapacidad en algunos pacientes" que tienen EM agresiva y altamente activa, "en ausencia de tratamiento crónico con agentes modificadores de la enfermedad". [88] Un ensayo clínico aleatorizado que incluyó a 110 pacientes mostró que el TPH prolongó significativamente el tiempo hasta la progresión de la enfermedad en comparación con la terapia modificadora de la enfermedad. [89] Los resultados a largo plazo en pacientes con enfermedad grave han demostrado que es posible la remisión completa de la enfermedad después del TPH. [90]
Otras enfermedades neurológicas autoinmunes
El TPH también se puede utilizar para tratar casos graves seleccionados de otras enfermedades neurológicas autoinmunes, como la neuromielitis óptica , la polineuropatía desmielinizante inflamatoria crónica y la miastenia gravis . [91]
Referencias
- ^ Monga I, Kaur K, Dhanda S (marzo de 2022). "Revisitando la hematopoyesis: aplicaciones de la transcriptómica de células individuales y en masa que analizan la heterogeneidad transcripcional en células madre hematopoyéticas". Briefings in Functional Genomics . 21 (3): 159–176. doi :10.1093/bfgp/elac002. PMID 35265979.
- ^ ab Nabarrete, JM; Pereira, Arizona; Garófolo, A.; Seber, A.; Venancio, AM; Greco, CE; Bonfim, CM; Nakamura, CH; Fernández, D.; Campos, DJ; Oliveira, Florida; Cousseiro, FK; Rossi, FF; Gurmini, J.; Viani, KH; Guterres, LF; Mantovani, LF; Darrigo LG, Junior; Albuquerque, Michigan; Brumatti, M.; Neves, MA; Durán, N.; Villela, Carolina del Norte; Zecchin, VG; Fernández, JF (2021). "Consenso Nutricional Brasileño en Trasplante de Células Madre Hematopoyéticas: Niños y Adolescentes". Einstein . 19 : eAE5254. doi :10.31744/einstein_journal/2021AE5254. PMC 8664291. PMID 34909973 .
- ^ Forman SJ, Negrin RS, Antin JH, Appelbaum FR. Trasplante de células hematopoyéticas de Thomas: trasplante de células madre. 5.ª ed. Vol. 2. Nueva Jersey: Wiley-Blackwell; 2016. pág. 1416.
- ^ ab Felfly H, Haddad GG (2014). "Células madre hematopoyéticas: nuevas aplicaciones potenciales para la medicina traslacional". Journal of Stem Cells . 9 (3): 163–197. PMID 25157450.
- ^ abcd Park B, Yoo KH, Kim C (diciembre de 2015). "Expansión y generación de células madre hematopoyéticas: las formas de lograr un avance". Blood Research . 50 (4): 194–203. doi :10.5045/br.2015.50.4.194. PMC 4705045 . PMID 26770947.
- ^ Mahla RS (2016). "Aplicaciones de células madre en medicina regenerativa y terapias de enfermedades". Revista internacional de biología celular . 2016 (7): 6940283. doi : 10.1155/2016/6940283 . PMC 4969512. PMID 27516776 .
- ^ Tyndall A, Fassas A, Passweg J, Ruiz de Elvira C, Attal M, Brooks P, et al. (octubre de 1999). "Trasplantes autólogos de células madre hematopoyéticas para enfermedades autoinmunes: viabilidad y mortalidad relacionada con el trasplante. Grupos de trabajo sobre enfermedades autoinmunes y linfomas del Grupo europeo de trasplante de sangre y médula ósea, la Liga Europea contra el Reumatismo y el Proyecto internacional de células madre para enfermedades autoinmunes". Trasplante de médula ósea . 24 (7): 729–734. doi : 10.1038/sj.bmt.1701987 . PMID 10516675.
- ^ Burt RK, Loh Y, Pearce W, Beohar N, Barr WG, Craig R, et al. (febrero de 2008). "Aplicaciones clínicas de células madre derivadas de la sangre y de la médula ósea para enfermedades no malignas". JAMA . 299 (8): 925–936. doi : 10.1001/jama.299.8.925 . PMID 18314435.
- ^ EL-Sobky TA, El-Haddad A, Elsobky E, Elsayed SM, Sakr HM (marzo de 2017). "Reversión de la patología radiográfica esquelética en un caso de osteopetrosis infantil maligna después del trasplante de células madre hematopoyéticas". The Egyptian Journal of Radiology and Nuclear Medicine . 48 (1): 237–243. doi : 10.1016/j.ejrnm.2016.12.013 .
- ^ Hashemi Taheri AP, Radmard AR, Kooraki S, Behfar M, Pak N, Hamidieh AA, Ghavamzadeh A (septiembre de 2015). "Resolución radiológica de los cambios esqueléticos de la osteopetrosis infantil maligna después del trasplante de células madre hematopoyéticas". Pediatric Blood & Cancer . 62 (9): 1645–1649. doi :10.1002/pbc.25524. PMID 25820806. S2CID 11287381.
- ^ Langereis EJ, den Os MM, Breen C, Jones SA, Knaven OC, Mercer J, et al. (marzo de 2016). "Progresión de la displasia de cadera en la mucopolisacaridosis tipo I de Hurler después de un trasplante exitoso de células madre hematopoyéticas". The Journal of Bone and Joint Surgery. Volumen estadounidense . 98 (5): 386–395. doi :10.2106/JBJS.O.00601. PMID 26935461. S2CID 207284951.
- ^ Alexander T, Arnold R, Hiepe F, Radbruch A (1 de julio de 2016). "Restablecimiento del sistema inmunológico con inmunoablación y trasplante autólogo de células madre hematopoyéticas en enfermedades autoinmunes". Reumatología clínica y experimental . 34 (4 Suppl 98): 53–57. PMID 27586805.
- ^ Fassas, A.; Kimiskidis, VK; Sakellari, I.; Kapinas, K.; Anagnostopoulos, A.; Tsimourtou, V.; Sotirakoglou, K.; Kazis, A. (22 de marzo de 2011). "Resultados a largo plazo del trasplante de células madre para la EM: una experiencia en un solo centro". Neurología . 76 (12): 1066–1070. doi :10.1212/WNL.0b013e318211c537. ISSN 0028-3878. PMID 21422458. S2CID 15117695.
- ^ Saccardi, Ricardo; Mancardi, Gian Luigi; Solari, Alessandra; Bosi, Alberto; Bruzzi, Paolo; Di Bartolomeo, Paolo; Donelli, Amedea; Filippi, Massimo; Guerrasio, Ángelo; Gualandi, Francesca; La Nasa, Giorgio (15 de marzo de 2005). "TCMH autólogo para la esclerosis múltiple progresiva grave en un ensayo multicéntrico: impacto en la actividad de la enfermedad y la calidad de vida". Sangre . 105 (6): 2601–2607. doi : 10.1182/sangre-2004-08-3205 . ISSN 0006-4971. PMID 15546956. S2CID 22645544.
- ^ Bladé J, Samson D, Reece D, Apperley J, Björkstrand B, Gahrton G, et al. (septiembre de 1998). "Criterios para evaluar la respuesta y progresión de la enfermedad en pacientes con mieloma múltiple tratados con terapia de dosis alta y trasplante de células madre hematopoyéticas. Subcomité de Mieloma del EBMT. Grupo Europeo de Trasplante de Sangre y Médula Ósea". British Journal of Haematology . 102 (5): 1115–1123. doi :10.1046/j.1365-2141.1998.00930.x. PMID 9753033. S2CID 767838.
- ^ Pavletic SZ, Khouri IF, Haagenson M, King RJ, Bierman PJ, Bishop MR, et al. (agosto de 2005). "Trasplante de médula ósea de donante no emparentado para leucemia linfocítica crónica de células B después de utilizar acondicionamiento mieloablativo: resultados del Centro de investigación internacional sobre trasplante de sangre y médula ósea". Journal of Clinical Oncology . 23 (24): 5788–5794. doi : 10.1200/JCO.2005.03.962 . PMID 16043827.
- ^ Locasciulli A, Oneto R, Bacigalupo A, Socié G, Korthof E, Bekassy A, et al. (enero de 2007). "Resultados de pacientes con anemia aplásica adquirida que recibieron un trasplante de médula ósea de primera línea o tratamiento inmunosupresor en la última década: un informe del Grupo Europeo de Trasplante de Sangre y Médula Ósea (EBMT)". Haematologica . 92 (1): 11–18. doi : 10.3324/haematol.10075 . PMID 17229630.
- ^ Centro de Investigación Internacional sobre Trasplante de Sangre y Médula Ósea. "CIBMTR Summary Slides I". Archivado desde el original el 14 de diciembre de 2012.
- ^ Cai B, Guo M, Ai H (noviembre de 2018). "Microtrasplante: aplicaciones clínicas y mecanismos". Curr Opin Hematol . 25 (6): 417–424. doi :10.1097/MOH.0000000000000470. PMID 30148720. S2CID 239799097.
- ^ Gratwohl A, Baldomero H, Aljurf M, Pasquini MC, Bouzas LF, Yoshimi A, et al. (abril de 2010). "Trasplante de células madre hematopoyéticas: una perspectiva global". JAMA . 303 (16): 1617–1624. doi :10.1001/jama.2010.491. PMC 3219875 . PMID 20424252.
- ^ Gratwohl A, Pasquini MC, ALjurf M, et al. (2015). "Un millón de trasplantes de células madre hematopoyéticas: un estudio observacional retrospectivo". Lancet Haematol . 2 (3): e91–100. doi :10.1016/S2352-3026(15)00028-9. PMID 26687803.Errata en: Lancet Haematol. 2015 mayo; 2(5): e184
- ^ Gráficos del "Informe anual 2014". Asociación Mundial de Donantes de Médula Ósea.[ enlace muerto permanente ]
- ^ Canellos, George (1997). "Actualización sobre linfoma: 1997". The Oncologist . 2 (3): 181–183. doi : 10.1634/theoncologist.2-3-181a .
- ^ Bruno B, Rotta M, Patriarca F, Mordini N, Allione B, Carnevale-Schianca F, et al. (marzo de 2007). "Una comparación entre el aloinjerto y el autoinjerto para el mieloma de diagnóstico reciente". The New England Journal of Medicine . 356 (11): 1110–1120. doi :10.1056/NEJMoa065464. PMID 17360989. S2CID 2031300.
- ^ Couri CE, Oliveira MC, Stracieri AB, Moraes DA, Pieroni F, Barros GM, et al. (abril de 2009). "Niveles de péptido C e independencia de insulina tras un trasplante autólogo no mieloablativo de células madre hematopoyéticas en pacientes con diabetes mellitus tipo 1 de diagnóstico reciente". JAMA . 301 (15): 1573–1579. doi : 10.1001/jama.2009.470 . PMID 19366777.
- ^ Penaforte-Saboia JG, Montenegro RM, Couri CE, Batista LA, Montenegro AP, Fernandes VO, et al. (23 de noviembre de 2017). "Complicaciones microvasculares en la diabetes tipo 1: un análisis comparativo de pacientes tratados con trasplante autólogo no mieloablativo de células madre hematopoyéticas y terapia médica convencional". Frontiers in Endocrinology . 8 : 331. doi : 10.3389/fendo.2017.00331 . PMC 5703738 . PMID 29218029.
- ^ D'Addio F, Valderrama Vasquez A, Ben Nasr M, Franek E, Zhu D, Li L, et al. (septiembre de 2014). "Trasplante autólogo no mieloablativo de células madre hematopoyéticas en la diabetes tipo 1 de nueva aparición: un análisis multicéntrico". Diabetes . 63 (9): 3041–3046. doi : 10.2337/db14-0295 . PMID 24947362.
- ^ Muraro, Paolo A.; Martin, Roland; Mancardi, Giovanni Luigi; Nicholas, Richard; Sormani, Maria Pia; Saccardi, Riccardo (julio de 2017). "Trasplante autólogo de células madre hematopoyéticas para el tratamiento de la esclerosis múltiple". Nature Reviews. Neurología . 13 (7): 391–405. doi :10.1038/nrneurol.2017.81. hdl : 10044/1/50510 . ISSN 1759-4766. PMID 28621766. S2CID 20836380.
- ^ Ge, Fangfang; Lin, Hong; Li, Zhuyi; Chang, Ting (marzo de 2019). "Eficacia y seguridad del trasplante autólogo de células madre hematopoyéticas en la esclerosis múltiple: una revisión sistemática y un metanálisis". Neurological Sciences . 40 (3): 479–487. doi :10.1007/s10072-018-3670-1. ISSN 1590-3478. PMID 30535563. S2CID 54461739.
- ^ ab Russell N, Bessell E, Stainer C, Haynes A, Das-Gupta E, Byrne J (2000). "Trasplante alogénico de células madre hematopoyéticas para el mieloma múltiple o la leucemia de células plasmáticas mediante radiación corporal total fraccionada y acondicionamiento con melfalán en dosis altas". Acta Oncologica . 39 (7): 837–841. doi : 10.1080/028418600750063596 . PMID 11145442. S2CID 218897646.
- ^ ab Nivison-Smith I, Bradstock KF, Dodds AJ, Hawkins PA, Szer J (enero de 2005). "Trasplante de células madre hematopoyéticas en Australia y Nueva Zelanda, 1992-2001: informe de progreso del Registro de receptores de trasplantes de médula ósea de Australasia". Revista de medicina interna . 35 (1): 18-27. doi :10.1111/j.1445-5994.2004.00704.x. PMID 15667464. S2CID 29779201.
- ^ Venkat, Chaya (19 de julio de 2005). "La única cura real que existe, por ahora". Archivado el 30 de mayo de 2008 en Wayback Machine . Temas de la LLC, Inc.
- ^ "Por qué la raza y la etnicidad son importantes" Archivado el 1 de febrero de 2014 en Wayback Machine . Be the Match. Consultado el 27 de enero de 2014.
- ^ Simaria, Ana Sofia; et al. (marzo de 2013). "Relación coste-efectividad de las tecnologías de un solo uso para la fabricación comercial de terapias celulares". Am. Pharm. Rev. : 40. ISSN 1099-8012.
- ^ "La FDA aprueba omidubicel para reducir el tiempo de recuperación de los neutrófilos y la infección en pacientes con neoplasias hematológicas". Administración de Alimentos y Medicamentos de los Estados Unidos (FDA) . 17 de abril de 2023. Consultado el 20 de abril de 2023 .
- ^ Marszołek A, Leśniak M, Sekunda A, Siwek A, Skiba Z, Lejman M, Zawitkowska J. TCMH haploidéntico en el tratamiento de trastornos hematológicos pediátricos. Int J Mol Ciencia. 9 de junio de 2024; 25 (12): 6380. doi: 10.3390/ijms25126380. PMID: 38928087; PMCID: PMC11204214.
- ^ Gorin NC. Obtención de médula ósea para trasplante de células madre hematopoyéticas. En: Carreras E, Dufour C, Mohty M, Kröger N, editores. Manual EBMT: trasplante de células madre hematopoyéticas y terapias celulares [Internet]. 7.ª ed. Cham (CH): Springer; 2019. Capítulo 14. PMID: 32091775.
- ^ Cutler C, Antin JH (2001). "Células madre de sangre periférica para trasplante alogénico: una revisión". Células madre . 19 (2): 108–117. doi : 10.1634/stemcells.19-2-108 . PMID 11239165.
- ^ Prisciandaro M, Santinelli E, Tomachio V, Tafuri MA, Bonchi C, Palazzo G, Nobile C, Marinucci A, Mele M, Annibali O, Rigacci L, Vacca M. Recolección y movilización de células madre en trasplantes autólogos/alogénicos de adultos: fundamental Puntos y Retos Futuros. Células. 28 de marzo de 2024; 13 (7): 586. doi: 10.3390/celdas13070586. PMID: 38607025; PMCID: PMC11011310.
- ^ Rosner M, Horer S, Feichtinger M, Hengstschläger M. Células madre fetales multipotentes en la investigación de biología reproductiva. Stem Cell Res Ther. 7 de junio de 2023;14(1):157. doi: 10.1186/s13287-023-03379-4. PMID: 37287077; PMCID: PMC10249329.
- ^ Hornberger K, Yu G, McKenna D, Hubel A. Criopreservación de células madre hematopoyéticas: nuevos ensayos, agentes crioprotectores y tecnología para mejorar los resultados. Transfus Med Hemother. 2019 junio;46(3):188-196. doi: 10.1159/000496068. Publicación electrónica 5 de febrero de 2019. PMID: 31244587; PMCID: PMC6558318.
- ^ ab Toze CL, Galal A, Barnett MJ, Shepherd JD, Conneally EA, Hogge DE, et al. (noviembre de 2005). "Aloinjerto mieloablativo para la leucemia linfocítica crónica: evidencia de un potente efecto injerto contra leucemia asociado con la enfermedad injerto contra huésped". Trasplante de médula ósea . 36 (9): 825–830. doi : 10.1038/sj.bmt.1705130 . PMID 16151430.
- ^ ab Kaushansky, K; Lichtman, M; Beutler, E; Kipps, T; Prchal, J; Seligsohn, U. (2010). Williams Hematology (8.ª ed.). McGraw-Hill. ISBN 978-0071621519.
- ^ Alyea EP, Kim HT, Ho V, Cutler C, DeAngelo DJ, Stone R, et al. (octubre de 2006). "Impacto de la intensidad del régimen de acondicionamiento en el resultado del trasplante alogénico de células hematopoyéticas para la leucemia mielógena aguda avanzada y el síndrome mielodisplásico". Biología del trasplante de sangre y médula ósea . 12 (10): 1047–1055. doi : 10.1016/j.bbmt.2006.06.003 . PMID 17067911.
- ^ ab Alyea EP, Kim HT, Ho V, Cutler C, Gribben J, DeAngelo DJ, et al. (febrero de 2005). "Resultado comparativo del trasplante de células hematopoyéticas alogénico mieloablativo y no mieloablativo para pacientes mayores de 50 años". Blood . 105 (4): 1810–1814. doi : 10.1182/blood-2004-05-1947 . PMID 15459007.
- ^ Mielcarek M, Martin PJ, Leisenring W, Flowers ME, Maloney DG, Sandmaier BM, et al. (julio de 2003). "Enfermedad de injerto contra huésped después de un trasplante de células madre hematopoyéticas no mieloablativo frente a uno convencional". Blood . 102 (2): 756–762. doi : 10.1182/blood-2002-08-2628 . PMID 12663454.
- ^ Sykes M. Monitorización inmunitaria de pacientes trasplantados en ensayos de tolerancia transitoria al quimerismo mixto. Hum Immunol. Mayo de 2018;79(5):334-342. doi: 10.1016/j.humimm.2017.12.011. Publicación electrónica 28 de diciembre de 2017. PMID: 29289741; PMCID: PMC5924718.
- ^ Ibikunle S, Grosso D, Gergis U. El enfoque de dos pasos para el trasplante alogénico de células madre hematopoyéticas. Front Immunol. 1 de septiembre de 2023;14:1237782. doi: 10.3389/fimmu.2023.1237782. PMID: 37720225; PMCID: PMC10502717.
- ^ Miura S, Ueda K, Minakawa K, Nollet KE, Ikeda K. Perspectivas y potencial para el análisis del quimerismo después del trasplante alogénico de células madre hematopoyéticas. Cells. 6 de junio de 2024;13(11):993. doi: 10.3390/cells13110993. PMID: 38891125; PMCID: PMC11172215.
- ^ "La tasa de supervivencia de un año de MSK después de un trasplante alogénico de médula ósea supera las expectativas - Memorial Sloan Kettering Cancer Center". mskcc.org . 2012. Archivado desde el original el 13 de octubre de 2017 . Consultado el 2 de mayo de 2018 .
- ^ Consejo editorial del PDQ sobre el tratamiento pediátrico. Complicaciones, enfermedad de injerto contra huésped y efectos tardíos después del trasplante pediátrico de células madre hematopoyéticas (PDQ®): versión para profesionales de salud. 13 de junio de 2024. En: PDQ Cancer Information Summaries [Internet]. Bethesda (MD): Instituto Nacional del Cáncer (EE. UU.); 2002–. PMID: 35133768.
- ^ Elad S, Zadik Y, Hewson I, Hovan A, Correa ME, Logan R, et al. (agosto de 2010). "Una revisión sistemática de las infecciones virales asociadas con afectación oral en pacientes con cáncer: un enfoque en Herpesviridea". Atención de apoyo en el cáncer . 18 (8): 993–1006. doi :10.1007/s00520-010-0900-3. PMID 20544224. S2CID 2969472.
- ^ Wickline M, McErlean G, Carpenter PA, Iribarren S, Reding K, Berry DL. Facilitadores y barreras para una revacunación exitosa después del trasplante de células madre hematopoyéticas entre sobrevivientes adultos: una revisión de alcance. Transplant Cell Ther. 2024 Mar;30(3):268-280. doi: 10.1016/j.jtct.2023.11.009. Publicación electrónica 11 de noviembre de 2023. PMID: 37952646.
- ^ "Obstrucción sinusoidal". livertox.nih.gov . 2012. PMID 31643176 . Consultado el 30 de julio de 2019 .
- ^ Sawyer J, Elliott T, Orton L, Sowell H, Gatwood K, Shultes K. Prevención y manejo de toxicidades agudas de regímenes de acondicionamiento durante el trasplante de células madre hematopoyéticas. Clin Hematol Int. 3 de abril de 2024;6(2):1-10. doi: 10.46989/001c.94952. PMID: 38817311; PMCID: PMC11087001.
- ^ Hamidieh, AA; Behfar, M.; Jabalameli, N.; Jalali, A.; Aliabadi, LS; Sadat Hosseini, A.; Basirpanah, S.; Ghavamzadeh, A. (2014). "Cistitis hemorrágica después de trasplantes de células madre hematopoyéticas en niños: experiencia en un solo centro". Biología del trasplante de sangre y médula ósea . 20 (2): S169–S170. doi : 10.1016/j.bbmt.2013.12.275 .
- ^ Shizuru JA, Jerabek L, Edwards CT, Weissman IL (febrero de 1996). "Trasplante de células madre hematopoyéticas purificadas: requisitos para superar las barreras del injerto alogénico". Biología del trasplante de sangre y médula ósea . 2 (1): 3–14. PMID 9078349.
- ^ Gottardi F, Leardini D, Muratore E, Baccelli F, Cerasi S, Venturelli F, Zanaroli A, Belotti T, Prete A, Masetti R. Tratamiento de la enfermedad de injerto contra huésped refractaria a esteroides en niños. Trasplante Frontal. 15 de septiembre de 2023; 2: 1251112. doi: 10.3389/frtra.2023.1251112. PMID: 38993897; PMCID: PMC11235274.
- ^ Fisher SA, Cutler A, Doree C, Brunskill SJ, Stanworth SJ, Navarrete C, Girdlestone J (enero de 2019). Grupo Cochrane de Neoplasias Hematológicas (ed.). "Células estromales mesenquimales como tratamiento o profilaxis para la enfermedad de injerto contra huésped aguda o crónica en receptores de trasplante de células madre hematopoyéticas (TCMH) con una afección hematológica". Base de Datos Cochrane de Revisiones Sistemáticas . 1 (1): CD009768. doi :10.1002/14651858.CD009768.pub2. PMC 6353308 . PMID 30697701.
- ^ Baron F, Maris MB, Sandmaier BM, Storer BE, Sorror M, Diaconescu R, et al. (marzo de 2005). "Efectos de injerto contra tumor después del trasplante alogénico de células hematopoyéticas con acondicionamiento no mieloablativo". Journal of Clinical Oncology . 23 (9): 1993–2003. doi : 10.1200/JCO.2005.08.136 . hdl :2268/102049. PMID 15774790.
- ^ ab Memorial Sloan-Kettering Cancer Center > Trasplante de células madre de la sangre y la médula ósea > El efecto injerto contra tumor Archivado el 4 de julio de 2008 en Wayback Machine. Última actualización: 20 de noviembre de 2003. Consultado el 6 de abril de 2009.
- ^ Elad S, Zadik Y, Zeevi I, Miyazaki A, de Figueiredo MA, Or R (diciembre de 2010). "Cáncer oral en pacientes tras un trasplante de células madre hematopoyéticas: el seguimiento a largo plazo sugiere un mayor riesgo de recurrencia". Trasplante . 90 (11): 1243–1244. doi : 10.1097/TP.0b013e3181f9caaa . PMID 21119507.
- ^ Heydari K, Shamshirian A, Lotfi-Foroushani P, Aref A, Hedayatizadeh-Omran A, Ahmadi M, et al. (octubre de 2020). "El riesgo de neoplasias malignas en pacientes que reciben trasplante de células madre hematopoyéticas: una revisión sistemática y un metanálisis". Oncología clínica y traslacional . 22 (10): 1825–1837. doi :10.1007/s12094-020-02322-w. PMID 32108275. S2CID 211539024.
- ^ "Diapositivas de análisis de datos del Centro de Investigación Internacional de Trasplante de Sangre y Médula Ósea". mcw.edu . Archivado desde el original el 6 de agosto de 2012. Consultado el 2 de mayo de 2018 .
- ^ Sorror ML, Maris MB, Storb R, Baron F, Sandmaier BM, Maloney DG, Storer B (octubre de 2005). "Índice de comorbilidad específico del trasplante de células hematopoyéticas (TCH): una nueva herramienta para la evaluación del riesgo antes del TCH alogénico". Blood . 106 (8): 2912–2919. doi :10.1182/blood-2005-05-2004. PMC 1895304 . PMID 15994282.
- ^ Charlson ME, Pompei P, Ales KL, MacKenzie CR (1987). "Un nuevo método de clasificación de la comorbilidad pronóstica en estudios longitudinales: desarrollo y validación". Journal of Chronic Diseases . 40 (5): 373–383. doi :10.1016/0021-9681(87)90171-8. PMID 3558716.
- ^ Öberg, Anders; Genberg, Margareta; Malinovschi, Andrei; Hedenstrom, Hans; Frisk, Per (febrero de 2018). "Capacidad de ejercicio en adultos jóvenes tras trasplante de células hematopoyéticas en la infancia". Revista americana de trasplantes . 18 (2): 417–423. doi : 10.1111/ajt.14456 . ISSN 1600-6135. PMID 28787762. S2CID 1397521.
- ^ Información sobre prescripción de Neupogen Archivado el 25 de mayo de 2010 en Wayback Machine.
- ^ abcd Halter J, Kodera Y, Ispizua AU, Greinix HT, Schmitz N, Favre G, et al. (enero de 2009). "Eventos graves en donantes después de la donación alogénica de células madre hematopoyéticas". Haematologica . 94 (1): 94–101. doi :10.3324/haematol.13668. PMC 2625420 . PMID 19059940.
- ^ abcdefghi Pulsipher MA, Chitphakdithai P, Miller JP, Logan BR, King RJ, Rizzo JD, et al. (abril de 2009). "Eventos adversos entre 2408 donantes no relacionados de células madre de sangre periférica: resultados de un ensayo prospectivo del Programa Nacional de Donantes de Médula Ósea". Sangre . 113 (15): 3604–3611. doi :10.1182/blood-2008-08-175323. PMC 2668845 . PMID 19190248.
- ^ abc Pamphilon D, Siddiq S, Brunskill S, Dorée C, Hyde C, Horowitz M, Stanworth S (octubre de 2009). "Donación de células madre: ¿qué consejo se le puede dar al donante?". British Journal of Haematology . 147 (1): 71–76. doi :10.1111/j.1365-2141.2009.07832.x. PMC 3409390 . PMID 19681886.
- ^ "Anemia aplásica tratada con transfusiones diarias y médula ósea intravenosa: informe de caso tratado con transfusiones diarias". Anales de Medicina Interna . 13 (2): 357. 1 de agosto de 1939. doi :10.7326/0003-4819-13-2-357. ISSN 0003-4819.
- ^ Thomas ED, Lochte HL, Lu WC, Ferrebee JW (septiembre de 1957). "Infusión intravenosa de médula ósea en pacientes que reciben radiación y quimioterapia". The New England Journal of Medicine . 257 (11): 491–496. doi :10.1056/NEJM195709122571102. PMID 13464965.
- ^ Saxon, Wolfgang (18 de junio de 2003). «Robert A. Good, 81, fundador de la inmunología moderna, muere». The New York Times . Archivado desde el original el 4 de noviembre de 2012.
- ^ The Bone Marrow Foundation. «Muere un pionero de la investigación del cáncer». Archivado desde el original el 6 de octubre de 2013. Consultado el 6 de octubre de 2013 .
- ^ "WMDA" (PDF) . WMDA . Archivado desde el original el 20 de diciembre de 2013.
- ^ ab McNeil, Donald (11 de mayo de 2012). "Encontrar una pareja y una misión: ayudar a los negros a sobrevivir al cáncer". The New York Times . Archivado desde el original el 5 de marzo de 2014. Consultado el 15 de mayo de 2012 .
- ^ "Un paciente alemán con VIH se cura tras un trasplante de células madre". Belfast Telegraph . 15 de diciembre de 2010 . Consultado el 15 de diciembre de 2010 .
- ^ "La médula ósea 'cura a un paciente con VIH'". BBC News . 13 de noviembre de 2008. Archivado desde el original el 7 de enero de 2009 . Consultado el 2 de enero de 2009 .
- ^ Novembre J, Galvani AP, Slatkin M (noviembre de 2005). "La propagación geográfica del alelo de resistencia al VIH CCR5 Delta32". PLOS Biology . 3 (11): e339. doi : 10.1371/journal.pbio.0030339 . PMC 1255740 . PMID 16216086.
- ^ Allers K, Hütter G, Hofmann J, Loddenkemper C, Rieger K, Thiel E, Schneider T (marzo de 2011). "Evidencia de la cura de la infección por VIH mediante trasplante de células madre CCR5Δ32/Δ32". Sangre . 117 (10): 2791–2799. doi : 10.1182/blood-2010-09-309591 . PMID 21148083. S2CID 27285440.
- ^ "Trasplantando esperanza: experimento con células madre sorprende en la CROI". aidsmeds.com . 11 de marzo de 2008. Archivado desde el original el 26 de enero de 2016 . Consultado el 2 de mayo de 2018 .
- ^ Levy JA (febrero de 2009). "No es una cura para el VIH, pero alienta nuevas direcciones". The New England Journal of Medicine . 360 (7): 724–725. doi :10.1056/NEJMe0810248. PMID 19213687.
- ^ van Lunzen J, Fehse B, Hauber J (junio de 2011). "Estrategias de terapia génica: ¿podemos erradicar el VIH?". Current HIV/AIDS Reports . 8 (2): 78–84. doi :10.1007/s11904-011-0073-9. PMID 21331536. S2CID 43463970.
- ^ "El VIH regresa a dos pacientes de Boston tras trasplantes de médula ósea". CNN. 9 de diciembre de 2013. Archivado desde el original el 8 de diciembre de 2013.
- ^ Mandavilli, Apoorva (4 de marzo de 2019). "Se informa que un segundo paciente se curó del VIH, un hito en la epidemia mundial de sida". The New York Times .
- ^ McAllister LD, Beatty PG, Rose J (febrero de 1997). "Trasplante alogénico de médula ósea para leucemia mieloide crónica en un paciente con esclerosis múltiple". Trasplante de médula ósea . 19 (4): 395–397. doi : 10.1038/sj.bmt.1700666 . PMID 9051253.
- ^ ab Atkins HL, Freedman MS (enero de 2013). "Terapia con células madre hematopoyéticas para la esclerosis múltiple: las 10 lecciones más importantes aprendidas". Neurotherapeutics . 10 (1): 68–76. doi :10.1007/s13311-012-0162-5. PMC 3557353 . PMID 23192675.
- ^ Burt RK, Balabanov R, Burman J, Sharrack B, Snowden JA, Oliveira MC, et al. (enero de 2019). "Efecto del trasplante de células madre hematopoyéticas no mieloablativo frente a la terapia continua modificadora de la enfermedad en la progresión de la enfermedad en pacientes con esclerosis múltiple recurrente-remitente: un ensayo clínico aleatorizado". JAMA . 321 (2): 165–174. doi :10.1001/jama.2018.18743. PMC 6439765 . PMID 30644983.
- ^ Tolf A, Fagius J, Carlson K, Åkerfeldt T, Granberg T, Larsson EM, Burman J (noviembre de 2019). "Remisión sostenida en esclerosis múltiple después del trasplante de células madre hematopoyéticas". Acta Neurologica Scandinavica . 140 (5): 320–327. doi : 10.1111/ane.13147 . PMID 31297793. S2CID 195894616.
- ^ Burman J, Tolf A, Hägglund H, Askmark H (febrero de 2018). "Trasplante autólogo de células madre hematopoyéticas para enfermedades neurológicas". Revista de neurología, neurocirugía y psiquiatría . 89 (2): 147–155. doi :10.1136/jnnp-2017-316271. PMC 5800332 . PMID 28866625.
Lectura adicional
- Cote GM, Hochberg EP, Muzikansky A, Hochberg FH, Drappatz J, McAfee SL, et al. (enero de 2012). "Trasplante autólogo de células madre con acondicionamiento con tiotepa, busulfán y ciclofosfamida (TBC) en pacientes con afectación del SNC por linfoma no Hodgkin". Biología del trasplante de sangre y médula ósea . 18 (1): 76–83. doi : 10.1016/j.bbmt.2011.07.006 . PMID 21749848.
- Akram A, Gilani M, Chaudhry QU, Iftikhar R, Ghafoor T, Khan MA, Haider M, Nisar H (6 de mayo de 2024). "Desafíos del mundo real del trasplante de células madre hematopoyéticas haploidénticas en un país en desarrollo: la experiencia de un solo centro". Cureus . 16 (5): e59744. doi : 10.7759/cureus.59744 . PMC 11152362 . PMID 38841039.
Enlaces externos
- Trasplante de médula ósea: qué ocurre en NHS Choices
- Calculadora en línea de HCT-CI (Sorror et al. 2005)
