Vacuna
| Vacuna | |
|---|---|
 Vacuna contra la viruela y equipo para administrarla | |
| Malla | D014612 |
| Parte de una serie sobre |
| Vacunación |
|---|
Una vacuna es una preparación biológica que proporciona inmunidad adquirida activa a una enfermedad infecciosa o maligna en particular. [1] [2] La seguridad y eficacia de las vacunas ha sido ampliamente estudiada y verificada. [3] [4] Una vacuna generalmente contiene un agente que se asemeja a un microorganismo causante de una enfermedad y a menudo está hecha de formas debilitadas o muertas del microbio, sus toxinas o una de sus proteínas de superficie. El agente estimula el sistema inmunológico del cuerpo para reconocer al agente como una amenaza, destruirlo y reconocer y destruir aún más cualquier microorganismo asociado con ese agente que pueda encontrar en el futuro.
Las vacunas pueden ser profilácticas (para prevenir o aliviar los efectos de una futura infección por un patógeno natural o "salvaje" ), o terapéuticas (para combatir una enfermedad ya manifestada, como el cáncer ). [5] [6] [7] [8] Algunas vacunas ofrecen inmunidad esterilizante completa , en la que se previene la infección. [9]
La administración de vacunas se denomina vacunación . La vacunación es el método más eficaz para prevenir enfermedades infecciosas; [10] la inmunidad generalizada debida a la vacunación es en gran medida responsable de la erradicación mundial de la viruela y la restricción de enfermedades como la poliomielitis , el sarampión y el tétanos en gran parte del mundo. La Organización Mundial de la Salud (OMS) informa que actualmente hay vacunas autorizadas disponibles para veinticinco infecciones prevenibles diferentes . [11]
El primer uso registrado de la inoculación para prevenir la viruela ocurrió en el siglo XVI en China, y los primeros indicios de la práctica en China llegaron durante el siglo X. [12] También fue la primera enfermedad para la que se produjo una vacuna. [13] [14] La práctica popular de la inoculación contra la viruela fue traída de Turquía a Gran Bretaña en 1721 por Lady Mary Wortley Montagu . [15] Los términos vacuna y vacunación se derivan de Variolae vaccinae (viruela de la vaca), el término ideado por Edward Jenner (quien desarrolló el concepto de vacunas y creó la primera vacuna) para denotar la viruela de las vacas . Utilizó la frase en 1798 para el título largo de su Investigación sobre la Variolae vaccinae conocida como la viruela de las vacas , en la que describió el efecto protector de la viruela de las vacas contra la viruela. [16] En 1881, para honrar a Jenner, Louis Pasteur propuso que los términos se extendieran para cubrir las nuevas inoculaciones protectoras que se estaban desarrollando entonces. [17] La ciencia del desarrollo y producción de vacunas se denomina vaccinología .

Efectos

Existe un consenso científico abrumador de que las vacunas son una forma muy segura y eficaz de combatir y erradicar las enfermedades infecciosas. [19] [20] [21] [22] El sistema inmunológico reconoce los agentes de la vacuna como extraños, los destruye y los "recuerda". Cuando se encuentra con la versión virulenta de un agente, el cuerpo reconoce la capa proteica del agente y, por lo tanto, está preparado para responder, primero neutralizando el agente objetivo antes de que pueda entrar en las células y, segundo, reconociendo y destruyendo las células infectadas antes de que ese agente pueda multiplicarse en grandes cantidades. [23] [24]
Sin embargo, su eficacia tiene limitaciones. [25] A veces, la protección falla por razones relacionadas con la vacuna, como fallas en la atenuación de la vacuna, los regímenes de vacunación o la administración. [26]
La falla también puede ocurrir por razones relacionadas con el huésped si el sistema inmunológico del huésped no responde adecuadamente o no responde en absoluto. Se estima que la falta de respuesta relacionada con el huésped ocurre en un 2-10% de los individuos, debido a factores que incluyen la genética, el estado inmunológico, la edad, la salud y el estado nutricional. [26] Un tipo de trastorno de inmunodeficiencia primaria que resulta en falla genética es la agammaglobulinemia ligada al cromosoma X , en la que la ausencia de una enzima esencial para el desarrollo de las células B impide que el sistema inmunológico del huésped genere anticuerpos contra un patógeno . [27] [28]
Las interacciones entre el huésped y el patógeno y las respuestas a la infección son procesos dinámicos que involucran múltiples vías en el sistema inmunológico. [29] [30] Un huésped no desarrolla anticuerpos instantáneamente: mientras que la inmunidad innata del cuerpo puede activarse en tan solo doce horas, la inmunidad adaptativa puede tardar entre una y dos semanas en desarrollarse por completo. Durante ese tiempo, el huésped aún puede infectarse. [31]
Una vez que se producen los anticuerpos, pueden promover la inmunidad de varias maneras, dependiendo de la clase de anticuerpos involucrados. Su éxito en la eliminación o inactivación de un patógeno dependerá de la cantidad de anticuerpos producidos y del grado en que esos anticuerpos sean efectivos para contrarrestar la cepa del patógeno involucrado, ya que diferentes cepas pueden ser susceptibles de manera diferente a una reacción inmune dada. [30] En algunos casos, las vacunas pueden resultar en una protección inmune parcial (en la que la inmunidad es menos del 100% efectiva pero aún reduce el riesgo de infección) o en una protección inmune temporal (en la que la inmunidad disminuye con el tiempo) en lugar de una inmunidad completa o permanente. Aún pueden elevar el umbral de reinfección para la población en su conjunto y tener un impacto sustancial. [32] También pueden mitigar la gravedad de la infección, lo que resulta en una tasa de mortalidad más baja , una morbilidad más baja , una recuperación más rápida de la enfermedad y una amplia gama de otros efectos. [33] [34]
Las personas mayores a menudo muestran una respuesta menor que las más jóvenes, un patrón conocido como inmunosenescencia . [35] Los adyuvantes se utilizan comúnmente para estimular la respuesta inmunitaria, en particular en las personas mayores cuya respuesta inmunitaria a una vacuna simple puede haberse debilitado. [36]
La eficacia o rendimiento de la vacuna depende de varios factores:
- La enfermedad en sí (para algunas enfermedades la vacunación funciona mejor que para otras)
- la cepa de la vacuna (algunas vacunas son específicas para determinadas cepas de la enfermedad o, al menos, son más eficaces contra ellas) [37]
- si se ha cumplido correctamente el calendario de vacunación .
- respuesta idiosincrásica a la vacunación; algunas personas "no responden" a ciertas vacunas, lo que significa que no generan anticuerpos incluso después de haber sido vacunadas correctamente.
- factores variados como la etnia, la edad o la predisposición genética.
Si un individuo vacunado desarrolla la enfermedad contra la cual fue vacunado ( infección irruptiva ), es probable que la enfermedad sea menos virulenta que en los casos no vacunados. [38]
Consideraciones importantes en un programa de vacunación eficaz: [39]
- Modelado cuidadoso para anticipar el efecto que una campaña de inmunización tendrá sobre la epidemiología de la enfermedad en el mediano y largo plazo
- Vigilancia continua de la enfermedad pertinente tras la introducción de una nueva vacuna
- Mantenimiento de altas tasas de inmunización, incluso cuando una enfermedad se ha vuelto rara
En 1958, hubo 763.094 casos de sarampión en los Estados Unidos; 552 muertes resultaron. [40] [41] Después de la introducción de nuevas vacunas, el número de casos se redujo a menos de 150 por año (media de 56). [41] A principios de 2008, hubo 64 casos sospechosos de sarampión. Cincuenta y cuatro de esas infecciones estaban asociadas con la importación de otro país, aunque solo el trece por ciento en realidad se adquirieron fuera de los Estados Unidos; 63 de las 64 personas nunca habían sido vacunadas contra el sarampión o no estaban seguras de haber sido vacunadas. [41]
Las vacunas llevaron a la erradicación de la viruela , una de las enfermedades más contagiosas y mortales en los seres humanos. [42] Otras enfermedades como la rubéola, la polio , el sarampión, las paperas, la varicela y la fiebre tifoidea no son tan comunes como lo eran hace cien años gracias a los programas generalizados de vacunación. Mientras la gran mayoría de las personas estén vacunadas, es mucho más difícil que se produzca un brote de la enfermedad, y mucho menos que se propague. Este efecto se llama inmunidad de grupo . La polio, que se transmite solo entre humanos, es el objetivo de una amplia campaña de erradicación que ha restringido la polio endémica a solo partes de tres países (Afganistán, Nigeria y Pakistán). [43] Sin embargo, la dificultad de llegar a todos los niños, los malentendidos culturales y la desinformación han hecho que se pase por alto varias veces la fecha de erradicación prevista. [44] [45] [46] [47]
Las vacunas también ayudan a prevenir el desarrollo de resistencia a los antibióticos. Por ejemplo, al reducir en gran medida la incidencia de neumonía causada por Streptococcus pneumoniae , los programas de vacunación han reducido en gran medida la prevalencia de infecciones resistentes a la penicilina u otros antibióticos de primera línea. [48]
Se estima que la vacuna contra el sarampión previene un millón de muertes cada año. [49]
Efectos adversos
Las vacunas que se administran a niños, adolescentes o adultos son generalmente seguras. [50] [51] Los efectos adversos, si los hay, son generalmente leves. [52] La tasa de efectos secundarios depende de la vacuna en cuestión. [52] Algunos efectos secundarios comunes incluyen fiebre, dolor alrededor del lugar de la inyección y dolores musculares. [52] Además, algunas personas pueden ser alérgicas a los ingredientes de la vacuna. [53] La vacuna MMR rara vez se asocia con convulsiones febriles . [51]
Los determinantes relacionados con el huésped ("vacunado") que hacen que una persona sea susceptible a la infección, como la genética , el estado de salud (enfermedad subyacente, nutrición, embarazo, sensibilidades o alergias ), la competencia inmunológica , la edad y el impacto económico o el entorno cultural pueden ser factores primarios o secundarios que afectan la gravedad de la infección y la respuesta a una vacuna. [26] Las personas mayores (mayores de 60 años), hipersensibles a los alérgenos y obesas tienen susceptibilidad a una inmunogenicidad comprometida , que impide o inhibe la eficacia de la vacuna, lo que posiblemente requiera tecnologías de vacunas separadas para estas poblaciones específicas o vacunaciones de refuerzo repetidas para limitar la transmisión del virus . [26]
Los efectos secundarios graves son extremadamente raros. [51] La vacuna contra la varicela rara vez se asocia con complicaciones en individuos inmunodeficientes , y las vacunas contra el rotavirus se asocian moderadamente con la invaginación intestinal . [51]
Al menos 19 países tienen programas de compensación sin culpa para brindar compensación a quienes sufren efectos adversos graves por la vacunación. [54] El programa de los Estados Unidos se conoce como Ley Nacional de Lesiones por Vacunas Infantiles , y el Reino Unido emplea el Pago por Daños por Vacunas .
Tipos

Las vacunas suelen contener organismos atenuados, inactivados o muertos o productos purificados derivados de ellos. Existen varios tipos de vacunas en uso. [55] Estas representan diferentes estrategias utilizadas para intentar reducir el riesgo de enfermedad y, al mismo tiempo, conservar la capacidad de inducir una respuesta inmunitaria beneficiosa.
Atenuado
Algunas vacunas contienen microorganismos vivos atenuados . Muchos de ellos son virus activos que se han cultivado en condiciones que inhabilitan sus propiedades virulentas o que utilizan organismos estrechamente relacionados pero menos peligrosos para producir una amplia respuesta inmunitaria. Aunque la mayoría de las vacunas atenuadas son virales, algunas son de naturaleza bacteriana. Algunos ejemplos son las enfermedades virales fiebre amarilla , sarampión , paperas y rubéola , y la enfermedad bacteriana fiebre tifoidea . La vacuna viva Mycobacterium tuberculosis desarrollada por Calmette y Guérin no está hecha de una cepa contagiosa , sino que contiene una cepa modificada virulentamente llamada " BCG " que se utiliza para provocar una respuesta inmunitaria a la vacuna. La vacuna viva atenuada que contiene la cepa Yersinia pestis EV se utiliza para la inmunización contra la peste. Las vacunas atenuadas tienen algunas ventajas y desventajas. Las vacunas atenuadas, o vivas, debilitadas, suelen provocar respuestas inmunológicas más duraderas. Pero es posible que no sean seguras para su uso en personas inmunodeprimidas y, en raras ocasiones, mutan a una forma virulenta y causan la enfermedad. [56]
Inactivado
Algunas vacunas contienen microorganismos que han sido eliminados o inactivados por medios físicos o químicos. Algunos ejemplos son la vacuna antipoliomielítica inactivada (IPV ), la vacuna contra la hepatitis A , la vacuna contra la rabia y la mayoría de las vacunas contra la gripe . [57] [58]
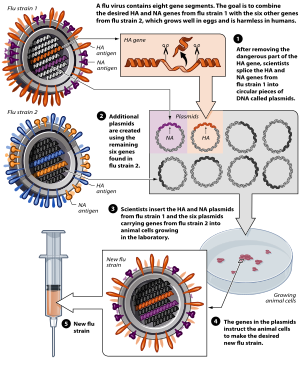
Toxoide
Las vacunas toxoides se elaboran a partir de compuestos tóxicos inactivados que son los que causan la enfermedad en lugar del microorganismo. [58] Entre los ejemplos de vacunas basadas en toxoides se incluyen la vacuna contra el tétanos y la difteria . [58] No todos los toxoides son para microorganismos; por ejemplo, el toxoide Crotalus atrox se utiliza para vacunar a los perros contra las mordeduras de serpientes de cascabel . [59]
Subunidad
En lugar de introducir un microorganismo inactivado o atenuado en un sistema inmunológico (lo que constituiría una vacuna de "agente completo"), una vacuna de subunidad utiliza un fragmento de éste para crear una respuesta inmunológica. Un ejemplo es la vacuna de subunidad contra la hepatitis B , que se compone únicamente de las proteínas de superficie del virus (anteriormente extraídas del suero sanguíneo de pacientes con infección crónica, pero que ahora se producen mediante la recombinación de los genes virales en levadura ). [60] Otros ejemplos incluyen la vacuna contra el virus del papiloma humano (VPH) con partículas similares al virus Gardasil , [61] las subunidades de hemaglutinina y neuraminidasa del virus de la gripe , [58] y las vacunas de algas comestibles . Una vacuna de subunidad se está utilizando para la inmunización contra la peste. [62]
Conjugado
Algunas bacterias tienen una capa externa de polisacárido que es poco inmunogénica . Al unir estas capas externas a proteínas (por ejemplo, toxinas), se puede hacer que el sistema inmunitario reconozca el polisacárido como si fuera un antígeno proteico. Este enfoque se utiliza en la vacuna contra Haemophilus influenzae tipo B. [63]
Vesícula de membrana externa
Las vesículas de membrana externa (VME) son inmunogénicas de forma natural y pueden manipularse para producir vacunas potentes. Las vacunas VME más conocidas son las desarrolladas para la enfermedad meningocócica del serotipo B. [ 64] [65]
Heterotípico
Las vacunas heterólogas, también conocidas como "vacunas de Jenner", son vacunas que contienen patógenos de otros animales que no causan enfermedades o causan enfermedades leves en el organismo que se está tratando. El ejemplo clásico es el uso de la viruela bovina por parte de Jenner para proteger contra la viruela. Un ejemplo actual es el uso de la vacuna BCG hecha a partir de Mycobacterium bovis para proteger contra la tuberculosis . [66]
Vacuna genética
Las vacunas genéticas se basan en el principio de la absorción de un ácido nucleico por las células, tras lo cual se produce una proteína según el patrón de ácido nucleico. Esta proteína suele ser el antígeno inmunodominante del patógeno o una proteína de superficie que permite la formación de anticuerpos neutralizantes. El subgrupo de vacunas genéticas abarca las vacunas de vector viral, las vacunas de ARN y las vacunas de ADN. [ cita requerida ]
Vector viral
Las vacunas de vector viral utilizan un virus seguro para insertar genes patógenos en el cuerpo para producir antígenos específicos , como proteínas de superficie , para estimular una respuesta inmune . [67] [68]
ARN
Una vacuna de ARNm (o vacuna de ARN ) es un nuevo tipo de vacuna que se compone del ácido nucleico ARN, empaquetado dentro de un vector como nanopartículas lipídicas . [69] Entre las vacunas contra la COVID-19 hay varias vacunas de ARN para combatir la pandemia de COVID-19 y algunas han sido aprobadas o han recibido autorización de uso de emergencia en algunos países. Por ejemplo, la vacuna Pfizer-BioNTech y la vacuna de ARNm de Moderna están aprobadas para su uso en adultos y niños en los EE. UU. [70] [71] [72]
ADN
Una vacuna de ADN utiliza un plásmido de ADN (pDNA) que codifica una proteína antigénica originada en el patógeno sobre el cual se dirigirá la vacuna. El pDNA es económico, estable y relativamente seguro, lo que lo convierte en una excelente opción para la administración de vacunas. [73]
Este enfoque ofrece una serie de ventajas potenciales sobre los enfoques tradicionales, incluida la estimulación de las respuestas de las células B y T, una mejor estabilidad de la vacuna, la ausencia de cualquier agente infeccioso y la relativa facilidad de fabricación a gran escala. [74]
Experimental
También se están desarrollando y utilizando muchas vacunas innovadoras.
- Las vacunas de células dendríticas combinan células dendríticas con antígenos para presentar los antígenos a los glóbulos blancos del cuerpo, estimulando así una reacción inmunitaria. Estas vacunas han mostrado algunos resultados preliminares positivos para el tratamiento de tumores cerebrales [75] y también se están probando en melanomas malignos. [76]
- Vector recombinante : al combinar la fisiología de un microorganismo y el ADN de otro, se puede crear inmunidad contra enfermedades que tienen procesos de infección complejos. Un ejemplo es la vacuna RVSV-ZEBOV autorizada a Merck que se está utilizando en 2018 para combatir el ébola en el Congo . [77]
- Se están desarrollando vacunas de péptidos receptores de células T para varias enfermedades utilizando modelos de fiebre del valle , estomatitis y dermatitis atópica . Se ha demostrado que estos péptidos modulan la producción de citocinas y mejoran la inmunidad celular.
- La focalización de las proteínas bacterianas identificadas que participan en la inhibición del complemento neutralizaría el mecanismo clave de virulencia bacteriana. [78]
- El uso de plásmidos se ha validado en estudios preclínicos como una estrategia de vacunación protectora contra el cáncer y las enfermedades infecciosas. Sin embargo, en estudios en humanos, este enfoque no ha logrado proporcionar un beneficio clínicamente relevante. La eficacia general de la inmunización con ADN plasmídico depende del aumento de la inmunogenicidad del plásmido y de la corrección de los factores implicados en la activación específica de las células efectoras inmunitarias. [79]
- Vector bacteriano : similar en principio a las vacunas de vector viral , pero utilizando bacterias en su lugar. [64]
- Célula presentadora de antígeno [64]
- Las tecnologías que pueden permitir la rápida implementación de una vacuna en respuesta a un nuevo patógeno incluyen el uso de partículas similares a virus [80] o nanopartículas de proteínas. [81]
Si bien la mayoría de las vacunas se crean utilizando compuestos inactivados o atenuados de microorganismos, las vacunas sintéticas están compuestas principal o totalmente de péptidos, carbohidratos o antígenos sintéticos. [ cita requerida ]
Valencia
Las vacunas pueden ser monovalentes (también llamadas univalentes ) o multivalentes (también llamadas polivalentes ). Una vacuna monovalente está diseñada para inmunizar contra un solo antígeno o un solo microorganismo. [82] Una vacuna multivalente o polivalente está diseñada para inmunizar contra dos o más cepas del mismo microorganismo, o contra dos o más microorganismos. [83] La valencia de una vacuna multivalente puede denotarse con un prefijo griego o latino (p. ej., bivalente , trivalente o tetravalente/cuadrivalente ). En ciertos casos, una vacuna monovalente puede ser preferible para desarrollar rápidamente una respuesta inmunitaria fuerte. [84]
Interacciones
Cuando se mezclan dos o más vacunas en la misma formulación, ambas pueden interferir. Esto ocurre con mayor frecuencia con las vacunas vivas atenuadas, en las que uno de los componentes de la vacuna es más robusto que los demás y suprime el crecimiento y la respuesta inmunitaria a los otros componentes. [85]
Este fenómeno se observó por primera vez [¿ cuándo? ] en la vacuna antipoliomielítica trivalente Sabin, donde se tuvo que reducir la cantidad de virus del serotipo 2 en la vacuna para evitar que interfiriera con la "captación" de los virus del serotipo 1 y 3 en la vacuna. [86] También se observó en un estudio de 2001 que era un problema con las vacunas contra el dengue , donde se encontró que el serotipo DEN-3 predominaba y suprimía la respuesta a los serotipos DEN-1, -2 y -4. [87]
Otros contenidos

Adyuvantes
Las vacunas suelen contener uno o más adyuvantes , que se utilizan para reforzar la respuesta inmunitaria. El toxoide tetánico, por ejemplo, suele adsorberse sobre alumbre . Esto presenta el antígeno de tal manera que produce una acción mayor que el simple toxoide tetánico acuoso. A las personas que tienen una reacción adversa al toxoide tetánico adsorbido se les puede administrar la vacuna simple cuando llega el momento de una dosis de refuerzo. [88]
En la preparación de la campaña del Golfo Pérsico de 1990, se utilizó la vacuna de células enteras contra la tos ferina como adyuvante de la vacuna contra el ántrax . Esto produce una respuesta inmunitaria más rápida que administrar sólo la vacuna contra el ántrax, lo que resulta beneficioso si la exposición puede ser inminente. [89]
Conservantes
Las vacunas también pueden contener conservantes para evitar la contaminación con bacterias u hongos . Hasta hace unos años, el conservante tiomersal ( también conocido como timerosal en los EE. UU. y Japón) se utilizaba en muchas vacunas que no contenían virus vivos. A partir de 2005, la única vacuna infantil en los EE. UU. que contiene tiomersal en cantidades superiores a trazas es la vacuna contra la gripe, [90] que actualmente se recomienda solo para niños con ciertos factores de riesgo. [91] Las vacunas antigripales de dosis única suministradas en el Reino Unido no enumeran el tiomersal entre los ingredientes. Los conservantes se pueden utilizar en varias etapas de la producción de vacunas, y los métodos de medición más sofisticados pueden detectar trazas de ellos en el producto terminado, como pueden hacerlo en el medio ambiente y la población en su conjunto. [92]
Muchas vacunas necesitan conservantes para prevenir efectos adversos graves, como la infección por Staphylococcus , que en un incidente de 1928 mató a 12 de 21 niños inoculados con una vacuna contra la difteria que carecía de conservante. [93] Hay varios conservantes disponibles, incluidos el tiomersal, el fenoxietanol y el formaldehído . El tiomersal es más eficaz contra las bacterias, tiene una mejor vida útil y mejora la estabilidad, la potencia y la seguridad de la vacuna; pero, en los EE. UU., la Unión Europea y algunos otros países ricos, ya no se usa como conservante en las vacunas infantiles, como medida de precaución debido a su contenido de mercurio . [94] Aunque se han hecho afirmaciones controvertidas de que el tiomersal contribuye al autismo , no hay evidencia científica convincente que respalde estas afirmaciones. [95] Además, un estudio de 10 a 11 años de 657.461 niños encontró que la vacuna MMR no causa autismo y, de hecho, redujo el riesgo de autismo en un siete por ciento. [96] [97]
Excipientes
Además de la vacuna activa en sí, los siguientes excipientes y compuestos de fabricación residuales están presentes o pueden estar presentes en las preparaciones de vacunas: [98]
- Se añaden sales o geles de aluminio como adyuvantes . Los adyuvantes se añaden para promover una respuesta más temprana y potente, y una respuesta inmunitaria más persistente a la vacuna; permiten una dosis de vacuna más baja.
- Se agregan antibióticos a algunas vacunas para prevenir el crecimiento de bacterias durante la producción y el almacenamiento de la vacuna.
- La proteína del huevo está presente en la vacuna contra la gripe y la vacuna contra la fiebre amarilla, ya que se preparan con huevos de gallina. Puede haber otras proteínas presentes.
- El formaldehído se utiliza para inactivar los productos bacterianos de las vacunas toxoides. El formaldehído también se utiliza para inactivar virus no deseados y matar bacterias que podrían contaminar la vacuna durante la producción.
- El glutamato monosódico (GMS) y el 2- fenoxietanol se utilizan como estabilizadores en algunas vacunas para ayudar a que la vacuna permanezca inalterada cuando se expone al calor, la luz, la acidez o la humedad.
- El tiomersal es un antimicrobiano que contiene mercurio y que se añade a los viales de vacunas que contienen más de una dosis para evitar la contaminación y el crecimiento de bacterias potencialmente dañinas. Debido a la controversia que rodea al tiomersal, se lo ha eliminado de la mayoría de las vacunas, excepto de la vacuna contra la gripe de uso múltiple, en la que se redujo a niveles tales que una sola dosis contenía menos de un microgramo de mercurio, un nivel similar al de comer diez gramos de atún enlatado. [99]
Nomenclatura
Se han desarrollado varias abreviaturas bastante estandarizadas para los nombres de las vacunas, aunque la estandarización no es en absoluto centralizada ni global. Por ejemplo, los nombres de las vacunas que se utilizan en los Estados Unidos tienen abreviaturas bien establecidas que también son ampliamente conocidas y utilizadas en otros lugares. Una lista extensa de ellas, proporcionada en una tabla ordenable y de libre acceso, está disponible en una página web de los Centros para el Control y la Prevención de Enfermedades de los Estados Unidos. [100] La página explica que "Las abreviaturas [en] esta tabla (columna 3) fueron estandarizadas conjuntamente por el personal de los Centros para el Control y la Prevención de Enfermedades, los grupos de trabajo del ACIP , el editor del Informe semanal de morbilidad y mortalidad (MMWR), el editor de Epidemiología y prevención de enfermedades prevenibles por vacunación (el Libro rosa), los miembros del ACIP y las organizaciones de enlace con el ACIP". [100]
Algunos ejemplos son " DTaP " para los toxoides diftérico y tetánico y la vacuna acelular contra la tos ferina, "DT" para los toxoides diftérico y tetánico, y "Td" para los toxoides diftérico y tetánico. En su página sobre la vacunación contra el tétanos, [101] el CDC explica además que "Las letras mayúsculas en estas abreviaturas indican dosis completas de toxoides diftérico (D) y tetánico (T) y vacuna contra la tos ferina (P). Las "d" y "p" minúsculas indican dosis reducidas de difteria y tos ferina utilizadas en las fórmulas para adolescentes y adultos. La "a" en DTaP y Tdap significa "acelular", lo que significa que el componente de la tos ferina contiene solo una parte del organismo de la tos ferina". [101]
Otra lista de abreviaturas de vacunas establecidas se encuentra en la página de los CDC llamada "Acrónimos y abreviaturas de vacunas", con abreviaturas utilizadas en los registros de inmunización de los EE. UU. [102] El sistema de nombres adoptados de los Estados Unidos tiene algunas convenciones para el orden de las palabras de los nombres de las vacunas, colocando los sustantivos principales primero y los adjetivos después . Esta es la razón por la que el USAN para " OPV " es "vacuna contra la poliomielitis oral viva" en lugar de "vacuna contra la poliomielitis oral".
Licencias
La licencia de una vacuna se obtiene después de la conclusión exitosa del ciclo de desarrollo y de los ensayos clínicos y otros programas involucrados a través de las Fases I a III que demuestran seguridad, inmunoactividad, seguridad inmunogenética a una dosis específica dada, eficacia probada en la prevención de infecciones para poblaciones objetivo y efecto preventivo duradero (se debe estimar la resistencia en el tiempo o la necesidad de revacunación). [103] Debido a que las vacunas preventivas se evalúan predominantemente en cohortes de población sana y se distribuyen entre la población general, se requiere un alto estándar de seguridad. [104] Como parte de una licencia multinacional de una vacuna, el Comité de Expertos en Normalización Biológica de la Organización Mundial de la Salud desarrolló directrices de estándares internacionales para la fabricación y el control de calidad de las vacunas, un proceso pensado como una plataforma para que las agencias reguladoras nacionales soliciten su propio proceso de licencia. [103] Los fabricantes de vacunas no reciben la licencia hasta que un ciclo clínico completo de desarrollo y ensayos demuestra que la vacuna es segura y tiene eficacia a largo plazo, luego de una revisión científica por parte de una organización reguladora multinacional o nacional, como la Agencia Europea de Medicamentos (EMA) o la Administración de Alimentos y Medicamentos de los Estados Unidos (FDA). [105] [106]
Cuando los países en desarrollo adoptan las directrices de la OMS para el desarrollo y la autorización de vacunas, cada país tiene su propia responsabilidad de emitir una licencia nacional y de gestionar, distribuir y supervisar la vacuna durante su uso en cada nación. [103] Generar confianza y aceptación de una vacuna autorizada entre el público es una tarea de comunicación por parte de los gobiernos y el personal sanitario para garantizar que una campaña de vacunación se desarrolle sin problemas, salve vidas y permita la recuperación económica. [107] [108] Cuando se autoriza una vacuna, inicialmente habrá un suministro limitado debido a factores variables de fabricación, distribución y logística, lo que requiere un plan de asignación para el suministro limitado y qué segmentos de la población deben priorizarse para recibir primero la vacuna. [107]
Organización Mundial de la Salud
Las vacunas desarrolladas para su distribución multinacional a través del Fondo de las Naciones Unidas para la Infancia (UNICEF) requieren una precalificación de la OMS para garantizar estándares internacionales de calidad, seguridad, inmunogenicidad y eficacia para su adopción por numerosos países. [103]
El proceso requiere consistencia en la fabricación en los laboratorios contratados por la OMS siguiendo las Buenas Prácticas de Fabricación (BPF). [103] Cuando las agencias de la ONU están involucradas en la concesión de licencias de vacunas, las naciones individuales colaboran 1) emitiendo la autorización de comercialización y una licencia nacional para la vacuna, sus fabricantes y socios de distribución; y 2) realizando una vigilancia posterior a la comercialización , incluidos los registros de eventos adversos después del programa de vacunación. La OMS trabaja con agencias nacionales para monitorear las inspecciones de las instalaciones de fabricación y los distribuidores para verificar el cumplimiento de las BPF y la supervisión regulatoria. [103]
Algunos países optan por comprar vacunas autorizadas por organizaciones nacionales de buena reputación, como la EMA, la FDA o agencias nacionales de otros países ricos, pero esas compras suelen ser más caras y es posible que no cuenten con recursos de distribución adecuados a las condiciones locales de los países en desarrollo. [103]
unión Europea
En la Unión Europea (UE), las vacunas contra patógenos pandémicos, como la gripe estacional , están autorizadas en toda la UE, donde todos los estados miembros cumplen ("centralizada"), están autorizadas solo para algunos estados miembros ("descentralizada"), o están autorizadas a nivel nacional individual. [105] En general, todos los estados de la UE siguen las directrices regulatorias y los programas clínicos definidos por el Comité Europeo de Medicamentos de Uso Humano (CHMP), un panel científico de la Agencia Europea de Medicamentos (EMA) responsable de la autorización de vacunas. [105] El CHMP cuenta con el apoyo de varios grupos de expertos que evalúan y monitorean el progreso de una vacuna antes y después de la autorización y distribución. [105]
Estados Unidos
En el marco de la FDA, el proceso de establecer evidencia de la seguridad y eficacia clínica de las vacunas es el mismo que el del proceso de aprobación de medicamentos de venta con receta . [109] Si se superan con éxito las etapas de desarrollo clínico, el proceso de licencia de la vacuna es seguido por una Solicitud de Licencia Biológica que debe proporcionar un equipo de revisión científica (de diversas disciplinas, como médicos, estadísticos, microbiólogos, químicos) y documentación completa para que la vacuna candidata tenga eficacia y seguridad a lo largo de su desarrollo. También durante esta etapa, la instalación de fabricación propuesta es examinada por revisores expertos para verificar el cumplimiento de las BPM, y la etiqueta debe tener una descripción que cumpla con las BPM para permitir que los proveedores de atención médica definan el uso específico de la vacuna, incluidos sus posibles riesgos, para comunicar y entregar la vacuna al público. [109] Después de la licencia, el monitoreo de la vacuna y su producción, incluidas las inspecciones periódicas para verificar el cumplimiento de las BPM, continúa mientras el fabricante conserve su licencia, lo que puede incluir presentaciones adicionales a la FDA de pruebas de potencia, seguridad y pureza para cada paso de fabricación de la vacuna. [109]
India
En la India, el Controlador General de Medicamentos , jefe de departamento de la Organización Central de Control de Normas de Medicamentos , el organismo regulador nacional de la India para cosméticos, productos farmacéuticos y dispositivos médicos, es responsable de la aprobación de licencias para categorías específicas de medicamentos, como vacunas y otros artículos medicinales, como sangre o productos sanguíneos, líquidos intravenosos y sueros. [110]
Vigilancia postcomercialización
Hasta que una vacuna se utilice entre la población general, es posible que no se conozcan todos los posibles efectos adversos de la vacuna, lo que requiere que los fabricantes realicen estudios de fase IV para la vigilancia posterior a la comercialización de la vacuna mientras se usa ampliamente en el público. [103] [109] La OMS trabaja con los estados miembros de la ONU para implementar la vigilancia posterior a la autorización. [103] La FDA se basa en un Sistema de notificación de eventos adversos de las vacunas para monitorear las preocupaciones de seguridad sobre una vacuna durante su uso en el público estadounidense. [109]
Programación
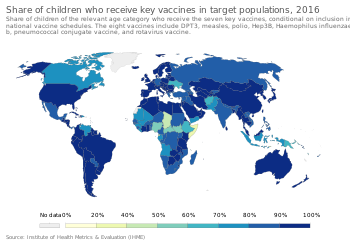
Para proporcionar la mejor protección, se recomienda que los niños reciban vacunas tan pronto como sus sistemas inmunológicos estén lo suficientemente desarrollados para responder a vacunas particulares, con dosis adicionales de "refuerzo" que a menudo se requieren para lograr la "inmunidad completa". Esto ha llevado al desarrollo de complejos programas de vacunación. Las recomendaciones globales del programa de vacunación son emitidas por el Grupo Asesor Estratégico de Expertos y serán traducidas posteriormente por el comité asesor a nivel de país teniendo en cuenta factores locales como la epidemiología de la enfermedad, la aceptabilidad de la vacunación, la equidad en las poblaciones locales y las limitaciones programáticas y financieras. [111] En los Estados Unidos, el Comité Asesor sobre Prácticas de Inmunización , que recomienda adiciones al programa para los Centros para el Control y la Prevención de Enfermedades , recomienda la vacunación sistemática de los niños contra [112] la hepatitis A , la hepatitis B , la poliomielitis, las paperas, el sarampión, la rubéola, la difteria , la tos ferina , el tétanos , la HiB , la varicela, el rotavirus , la gripe , la enfermedad meningocócica y la neumonía . [113]
La gran cantidad de vacunas y dosis de refuerzo recomendadas (hasta 24 inyecciones antes de los dos años) ha generado problemas para lograr el cumplimiento total de la vacuna. Para combatir la disminución de las tasas de cumplimiento, se han instituido varios sistemas de notificación y ahora se comercializan muchas vacunas combinadas (por ejemplo, la vacuna pentavalente y la vacuna MMRV ), que protegen contra múltiples enfermedades.
Además de las recomendaciones para las vacunas infantiles y las dosis de refuerzo, se recomiendan muchas vacunas específicas para otras edades o para inyecciones repetidas a lo largo de la vida, las más comunes son las del sarampión, el tétanos, la gripe y la neumonía. A las mujeres embarazadas se les suele hacer una prueba para detectar la resistencia continua a la rubéola. La vacuna contra el virus del papiloma humano se recomienda en los EE. UU. (a partir de 2011) [114] y el Reino Unido (a partir de 2009). [115] Las recomendaciones de vacunas para los ancianos se concentran en la neumonía y la gripe, que son más mortales para ese grupo. En 2006, se introdujo una vacuna contra el herpes zóster , una enfermedad causada por el virus de la varicela, que generalmente afecta a los ancianos. [116]
La programación y la dosificación de una vacunación se pueden adaptar al nivel de inmunocompetencia de un individuo [117] y para optimizar la distribución de una vacuna en toda la población cuando su suministro es limitado, [118] por ejemplo, en el contexto de una pandemia.
Economía del desarrollo
Uno de los desafíos que plantea el desarrollo de vacunas es económico: muchas de las enfermedades que más exigen una vacuna, como el VIH , la malaria y la tuberculosis, se dan principalmente en países pobres. Las empresas farmacéuticas y de biotecnología tienen pocos incentivos para desarrollar vacunas para estas enfermedades porque el potencial de ingresos es escaso. Incluso en los países más ricos, los beneficios financieros suelen ser mínimos y los riesgos financieros y de otro tipo son grandes. [119]
Hasta la fecha, la mayor parte del desarrollo de vacunas se ha basado en la financiación "impulsada" por parte del gobierno, las universidades y las organizaciones sin fines de lucro. [120] Muchas vacunas han sido muy rentables y beneficiosas para la salud pública . [121] El número de vacunas realmente administradas ha aumentado drásticamente en las últimas décadas. [122] Este aumento, en particular en el número de vacunas diferentes administradas a los niños antes de su entrada en las escuelas, puede deberse a los mandatos y el apoyo del gobierno, más que a incentivos económicos. [123]
Patentes
Según la Organización Mundial de la Salud, la mayor barrera para la producción de vacunas en los países menos desarrollados no han sido las patentes , sino los importantes requisitos financieros, de infraestructura y de mano de obra necesarios para entrar en el mercado. Las vacunas son mezclas complejas de compuestos biológicos y, a diferencia de lo que ocurre con los medicamentos de venta con receta , no existen vacunas genéricas verdaderas. La vacuna producida por una nueva instalación debe someterse a pruebas clínicas completas de seguridad y eficacia por parte del fabricante. En el caso de la mayoría de las vacunas, se patentan procesos tecnológicos específicos que se pueden evitar con métodos de fabricación alternativos, pero esto requiere una infraestructura de I+D y una mano de obra debidamente cualificada. En el caso de unas pocas vacunas relativamente nuevas, como la vacuna contra el virus del papiloma humano , las patentes pueden suponer una barrera adicional. [124]
Cuando se necesitó urgentemente aumentar la producción de vacunas durante la pandemia de COVID-19 en 2021, la Organización Mundial del Comercio y los gobiernos de todo el mundo evaluaron la posibilidad de renunciar a los derechos de propiedad intelectual y las patentes sobre las vacunas contra la COVID-19 , lo que "eliminaría todas las barreras potenciales al acceso oportuno a productos médicos asequibles contra la COVID-19, incluidas vacunas y medicamentos, y aumentaría la fabricación y el suministro de productos médicos esenciales". [125]
Producción

La producción de vacunas es fundamentalmente diferente de otros tipos de fabricación –incluida la fabricación farmacéutica convencional– en el sentido de que las vacunas están destinadas a ser administradas a millones de personas, de las cuales la gran mayoría están perfectamente sanas. [126] Este hecho impulsa un proceso de producción extraordinariamente riguroso con estrictos requisitos de cumplimiento que van mucho más allá de lo que se exige a otros productos. [126]
Dependiendo del antígeno, puede costar entre 50 y 500 millones de dólares construir una planta de producción de vacunas, lo que requiere equipo altamente especializado, salas blancas y salas de contención. [127] Existe una escasez mundial de personal con la combinación adecuada de habilidades, experiencia, conocimiento, competencia y personalidad para dotar de personal a las líneas de producción de vacunas. [127] Con las notables excepciones de Brasil, China e India, los sistemas educativos de muchos países en desarrollo no pueden proporcionar suficientes candidatos calificados, y los fabricantes de vacunas con sede en esos países deben contratar personal expatriado para mantener la producción en marcha. [127]
La producción de vacunas consta de varias etapas. En primer lugar, se genera el propio antígeno. Los virus se cultivan en células primarias, como huevos de gallina (p. ej., para la gripe) o en líneas celulares continuas, como células humanas cultivadas (p. ej., para la hepatitis A ). [128] Las bacterias se cultivan en biorreactores (p. ej., Haemophilus influenzae tipo b). Asimismo, se puede generar una proteína recombinante derivada de los virus o bacterias en cultivos de levaduras, bacterias o células. [129] [130]
Una vez generado el antígeno, se lo aísla de las células utilizadas para generarlo. Puede ser necesario inactivar un virus, posiblemente sin necesidad de purificarlo más. Las proteínas recombinantes necesitan muchas operaciones que implican ultrafiltración y cromatografía en columna. Finalmente, la vacuna se formula añadiendo adyuvante, estabilizadores y conservantes según sea necesario. El adyuvante mejora la respuesta inmunitaria al antígeno, los estabilizadores aumentan la vida útil y los conservantes permiten el uso de viales multidosis. [129] [130] Las vacunas combinadas son más difíciles de desarrollar y producir, debido a las posibles incompatibilidades e interacciones entre los antígenos y otros ingredientes involucrados. [131]
La última etapa de la fabricación de vacunas antes de su distribución es el llenado y acabado , que es el proceso de llenar viales con vacunas y envasarlos para su distribución. Aunque esta es una parte conceptualmente simple del proceso de fabricación de vacunas, a menudo es un cuello de botella en el proceso de distribución y administración de vacunas. [132] [133] [134]
Las técnicas de producción de vacunas están evolucionando. Se espera que las células de mamíferos cultivadas adquieran cada vez más importancia, en comparación con las opciones convencionales, como los huevos de gallina, debido a su mayor productividad y a la baja incidencia de problemas de contaminación. Se espera que la tecnología de recombinación que produce vacunas desintoxicadas genéticamente aumente en popularidad para la producción de vacunas bacterianas que utilizan toxoides. Se espera que las vacunas combinadas reduzcan las cantidades de antígenos que contienen y, por lo tanto, disminuyan las interacciones indeseables, mediante el uso de patrones moleculares asociados a patógenos . [131]
Fabricantes de vacunas
Las empresas con mayor participación de mercado en la producción de vacunas son Merck , Sanofi , GlaxoSmithKline , Pfizer y Novartis , con un 70% de las ventas de vacunas concentradas en la UE o EE. UU. (2013). [135] : 42 Las plantas de fabricación de vacunas requieren grandes inversiones de capital (de $50 millones a $300 millones) y su construcción puede llevar entre 4 y 6 años, y el proceso completo de desarrollo de la vacuna demora entre 10 y 15 años. [135] : 43 La fabricación en los países en desarrollo está desempeñando un papel cada vez más importante en el suministro a estos países, específicamente en lo que respecta a las vacunas más antiguas y en Brasil, India y China. [135] : 47 Los fabricantes en la India son los más avanzados en el mundo en desarrollo e incluyen al Serum Institute of India , uno de los mayores productores de vacunas por número de dosis y un innovador en procesos, que recientemente mejoró la eficiencia de producción de la vacuna contra el sarampión de 10 a 20 veces, debido al cambio a un cultivo de células MRC-5 en lugar de huevos de gallina. [135] : 48 Las capacidades de fabricación de China se centran en satisfacer sus propias necesidades internas, y Sinopharm (CNPGC) por sí sola proporciona más del 85% de las dosis para 14 vacunas diferentes en China. [135] : 48 Brasil se está acercando al punto de satisfacer sus propias necesidades internas utilizando tecnología transferida del mundo desarrollado. [135] : 49
Sistemas de entrega

Uno de los métodos más comunes para administrar vacunas al cuerpo humano es la inyección .
El desarrollo de nuevos sistemas de administración hace abrigar la esperanza de que se puedan desarrollar vacunas más seguras y eficientes de administrar. Las líneas de investigación incluyen los liposomas y el complejo inmunoestimulante ISCOM (inmunostimulante complex). [136]
Entre los avances más notables en materia de tecnologías de administración de vacunas se encuentran las vacunas orales. Los primeros intentos de aplicar vacunas orales mostraron distintos grados de promesa, a principios del siglo XX, en una época en la que la posibilidad misma de una vacuna antibacteriana oral eficaz era controvertida. [137] En la década de 1930, por ejemplo, había un creciente interés en el valor profiláctico de una vacuna oral contra la fiebre tifoidea . [138]
Una vacuna oral contra la polio resultó ser eficaz cuando las vacunas fueron administradas por personal voluntario sin capacitación formal; los resultados también demostraron una mayor facilidad y eficiencia en la administración de las vacunas. Las vacunas orales eficaces tienen muchas ventajas; por ejemplo, no hay riesgo de contaminación de la sangre. Las vacunas destinadas a la administración oral no necesitan ser líquidas y, como son sólidas, suelen ser más estables y menos propensas a dañarse o estropearse por congelación durante el transporte y el almacenamiento. [139] Esa estabilidad reduce la necesidad de una " cadena de frío ": los recursos necesarios para mantener las vacunas dentro de un rango restringido de temperaturas desde la etapa de fabricación hasta el punto de administración, lo que, a su vez, puede reducir los costos de las vacunas.
Un método de microagujas, que todavía está en etapas de desarrollo, utiliza "proyecciones puntiagudas fabricadas en matrices que pueden crear vías de administración de vacunas a través de la piel". [140]
Actualmente se están realizando pruebas en animales con un sistema experimental de administración de vacunas sin agujas [141] . [142] [143] Un parche del tamaño de un sello similar a una venda adhesiva contiene alrededor de 20.000 proyecciones microscópicas por cm cuadrado. [144] Esta administración dérmica aumenta potencialmente la eficacia de la vacunación, al tiempo que requiere menos vacuna que una inyección. [145]
En medicina veterinaria

Las vacunas de los animales se utilizan tanto para prevenir que contraigan enfermedades como para prevenir la transmisión de enfermedades a los seres humanos. [146] Tanto los animales que se tienen como mascotas como los animales criados como ganado se vacunan de forma rutinaria. En algunos casos, se puede vacunar a las poblaciones silvestres. Esto a veces se logra con alimentos mezclados con vacunas que se esparcen en una zona propensa a enfermedades y se ha utilizado para intentar controlar la rabia en los mapaches .
En los casos de rabia, la vacunación de los perros puede ser obligatoria por ley. Otras vacunas caninas incluyen la vacuna contra el moquillo canino , el parvovirus canino , la hepatitis canina infecciosa , el adenovirus-2 , la leptospirosis , la Bordetella , el virus de la parainfluenza canina y la enfermedad de Lyme , entre otras.
Se han documentado casos de vacunas veterinarias utilizadas en humanos, ya sea intencional o accidentalmente, con algunos casos de enfermedad resultante, más notablemente con brucelosis . [147] Sin embargo, la notificación de tales casos es rara y se ha estudiado muy poco sobre la seguridad y los resultados de tales prácticas. Con el advenimiento de la vacunación con aerosol en las clínicas veterinarias, la exposición humana a patógenos que no son naturalmente transportados por los humanos, como Bordetella bronchiseptica , probablemente ha aumentado en los últimos años. [147] En algunos casos, más notablemente la rabia , la vacuna veterinaria paralela contra un patógeno puede ser hasta órdenes de magnitud más económica que la humana.
Vacunas DIVA
Las vacunas DIVA (Diferenciación de Animales Infectados de Vacunados), también conocidas como SIVA (Segregación de Animales Infectados de Vacunados), permiten diferenciar entre animales infectados y vacunados. Las vacunas DIVA contienen al menos un epítopo menos que el microorganismo salvaje equivalente. Una prueba diagnóstica complementaria que detecta el anticuerpo contra ese epítopo ayuda a identificar si el animal ha sido vacunado o no. [ cita requerida ]
Las primeras vacunas DIVA (antes denominadas vacunas marcadoras y desde 1999 denominadas vacunas DIVA) y pruebas diagnósticas complementarias fueron desarrolladas por JT van Oirschot y colegas en el Instituto Veterinario Central de Lelystad, Países Bajos. [148] [149] Encontraron que algunas vacunas existentes contra la pseudorrabia (también denominada enfermedad de Aujeszky) tenían deleciones en su genoma viral (entre las que se encontraba el gen gE). Se produjeron anticuerpos monoclonales contra esa deleción y se seleccionaron para desarrollar un ELISA que demostró anticuerpos contra gE. Además, se construyeron nuevas vacunas gE-negativas diseñadas genéticamente. [150] En la misma línea, se han desarrollado vacunas DIVA y pruebas diagnósticas complementarias contra infecciones por herpesvirus bovino 1. [149] [151]
La estrategia DIVA se ha aplicado en varios países para erradicar con éxito el virus de la pseudorrabia en ellos. Las poblaciones porcinas fueron vacunadas intensivamente y monitoreadas mediante la prueba diagnóstica complementaria y, posteriormente, los cerdos infectados fueron eliminados de la población. Las vacunas DIVA contra el herpesvirus bovino 1 también se utilizan ampliamente en la práctica. [ cita requerida ] Se están realizando esfuerzos considerables para aplicar el principio DIVA a una amplia gama de enfermedades infecciosas, como la peste porcina clásica, [152] la influenza aviar, [153] la pleuroneumonía por Actinobacillus [154] y las infecciones por Salmonella en cerdos. [155]
Historia

Antes de la introducción de la vacunación con material de casos de viruela vacuna (inmunización heterotípica), la viruela podía prevenirse mediante la variolación deliberada con el virus de la viruela. Los primeros indicios de la práctica de la variolación para la viruela en China aparecen durante el siglo X. [156] [ se necesita más explicación ] Los chinos también practicaron el uso más antiguo documentado de la variolación, que se remonta al siglo XV. Implementaron un método de " insuflación nasal " administrado soplando material de viruela en polvo, generalmente costras, en las fosas nasales. Se han registrado varias técnicas de insuflación a lo largo de los siglos XVI y XVII en China. [157] : 60 La Royal Society de Londres recibió dos informes sobre la práctica china de inoculación en 1700; uno de Martin Lister , que recibió un informe de un empleado de la Compañía de las Indias Orientales destinado en China, y otro de Clopton Havers . [158] En Francia, Voltaire informa que los chinos han practicado la variolización "estos cien años". [159]

Mary Wortley Montagu , que había presenciado la variolación en Turquía, hizo variolar a su hija de cuatro años en presencia de médicos de la Corte Real en 1721 a su regreso a Inglaterra. [157] Más tarde ese año, Charles Maitland llevó a cabo una variolación experimental de seis prisioneros en la prisión de Newgate en Londres. [160] El experimento fue un éxito, y pronto la variolación atrajo la atención de la familia real, que ayudó a promover el procedimiento. Sin embargo, en 1783, varios días después de que el príncipe Octavio de Gran Bretaña fuera inoculado, murió. [161] En 1796, el médico Edward Jenner tomó pus de la mano de una lechera con viruela vacuna , lo rascó en el brazo de un niño de 8 años, James Phipps , y seis semanas después varioló al niño con viruela, observando después que no contrajo viruela. [162] [163] Jenner amplió sus estudios y, en 1798, informó que su vacuna era segura en niños y adultos, y podía transferirse de brazo a brazo, lo que reducía la dependencia de suministros inciertos de vacas infectadas. [161] En 1804, la expedición española de vacunación contra la viruela de Balmis a las colonias españolas de México y Filipinas utilizó el método de transporte de brazo a brazo para evitar el hecho de que la vacuna sobrevivía solo 12 días in vitro . Utilizaron viruela bovina. [164] Dado que la vacunación con viruela bovina era mucho más segura que la inoculación de viruela, [165] esta última, aunque todavía se practicaba ampliamente en Inglaterra, fue prohibida en 1840. [166]

Siguiendo el trabajo de Jenner, la segunda generación de vacunas fue introducida en la década de 1880 por Louis Pasteur , quien desarrolló vacunas contra el cólera aviar y el ántrax , [17] y desde finales del siglo XIX las vacunas fueron consideradas una cuestión de prestigio nacional. Se adoptaron políticas nacionales de vacunación y se aprobaron leyes de vacunación obligatoria. [162] En 1931, Alice Miles Woodruff y Ernest Goodpasture documentaron que el virus de la viruela aviar podía cultivarse en huevos de gallina embrionados . Pronto los científicos comenzaron a cultivar otros virus en huevos. Los huevos se utilizaron para la propagación del virus en el desarrollo de una vacuna contra la fiebre amarilla en 1935 y una vacuna contra la gripe en 1945. En 1959, los medios de crecimiento y el cultivo celular reemplazaron a los huevos como el método estándar de propagación del virus para las vacunas. [167]
La vacunología floreció en el siglo XX, cuando se introdujeron varias vacunas exitosas, incluidas las de la difteria , el sarampión , las paperas y la rubéola . Los logros más importantes incluyeron el desarrollo de la vacuna contra la polio en la década de 1950 y la erradicación de la viruela durante las décadas de 1960 y 1970. Maurice Hilleman fue el más prolífico de los desarrolladores de vacunas en el siglo XX. A medida que las vacunas se volvieron más comunes, muchas personas comenzaron a darlas por sentado. Sin embargo, las vacunas siguen siendo difíciles de conseguir para muchas enfermedades importantes, como el herpes simple , la malaria , la gonorrea y el VIH . [162] [168]
Generaciones de vacunas

Las vacunas de primera generación son vacunas de organismo completo, ya sean vivas y debilitadas o muertas. [169] Las vacunas vivas atenuadas, como las vacunas contra la viruela y la polio, pueden inducir respuestas de células T asesinas (T C o CTL), respuestas de células T auxiliares (T H ) e inmunidad de anticuerpos . Sin embargo, las formas atenuadas de un patógeno pueden convertirse en una forma peligrosa y pueden causar enfermedad en receptores de vacunas inmunodeprimidos (como aquellos con SIDA ). Si bien las vacunas muertas no tienen este riesgo, no pueden generar respuestas específicas de células T asesinas y pueden no funcionar en absoluto para algunas enfermedades. [169]
Las vacunas de segunda generación se desarrollaron para reducir los riesgos de las vacunas vivas. Se trata de vacunas de subunidades, que consisten en antígenos proteicos específicos (como el toxoide tetánico o diftérico ) o componentes proteicos recombinantes (como el antígeno de superficie de la hepatitis B ). Pueden generar respuestas de linfocitos T y anticuerpos , pero no respuestas de linfocitos T citotóxicos. [ cita requerida ]
Las vacunas de ARN y las vacunas de ADN son ejemplos de vacunas de tercera generación. [169] [170] [171] En 2016, una vacuna de ADN para el virus del Zika comenzó a probarse en los Institutos Nacionales de Salud . Por otra parte, Inovio Pharmaceuticals y GeneOne Life Science comenzaron las pruebas de una vacuna de ADN diferente contra el Zika en Miami. La fabricación de las vacunas en volumen estaba sin resolver en 2016. [172] Los ensayos clínicos de vacunas de ADN para prevenir el VIH están en marcha. [173] Las vacunas de ARNm como BNT162b2 se desarrollaron en el año 2020 con la ayuda de la Operación Warp Speed y se desplegaron masivamente para combatir la pandemia de COVID-19 . En 2021, Katalin Karikó y Drew Weissman recibieron el Premio Horwitz de la Universidad de Columbia por su investigación pionera en tecnología de vacunas de ARNm. [174]
Tendencias
Esta sección necesita ser actualizada . ( Junio de 2018 ) |
Desde al menos 2013, los científicos han estado tratando de desarrollar vacunas sintéticas de tercera generación reconstruyendo la estructura externa de un virus ; se esperaba que esto ayudara a prevenir la resistencia a las vacunas . [175]
Los principios que rigen la respuesta inmune ahora se pueden utilizar en vacunas hechas a medida contra muchas enfermedades humanas no infecciosas, como cánceres y trastornos autoinmunes. [176] Por ejemplo, la vacuna experimental CYT006-AngQb se ha investigado como un posible tratamiento para la presión arterial alta . [177] Los factores que afectan las tendencias del desarrollo de vacunas incluyen el progreso en la medicina traslacional, la demografía , la ciencia regulatoria , las respuestas políticas, culturales y sociales. [178]
Plantas como biorreactores para la producción de vacunas
La idea de producir vacunas a través de plantas transgénicas fue identificada ya en 2003. Plantas como el tabaco , la papa , el tomate y el plátano pueden tener genes insertados que hacen que produzcan vacunas utilizables para humanos. [179] En 2005, se desarrollaron plátanos que producen una vacuna humana contra la hepatitis B. [180]
Vacilación ante las vacunas

La reticencia a las vacunas es el retraso en la aceptación o el rechazo de las vacunas a pesar de la disponibilidad de servicios de vacunación. El término abarca las negativas rotundas a vacunar, el retraso en la vacunación, la aceptación de las vacunas pero la incertidumbre sobre su uso o el uso de ciertas vacunas pero no de otras. [182] [183] [184] [185] Existe un consenso científico abrumador de que las vacunas son generalmente seguras y eficaces. [186] [187] [188] [189] La reticencia a las vacunas a menudo da lugar a brotes de enfermedades y muertes por enfermedades prevenibles mediante vacunación . [190] [191] [192] [193] [194] [195] Por tanto, la Organización Mundial de la Salud caracterizó la reticencia a las vacunas como una de las diez principales amenazas sanitarias mundiales en 2019. [196] [197]
Véase también
- Ley de control de productos biológicos
- Coalición para la innovación en preparación para epidemias
- Jeringa voladora
- Registro de vacunación
- Inmunoterapia
- Lista de ingredientes de la vacuna
- Lista de temas sobre vacunas
- Efecto no específico de las vacunas
- Hipótesis de la vacuna antipoliomielítica oral contra el sida
- Atención sanitaria preventiva
- Vacunología inversa
- TA-CD
- Cronología de las vacunas
- Virosoma
- Vacunador
- Evento adverso relacionado con la vacuna (problemas de seguridad)
- Enfriador de vacunas
- Fracaso de la vacuna
- Vacilación ante las vacunas
- Vacunas
- Vector viral
- Partícula parecida a un virus
- Vacuna nasal
Referencias
- ^ "Estándares de práctica ampliados" (PDF) . Código administrativo de Iowa . 2019. Archivado (PDF) del original el 19 de enero de 2023 . Consultado el 16 de enero de 2023 .
- ^ "Inmunización: conceptos básicos". Centros para el Control y la Prevención de Enfermedades . 22 de noviembre de 2022. Archivado desde el original el 12 de julio de 2023. Consultado el 8 de julio de 2023 .
- ^ Amanna, Ian J.; Slifka, Mark K. (2018). "Vacunas exitosas". En Lars Hangartner; Dennis R. Burton (eds.). Estrategias de vacunación contra patógenos altamente variables . Temas actuales en microbiología e inmunología, vol. 428. Vol. 428. Springer. págs. 1–30. doi :10.1007/82_2018_102. ISBN. 978-3-030-58003-2. PMC 6777997 . PMID 30046984.
El efecto de las vacunas en la salud pública es verdaderamente notable. Un estudio que examinó el impacto de la vacunación infantil en la cohorte de nacimientos de EE. UU. de 2001 encontró que las vacunas evitaron 33.000 muertes y 14 millones de casos de enfermedad (Zhou et al. 2005). Entre 73 naciones apoyadas por la alianza GAVI, los modelos matemáticos proyectan que las vacunas evitarán 23,3 millones de muertes entre 2011 y 2020 en comparación con lo que habría ocurrido si no hubiera vacunas disponibles (Lee et al. 2013). Se han desarrollado vacunas contra una amplia variedad de patógenos humanos.
- ^ Zimmer, Carl (20 de noviembre de 2020). "Dos empresas afirman que sus vacunas tienen una eficacia del 95 %. ¿Qué significa eso? Se podría suponer que 95 de cada 100 personas vacunadas estarán protegidas contra la COVID-19, pero no es así como funcionan las matemáticas". The New York Times . Archivado desde el original el 22 de noviembre de 2020. Consultado el 21 de noviembre de 2020 .
- ^ Melief CJ, van Hall T, Arens R, Ossendorp F, van der Burg SH (septiembre de 2015). "Vacunas terapéuticas contra el cáncer". The Journal of Clinical Investigation . 125 (9): 3401–3412. doi :10.1172/JCI80009. PMC 4588240 . PMID 26214521.
- ^ Bol KF, Aarntzen EH, Pots JM, Olde Nordkamp MA, van de Rakt MW, Scharenborg NM, de Boer AJ, van Oorschot TG, Croockewit SA, Blokx WA, Oyen WJ, Boerman OC, Mus RD, van Rossum MM, van der Graaf CA, Punt CJ, Adema GJ, Figdor CG, de Vries IJ, Schreibelt G (marzo de 2016). "Las vacunas profilácticas son potentes activadores de células dendríticas derivadas de monocitos e impulsan respuestas antitumorales eficaces en pacientes con melanoma a costa de la toxicidad". Inmunología del Cáncer, Inmunoterapia . 65 (3): 327–339. doi :10.1007/s00262-016-1796-7. PMC 4779136 . Número de modelo: PMID26861670.
- ^ Brotherton J (2015). "Vacunas profilácticas contra el VPH: lecciones aprendidas a partir de 10 años de experiencia". Future Virology . 10 (8): 999–1009. doi :10.2217/fvl.15.60.
- ^ Frazer IH (mayo de 2014). "Desarrollo e implementación de vacunas profilácticas contra el virus del papiloma". Revista de inmunología . 192 (9): 4007–4011. doi : 10.4049/jimmunol.1490012 . PMID 24748633.
- ^ Ledford, Heidi (17 de agosto de 2020). «Lo que la respuesta inmunitaria al coronavirus dice sobre las perspectivas de una vacuna». Nature . 585 (7823): 20–21. Bibcode :2020Natur.585...20L. doi : 10.1038/d41586-020-02400-7 . PMID 32811981. S2CID 221180503.
- ^ *Centros para el Control y la Prevención de Enfermedades de los Estados Unidos (2011). Un marco de trabajo de los CDC para prevenir enfermedades infecciosas. Archivado el 29 de agosto de 2017 en Wayback Machine. Consultado el 11 de septiembre de 2012. "Las vacunas son nuestras herramientas más eficaces y económicas para la prevención de enfermedades, ya que evitan un sufrimiento incalculable y ahorran decenas de miles de vidas y miles de millones de dólares en costos de atención médica cada año".
- Asociación Médica Estadounidense (2000). Vacunas y enfermedades infecciosas: poner el riesgo en perspectiva. Archivado el 5 de febrero de 2015 en Wayback Machine. Consultado el 11 de septiembre de 2012. "Las vacunas son la herramienta de salud pública más eficaz jamás creada".
- Agencia de Salud Pública de Canadá. Enfermedades prevenibles mediante vacunación. Archivado el 13 de marzo de 2015 en Wayback Machine. Consultado el 11 de septiembre de 2012. "Las vacunas siguen siendo el método más eficaz y duradero para prevenir enfermedades infecciosas en todos los grupos de edad".
- Instituto Nacional de Alergias y Enfermedades Infecciosas de los Estados Unidos (NIAID). Agenda de investigación de biodefensa del NIAID para patógenos prioritarios de categorías B y C. Archivado el 4 de marzo de 2016 en Wayback Machine. Consultado el 11 de septiembre de 2012. "Las vacunas son el método más eficaz para proteger al público contra las enfermedades infecciosas".
- ^ Organización Mundial de la Salud, Plan de acción mundial sobre vacunas 2011-2020. Archivado el 14 de abril de 2014 en Wayback Machine . Ginebra, 2012.
- ^ Williams 2010, pág. 60.
- ^ Lombard M, Pastoret PP, Moulin AM (abril de 2007). "Una breve historia de las vacunas y la vacunación". Revue Scientifique et Technique . 26 (1): 29–48. doi : 10.20506/rst.26.1.1724 . PMID 17633292. S2CID 6688481.
- ^ Behbehani AM (diciembre de 1983). "La historia de la viruela: vida y muerte de una vieja enfermedad". Microbiological Reviews . 47 (4): 455–509. doi :10.1128/MMBR.47.4.455-509.1983. PMC 281588 . PMID 6319980.
- ^ Ferguson, Donna (28 de marzo de 2021). «Cómo el audaz experimento de Mary Wortley Montagu condujo a la vacuna contra la viruela, 75 años antes que Jenner». The Guardian . Archivado desde el original el 11 de julio de 2022. Consultado el 11 de julio de 2022 .
- ^ Baxby D (enero de 1999). "La investigación de Edward Jenner; un análisis del bicentenario". Vacuna . 17 (4): 301–307. doi :10.1016/s0264-410x(98)00207-2. PMID 9987167.
- ^ ab Pasteur L (1881). "Discurso sobre la teoría de los gérmenes". Lancet . 118 (3024): 271–272. doi :10.1016/s0140-6736(02)35739-8.
- ^ "Vacunación contra el sarampión CDC". 5 de febrero de 2018. Archivado desde el original el 19 de noviembre de 2019. Consultado el 13 de noviembre de 2018 .
- ^ Orenstein WA, Bernier RH, Dondero TJ, Hinman AR, Marks JS, Bart KJ, Sirotkin B (1985). "Evaluación de campo de la eficacia de la vacuna". Boletín de la Organización Mundial de la Salud . 63 (6): 1055–1068. PMC 2536484 . PMID 3879673.
- ^ "La ciencia es clara: las vacunas son seguras, eficaces y no causan autismo". The Hub . 11 de enero de 2017. Archivado desde el original el 28 de septiembre de 2017 . Consultado el 16 de abril de 2019 .
- ^ Ellenberg SS, Chen RT (1997). "La complicada tarea de monitorear la seguridad de las vacunas". Public Health Reports . 112 (1): 10–20, discusión 21. PMC 1381831 . PMID 9018282.
- ^ "Seguridad de las vacunas: los hechos". HealthyChildren.org . 10 de octubre de 2018. Archivado desde el original el 16 de abril de 2019 . Consultado el 16 de abril de 2019 .
- ^ Mak, Tak W.; Saunders, Mary E.; Jett, Bradley D. (2014). "Capítulo 1: Introducción a la respuesta inmunitaria". Introducción a la respuesta inmunitaria (2.ª ed.). Burlington, MA: Academic Cell. págs. 3–20. ISBN 978-0-12-385245-8Archivado del original el 18 de abril de 2022 . Consultado el 18 de abril de 2022 .
- ^ Clem, Angela S (2011). "Fundamentos de la inmunología de las vacunas". Revista de enfermedades infecciosas mundiales . 3 (1): 73–78. doi : 10.4103/0974-777X.77299 . ISSN 0974-777X. PMC 3068582 . PMID 21572612.
- ^ Grammatikos AP, Mantadakis E, Falagas ME (junio de 2009). "Metaanálisis sobre infecciones y vacunas pediátricas". Clínicas de enfermedades infecciosas de Norteamérica . 23 (2): 431–457. doi :10.1016/j.idc.2009.01.008. PMID 19393917.
- ^ abcd Wiedermann U, Garner-Spitzer E, Wagner A (2016). "Fallo primario de la vacuna en las vacunas de rutina: ¿por qué y qué hacer?". Vacunas e inmunoterapias humanas . 12 (1): 239–243. doi :10.1080/21645515.2015.1093263. ISSN 2164-554X. PMC 4962729. PMID 26836329 .
- ^ Justiz Vaillant, AA; Ramphul, K (enero de 2022). Trastorno por deficiencia de anticuerpos. Treasure Island, FL: StatPearls Publishing. PMID 29939682. Consultado el 18 de abril de 2022 .
- ^ Reda, Shereen M.; Cant, Andrew J. (mayo de 2015). "La importancia de la vacunación y el tratamiento con inmunoglobulina para pacientes con enfermedades de inmunodeficiencia primaria (IDP) - Semana Mundial de las IDP del 22 al 29 de abril de 2015: FORUM". Revista Europea de Inmunología . 45 (5): 1285–1286. doi :10.1002/eji.201570054. PMID 25952627. S2CID 1922332.
- ^ Jo, Eun-Kyeong (diciembre de 2019). "Interacción entre el huésped y el patógeno: defensa inmunitaria y más allá". Medicina experimental y molecular . 51 (12): 1–3. doi :10.1038/s12276-019-0281-8. ISSN 2092-6413. PMC 6906370. PMID 31827066 .
- ^ ab Janeway, Charles A Jr.; Travers, Paul; Walport, Mark; Shlomchik, Mark J. (2001). "La respuesta inmunitaria humoral". Inmunobiología: el sistema inmunitario en la salud y la enfermedad (5.ª ed.). Archivado desde el original el 2 de enero de 2021. Consultado el 18 de abril de 2022 .
- ^ Grubbs, Hailey; Kahwaji, Chadi I. (enero de 2022). Fisiología, inmunidad activa. Treasure Island, FL: StatPearls Publishing. PMID 29939682. Archivado desde el original el 12 de noviembre de 2021 . Consultado el 18 de abril de 2022 .
- ^ Gomes, M. Gabriela M.; White, Lisa J.; Medley, Graham F. (21 de junio de 2004). "Infección, reinfección y vacunación bajo protección inmunitaria subóptima: perspectivas epidemiológicas". Journal of Theoretical Biology . 228 (4): 539–549. Bibcode :2004JThBi.228..539G. doi :10.1016/j.jtbi.2004.02.015. hdl : 10400.7/53 . ISSN 0022-5193. PMID 15178201.
- ^ Bonanni, Paolo; Picazo, Juan José; Rémy, Vanessa (12 de agosto de 2015). "Los beneficios intangibles de la vacunación: ¿cuál es el verdadero valor económico de la vacunación?". Journal of Market Access & Health Policy . 3 : 10.3402/jmahp.v3.26964. doi :10.3402/jmahp.v3.26964. ISSN 2001-6689. PMC 4802696 . PMID 27123182.
- ^ Stanciu, Stefan G. (24 de agosto de 2016). Micro y nanotecnologías para la biotecnología. BoD – Libros a pedido. ISBN 978-953-51-2530-3Archivado del original el 14 de enero de 2023 . Consultado el 19 de abril de 2022 .
- ^ Frasca, Daniela; Diaz, Alain; Romero, Maria; Garcia, Denisse; Blomberg, Bonnie B. (6 de octubre de 2020). "Inmunosenescencia de células B". Revisión anual de biología celular y del desarrollo . 36 (1): 551–574. doi :10.1146/annurev-cellbio-011620-034148. ISSN 1081-0706. PMC 8060858. PMID 33021823 .
- ^ Neighmond P (7 de febrero de 2010). "Adaptación de las vacunas a nuestros sistemas inmunológicos envejecidos". Morning Edition . NPR. Archivado desde el original el 16 de diciembre de 2013 . Consultado el 9 de enero de 2014 .
- ^ Schlegel M, Osterwalder JJ, Galeazzi RL, Vernazza PL (agosto de 1999). "Eficacia comparativa de tres vacunas contra las paperas durante un brote de la enfermedad en el este de Suiza: estudio de cohorte". BMJ . 319 (7206): 352. doi :10.1136/bmj.319.7206.352. PMC 32261 . PMID 10435956.
- ^ Préziosi MP, Halloran ME (septiembre de 2003). "Efectos de la vacunación contra la tos ferina en la enfermedad: eficacia de la vacuna en la reducción de la gravedad clínica". Clinical Infectious Diseases . 37 (6): 772–779. doi : 10.1086/377270 . PMID 12955637.
- ^ Miller, E.; Beverley, PCL; Salisbury, DM (1 de julio de 2002). "Programas y políticas de vacunación". British Medical Bulletin . 62 (1): 201–211. doi : 10.1093/bmb/62.1.201 . ISSN 0007-1420. PMID 12176861.
- ^ Orenstein WA, Papania MJ, Wharton ME (mayo de 2004). "Eliminación del sarampión en los Estados Unidos". The Journal of Infectious Diseases . 189 (Supl 1): S1–3. doi : 10.1086/377693 . PMID 15106120.
- ^ abc "Sarampión – Estados Unidos, 1 de enero – 25 de abril de 2008". MMWR. Informe semanal de morbilidad y mortalidad . 57 (18): 494–498. Mayo de 2008. PMID 18463608. Archivado desde el original el 11 de octubre de 2017.
- ^ "OMS | Viruela". OMS . Organización Mundial de la Salud . Archivado desde el original el 22 de septiembre de 2007 . Consultado el 16 de abril de 2019 .
- ^ "La OMS certifica que la región del Sudeste Asiático está libre de polio". OMS. 27 de marzo de 2014. Archivado desde el original el 27 de marzo de 2014 . Consultado el 3 de noviembre de 2014 .
- ^ "Declaración tras la 28.ª reunión del Comité de Emergencia del RSI para la poliomielitis". Organización Mundial de la Salud . 21 de mayo de 2021. Archivado desde el original el 19 de abril de 2022 . Consultado el 19 de abril de 2022 .
- ^ Grassly, Nicholas C. (5 de agosto de 2013). "Las etapas finales de la erradicación mundial de la poliomielitis". Philosophical Transactions of the Royal Society B: Biological Sciences . 368 (1623): 20120140. doi :10.1098/rstb.2012.0140. ISSN 0962-8436. PMC 3720038 . PMID 23798688.
- ^ Ittefaq, Muhammad; Abwao, Mauryne; Rafique, Shanawer (3 de agosto de 2021). "Desinformación sobre la vacuna contra la poliomielitis en las redes sociales: punto de inflexión en la lucha contra la erradicación de la poliomielitis en Pakistán". Vacunas humanas e inmunoterapias . 17 (8): 2575–2577. doi :10.1080/21645515.2021.1894897. ISSN 2164-554X. PMC 8475597 . PMID 33705246.
- ^ "La desinformación perturba las campañas contra la polio". The Express Tribune . 24 de enero de 2022. Archivado desde el original el 10 de mayo de 2022 . Consultado el 19 de abril de 2022 .
- ^ "19 de julio de 2017 Las vacunas son la clave para acabar con los microbios resistentes a los medicamentos "La inmunización puede detener las infecciones resistentes antes de que se produzcan, afirman científicos de la industria y el mundo académico." Archivado desde el original el 22 de julio de 2017.
- ^ Sullivan P (13 de abril de 2005). «Muere Maurice R. Hilleman; creó vacunas». Washington Post . Archivado desde el original el 20 de octubre de 2012. Consultado el 9 de enero de 2014 .
- ^ Dudley, Matthew Z; Halsey, Neal A; Omer, Saad B; Orenstein, Walter A; O'Leary, Sean T; Limaye, Rupali J; Salmon, Daniel A (mayo de 2020). "El estado de la ciencia de la seguridad de las vacunas: revisiones sistemáticas de la evidencia". The Lancet Infectious Diseases . 20 (5): e80–e89. doi :10.1016/s1473-3099(20)30130-4. ISSN 1473-3099. PMID 32278359. S2CID 215751248.
- ^ abcd Maglione MA, Das L, Raaen L, Smith A, Chari R, Newberry S, Shanman R, Perry T, Goetz MB, Gidengil C (agosto de 2014). "Seguridad de las vacunas utilizadas para la inmunización de rutina de niños estadounidenses: una revisión sistemática". Pediatría . 134 (2): 325–337. doi : 10.1542/peds.2014-1079 . PMID 25086160. Archivado desde el original el 30 de enero de 2020 . Consultado el 1 de julio de 2019 .
- ^ abc «Posibles efectos secundarios de las vacunas». Centros para el Control y la Prevención de Enfermedades . 12 de julio de 2018. Archivado desde el original el 17 de marzo de 2017. Consultado el 24 de febrero de 2014 .
- ^ "Vacuna contra la gripe estacional: influenza estacional". CDC. 2 de octubre de 2018. Archivado desde el original el 1 de octubre de 2015. Consultado el 17 de septiembre de 2017 .
- ^ Looker C, Heath K (2011). "Compensación sin culpa después de eventos adversos atribuidos a la vacunación: una revisión de los programas internacionales". Boletín de la Organización Mundial de la Salud . 89 (5). Organización Mundial de la Salud: 371–378. doi :10.2471/BLT.10.081901. PMC 3089384 . PMID 21556305. Archivado desde el original el 11 de agosto de 2013.
- ^ "Tipos de vacunas". Instituto Nacional de Alergias y Enfermedades Infecciosas . 3 de abril de 2012. Archivado desde el original el 5 de septiembre de 2015. Consultado el 27 de enero de 2015 .
- ^ Sinha JK, Bhattacharya S. Un libro de texto de inmunología (Vista previa de Google Books) . Academic Publishers. pág. 318. ISBN 978-81-89781-09-5. Recuperado el 9 de enero de 2014 .
- ^ "Tipos de vacunas". Archivado desde el original el 29 de julio de 2017 . Consultado el 19 de octubre de 2017 .
- ^ abcd «Diferentes tipos de vacunas | Historia de las vacunas». www.historyofvaccines.org . Archivado desde el original el 26 de enero de 2019 . Consultado el 14 de junio de 2019 .
- ^ "Tipos de vacunas". coastalcarolinaresearch.com . Archivado desde el original el 3 de mayo de 2019 . Consultado el 3 de mayo de 2019 .
- ^ Philadelphia, The Children's Hospital of (18 de agosto de 2014). "Una mirada a cada vacuna: vacuna contra la hepatitis B". www.chop.edu . Archivado desde el original el 31 de mayo de 2019 . Consultado el 14 de junio de 2019 .
- ^ "Vacuna contra el VPH | Virus del papiloma humano | CDC". www.cdc.gov . 13 de mayo de 2019. Archivado desde el original el 18 de junio de 2019 . Consultado el 14 de junio de 2019 .
- ^ Williamson, ED; Eley, SM; Griffin, KF; Green, M.; Russell, P.; Leary, SE; Oyston, PC; Easterbrook, T.; Reddin, KM (diciembre de 1995). "Una nueva vacuna de subunidades mejorada para la peste: la base de la protección". Inmunología y microbiología médica de FEMS . 12 (3–4): 223–230. doi : 10.1111/j.1574-695X.1995.tb00196.x . ISSN 0928-8244. PMID 8745007.
- ^ "Vacunas conjugadas de proteínas polisacáridas". www.globalhealthprimer.emory.edu . Archivado desde el original el 23 de junio de 2019. Consultado el 14 de junio de 2019 .
- ^ abc Pollard AJ, Bijker EM (22 de diciembre de 2020). "Una guía sobre vacunología: desde los principios básicos hasta los nuevos avances". Nature Reviews Immunology . 21 (2): 83–100. doi : 10.1038/s41577-020-00479-7 . ISSN 1474-1741. PMC 7754704 . PMID 33353987.
- ^ Pol L, Stork M, Ley P (11 de noviembre de 2015). "Vesículas de membrana externa como plataforma tecnológica para vacunas". Revista de biotecnología . 10 (11): 1689–1706. doi :10.1002/biot.201400395. ISSN 1860-7314. PMC 4768646 . PMID 26912077.
- ^ Scott (abril de 2004). «Clasificación de vacunas» (PDF) . BioProcesses International : 14–23. Archivado (PDF) desde el original el 12 de diciembre de 2013. Consultado el 9 de enero de 2014 .
- ^ "Tipos de vacunas". Vaccines.org . Oficina de Enfermedades Infecciosas del Departamento de Salud y Servicios Humanos de los Estados Unidos . Archivado desde el original el 23 de mayo de 2019 . Consultado el 13 de marzo de 2021 .
- ^ "Comprensión y explicación de las vacunas contra la COVID-19 basadas en vectores virales". Centros para el Control y la Prevención de Enfermedades . Archivado desde el original el 2 de febrero de 2021. Consultado el 13 de marzo de 2021 .
- ^ Garde, Damian; Feuerstein, Adam (1 de noviembre de 2020). «Cómo la nanotecnología ayuda a que funcionen las vacunas de ARNm contra la COVID-19». STAT . Archivado desde el original el 1 de diciembre de 2020. Consultado el 21 de diciembre de 2020 .
- ^ CDC (11 de febrero de 2020). «COVID-19 y su salud». Centros para el Control y la Prevención de Enfermedades . Archivado desde el original el 3 de marzo de 2021. Consultado el 21 de diciembre de 2020 .
- ^ Banks, Marcus A. (16 de julio de 2020). «¿Qué son las vacunas de ARNm y podrían funcionar contra la COVID-19?». Revista Smithsonian . Archivado desde el original el 21 de diciembre de 2020. Consultado el 21 de diciembre de 2020 .
- ^ Branswell, Helen (19 de diciembre de 2020). «La FDA otorga autorización a la vacuna contra la Covid-19 de Moderna». STAT . Archivado desde el original el 21 de diciembre de 2020. Consultado el 21 de diciembre de 2020 .
- ^ Cuffari, Benedette (17 de marzo de 2021). "¿Qué es una vacuna de ADN?". Noticias-Medical.net . Consultado el 14 de enero de 2024 .
- ^ "Vacunas de ADN". Organización Mundial de la Salud . Consultado el 14 de enero de 2024 .
- ^ Kim W, Liau LM (enero de 2010). "Vacunas de células dendríticas para tumores cerebrales". Clínicas de neurocirugía de Norteamérica . 21 (1): 139–157. doi :10.1016/j.nec.2009.09.005. PMC 2810429. PMID 19944973 .
- ^ Anguille S, Smits EL, Lion E, van Tendeloo VF, Berneman ZN (junio de 2014). "Uso clínico de células dendríticas para la terapia del cáncer". The Lancet. Oncología . 15 (7): e257–267. doi :10.1016/S1470-2045(13)70585-0. PMID 24872109.
- ^ McKenzie, David (26 de mayo de 2018). «Miedo y fracaso: cómo el ébola desencadenó una revolución sanitaria mundial». CNN. Archivado desde el original el 26 de agosto de 2019. Consultado el 26 de mayo de 2018 .
- ^ Meri S, Jördens M, Jarva H (diciembre de 2008). "Inhibidores del complemento microbiano como vacunas". Vaccine . 26 (Supl. 8): I113–117. doi :10.1016/j.vaccine.2008.11.058. PMID 19388175.
- ^ Lowe (2008). "ADN plasmídico como vacunas profilácticas y terapéuticas para el cáncer y las enfermedades infecciosas". Plásmidos: investigación actual y tendencias futuras . Caister Academic Press. ISBN 978-1-904455-35-6Archivado desde el original el 11 de abril de 2008 . Consultado el 15 de abril de 2008 .
- ^ Chang, Lee-Jah; Blair, Wade (11 de diciembre de 2023). "Imitando a la naturaleza: partículas similares a virus y la próxima generación de vacunas". AstraZeneca .
- ^ Cambridge, Universidad de. "La vacuna 'Quartet Nanocage' es eficaz contra coronavirus que aún no han surgido". phys.org . Consultado el 6 de mayo de 2024 .
- ^ "Monovalente" en el Diccionario médico de Dorland
- ^ "Vacuna polivalente". Diccionario médico de Dorland . 7 de marzo de 2012. Archivado desde el original el 7 de marzo de 2012.
- ^ "Preguntas y respuestas sobre la vacuna antipoliomielítica oral monovalente tipo 1 (mOPV1) 'publicadas conjuntamente por la OMS y el UNICEF'". Pediatric Oncall . 2 (8). 3. ¿Qué ventajas tiene la mOPV1 sobre la vacuna antipoliomielítica oral trivalente (tOPV)?. 8 de enero de 2005. Archivado desde el original el 29 de febrero de 2012.
- ^ Gizurarson, Sveinbj??rn (1998). "Interacciones vacuna-vacuna clínicamente relevantes: una guía para profesionales". BioDrugs . 9 (6): 443–453. doi : 10.2165/00063030-199809060-00002 . PMID 18020577.
- ^ Sutter RW, Cochi SL, Melnick JL (1999). "Vacunas vivas atenuadas contra la poliomielitis". En Plotkin SA, Orenstein WA (eds.). Vacunas . Filadelfia: WB Saunders. págs. 364–408.
- ^ Kanesa-thasan N, Sun W, Kim-Ahn G, Van Albert S, Putnak JR, King A, Raengsakulsrach B, Christ-Schmidt H, Gilson K, Zahradnik JM, Vaughn DW, Innis BL, Saluzzo JF, Hoke CH (abril de 2001). "Seguridad e inmunogenicidad de las vacunas atenuadas contra el virus del dengue (Aventis Pasteur) en voluntarios humanos". Vaccine . 19 (23–24): 3179–3188. CiteSeerX 10.1.1.559.8311 . doi :10.1016/S0264-410X(01)00020-2. PMID 11312014.
- ^ Engler, Renata JM; Greenwood, John T.; Pittman, Phillip R.; Grabenstein, John D. (1 de agosto de 2006). "Inmunización para proteger a las Fuerzas Armadas de los Estados Unidos: herencia, práctica actual y perspectivas". Epidemiologic Reviews . 28 (1): 3–26. doi : 10.1093/epirev/mxj003 . ISSN 0193-936X. PMID 16763072.
- ^ Sox, Harold C.; Liverman, Catharyn T.; Fulco, Carolyn E.; War, Institute of Medicine (EE. UU.) Committee on Health Effects Associated with Exposures During the Gulf (2000). Vacunas. National Academies Press (EE. UU.). Archivado desde el original el 16 de noviembre de 2021. Consultado el 3 de mayo de 2019 .
- ^ "Instituto para la Seguridad de las Vacunas – Tabla sobre el timerosal". Archivado desde el original el 10 de diciembre de 2005.
- ^ Wharton, Melinda E.; Comité Asesor Nacional de Vacunas "Plan nacional de vacunación de EE. UU." Archivado el 4 de mayo de 2016 en Wayback Machine.
- ^ "Medidas de contaminantes atmosféricos no gaseosos > Metales". npl.co.uk . Laboratorio Nacional de Física. Archivado desde el original el 29 de septiembre de 2007 . Consultado el 28 de junio de 2020 .
- ^ "Thimerosal en vacunas". Centro de Evaluación e Investigación Biológica, Administración de Alimentos y Medicamentos de Estados Unidos. 6 de septiembre de 2007. Archivado desde el original el 6 de enero de 2013. Consultado el 1 de octubre de 2007 .
- ^ Bigham M, Copes R (2005). "Tiomersal en vacunas: equilibrio entre el riesgo de efectos adversos y el riesgo de enfermedades prevenibles mediante vacunas". Drug Safety . 28 (2): 89–101. doi :10.2165/00002018-200528020-00001. PMID 15691220. S2CID 11570020.
- ^ Offit PA (septiembre de 2007). "Thimerosal y vacunas: una advertencia". The New England Journal of Medicine . 357 (13): 1278–1279. doi : 10.1056/NEJMp078187 . PMID 17898096. S2CID 36318722.
- ^ "Otro estudio, este de 657.000 niños, descubre que la vacuna MMR no causa autismo". National Post . 5 de marzo de 2019 . Consultado el 13 de marzo de 2019 .
- ^ Hoffman J (5 de marzo de 2019). «Una vez más, con Big Data: la vacuna contra el sarampión no causa autismo». The New York Times . ISSN 0362-4331. Archivado desde el original el 12 de marzo de 2019. Consultado el 13 de marzo de 2019 .
- ^ CDC (12 de julio de 2018). «Ingredientes de las vacunas: hoja informativa». Archivado desde el original el 17 de diciembre de 2009. Consultado el 20 de diciembre de 2009 .
- ^ Los niveles de mercurio que aparecen en la tabla, a menos que se indique lo contrario, se han tomado de Mercury Levels in Commercial Fish and Shellfish (1990–2010) Archivado el 3 de mayo de 2015 en Wayback Machine . Administración de Alimentos y Medicamentos de los Estados Unidos. Consultado el 8 de enero de 2012.
- ^ ab Centros para el Control y la Prevención de Enfermedades (12 de noviembre de 2020), Nombres de las vacunas en EE. UU., archivado desde el original el 21 de agosto de 2021 , consultado el 21 de agosto de 2021 .
- ^ ab Centros para el Control y la Prevención de Enfermedades (7 de agosto de 2018), Vacunación contra el tétanos (trismo), archivado desde el original el 16 de mayo de 2016 , consultado el 21 de mayo de 2016 .
- ^ Centros para el Control y la Prevención de Enfermedades (2 de febrero de 2018), Acrónimos y abreviaturas de vacunas [Abreviaturas utilizadas en los registros de vacunación de EE. UU.], archivado desde el original el 2 de junio de 2017 , consultado el 22 de mayo de 2017 .
- ^ abcdefghi «Principios y consideraciones para añadir una vacuna a un programa nacional de inmunización» (PDF) . Organización Mundial de la Salud. 1 de abril de 2014. Archivado (PDF) del original el 29 de septiembre de 2020. Consultado el 17 de agosto de 2020 .
- ^ Bok, Karin; Sitar, Sandra; Graham, Barney S.; Mascola, John R. (agosto de 2021). "Desarrollo acelerado de la vacuna contra la COVID-19: hitos, lecciones y perspectivas". Inmunidad . 54 (8): 1636–1651. doi :10.1016/j.immuni.2021.07.017. PMC 8328682 . PMID 34348117.
- ^ abcd Wijnans, Leonoor; Voordouw, Bettie (11 de diciembre de 2015). "Una revisión de los cambios en la concesión de licencias de vacunas contra la gripe en Europa". Influenza y otros virus respiratorios . 10 (1): 2–8. doi :10.1111/irv.12351. ISSN 1750-2640. PMC 4687503 . PMID 26439108.
- ^ Offit, Paul A. (2020). «Fabricación de vacunas: licencias, recomendaciones y requisitos». Hospital Infantil de Filadelfia. Archivado desde el original el 8 de septiembre de 2020. Consultado el 20 de agosto de 2020 .
- ^ ab Toner E, Barnill A, Krubiner C, Bernstein J, Privor-Dumm L, Watson M, et al. (2020). Marco provisional para la asignación y distribución de vacunas contra la COVID-19 en los Estados Unidos (PDF) (Informe). Baltimore, MD: Centro de Seguridad Sanitaria de Johns Hopkins. Archivado (PDF) del original el 22 de agosto de 2020. Consultado el 24 de agosto de 2020 .
- ^ Dooling K, Marin M, Wallace M, McClung N, Chamberland M, Lee GM, et al. (diciembre de 2020). "Recomendación provisional actualizada del Comité Asesor sobre Prácticas de Inmunización para la asignación de la vacuna contra la COVID-19 – Estados Unidos, diciembre de 2020". MMWR. Informe semanal de morbilidad y mortalidad . 69 (5152): 1657–1660. doi : 10.15585/mmwr.mm695152e2 . PMC 9191902 . PMID 33382671.
- ^ abcde «Proceso de aprobación de productos vacunales». Administración de Alimentos y Medicamentos de Estados Unidos (FDA). 30 de enero de 2020. Archivado desde el original el 27 de septiembre de 2020. Consultado el 17 de agosto de 2020 .
- ^ "inicio". Cdsco.gov.in. 15 de abril de 2021. Archivado desde el original el 4 de enero de 2022. Consultado el 10 de enero de 2022 .
- ^ Steffen, Christoph A.; Henaff, Louise; et al. (8 de abril de 2021). "Toma de decisiones de vacunación basada en evidencia en los países: avances, desafíos y oportunidades". Vacuna . 39 (15). Elsevier: 2146–2152. doi : 10.1016/j.vaccine.2021.02.055 . PMID 33712350.
- ^ "Página de inicio de las recomendaciones de vacunas del ACIP". CDC. 15 de noviembre de 2013. Archivado desde el original el 31 de diciembre de 2013. Consultado el 10 de enero de 2014 .
- ^ "Tabla de estado de vacunación". Red Book Online . Academia Estadounidense de Pediatría. 26 de abril de 2011. Archivado desde el original el 27 de diciembre de 2013 . Consultado el 9 de enero de 2013 .
- ^ "Seguridad de la vacuna contra el VPH". Centros para el Control y la Prevención de Enfermedades (CDC). 20 de diciembre de 2013. Archivado desde el original el 10 de noviembre de 2009. Consultado el 10 de enero de 2014 .
- ^ "La vacuna contra el VPH está libre de riesgos". Opciones del NHS . 2 de octubre de 2009. Archivado desde el original el 10 de enero de 2014. Consultado el 10 de enero de 2014 .
- ^ «Zostavax EPAR». Agencia Europea de Medicamentos (EMA) . 29 de julio de 2021. Archivado desde el original el 5 de agosto de 2020. Consultado el 1 de septiembre de 2021 .
- ^ Dooling, Kathleen (13 de agosto de 2021). «Recomendación provisional actualizada del Comité Asesor sobre Prácticas de Inmunización para la asignación de la vacuna contra la COVID-19 – Estados Unidos, diciembre de 2020» (PDF) . CDC, Comité Asesor sobre Prácticas de Inmunización . 69 (5152): 1657–1660. PMC 9191902. PMID 33382671. Archivado (PDF) del original el 19 de agosto de 2021. Consultado el 17 de agosto de 2021 .
- ^ Hunziker, Patrick (24 de julio de 2021). «Vacunación contra la COVID-19 con dosis personalizadas en una ola de variantes del virus que son motivo de preocupación: intercambiar la eficacia individual por el beneficio social». Precision Nanomedicine . 4 (3): 805–820. doi : 10.33218/001c.26101 . ISSN 2639-9431. Archivado desde el original el 9 de octubre de 2021 . Consultado el 17 de agosto de 2021 .
- ^ Goodman JL (4 de mayo de 2005). "Declaración de Jesse L. Goodman, MD, MPH Director del Centro de Evaluación e Investigación de Productos Biológicos de la Administración de Alimentos y Medicamentos del Departamento de Salud y Servicios Humanos de los Estados Unidos sobre el suministro de vacunas contra la gripe en los Estados Unidos y los preparativos para la próxima temporada de gripe ante el Subcomité de Supervisión e Investigaciones del Comité de Energía y Comercio de la Cámara de Representantes de los Estados Unidos". Archivado desde el original el 21 de septiembre de 2008. Consultado el 15 de junio de 2008 .
- ^ Olesen OF, Lonnroth A, Mulligan B (enero de 2009). "Investigación sobre vacunas humanas en la Unión Europea". Vaccine . 27 (5): 640–645. doi :10.1016/j.vaccine.2008.11.064. PMC 7115654 . PMID 19059446.
- ^ Jit M, Newall AT, Beutels P (abril de 2013). "Cuestiones clave para estimar el impacto y la relación coste-eficacia de las estrategias de vacunación contra la gripe estacional". Vacunas humanas e inmunoterapias . 9 (4): 834–840. doi :10.4161/hv.23637. PMC 3903903 . PMID 23357859.
- ^ Newall AT, Reyes JF, Wood JG, McIntyre P, Menzies R, Beutels P (febrero de 2014). "Evaluaciones económicas de los programas de vacunación implementados: desafíos metodológicos clave en los análisis retrospectivos". Vaccine . 32 (7): 759–765. doi :10.1016/j.vaccine.2013.11.067. PMID 24295806.
- ^ Roser, Max; Vanderslott, Samantha (10 de mayo de 2013). «Vacunación». Our World in Data . Archivado desde el original el 1 de septiembre de 2020. Consultado el 3 de mayo de 2019 .
- ^ "Aumentar el acceso a las vacunas mediante la transferencia de tecnología y la producción local" (PDF) . Organización Mundial de la Salud. 2011. Archivado (PDF) del original el 23 de noviembre de 2015.
- ^ Christy Somos (7 de mayo de 2021). «Todo lo que necesita saber sobre la propuesta de patente de la vacuna contra la COVID-19 de la OMC». CTV News . Archivado desde el original el 23 de mayo de 2021. Consultado el 23 de mayo de 2021 .
- ^ ab Gomez, Phillip L.; Robinson, James M.; Rogalewicz, James (2008). "Capítulo 4: Fabricación de vacunas". En Plotkin, Stanley A.; Orenstein, Walter A.; Offit, Paul A. (eds.). Vacunas (5.ª ed.). Nueva York: Saunders Elsevier. págs. 45–58. ISBN 978-1-4377-2158-4Archivado del original el 18 de abril de 2023 . Consultado el 26 de marzo de 2021 .
- ^ abc Plotkin, Stanley; Robinson, James M.; Cunningham, Gerard; Iqbal, Robyn; Larsen, Shannon (24 de julio de 2017). "La complejidad y el coste de la fabricación de vacunas: una descripción general". Vacuna . 35 (33): 4064–4071. doi :10.1016/j.vaccine.2017.06.003. PMC 5518734 . PMID 28647170.
- ^ "Tres maneras de fabricar una vacuna" (infografía). Archivado desde el original el 23 de diciembre de 2015. Consultado el 5 de agosto de 2015., en Stein, Rob (24 de noviembre de 2009). «El sistema de vacunación sigue siendo anticuado». The Washington Post . Archivado desde el original el 19 de octubre de 2017.
- ^ ab Muzumdar JM, Cline RR (2009). "Oferta, demanda y política de vacunas: una introducción". Revista de la Asociación Estadounidense de Farmacéuticos . 49 (4): e87–99. doi :10.1331/JAPhA.2009.09007. PMC 7185851 . PMID 19589753.
- ^ ab «Componentes de una vacuna». Archivado desde el original el 13 de junio de 2017.
- ^ ab Bae K, Choi J, Jang Y, Ahn S, Hur B (abril de 2009). "Tecnologías innovadoras de producción de vacunas: evolución y valor de las tecnologías de producción de vacunas". Archivos de investigación farmacéutica . 32 (4): 465–480. doi : 10.1007/s12272-009-1400-1 . PMID: 19407962. S2CID : 9066150.
- ^ "Objetivos del grupo de trabajo sobre vacunas" (PDF) . assets.publishing.service.gov.uk . 6 de abril de 2020. Archivado (PDF) del original el 26 de julio de 2020 . Consultado el 26 de julio de 2020 .
- ^ Pagliusi, Sonia; Jarrett, Stephen; Hayman, Benoit; Kreysa, Ulrike; Prasad, Sai D.; Reers, Martin; Hong Thai, Pham; Wu, Ke; Zhang, Youn Tao; Baek, Yeong Ok; Kumar, Anand (julio de 2020). "Participación de los fabricantes emergentes en la investigación, el desarrollo y el suministro de vacunas contra la COVID-19". Vacuna . 38 (34): 5418–5423. doi :10.1016/j.vaccine.2020.06.022. PMC 7287474 . PMID 32600908.
- ^ Miller, Joe; Kuchler, Hannah (28 de abril de 2020). "Los fabricantes de medicamentos compiten por aumentar la capacidad de producción de vacunas". www.ft.com . Archivado desde el original el 10 de diciembre de 2022 . Consultado el 26 de julio de 2020 .
- ^ abcdef Plotkin, Stanley A.; Orenstein, Walter A.; Offit, Paul A.; Edwards, Kathryn M. (2017). Vacunas . Elsevier. ISBN 978-0-323-39301-0.
- ^ Morein B, Hu KF, Abusugra I (junio de 2004). "Estado actual y posible aplicación de los ISCOM en medicina veterinaria". Advanced Drug Delivery Reviews . 56 (10): 1367–1382. doi :10.1016/j.addr.2004.02.004. PMID 15191787.
- ^ Medicina americana. Compañía editorial American-Medicine. 1926.
- ^ Instituto Sudafricano de Investigaciones Médicas (1929). Informe anual [Jaarverslag]. Instituto Sudafricano de Investigaciones Médicas - Suid-Afrikaanse Instituut vir Mediese Navorsing.
- ^ Khan FA (20 de septiembre de 2011). Fundamentos de biotecnología. CRC Press. p. 270. ISBN 978-1-4398-2009-4.
- ^ Giudice EL, Campbell JD (abril de 2006). "Administración de vacunas sin agujas". Advanced Drug Delivery Reviews . 58 (1): 68–89. doi :10.1016/j.addr.2005.12.003. PMID 16564111.
- ^ La OMS probará el sistema de administración sin agujas Nanopatch | ABC News , 16 de septiembre de 2014 | "La vacuna antipoliomielítica sin agujas es un 'factor decisivo'". ABC News . 16 de septiembre de 2014. Archivado desde el original el 2 de abril de 2015 . Consultado el 15 de septiembre de 2015 .
- ^ "Científicos australianos desarrollan una vacuna 'sin agujas'". The Sydney Morning Herald . 18 de agosto de 2013. Archivado desde el original el 25 de septiembre de 2015.
- ^ "Vaxxas recauda 25 millones de dólares para llevar Nanopatch de Brisbane a nivel mundial". Business Review Weekly . 10 de febrero de 2015. Archivado desde el original el 16 de marzo de 2015 . Consultado el 5 de marzo de 2015 .
- ^ "Científicos australianos desarrollan una vacuna 'sin agujas'". The Hindu . Chennai, India. 28 de septiembre de 2011. Archivado desde el original el 1 de enero de 2014.
- ^ "Sistema de administración de vacunas mediante nanoparches sin aguja". News Medical. 3 de agosto de 2011. Archivado desde el original el 11 de mayo de 2012.
- ^ Patel JR, Heldens JG (marzo de 2009). "Inmunoprofilaxis contra enfermedades virales importantes de caballos, animales de granja y aves". Vaccine . 27 (12): 1797–1810. doi :10.1016/j.vaccine.2008.12.063. PMC 7130586 . PMID 19402200.
- ^ ab Berkelman RL (agosto de 2003). "Enfermedades humanas asociadas con el uso de vacunas veterinarias". Enfermedades infecciosas clínicas . 37 (3): 407–414. doi : 10.1086/375595 . PMID: 12884166.
- ^ van Oirschot JT, Rziha HJ, Moonen PJ, Pol JM, van Zaane D (junio de 1986). "Diferenciación de anticuerpos séricos de cerdos vacunados o infectados con el virus de la enfermedad de Aujeszky mediante un inmunoensayo enzimático competitivo". The Journal of General Virology . 67 (Pt 6) (6): 1179–1182. doi : 10.1099/0022-1317-67-6-1179 . PMID 3011974.
- ^ ab van Oirschot JT (agosto de 1999). "Vacunas Diva que reducen la transmisión del virus". Revista de biotecnología . 73 (2–3): 195–205. doi :10.1016/S0168-1656(99)00121-2. PMID 10486928.
- ^ van Oirschot JT, Gielkens AL, Moormann RJ, Berns AJ (junio de 1990). "Vacunas marcadoras, ensayos de anticuerpos específicos de proteínas virales y el control de la enfermedad de Aujeszky". Microbiología veterinaria . 23 (1–4): 85–101. doi :10.1016/0378-1135(90)90139-M. PMID 2169682.
- ^ Kaashoek MJ, Moerman A, Madić J, Rijsewijk FA, Quak J, Gielkens AL, van Oirschot JT (abril de 1994). "Una cepa convencionalmente atenuada negativa para la glicoproteína E del herpesvirus bovino tipo 1 es una vacuna eficaz y segura". Vacuna . 12 (5): 439–444. doi :10.1016/0264-410X(94)90122-8. PMID 8023552.
- ^ Hulst MM, Westra DF, Wensvoort G, Moormann RJ (septiembre de 1993). "La glicoproteína E1 del virus del cólera porcino expresada en células de insectos protege a los cerdos del cólera porcino". Revista de Virología . 67 (9): 5435–5442. doi :10.1128/JVI.67.9.5435-5442.1993. PMC 237945 . PMID 8350404.
- ^ Capua I, Terregino C, Cattoli G, Mutinelli F, Rodriguez JF (febrero de 2003). "Desarrollo de una estrategia DIVA (Diferenciación de animales infectados de vacunados) utilizando una vacuna que contiene una neuraminidasa heteróloga para el control de la influenza aviar". Patología aviar . 32 (1): 47–55. doi : 10.1080/0307945021000070714 . PMID 12745380. S2CID 22827454.
- ^ Maas A, Meens J, Baltes N, Hennig-Pauka I, Gerlach GF (noviembre de 2006). "Desarrollo de una vacuna de subunidad DIVA contra la infección por Actinobacillus pleuropneumoniae". Vaccine . 24 (49–50): 7226–7237. doi :10.1016/j.vaccine.2006.06.047. PMID 17027123.
- ^ Leyman B, Boyen F, Van Parys A, Verbrugghe E, Haesebrouck F, Pasmans F (mayo de 2011). "Mutaciones de LPS de Salmonella Typhimurium para su uso en vacunas que permitan la diferenciación de cerdos infectados y vacunados". Vaccine . 29 (20): 3679–3685. doi :10.1016/j.vaccine.2011.03.004. hdl : 1854/LU-1201519 . PMID 21419163. Archivado desde el original el 28 de octubre de 2017.
- ^ Needham, Joseph (2000). Ciencia y civilización en China: Volumen 6, Biología y tecnología biológica, Parte 6, Medicina . Cambridge University Press. pág. 154. ISBN 978-0-521-63262-1.
- ^ ab Williams G (2010). El ángel de la muerte . Basingstoke: Palgrave Macmillan. ISBN 978-0-230-27471-6.
- ^ Silverstein, Arthur M. (2009). Una historia de la inmunología (2.ª ed.). Academic Press. pág. 293. ISBN 978-0-08-091946-1.
- ↑ Voltaire (1742). «Carta XI». Cartas sobre los ingleses . Archivado desde el original el 16 de octubre de 2018. Consultado el 26 de julio de 2023 .
- ^ Fenner, F.; Henderson, DA; Arita, I.; Jezek, Z.; Ladnyi, ID (1988). La viruela y su erradicación . Ginebra: Organización Mundial de la Salud. ISBN 92-4-156110-6.
- ^ ab Baxby, Derrick (1984). "Una muerte por viruela inoculada en la familia real inglesa". Med Hist . 28 (3): 303–307. doi :10.1017/s0025727300035961. PMC 1139449 . PMID 6390027.
- ^ abc Stern AM, Markel H (2005). "La historia de las vacunas y la inmunización: patrones familiares, nuevos desafíos". Health Affairs . 24 (3): 611–621. doi : 10.1377/hlthaff.24.3.611 . PMID 15886151.
- ^ Dunn PM (enero de 1996). "El Dr. Edward Jenner (1749-1823) de Berkeley y la vacunación contra la viruela" (PDF) . Archivos de enfermedades de la infancia: edición fetal y neonatal . 74 (1): F77–78. doi :10.1136/fn.74.1.F77. PMC 2528332. PMID 8653442. Archivado desde el original (PDF) el 8 de julio de 2011.
- ^ Una exposición cuenta la historia de los niños españoles utilizados como frigoríficos de vacunas en 1803 Archivado el 30 de agosto de 2022 en Wayback Machine The Guardian, 2021
- ^ Van Sant JE (2008). "Los vacunadores: viruela, conocimiento médico y la 'apertura' de Japón". J Hist Med Allied Sci . 63 (2): 276–279. doi :10.1093/jhmas/jrn014.
- ^ Didgeon JA (mayo de 1963). "Desarrollo de la vacuna contra la viruela en Inglaterra en los siglos XVIII y XIX". British Medical Journal . 1 (5342): 1367–1372. doi :10.1136/bmj.1.5342.1367. PMC 2124036 . PMID 20789814.
- ^ Louten, Jennifer (2016). Virología humana esencial . Prensa académica. págs. 134-135. ISBN 978-0-12-801171-3.
- ^ Baarda BI, Sikora AE (2015). "Proteómica de Neisseria gonorrhoeae: la búsqueda del tesoro en busca de contramedidas contra una antigua enfermedad". Fronteras en Microbiología . 6 : 1190. doi : 10.3389/fmicb.2015.01190 . PMC 4620152 . PMID 26579097;
- ^ abc Alarcon JB, Waine GW, McManus DP (1999). "Vacunas de ADN: tecnología y aplicación como agentes antiparasitarios y antimicrobianos". Avances en parasitología , volumen 42. Vol. 42. págs. 343–410. doi :10.1016/S0065-308X(08)60152-9. ISBN 978-0-12-031742-4. PMID 10050276.
- ^ Robinson HL, Pertmer TM (2000). Vacunas de ADN para infecciones virales: estudios básicos y aplicaciones . Avances en la investigación de virus. Vol. 55. págs. 1–74. doi :10.1016/S0065-3527(00)55001-5. ISBN 978-0-12-039855-3. Número de identificación personal 11050940.
- ^ Naftalis, Kramer Levin; Royzman, Frankel LLP-Irena; Pineda, ré (30 de noviembre de 2020). «Las vacunas de tercera generación ocupan un lugar central en la batalla contra la COVID-19 | Lexology». www.lexology.com . Archivado desde el original el 30 de enero de 2021 . Consultado el 24 de enero de 2021 .
- ^ Regalado, Antonio. «El gobierno de Estados Unidos ha comenzado a probar su primera vacuna contra el Zika en humanos». Archivado desde el original el 21 de agosto de 2016. Consultado el 6 de agosto de 2016 .
- ^ Chen Y, Wang S, Lu S (febrero de 2014). "Inmunización con ADN para el desarrollo de una vacuna contra el VIH". Vacunas . 2 (1): 138–159. doi : 10.3390/vaccines2010138 . PMC 4494200 . PMID 26344472.
- ^ "Katalin Karikó y Drew Weissman reciben el premio Horwitz por su investigación pionera sobre las vacunas contra la COVID-19". Centro Médico Irving de la Universidad de Columbia . 12 de agosto de 2021. Archivado desde el original el 16 de agosto de 2021. Consultado el 7 de septiembre de 2021 .
- ^ Staff (28 de marzo de 2013). «Se crea una vacuna más segura sin virus». The Japan Times . Agence France-Presse – Jiji Press. Archivado desde el original el 30 de marzo de 2013. Consultado el 28 de marzo de 2013 .
- ^ Spohn G, Bachmann MF (febrero de 2008). "Explotación de las propiedades virales para el diseño racional de vacunas modernas". Expert Review of Vaccines . 7 (1): 43–54. doi :10.1586/14760584.7.1.43. PMID 18251693. S2CID 40130001.
- ^ Samuelsson O, Herlitz H (marzo de 2008). "Vacunación contra la hipertensión arterial: una nueva estrategia". Lancet . 371 (9615): 788–789. doi :10.1016/S0140-6736(08)60355-4. PMID 18328909. S2CID 38323966.
- ^ Polonia GA, Jacobson RM, Ovsyannikova IG (mayo de 2009). "Tendencias que afectan el futuro del desarrollo y la distribución de vacunas: el papel de la demografía, la ciencia regulatoria, el movimiento antivacunas y la vaccinómica". Vaccine . 27 (25–26): 3240–3244. doi :10.1016/j.vaccine.2009.01.069. PMC 2693340 . PMID 19200833.
- ^ Sala F, Manuela Rigano M, Barbante A, Basso B, Walmsley AM, Castiglione S (enero de 2003). "Producción de antígenos vacunales en plantas transgénicas: estrategias, construcciones genéticas y perspectivas". Vaccine . 21 (7–8): 803–808. doi :10.1016/s0264-410x(02)00603-5. PMID 12531364.
- ^ Kumar GB, Ganapathi TR, Revathi CJ, Srinivas L, Bapat VA (octubre de 2005). "Expresión del antígeno de superficie de la hepatitis B en plantas de banano transgénicas". Planta . 222 (3): 484–493. Código Bibliográfico :2005Plant.222..484K. doi :10.1007/s00425-005-1556-y. PMID 15918027. S2CID 23987319.
- ^ ab Leonhardt, David (11 de marzo de 2024). «El cuarto aniversario de la pandemia de Covid». The New York Times . Archivado desde el original el 11 de marzo de 2024."Los datos excluyen a Alaska. Fuentes: CDC Wonder; Edison Research. (Gráfico) Por The New York Times. La fuente del gráfico se atribuye a Ashley Wu.
- ^ The Lancet Child & Adolescent Health (2019). "La indecisión ante las vacunas: una generación en riesgo". The Lancet . 3 (5): 281. doi : 10.1016/S2352-4642(19)30092-6 . PMID 30981382. S2CID 115201206.
- ^ Smith, MJ (noviembre de 2015). "Promoción de la confianza en las vacunas". Clínicas de enfermedades infecciosas de Norteamérica (revisión). 29 (4): 759–69. doi :10.1016/j.idc.2015.07.004. PMID 26337737.
- ^ Larson, HJ; Jarrett, C; Eckersberger, E; Smith, DM; Paterson, P (abril de 2014). "Comprender la reticencia a las vacunas y la vacunación desde una perspectiva global: una revisión sistemática de la literatura publicada, 2007-2012". Vaccine . 32 (19): 2150–59. doi :10.1016/j.vaccine.2014.01.081. PMID 24598724.
- ^ Cataldi, Jessica; O'Leary, Sean (2021). "Reticencia de los padres a la vacuna: alcance, causas y posibles respuestas". Current Opinion in Infectious Diseases . 34 (5): 519–526. doi :10.1097/QCO.0000000000000774. PMID 34524202. S2CID 237437018. Archivado desde el original el 24 de diciembre de 2023 . Consultado el 24 de junio de 2022 .
- ^ "Comunicación de mensajes basados en la ciencia sobre las vacunas". Boletín de la Organización Mundial de la Salud . 95 (10): 670–71. Octubre de 2017. doi :10.2471/BLT.17.021017. PMC 5689193 . PMID 29147039.
- ^ "¿Por qué algunas personas se oponen a la vacunación?". Vox . Archivado desde el original el 21 de septiembre de 2019. Consultado el 26 de noviembre de 2018 .
- ^ Ceccarelli L. «Defendiendo la ciencia: cómo el arte de la retórica puede ayudar». The Conversation . Archivado desde el original el 5 de noviembre de 2019. Consultado el 26 de noviembre de 2018 .
- ^ Departamento de Salud y Servicios Humanos de Estados Unidos. «Vaccines.gov». Vaccines.gov . Archivado desde el original el 13 de marzo de 2019. Consultado el 5 de agosto de 2018 .
- ^ "Preguntas frecuentes (FAQ)". Boston Children's Hospital . Archivado desde el original el 17 de octubre de 2013. Consultado el 11 de febrero de 2014 .
- ^ Phadke VK, Bednarczyk RA, Salmon DA, Omer SB (marzo de 2016). "Asociación entre el rechazo a la vacuna y las enfermedades prevenibles mediante vacunación en los Estados Unidos: una revisión del sarampión y la tos ferina". JAMA . 315 (11): 1149–58. doi :10.1001/jama.2016.1353. PMC 5007135 . PMID 26978210.
- ^ Wolfe R, Sharp L (2002). "Anti-vaccinationists past and present" (Antivacunacionistas pasados y presentes). BMJ . 325 (7361): 430–2. doi :10.1136/bmj.325.7361.430. PMC 1123944 . PMID 12193361. Archivado desde el original el 25 de agosto de 2006 . Consultado el 14 de enero de 2008 .
- ^ Poland GA, Jacobson RM (enero de 2011). "La antigua lucha contra los antivacunacionistas". The New England Journal of Medicine . 364 (2): 97–99. doi :10.1056/NEJMp1010594. PMID 21226573. S2CID 39229852.
- ^ Wallace A (19 de octubre de 2009). "Una epidemia de miedo: cómo los padres en pánico que se saltan las vacunas nos ponen en peligro a todos". Wired . Archivado desde el original el 25 de diciembre de 2013. Consultado el 21 de octubre de 2009 .
- ^ Poland GA, Jacobson RM (marzo de 2001). "Entender a quienes no entienden: una breve revisión del movimiento antivacunas". Vaccine . 19 (17–19): 2440–45. doi :10.1016/S0264-410X(00)00469-2. PMID 11257375. S2CID 1978650.
- ^ "Diez amenazas para la salud mundial en 2019". Who.int . Archivado desde el original el 27 de junio de 2019 . Consultado el 9 de diciembre de 2020 .
- ^ PM, Aristos Georgiou (15 de enero de 2019). «La OMS ha incluido al movimiento antivacunas como una de las 10 principales amenazas para la salud en 2019». Archivado desde el original el 22 de noviembre de 2019. Consultado el 16 de enero de 2019 .
Lectura adicional
- Hall E, Wodi AP, Hamborsky J, Morelli V, Schillie S, eds. (2021). Epidemiología y prevención de enfermedades prevenibles mediante vacunación (14.ª ed.). Washington DC: Centros para el Control y la Prevención de Enfermedades (CDC) de EE. UU.
Enlaces externos
| Videos externos | |
|---|---|
 Producción y caracterización de vacunas y adyuvantes modernos, novedades en ingeniería genética y biotecnología Producción y caracterización de vacunas y adyuvantes modernos, novedades en ingeniería genética y biotecnología |
- OMS Enfermedades prevenibles mediante vacunación e inmunización
- Documentos de posición de la Organización Mundial de la Salud sobre las vacunas
- La historia de las vacunas, del Colegio de Médicos de Filadelfia
- Este sitio web fue destacado por Genetic Engineering & Biotechnology News en su sección "Lo mejor de la Web" en enero de 2015. Véase: "La historia de las vacunas". Lo mejor de la Web. Genetic Engineering & Biotechnology News . Vol. 35, núm. 2. 15 de enero de 2015. pág. 38.




