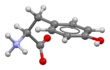
Tirosina
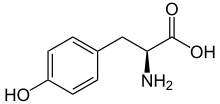 Fórmula esquelética de la L -tirosina | |||
 L -tirosina a pH fisiológico | |||
| |||
| Nombres | |||
|---|---|---|---|
| Nombre IUPAC ( S )-Tirosina | |||
| Otros nombres Ácido L -2-amino-3-(4-hidroxifenil)propanoico | |||
| Identificadores | |||
Modelo 3D ( JSmol ) |
| ||
| EBICh | |||
| Química biológica | |||
| Araña química | |||
| Banco de medicamentos | |||
| Tarjeta informativa de la ECHA | 100.000.419 | ||
| |||
| BARRIL |
| ||
Identificador de centro de PubChem |
| ||
| UNIVERSIDAD | |||
Panel de control CompTox ( EPA ) |
| ||
| |||
| |||
| Propiedades | |||
| C9H11NO3 | |||
| Masa molar | 181,191 g·mol −1 | ||
| Apariencia | sólido blanco | ||
| .0453 g/100 ml | |||
| -105,3·10 −6 cm3 / mol | |||
| Peligros | |||
| NFPA 704 (rombo cortafuegos) | |||
| Página de datos complementarios | |||
| Tirosina (página de datos) | |||
Salvo que se indique lo contrario, los datos se proporcionan para los materiales en su estado estándar (a 25 °C [77 °F], 100 kPa). | |||
La L -tirosina o tirosina (símbolo Tyr o Y ) [2] o 4-hidroxifenilalanina es uno de los 20 aminoácidos estándar que utilizan las células para sintetizar proteínas . Es un aminoácido condicionalmente esencial con un grupo lateral polar . La palabra "tirosina" proviene del griego tyrós , que significa queso , ya que fue descubierta por primera vez en 1846 por el químico alemán Justus von Liebig en la proteína caseína del queso. [3] [4] Se llama tirosilo cuando se hace referencia a un grupo funcional o cadena lateral. Si bien la tirosina generalmente se clasifica como unaminoácido hidrófobo , es más hidrófilo que la fenilalanina . [5] Está codificada por los codones UAC y UAU en el ARN mensajero .
El símbolo de una letra Y se asignó a la tirosina por ser la letra más cercana alfabéticamente de las disponibles. Nótese que T se asignó a la treonina estructuralmente más simple, U se evitó por su similitud con V para valina, W se asignó al triptófano, mientras que X se reservó para aminoácidos indeterminados o atípicos. [6] También se propuso el símbolo mnemotécnico t Y rosina. [7]
Funciones
Además de ser un aminoácido proteinogénico , la tirosina tiene un papel especial en virtud de la funcionalidad fenólica . Su grupo hidroxilo es capaz de formar el enlace éster , en particular con el fosfato. Los grupos fosfato se transfieren a los residuos de tirosina por medio de las proteincinasas . Esta es una de las modificaciones postraduccionales . La tirosina fosforilada se produce en proteínas que forman parte de los procesos de transducción de señales .
Una funcionalidad similar se presenta también en la serina y la treonina , cuyas cadenas laterales tienen un grupo hidroxi, pero son alcoholes . La fosforilación de las fracciones de estos tres aminoácidos (incluida la tirosina) crea una carga negativa en sus extremos, que es mayor que la carga negativa de los únicos ácidos aspártico y glutámico con carga negativa . Las proteínas fosforiladas mantienen estas mismas propiedades, que son útiles para interacciones proteína-proteína más fiables, por medio de la fosfotirosina, la fosfoserina y la fosfotreonina. [8]
Los sitios de unión de una fosfoproteína de señalización pueden ser diversos en su estructura química. [9]
La fosforilación del grupo hidroxilo puede cambiar la actividad de la proteína objetivo o puede formar parte de una cascada de señalización a través de la unión del dominio SH2 . [10]
Un residuo de tirosina también juega un papel importante en la fotosíntesis . En los cloroplastos ( fotosistema II ), actúa como donador de electrones en la reducción de la clorofila oxidada . En este proceso, pierde el átomo de hidrógeno de su grupo OH fenólico. Este radical es posteriormente reducido en el fotosistema II por los cuatro grupos centrales de manganeso . [11]
Requerimientos dietéticos y fuentes
La ingesta dietética de referencia para la tirosina se estima generalmente junto con la fenilalanina . Varía según el método de estimación, sin embargo, se considera que la proporción ideal de estos dos aminoácidos es 60:40 (fenilalanina:tirosina) ya que el cuerpo humano tiene dicha composición. [12] La tirosina, que también se puede sintetizar en el cuerpo a partir de la fenilalanina, se encuentra en muchos productos alimenticios ricos en proteínas , como la carne , el pescado , el queso , el requesón , la leche , el yogur , los cacahuetes , las almendras , las semillas de calabaza , las semillas de sésamo , la proteína de soja y las habas . [13] [14] Por ejemplo, la clara de un huevo tiene unos 250 mg por huevo, [15] mientras que la carne de ternera, cordero, cerdo, atún, salmón, pollo y pavo contienen unos 500-1000 mg por porción de 3 onzas (85 g). [15] [16]
Biosíntesis

En las plantas y la mayoría de los microorganismos, la tirosina se produce a través del prefenato , un intermediario en la vía del shikimato . El prefenato se descarboxila oxidativamente con retención del grupo hidroxilo para dar p -hidroxifenilpiruvato, que se transamina utilizando glutamato como fuente de nitrógeno para dar tirosina y α-cetoglutarato .
Los mamíferos sintetizan tirosina a partir del aminoácido esencial fenilalanina (Phe), que se obtiene de los alimentos. La conversión de Phe en Tyr es catalizada por la enzima fenilalanina hidroxilasa , una monooxigenasa. Esta enzima cataliza la reacción provocando la adición de un grupo hidroxilo al extremo del anillo aromático de 6 carbonos de la fenilalanina , de modo que se convierte en tirosina.
Metabolismo

Fosforilación y sulfatación
Algunos de los residuos de tirosina pueden ser marcados (en el grupo hidroxilo) con un grupo fosfato ( fosforilados ) por las proteínas quinasas . En su forma fosforilada, la tirosina se llama fosfotirosina . La fosforilación de la tirosina se considera uno de los pasos clave en la transducción de señales y la regulación de la actividad enzimática. La fosfotirosina se puede detectar a través de anticuerpos específicos . Los residuos de tirosina también pueden modificarse mediante la adición de un grupo sulfato, un proceso conocido como sulfatación de tirosina . [17] La sulfatación de tirosina es catalizada por la tirosilproteína sulfotransferasa (TPST). Al igual que los anticuerpos de fosfotirosina mencionados anteriormente, recientemente se han descrito anticuerpos que detectan específicamente la sulfotirosina. [18]
Precursor de neurotransmisores y hormonas.
En las células dopaminérgicas del cerebro , la tirosina se convierte en L-DOPA por acción de la enzima tirosina hidroxilasa (TH). La TH es la enzima limitante de la velocidad de síntesis del neurotransmisor dopamina . La dopamina puede convertirse luego en otras catecolaminas , como la noradrenalina y la epinefrina .
Las hormonas tiroideas triyodotironina (T 3 ) y tiroxina (T 4 ) en el coloide de la tiroides también se derivan de la tirosina.
Precursor de otros compuestos
Se ha demostrado que el látex de Papaver somniferum , la adormidera, convierte la tirosina en el alcaloide morfina y se ha establecido la vía biosintética de tirosina a morfina utilizando tirosina marcada con radiocarbono 14 para rastrear la ruta sintética in vivo. [22] La tirosina amoniaco liasa (TAL) es una enzima en la vía de biosíntesis de fenoles naturales. Transforma la L-tirosina en ácido p-cumárico . La tirosina también es el precursor del pigmento melanina . La tirosina (o su precursora fenilalanina) es necesaria para sintetizar la estructura de benzoquinona que forma parte de la coenzima Q10 . [23] [24]
Degradación

[ cita requerida ]
La descomposición de la L-tirosina (sin. para -hidroxifenilalanina) comienza con una transaminación dependiente de α-cetoglutarato a través de la tirosina transaminasa hasta para -hidroxifenilpiruvato . La descripción posicional para , abreviada p , significa que el grupo hidroxilo y la cadena lateral en el anillo de fenilo están uno frente al otro (ver la ilustración a continuación).
El siguiente paso de oxidación es catalizado por la p -hidroxifenilpiruvato dioxigenasa y la separación del CO2 homogentisato ( 2,5-dihidroxifenil-1-acetato). [25] Para separar el anillo aromático del homogentisato, se requiere otra dioxigenasa, la homogentisato 1,2-dioxigenasa . De este modo, mediante la incorporación de otra molécula de O2 , se crea maleilacetoacetato .
El fumarilacetoacetato es creado por la maleilacetoacetato cis - trans -isomerasa a través de la rotación del grupo carboxilo creado a partir del grupo hidroxilo por oxidación. Esta cis-trans -isomerasa contiene glutatión como coenzima . El fumarilacetoacetato es finalmente dividido por la enzima fumarilacetoacetato hidrolasa a través de la adición de una molécula de agua.
De esta manera se liberan fumarato (también un metabolito del ciclo del ácido cítrico) y acetoacetato (3-cetobutiroato). El acetoacetato es un cuerpo cetónico , que se activa con succinil-CoA, y luego se puede convertir en acetil-CoA , que a su vez puede oxidarse mediante el ciclo del ácido cítrico o usarse para la síntesis de ácidos grasos .
El ácido florético también es un metabolito urinario de la tirosina en ratas. [26]
Orto- y meta-tirosina

Se conocen tres isómeros estructurales de la L-tirosina. Además del aminoácido común L-tirosina, que es el isómero para ( para -tyr, p -tyr o 4-hidroxifenilalanina), hay dos regioisómeros adicionales, a saber, meta -tirosina (también conocida como 3-hidroxifenilalanina , L- m -tirosina y m -tyr) y orto -tirosina ( o -tyr o 2-hidroxifenilalanina), que se encuentran en la naturaleza. Los isómeros m -tyr y o -tyr, que son raros, surgen a través de la hidroxilación no enzimática de radicales libres de fenilalanina en condiciones de estrés oxidativo . [27] [28]
Uso médico
La tirosina es un precursor de los neurotransmisores y aumenta los niveles plasmáticos de neurotransmisores (en particular la dopamina y la noradrenalina), [29] pero tiene poco o ningún efecto sobre el estado de ánimo en sujetos normales. [30] [31] [32]
Una revisión sistemática de 2015 encontró que "la carga de tirosina contrarresta agudamente las disminuciones en la memoria de trabajo y el procesamiento de la información que son inducidas por condiciones situacionales exigentes, como el clima extremo o la carga cognitiva " y, por lo tanto, "la tirosina puede beneficiar a individuos sanos expuestos a condiciones situacionales exigentes". [33]
Síntesis industrial
La L-tirosina se utiliza en productos farmacéuticos , suplementos dietéticos y aditivos alimentarios . Anteriormente se utilizaban dos métodos para fabricar L-tirosina. El primero implica la extracción del aminoácido deseado de hidrolizados de proteínas mediante un enfoque químico. El segundo utiliza la síntesis enzimática a partir de fenólicos, piruvato y amoníaco mediante el uso de tirosina fenol-liasa . [34] Los avances en ingeniería genética y el advenimiento de la fermentación industrial han cambiado la síntesis de L-tirosina al uso de cepas modificadas de E. coli . [35] [34]
Véase también
- Albinismo
- Alcaptonuria
- Betalaína
- Derivados yodados de tirosina
- Reacción de Pauly
- Tiramina
- Sulfatación de tirosina
- Tirosinemia
Referencias
- ^ ab Frey MN, Koetzle TF, Lehmann MS, Hamilton WC (1973). "Determinación precisa de la estructura de componentes de proteínas y ácidos nucleicos mediante difracción de neutrones. X. Una comparación entre las estructuras cristalinas y moleculares de L-tirosina y clorhidrato de L-tirosina". J. Chem. Phys. 58 (6): 2547–2556. Código Bibliográfico :1973JChPh..58.2547F. doi :10.1063/1.1679537.
- ^ "Nomenclatura y simbolismo de aminoácidos y péptidos". Comisión Conjunta IUPAC-IUB sobre Nomenclatura Bioquímica. 1983. Archivado desde el original el 9 de octubre de 2008. Consultado el 5 de marzo de 2018 .
- ^ "Tirosina". The Columbia Electronic Encyclopedia, 6.ª ed . Infoplease.com — Columbia University Press. 2007. Consultado el 20 de abril de 2008 .
- ^ Harper D (2001). "Tirosina". Diccionario Etimológico en Línea . Consultado el 20 de abril de 2008 .
- ^ "Aminoácidos - Tirosina". www.biology.arizona.edu . Consultado el 31 de enero de 2018 .
- ^ "Comisión IUPAC-IUB sobre nomenclatura bioquímica: una notación de una letra para secuencias de aminoácidos". Journal of Biological Chemistry . 243 (13): 3557–3559. 10 de julio de 1968. doi : 10.1016/S0021-9258(19)34176-6 .
- ^ Saffran M (abril de 1998). "Nombres de aminoácidos y juegos de salón: desde nombres triviales hasta códigos de una sola letra, los nombres de aminoácidos han puesto a prueba la memoria de los estudiantes. ¿Es posible una nomenclatura más racional?". Educación bioquímica . 26 (2): 116–118. doi :10.1016/S0307-4412(97)00167-2.
- ^ Hunter T (19 de septiembre de 2012). "Por qué la naturaleza eligió el fosfato para modificar las proteínas". Philosophical Transactions of the Royal Society B: Biological Sciences . 367 (1602): 2513–2516. doi :10.1098/rstb.2012.0013. ISSN 0962-8436. PMC 3415839 . PMID 22889903.
- ^ Lu ZC, Jiang F, Wu YD (11 de diciembre de 2021). "Predicción de sitios de unión de fosfato en interacciones proteína-proteína dependientes de la fosforilación". Bioinformática . 37 (24): 4712–4718. doi :10.1093/bioinformatics/btab525. ISSN 1367-4811. PMID 34270697.
- ^ Liu BA, Nash PD (19 de septiembre de 2012). "Evolución de los dominios SH2 y las redes de señalización de fosfotirosina". Philosophical Transactions of the Royal Society B: Biological Sciences . 367 (1602): 2556–2573. doi :10.1098/rstb.2012.0107. ISSN 0962-8436. PMC 3415846 . PMID 22889907.
- ^ Barry BA (enero de 2015). "Dinámica de reacción y transferencia de electrones acoplada a protones: estudios de transferencia de carga basada en tirosina en sistemas naturales y biomiméticos". Biochimica et Biophysica Acta (BBA) - Bioenergetics . 1847 (1): 46–54. doi :10.1016/j.bbabio.2014.09.003. ISSN 0006-3002. PMID 25260243.
- ^ Pencharz PB, Hsu JW, Ball RO (junio de 2007). "Requerimientos de aminoácidos aromáticos en sujetos humanos sanos". The Journal of Nutrition . 137 (6 Suppl 1): 1576S–1578S, discusión 1597S-1598S. doi : 10.1093/jn/137.6.1576S . PMID 17513429.
- ^ Herramienta de clasificación de nutrientes. MyFoodData.com. https://tools.myfooddata.com/nutrient-ranking-tool/tyrosine/all/highest
- ^ "Tirosina". Centro Médico de la Universidad de Maryland . Archivado desde el original el 4 de junio de 2013. Consultado el 17 de marzo de 2011 .
- ^ ab Los 10 alimentos con mayor contenido de tirosina
- ^ Herramienta de clasificación de nutrientes. MyFoodData.com. https://tools.myfooddata.com https://tools.myfooddata.com/nutrient-ranking-tool/tyrosine/meats/highest/ounces/common/no
- ^ Hoffhines AJ, Damoc E, Bridges KG, Leary JA, Moore KL (diciembre de 2006). "Detección y purificación de proteínas sulfatadas con tirosina utilizando un nuevo anticuerpo monoclonal anti-sulfotirosina". The Journal of Biological Chemistry . 281 (49): 37877–87. doi : 10.1074/jbc.M609398200 . PMC 1764208 . PMID 17046811.
- ^ Kanan Y, Hamilton RA, Sherry DM, Al-Ubaidi MR (diciembre de 2012). "Enfoque en las moléculas: sulfotirosina". Experimental Eye Research . 105 : 85–6. doi :10.1016/j.exer.2012.02.014. PMC 3629733 . PMID 22406006.
- ^ Broadley KJ (marzo de 2010). "Los efectos vasculares de las trazas de aminas y anfetaminas". Farmacología y terapéutica . 125 (3): 363–375. doi :10.1016/j.pharmthera.2009.11.005. PMID 19948186.
- ^ Lindemann L, Hoener MC (mayo de 2005). "Un renacimiento de las aminas traza inspirado en una nueva familia de GPCR". Tendencias en ciencias farmacológicas . 26 (5): 274–281. doi :10.1016/j.tips.2005.03.007. PMID 15860375.
- ^ Wang X, Li J, Dong G, Yue J (febrero de 2014). "Los sustratos endógenos del CYP2D cerebral". Revista Europea de Farmacología . 724 : 211–218. doi :10.1016/j.ejphar.2013.12.025. PMID 24374199.
- ^ Battersby AR, Binks R, Harper BJ (1 de enero de 1962). "692. Biosíntesis de alcaloides. Parte II. La biosíntesis de la morfina". Journal of the Chemical Society : 3534–3544. doi :10.1039/JR9620003534. ISSN 0368-1769.
- ^ Bentinger M, Tekle M, Dallner G (mayo de 2010). "Coenzima Q: biosíntesis y funciones". Comunicaciones de investigación bioquímica y biofísica . 396 (1): 74–9. doi :10.1016/j.bbrc.2010.02.147. PMID 20494114.
- ^ Acosta MJ, Vázquez Fonseca L, Desbats MA, Cerqua C, Zordan R, Trevisson E, et al. (2016). "Biosíntesis de coenzima Q en la salud y la enfermedad". Biochimica et Biophysica Acta (BBA) - Bioenergética . 1857 (8): 1079–1085. doi : 10.1016/j.bbabio.2016.03.036 . PMID 27060254.
- ^ Zea-Rey AV, Cruz-Camino H, Vazquez-Cantu DL, Gutiérrez-García VM, Santos-Guzmán J, Cantú-Reyna C (27 de noviembre de 2017). "La incidencia de tirosinemia neonatal transitoria en una población mexicana". Revista de errores innatos del metabolismo y el cribado . 5 : 232640981774423. doi : 10.1177/2326409817744230 .
- ^ Booth AN, Masri MS, Robbins DJ, Emerson OH, Jones FT, DeEds F (1960). "Metabolismos de la tirosina por ácidos fenólicos urinarios". Journal of Biological Chemistry . 235 (9): 2649–2652. doi : 10.1016/S0021-9258(19)76930-0 .
- ^ Molnár GA, Wagner Z, Markó L, Kó Szegi T, Mohás M, Kocsis B, et al. (noviembre de 2005). "Excreción urinaria de ortotirosina en diabetes mellitus e insuficiencia renal: evidencia de producción de radicales hidroxilo". Riñón Internacional . 68 (5): 2281–7. doi : 10.1111/j.1523-1755.2005.00687.x . PMID 16221230.
- ^ Molnár GA, Nemes V, Biró Z, Ludány A, Wagner Z, Wittmann I (diciembre de 2005). "La acumulación de los marcadores de radicales libres de hidroxilo meta-, orto-tirosina y DOPA en lentes con cataratas se acompaña de un menor contenido de proteína y fenilalanina en la fase soluble en agua". Free Radical Research . 39 (12): 1359–66. doi :10.1080/10715760500307107. PMID 16298866. S2CID 31154432.
- ^ Rasmussen DD, Ishizuka B, Quigley ME, Yen SS (octubre de 1983). "Efectos de la ingestión de tirosina y triptófano en las concentraciones plasmáticas de catecolaminas y ácido 3,4-dihidroxifenilacético". The Journal of Clinical Endocrinology and Metabolism . 57 (4): 760–3. doi :10.1210/jcem-57-4-760. PMID 6885965.
- ^ Leathwood PD, Pollet P (1982). "Cambios de humor inducidos por la dieta en poblaciones normales". Revista de investigación psiquiátrica . 17 (2): 147–54. doi :10.1016/0022-3956(82)90016-4. PMID 6764931.
- ^ Deijen JB, Orlebeke JF (1994). "Efecto de la tirosina en la función cognitiva y la presión arterial bajo estrés". Boletín de investigación cerebral . 33 (3): 319–23. doi :10.1016/0361-9230(94)90200-3. PMID 8293316. S2CID 33823121.
- ^ Lieberman HR, Corkin S, Spring BJ, Wurtman RJ, Growdon JH (agosto de 1985). "Los efectos de los precursores de neurotransmisores dietéticos en el comportamiento humano". The American Journal of Clinical Nutrition . 42 (2): 366–70. doi :10.1093/ajcn/42.2.366. PMID 4025206.
- ^ Jung SE, Hase A, ann het Rot M (2015). "Efectos cognitivos y conductuales de la ingesta de tirosina en adultos humanos sanos". Farmacología, bioquímica y comportamiento . 133 : 1–6. doi :10.1016/j.pbb.2015.03.008. PMID 25797188. S2CID 30331663.
- ^ ab Lütke-Eversloh T, Santos CN, Stephanopoulos G (diciembre de 2007). "Perspectivas de la producción biotecnológica de L-tirosina y sus aplicaciones". Applied Microbiology and Biotechnology . 77 (4): 751–62. doi :10.1007/s00253-007-1243-y. PMID 17968539. S2CID 23088822.
- ^ Chavez-Bejar M, Baez-Viveros J, Martinez A, Bolivar F, Gosset G (2012). "Producción biotecnológica de L-tirosina y compuestos derivados". Process Biochemistry . 47 (7): 1017–1026. doi :10.1016/j.procbio.2012.04.005.
Enlaces externos
- Espectro MS de tirosina
- Metabolismo de la tirosina Archivado el 26 de julio de 2019 en Wayback Machine.
- Biosíntesis de fenilalanina y tirosina
- Biosíntesis de fenilalanina, tirosina y triptófano Archivado el 6 de mayo de 2021 en Wayback Machine.