Ácido biliar
Los ácidos biliares son ácidos esteroides que se encuentran predominantemente en la bilis de los mamíferos y otros vertebrados . Diversos ácidos biliares se sintetizan en el hígado . [1] Los ácidos biliares se conjugan con residuos de taurina o glicina para dar aniones llamados sales biliares . [2] [3] [4]
Los ácidos biliares primarios son aquellos sintetizados por el hígado. Los ácidos biliares secundarios resultan de acciones bacterianas en el colon . En humanos, el ácido taurocólico y el ácido glicocólico (derivados del ácido cólico ) y el ácido tauroquenodesoxicólico y el ácido glicoquenodesoxicólico (derivados del ácido quenodesoxicólico ) son las principales sales biliares. Son aproximadamente iguales en concentración. [5] También se encuentran las sales de sus derivados 7-alfa-deshidroxilados, el ácido desoxicólico y el ácido litocólico , y los derivados de los ácidos cólico, quenodesoxicólico y desoxicólico representan más del 90% de los ácidos biliares humanos. [5]
Los ácidos biliares comprenden alrededor del 80% de los compuestos orgánicos de la bilis (otros son los fosfolípidos y el colesterol ). [5] Una mayor secreción de ácidos biliares produce un aumento en el flujo biliar. Los ácidos biliares facilitan la digestión de las grasas y aceites de la dieta . Actúan como surfactantes formadores de micelas , que encapsulan los nutrientes, facilitando su absorción. [6] Estas micelas están suspendidas en el quimo antes de su posterior procesamiento . Los ácidos biliares también tienen acciones hormonales en todo el cuerpo, particularmente a través del receptor farnesoide X y GPBAR1 (también conocido como TGR5). [7]
La síntesis de ácidos biliares es la única forma en que los humanos u otros mamíferos pueden excretar el exceso de colesterol, ya que el compuesto original de todos los ácidos biliares es el colesterol. [ cita requerida ]

Producción
Ácidos biliares primarios
La síntesis de ácidos biliares se produce en las células hepáticas , que sintetizan ácidos biliares primarios ( ácido cólico y ácido quenodesoxicólico en humanos) a través de la oxidación del colesterol mediada por el citocromo P450 en un proceso de varios pasos. Se sintetizan aproximadamente 600 mg de sales biliares diariamente para reemplazar los ácidos biliares perdidos en las heces, aunque, como se describe a continuación, se secretan cantidades mucho mayores, se reabsorben en el intestino y se reciclan.
El paso limitante de la velocidad de la síntesis es la adición de un grupo hidroxilo de la posición 7 del núcleo esteroide por la enzima colesterol 7 alfa-hidroxilasa . Esta enzima es regulada a la baja por el ácido cólico, regulada al alza por el colesterol y es inhibida por las acciones de la hormona ileal FGF15/19 . [2] [3]
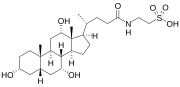
Antes de secretar cualquiera de los ácidos biliares (primarios o secundarios, ver más abajo), las células hepáticas los conjugan con glicina o taurina , para formar un total de 8 posibles ácidos biliares conjugados . Estos ácidos biliares conjugados a menudo se denominan sales biliares . El pKa de los ácidos biliares no conjugados está entre 5 y 6,5, [4] y el pH del duodeno varía entre 3 y 5, por lo que cuando los ácidos biliares no conjugados están en el duodeno, casi siempre están protonados (forma HA), lo que los hace relativamente insolubles en agua. La conjugación de ácidos biliares con aminoácidos reduce el pKa del conjugado ácido biliar/aminoácido a entre 1 y 4. Por lo tanto, los ácidos biliares conjugados casi siempre están en su forma desprotonada (A-) en el duodeno, lo que los hace mucho más solubles en agua y mucho más capaces de cumplir su función fisiológica de emulsionar grasas. [8] [9]
Ácidos biliares secundarios
Una vez secretadas en el lumen del intestino, las sales biliares son modificadas por las bacterias intestinales. Se deshidroxilan parcialmente. Sus grupos glicina y taurina se eliminan para dar lugar a los ácidos biliares secundarios , ácido desoxicólico y ácido litocólico . El ácido cólico se convierte en ácido desoxicólico y el ácido quenodesoxicólico en ácido litocólico. Estos cuatro ácidos biliares se reciclan, en un proceso conocido como circulación enterohepática . [2] [3]
Funciones
Digestión de lípidos
Como moléculas con regiones hidrofóbicas e hidrofílicas , las sales biliares conjugadas se asientan en la interfase lípido/agua y, por encima de la concentración adecuada, forman micelas . [9] La solubilidad añadida de las sales biliares conjugadas ayuda a su función al evitar la reabsorción pasiva en el intestino delgado. Como resultado, la concentración de ácidos biliares/sales en el intestino delgado es lo suficientemente alta como para formar micelas y solubilizar los lípidos. La "concentración micelar crítica" se refiere tanto a una propiedad intrínseca del propio ácido biliar como a la cantidad de ácido biliar necesaria para funcionar en la formación espontánea y dinámica de micelas. [9] Las micelas que contienen ácidos biliares ayudan a las lipasas a digerir los lípidos y a acercarlos a la membrana del borde en cepillo intestinal , lo que da como resultado la absorción de grasas. [6]
La síntesis de ácidos biliares es una de las principales vías metabólicas del colesterol en la mayoría de las especies, excepto los humanos. El cuerpo produce unos 800 mg de colesterol al día y aproximadamente la mitad de esa cantidad se utiliza para la síntesis de ácidos biliares, lo que supone entre 400 y 600 mg diarios. Los adultos humanos secretan entre 12 y 18 g de ácidos biliares en el intestino cada día, sobre todo después de las comidas. El tamaño del depósito de ácidos biliares es de entre 4 y 6 g, lo que significa que los ácidos biliares se reciclan varias veces al día. Alrededor del 95 % de los ácidos biliares se reabsorben mediante transporte activo en el íleon y se reciclan de nuevo al hígado para su posterior secreción en el sistema biliar y la vesícula biliar . Esta circulación enterohepática de los ácidos biliares permite una baja tasa de síntesis, sólo unos 0,3 g/día, pero con grandes cantidades secretadas en el intestino. [5]
Los ácidos biliares tienen otras funciones, entre ellas eliminar el colesterol del cuerpo, impulsar el flujo de bilis para eliminar ciertos catabolitos (incluida la bilirrubina ), emulsionar vitaminas liposolubles para permitir su absorción y ayudar en la motilidad y la reducción de la flora bacteriana que se encuentra en el intestino delgado y el tracto biliar. [5]
Señalización celular
Los ácidos biliares tienen acciones metabólicas en el cuerpo similares a las de las hormonas , actuando a través de dos receptores específicos, el receptor farnesoide X y el receptor de ácidos biliares acoplado a proteína G/TGR5 . [7] [10] Se unen de forma menos específica a otros receptores y se ha informado que regulan la actividad de ciertas enzimas [11] y canales iónicos [12] y la síntesis de diversas sustancias, incluidas las etanolamidas de ácidos grasos endógenos . [13] [14]
Estructura y síntesis
- Las estructuras de los principales ácidos biliares humanos
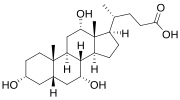
Las sales biliares constituyen una gran familia de moléculas, compuestas por una estructura esteroide con cuatro anillos, una cadena lateral de cinco u ocho carbonos que termina en un ácido carboxílico y varios grupos hidroxilo, cuyo número y orientación es diferente entre las sales biliares específicas. [1] Los cuatro anillos están etiquetados como A, B, C y D, desde el más lejano hasta el más cercano a la cadena lateral con el grupo carboxilo. El anillo D es un carbono más pequeño que los otros tres. La estructura se dibuja comúnmente con A a la izquierda y D a la derecha. Los grupos hidroxilo pueden estar en cualquiera de dos configuraciones: hacia arriba (o hacia afuera), denominado beta (β; a menudo dibujado por convención como una línea sólida), o hacia abajo, denominado alfa (α; mostrado como una línea discontinua). Todos los ácidos biliares tienen un grupo 3-hidroxilo, derivado de la molécula original, el colesterol, en el que el 3-hidroxilo es beta. [1]

El paso inicial en la vía clásica de síntesis hepática de ácidos biliares es la adición enzimática de un grupo hidroxilo 7α por la colesterol 7α-hidroxilasa (CYP7A1) formando 7α-hidroxicolesterol . Este luego se metaboliza a 7α-hidroxi-4-colesten-3-ona . Hay múltiples pasos en la síntesis de ácidos biliares que requieren 14 enzimas en total. [3] Estos dan como resultado que se altere la unión entre los dos primeros anillos esteroides (A y B), haciendo que la molécula se doble; en este proceso, el 3-hidroxilo se convierte a la orientación α. El ácido biliar de 24 carbonos más simple tiene dos grupos hidroxilo en las posiciones 3α y 7α. Este es el ácido 3α,7α-dihidroxi-5β-colan-24-oico o, como se lo conoce más comúnmente, ácido quenodesoxicólico . Este ácido biliar se aisló por primera vez del ganso doméstico , de donde se derivó la parte "cheno" del nombre (griego: χήν = ganso). El 5β en el nombre denota la orientación de la unión entre los anillos A y B del núcleo esteroide (en este caso, están doblados). El término "cholan" denota una estructura esteroide particular de 24 carbonos, y el "ácido 24-oico" indica que el ácido carboxílico se encuentra en la posición 24, al final de la cadena lateral. El ácido quenodesoxicólico es producido por muchas especies y es el ácido biliar funcional prototípico. [2] [3]
Una vía alternativa (ácida) de síntesis de ácidos biliares es iniciada por la esterol 27-hidroxilasa mitocondrial ( CYP27A1 ), expresada en el hígado, y también en macrófagos y otros tejidos. CYP27A1 contribuye significativamente a la síntesis total de ácidos biliares al catalizar la oxidación de la cadena lateral del esterol, después de lo cual la escisión de una unidad de tres carbonos en los peroxisomas conduce a la formación de un ácido biliar C24. Las vías menores iniciadas por la 25-hidroxilasa en el hígado y la 24-hidroxilasa en el cerebro también pueden contribuir a la síntesis de ácidos biliares. La 7α-hidroxilasa ( CYP7B1 ) genera oxiesteroles , que pueden convertirse posteriormente en el hígado en CDCA. [2] [3]
El ácido cólico , ácido 3α,7α,12α-trihidroxi-5β-colan-24-oico, el ácido biliar más abundante en humanos y muchas otras especies, fue descubierto antes que el ácido quenodesoxicólico. Es un ácido biliar trihidroxi con 3 grupos hidroxilo (3α, 7α y 12α). En su síntesis en el hígado, la hidroxilación de 12α se realiza por la acción adicional del CYP8B1 . Como esto ya había sido descrito, el descubrimiento del ácido quenodesoxicólico (con 2 grupos hidroxilo) convirtió a este nuevo ácido biliar en un "ácido desoxicólico" ya que tenía un grupo hidroxilo menos que el ácido cólico. [2] [3]
El ácido desoxicólico se forma a partir del ácido cólico mediante 7-deshidroxilación, lo que da lugar a 2 grupos hidroxilo (3α y 12α). Este proceso con ácido quenodesoxicólico da lugar a un ácido biliar con solo un grupo hidroxilo 3α, denominado ácido litocólico (litho = piedra), que se identificó por primera vez en un cálculo biliar de un ternero. Es poco soluble en agua y bastante tóxico para las células. [2] [3]
Diferentes familias de vertebrados han evolucionado para utilizar modificaciones de la mayoría de las posiciones en el núcleo esteroide y la cadena lateral de la estructura del ácido biliar. Para evitar los problemas asociados con la producción de ácido litocólico, la mayoría de las especies añaden un tercer grupo hidroxilo al ácido quenodesoxicólico. La posterior eliminación del grupo hidroxilo 7α por las bacterias intestinales dará como resultado un ácido biliar dihidroxilado menos tóxico pero aún funcional. A lo largo de la evolución de los vertebrados, se han elegido varias posiciones para la colocación del tercer grupo hidroxilo. Inicialmente, se favoreció la posición 16α, en particular en las aves. Más tarde, esta posición fue reemplazada en una gran cantidad de especies que seleccionaron la posición 12α. Los primates (incluidos los humanos) utilizan 12α para su tercera posición de grupo hidroxilo, produciendo ácido cólico. En ratones y otros roedores, la hidroxilación 6β forma ácidos muricolicos (α o β dependiendo de la posición 7 del hidroxilo). Los cerdos tienen hidroxilación 6α en el ácido hiocólico (ácido 3α,6α,7α-trihidroxi-5β-colanoico), y otras especies tienen un grupo hidroxilo en la posición 23 de la cadena lateral.
Se han descrito muchos otros ácidos biliares, a menudo en pequeñas cantidades, resultantes de modificaciones enzimáticas o de otro tipo de las bacterias. Los epímeros "iso-" tienen el grupo 3-hidroxilo en la posición β. Los epímeros "alo-" tienen la configuración 5α, que cambia la posición relativa de los anillos A y B. [1]
El ácido ursodesoxicólico se aisló por primera vez de la bilis de oso , que se ha utilizado con fines medicinales durante siglos. Su estructura se asemeja a la del ácido quenodesoxicólico, pero con el grupo 7-hidroxilo en la posición β. [1]
El ácido obeticólico , ácido 6α-etil-quenodesoxicólico, es un ácido biliar semisintético con mayor actividad como agonista del FXR, que se ha desarrollado como agente farmacéutico en ciertas enfermedades hepáticas. [15]
Acciones hormonales
Los ácidos biliares también actúan como hormonas esteroides, secretadas por el hígado, absorbidas por el intestino y que tienen varias acciones metabólicas directas en el cuerpo a través del receptor nuclear Farnesoid X receptor (FXR), también conocido por su nombre genético NR1H4 . [16] [17] [18] Otro receptor de ácidos biliares es el receptor de membrana celular conocido como receptor de ácidos biliares acoplado a proteína G 1 o TGR5 . Muchas de sus funciones como moléculas de señalización en el hígado y los intestinos son activando FXR, mientras que TGR5 puede estar involucrado en funciones metabólicas, endocrinas y neurológicas. [7] [19]
Regulación de la síntesis
Como surfactantes o detergentes , los ácidos biliares son potencialmente tóxicos para las células, por lo que sus concentraciones están estrechamente reguladas. La activación de FXR en el hígado inhibe la síntesis de ácidos biliares y es un mecanismo de control de retroalimentación cuando los niveles de ácidos biliares son demasiado altos. En segundo lugar, la activación de FXR por los ácidos biliares durante la absorción en el intestino aumenta la transcripción y síntesis de FGF19 , que luego inhibe la síntesis de ácidos biliares en el hígado. [20]
Funciones metabólicas
Nuevas evidencias asocian la activación de FXR con alteraciones en el metabolismo de los triglicéridos , el metabolismo de la glucosa y el crecimiento del hígado. [7] [21] [19]
Otras interacciones
Los ácidos biliares se unen a otras proteínas además de a sus receptores hormonales (FXR y TGR5) y sus transportadores. Entre estos objetivos proteicos, la enzima fosfolipasa D específica de la N-acilfosfatidiletanolamina (NAPE-PLD) genera amidas lipídicas bioactivas (por ejemplo, el cannabinoide endógeno anandamida ) que desempeñan papeles importantes en varias vías fisiológicas, incluidas las respuestas al estrés y al dolor, el apetito y la esperanza de vida. La NAPE-PLD organiza una comunicación cruzada directa entre las señales de las amidas lipídicas y la fisiología de los ácidos biliares. [13] [14]
Importancia clínica
Hiperlipidemia
Como los ácidos biliares se forman a partir del colesterol endógeno, la alteración de la circulación enterohepática de los ácidos biliares reducirá el colesterol. Los secuestradores de ácidos biliares se unen a los ácidos biliares en el intestino, impidiendo la reabsorción. Al hacerlo, más colesterol endógeno se desvía hacia la producción de ácidos biliares, lo que reduce los niveles de colesterol. Los ácidos biliares secuestrados se excretan luego en las heces. [22]
Colestasis
Las pruebas de ácidos biliares son útiles tanto en medicina humana como veterinaria, ya que ayudan en el diagnóstico de una serie de afecciones, incluidos tipos de colestasis como la colestasis intrahepática del embarazo , la derivación portosistémica y la displasia microvascular hepática en perros. [23] Las anomalías estructurales o funcionales del sistema biliar dan lugar a un aumento de la bilirrubina ( ictericia ) y de los ácidos biliares en la sangre. Los ácidos biliares están relacionados con el prurito , que es común en afecciones colestásicas como la cirrosis biliar primaria (CBP), la colangitis esclerosante primaria o la colestasis intrahepática del embarazo . [24] El tratamiento con ácido ursodesoxicólico se ha utilizado durante muchos años en estos trastornos colestásicos. [25] [26]
Cálculos biliares
Se ha estudiado ampliamente la relación entre los ácidos biliares y la saturación de colesterol en la bilis y la precipitación de colesterol para producir cálculos biliares. Los cálculos biliares pueden ser resultado de una mayor saturación de colesterol o bilirrubina , o de estasis biliar. Concentraciones más bajas de ácidos biliares o fosfolípidos en la bilis reducen la solubilidad del colesterol y conducen a la formación de microcristales. Se ha utilizado la terapia oral con ácido quenodesoxicólico y/o ácido ursodesoxicólico para disolver los cálculos biliares de colesterol. [27] [28] [29] Los cálculos pueden volver a aparecer cuando se interrumpe el tratamiento. La terapia con ácidos biliares puede ser útil para prevenir los cálculos en ciertas circunstancias, como después de una cirugía bariátrica . [30]
Diarrea por ácidos biliares
Las concentraciones excesivas de ácidos biliares en el colon son una causa de diarrea crónica . Se encuentra comúnmente cuando el íleon es anormal o ha sido extirpado quirúrgicamente, como en la enfermedad de Crohn , o causa una afección que se asemeja al síndrome del intestino irritable con predominio de diarrea (SII-D). Esta afección de diarrea por ácidos biliares/ malabsorción de ácidos biliares se puede diagnosticar mediante la prueba SeHCAT y tratar con secuestradores de ácidos biliares . [31]
Ácidos biliares y cáncer de colon
Los ácidos biliares pueden tener cierta importancia en el desarrollo del cáncer colorrectal . [32] El ácido desoxicólico (DCA) aumenta en el contenido colónico de los humanos en respuesta a una dieta rica en grasas. [33] En poblaciones con una alta incidencia de cáncer colorrectal, las concentraciones fecales de ácidos biliares son más altas, [34] [35] y esta asociación sugiere que una mayor exposición colónica a los ácidos biliares podría desempeñar un papel en el desarrollo del cáncer. En una comparación particular, las concentraciones fecales de DCA en africanos nativos en Sudáfrica (que consumen una dieta baja en grasas) en comparación con los afroamericanos (que consumen una dieta más alta en grasas) fue de 7,30 frente a 37,51 nmol/g de peso húmedo de heces. [36] Los africanos nativos en Sudáfrica tienen una baja tasa de incidencia de cáncer de colon de menos de 1:100.000, [37] en comparación con la alta tasa de incidencia de los afroamericanos varones de 72:100.000. [38]
Los estudios experimentales también sugieren mecanismos para los ácidos biliares en el cáncer de colon. La exposición de las células colónicas a altas concentraciones de DCA aumenta la formación de especies reactivas de oxígeno , lo que causa estrés oxidativo y también aumenta el daño del ADN. [39] Los ratones alimentados con una dieta con DCA añadido que imitaba los niveles de DCA colónico en humanos con una dieta alta en grasas desarrollaron neoplasia colónica , incluidos adenomas y adenocarcinomas ( cánceres ), a diferencia de los ratones alimentados con una dieta de control que producía una décima parte del nivel de DCA colónico que no tenían neoplasia colónica. [40] [41]
Los efectos del ácido ursodesoxicólico (UDCA) en la modificación del riesgo de cáncer colorrectal se han analizado en varios estudios, en particular en la colangitis esclerosante primaria y la enfermedad inflamatoria intestinal , con resultados variables relacionados en parte con la dosis. [42] [43] La variación genética en la enzima clave de síntesis de ácidos biliares, CYP7A1 , influyó en la eficacia del UDCA en la prevención del adenoma colorrectal en un ensayo a gran escala. [44]
Dermatología
Los ácidos biliares pueden utilizarse en inyecciones subcutáneas para eliminar la grasa no deseada (ver Mesoterapia ). El ácido desoxicólico como inyectable ha recibido la aprobación de la FDA para disolver la grasa submentoniana. [45] Los ensayos de fase III mostraron respuestas significativas, aunque muchos sujetos tuvieron reacciones adversas leves de hematomas, hinchazón, dolor, entumecimiento, eritema y rigidez alrededor del área tratada. [46] [47]
Referencias
- ^ abcde Hofmann AF, Hagey LR, Krasowski MD (febrero de 2010). "Sales biliares de vertebrados: variación estructural y posible significado evolutivo". J. Lipid Res . 51 (2): 226–46. doi : 10.1194/jlr.R000042 . PMC 2803226 . PMID 19638645.
- ^ abcdefg Russell DW (2003). "Las enzimas, la regulación y la genética de la síntesis de ácidos biliares". Annu. Rev. Biochem . 72 : 137–74. doi :10.1146/annurev.biochem.72.121801.161712. PMID 12543708.
- ^ abcdefgh Chiang JY (octubre de 2009). "Ácidos biliares: regulación de la síntesis". J. Lipid Res . 50 (10): 1955–66. doi : 10.1194/jlr.R900010-JLR200 . PMC 2739756 . PMID 19346330.
- ^ ab Carey, MC.; Small, DM. (Oct 1972). "Formación de micelas por sales biliares. Consideraciones físico-químicas y termodinámicas". Arch Intern Med . 130 (4): 506–27. doi :10.1001/archinte.1972.03650040040005. PMID 4562149.
- ^ abcde Hofmann AF (1999). "La importancia continua de los ácidos biliares en las enfermedades hepáticas e intestinales". Arch. Intern. Med . 159 (22): 2647–58. doi : 10.1001/archinte.159.22.2647 . PMID 10597755.
- ^ ab Hofmann AF, Borgström B (febrero de 1964). "La fase intraluminal de la digestión de las grasas en el hombre: el contenido lipídico de las fases micelar y oleosa del contenido intestinal obtenido durante la digestión y absorción de las grasas". J. Clin. Invest . 43 (2): 247–57. doi :10.1172/JCI104909. PMC 289518. PMID 14162533 .
- ^ abcd Fiorucci S, Mencarelli A, Palladino G, Cipriani S (noviembre de 2009). "Receptores activados por ácidos biliares: diana TGR5 y receptor farnesoide-X en trastornos lipídicos y de glucosa". Trends Pharmacol. Sci . 30 (11): 570–80. doi :10.1016/j.tips.2009.08.001. PMID 19758712.
- ^ 'Fundamentos de bioquímica médica, Lieberman, Marks y Smith, eds, pág. 432, 2007'
- ^ abc Hofmann AF (octubre de 1963). "La función de las sales biliares en la absorción de grasas. Las propiedades disolventes de soluciones micelares diluidas de sales biliares conjugadas". Biochem. J . 89 (1): 57–68. doi :10.1042/bj0890057. PMC 1202272 . PMID 14097367.
- ^ Li T, Chiang JY (2014). "Señalización de ácidos biliares en enfermedades metabólicas y terapia farmacológica". Pharmacol. Rev . 66 (4): 948–83. doi :10.1124/pr.113.008201. PMC 4180336 . PMID 25073467.
- ^ Nagahashi M, Takabe K, Liu R, Peng K, Wang X, Wang Y, Hait NC, Wang X, Allegood JC, Yamada A, Aoyagi T, Liang J, Pandak WM, Spiegel S, Hylemon PB, Zhou H (2015). "El receptor S1P 2 activado por ácidos biliares conjugados es un regulador clave de la esfingosina quinasa 2 y la expresión génica hepática". Hepatología . 61 (4): 1216–26. doi :10.1002/hep.27592. PMC 4376566 . PMID 25363242.
- ^ Wiemuth D, Sahin H, Falkenburger BH, Lefevre CM, Wasmuth HE, Grunder S (2012). "BASIC: un canal iónico sensible a los ácidos biliares altamente expresado en los conductos biliares". FASEB J . 26 (10): 4122–30. doi : 10.1096/fj.12-207043 . PMID 22735174. S2CID 205369332.
- ^ ab Magotti P, Bauer I, Igarashi M, Babagoli M, Marotta R, Piomelli D, Garau G (2015). "Estructura de la fosfolipasa D humana que hidroliza la N-acilfosfatidiletanolamina: regulación de la biosíntesis de etanolamida de ácidos grasos por los ácidos biliares". Estructura . 23 (3): 598–604. doi :10.1016/j.str.2014.12.018. PMC 4351732 . PMID 25684574.
- ^ ab Margheritis, E, Castellani B, Magotti P, Peruzzi S, Romeo E, Natali F, Mostarda S, Gioiello A, Piomelli D, Garau G (2016). "Reconocimiento de ácidos biliares por NAPE-PLD". Biología Química ACS . 11 (10): 2908–2914. doi :10.1021/acschembio.6b00624. PMC 5074845 . PMID 27571266.
- ^ Kulkarni AV, Tevethia HV, Arab JP, Candia R, Premkumar M, Kumar P, Sharma M, Reddy DN, Padaki NR (mayo de 2021). "Eficacia y seguridad del ácido obeticólico en la enfermedad hepática: una revisión sistemática y un metanálisis". Clínicas e investigación en hepatología y gastroenterología . 45 (3): 101675. doi :10.1016/j.clinre.2021.101675. PMID 33722778. S2CID 232242410.
- ^ Makishima M, Okamoto AY, Repa JJ, et al. (mayo de 1999). "Identificación de un receptor nuclear para ácidos biliares". Science . 284 (5418): 1362–5. Bibcode :1999Sci...284.1362M. doi :10.1126/science.284.5418.1362. PMID 10334992.
- ^ Parks DJ, Blanchard SG, Bledsoe RK, et al. (mayo de 1999). "Ácidos biliares: ligandos naturales para un receptor nuclear huérfano". Science . 284 (5418): 1365–8. Bibcode :1999Sci...284.1365P. doi :10.1126/science.284.5418.1365. PMID 10334993.
- ^ Wang H, Chen J, Hollister K, Sowers LC, Forman BM (mayo de 1999). "Los ácidos biliares endógenos son ligandos para el receptor nuclear FXR/BAR". Mol. Cell . 3 (5): 543–53. doi : 10.1016/s1097-2765(00)80348-2 . PMID 10360171.
- ^ ab Chiang JY, Ferrell JM (marzo de 2020). "Señalización de los receptores de ácidos biliares FXR y TGR5 en enfermedades del hígado graso y su tratamiento". American Journal of Physiology. Fisiología gastrointestinal y hepática . 318 (3): G554–G573. doi : 10.1152/ajpgi.00223.2019. PMC 7099488. PMID 31984784.
- ^ Kim, I; Ahn, SH; Inagaki, T; Choi, M; Ito, S; Guo, GL; Kliewer, SA; Gonzalez, FJ (2007). "Regulación diferencial de la homeostasis de los ácidos biliares por el receptor farnesoide X en el hígado y el intestino". Journal of Lipid Research . 48 (12): 2664–72. doi : 10.1194/jlr.M700330-JLR200 . PMID 17720959.
- ^ Shapiro, Hagit; Kolodziejczyk, Aleksandra A.; Halstuch, Daniel; Elinav, Eran (16 de enero de 2018). "Ácidos biliares en el metabolismo de la glucosa en la salud y la enfermedad". Revista de Medicina Experimental . 215 (2): 383–396. doi :10.1084/jem.20171965. ISSN 0022-1007. PMC 5789421 . PMID 29339445.
- ^ Davidson MH (2011). "Una revisión sistemática de la terapia secuestradora de ácidos biliares en niños con hipercolesterolemia familiar". J Clin Lipidol . 5 (2): 76–81. doi :10.1016/j.jacl.2011.01.005. PMID 21392720.
- ^ Allen L, Stobie D, Mauldin GN, Baer KE (enero de 1999). "Características clínico-patológicas de perros con displasia microvascular hepática con y sin derivaciones portosistémicas: 42 casos (1991-1996)". J. Am. Vet. Med. Assoc . 214 (2): 218–20. doi :10.2460/javma.1999.214.02.218. PMID 9926012.
- ^ Pusl T, Beuers U (2007). "Colestasis intrahepática del embarazo". Orphanet J Rare Dis . 2 : 26. doi : 10.1186/1750-1172-2-26 . PMC 1891276 . PMID 17535422.
- ^ Poupon RE, Balkau B, Eschwège E, Poupon R (mayo de 1991). "Un ensayo controlado multicéntrico de ursodiol para el tratamiento de la cirrosis biliar primaria. Grupo de estudio UDCA-PBC". N. Engl. J. Med . 324 (22): 1548–54. doi : 10.1056/NEJM199105303242204 . PMID 1674105.
- ^ Glantz A, Marschall HU, Lammert F, Mattsson LA (diciembre de 2005). "Colestasis intrahepática del embarazo: un ensayo controlado aleatorizado que compara la dexametasona y el ácido ursodesoxicólico". Hepatología . 42 (6): 1399–405. doi : 10.1002/hep.20952 . PMID 16317669. S2CID 19147632.
- ^ Danzinger RG, Hofmann AF, Schoenfield LJ, Thistle JL (enero de 1972). "Disolución de cálculos biliares de colesterol mediante ácido quenodesoxicólico". N. Engl. J. Med . 286 (1): 1–8. doi :10.1056/NEJM197201062860101. PMID 5006919.
- ^ Thistle JL, Hofmann AF (septiembre de 1973). "Eficacia y especificidad de la terapia con ácido quenodesoxicólico para disolver los cálculos biliares". N. Engl. J. Med . 289 (13): 655–9. doi :10.1056/NEJM197309272891303. PMID 4580472.
- ^ Petroni ML, Jazrawi RP, Pazzi P, et al. (enero de 2001). "Ácido ursodesoxicólico solo o con ácido quenodesoxicólico para la disolución de cálculos biliares de colesterol: un ensayo multicéntrico aleatorizado. El grupo de estudio británico-italiano de cálculos biliares". Aliment. Pharmacol. Ther . 15 (1): 123–8. doi : 10.1046/j.1365-2036.2001.00853.x . PMID 11136285.
- ^ Uy MC, Talingdan-Te MC, Espinosa WZ, Daez ML, Ong JP (diciembre de 2008). "Ácido ursodesoxicólico en la prevención de la formación de cálculos biliares después de la cirugía bariátrica: un metaanálisis". Obes Surg . 18 (12): 1532–8. doi :10.1007/s11695-008-9587-7. PMID 18574646. S2CID 207302960.
- ^ Pattni, S; Walters, JR (2009). "Avances recientes en la comprensión de la malabsorción de ácidos biliares". British Medical Bulletin . 92 : 79–93. doi : 10.1093/bmb/ldp032 . PMID 19900947.
- ^ Degirolamo C, Modica S, Palasciano G, Moschetta A (2011). "Ácidos biliares y cáncer de colon: Resolviendo el rompecabezas con receptores nucleares". Trends Mol Med . 17 (10): 564–72. doi :10.1016/j.molmed.2011.05.010. PMID 21724466.
- ^ Reddy BS, Hanson D, Mangat S, et al. (septiembre de 1980). "Efecto de una dieta rica en grasas y carne de vacuno y del modo de cocción de la carne de vacuno en la dieta sobre las enzimas bacterianas fecales y los ácidos biliares fecales y los esteroles neutros". J. Nutr . 110 (9): 1880–7. doi :10.1093/jn/110.9.1880. PMID 7411244.
- ^ Hill MJ (mayo de 1990). "Flujo biliar y cáncer de colon". Mutat. Res . 238 (3): 313–20. doi :10.1016/0165-1110(90)90023-5. PMID 2188127.
- ^ Cheah PY (1990). "Hipótesis sobre la etiología del cáncer colorrectal: una descripción general". Nutr Cancer . 14 (1): 5–13. doi :10.1080/01635589009514073. PMID 2195469.
- ^ Ou J, DeLany JP, Zhang M, Sharma S, O'Keefe SJ (2012). "Asociación entre niveles bajos de ácidos grasos de cadena corta en el colon y niveles altos de ácidos biliares en poblaciones con alto riesgo de cáncer de colon". Nutr Cancer . 64 (1): 34–40. doi :10.1080/01635581.2012.630164. PMC 6844083 . PMID 22136517.
- ^ O'Keefe SJ, Kidd M, Espitalier-Noel G, Owira P (mayo de 1999). "La rareza del cáncer de colon en los africanos se asocia con un bajo consumo de productos animales, no de fibra". Am. J. Gastroenterol . 94 (5): 1373–80. doi :10.1111/j.1572-0241.1999.01089.x. PMID 10235221. S2CID 6402410.
- ^ Sociedad Estadounidense del Cáncer. Datos y cifras sobre el cáncer 2009. http://www.cancer.org/Research/CancerFactsFigures/cancer-facts-figures-2009 Archivado el 13 de septiembre de 2012 en Wayback Machine.
- ^ Bernstein H, Bernstein C, Payne CM, Dvorak K (julio de 2009). "Ácidos biliares como agentes etiológicos endógenos en el cáncer gastrointestinal". World J. Gastroenterol . 15 (27): 3329–40. doi : 10.3748/wjg.15.3329 . PMC 2712893 . PMID 19610133.
- ^ Bernstein C, Holubec H, Bhattacharyya AK, et al. (agosto de 2011). "Carcinogenicidad del desoxicolato, un ácido biliar secundario". Arch. Toxicol . 85 (8): 863–71. doi :10.1007/s00204-011-0648-7. PMC 3149672 . PMID 21267546.
- ^ Prasad AR, Prasad S, Nguyen H, Facista A, Lewis C, Zaitlin B, Bernstein H, Bernstein C (julio de 2014). "Un nuevo modelo de cáncer de colon en ratones relacionado con la dieta es paralelo al cáncer de colon humano". World J Gastrointest Oncol . 6 (7): 225–43. doi : 10.4251/wjgo.v6.i7.225 . PMC 4092339 . PMID 25024814.
- ^ Singh S, Khanna S, Pardi DS, Loftus EV, Talwalkar JA (2013). "Efecto del uso de ácido ursodesoxicólico en el riesgo de neoplasia colorrectal en pacientes con colangitis esclerosante primaria y enfermedad inflamatoria intestinal: una revisión sistemática y metanálisis". Inflamm. Bowel Dis . 19 (8): 1631–8. doi :10.1097/MIB.0b013e318286fa61. PMID 23665966. S2CID 39918727.
- ^ Eaton JE, Silveira MG, Pardi DS, Sinakos E, Kowdley KV, Luketic VA, Harrison ME, McCashland T, Befeler AS, Harnois D, Jorgensen R, Petz J, Lindor KD (2011). "El ácido ursodesoxicólico en dosis altas se asocia con el desarrollo de neoplasia colorrectal en pacientes con colitis ulcerosa y colangitis esclerosante primaria". Am. J. Gastroenterol . 106 (9): 1638–45. doi :10.1038/ajg.2011.156. PMC 3168684 . PMID 21556038.
- ^ Wertheim BC, Smith JW, Fang C, Alberts DS, Lance P, Thompson PA (2012). "Modificación del riesgo de adenoma colorrectal por polimorfismos de CYP7A1 y el papel del metabolismo de los ácidos biliares en la carcinogénesis". Cancer Prev Res (Phila) . 5 (2): 197–204. doi :10.1158/1940-6207.CAPR-11-0320. PMC 3400261. PMID 22058145 .
- ^ "Inyección de ácido desoxicólico". Medline plus . Consultado el 26 de agosto de 2015 .
- ^ Ascher B, Hoffmann K, Walker P, Lippert S, Wollina U, Havlickova B (2014). "Eficacia, resultados informados por los pacientes y perfil de seguridad de ATX-101 (ácido desoxicólico), un fármaco inyectable para la reducción de la grasa submentoniana no deseada: resultados de un estudio de fase III, aleatorizado y controlado con placebo". J Eur Acad Dermatol Venereol . 28 (12): 1707–15. doi :10.1111/jdv.12377. PMC 4263247 . PMID 24605812.
- ^ Wollina U, Goldman A (2015). "ATX-101 para la reducción de la grasa submentoniana". Opinión de expertos Pharmacother . 16 (5): 755–62. doi :10.1517/14656566.2015.1019465. PMID 25724831. S2CID 23094631.
Enlaces externos
- Ácidos biliares y sales en los encabezados de materias médicas (MeSH) de la Biblioteca Nacional de Medicina de EE. UU.
- Número especial sobre los "Ácidos biliares"