Mesotelioma
| Mesotelioma | |
|---|---|
| Otros nombres | Mesotelioma maligno |
 | |
| Tomografía computarizada que muestra un mesotelioma del lado izquierdo con un ganglio linfático mediastínico agrandado | |
| Especialidad | Oncología |
| Síntomas | Dificultad para respirar , abdomen hinchado, dolor en la pared torácica, tos, sensación de cansancio, pérdida de peso [1] |
| Complicaciones | Líquido alrededor del pulmón [1] |
| Inicio habitual | Inicio gradual [2] |
| Causas | c. 40 años después de la exposición al amianto [3] |
| Factores de riesgo | Genética , posiblemente, infección con virus simio 40 [3] [4] |
| Método de diagnóstico | Imágenes médicas , examen del líquido producido por el cáncer , biopsia de tejido [2] |
| Prevención | Disminución de la exposición al amianto [5] |
| Tratamiento | Cirugía, radioterapia , quimioterapia , pleurodesis [6] |
| Pronóstico | Supervivencia a cinco años : aproximadamente 8-12 % (EE. UU.; varía según la raza) [7] |
| Frecuencia | 60.800 (afectados durante 2015) [8] |
| Fallecidos | 32.400 (2015) [9] |
El mesotelioma es un tipo de cáncer que se desarrolla a partir de la fina capa de tejido que cubre muchos de los órganos internos (conocida como mesotelio ). [10] El área afectada con mayor frecuencia es el revestimiento de los pulmones y la pared torácica . [1] [3] Con menor frecuencia, el revestimiento del abdomen y, en raras ocasiones, el saco que rodea el corazón , [11] o el saco que rodea los testículos pueden verse afectados. [1] [12] Los signos y síntomas del mesotelioma pueden incluir dificultad para respirar debido al líquido alrededor del pulmón , abdomen hinchado, dolor en la pared torácica, tos, sensación de cansancio y pérdida de peso. [1] Estos síntomas suelen aparecer lentamente. [2]
Más del 80% de los casos de mesotelioma son causados por la exposición al asbesto . [3] Cuanto mayor sea la exposición, mayor será el riesgo. [3] A partir de 2013, alrededor de 125 millones de personas en todo el mundo han estado expuestas al asbesto en el trabajo. [13] Se producen altas tasas de enfermedad en personas que extraen asbesto, producen productos a partir de asbesto, trabajan con productos de asbesto, viven con trabajadores de asbesto o trabajan en edificios que contienen asbesto. [3] La exposición al asbesto y la aparición del cáncer generalmente están separadas por unos 40 años. [3] Lavar la ropa de alguien que trabajó con asbesto también aumenta el riesgo. [13] Otros factores de riesgo incluyen la genética y la infección con el virus simio 40 . [3] El diagnóstico puede sospecharse basándose en los hallazgos de la radiografía de tórax y la tomografía computarizada , y se confirma examinando el líquido producido por el cáncer o mediante una biopsia de tejido del cáncer. [2]
La prevención se centra en reducir la exposición al amianto. [5] El tratamiento suele incluir cirugía, radioterapia y quimioterapia . [6] Se puede utilizar un procedimiento conocido como pleurodesis , que implica el uso de sustancias como el talco para cicatrizar la pleura , para evitar que se acumule más líquido alrededor de los pulmones. [6] La quimioterapia suele incluir los medicamentos cisplatino y pemetrexed . [2] El porcentaje de personas que sobreviven cinco años después del diagnóstico es, en promedio, del 8 % en los Estados Unidos. [7]
En 2015, alrededor de 60.800 personas tenían mesotelioma y 32.000 murieron a causa de la enfermedad. [8] [9] Las tasas de mesotelioma varían en diferentes áreas del mundo. [3] Las tasas son más altas en Australia, el Reino Unido y más bajas en Japón. [3] Ocurre en alrededor de 3.000 personas por año en los Estados Unidos. [14] Ocurre con más frecuencia en hombres que en mujeres. [3] Las tasas de la enfermedad han aumentado desde la década de 1950. [3] El diagnóstico generalmente ocurre después de los 65 años y la mayoría de las muertes ocurren alrededor de los 70 años. [3] La enfermedad era rara antes del uso comercial del asbesto. [3]
Signos y síntomas
Pulmones
Los síntomas o signos del mesotelioma pueden no aparecer hasta 20 a 50 años (o más) después de la exposición al asbesto. La falta de aliento, la tos y el dolor en el pecho debido a una acumulación de líquido en el espacio pleural ( derrame pleural ) son a menudo síntomas del mesotelioma pleural. [15]
El mesotelioma que afecta la pleura puede causar estos signos y síntomas: [15]
- Dolor en la pared torácica
- Derrame pleural o líquido que rodea el pulmón.
- Dificultad para respirar, que podría deberse a un colapso pulmonar o a un derrame pleural.
- Fatiga o anemia
- Sibilancia, ronquera o tos
- Sangre en el esputo (líquido) expectorado ( hemoptisis )
En casos graves, la persona puede tener muchas masas tumorales . El individuo puede desarrollar un neumotórax o colapso del pulmón . La enfermedad puede hacer metástasis o propagarse a otras partes del cuerpo. [ cita requerida ]
Abdomen
Los síntomas más comunes del mesotelioma peritoneal son hinchazón abdominal y dolor debido a la ascitis (acumulación de líquido en la cavidad abdominal). Otras características pueden incluir pérdida de peso, fiebre , sudores nocturnos , falta de apetito, vómitos, estreñimiento y hernia umbilical . [16] Si el cáncer se ha propagado más allá del mesotelio a otras partes del cuerpo, los síntomas pueden incluir dolor, dificultad para tragar o hinchazón del cuello o la cara. Estos síntomas pueden ser causados por el mesotelioma o por otras afecciones menos graves. [ cita requerida ]
Los tumores que afectan la cavidad abdominal a menudo no causan síntomas hasta que se encuentran en una etapa avanzada. Los síntomas incluyen: [ cita requerida ]
- Dolor abdominal
- Ascitis o acumulación anormal de líquido en el abdomen.
- Una masa en el abdomen
- Problemas con la función intestinal
- Pérdida de peso
Corazón
El mesotelioma pericárdico no está bien caracterizado, pero los casos observados han incluido síntomas cardíacos, específicamente pericarditis constrictiva , insuficiencia cardíaca , embolia pulmonar y taponamiento cardíaco . También han incluido síntomas inespecíficos, como dolor torácico subesternal, ortopnea (dificultad para respirar al acostarse) y tos. Estos síntomas son causados por el tumor que encierra o infiltra el corazón. [11]
Etapa final
En casos graves de la enfermedad, pueden presentarse los siguientes signos y síntomas: [8]
- Coágulos de sangre en las venas, que pueden causar tromboflebitis.
- Coagulación intravascular diseminada , un trastorno que causa sangrado grave en muchos órganos del cuerpo.
- Ictericia o coloración amarillenta de los ojos y la piel.
- Nivel bajo de azúcar en sangre
- Derrame pleural
- Embolia pulmonar o coágulos de sangre en las arterias de los pulmones.
- Ascitis severa
Si un mesotelioma forma metástasis , estas generalmente afectan el hígado , la glándula suprarrenal , el riñón u otros pulmones. [17]
Causas
Trabajar con amianto es el factor de riesgo más común para el mesotelioma. [18] Sin embargo, se han reportado casos de mesotelioma en algunas personas sin exposición conocida al amianto. La evidencia preliminar también genera preocupación sobre los nanotubos de carbono . [19] [20]
Amianto
Se ha descubierto que la incidencia del mesotelioma es mayor en las poblaciones que viven cerca de asbesto natural. Las personas pueden estar expuestas al asbesto natural en áreas donde se realizan actividades mineras o de construcción de carreteras, o cuando la roca que contiene asbesto se erosiona naturalmente. Otra vía común de exposición es a través del suelo que contiene asbesto, que se utiliza para blanquear, enlucir y techar las casas en Grecia. [13] En el centro de Capadocia , Turquía, el mesotelioma causaba el 50% de todas las muertes en tres pequeñas aldeas: Tuzköy, Karain y Sarıhıdır. Inicialmente, esto se atribuyó a la erionita . La exposición ambiental al asbesto ha causado mesotelioma en lugares distintos de Turquía, incluidos Córcega, Grecia, Chipre, China y California. [13] [21] [22] En la ciudad montañosa de Metsovo , en el norte de Grecia , esta exposición había dado como resultado una incidencia de mesotelioma alrededor de 300 veces más de lo esperado en poblaciones libres de asbesto, y se asoció con una calcificación pleural muy frecuente conocida como pulmón de Metsovo . [23] [24]
La presencia documentada de fibras de amianto en suministros de agua y productos alimenticios ha fomentado preocupaciones sobre el posible impacto de la exposición a largo plazo y aún desconocida de la población general a estas fibras. [25]
La exposición al talco también es un factor de riesgo para el mesotelioma; la exposición puede afectar a quienes viven cerca de minas de talco, trabajan en minas de talco o trabajan en fábricas de talco. [26]
En los Estados Unidos, el asbesto se considera la principal causa de mesotelioma maligno [27] y se ha considerado que está "indiscutiblemente" [28] asociado con el desarrollo del mesotelioma. De hecho, la relación entre el asbesto y el mesotelioma es tan fuerte que muchos consideran al mesotelioma un tumor "señal" o "centinela". [29] [30] [31] [32] En la mayoría de los casos existe un historial de exposición al asbesto.
El mesotelioma pericárdico puede no estar asociado con la exposición al asbesto. [11]
El amianto era conocido en la antigüedad, pero no se extraía ni se utilizaba ampliamente con fines comerciales hasta finales del siglo XIX. Su uso aumentó considerablemente durante la Segunda Guerra Mundial . Desde principios de la década de 1940, millones de trabajadores estadounidenses han estado expuestos al polvo de amianto. Inicialmente, los riesgos asociados con la exposición al amianto no se conocían públicamente. Sin embargo, más tarde se encontró un mayor riesgo de desarrollar mesotelioma entre el personal naval (por ejemplo, la Armada, el Cuerpo de Marines y la Guardia Costera), los trabajadores de los astilleros, las personas que trabajan en minas y molinos de amianto, los productores de productos de amianto, los trabajadores de las industrias de la calefacción y la construcción y otros comerciantes. Hoy, la posición oficial de la Administración de Seguridad y Salud Ocupacional de los Estados Unidos (OSHA) y la Agencia de Protección Ambiental de los Estados Unidos (EPA) es que las protecciones y los "límites de exposición permisibles" requeridos por las regulaciones estadounidenses, si bien son adecuados para prevenir la mayoría de las enfermedades no malignas relacionadas con el amianto, no son adecuados para prevenir o proteger contra los cánceres relacionados con el amianto, como el mesotelioma. [33] Asimismo, la Dirección de Salud y Seguridad del Gobierno británico (HSE) afirma formalmente que cualquier umbral de exposición al amianto debe ser de un nivel muy bajo y existe un amplio consenso en que, si existe dicho umbral, actualmente no se puede cuantificar. Por lo tanto, a efectos prácticos, la HSE supone que no existe tal umbral "seguro". Otros han señalado también que no hay evidencia de un nivel umbral por debajo del cual no haya riesgo de mesotelioma. [34] Parece haber una relación lineal dosis-respuesta , en la que una dosis creciente produce un riesgo creciente de enfermedad. [35] Sin embargo, el mesotelioma puede estar relacionado con exposiciones breves, de bajo nivel o indirectas al amianto. [28] La dosis necesaria para el efecto parece ser menor para el mesotelioma inducido por amianto que para la asbestosis pulmonar o el cáncer de pulmón. [28] Una vez más, no se conoce un nivel seguro de exposición al amianto en relación con un mayor riesgo de mesotelioma.
El tiempo transcurrido desde la primera exposición hasta la aparición de la enfermedad oscila entre 25 y 70 años. [36] Prácticamente nunca es inferior a quince años y alcanza su punto máximo a los 30-40 años. [28] [37] La duración de la exposición al amianto que causa mesotelioma puede ser breve. Por ejemplo, se han documentado casos de mesotelioma con tan solo 1-3 meses de exposición. [38] [39]
Ocupacional
La exposición a fibras de amianto se ha reconocido como un riesgo para la salud ocupacional desde principios del siglo XX. Numerosos estudios epidemiológicos han asociado la exposición ocupacional al amianto con el desarrollo de placas pleurales, engrosamiento pleural difuso, asbestosis, carcinoma de pulmón y laringe, tumores gastrointestinales y mesotelioma maligno difuso de la pleura y el peritoneo. El amianto se ha utilizado ampliamente en muchos productos industriales, incluidos cemento, forros de freno, juntas, tejas para techos, productos para pisos, textiles y aislamientos. [40]
La minería de amianto comercial en Wittenoom, Australia Occidental , tuvo lugar entre 1937 y 1966. El primer caso de mesotelioma en la ciudad se produjo en 1960. El segundo caso fue en 1969, y a partir de entonces empezaron a aparecer nuevos casos con mayor frecuencia. El tiempo transcurrido entre la exposición inicial al amianto y el desarrollo del mesotelioma varió de 12 años y 9 meses a 58 años. [41] Un estudio de cohorte de mineros empleados en la mina informó que en 1985 se habían producido 85 muertes atribuibles al mesotelioma. En 1994, se habían notificado 539 muertes debidas a mesotelioma en Australia Occidental. [ cita requerida ]
En Estados Unidos, la exposición ocupacional al amianto se produce principalmente cuando las personas realizan tareas de mantenimiento en edificios que ya tienen amianto. Aproximadamente 1,3 millones de trabajadores estadounidenses están expuestos al amianto cada año; en 2002, se estima que 44.000 mineros estuvieron potencialmente expuestos al amianto. [26]
Exposición secundaria paraocupacional
Los familiares y otras personas que viven con trabajadores del amianto tienen un mayor riesgo de desarrollar mesotelioma y posiblemente otras enfermedades relacionadas con el amianto. [12] [42] [43] Este riesgo puede ser el resultado de la exposición al polvo de amianto que los trabajadores del amianto llevan a casa en la ropa y el cabello al lavar la ropa de un trabajador o al entrar en contacto con ropa de trabajo contaminada con amianto. [13] [26] Para reducir la posibilidad de exponer a los miembros de la familia a las fibras de amianto, los trabajadores del amianto generalmente deben ducharse y cambiarse de ropa antes de abandonar el lugar de trabajo. [ cita requerida ]
Amianto en los edificios
Muchos materiales de construcción utilizados en locales públicos y domésticos antes de la prohibición del amianto pueden contener amianto. Quienes realizan trabajos de renovación o actividades de bricolaje pueden exponerse al polvo de amianto. En el Reino Unido, el uso de amianto crisotilo se prohibió a finales de 1999. El amianto marrón y azul se prohibieron en el Reino Unido alrededor de 1985. Los edificios construidos o renovados antes de estas fechas pueden contener materiales de amianto. [44]
Por lo tanto, es un requisito legal que todas aquellas personas que puedan entrar en contacto con el amianto en su trabajo diario hayan recibido la formación pertinente sobre el amianto. [ cita requerida ]
Disposición genética
En una investigación reciente realizada en la población blanca estadounidense en 2012, se descubrió que las personas con una mutación de la línea germinal en su gen BAP1 tienen un mayor riesgo de desarrollar mesotelioma y melanoma uveal . [45]
Erionita
La erionita es un mineral de zeolita con propiedades similares al amianto y se sabe que causa mesotelioma. [12] Una investigación epidemiológica detallada ha demostrado que la erionita causa mesotelioma principalmente en familias con predisposición genética. [13] [21] [22] La erionita se encuentra en depósitos en el oeste de los Estados Unidos, donde se utiliza en grava para pavimentar carreteras , y en Turquía, donde se utiliza para construir viviendas. En Turquía, Estados Unidos y México, la erionita se ha asociado con el mesotelioma y, por lo tanto, ha sido designada como "carcinógeno humano conocido" por el Programa Nacional de Toxicología de los Estados Unidos . [22]
Otro
En casos raros, el mesotelioma también se ha asociado con la irradiación del tórax o el abdomen, dióxido de torio intrapleural ( thorotrast ) como medio de contraste e inhalación de otros silicatos fibrosos, como erionita o talco . [12] [26] Algunos estudios sugieren que el virus simio 40 ( SV40 ) puede actuar como un cofactor en el desarrollo del mesotelioma. [26] Esto se ha confirmado en estudios con animales, [46] [47] pero los estudios en humanos no son concluyentes. [46] [48] [49]
Fisiopatología

Sistémico
El mesotelio consiste en una sola capa de células aplanadas a cuboidales que forman el revestimiento epitelial de las cavidades serosas del cuerpo, incluyendo las cavidades peritoneal , pericárdica y pleural . [50] La deposición de fibras de asbesto en el parénquima del pulmón puede resultar en la penetración de la pleura visceral desde donde la fibra puede luego ser transportada a la superficie pleural, conduciendo así al desarrollo de placas mesoteliales malignas. Los procesos que conducen al desarrollo del mesotelioma peritoneal siguen sin resolverse, aunque se ha propuesto que las fibras de asbesto del pulmón son transportadas al abdomen y órganos asociados a través del sistema linfático . [51] Además, las fibras de asbesto pueden depositarse en el intestino después de la ingestión de esputo contaminado con fibras de asbesto. [ cita requerida ]
Se ha demostrado que la contaminación pleural con amianto u otras fibras minerales causa cáncer. Las fibras de amianto largas y delgadas (amianto azul, fibras de anfíbol ) son carcinógenos más potentes que las "fibras plumosas" ( fibras de amianto crisotilo o blanco). [28] Sin embargo, ahora hay evidencia de que las partículas más pequeñas pueden ser más peligrosas que las fibras más grandes. Permanecen suspendidas en el aire, donde pueden ser inhaladas, y pueden penetrar más fácilmente y más profundamente en los pulmones. "Probablemente descubramos mucho más sobre los aspectos de salud del amianto a partir del [ataque al World Trade Center], lamentablemente", dijo el Dr. Alan Fein, jefe de medicina pulmonar y de cuidados intensivos en el Sistema de Salud Judío de North Shore-Long Island. [52]
Se ha demostrado el desarrollo de mesotelioma en ratas tras la inoculación intrapleural de fibras de crisotilo fosforiladas. Se ha sugerido que en los seres humanos, el transporte de fibras a la pleura es fundamental para la patogénesis del mesotelioma. Esto está respaldado por el reclutamiento observado de un número significativo de macrófagos y otras células del sistema inmunitario hacia lesiones localizadas de fibras de amianto acumuladas en las cavidades pleural y peritoneal de ratas. Estas lesiones continuaron atrayendo y acumulando macrófagos a medida que avanzaba la enfermedad, y los cambios celulares dentro de la lesión culminaron en un tumor morfológicamente maligno. [ cita requerida ]
La evidencia experimental sugiere que el asbesto actúa como un carcinógeno completo y que el desarrollo del mesotelioma ocurre en etapas secuenciales de iniciación y promoción. Los mecanismos moleculares subyacentes a la transformación maligna de células mesoteliales normales por fibras de asbesto siguen sin estar claros a pesar de la demostración de sus capacidades oncogénicas (ver el párrafo siguiente). Sin embargo, aún no se ha logrado la transformación completa in vitro de células mesoteliales humanas normales a un fenotipo maligno después de la exposición a fibras de asbesto. En general, se cree que las fibras de asbesto actúan a través de interacciones físicas directas con las células del mesotelio junto con efectos indirectos después de la interacción con células inflamatorias como los macrófagos. [ cita requerida ]
Intracelular
El análisis de las interacciones entre las fibras de amianto y el ADN ha demostrado que las fibras fagocitadas son capaces de entrar en contacto con los cromosomas , a menudo adhiriéndose a las fibras de cromatina o enredándose dentro del cromosoma. [53] Este contacto entre la fibra de amianto y los cromosomas o las proteínas estructurales del aparato del huso puede inducir anomalías complejas. La anomalía más común es la monosomía del cromosoma 22. Otras anomalías frecuentes incluyen la reorganización estructural de los brazos cromosómicos 1p, 3p, 9p y 6q. [ cita requerida ]
Las anomalías genéticas comunes en las líneas celulares del mesotelioma incluyen la eliminación de los genes supresores de tumores : [ cita requerida ]
- Neurofibromatosis tipo 2 en 22q12 [54]
- P16 TINTA4A [55]
- P14 ARF [56]
También se ha demostrado que el amianto media la entrada de ADN extraño en las células diana. La incorporación de este ADN extraño puede provocar mutaciones y oncogénesis mediante varios mecanismos posibles: [ cita requerida ]
- Inactivación de genes supresores de tumores
- Activación de oncogenes [57] En las células tumorales , estos genes a menudo están mutados o se expresan en niveles elevados. [58]
- Activación de protooncogenes debido a la incorporación de ADN extraño que contiene una región promotora
- Activación de enzimas reparadoras del ADN , que pueden ser propensas a errores [59]
- Activación de la telomerasa [60]
- Prevención de la apoptosis [61]
Varios genes están comúnmente mutados en el mesotelioma y pueden ser factores pronósticos. Estos incluyen principalmente BAP1 , NF2 y TP53 ; [62] el receptor del factor de crecimiento epidérmico (EGFR) y C-Met , las tirosina quinasas receptoras también pueden estar alteradas y sobreexpresadas en muchos mesoteliomas. Se ha encontrado cierta asociación con EGFR y la histología epitelioide, pero no se ha encontrado una asociación clara entre la sobreexpresión de EGFR y la supervivencia general; las alteraciones de BAP1 también son predominantemente en la histología epitelioide. La aneuploidía , que va desde la haploidía a la tetraploidía, y la hipermetilación de la isla CpG también han demostrado ser frecuentes y estar asociadas con la supervivencia. [63] La expresión de la tirosina quinasa del receptor AXL es un factor pronóstico negativo. La expresión de PDGFRB es un factor pronóstico positivo. [64] En general, el mesotelioma se caracteriza por la pérdida de función en los genes supresores de tumores , más que por una sobreexpresión o ganancia de función en los oncogenes . [65]
Como una neoplasia maligna desencadenada por el medio ambiente, se ha descubierto que los tumores de mesotelioma son de origen policlonal , al realizar un ensayo basado en la inactivación del cromosoma X en tumores epiteloides y bifásicos obtenidos de pacientes femeninas. [66] Estos resultados sugieren que un factor ambiental, muy probablemente la exposición al asbesto, puede dañar y transformar un grupo de células en el tejido, lo que resulta en una población de células tumorales que son, aunque solo ligeramente, genéticamente diferentes. [67]
Sistema inmunitario
Se ha demostrado que las fibras de amianto alteran la función y las propiedades secretoras de los macrófagos, creando en última instancia condiciones que favorecen el desarrollo del mesotelioma. Tras la fagocitosis del amianto, los macrófagos generan mayores cantidades de radicales hidroxilo , que son subproductos normales del metabolismo anaeróbico celular. Sin embargo, estos radicales libres también son agentes clastogénicos (que rompen los cromosomas) y que actúan sobre la membrana y que se cree que promueven la carcinogenicidad del amianto. Estos oxidantes pueden participar en el proceso oncogénico interactuando directa e indirectamente con el ADN, modificando los eventos celulares asociados a la membrana, incluida la activación de oncogenes y la perturbación de las defensas antioxidantes celulares. [ cita requerida ]
El amianto también puede poseer propiedades inmunosupresoras . Por ejemplo, se ha demostrado que las fibras de crisotilo inhiben la proliferación in vitro de linfocitos de sangre periférica estimulados por fitohemaglutinina, suprimen la lisis de las células asesinas naturales y reducen significativamente la viabilidad y la recuperación de las células asesinas activadas por linfocinas . Además, las alteraciones genéticas en los macrófagos activados por el amianto pueden dar lugar a la liberación de potentes mitógenos de células mesoteliales, como el factor de crecimiento derivado de plaquetas (PDGF) y el factor de crecimiento transformante β (TGF-β), que a su vez pueden inducir la estimulación y proliferación crónicas de células mesoteliales después de una lesión por fibras de amianto. [ cita requerida ]
Diagnóstico
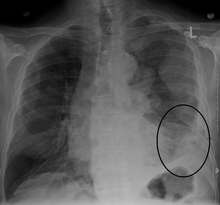


El diagnóstico de mesotelioma puede sospecharse mediante imágenes, pero se confirma con una biopsia. Debe diferenciarse clínica e histológicamente de otras neoplasias malignas pleurales y pulmonares, incluida la enfermedad pleural reactiva, el carcinoma pulmonar primario, las metástasis pleurales de otros cánceres y otros cánceres pleurales primarios. [12] El mesotelioma pericárdico primario a menudo se diagnostica después de que ha hecho metástasis en los ganglios linfáticos o los pulmones. [11]

Imágenes
El diagnóstico del mesotelioma suele ser difícil porque los síntomas son similares a los de otras enfermedades. El diagnóstico comienza con una revisión de la historia clínica del paciente. Una historia de exposición al asbesto puede aumentar la sospecha clínica de mesotelioma. Se realiza un examen físico, seguido de una radiografía de tórax y, a menudo, pruebas de función pulmonar . La radiografía puede revelar un engrosamiento pleural que se observa comúnmente después de la exposición al asbesto y aumenta la sospecha de mesotelioma. [15] Por lo general, se realiza una tomografía computarizada (o TAC) o una resonancia magnética . Si hay una gran cantidad de líquido, se pueden detectar células anormales mediante citopatología si este líquido se aspira con una jeringa. [11] Para el líquido pleural, esto se realiza mediante toracocentesis o toracostomía con tubo ( tubo torácico ); para la ascitis, con paracentesis o drenaje ascítico; y para el derrame pericárdico con pericardiocentesis . Si bien la ausencia de células malignas en la citología no excluye por completo el mesotelioma, lo hace mucho más improbable, especialmente si se puede hacer un diagnóstico alternativo (p. ej., tuberculosis , insuficiencia cardíaca ). [ cita requerida ] Sin embargo, en el caso del mesotelioma pericárdico primario, el líquido pericárdico puede no contener células malignas y una biopsia de tejido es más útil para el diagnóstico. [11] El uso de la citología convencional para el diagnóstico del mesotelioma maligno es difícil, pero la inmunohistoquímica ha mejorado enormemente la precisión de la citología. [ cita requerida ]
Biopsia
Generalmente, se necesita una biopsia para confirmar el diagnóstico de mesotelioma maligno. Un médico extrae una muestra de tejido para que un patólogo la examine bajo un microscopio . Una biopsia se puede realizar de diferentes maneras, dependiendo de dónde se encuentre el área anormal. Si el cáncer está en el pecho, el médico puede realizar una toracoscopia . En este procedimiento, el médico hace un pequeño corte a través de la pared torácica e introduce un tubo delgado e iluminado llamado toracoscopio en el pecho entre dos costillas. La toracoscopia le permite al médico mirar dentro del pecho y obtener muestras de tejido. Alternativamente, el cirujano cardiotorácico puede abrir directamente el pecho ( toracotomía ). Si el cáncer está en el abdomen, el médico puede realizar una laparoscopia . Para obtener tejido para examinar, el médico hace una pequeña incisión en el abdomen e inserta un instrumento especial en la cavidad abdominal. Si estos procedimientos no producen suficiente tejido, puede ser necesario un procedimiento quirúrgico abierto . [ cita requerida ]
Inmunoquímica
Los estudios inmunohistoquímicos desempeñan un papel importante para el patólogo a la hora de diferenciar el mesotelioma maligno de los tumores que imitan a los neoplásicos, como el cáncer de mama o de pulmón que ha hecho metástasis en la pleura. Hay numerosas pruebas y paneles disponibles, pero ninguna prueba es perfecta para distinguir el mesotelioma del carcinoma o incluso para distinguir entre benigno y maligno. Los marcadores positivos indican la presencia de mesotelioma; si otros marcadores son positivos, pueden indicar otro tipo de cáncer, como el adenocarcinoma de mama o de pulmón. La calretinina es un marcador especialmente importante para distinguir el mesotelioma del cáncer de mama o de pulmón metastásico. [12]
| Positivo | Negativo |
| EMA ( antígeno de membrana epitelial ) en una distribución membranosa | CEA ( antígeno carcinoembrionario ) [12] |
| WT1 ( tumor de Wilms 1) [12] | AcM B72.3 |
| Calretinina [12] | MOC-3 1 |
| Mesotelina [12] | CD15 |
| Citoqueratina 5 [12] | Ber-EP4 |
| HBME-1 (célula mesotelial humana 1) | TTF-1 ( factor de transcripción tiroideo-1 ) [12] |
| Podoplanina (PDPN) [12] | Claudin-4 [12] |
| Osteopontina [12] | Molécula de adhesión de células epiteliales (EpCAM) [12] |
| Receptor de estrógeno alfa [12] | |
| Mamoglobina [12] |
Subtipos
Existen tres subtipos histológicos principales de mesotelioma maligno: epitelioide, sarcomatoso y bifásico. El mesotelioma epitelioide y bifásico representa aproximadamente el 75-95% de los mesoteliomas y se ha caracterizado bien histológicamente, mientras que el mesotelioma sarcomatoso no se ha estudiado en profundidad. La mayoría de los mesoteliomas expresan altos niveles de citoqueratina 5 independientemente del subtipo. [12]
El mesotelioma epitelioide se caracteriza por niveles elevados de calretinina. [12]
El mesotelioma sarcomatoso no expresa niveles elevados de calretinina. [12]
Se han descrito otros subtipos morfológicos: [ cita requerida ]
- Desmoplásico
- Limpiar celda
- Deciduoide
- Adenomatoide
- Glandular
- Mucohialina
- Metaplasia cartilaginosa y ósea
- Linfohistiocítico
Diagnóstico diferencial
- Adenocarcinoma metastásico
- Sarcoma pleural
- Sarcoma sinovial
- Timoma
- Carcinoma renal de células claras metastásico
- Osteosarcoma metastásico
Puesta en escena
La estadificación del mesotelioma se basa en la recomendación del Grupo Internacional de Interés en Mesotelioma. [68] Se realiza la clasificación TNM del tumor primario, la afectación de los ganglios linfáticos y la metástasis a distancia . El mesotelioma se clasifica en estadios Ia-IV (uno-A a cuatro) según el estado TNM. [68] [69]
Prevención
El mesotelioma se puede prevenir en la mayoría de los casos evitando la exposición al amianto. El Instituto Nacional de Seguridad y Salud Ocupacional de los Estados Unidos mantiene un límite de exposición recomendado de 0,1 fibras de amianto por centímetro cúbico. [26]
Cribado
No existe un protocolo universalmente acordado para la detección de personas que han estado expuestas al amianto. Las pruebas de detección podrían diagnosticar el mesotelioma antes que los métodos convencionales, mejorando así las perspectivas de supervivencia de los pacientes. El nivel sérico de osteopontina podría ser útil para la detección del mesotelioma en personas expuestas al amianto. El nivel de proteína soluble relacionada con la mesotelina está elevado en el suero de aproximadamente el 75% de los pacientes en el momento del diagnóstico y se ha sugerido que podría ser útil para la detección. [70] Los médicos han comenzado a probar el ensayo Mesomark , que mide los niveles de proteínas solubles relacionadas con la mesotelina (SMRP) liberadas por las células del mesotelioma. [71]
Tratamiento
El mesotelioma es generalmente resistente a la radioterapia y a la quimioterapia. [72] La supervivencia a largo plazo y la curación son extremadamente raras. [12] El tratamiento del mesotelioma maligno en estadios más tempranos tiene un mejor pronóstico. El comportamiento clínico de la malignidad se ve afectado por varios factores, entre ellos la superficie mesotelial continua de la cavidad pleural que favorece la metástasis local a través de células exfoliadas, la invasión del tejido subyacente y otros órganos dentro de la cavidad pleural, y el período de latencia extremadamente largo entre la exposición al asbesto y el desarrollo de la enfermedad. El subtipo histológico y la edad y el estado de salud del paciente también ayudan a predecir el pronóstico. La histología epitelioide responde mejor al tratamiento y tiene una ventaja de supervivencia sobre la histología sarcomatoide. [73]
No se conoce la eficacia de la radioterapia en comparación con la quimioterapia o la cirugía para el mesotelioma pleural maligno. [74]
Cirugía
La cirugía, por sí sola, ha demostrado ser decepcionante. En una serie grande, la supervivencia media con cirugía (incluyendo neumonectomía extrapleural ) fue de sólo 11,7 meses. [75] Sin embargo, la investigación indica un éxito variado cuando se utiliza en combinación con radiación y quimioterapia (Duke, 2008), o con una de estas últimas. [76] Una pleurectomía/decorticación es la cirugía más común, en la que se elimina el revestimiento del tórax. Menos común es una neumonectomía extrapleural (EPP), en la que se eliminan el pulmón, el revestimiento del interior del tórax, el hemidiafragma y el pericardio . [ cita requerida ] En el mesotelioma pericárdico localizado, la pericardectomía puede ser curativa; cuando el tumor ha hecho metástasis, la pericardectomía es una opción de cuidados paliativos. A menudo no es posible extirpar todo el tumor. [11]
Radiación
En el caso de los pacientes con enfermedad localizada que pueden tolerar una cirugía radical, se puede administrar radioterapia en el posoperatorio como tratamiento de consolidación. Se trata todo el hemitórax con radioterapia, que a menudo se administra simultáneamente con quimioterapia. La administración de radioterapia y quimioterapia después de una cirugía radical ha permitido prolongar la expectativa de vida en poblaciones seleccionadas de pacientes. También puede inducir efectos secundarios graves, incluida la neumonitis mortal. [77] Como parte de un enfoque curativo del mesotelioma, la radioterapia se aplica comúnmente en los sitios de inserción del drenaje torácico , con el fin de prevenir el crecimiento del tumor a lo largo del trayecto en la pared torácica. [ cita requerida ]
Aunque el mesotelioma es generalmente resistente al tratamiento curativo con radioterapia sola, a veces se utilizan regímenes de tratamiento paliativo para aliviar los síntomas que surgen del crecimiento del tumor, como la obstrucción de un vaso sanguíneo importante. Nunca se ha demostrado que la radioterapia, cuando se administra sola con intención curativa, mejore la supervivencia del mesotelioma. La dosis de radiación necesaria para tratar el mesotelioma que no se ha extirpado quirúrgicamente estaría más allá de la tolerancia humana. [ cita requerida ] La radioterapia tiene cierta utilidad en el mesotelioma pericárdico. [ 11 ]
Quimioterapia
La quimioterapia es el único tratamiento para el mesotelioma que ha demostrado mejorar la supervivencia en ensayos controlados y aleatorizados. El estudio de referencia publicado en 2003 por Vogelzang y colegas comparó la quimioterapia con cisplatino solo con una combinación de quimioterapia con cisplatino y pemetrexed (nombre comercial Alimta) en pacientes que no habían recibido quimioterapia para el mesotelioma pleural maligno anteriormente y no eran candidatos a una cirugía "curativa" más agresiva. [78] Este ensayo fue el primero en informar una ventaja de supervivencia de la quimioterapia en el mesotelioma pleural maligno, mostrando una mejora estadísticamente significativa en la supervivencia media de 10 meses en los pacientes tratados con cisplatino solo a 13,3 meses en el grupo de pacientes tratados con cisplatino en combinación con pemetrexed y que también recibieron suplementos de folato y vitamina B 12 . La mayoría de los pacientes del ensayo recibieron suplementos vitamínicos y los efectos secundarios relacionados con el pemetrexed fueron significativamente menores en los pacientes que recibieron pemetrexed cuando también recibieron 500 mcg de folato oral diario y 1000 mcg de vitamina B 12 intramuscular cada 9 semanas en comparación con los pacientes que recibieron pemetrexed sin suplementos vitamínicos. La tasa de respuesta objetiva aumentó del 20% en el grupo de cisplatino al 46% en el grupo de combinación con pemetrexed. Algunos efectos secundarios como náuseas y vómitos, estomatitis y diarrea fueron más comunes en el grupo de combinación con pemetrexed, pero solo afectaron a una minoría de pacientes y, en general, la combinación de pemetrexed y cisplatino fue bien tolerada cuando los pacientes recibieron suplementos vitamínicos; tanto la calidad de vida como las pruebas de función pulmonar mejoraron en el grupo de combinación con pemetrexed. En febrero de 2004, la Administración de Alimentos y Medicamentos de los Estados Unidos (FDA) aprobó el pemetrexed para el tratamiento del mesotelioma pleural maligno. [79] Sin embargo, todavía hay preguntas sin respuesta sobre el uso óptimo de la quimioterapia, incluyendo cuándo iniciar el tratamiento y el número óptimo de ciclos a administrar. [ cita requerida ] El cisplatino y el pemetrexed juntos dan a los pacientes una supervivencia media de 12,1 meses. [12]
El cisplatino en combinación con raltitrexed ha demostrado una mejora en la supervivencia similar a la descrita para pemetrexed en combinación con cisplatino, pero raltitrexed ya no está disponible comercialmente para esta indicación. Para los pacientes que no pueden tolerar pemetrexed, el cisplatino en combinación con gemcitabina o vinorelbina es una alternativa, o vinorelbina por sí sola, aunque no se ha demostrado un beneficio en la supervivencia con estos fármacos. Para los pacientes en los que no se puede utilizar cisplatino, se puede sustituir por carboplatino , pero los datos no aleatorizados han demostrado tasas de respuesta más bajas y tasas altas de toxicidad hematológica para las combinaciones basadas en carboplatino, aunque con cifras de supervivencia similares a las de los pacientes que reciben cisplatino. [80] El cisplatino en combinación con premetrexed disódico, ácido fólico y vitamina B12 también puede mejorar la supervivencia de las personas que están respondiendo a la quimioterapia. [81]
En enero de 2009, la FDA de los Estados Unidos aprobó el uso de terapias convencionales como la cirugía en combinación con radiación y/o quimioterapia en el mesotelioma en estadio I o II después de que una investigación realizada a nivel nacional por la Universidad de Duke concluyera un aumento de casi 50 puntos en las tasas de remisión. [ cita requerida ]
En el mesotelioma pericárdico, la quimioterapia (normalmente adriamicina o cisplatino) se utiliza principalmente para reducir el tamaño del tumor y no es curativa. [11]
Inmunoterapia
Los regímenes de tratamiento que incluyen inmunoterapia han dado resultados variables. Por ejemplo, se ha descubierto que la inoculación intrapleural de Bacillus Calmette-Guérin (BCG) en un intento de reforzar la respuesta inmunitaria no aporta ningún beneficio al paciente (aunque puede beneficiar a los pacientes con cáncer de vejiga ). Las células de mesotelioma demostraron ser susceptibles a la lisis in vitro por las células LAK tras la activación por interleucina-2 (IL-2), pero los pacientes sometidos a esta terapia en particular experimentaron importantes efectos secundarios. De hecho, este ensayo se suspendió en vista de los niveles inaceptablemente altos de toxicidad de IL-2 y la gravedad de los efectos secundarios, como fiebre y caquexia. No obstante, otros ensayos que incluían interferón alfa han resultado más alentadores, ya que el 20% de los pacientes experimentaron una reducción de más del 50% de la masa tumoral combinada con efectos secundarios mínimos. [ cita requerida ]
En octubre de 2020, la FDA aprobó la combinación de nivolumab (Opdivo) con ipilimumab (Yervoy) para el tratamiento de primera línea de adultos con mesotelioma pleural maligno (MPM) que no se puede extirpar mediante cirugía. [79] Nivolumab e ipilimumab son anticuerpos monoclonales que, cuando se combinan, disminuyen el crecimiento del tumor al mejorar la función de las células T. [79] La terapia combinada se evaluó a través de un ensayo aleatorizado y abierto en el que los participantes que recibieron nivolumab en combinación con ipilimumab sobrevivieron una mediana de 18,1 meses, mientras que los participantes que se sometieron a quimioterapia sobrevivieron una mediana de 14,1 meses. [79]
Quimioterapia intratorácica hipertérmica
La quimioterapia intratorácica hipertérmica se utiliza junto con la cirugía, [82] [83] incluso en pacientes con mesotelioma pleural maligno. [84] El cirujano extirpa la mayor cantidad posible del tumor y luego administra directamente un agente quimioterapéutico, calentado a una temperatura de entre 40 y 48 °C, en el abdomen. El líquido se perfunde durante 60 a 120 minutos y luego se drena. Luego se administran altas concentraciones de medicamentos seleccionados en la cavidad pleural. Calentar el tratamiento de quimioterapia aumenta la penetración de los medicamentos en los tejidos. Además, el calentamiento en sí mismo daña las células malignas más que las células normales. [ cita requerida ]
Terapia multimodal
La terapia multimodal , que incluye un enfoque combinado de cirugía, radiación o terapia fotodinámica y quimioterapia, no se recomienda para la práctica de rutina para el tratamiento del mesotelioma pleural maligno. [85] La efectividad y seguridad de la terapia multimodal no está clara (no se han realizado suficientes investigaciones) y un ensayo clínico ha sugerido un posible aumento del riesgo de efectos adversos. [85]
Grandes series de estudios que han examinado el tratamiento multimodal han demostrado solo una modesta mejoría en la supervivencia (supervivencia media de 14,5 meses y solo el 29,6% sobrevive 2 años). [75] Reducir el volumen del tumor con cirugía citorreductora es clave para prolongar la supervivencia. Se han desarrollado dos cirugías: neumonectomía extrapleural y pleurectomía/ decorticación . Las indicaciones para realizar estas operaciones son únicas. La elección de la operación depende, en particular, del tamaño del tumor del paciente. Esta es una consideración importante porque el volumen del tumor se ha identificado como un factor pronóstico en el mesotelioma. [86] La pleurectomía/decorticación preserva el pulmón subyacente y se realiza en pacientes con enfermedad en etapa temprana cuando la intención es eliminar todo el tumor visible macroscópicamente (resección completa macroscópica), no simplemente paliación. [87] La neumonectomía extrapleural es una operación más extensa que implica la resección de las pleuras parietal y visceral , el pulmón subyacente, el diafragma ipsilateral (del mismo lado) y el pericardio ipsilateral . Esta operación está indicada para un subconjunto de pacientes con tumores más avanzados, que pueden tolerar una neumonectomía . [88]
Pronóstico
El mesotelioma suele tener un mal pronóstico. La supervivencia típica a pesar de la cirugía es de entre 12 y 21 meses, dependiendo del estadio de la enfermedad en el momento del diagnóstico, y aproximadamente el 7,5 % de los pacientes sobrevive durante 5 años. [89]
Las mujeres, los jóvenes, las personas con cánceres en estadios bajos y las personas con cánceres epitelioides tienen mejores pronósticos. [12] Los factores pronósticos negativos incluyen histología sarcomatoide o bifásica, recuentos elevados de plaquetas (por encima de 400.000), edad superior a 50 años, recuentos de glóbulos blancos superiores a 15,5, niveles bajos de glucosa en el líquido pleural, niveles bajos de albúmina y niveles elevados de fibrinógeno. Se están investigando varios marcadores como factores pronósticos, incluido el grado nuclear y la proteína C reactiva sérica. La supervivencia a largo plazo es poco frecuente. [64]
El mesotelioma pericárdico tiene un tiempo de supervivencia medio de 10 meses. [11]
En el mesotelioma peritoneal, la alta expresión de la proteína WT-1 indica un peor pronóstico. [12]
Epidemiología
Aunque las tasas de incidencia notificadas han aumentado en los últimos 20 años, el mesotelioma sigue siendo un cáncer relativamente raro. La tasa de incidencia varía de un país a otro, desde una tasa baja de menos de 1 por 1.000.000 en Túnez y Marruecos, hasta la tasa más alta en Gran Bretaña, Australia y Bélgica: 30 por 1.000.000 por año. [90] A modo de comparación, las poblaciones con altos niveles de tabaquismo pueden tener una incidencia de cáncer de pulmón de más de 1.000 por 1.000.000. La incidencia del mesotelioma maligno actualmente varía de aproximadamente 7 a 40 por 1.000.000 en las naciones occidentales industrializadas, dependiendo de la cantidad de exposición al amianto de las poblaciones durante las últimas décadas. [91] La incidencia mundial se estima en 1-6 por 1.000.000. [12]
La incidencia del mesotelioma es menor que la de la asbestosis debido al mayor tiempo que tarda en desarrollarse; debido al cese del uso del asbesto en los países desarrollados, se espera que la incidencia del mesotelioma disminuya. [26] Se espera que la incidencia continúe aumentando en los países en desarrollo debido al uso continuo del asbesto. [12] El mesotelioma se presenta con mayor frecuencia en hombres que en mujeres y el riesgo aumenta con la edad, pero esta enfermedad puede aparecer en hombres o mujeres a cualquier edad. Aproximadamente entre una quinta parte y una tercera parte de todos los mesoteliomas son peritoneales. [ cita requerida ] Menos del 5% de los mesoteliomas son pericárdicos. La prevalencia del mesotelioma pericárdico es inferior al 0,002%; es más común en hombres que en mujeres. Por lo general, se presenta en personas de entre 50 y 70 años. [11] [92]
Entre 1940 y 1979, aproximadamente 27,5 millones de personas estuvieron expuestas ocupacionalmente al asbesto en los Estados Unidos. [93] Entre 1973 y 1984, la incidencia del mesotelioma pleural entre los varones caucásicos aumentó un 300%. Desde 1980 hasta finales de los años 1990, la tasa de mortalidad por mesotelioma en los EE. UU. aumentó de 2000 por año a 3000, y los hombres tenían cuatro veces más probabilidades de contraerlo que las mujeres. [ cita requerida ] Más del 80% de los mesoteliomas son causados por la exposición al asbesto. [12]
La incidencia del mesotelioma peritoneal es de 0,5 a 3,0 por millón por año en hombres y de 0,2 a 2,0 por millón por año en mujeres. [94]
Reino Unido
El mesotelioma representa menos del 1% de todos los cánceres diagnosticados en el Reino Unido (alrededor de 2.600 personas fueron diagnosticadas con la enfermedad en 2011) y es la decimoséptima causa más común de muerte por cáncer (alrededor de 2.400 personas murieron en 2012). [95]
Historia
Las primeras conexiones entre la exposición al asbesto y el mesotelioma se identificaron en la década de 1960, con evidencia significativa que surgió en Sudáfrica. [96] En los Estados Unidos, la fabricación de asbesto se detuvo en 2002. La exposición al asbesto pasó así de los trabajadores de las fábricas textiles de asbesto, la fabricación de productos de fricción, la fabricación de tuberías de cemento y la fabricación e instalación de material aislante a los trabajadores de mantenimiento en edificios que contienen asbesto. [26]
Sociedad y cultura
Casos notables
El mesotelioma, aunque es poco común, ha tenido varios pacientes notables:
- Malcolm McLaren , músico y manager de la banda de punk rock Sex Pistols , fue diagnosticado con mesotelioma peritoneal en octubre de 2009 y murió el 8 de abril de 2010 en Suiza. [97]
- Steve McQueen , actor estadounidense, fue diagnosticado con mesotelioma peritoneal el 22 de diciembre de 1979. No le ofrecieron cirugía ni quimioterapia porque los médicos consideraron que el cáncer estaba demasiado avanzado. Posteriormente, McQueen buscó tratamientos alternativos en clínicas de México. Murió de un ataque cardíaco el 7 de noviembre de 1980, en Juárez, México , después de una cirugía de cáncer. Es posible que haya estado expuesto al asbesto mientras servía con los Marines de los EE. UU. cuando era un adulto joven (el asbesto se usaba comúnmente para aislar las tuberías de los barcos) o por su uso como material aislante en los trajes de carreras de automóviles (McQueen era un ávido piloto de carreras y fanático). [98]
- Mickie Most , productor de discos, murió de mesotelioma peritoneal en mayo de 2003; sin embargo, se ha cuestionado si esto se debió a la exposición al asbesto. [99]
- Warren Zevon , músico estadounidense, fue diagnosticado con mesotelioma pleural en 2002 y murió el 7 de septiembre de 2003. Se cree que esto fue causado por la exposición infantil al aislamiento de asbesto en el ático de la tienda de su padre. [100]
- David Martin , marino y político australiano, murió el 10 de agosto de 1990 de mesotelioma pleural. Se cree que esto fue causado por su exposición al amianto en buques militares durante su carrera en la Marina Real Australiana. [101]
- Paul Kraus , diagnosticado en 1997, es considerado el sobreviviente de mesotelioma que vive más tiempo en el mundo (hasta 2017). [102]
- FW De Klerk , político sudafricano retirado, fue diagnosticado con mesotelioma el 19 de marzo de 2021 y murió en noviembre de 2021. [103]
- Paul Gleason , actor estadounidense, murió el 27 de mayo de 2006, apenas unos meses después del diagnóstico. [104]
- Merlin Olsen , jugador de fútbol americano, locutor y actor, murió el 11 de marzo de 2010.
Aunque la expectativa de vida con esta enfermedad es típicamente limitada, hay sobrevivientes notables. En julio de 1982, Stephen Jay Gould , un paleontólogo muy respetado, fue diagnosticado con mesotelioma peritoneal . Después de su diagnóstico, Gould escribió "La mediana no es el mensaje", [105] en el que argumentó que las estadísticas como la supervivencia media son abstracciones útiles, no el destino. Gould vivió otros 20 años, y finalmente sucumbió a un cáncer no relacionado con su mesotelioma.
Cuestiones jurídicas
Algunas personas que estuvieron expuestas al asbesto han recibido daños y perjuicios por una enfermedad relacionada con el asbesto, incluido el mesotelioma. La compensación a través de fondos para el asbesto o demandas colectivas es un tema importante en las prácticas legales relacionadas con el mesotelioma. [ cita requerida ]
Las primeras demandas contra los fabricantes de amianto se iniciaron en 1929. Desde entonces, se han presentado muchas demandas contra los fabricantes y los empleadores de amianto por no haber implementado medidas de seguridad después de que se conocieran los vínculos entre el amianto, la asbestosis y el mesotelioma (algunos informes parecen situar esto en 1898). La responsabilidad resultante de la gran cantidad de demandas y personas afectadas ha alcanzado miles de millones de dólares. [106] Las cantidades y el método de asignación de la compensación han sido la fuente de muchos casos judiciales, que llegaron hasta la Corte Suprema de los Estados Unidos, y de intentos gubernamentales de resolver casos existentes y futuros. Sin embargo, hasta la fecha, el Congreso de los Estados Unidos no ha intervenido y no existen leyes federales que regulen la compensación por amianto. [107] En 2013, la "Ley de Transparencia en las Reclamaciones por Amianto (FACT) de 2013" fue aprobada por la Cámara de Representantes de los Estados Unidos y se envió al Senado de los Estados Unidos, donde fue remitida al Comité Judicial del Senado. [108] Como el Senado no votó sobre el proyecto antes de que terminara el 113.º Congreso, el proyecto quedó en el comité y fue revivido en el 114.º Congreso, donde aún no ha sido presentado ante la Cámara para su votación. [109] [ Necesita actualización ]
Historia
La primera demanda contra los fabricantes de amianto se presentó en 1929. Las partes llegaron a un acuerdo y, como parte del mismo, los abogados acordaron no presentar más demandas. En 1960, un artículo publicado por Wagner et al. fue fundamental para establecer el mesotelioma como una enfermedad derivada de la exposición al amianto. [110] El artículo hacía referencia a más de 30 estudios de casos de personas que habían tenido mesotelioma en Sudáfrica. Algunas exposiciones fueron transitorias y otras eran trabajadores de minas. Antes del uso de técnicas avanzadas de microscopía, el mesotelioma maligno se diagnosticaba a menudo como una forma variante del cáncer de pulmón. [111] En 1962, McNulty informó del primer caso diagnosticado de mesotelioma maligno en un trabajador australiano del amianto. [112] El trabajador había trabajado en la fábrica de la mina de amianto de Wittenoom desde 1948 hasta 1950. [ cita requerida ]
En la ciudad de Wittenoom , los desechos mineros que contenían amianto se utilizaron para cubrir patios de escuelas y parques infantiles. En 1965, un artículo del British Journal of Industrial Medicine estableció que las personas que vivían en los barrios de fábricas y minas de amianto, pero que no trabajaban en ellas, habían contraído mesotelioma. [ cita requerida ]
A pesar de las pruebas de que el polvo asociado con la extracción y molienda de amianto causa enfermedades relacionadas con el amianto, la extracción comenzó en Wittenoom en 1943 y continuó hasta 1966. En 1974, las primeras advertencias públicas sobre los peligros del amianto azul se publicaron en un artículo de portada titulado "¿Es este asesino en su hogar?" en la revista Bulletin de Australia . En 1978, el Gobierno de Australia Occidental decidió desmantelar la ciudad de Wittenoom, tras la publicación de un folleto del Departamento de Salud, "El peligro para la salud en Wittenoom", que contenía los resultados de un muestreo de aire y una evaluación de la información médica mundial. [113]
En 1979, se emitieron los primeros recursos por negligencia relacionados con Wittenoom contra CSR y su subsidiaria ABA, y se formó la Sociedad de Enfermedades Provocadas por Amianto para representar a las víctimas de Wittenoom. [ cita requerida ]
En Leeds , Inglaterra, el desastre del amianto en Armley dio lugar a varios procesos judiciales contra Turner & Newall , en los que los residentes locales que contrajeron mesotelioma exigieron una indemnización debido a la contaminación por amianto procedente de la fábrica de la empresa. Un caso notable fue el de June Hancock, que contrajo la enfermedad en 1993 y murió en 1997. [114]
Investigación
La proteína WT-1 está sobreexpresada en el mesotelioma y se está investigando como un objetivo potencial para medicamentos. [12]
Existen dos microARN de alta confianza que podrían servir como biomarcadores de exposición al asbesto y mesotelioma maligno. Se necesitan estudios de validación para evaluar su relevancia. [ cita requerida ]
Se han identificado algunos factores de crecimiento y, como resultado, han surgido terapias dirigidas para ayudar a frenar el crecimiento de anomalías oncogénicas. Por ejemplo, el bevacizumab, un anticuerpo monoclonal humanizado, está dirigido al receptor del factor de crecimiento endotelial vascular (VEGFR). [115]
Referencias
- ^ abcde «Tratamiento del mesotelioma maligno: versión para pacientes (PDQ®)». NCI. 4 de septiembre de 2015. Archivado desde el original el 5 de abril de 2016. Consultado el 3 de abril de 2016 .
- ^ abcde Kondola S, Manners D, Nowak AK (junio de 2016). "Mesotelioma pleural maligno: una actualización sobre el diagnóstico y las opciones de tratamiento". Avances terapéuticos en enfermedades respiratorias . 10 (3): 275–288. doi :10.1177/1753465816628800. PMC 5933604. PMID 26873306 .
- ^ abcdefghijklmn Robinson BM (noviembre de 2012). "Mesotelioma pleural maligno: una perspectiva epidemiológica". Anales de cirugía cardiotorácica . 1 (4): 491–496. doi :10.3978/j.issn.2225-319X.2012.11.04. PMC 3741803 . PMID 23977542.
- ^ Vilchez RA, Butel JS (julio de 2004). "El virus simio 40, un patógeno humano emergente, y su papel en el cáncer". Clinical Microbiology Reviews . 17 (3): 495–508. doi :10.1128/CMR.17.3.495-508.2004. PMC 452549 . PMID 15258090.
- ^ ab Whittemore AS (2006). Epidemiología y prevención del cáncer (3.ª ed.). Oxford: Oxford University Press. pág. 669. ISBN 978-0-19-974797-9.
- ^ abc «Tratamiento del mesotelioma maligno: versión para pacientes (PDQ®)». NCI . 4 de septiembre de 2015. Archivado desde el original el 5 de abril de 2016 . Consultado el 3 de abril de 2016 .
- ^ ab "Incidencia SEER ajustada por edad y tasas de mortalidad en EE. UU. y supervivencia relativa a 5 años (porcentaje) por sitio de cáncer primario, sexo y período de tiempo" (PDF) . NCI . Archivado (PDF) del original el 6 de septiembre de 2015 . Consultado el 3 de abril de 2016 .
- ^ abc Vos T, Allen C, Arora M, Barber RM, Bhutta ZA, Brown A, et al. (Colaboradores de incidencia y prevalencia de enfermedades y lesiones del GBD 2015) (octubre de 2016). "Incidencia, prevalencia y años vividos con discapacidad a nivel mundial, regional y nacional para 310 enfermedades y lesiones, 1990-2015: un análisis sistemático para el Estudio de la carga mundial de enfermedades de 2015". Lancet . 388 (10053): 1545–1602. doi :10.1016/S0140-6736(16)31678-6. PMC 5055577 . PMID 27733282.
- ^ ab Wang H, Naghavi M, Allen C, Barber RM, Bhutta ZA, Carter A, et al. (Colaboradores de GBD 2015 Mortality and Causes of Death) (octubre de 2016). "Esperanza de vida global, regional y nacional, mortalidad por todas las causas y mortalidad por causas específicas para 249 causas de muerte, 1980-2015: un análisis sistemático para el Estudio de la Carga Global de Enfermedades 2015". Lancet . 388 (10053): 1459–1544. doi :10.1016/s0140-6736(16)31012-1. PMC 5388903 . PMID 27733281.
- ^ "Mesotelioma maligno: versión para pacientes". NCI . Enero de 1980. Archivado desde el original el 6 de abril de 2016 . Consultado el 3 de abril de 2016 .
- ^ abcdefghijk Sardar MR, Kuntz C, Patel T, Saeed W, Gnall E, Imaizumi S, et al. (2012). "Caso único de mesotelioma pericárdico primario y revisión de la literatura". Revista del Instituto del Corazón de Texas . 39 (2): 261–264. PMC 3384041 . PMID 22740748.
- ^ abcdefghijklmnopqrstu vwxyz aa ab ac Panou V, Vyberg M, Weinreich UM, Meristoudis C, Falkmer UG, Røe OD (junio de 2015). "Los biomarcadores establecidos y futuros del mesotelioma pleural maligno". Cancer Treatment Reviews . 41 (6): 486–495. doi :10.1016/j.ctrv.2015.05.001. PMID 25979846.
- ^ abcdef Gulati M, Redlich CA (marzo de 2015). "Asbestosis y causas ambientales de neumonía intersticial habitual". Current Opinion in Pulmonary Medicine . 21 (2): 193–200. doi :10.1097/MCP.0000000000000144. PMC 4472384 . PMID 25621562.
- ^ "¿Cuáles son las estadísticas clave sobre el mesotelioma maligno?". Sociedad Estadounidense del Cáncer . 17 de febrero de 2016. Archivado desde el original el 8 de abril de 2016. Consultado el 3 de abril de 2016 .
- ^ abc Barreiro TJ, Katzman PJ (diciembre de 2006). "Mesotelioma maligno: presentación y revisión de un caso". Revista de la Asociación Estadounidense de Osteopatía . 106 (12): 699–704. PMID 17242414.
- ^ Raza A, Huang WC, Takabe K (septiembre de 2014). "Avances en el tratamiento del mesotelioma peritoneal". Revista Mundial de Gastroenterología . 20 (33): 11700–11712. doi : 10.3748/wjg.v20.i33.11700 . PMC 4155360 . PMID 25206274.
- ^ Cedrés S, Fariñas L, Stejpanovic N, Martinez P, Martinez A, Zamora E, et al. (abril de 2013). "Metástasis óseas con compresión de la raíz nerviosa como complicación tardía en pacientes con mesotelioma pleural epitelial". Journal of Thoracic Disease . 5 (2): E35–E37. doi :10.3978/j.issn.2072-1439.2012.07.08. PMC 3621936 . PMID 23585954.
- ^ "Base de datos EBSCO". Archivado desde el original el 12 de mayo de 2012.verificado por URAC ; consultado desde el Hospital Mount Sinai, Nueva York
- ^ "Estudio afirma que los nanotubos de carbono son tan peligrosos como el amianto". Scientific American .
- ^ Attanoos RL, Churg A, Galateau-Salle F, Gibbs AR, Roggli VL (junio de 2018). "Mesotelioma maligno y sus causas no relacionadas con el amianto". Archivos de patología y medicina de laboratorio . 142 (6): 753–760. doi : 10.5858/arpa.2017-0365-RA . PMID 29480760.
- ^ ab Constantopoulos SH (octubre de 2008). "Mesotelioma ambiental asociado con amianto tremolita: lecciones de las experiencias de Turquía, Grecia, Córcega, Nueva Caledonia y Chipre". Toxicología y farmacología regulatorias . 52 (1 Suppl): S110–S115. doi :10.1016/j.yrtph.2007.11.001. PMID 18171598.
- ^ abc Weissman D, Kiefer M (22 de noviembre de 2011). "Erionita: un peligro emergente en América del Norte". Instituto Nacional de Seguridad y Salud Ocupacional. Archivado desde el original el 5 de septiembre de 2015.
- ^ Dogan U (2003). "Mesotelioma en pueblos de Capadocia". Entorno interior y construido . 12 (6): 367–375. doi :10.1177/1420326X03039065. ISSN 1420-326X. S2CID 110334356.
- ^ Carbone M, Emri S, Dogan AU, Steele I, Tuncer M, Pass HI, et al. (febrero de 2007). "Una epidemia de mesotelioma en Capadocia: avances científicos y resultados sociales inesperados". Nature Reviews. Cancer . 7 (2): 147–154. doi :10.1038/nrc2068. PMID 17251920. S2CID 9440201.
- ^ "Asbestos in Drinking-water: Background document for development of WHO Guidelines for Drinking-water quality" (PDF) . 2003 . Consultado el 30 de julio de 2019 .
- ^ abcdefgh "Fibras de amianto y otras partículas minerales alargadas: estado de la ciencia y hoja de ruta para la investigación". Boletín de inteligencia actual 62. 10 de julio de 2020. doi : 10.26616/NIOSHPUB2011159 .
- ^ Kanarek MS (septiembre de 2011). "Mesotelioma por amianto crisotilo: actualización". Anales de Epidemiología . 21 (9): 688–697. doi :10.1016/j.annepidem.2011.05.010. PMID 21820631.
- ^ abcde Roggli VL, Sharma A, Butnor KJ, Sporn T, Vollmer RT (2002). "Mesotelioma maligno y exposición ocupacional al asbesto: una correlación clinicopatológica de 1445 casos". Patología ultraestructural . 26 (2): 55–65. doi :10.1080/01913120252959227. PMID 12036093. S2CID 25204873.
- ^ Sporn TA, Roggli VL (2004). "Mesotelioma". En Roggli VL, Oury TD, Sporn TA (eds.). Patología de las enfermedades asociadas al amianto (2ª ed.). Saltador. pag. 104.
- ^ Gennaro V, Finkelstein MM, Ceppi M, Fontana V, Montanaro F, Perrotta A, et al. (marzo de 2000). "Mesotelioma y tumores pulmonares atribuibles al asbesto entre trabajadores del petróleo". American Journal of Industrial Medicine . 37 (3): 275–282. doi :10.1002/(SICI)1097-0274(200003)37:3<275::AID-AJIM5>3.0.CO;2-I. PMID 10642417.
- ^ Selikoff IJ (1986). "Enfermedades respiratorias ocupacionales". Salud pública y medicina preventiva (12.ª ed.). Appleton-Century-Crofts. pág. 532.
- ^ Henderson DW, Rödelsperger K, Woitowitz HJ, Leigh J (diciembre de 2004). "Después de Helsinki: una revisión multidisciplinaria de la relación entre la exposición al asbesto y el cáncer de pulmón, con énfasis en los estudios publicados durante 1997-2004". Patología . 36 (6): 517–550. doi :10.1080/00313020400010955. PMID 15841689. S2CID 35280387.
- ^ "Documento del grupo de trabajo del NIOSH" (PDF) . Centros para el Control y la Prevención de Enfermedades de EE. UU . . 1980. Archivado desde el original (PDF) el 18 de junio de 2017.
- ^ Hillerdal G (agosto de 1999). "Mesotelioma: casos asociados con exposiciones no ocupacionales y a dosis bajas". Medicina ocupacional y ambiental . 56 (8): 505–513. doi :10.1136/oem.56.8.505. PMC 1757769. PMID 10492646 .
- ^ Peto J, Seidman H, Selikoff IJ (enero de 1982). "Mortalidad por mesotelioma en trabajadores del amianto: implicaciones para los modelos de carcinogénesis y evaluación de riesgos". British Journal of Cancer . 45 (1): 124–135. doi :10.1038/bjc.1982.15. PMC 2010947 . PMID 7059455.
- ^ Carbone M, Ly BH, Dodson RF, Pagano I, Morris PT, Dogan UA, et al. (enero de 2012). "Mesotelioma maligno: hechos, mitos e hipótesis". Journal of Cellular Physiology . 227 (1): 44–58. doi :10.1002/jcp.22724. PMC 3143206 . PMID 21412769.
- ^ Lanphear BP, Buncher CR (julio de 1992). "Período de latencia del mesotelioma maligno de origen ocupacional". Revista de Medicina del Trabajo . 34 (7): 718–721. PMID 1494965.
- ^ Burdorf A, Dahhan M, Swuste P (agosto de 2003). "Características ocupacionales de casos con enfermedades relacionadas con el amianto en los Países Bajos". Anales de Higiene Ocupacional . 47 (6): 485–492. doi : 10.1093/annhyg/meg062 . hdl : 1765/10196 . PMID: 12890657.
- ^ Glover J (abril de 1973). "Normas de higiene para el polvo de amianto amosita en suspensión en el aire. Comité de Normas de Higiene de la Sociedad Británica de Higiene Ocupacional". Anales de Higiene Ocupacional . 16 (1): 1–5. doi :10.1093/annhyg/16.1.1. PMID 4775386.
- ^ "Aprenda sobre el amianto". Agencia de Protección Ambiental de Estados Unidos. 5 de marzo de 2013. Archivado desde el original el 23 de junio de 2016. Consultado el 8 de julio de 2016 .
- ^ Berry G, Reid A, Aboagye-Sarfo P, de Klerk NH, Olsen NJ, Merler E, et al. (febrero de 2012). "Mesoteliomas malignos en antiguos mineros y molineros de crocidolita en Wittenoom (Australia Occidental) después de más de 50 años de seguimiento". British Journal of Cancer . 106 (5): 1016–1020. doi :10.1038/bjc.2012.23. PMC 3305966 . PMID 22315054.
- ^ "Protección de las familias de los trabajadores: una agenda de investigación del Grupo de trabajo para la protección de las familias de los trabajadores". Instituto Nacional de Seguridad y Salud Ocupacional. DHHS (NIOSH) . Mayo de 2002. Publicación n.º 2002-113. Archivado desde el original el 19 de junio de 2017.
- ^ Peipins LA, Lewin M, Campolucci S, Lybarger JA, Miller A, Middleton D, et al. (noviembre de 2003). "Anormalidades radiográficas y exposición a vermiculita contaminada con asbesto en la comunidad de Libby, Montana, EE. UU." Environmental Health Perspectives . 111 (14): 1753–1759. doi :10.1289/ehp.6346. PMC 1241719 . PMID 14594627.
- ^ "¿Dónde se puede encontrar amianto?". www.hse.gov.uk . Archivado desde el original el 2022-07-03 . Consultado el 2022-06-27 .
- ^ Testa JR, Cheung M, Pei J, Below JE, Tan Y, Sementino E, et al. (Agosto de 2011). "Las mutaciones de la línea germinal BAP1 predisponen al mesotelioma maligno". Genética de la Naturaleza . 43 (10): 1022-1025. doi :10.1038/ng.912. PMC 3184199 . PMID 21874000.
- ^ de Broaddus VC, Robinson BW (2010). "Capítulo 75". Murray & Nadel's Textbook of Respiratory Medicine (5.ª ed.). Saunders Elsevier. ISBN 978-1-4160-4710-0.
- ^ Holland-Frei (2010). "Capítulo 79". Medicina del cáncer (8.ª ed.). People's Medical Publishing House, EE. UU. ISBN 978-1-60795-014-1.
- ^ Enfermedades y trastornos pulmonares de Fishman (4.ª ed.). McGraw-Hill. 2008. pág. 1537. ISBN 978-0-07-145739-2.
- ^ Maitra A, Kumar V (2007). Patología básica de Robbins (8ª ed.). Saunders Elsevier. pag. 536.ISBN 978-1-4160-2973-1.
- ^ Mutsaers SE (septiembre de 2002). "Células mesoteliales: su estructura, función y papel en la reparación serosal". Respirology . 7 (3): 171–191. doi : 10.1046/j.1440-1843.2002.00404.x . PMID 12153683. S2CID 23976724.
- ^ Miserocchi G, Sancini G, Mantegazza F, Chiappino G (enero de 2008). "Vías de translocación de fibras de amianto inhaladas". Salud Ambiental . 7 (1): 4. Código Bib : 2008EnvHe...7....4M. doi : 10.1186/1476-069X-7-4 . PMC 2265277 . PMID 18218073.
- ^ "La respuesta del basurero al terrorismo: utilizar más amianto" (PDF) . Centro para los Medios y la Democracia: Prwatch.org. 2001. Archivado (PDF) desde el original el 16 de octubre de 2011. Consultado el 20 de agosto de 2010 .
- ^ Agencia para Sustancias Tóxicas y el Registro de Enfermedades (ATSDR) (2001). Perfil toxicológico del amianto (PDF) (Informe). Atlanta, GA: Departamento de Salud y Servicios Humanos de los Estados Unidos, Servicio de Salud Pública.
- ^ "Hoja informativa sobre neurofibromatosis". NINDS . 3 de febrero de 2016. Archivado desde el original el 23 de enero de 2018 . Consultado el 16 de abril de 2018 .
 Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público .
Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público . - ^ Chiosea S, Krasinskas A, Cagle PT, Mitchell KA, Zander DS, Dacic S (junio de 2008). "Importancia diagnóstica de la deleción homocigótica de 9p21 en mesoteliomas malignos". Patología moderna . 21 (6): 742–747. doi :10.1038/modpathol.2008.45. PMID 18327208. S2CID 7743919.
- ^ Sherr CJ (septiembre de 2006). "Divorcio entre ARF y p53: un caso pendiente". Nature Reviews. Cancer . 6 (9): 663–673. doi :10.1038/nrc1954. PMID 16915296. S2CID 29465278.
- ^ Wilbur B, ed. (2009). El mundo de la célula (7.ª ed.). San Francisco, C.
{{cite book}}: Mantenimiento de CS1: falta la ubicación del editor ( enlace ) - ^ "Oncogenes". Páginas de biología de Kimball . Archivado desde el original el 31 de diciembre de 2017.
- ^ Dehé PM, Gaillard PH (mayo de 2017). "Control de endonucleasas específicas de estructura para mantener la estabilidad del genoma". Nature Reviews Molecular Cell Biology . 18 (5): 315–330. doi :10.1038/nrm.2016.177. PMID 28327556. S2CID 24009279.
- ^ Shay JW, Wright WE. "¿Qué son los telómeros y la telomerasa?". The University of Texas Southwestern Medical Center at Dallas . Archivado desde el original el 10 de marzo de 2008.
- ^ Green D (2011). Medios para un fin: apoptosis y otros mecanismos de muerte celular . Cold Spring Harbor, Nueva York: Cold Spring Harbor Laboratory Press. ISBN 978-0-87969-888-1.[ página necesaria ]
- ^ Bueno, Stawiski, Goldstein, Durinck, De Rienzo (2016). "El análisis genómico exhaustivo del mesotelioma pleural maligno identifica mutaciones recurrentes, fusiones genéticas y alteraciones de empalme". Nature Genetics . 48 (4): 407–416. doi :10.1038/ng.3520. PMID 26928227. S2CID 13480173.
- ^ Mangiante, Alcala, Sexton-Oates, Di Genova, Gonzalez-Perez (2023). "El análisis multiómico del mesotelioma pleural maligno identifica ejes moleculares y perfiles tumorales especializados que impulsan la heterogeneidad intertumoral". Nature Genetics . 55 (4): 607–618. doi :10.1038/s41588-023-01321-1. PMC 10101853 . PMID 36928603. S2CID 257582839.
- ^ ab Davidson B (junio de 2015). "Factores pronósticos en el mesotelioma pleural maligno". Patología humana . 46 (6): 789–804. doi :10.1016/j.humpath.2015.02.006. PMID 25824607.
- ^ Reid G (junio de 2015). "MicroARN en mesotelioma: de supresores tumorales y biomarcadores a dianas terapéuticas". Journal of Thoracic Disease . 7 (6): 1031–1040. doi :10.3978/j.issn.2072-1439.2015.04.56. PMC 4466421 . PMID 26150916.
- ^ Comertpay S, Pastorino S, Tanji M, Mezzapelle R, Strianese O, Napolitano A, et al. (diciembre de 2014). "Evaluación del origen clonal del mesotelioma maligno". Journal of Translational Medicine . 12 : 301. doi : 10.1186/s12967-014-0301-3 . PMC 4255423 . PMID 25471750.
- ^ Weder W (octubre de 2010). "Mesotelioma". Anales de Oncología . 21 (7): vii326–vii333. doi : 10.1093/annonc/mdq471 . PMID 20943637.
- ^ ab Ceresoli GL, Gridelli C, Santoro A (julio de 2007). "Tratamiento multidisciplinario del mesotelioma pleural maligno". The Oncologist . 12 (7): 850–863. doi : 10.1634/theoncologist.12-7-850 . PMID 17673616. S2CID 41668550.
- ^ Berzenji L, Van Schil PE, Carp L (octubre de 2018). "La octava clasificación TNM para el mesotelioma pleural maligno". Investigación traslacional del cáncer de pulmón . 7 (5): 543–549. doi : 10.21037/tlcr.2018.07.05 . PMC 6204412. PMID 30450292 .
- ^ Robinson BW, Creaney J, Lake R, Nowak A, Musk AW, de Klerk N, et al. (julio de 2005). "Proteína soluble relacionada con la mesotelina: un análisis de sangre para el mesotelioma". Cáncer de pulmón . 49 (Supl. 1): S109–S111. doi :10.1016/j.lungcan.2005.03.020. PMID 15950789.
- ^ Beyer HL, Geschwindt RD, Glover CL, Tran L, Hellstrom I, Hellstrom KE, et al. (abril de 2007). "MESOMARK: una prueba potencial para el mesotelioma pleural maligno". Química clínica . 53 (4): 666–672. doi : 10.1373/clinchem.2006.079327 . PMID 17289801.
- ^ Milosevic V, Kopecka J, Salaroglio IC, Libener R, Napoli F, Izzo S, et al. (2020). "Los circuitos autocrinos Wnt/IL-1β/IL-8 controlan la quimiorresistencia en las células iniciadoras del mesotelioma mediante la inducción de ABCB5". Revista Internacional del Cáncer . 146 (1): 192–207. doi :10.1002/ijc.32419. hdl : 2318/1711962 . PMID 31107974. S2CID 160014053.
- ^ Haber SE, Haber JM (2011). "Mesotelioma maligno: un estudio clínico de 238 casos". Salud industrial . 49 (2): 166–172. doi : 10.2486/indhealth.MS1147 . PMID 21173534.
- ^ Chapman E, Berenstein EG, Diéguez M, Ortiz Z (julio de 2006). "Radioterapia para el mesotelioma pleural maligno". Base de Datos Cochrane de Revisiones Sistemáticas . 2010 (3): CD003880. doi :10.1002 / 14651858.CD003880.pub4. PMC 8746191. PMID 16856023. S2CID 26025607.
- ^ ab Borasio P, Berruti A, Billé A, Lausi P, Levra MG, Giardino R, et al. (febrero de 2008). "Mesotelioma pleural maligno: características clinicopatológicas y de supervivencia en una serie consecutiva de 394 pacientes". Revista Europea de Cirugía Cardiotorácica . 33 (2): 307–313. doi : 10.1016/j.ejcts.2007.09.044 . PMID 18164622.
- ^ Tilleman RT, Richards WG (2009). "Neumonectomía extrapleural seguida de cisplatino hipertérmico intraoperatorio intracavitario con citoprotección farmacológica para el tratamiento del mesotelioma pleural maligno: un estudio prospectivo de fase II". JTCVS . 138 (2): 405–11. doi : 10.1016/j.jtcvs.2009.02.046 . PMID 19619785.
- ^ Allen AM, Czerminska M, Jänne PA, Sugarbaker DJ, Bueno R, Harris JR, et al. (1 de julio de 2006). "Neumonitis fatal asociada con radioterapia de intensidad modulada para mesotelioma". Revista internacional de oncología radioterápica, biología y física . 65 (3): 640–645. doi :10.1016/j.ijrobp.2006.03.012. PMID 16751058.
- ^ Vogelzang NJ, Rusthoven JJ, Symanowski J, Denham C, Kaukel E, Ruffie P, et al. (julio de 2003). "Estudio de fase III de pemetrexed en combinación con cisplatino frente a cisplatino solo en pacientes con mesotelioma pleural maligno". Journal of Clinical Oncology . 21 (14): 2636–2644. doi :10.1200/JCO.2003.11.136. PMID 12860938.
- ^ abcd "La FDA aprueba una combinación de medicamentos para tratar el mesotelioma". Administración de Alimentos y Medicamentos de Estados Unidos (FDA) (Comunicado de prensa). 2 de octubre de 2020. Consultado el 2 de octubre de 2020 .
 Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público .
Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público . - ^ Santoro A, O'Brien ME, Stahel RA, Nackaerts K, Baas P, Karthaus M, et al. (julio de 2008). "Pemetrexed más cisplatino o pemetrexed más carboplatino para pacientes con mesotelioma pleural maligno tratados con quimioterapia: resultados del Programa de Acceso Expandido Internacional". Journal of Thoracic Oncology . 3 (7): 756–763. doi : 10.1097/JTO.0b013e31817c73d6 . PMID 18594322. S2CID 29137806.
- ^ Green J, Dundar Y, Dodd S, Dickson R, Walley T (enero de 2007). Green JA (ed.). "Pemetrexed disódico en combinación con cisplatino frente a otros agentes citotóxicos o cuidados paliativos para el tratamiento del mesotelioma pleural maligno". Base de Datos Cochrane de Revisiones Sistemáticas . 2012 (1): CD005574. doi :10.1002/14651858.CD005574.pub2. PMC 8895712. PMID 17253564 .
- ^ Sugarbaker PH, Welch LS, Mohamed F, Glehen O (julio de 2003). "Una revisión del mesotelioma peritoneal en el Washington Cancer Institute". Clínicas de oncología quirúrgica de Norteamérica . 12 (3): 605–621, xi. doi :10.1016/S1055-3207(03)00045-0. PMID 14567020.
Manual en línea: Sugarbaker PH (noviembre de 1998). Tratamiento de la neoplasia maligna de la superficie peritoneal (tercera edición). Grand Rapids, Michigan: The Ludann Company. Archivado desde el original el 28 de diciembre de 2005. - ^ Ambrogi MC, Bertoglio P, Aprile V (2018). "Cirugía de preservación del diafragma y los pulmones con quimioterapia hipertérmica para el mesotelioma pleural maligno: una experiencia de 10 años". The Journal of Thoracic and Cardiovascular Surgery . 155 (4): 1857–1866.e2. doi :10.1016/j.jtcvs.2017.10.070. hdl : 11568/888183 . PMID 29191688 . Consultado el 1 de marzo de 2018 .
- ^ Richards WG, Zellos L, Bueno R, Jaklitsch MT, Jänne PA, Chirieac LR, et al. (abril de 2006). "Estudio de fase I a II de pleurectomía/decorticación y lavado hipertérmico intracavitario con cisplatino para el mesotelioma". Journal of Clinical Oncology . 24 (10): 1561–1567. doi : 10.1200/JCO.2005.04.6813 . PMID 16575008.
- ^ ab Abdel-Rahman O, Elsayed Z, Mohamed H, Eltobgy M (enero de 2018). "Terapia multimodal radical para el mesotelioma pleural maligno". Base de datos Cochrane de revisiones sistemáticas . 1 (1): CD012605. doi : 10.1002 /14651858.CD012605.pub2. PMC 6491325. PMID 29309720.
- ^ Pass HI, Temeck BK, Kranda K, Steinberg SM, Feuerstein IR (febrero de 1998). "El volumen tumoral preoperatorio se asocia con el resultado en el mesotelioma pleural maligno". The Journal of Thoracic and Cardiovascular Surgery . 115 (2): 310–317, discusión 317–318. doi : 10.1016/S0022-5223(98)70274-0 . PMID 9475525.
- ^ Sugarbaker DJ (febrero de 2006). "Resección completa macroscópica: el objetivo de la cirugía primaria en la terapia multimodal para el mesotelioma pleural". Journal of Thoracic Oncology . 1 (2): 175–176. doi :10.1097/01243894-200602000-00014. PMID 17409850.
- ^ Sugarbaker DJ, Jaklitsch MT, Bueno R, Richards W, Lukanich J, Mentzer SJ, et al. (julio de 2004). "Prevención, detección temprana y manejo de complicaciones después de 328 neumonectomías extrapleurales consecutivas". The Journal of Thoracic and Cardiovascular Surgery . 128 (1): 138–146. doi : 10.1016/j.jtcvs.2004.02.021 . PMID 15224033.
- ^ "Estadísticas de supervivencia del mesotelioma". www.cancer.org . 17 de febrero de 2016. Archivado desde el original el 6 de noviembre de 2016 . Consultado el 28 de noviembre de 2016 .
- ^ Bianchi C, Bianchi T (junio de 2007). "Mesotelioma maligno: incidencia global y relación con el amianto". Salud industrial . 45 (3): 379–387. doi : 10.2486/indhealth.45.379 . PMID 17634686.
- ^ Robinson BW, Lake RA (octubre de 2005). "Avances en el mesotelioma maligno". The New England Journal of Medicine . 353 (15): 1591–1603. doi :10.1056/NEJMra050152. PMID 16221782. S2CID 46621520.
- ^ Restrepo CS, Vargas D, Ocazionez D, Martínez-Jiménez S, Betancourt Cuellar SL, Gutiérrez FR (octubre de 2013). "Tumores pericárdicos primarios". Radiografías . 33 (6): 1613-1630. doi :10.1148/rg.336135512. PMID 24108554.
- ^ "Costos y compensación de los litigios relacionados con el amianto: un informe provisional" (PDF) . Archivado desde el original (PDF) el 24 de abril de 2009 . Consultado el 20 de agosto de 2010 .
- ^ Boffetta P (junio de 2007). "Epidemiología del mesotelioma peritoneal: una revisión". Anales de Oncología . 18 (6): 985–990. doi : 10.1093/annonc/mdl345 . PMID 17030547.
- ^ "Estadísticas de mesotelioma". Cancer Research UK . 14 de mayo de 2015. Archivado desde el original el 30 de octubre de 2014. Consultado el 28 de octubre de 2014 .
- ^ Wagner J, Sleggs C, Marchard P (1960). "Mesotelioma pleural difuso y exposición al asbesto en la provincia del Cabo Occidental del Noroeste". Medicina ocupacional y ambiental . 17 (4): 260–271. doi :10.1136/oem.17.4.260. PMC 1038078 . PMID 13782506.
- ^ "McLaren será enterrado en Highgate". The Independent . 10 de abril de 2010. Archivado desde el original el 19 de agosto de 2017 . Consultado el 13 de febrero de 2017 .
- ^ Lerner BH (15 de noviembre de 2005). «El legado de McQueen del laetrilo». The New York Times . Archivado desde el original el 11 de agosto de 2010. Consultado el 12 de mayo de 2010 .
- ^ "El amianto 'no mató' al productor". BBC News . 10 de junio de 2003.
- ^ Bradley PT (5 de julio de 2016). "El amianto mató a Warren Zevon. Ahora su hijo lucha por prohibirlo de una vez por todas". LA Weekly . Archivado desde el original el 16 de noviembre de 2016. Consultado el 13 de mayo de 2017 .
- ^ "Vive en el polvo". The Sydney Morning Herald . 25 de septiembre de 2004.
- ^ Branley A (7 de mayo de 2013). «Un sobreviviente ve su enfermedad como un 'regalo'». Herald News . Archivado desde el original el 12 de noviembre de 2014. Consultado el 7 de mayo de 2013 .
- ^ "FW de Klerk diagnosticado con cáncer, se somete a tratamiento".
- ^ "Paul Gleason, 67, actor de 'Breakfast Club', ha muerto". The New York Times . No. 29 de mayo de 2016. Associated Press. 29 de mayo de 2006 . Consultado el 3 de julio de 2021 .
- ^ Gould SJ (2013). "La mediana no es el mensaje". Revista AMA de Ética . 15 (1): 77–81. doi : 10.1001/virtualmentor.2013.15.1.mnar1-1301 . PMID 23356812.
- ^ ORTIZ V. FIBREBOARD CORP. (97-1704) 527 US 815 (1999) tenía responsabilidad individual de una sola corporación y sus compañías de seguros de casi $2 mil millones.
- ^ ORTIZ V. FIBREBOARD CORP. (97-1704) 527 US 815 (1999)
- ^ "HR982 - 113.º Congreso (2013-2014): Ley de Transparencia en las Reclamaciones por Amianto (FACT) de 2013 - Congress.gov - Biblioteca del Congreso". Biblioteca del Congreso. 14 de noviembre de 2013. Archivado desde el original el 24 de julio de 2014. Consultado el 20 de octubre de 2014 .
- ^ "HR526 - 114.º Congreso (2015-2016): Ley de Transparencia en las Reclamaciones por Asbesto (FACT) de 2015 - Congress.gov - Biblioteca del Congreso". Biblioteca del Congreso. 2015-11-30. Archivado desde el original el 2015-09-07 . Consultado el 1 de diciembre de 2015 .
- ^ Wagner JC, Sleggs CA, Marchand P (octubre de 1960). "Mesotelioma pleural difuso y exposición al amianto en la provincia del Cabo Occidental del Noroeste". British Journal of Industrial Medicine . 17 (4): 260–271. doi :10.1136/oem.17.4.260. PMC 1038078 . PMID 13782506.
- ^ Moore AJ, Parker RJ, Wiggins J (diciembre de 2008). "Mesotelioma maligno". Orphanet Journal of Rare Diseases . 3 : 34. doi : 10.1186/1750-1172-3-34 . PMC 2652430 . PMID 19099560.
- ^ Mcnulty JC (diciembre de 1962). "Mesotelioma pleural maligno en un trabajador del amianto". The Medical Journal of Australia . 49 (2): 953–954. doi :10.5694/j.1326-5377.1962.tb24396.x. PMID 13932248. S2CID 40173789.
- ^ "Cronología de Wittenoom - Sociedad de Enfermedades por Asbesto de Australia Inc." asbestosdiseases.org.au/ . Consultado el 15 de abril de 2024 .
- ^ "Fondo de investigación June Hancock". Archivado desde el original el 28 de enero de 2010. Consultado el 1 de marzo de 2010 .
- ^ Mott FE (2012). "Mesotelioma: una revisión". The Ochsner Journal . 12 (1): 70–79. PMC 3307510 . PMID 22438785.
- Este artículo incluye información de una hoja informativa de dominio público del Instituto Nacional del Cáncer de EE. UU.


