Cáncer de páncreas
| Cáncer de páncreas | |
|---|---|
 | |
| Diagrama que muestra la posición del páncreas, detrás del estómago (que es transparente en este esquema). | |
| Especialidad | |
| Síntomas |
|
| Inicio habitual | 40+ años de edad [2] |
| Factores de riesgo |
|
| Método de diagnóstico |
|
| Prevención | No fumar, consumo reducido de alcohol, mantener un peso saludable, dieta baja en carne roja [5] |
| Tratamiento |
|
| Pronóstico | Tasa de supervivencia a cinco años 13% [6] |
| Frecuencia | 393.800 (2015) [7] |
| Fallecidos | 411.600 (2015) [8] |
El cáncer de páncreas surge cuando las células del páncreas , un órgano glandular ubicado detrás del estómago , comienzan a multiplicarse sin control y forman una masa . Estas células cancerosas tienen la capacidad de invadir otras partes del cuerpo. [9] Se conocen varios tipos de cáncer de páncreas. [10]
El adenocarcinoma de páncreas , el más común , representa alrededor del 90% de los casos, [11] y el término "cáncer de páncreas" a veces se utiliza para referirse solo a ese tipo. [10] Estos adenocarcinomas comienzan dentro de la parte del páncreas que produce enzimas digestivas . [10] Varios otros tipos de cáncer, que colectivamente representan la mayoría de los no adenocarcinomas, también pueden surgir de estas células. [10]
Entre el 1 y el 2 % de los casos de cáncer de páncreas son tumores neuroendocrinos , que surgen de las células productoras de hormonas del páncreas. [10] Estos son generalmente menos agresivos que el adenocarcinoma de páncreas. [10]
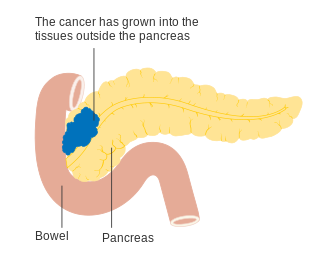
Los signos y síntomas de la forma más común de cáncer de páncreas pueden incluir piel amarilla , dolor abdominal o de espalda , pérdida de peso inexplicable , heces de color claro , orina oscura y pérdida de apetito . [1] Por lo general, no se observan síntomas en las primeras etapas de la enfermedad, y los síntomas que son lo suficientemente específicos como para sugerir cáncer de páncreas generalmente no se desarrollan hasta que la enfermedad ha alcanzado una etapa avanzada. [1] [2] En el momento del diagnóstico, el cáncer de páncreas a menudo se ha propagado a otras partes del cuerpo. [10] [12]
El cáncer de páncreas rara vez ocurre antes de los 40 años, y más de la mitad de los casos de adenocarcinoma de páncreas ocurren en personas mayores de 70 años . [2] Los factores de riesgo para el cáncer de páncreas incluyen el tabaquismo , la obesidad , la diabetes y ciertas enfermedades genéticas raras. [2] Alrededor del 25% de los casos están relacionados con el tabaquismo, [3] y entre el 5 y el 10% están relacionados con genes heredados . [2]
El cáncer de páncreas se suele diagnosticar mediante una combinación de técnicas de diagnóstico por imágenes, como ecografía o tomografía computarizada , análisis de sangre y examen de muestras de tejido ( biopsia ). [3] [4] La enfermedad se divide en estadios , desde el estadio temprano (estadio I) hasta el estadio tardío (estadio IV). [12] No se ha demostrado que el cribado en la población general sea eficaz. [13]
El riesgo de desarrollar cáncer de páncreas es menor entre los no fumadores y las personas que mantienen un peso saludable y limitan su consumo de carne roja o procesada ; [5] el riesgo es mayor para los hombres, los fumadores y las personas con diabetes. [14] Existe cierta evidencia que vincula los altos niveles de consumo de carne roja con un mayor riesgo de cáncer de páncreas. [15] [16] [17] El riesgo de los fumadores de desarrollar la enfermedad disminuye inmediatamente después de dejar de fumar y casi vuelve al del resto de la población después de 20 años. [10] El cáncer de páncreas se puede tratar con cirugía, radioterapia , quimioterapia , cuidados paliativos o una combinación de estos. [1] Las opciones de tratamiento se basan en parte en el estadio del cáncer. [1] La cirugía es el único tratamiento que puede curar el adenocarcinoma de páncreas, [12] y también se puede realizar para mejorar la calidad de vida sin el potencial de cura. [1] [12] A veces se necesitan analgésicos y medicamentos para mejorar la digestión. [12] Se recomiendan cuidados paliativos tempranos incluso para quienes reciben un tratamiento que tiene como objetivo la cura. [18]
El cáncer de páncreas es una de las formas de cáncer más letales a nivel mundial, con una de las tasas de supervivencia más bajas. En 2015, los cánceres de páncreas de todos los tipos provocaron 411.600 muertes en todo el mundo. [8] El cáncer de páncreas es la quinta causa más común de muerte por cáncer en el Reino Unido, [19] y la tercera más común en los Estados Unidos. [20] La enfermedad se presenta con mayor frecuencia en el mundo desarrollado, donde se originó alrededor del 70% de los nuevos casos en 2012. [10] El adenocarcinoma de páncreas generalmente tiene un pronóstico muy malo; después del diagnóstico, el 25% de las personas sobreviven un año y el 12% vive cinco años. [6] [10] Para los cánceres diagnosticados temprano, la tasa de supervivencia a cinco años aumenta a aproximadamente el 20%. [21] Los cánceres neuroendocrinos tienen mejores resultados; a los cinco años del diagnóstico, el 65% de los diagnosticados están vivos, aunque la supervivencia varía considerablemente según el tipo de tumor. [10]
Tipos


Los numerosos tipos de cáncer de páncreas se pueden dividir en dos grupos generales. La gran mayoría de los casos (alrededor del 95%) se producen en la parte del páncreas que produce enzimas digestivas , conocida como componente exocrino . Se describen varios subtipos de cánceres de páncreas exocrinos, pero su diagnóstico y tratamiento tienen mucho en común.
La pequeña minoría de cánceres que surgen en el tejido productor de hormonas ( endocrino ) del páncreas tienen características clínicas diferentes y se denominan tumores neuroendocrinos pancreáticos , a veces abreviados como "PanNET". Ambos grupos se presentan principalmente (pero no exclusivamente) en personas mayores de 40 años, y son ligeramente más comunes en hombres, pero algunos subtipos raros se presentan principalmente en mujeres o niños. [23] [24]
Cánceres exocrinos
El grupo exocrino está dominado por el adenocarcinoma pancreático (las variaciones de este nombre pueden agregar "invasivo" y "ductal"), que es por lejos el tipo más común, representando aproximadamente el 85% de todos los cánceres pancreáticos. [2] Casi todos estos comienzan en los conductos del páncreas, como adenocarcinoma ductal pancreático (PDAC). [25] Esto es a pesar del hecho de que el tejido del que surge -el epitelio ductal pancreático- representa menos del 10% del páncreas por volumen celular, porque constituye solo los conductos (un sistema de conductos extenso pero similar a un capilar que se abre en abanico) dentro del páncreas. [26] Este cáncer se origina en los conductos que transportan secreciones (como enzimas y bicarbonato ) fuera del páncreas. Aproximadamente el 60-70% de los adenocarcinomas ocurren en la cabeza del páncreas . [2]
El siguiente tipo más común, el carcinoma de células acinares del páncreas , surge en los grupos de células que producen estas enzimas y representa el 5% de los cánceres de páncreas exocrinos. [27] Al igual que los cánceres endocrinos "funcionales" descritos a continuación, los carcinomas de células acinares pueden causar una sobreproducción de ciertas moléculas, en este caso enzimas digestivas, que pueden causar síntomas como erupciones cutáneas y dolor en las articulaciones.
Los cistadenocarcinomas representan el 1% de los cánceres de páncreas y tienen un mejor pronóstico que los otros tipos exocrinos. [27]
El pancreatoblastoma es una forma rara, que se presenta principalmente en la infancia y tiene un pronóstico relativamente bueno. Otros cánceres exocrinos incluyen carcinomas adenoescamosos , carcinomas de células en anillo de sello , carcinomas hepatoides , carcinomas coloides, carcinomas indiferenciados y carcinomas indiferenciados con células gigantes similares a osteoclastos . El tumor pseudopapilar sólido es una neoplasia rara de bajo grado que afecta principalmente a mujeres jóvenes y generalmente tiene un pronóstico muy bueno. [2] [28]
Las neoplasias quísticas mucinosas pancreáticas son un grupo amplio de tumores pancreáticos que tienen un potencial maligno variable. Se están detectando a una tasa mucho mayor a medida que las tomografías computarizadas se vuelven más potentes y comunes, y continúa el debate sobre cuál es la mejor manera de evaluarlas y tratarlas, dado que muchas son benignas. [29]
Neuroendocrino
La pequeña minoría de tumores que surgen en otras partes del páncreas son principalmente tumores neuroendocrinos pancreáticos (PanNET). [30] Los tumores neuroendocrinos (NET) son un grupo diverso de tumores benignos o malignos que surgen de las células neuroendocrinas del cuerpo , que son responsables de integrar los sistemas nervioso y endocrino. Los NET pueden comenzar en la mayoría de los órganos del cuerpo, incluido el páncreas, donde los diversos tipos malignos se consideran raros . Los PanNET se agrupan en tipos "funcionales" y "no funcionales", según el grado en que producen hormonas. Los tipos funcionales secretan hormonas como insulina , gastrina y glucagón en el torrente sanguíneo, a menudo en grandes cantidades, lo que da lugar a síntomas graves como bajo nivel de azúcar en sangre , pero también favorece una detección relativamente temprana. Los PanNET funcionales más comunes son los insulinomas y los gastrinomas , llamados así por las hormonas que secretan. Los tipos no funcionales no secretan hormonas en una cantidad suficiente como para dar lugar a síntomas clínicos evidentes, por lo que los PanNET no funcionales a menudo se diagnostican sólo después de que el cáncer se ha propagado a otras partes del cuerpo. [31]
Al igual que con otros tumores neuroendocrinos, la historia de la terminología y la clasificación de los PanNET es compleja. [30] A los PanNET a veces se los llama "cánceres de células de los islotes", [32] aunque ahora se sabe que en realidad no surgen de las células de los islotes como se creía anteriormente. [31]
Signos y síntomas

Dado que el cáncer de páncreas no suele causar síntomas reconocibles en sus primeras etapas, la enfermedad no suele diagnosticarse hasta que se ha propagado más allá del páncreas. [4] Esta es una de las principales razones de las tasas de supervivencia generalmente bajas. Las excepciones a esto son los PanNET funcionales, en los que la sobreproducción de varias hormonas activas puede dar lugar a síntomas (que dependen del tipo de hormona). [33]
Los síntomas de presentación comunes del adenocarcinoma de páncreas incluyen:
- Dolor en la parte superior del abdomen o la espalda, que a menudo se extiende desde el estómago hasta la espalda. La ubicación del dolor puede indicar la parte del páncreas donde se encuentra el tumor. El dolor puede empeorar por la noche y aumentar con el tiempo hasta volverse intenso y persistente. [27] Puede aliviarse ligeramente al inclinarse hacia adelante. En el Reino Unido, aproximadamente la mitad de los nuevos casos de cáncer de páncreas se diagnostican después de una visita al servicio de urgencias de un hospital por dolor o ictericia. En hasta dos tercios de las personas, el dolor abdominal es el síntoma principal, en el 46% del total acompañado de ictericia, y el 13% tiene ictericia sin dolor. [12]
- La ictericia , un tinte amarillento en la parte blanca de los ojos o la piel, con o sin dolor y posiblemente en combinación con orina oscura, se produce cuando un cáncer en la cabeza del páncreas obstruye el conducto biliar común a su paso por el páncreas. [34]
- Pérdida de peso inexplicable , ya sea por pérdida de apetito o pérdida de la función exocrina que resulta en una mala digestión . [12]
- El tumor puede comprimir los órganos vecinos, lo que altera los procesos digestivos y dificulta el vaciado del estómago , lo que puede provocar náuseas y sensación de saciedad. La grasa no digerida produce heces grasosas y malolientes que son difíciles de eliminar. [12] El estreñimiento también es común. [35]
- Al menos el 50% de las personas con adenocarcinoma de páncreas tienen diabetes en el momento del diagnóstico. [2] Si bien la diabetes de larga duración es un factor de riesgo conocido para el cáncer de páncreas (ver Factores de riesgo), el cáncer puede causar diabetes en sí mismo, en cuyo caso la aparición reciente de diabetes podría considerarse un signo temprano de la enfermedad. [36] Las personas mayores de 50 años que desarrollan diabetes tienen ocho veces el riesgo habitual de desarrollar adenocarcinoma de páncreas en un plazo de tres años, después de lo cual el riesgo relativo disminuye. [12]
Otros hallazgos
- El síndrome de Trousseau , en el que se forman coágulos de sangre espontáneamente en los vasos sanguíneos portales ( trombosis de la vena porta ), las venas profundas de las extremidades ( trombosis venosa profunda ) o las venas superficiales ( trombosis venosa superficial ) en cualquier parte del cuerpo, puede estar asociado con el cáncer de páncreas y se encuentra en aproximadamente el 10% de los casos. [3]
- Se ha informado de depresión clínica asociada al cáncer de páncreas en un 10-20% de los casos, y puede ser un obstáculo para un tratamiento óptimo. La depresión a veces aparece antes del diagnóstico de cáncer, lo que sugiere que puede ser provocada por la biología de la enfermedad. [3]
Otras manifestaciones comunes de la enfermedad incluyen debilidad y cansancio fácil, boca seca , problemas para dormir y una masa abdominal palpable . [35]
Síntomas de propagación

La propagación del cáncer de páncreas a otros órganos ( metástasis ) también puede causar síntomas. Por lo general, el adenocarcinoma de páncreas se propaga primero a los ganglios linfáticos cercanos y luego al hígado o a la cavidad peritoneal , el intestino grueso o los pulmones. [3] Con poca frecuencia, se propaga a los huesos o al cerebro. [37]
Los cánceres de páncreas también pueden ser cánceres secundarios que se han propagado desde otras partes del cuerpo. Esto es poco común y se encuentra en solo alrededor del 2% de los casos de cáncer de páncreas. El cáncer de riñón es, con mucho, el cáncer más común que se propaga al páncreas, seguido por el cáncer colorrectal y luego los cánceres de piel , mama y pulmón . En estos casos, se puede realizar una cirugía en el páncreas, ya sea con la esperanza de una cura o para aliviar los síntomas. [38]
Factores de riesgo
Los factores de riesgo del adenocarcinoma de páncreas incluyen: [2] [10] [12] [39] [40] [ citas excesivas ]
- Edad, sexo y origen étnico : el riesgo de desarrollar cáncer de páncreas aumenta con la edad. La mayoría de los casos se presentan después de los 65 años [10] , mientras que los casos antes de los 40 años son poco comunes. La enfermedad es ligeramente más común en hombres que en mujeres [10] . En los Estados Unidos, es más de 1,5 veces más común en afroamericanos , aunque la incidencia en África es baja [10] .
- El tabaquismo es el factor de riesgo evitable más conocido del cáncer de páncreas, que aproximadamente duplica el riesgo entre los fumadores crónicos y aumenta con la cantidad de cigarrillos fumados y los años de tabaquismo. El riesgo disminuye lentamente después de dejar de fumar y tarda unos 20 años en volver a ser casi el mismo que en los no fumadores. [41]
- Obesidad : un índice de masa corporal superior a 35 aumenta el riesgo relativo aproximadamente a la mitad. [12] [42]
- Antecedentes familiares: entre el 5 y el 10 % de los casos de cáncer de páncreas tienen un componente hereditario, es decir, las personas tienen antecedentes familiares de cáncer de páncreas. [2] [43] El riesgo aumenta considerablemente si más de un familiar de primer grado tuvo la enfermedad, y de forma más modesta si la desarrollaron antes de los 50 años. [4] La mayoría de los genes implicados no han sido identificados. [2] [44] La pancreatitis hereditaria da lugar a un riesgo de por vida muy superior de padecer cáncer de páncreas, del 30 al 40 %, hasta los 70 años. [3] A las personas con pancreatitis hereditaria se les puede ofrecer la detección temprana del cáncer de páncreas con fines de investigación. [45] Algunas personas pueden optar por extirparse quirúrgicamente el páncreas para evitar que se desarrolle cáncer en el futuro. [3]
- El cáncer de páncreas se ha asociado con estos otros síndromes hereditarios raros: síndrome de Peutz-Jeghers debido a mutaciones en el gen supresor de tumores STK11 (muy raro, pero un factor de riesgo muy fuerte); síndrome del nevo displásico (o síndrome familiar de lunares múltiples atípicos y melanoma, FAMMM-PC) debido a mutaciones en el gen supresor de tumores CDKN2A ; mutaciones autosómicas recesivas ATM y mutaciones autosómicas dominantes heredadas en los genes BRCA2 y PALB2 ; cáncer de colon hereditario sin poliposis (síndrome de Lynch); y poliposis adenomatosa familiar . Los PanNET se han asociado con neoplasia endocrina múltiple tipo 1 (MEN1) y síndromes de von Hippel Lindau . [2] [3] [4]
- La pancreatitis crónica parece triplicar el riesgo y, al igual que con la diabetes, la pancreatitis de nueva aparición puede ser un síntoma de un tumor. [3] El riesgo de cáncer de páncreas en personas con pancreatitis familiar es particularmente alto. [3] [44]
- La diabetes mellitus es un factor de riesgo para el cáncer de páncreas y (como se indica en la sección Signos y síntomas) la diabetes de nueva aparición también puede ser un signo temprano de la enfermedad. Las personas a las que se les ha diagnosticado diabetes tipo 2 durante más de 10 años pueden tener un riesgo 50% mayor, en comparación con las personas sin diabetes. [3] En 2021, Venturi informó que el páncreas es capaz de absorber en gran cantidad cesio radiactivo (Cs-134 y Cs-137) causando pancreatitis crónica y probablemente cáncer de páncreas con daño de las islas pancreáticas, causando diabetes tipo 3c (pancreatogénica) . [46] La pancreatitis crónica, el cáncer de páncreas y la diabetes mellitus aumentaron en las poblaciones contaminadas, en particular niños y adolescentes, después de los incidentes nucleares de Fukushima y Chernóbil. Al mismo tiempo, las enfermedades pancreáticas, la diabetes y el radiocesio ambiental están aumentando en todo el mundo.
- No se ha demostrado claramente que tipos específicos de alimentos (a diferencia de la obesidad) aumenten el riesgo de cáncer de páncreas. [2] [47] Los factores dietéticos para los que algunas evidencias muestran un riesgo ligeramente mayor incluyen la carne procesada , la carne roja y la carne cocinada a temperaturas muy altas (por ejemplo, friendo, asando o a la parrilla). [16] [47]
Alcohol
El consumo excesivo de alcohol es una de las principales causas de pancreatitis crónica , que a su vez predispone al cáncer de páncreas, pero numerosas investigaciones no han logrado establecer firmemente que el consumo de alcohol sea un factor de riesgo directo para el cáncer de páncreas. En general, la asociación es consistentemente débil y la mayoría de los estudios no han encontrado ninguna asociación, siendo el tabaquismo un importante factor de confusión . La evidencia es más sólida en cuanto a un vínculo con el consumo excesivo de alcohol, de al menos seis bebidas por día. [3] [48]
Fisiopatología
_Case_01.jpg/440px-Pancreas_adenocarcinoma_(4)_Case_01.jpg)
Precáncer


Se cree que los cánceres exocrinos surgen de varios tipos de lesiones precancerosas dentro del páncreas, pero estas lesiones no siempre progresan a cáncer, y los números crecientes detectados como un subproducto del uso creciente de tomografías computarizadas por otras razones no son todos tratados. [3] Aparte de los cistoadenomas serosos pancreáticos , que casi siempre son benignos, se reconocen cuatro tipos de lesiones precancerosas.
La primera es la neoplasia intraepitelial pancreática (PanIN). Estas lesiones son anomalías microscópicas en el páncreas y se encuentran a menudo en autopsias de personas sin cáncer diagnosticado. Estas lesiones pueden progresar de grado bajo a grado alto y luego convertirse en un tumor. Más del 90% de los casos en todos los grados tienen un gen KRAS defectuoso, mientras que en los grados 2 y 3, se encuentran cada vez más daños en otros tres genes: CDKN2A ( p16 ), p53 y SMAD4 . [2]
Un segundo tipo es la neoplasia mucinosa papilar intraductal (NMPI). Se trata de lesiones macroscópicas que se encuentran en aproximadamente el 2% de todos los adultos. Esta tasa aumenta a aproximadamente el 10% a los 70 años. Estas lesiones tienen un riesgo de alrededor del 25% de convertirse en cáncer invasivo. Pueden tener mutaciones en el gen KRAS (40-65% de los casos) y en la subunidad alfa Gs de GNAS y RNF43, que afectan la vía de señalización Wnt . [2] Incluso si se extirpan quirúrgicamente, sigue habiendo un riesgo considerablemente mayor de que se desarrolle cáncer de páncreas posteriormente. [3]
El tercer tipo, la neoplasia quística mucinosa pancreática (MCN), se presenta principalmente en mujeres y puede permanecer benigna o progresar a cáncer. [50] Si estas lesiones se vuelven grandes, causan síntomas o tienen características sospechosas, generalmente se pueden extirpar con éxito mediante cirugía. [3]
Un cuarto tipo de cáncer que se origina en el páncreas es la neoplasia tubulopapilar intraductal. Este tipo fue reconocido por la OMS en 2010 y constituye alrededor del 1-3% de todas las neoplasias pancreáticas. La edad media en el momento del diagnóstico es de 61 años (rango 35-78 años). Alrededor del 50% de estas lesiones se vuelven invasivas. El diagnóstico depende de la histología, ya que estas lesiones son muy difíciles de diferenciar de otras lesiones tanto por criterios clínicos como radiológicos. [51]
Cáncer invasivo
Los eventos genéticos encontrados en el adenocarcinoma ductal han sido bien caracterizados, y se ha realizado una secuenciación completa del exoma para los tipos comunes de tumores. Se ha encontrado que cuatro genes están mutados en la mayoría de los adenocarcinomas: KRAS (en el 95% de los casos), CDKN2A (también en el 95%), TP53 (75%) y SMAD4 (55%). El último de estos está especialmente asociado con un mal pronóstico. [3] Las mutaciones/ deleciones SWI/SNF ocurren en aproximadamente el 10-15% de los adenocarcinomas. [2] También se han investigado las alteraciones genéticas en varios otros tipos de cáncer de páncreas y lesiones precancerosas. [3] Los análisis transcriptómicos y la secuenciación de ARNm para las formas comunes de cáncer de páncreas han descubierto que el 75% de los genes humanos se expresan en los tumores, con unos 200 genes expresados más específicamente en el cáncer de páncreas en comparación con otros tipos de tumores. [52] [53]
Se sabe que las células cancerosas del adenocarcinoma ductal pancreático secretan citocinas inmunosupresoras, lo que crea un microambiente tumoral que inhibe la detección inmunitaria y bloquea la inmunidad contra el cáncer. Los fibroblastos asociados al cáncer secretan tejido fibroso ( desmoplasia ) que consiste en metaloproteinasas de matriz y ácido hialurónico que impiden que las células T CD8+ del huésped lleguen al tumor. Los macrófagos , neutrófilos y células T reguladoras asociados al tumor secretan citocinas y trabajan para crear un microambiente tumoral que promueve el crecimiento del cáncer. [54]
PanNET
Los genes que suelen encontrarse mutados en los tumores neuroendocrinos pancreáticos (PanNET) son diferentes de los del cáncer pancreático exocrino. [55] Por ejemplo, la mutación KRAS normalmente está ausente. En cambio, las mutaciones hereditarias del gen MEN1 dan riesgo de síndrome MEN1 , en el que los tumores primarios aparecen en dos o más glándulas endocrinas . Alrededor del 40-70% de las personas que nacen con una mutación MEN1 acaban desarrollando un PanNet. [56] Otros genes que mutan con frecuencia son DAXX , mTOR y ATRX . [31]
Diagnóstico
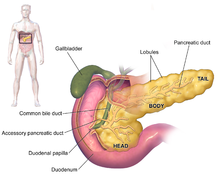


Los síntomas del adenocarcinoma de páncreas no suelen aparecer en las primeras etapas de la enfermedad y no son distintivos de cada caso. [3] [12] [34] Los síntomas en el momento del diagnóstico varían según la ubicación del cáncer en el páncreas, que los anatomistas dividen (de izquierda a derecha en la mayoría de los diagramas) en la cabeza gruesa, el cuello y el cuerpo afilado que termina en la cola.
Independientemente de la ubicación del tumor, el síntoma más común es la pérdida de peso inexplicable, que puede ser considerable. Una gran minoría (entre el 35% y el 47%) de las personas diagnosticadas con la enfermedad habrán tenido náuseas, vómitos o una sensación de debilidad. Los tumores en la cabeza del páncreas generalmente también causan ictericia, dolor, pérdida de apetito , orina oscura y heces de color claro. Los tumores en el cuerpo y la cola generalmente también causan dolor. [34]
Las personas a veces tienen un inicio reciente de diabetes tipo 2 atípica que es difícil de controlar, antecedentes de inflamación reciente pero inexplicable de los vasos sanguíneos causada por coágulos de sangre ( tromboflebitis ) conocida como signo de Trousseau , o un ataque previo de pancreatitis . [34] Un médico puede sospechar cáncer de páncreas cuando el inicio de la diabetes en alguien mayor de 50 años se acompaña de síntomas típicos como pérdida de peso inexplicable, dolor abdominal o de espalda persistente, indigestión, vómitos o heces grasas. [12] La ictericia acompañada de una vesícula biliar hinchada sin dolor (conocida como signo de Courvoisier ) también puede generar sospechas y puede ayudar a diferenciar el cáncer de páncreas de los cálculos biliares . [57]
Las técnicas de diagnóstico por imágenes , como la tomografía computarizada (TC) y la ecografía endoscópica (EUS), se utilizan tanto para confirmar el diagnóstico como para ayudar a decidir si el tumor se puede extirpar quirúrgicamente (su " resecabilidad "). [12] En la tomografía computarizada con contraste , el cáncer de páncreas suele mostrar una captación de radiocontraste que aumenta gradualmente, en lugar de un lavado rápido como el que se ve en un páncreas normal o un lavado tardío como el que se ve en la pancreatitis crónica. [58] También se pueden utilizar la resonancia magnética y la tomografía por emisión de positrones , [2] y la colangiopancreatografía por resonancia magnética puede ser útil en algunos casos. [34] La ecografía abdominal es menos sensible y no detectará tumores pequeños, pero puede identificar cánceres que se han diseminado al hígado y la acumulación de líquido en la cavidad peritoneal ( ascitis ). [12] Se puede utilizar para un primer examen rápido y económico antes de otras técnicas. [59]
.jpg/440px-Adenocarcinoma_of_Pancreas,_FNA_(5558060087).jpg)
Se puede utilizar una biopsia por aspiración con aguja fina , a menudo guiada por ecografía endoscópica, cuando hay incertidumbre sobre el diagnóstico, pero por lo general no se requiere un diagnóstico histológico para proceder a la extirpación quirúrgica del tumor. [12]
Las pruebas de función hepática pueden mostrar una combinación de resultados indicativos de obstrucción del conducto biliar ( niveles elevados de bilirrubina conjugada , γ-glutamil transpeptidasa y fosfatasa alcalina ). El CA19-9 (antígeno carbohidrato 19.9) es un marcador tumoral que frecuentemente está elevado en el cáncer de páncreas. Sin embargo, carece de sensibilidad y especificidad , sobre todo porque el 5% de las personas carecen del antígeno Lewis (a) y no pueden producir CA19-9. Tiene una sensibilidad del 80% y una especificidad del 73% en la detección del adenocarcinoma de páncreas, y se utiliza para el seguimiento de casos conocidos en lugar de para el diagnóstico. [2] [12]
Todas las personas con cáncer de páncreas requieren pruebas genéticas, ya que las mutaciones oncogénicas de alto riesgo pueden proporcionar información pronóstica y ciertas mutaciones con características de alto riesgo requieren que los familiares de primer grado también se sometan a pruebas genéticas. [54]
Histopatología
La forma más común de cáncer de páncreas (adenocarcinoma) se caracteriza típicamente por estructuras glandulares moderadamente a pobremente diferenciadas en el examen microscópico. Por lo general, hay una desmoplasia considerable o formación de un estroma fibroso denso o tejido estructural que consiste en una variedad de tipos de células (incluidos miofibroblastos , macrófagos , linfocitos y mastocitos ) y material depositado (como colágeno tipo I y ácido hialurónico ). Esto crea un microambiente tumoral que carece de vasos sanguíneos (hipovascular) y, por lo tanto, de oxígeno ( hipoxia tumoral ). [2] Se cree que esto impide que muchos medicamentos de quimioterapia lleguen al tumor, como un factor que hace que el cáncer sea especialmente difícil de tratar. [2] [3]
| Tipo de cáncer | Incidencia relativa [11] | Hallazgos microscópicos [11] | Micrografía | Marcadores de inmunohistoquímica [11] | Alteraciones genéticas [11] |
|---|---|---|---|---|---|
| Adenocarcinoma ductal pancreático (PDAC) | 90% | Glándulas y desmoplasia |  | ||
| Carcinoma de células acinares pancreáticas (ACC) | 1% a 2% | Aspecto granular |  | ||
| Tumor pseudopapilar sólido | Nidos tumorales discohesivos rodeados de finas bandas fibrosas. |  Aumentos bajos y altos [60] |
|
| |
| Carcinoma adenoescamoso | 1% a 4% [61] | Combinación de células glandulares y células epiteliales escamosas. |  | Positivo para: Negativo para: | |
| Tumor neuroendocrino pancreático | 5% | Múltiples nidos de células tumorales |  | ||
| Precáncer a continuación para comparación: | |||||
| Precáncer: Neoplasia mucinosa papilar intraductal (NMPI) | 3% | Células epiteliales mucinosas. [62] Crecimiento dentro de los conductos pancreáticos . [63] |  | ||
Puesta en escena
Cánceres exocrinos
El cáncer de páncreas se suele estadificar mediante una tomografía computarizada . [34] El sistema de estadificación del cáncer de páncreas más utilizado es el formulado por el Comité Conjunto Estadounidense sobre Cáncer (AJCC) junto con la Unión para el Control Internacional del Cáncer (UICC). El sistema de estadificación AJCC-UICC designa cuatro estadios generales principales, que van desde la enfermedad temprana hasta la avanzada, según la clasificación TNM del tamaño del tumor, la propagación a los ganglios linfáticos y la metástasis . [64]
Para ayudar a decidir el tratamiento, los tumores también se dividen en tres categorías más amplias en función de si la extirpación quirúrgica parece posible: de esta manera, los tumores se juzgan como "resecables", "resecables en el límite" o "irresecables". [65] Cuando la enfermedad todavía está en una etapa temprana (estadios I y II de la AJCC-UICC), sin propagación a grandes vasos sanguíneos u órganos distantes como el hígado o los pulmones, normalmente se puede realizar la resección quirúrgica del tumor, si el paciente está dispuesto a someterse a esta importante operación y se cree que está lo suficientemente en forma. [12]
El sistema de estadificación AJCC-UICC permite distinguir entre tumores en estadio III que se juzgan como "resecables en el límite" (donde la cirugía es técnicamente factible porque el eje celíaco y la arteria mesentérica superior todavía están libres) y aquellos que son "irresecables" (debido a una enfermedad localmente más avanzada); en términos de la clasificación TNM más detallada, estos dos grupos corresponden a T3 y T4 respectivamente. [3]
- Estadificación del cáncer de páncreas (clasificación TNM)
- Cáncer de páncreas en estadio T1
- Cáncer de páncreas en estadio T2
- Cáncer de páncreas en estadio T3
- Cáncer de páncreas en estadio T4
- Cáncer de páncreas en ganglios linfáticos cercanos – Estadio N1

Los adenocarcinomas localmente avanzados se han diseminado a órganos vecinos, que pueden ser cualquiera de los siguientes (en orden decreciente de frecuencia aproximadamente): el duodeno , el estómago , el colon transverso , el bazo , la glándula suprarrenal o el riñón . Muy a menudo también se diseminan a los vasos sanguíneos o linfáticos y nervios importantes que pasan cerca del páncreas, lo que dificulta mucho la cirugía. Los sitios típicos de diseminación metastásica (enfermedad en etapa IV) son el hígado, la cavidad peritoneal y los pulmones , todos los cuales ocurren en el 50% o más de los casos completamente avanzados. [66]
PanNET
La clasificación de la OMS de 2010 de los tumores del sistema digestivo clasifica todos los tumores neuroendocrinos pancreáticos (PanNET) en tres categorías, según su grado de diferenciación celular (desde "NET G1" hasta el pobremente diferenciado "NET G3"). [24] La Red Nacional Integral del Cáncer de los EE. UU. recomienda el uso del mismo sistema de estadificación AJCC-UICC que el adenocarcinoma de páncreas. [67] : 52 Con este esquema, los resultados etapa por etapa para los PanNET son diferentes a los de los cánceres exocrinos. [68] La Sociedad Europea de Tumores Neuroendocrinos ha propuesto un sistema TNM diferente para los PanNET. [24]
Prevención y detección
Además de no fumar, la Sociedad Estadounidense del Cáncer recomienda mantener un peso saludable y aumentar el consumo de frutas, verduras y cereales integrales , al tiempo que se reduce el consumo de carne roja y procesada , aunque no hay evidencia consistente de que esto prevenga o reduzca específicamente el cáncer de páncreas. [69] Una revisión de investigaciones de 2014 concluyó que había evidencia de que el consumo de frutas cítricas y curcumina reducía el riesgo de cáncer de páncreas, mientras que posiblemente había un efecto beneficioso de los cereales integrales, el folato , el selenio y el pescado no frito. [48]
En la población general, el cribado de grandes grupos no se considera eficaz y puede ser perjudicial a partir de 2019, [70] aunque se están evaluando técnicas más nuevas y el cribado de grupos muy específicos. [71] [72] No obstante, se recomienda el cribado regular con ecografía endoscópica e imágenes por resonancia magnética/TC para aquellos con alto riesgo de genética hereditaria. [4] [59] [72] [73]
Un metanálisis de 2019 encontró que el uso de aspirina podría estar asociado negativamente con el riesgo de incidencia de cáncer de páncreas, pero no encontró una relación significativa con la mortalidad por cáncer de páncreas. [74]
Gestión
Cáncer exocrino
Una evaluación clave que se realiza después del diagnóstico es si es posible la extirpación quirúrgica del tumor (ver Estadificación), ya que es la única cura para este cáncer. La posibilidad de ofrecer o no la resección quirúrgica depende de cuánto se haya propagado el cáncer. La ubicación exacta del tumor también es un factor significativo, y la TC puede mostrar cómo se relaciona con los vasos sanguíneos principales que pasan cerca del páncreas. También se debe evaluar la salud general de la persona, aunque la edad en sí no es un obstáculo para la cirugía. [3]
Es probable que a la mayoría de las personas se les ofrezca quimioterapia y, en menor medida, radioterapia, independientemente de que la cirugía sea posible o no. Los especialistas recomiendan que el tratamiento del cáncer de páncreas esté en manos de un equipo multidisciplinario que incluya especialistas en varios aspectos de la oncología y, por lo tanto, es mejor que se lleve a cabo en centros más grandes. [2] [3]
Cirugía

La cirugía con la intención de curar el tumor sólo es posible en alrededor de una quinta parte (20%) de los casos nuevos. [12] Aunque las tomografías computarizadas ayudan, en la práctica puede ser difícil determinar si el tumor puede ser extirpado completamente (su "resecabilidad"), y sólo puede resultar evidente durante la cirugía que no es posible extirpar con éxito el tumor sin dañar otros tejidos vitales. La posibilidad de ofrecer o no una resección quirúrgica depende de varios factores, entre ellos la extensión precisa de la adyacencia anatómica local a los vasos sanguíneos venosos o arteriales o su afectación, [2] así como la experiencia quirúrgica y una consideración cuidadosa de la recuperación posoperatoria prevista. [75] [76] La edad de la persona no es en sí misma una razón para no operar, pero su estado general de rendimiento debe ser adecuado para una operación importante. [12]
Una característica particular que se evalúa es la presencia alentadora, o la ausencia desalentadora, de una capa o plano claro de grasa que crea una barrera entre el tumor y los vasos. [3] Tradicionalmente, se realiza una evaluación de la proximidad del tumor a los vasos venosos o arteriales principales, en términos de "tope" (definido como el tumor que toca no más de la mitad de la circunferencia de un vaso sanguíneo sin ninguna grasa que lo separe), "encapsulamiento" (cuando el tumor encierra la mayor parte de la circunferencia del vaso) o afectación total del vaso. [77] : 22 Una resección que incluya secciones encapsuladas de vasos sanguíneos puede ser posible en algunos casos, [78] [79] particularmente si es factible una terapia neoadyuvante preliminar , [80] [81] [82] utilizando quimioterapia [76] [77] : 36 [83] y/o radioterapia. [77] : 29–30
Incluso cuando la operación parece haber sido exitosa, a menudo se encuentran células cancerosas alrededor de los bordes (" márgenes ") del tejido extirpado, cuando un patólogo las examina microscópicamente (esto siempre se hará), lo que indica que el cáncer no se ha eliminado por completo. [2] Además, las células madre cancerosas generalmente no son evidentes microscópicamente, y si están presentes, pueden continuar desarrollándose y diseminándose. [84] [85] Por lo tanto, se puede realizar una laparoscopia exploratoria (un pequeño procedimiento quirúrgico guiado por cámara) para obtener una idea más clara del resultado de una operación completa. [86]

En el caso de los cánceres que afectan a la cabeza del páncreas, el tratamiento quirúrgico curativo más frecuentemente intentado es el procedimiento de Whipple . Se trata de una operación mayor que implica la extirpación conjunta de la cabeza del páncreas y la curva del duodeno ("pancreatoduodenectomía"), la realización de una derivación para que los alimentos pasen del estómago al yeyuno ("gastroyeyunostomía") y la unión de un asa de yeyuno al conducto cístico para drenar la bilis ("colecistoyeyunostomía"). Se puede realizar únicamente si es probable que la persona sobreviva a una cirugía mayor y si el cáncer está localizado sin invadir estructuras locales ni hacer metástasis. Por lo tanto, se puede realizar únicamente en una minoría de los casos. Los cánceres de la cola del páncreas se pueden resecar mediante un procedimiento conocido como pancreatectomía distal , que a menudo también implica la extirpación del bazo . [2] [3] Hoy en día, esto a menudo se puede realizar mediante cirugía mínimamente invasiva . [2] [3]
Aunque la cirugía curativa ya no conlleva las altísimas tasas de mortalidad que se daban hasta la década de 1980, una gran proporción de personas (alrededor del 30-45%) todavía tienen que ser tratadas por una enfermedad posoperatoria que no es causada por el cáncer en sí. La complicación más común de la cirugía es la dificultad para vaciar el estómago. [3] También se pueden utilizar ciertos procedimientos quirúrgicos más limitados para aliviar los síntomas (véase Cuidados paliativos): por ejemplo, si el cáncer está invadiendo o comprimiendo el duodeno o el colon . En tales casos, la cirugía de bypass puede superar la obstrucción y mejorar la calidad de vida, pero no está destinada a ser una cura. [12]
Quimioterapia
Después de la cirugía, se puede ofrecer quimioterapia adyuvante con gemcitabina o 5-FU si la persona está lo suficientemente en forma , después de un período de recuperación de uno a dos meses. [4] [59] En personas no aptas para la cirugía curativa, se puede utilizar quimioterapia para prolongar la vida o mejorar su calidad . [3] Antes de la cirugía, se puede utilizar quimioterapia neoadyuvante o quimiorradioterapia en casos que se consideran "resecables al límite" (ver Estadificación) para reducir el cáncer a un nivel en el que la cirugía podría ser beneficiosa. En otros casos, la terapia neoadyuvante sigue siendo controvertida, porque retrasa la cirugía. [3] [4] [87]
La gemcitabina fue aprobada por la Administración de Alimentos y Medicamentos de los Estados Unidos (FDA) en 1997, después de que un ensayo clínico informara mejoras en la calidad de vida y una mejora de cinco semanas en la duración media de supervivencia en personas con cáncer de páncreas avanzado. [88] Este fue el primer fármaco de quimioterapia aprobado por la FDA principalmente para un criterio de valoración de ensayo clínico no de supervivencia. [89] La quimioterapia con gemcitabina sola fue el estándar durante aproximadamente una década, ya que varios ensayos que la probaron en combinación con otros fármacos no lograron demostrar resultados significativamente mejores. Sin embargo, se descubrió que la combinación de gemcitabina con erlotinib aumentaba la supervivencia modestamente, y la FDA autorizó el uso de erlotinib en el cáncer de páncreas en 2005. [90]
El régimen de quimioterapia FOLFIRINOX , que utiliza cuatro fármacos, resultó ser más eficaz que la gemcitabina, pero con importantes efectos secundarios, por lo que solo es adecuado para personas con un buen estado funcional. Esto también es cierto en el caso del paclitaxel unido a proteínas (nab-paclitaxel), que fue autorizado por la FDA en 2013 para su uso con gemcitabina en el cáncer de páncreas. [91] A finales de 2013, tanto FOLFIRINOX como nab-paclitaxel con gemcitabina se consideraban buenas opciones para quienes podían tolerar los efectos secundarios, y la gemcitabina seguía siendo una opción eficaz para quienes no los toleraban. Se espera un ensayo comparativo entre las dos nuevas opciones, y continúan los ensayos que investigan otras variaciones. Sin embargo, los cambios de los últimos años solo han aumentado los tiempos de supervivencia en unos pocos meses. [88] A menudo se realizan ensayos clínicos para terapias adyuvantes novedosas. [4]
Radioterapia
El papel de la radioterapia como tratamiento auxiliar (adyuvante) después de una cirugía potencialmente curativa ha sido controvertido desde la década de 1980. [3] A principios de la década de 2000, el Grupo de Estudio Europeo para la Investigación del Cáncer de Páncreas ( ESPAC ) mostró la superioridad pronóstica de la quimioterapia adyuvante sobre la quimiorradioterapia. [92] [93] [4] La Sociedad Europea de Oncología Médica recomienda que la radioterapia adyuvante solo se utilice en personas inscritas en ensayos clínicos. [59] Sin embargo, existe una tendencia continua entre los médicos de los EE. UU. a estar más dispuestos a utilizar la radioterapia adyuvante que los de Europa. Muchos ensayos clínicos han probado una variedad de combinaciones de tratamientos desde la década de 1980, pero no han logrado resolver el asunto de manera concluyente. [3] [4]
La radioterapia puede formar parte del tratamiento para intentar reducir el tamaño de un tumor hasta que sea resecable, pero su uso en tumores irresecables sigue siendo controvertido, ya que existen resultados contradictorios de los ensayos clínicos. Los resultados preliminares de un ensayo, presentado en 2013, "redujeron notablemente el entusiasmo" por su uso en tumores localmente avanzados. [2]
PanNET
El tratamiento de los PanNET, incluidos los tipos malignos menos comunes , puede incluir una serie de enfoques. [67] [94] [95] [96] Algunos tumores pequeños de menos de 1 cm que se identifican incidentalmente, por ejemplo en una tomografía computarizada realizada para otros fines, pueden ser seguidos por una espera vigilante . [67] Esto depende del riesgo evaluado de la cirugía que está influenciado por el sitio del tumor y la presencia de otros problemas médicos . [67] Los tumores dentro del páncreas únicamente (tumores localizados), o con metástasis limitadas, por ejemplo al hígado, pueden extirparse mediante cirugía. El tipo de cirugía depende de la ubicación del tumor y el grado de propagación a los ganglios linfáticos. [24]
En el caso de tumores localizados, el procedimiento quirúrgico puede ser mucho menos extenso que los tipos de cirugía utilizados para tratar el adenocarcinoma pancreático descritos anteriormente, pero por lo demás los procedimientos quirúrgicos son similares a los de los tumores exocrinos. El rango de posibles resultados varía mucho; algunos tipos tienen una tasa de supervivencia muy alta después de la cirugía, mientras que otros tienen un pronóstico desfavorable. Como todos los de este grupo son raros, las pautas enfatizan que el tratamiento debe realizarse en un centro especializado. [24] [31] El uso del trasplante de hígado puede considerarse en ciertos casos de metástasis hepática. [97]
En el caso de tumores funcionales, la clase de medicamentos análogos de la somatostatina , como la octreotida , puede reducir la producción excesiva de hormonas. [24] La lanreotida puede retardar el crecimiento del tumor. [98] Si el tumor no se puede extirpar quirúrgicamente y está causando síntomas, la terapia dirigida con everolimus o sunitinib puede reducir los síntomas y retardar la progresión de la enfermedad. [31] [99] [100] La quimioterapia citotóxica estándar generalmente no es muy eficaz para los PanNET, pero se puede utilizar cuando otros tratamientos farmacológicos no logran prevenir la progresión de la enfermedad, [31] o en cánceres PanNET poco diferenciados. [101]
En ocasiones, se utiliza radioterapia si hay dolor debido a la extensión anatómica, como la metástasis ósea. Algunos PanNET absorben péptidos u hormonas específicos y pueden responder a la terapia de medicina nuclear con péptidos u hormonas radiomarcados como el iobenguano (yodo-131-MIBG). [102] [103] [104] [105] También se pueden utilizar la ablación por radiofrecuencia (ARF), la crioablación y la embolización de la arteria hepática . [106] [107]
Cuidados paliativos
Los cuidados paliativos son cuidados médicos que se centran en el tratamiento de los síntomas de enfermedades graves, como el cáncer, y en mejorar la calidad de vida. [108] Debido a que el adenocarcinoma de páncreas generalmente se diagnostica después de que ha progresado a una etapa avanzada, los cuidados paliativos como tratamiento de los síntomas suelen ser el único tratamiento posible. [109]
Los cuidados paliativos no se centran en tratar el cáncer subyacente, sino en tratar síntomas como el dolor o las náuseas, y pueden ayudar a tomar decisiones, como cuándo y si los cuidados paliativos serán beneficiosos. [110] El dolor se puede controlar con medicamentos como los opioides o mediante una intervención procedimental, mediante un bloqueo nervioso del plexo celíaco (CPB). Esto altera o, según la técnica utilizada, destruye los nervios que transmiten el dolor desde el abdomen. El CPB es una forma segura y eficaz de reducir el dolor, lo que generalmente reduce la necesidad de usar analgésicos opioides, que tienen efectos secundarios negativos significativos. [3] [111]
Otros síntomas o complicaciones que pueden tratarse con cirugía paliativa son la obstrucción por el tumor de los intestinos o de los conductos biliares . Para esto último, que se produce en más de la mitad de los casos, se puede insertar un pequeño tubo de metal llamado stent mediante un endoscopio para mantener el drenaje de los conductos. [34] Los cuidados paliativos también pueden ayudar a tratar la depresión que a menudo acompaña al diagnóstico de cáncer de páncreas. [3]
Tanto la cirugía como los tumores avanzados inoperables a menudo conducen a trastornos del sistema digestivo por falta de productos exocrinos del páncreas (insuficiencia exocrina). Estos pueden tratarse tomando pancreatina , que contiene enzimas pancreáticas fabricadas y se toma mejor con alimentos. [12] La dificultad para vaciar el estómago (vaciamiento gástrico retardado) es común y puede ser un problema grave, que implica hospitalización. El tratamiento puede implicar una variedad de enfoques, incluido el drenaje del estómago mediante aspiración nasogástrica y medicamentos llamados inhibidores de la bomba de protones o antagonistas H 2 , que reducen la producción de ácido gástrico . [12] También se pueden utilizar medicamentos como la metoclopramida para limpiar el contenido del estómago.
Resultados
| Estadio clínico | Supervivencia a cinco años en Estados Unidos (%) para diagnósticos de 1992 a 1998 | |
|---|---|---|
| Cáncer de páncreas exocrino | Neuroendocrino tratado con cirugía | |
| Yo / Yo | 14 | 61 |
| IB | 12 | |
| IIa / II | 7 | 52 |
| IIB | 5 | |
| III | 3 | 41 |
| IV | 1 | 16 |
El adenocarcinoma de páncreas y otros cánceres exocrinos menos comunes tienen un pronóstico muy malo , ya que normalmente se diagnostican en una etapa tardía cuando el cáncer ya está localmente avanzado o se ha diseminado a otras partes del cuerpo. [2] Los resultados son mucho mejores para los PanNET: muchos son benignos y completamente asintomáticos, e incluso aquellos casos no tratables con cirugía tienen una tasa de supervivencia promedio a cinco años del 16%, [65] aunque el pronóstico varía considerablemente según el tipo. [33]
En el caso de los adenocarcinomas pancreáticos localmente avanzados y metastásicos , que juntos representan más del 80% de los casos, numerosos ensayos que comparan regímenes de quimioterapia han demostrado tiempos de supervivencia mayores, pero no más de un año. [2] [88] La supervivencia general a cinco años para el cáncer de páncreas en los EE. UU. ha mejorado del 2% en los casos diagnosticados entre 1975 y 1977, y del 4% en los diagnósticos entre 1987 y 1989, al 6% entre 2003 y 2009. [112] En menos del 20% de los casos de adenocarcinoma pancreático con diagnóstico de un crecimiento canceroso localizado y pequeño (menos de 2 cm en estadio T1), aproximadamente el 20% de los estadounidenses sobreviven hasta cinco años. [21]
Alrededor de 1500 genes están vinculados a los resultados del adenocarcinoma de páncreas. Estos incluyen tanto genes desfavorables, donde la expresión alta se relaciona con un mal resultado, por ejemplo C-Met y MUC-1 , como genes favorables donde la expresión alta se asocia con una mejor supervivencia, por ejemplo el factor de transcripción PELP1 . [52] [53]
Distribución

En 2015, los cánceres de páncreas de todo tipo provocaron 411.600 muertes en todo el mundo. [8] Se estima que en 2014 se diagnosticará cáncer de páncreas a unas 46.000 personas en los EE. UU. y que 40.000 morirán a causa de esta enfermedad. [2] Aunque representa solo el 2,5 % de los casos nuevos, el cáncer de páncreas es responsable del 6 % de las muertes por cáncer cada año. [113] Es la séptima causa de muerte por cáncer en todo el mundo. [10] El cáncer de páncreas es la quinta causa más común de muerte por cáncer en el Reino Unido, [19] y la tercera más común en los Estados Unidos. [20]
A nivel mundial, el cáncer de páncreas es el undécimo cáncer más común en mujeres y el duodécimo más común en hombres. [10] La mayoría de los casos registrados ocurren en países desarrollados . [10] Las personas de los Estados Unidos tienen un riesgo de por vida promedio de aproximadamente 1 en 67 (o 1,5%) de desarrollar la enfermedad, [114] ligeramente más alto que la cifra para el Reino Unido. [115] La enfermedad es más común en hombres que en mujeres, [2] [10] aunque la diferencia en las tasas se ha reducido en las últimas décadas, probablemente reflejando aumentos anteriores en el tabaquismo femenino. En los Estados Unidos, el riesgo para los afroamericanos es más del 50% mayor que para los blancos , pero las tasas en África y Asia Oriental son mucho más bajas que las de América del Norte o Europa. Estados Unidos, Europa Central y Oriental, y Argentina y Uruguay tienen tasas altas. [10]
PanNET
La incidencia anual de tumores neuroendocrinos pancreáticos (PanNET) clínicamente reconocidos es baja (alrededor de 5 por un millón de personas-año) y está dominada por los tipos no funcionales. [28] Se cree que entre el 45% y el 90% de los PanNET son de tipos no funcionales. [24] [31] Los estudios de autopsias han descubierto PanNET pequeños con bastante frecuencia, lo que sugiere que la prevalencia de tumores que permanecen inertes y asintomáticos puede ser relativamente alta. [31] En general, se cree que los PanNET representan alrededor del 1 al 2% de todos los tumores pancreáticos. [28] La definición y clasificación de los PanNET ha cambiado con el tiempo, lo que afecta lo que se sabe sobre su epidemiología y relevancia clínica. [55]
Historia
Reconocimiento y diagnóstico
El reconocimiento más temprano del cáncer de páncreas se ha atribuido al científico italiano del siglo XVIII Giovanni Battista Morgagni , el padre histórico de la patología anatómica moderna , quien afirmó haber rastreado varios casos de cáncer en el páncreas. Muchos médicos de los siglos XVIII y XIX eran escépticos sobre la existencia de la enfermedad, dada la apariencia similar de la pancreatitis. Algunos informes de casos se publicaron en las décadas de 1820 y 1830, y finalmente el médico estadounidense Jacob Mendes Da Costa registró un diagnóstico histopatológico genuino , quien también dudó de la confiabilidad de las interpretaciones de Morgagni. A principios del siglo XX, el cáncer de la cabeza del páncreas se había convertido en un diagnóstico bien establecido. [116]
En cuanto al reconocimiento de los PanNET, la posibilidad de cáncer de las células de los islotes se sugirió inicialmente en 1888. El primer caso de hiperinsulinismo debido a un tumor de este tipo se informó en 1927. El reconocimiento de un tipo de PanNET no secretor de insulina se atribuye generalmente a los cirujanos estadounidenses, R. M. Zollinger y E. H. Ellison, quienes dieron sus nombres al síndrome de Zollinger-Ellison , después de postular la existencia de un tumor pancreático secretor de gastrina en un informe de dos casos de úlceras pépticas inusualmente graves publicado en 1955. [116] En 2010, la OMS recomendó que los PanNET se denominen tumores "neuroendocrinos" en lugar de "endocrinos". [30]
Las técnicas modernas de diagnóstico por imagen están detectando cada vez más neoplasias precancerosas pequeñas de muchos cánceres de páncreas. Un tipo, la neoplasia mucinosa papilar intraductal (NMPI), fue descrita por primera vez por investigadores japoneses en 1982. En 2010 se observó que: "Durante la década siguiente, se prestó poca atención a este informe; sin embargo, durante los 15 años posteriores, ha habido una explosión virtual en el reconocimiento de este tumor". [66]
Cirugía
La primera pancreatoduodenectomía parcial de la que se tiene noticia fue realizada por el cirujano italiano Alessandro Codivilla en 1898, pero el paciente sólo sobrevivió 18 días antes de sucumbir a las complicaciones. Las primeras operaciones se vieron comprometidas en parte por la creencia errónea de que las personas morirían si se les extirpaba el duodeno y también, al principio, si se detenía el flujo de jugos pancreáticos. Más tarde se creyó, también erróneamente, que el conducto pancreático podía simplemente ligarse sin efectos adversos graves; de hecho, muy a menudo supura más adelante. En 1907-1908, después de algunas operaciones más infructuosas realizadas por otros cirujanos, cirujanos franceses probaron procedimientos experimentales en cadáveres. [117]
En 1912, el cirujano alemán Walther Kausch fue el primero en extirpar grandes partes del duodeno y el páncreas juntos ( en bloque ). Esto ocurrió en Breslau, hoy Wrocław , en Polonia. En 1918 se demostró, en operaciones en perros, que es posible sobrevivir incluso después de la extirpación completa del duodeno, pero no se informó de un resultado similar en cirugía humana hasta 1935, cuando el cirujano estadounidense Allen Oldfather Whipple publicó los resultados de una serie de tres operaciones en el Hospital Presbiteriano de Columbia en Nueva York. Solo a uno de los pacientes se le extirpó el duodeno por completo, pero sobrevivió durante dos años antes de morir de metástasis en el hígado.
La primera operación no fue planificada, ya que el cáncer se descubrió en el quirófano. El éxito de Whipple mostró el camino para el futuro, pero la operación siguió siendo difícil y peligrosa hasta las últimas décadas. Publicó varias mejoras de su procedimiento, incluida la primera extirpación total del duodeno en 1940, pero solo realizó un total de 37 operaciones. [117]
El descubrimiento a finales de los años 30 de que la vitamina K prevenía el sangrado por ictericia y el desarrollo de la transfusión sanguínea como un proceso cotidiano mejoraron la supervivencia posoperatoria, [117] pero alrededor del 25% de las personas nunca salían con vida del hospital hasta los años 70. [118] En los años 70, un grupo de cirujanos estadounidenses escribió instando a que el procedimiento era demasiado peligroso y debería abandonarse. Desde entonces, los resultados en centros más grandes han mejorado considerablemente y la mortalidad de la operación suele ser inferior al 4%. [26]
En 2006 se publicó un informe sobre una serie de 1.000 pancreatoduodenectomías consecutivas realizadas por un solo cirujano del Hospital Johns Hopkins entre 1969 y 2003. La tasa de estas operaciones había aumentado de manera constante durante este período, con solo tres de ellas antes de 1980, y el tiempo operatorio medio se redujo de 8,8 horas en la década de 1970 a 5,5 horas en la década de 2000, y la mortalidad dentro de los 30 días o en el hospital fue solo del 1%. [117] [118] Otra serie de 2.050 operaciones en el Hospital General de Massachusetts entre 1941 y 2011 mostró un panorama similar de mejora. [119]
Direcciones de investigación
Esta sección necesita ser actualizada . ( Mayo de 2023 ) |
La investigación en etapa temprana sobre el cáncer de páncreas incluye estudios de genética y detección temprana, tratamiento en diferentes etapas del cáncer, estrategias quirúrgicas y terapias dirigidas , como la inhibición de factores de crecimiento , terapias inmunológicas y vacunas . [44] [120] [121] [122] [123] Los ácidos biliares pueden tener un papel en la carcinogénesis del cáncer de páncreas. [124] [125]
Una pregunta clave es el momento en que se producen los acontecimientos a medida que la enfermedad se desarrolla y progresa, en particular el papel de la diabetes [120] [36] y cómo y cuándo se propaga la enfermedad. [126] El conocimiento de que la aparición de diabetes puede ser un signo temprano de la enfermedad podría facilitar el diagnóstico y la prevención oportunos si se puede desarrollar una estrategia de detección viable. [120] [36] [127] El ensayo del Registro Europeo de Pancreatitis Hereditaria y Cáncer de Páncreas Familiar (EUROPAC) tiene como objetivo determinar si la detección regular es apropiada para las personas con antecedentes familiares de la enfermedad. [128]
Se está evaluando la cirugía por ojo de cerradura ( laparoscopia ) en lugar del procedimiento de Whipple , particularmente en términos de tiempo de recuperación. [129] La electroporación irreversible es una técnica de ablación relativamente novedosa con potencial para reducir la estadificación y prolongar la supervivencia en personas con enfermedad localmente avanzada, especialmente para tumores en proximidad a vasos peripancreáticos sin riesgo de traumatismo vascular. [130] [131]
Se están realizando esfuerzos para desarrollar nuevos medicamentos, incluidos aquellos dirigidos a los mecanismos moleculares de la aparición del cáncer, [132] [133] células madre , [85] y proliferación celular . [133] [134] Un enfoque adicional implica el uso de inmunoterapia , como virus oncolíticos . [135] Se están estudiando los mecanismos específicos de galectina del microambiente tumoral . [136]
Las nanopartículas ayudan en la liberación sostenida y dirigida de un régimen farmacológico a sitios específicos del cáncer o tumor en lugar de afectar las células sanas, lo que produce una toxicidad insignificante o nula. [137]
Véase también
- Cáncer gastrointestinal
- Red de Acción contra el Cáncer de Páncreas (organización en EE. UU.)
- Fundación Lustgarten para la investigación del cáncer de páncreas (organización en EE. UU.)
- Lista de personas diagnosticadas con cáncer de páncreas
Referencias
- ^ abcdefg «Pancreatic Cancer Treatment (PDQ®) Patient Version» (Tratamiento del cáncer de páncreas [PDQ®], versión para pacientes). Instituto Nacional del Cáncer. Institutos Nacionales de la Salud. 17 de abril de 2014. Archivado desde el original el 5 de julio de 2014. Consultado el 8 de junio de 2014 .
- ^ abcdefghijklmnopqrstu vwxyz aa ab ac ad ae af Ryan DP, Hong TS, Bardeesy N (septiembre de 2014). "Adenocarcinoma de páncreas". La Revista de Medicina de Nueva Inglaterra . 371 (11): 1039–49. doi :10.1056/NEJMra1404198. PMID 25207767.
- ^ abcdefghijklmnopqrstu vwxyz aa ab ac ad ae af ag Wolfgang CL, Herman JM, Laheru DA, Klein AP, Erdek MA, Fishman EK, et al. (septiembre de 2013). "Progreso reciente en cáncer de páncreas". CA: A Cancer Journal for Clinicians . 63 (5): 318–48. doi :10.3322/caac.21190. PMC 3769458 . PMID 23856911.
- ^ abcdefghijk Vincent A, Herman J, Schulick R, Hruban RH, Goggins M (agosto de 2011). "Pancreatic cancer" (PDF) . Lancet . 378 (9791): 607–20. doi :10.1016/S0140-6736(10)62307-0. PMC 3062508 . PMID 21620466. Archivado desde el original (PDF) el 12 de enero de 2015.
- ^ ab "¿Se puede prevenir el cáncer de páncreas?". Sociedad Estadounidense del Cáncer. 11 de junio de 2014. Archivado desde el original el 13 de noviembre de 2014. Consultado el 13 de noviembre de 2014 .
- ^ ab "La tasa de supervivencia del cáncer de páncreas a cinco años aumenta al 12%". PANCAN . 2023. Archivado desde el original el 4 de marzo de 2023 . Consultado el 3 de marzo de 2023 .
- ^ Vos T, Allen C, Arora M, Barber RM, Bhutta ZA, Brown A, et al. (Colaboradores de incidencia y prevalencia de enfermedades y lesiones del GBD 2015) (octubre de 2016). "Incidencia, prevalencia y años vividos con discapacidad a nivel mundial, regional y nacional para 310 enfermedades y lesiones, 1990-2015: un análisis sistemático para el Estudio de la carga mundial de enfermedades de 2015". The Lancet . 388 (10053): 1545–1602. doi :10.1016/S0140-6736(16)31678-6. PMC 5055577 . PMID 27733282.
- ^ abc Wang H, Naghavi M, Allen C, Barber RM, Bhutta ZA, Carter A, et al. (Colaboradores de GBD 2015 Mortality and Causes of Death) (octubre de 2016). "Esperanza de vida global, regional y nacional, mortalidad por todas las causas y mortalidad por causas específicas para 249 causas de muerte, 1980-2015: un análisis sistemático para el Estudio de la Carga Global de Enfermedades 2015". The Lancet . 388 (10053): 1459–1544. doi :10.1016/s0140-6736(16)31012-1. PMC 5388903 . PMID 27733281.
- ^ "¿Qué es el cáncer? Definición del cáncer". Instituto Nacional del Cáncer, Institutos Nacionales de Salud. 7 de marzo de 2014. Archivado desde el original el 25 de junio de 2014 . Consultado el 5 de diciembre de 2014 .
- ^ abcdefghijklmnopqrst Informe mundial sobre el cáncer . Organización Mundial de la Salud. 2014. Capítulo 5.7. ISBN 978-92-832-0429-9.
- ^ abcde A menos que se especifique lo contrario en los recuadros, la referencia es: Pishvaian MJ, Brody JR (marzo de 2017). "Implicaciones terapéuticas de la subtipificación molecular para el cáncer de páncreas". Oncología . 31 (3): 159–66, 168. PMID 28299752.
- ^ abcdefghijklmnopqrstu vw Bond-Smith G, Banga N, Hammond TM, Imber CJ (mayo de 2012). "Adenocarcinoma de páncreas". BMJ . 344 (1 de mayo de 2012): e2476. doi :10.1136/bmj.e2476. PMID 22592847. S2CID 206894869.
- ^ "Declaración preliminar de recomendación: Cáncer de páncreas: detección". Grupo de trabajo de servicios preventivos de Estados Unidos . Consultado el 11 de febrero de 2019 .
- ^ Amri F, Belkhayat C, Yeznasni A, Koulali H, Jabi R, Zazour A, et al. (septiembre de 2023). "Asociación entre el cáncer de páncreas y la diabetes: perspectivas de un estudio de cohorte retrospectivo". BMC Cancer . 23 (1): 856. doi : 10.1186/s12885-023-11344-w . PMC 10496157 . PMID 37697301.
- ^ Sun Y, He X, Sun Y (27 de septiembre de 2023). "Carne roja y procesada y riesgo de cáncer de páncreas: un metanálisis". Frontiers in Nutrition . 10 : 1249407. doi : 10.3389/fnut.2023.1249407 . PMC 10565855 . PMID 37829734.
- ^ ab Larsson SC, Wolk A (enero de 2012). "Consumo de carne roja y procesada y riesgo de cáncer de páncreas: metaanálisis de estudios prospectivos". British Journal of Cancer . 106 (3): 603–607. doi :10.1038/bjc.2011.585. PMC 3273353 . PMID 22240790.
- ^ Rohrmann S, Linseisen J, Nöthlings U, Overvad K, Egeberg R, Tjønneland A, et al. (febrero de 2013). "Consumo de carne y pescado y riesgo de cáncer de páncreas: resultados de la investigación prospectiva europea sobre cáncer y nutrición". Revista internacional del cáncer . 132 (3): 617–624. doi : 10.1002/ijc.27637 . PMID 22610753. S2CID 2613568.
- ^ Bardou M, Le Ray I (diciembre de 2013). "Tratamiento del cáncer de páncreas: una revisión narrativa de estudios de costo-efectividad". Mejores prácticas e investigación. Gastroenterología clínica . 27 (6): 881–892. doi :10.1016/j.bpg.2013.09.006. PMID 24182608.
- ^ ab "Datos y cifras sobre el cáncer: por qué existimos". Fondo de investigación sobre el cáncer de páncreas . Consultado el 5 de abril de 2019 .
- ^ ab "Cáncer de páncreas: estadísticas sobre el cáncer". SEER . Consultado el 4 de abril de 2019 .
- ^ ab "Tratamiento del cáncer de páncreas (PDQ®) Versión para profesionales de la salud". Instituto Nacional del Cáncer. Institutos Nacionales de la Salud. 21 de febrero de 2014. Archivado desde el original el 22 de octubre de 2014 . Consultado el 24 de noviembre de 2014 ."La tasa de curación más alta se da si el tumor está realmente localizado en el páncreas; sin embargo, esta etapa de la enfermedad representa menos del 20% de los casos. En los casos con enfermedad localizada y cánceres pequeños (<2 cm) sin metástasis en los ganglios linfáticos y sin extensión más allá de la cápsula del páncreas, la resección quirúrgica completa todavía se asocia con una tasa de supervivencia actuarial a cinco años baja del 18% al 24%".
- ^ Wang Y, Miller FH, Chen ZE, Merrick L, Mortele KJ, Hoff FL, et al. (2011). "Imágenes por resonancia magnética ponderadas por difusión de lesiones sólidas y quísticas del páncreas". Radiographics . 31 (3): E47–E64. doi :10.1148/rg.313105174. PMID 21721197.
- ^ Harris RE (2013). "Epidemiología del cáncer de páncreas". Epidemiología de las enfermedades crónicas . Jones & Bartlett. págs. 181–190. ISBN 978-0-7637-8047-0Archivado desde el original el 24 de junio de 2016.
- ^ abcdefg Öberg K, Knigge U, Kwekkeboom D, Perren A, et al. (Grupo de trabajo de directrices de la ESMO) (octubre de 2012). "Tumores neuroendocrinos gastroenteropancreáticos: directrices de práctica clínica de la ESMO para el diagnóstico, el tratamiento y el seguimiento". Annals of Oncology . 23 (Supl. 7): vii124–vii130. doi : 10.1093/annonc/mds295 . PMID 22997445.(La Tabla 5 describe el sistema de estadificación TNM propuesto para PanNET).
- ^ Manual del cáncer de páncreas. Nueva York: Springer. 2009. pág. 288. ISBN 978-0-387-77497-8Archivado desde el original el 10 de septiembre de 2017 . Consultado el 12 de junio de 2016 .
- ^ ab Govindan R (2011). Cáncer de DeVita, Hellman y Rosenberg: Cáncer: Principios y práctica de la oncología (novena edición). Lippincott Williams & Wilkins. Capítulo 35: Cáncer de páncreas: tratamiento quirúrgico. ISBN 978-1-4511-0545-2.Edición en línea, con actualizaciones hasta 2014
- ^ abc Tobias JS, Hochhauser D (2014). Cáncer y su tratamiento (7.ª ed.). John Wiley & Sons. pág. 297. ISBN 978-1-118-46871-5.
- ^ abc "Tipos de tumores de páncreas". Centro de investigación del cáncer de páncreas Sol Goldman . Johns Hopkins Medicine. 2012. Archivado desde el original el 8 de octubre de 2014. Consultado el 18 de noviembre de 2014 .
- ^ Farrell JJ, Fernández-del Castillo C (junio de 2013). "Neoplasias quísticas pancreáticas: manejo y preguntas sin respuesta". Gastroenterología . 144 (6): 1303–15. doi :10.1053/j.gastro.2013.01.073. PMID 23622140.
- ^ abc La denominación PanNET está en línea con las directrices de la OMS para la clasificación de tumores del sistema digestivo «Clasificación de tumores del sistema digestivo de la OMS – Catálogo NLM – NCBI». Archivado desde el original el 9 de septiembre de 2017 . Consultado el 7 de septiembre de 2017 .publicado en 2010. Históricamente, los PanNET también han recibido diversos términos y todavía se los llama comúnmente "tumores endocrinos pancreáticos". Véase: Klimstra DS, Modlin IR, Coppola D, Lloyd RV, Suster S (agosto de 2010). "La clasificación patológica de los tumores neuroendocrinos: una revisión de los sistemas de nomenclatura, clasificación y estadificación". Páncreas . 39 (6): 707–12. doi : 10.1097/MPA.0b013e3181ec124e . PMID 20664470. S2CID 3735444.
- ^ abcdefgh Burns WR, Edil BH (marzo de 2012). "Tumores pancreáticos neuroendocrinos: pautas para el manejo y actualización". Opciones de tratamiento actuales en oncología . 13 (1): 24–34. doi :10.1007/s11864-011-0172-2. PMID 22198808. S2CID 7329783.
- ^ El sistema de indexación de encabezamientos de materias médicas hace referencia al "carcinoma de células de los islotes", que se subdivide en gastrinoma, glucagonoma , somatostatinoma y VIPoma . Véase: árbol MeSH de 2014 en "Pancreatic Neoplasms [C04.588.322.475]" Archivado el 19 de marzo de 2016 en Wayback Machine. 16 de octubre de 2014
- ^ ab "Tumores de células de los islotes del páncreas / Neoplasias endocrinas del páncreas". Centro de investigación del cáncer de páncreas Sol Goldman . Johns Hopkins Medicine. 2012. Archivado desde el original el 5 de enero de 2015. Consultado el 5 de enero de 2015 .
- ^ abcdefg De La Cruz MS, Young AP, Ruffin MT (abril de 2014). "Diagnóstico y tratamiento del cáncer de páncreas". American Family Physician . 89 (8): 626–32. PMID 24784121.
- ^ ab Alberts SR, Goldberg RM (2009). "Capítulo 9: Cánceres del tracto gastrointestinal" . En Casciato DA, Territo MC (eds.). Manual de oncología clínica. Lippincott Williams & Wilkins. págs. 188–236. ISBN 978-0-7817-6884-9.
- ^ abc Pannala R, Basu A, Petersen GM, Chari ST (enero de 2009). "Diabetes de nueva aparición: una posible pista para el diagnóstico temprano del cáncer de páncreas". The Lancet. Oncología . 10 (1): 88–95. doi :10.1016/S1470-2045(08)70337-1. PMC 2795483 . PMID 19111249.
- ^ "Capítulo 15; Páncreas" (PDF) . Manual de estadificación del cáncer (2.ª ed.). Comité Conjunto Estadounidense sobre Cáncer. págs. 95–98. Archivado (PDF) desde el original el 29 de noviembre de 2014.Consulte la página 95 para la cita sobre "... menor grado de afectación de los huesos, el cerebro y otros sitios anatómicos".
- ^ Sperti C, Moletta L, Patanè G (octubre de 2014). "Tumores metastásicos en el páncreas: el papel de la cirugía". Revista mundial de oncología gastrointestinal . 6 (10): 381–92. doi : 10.4251/wjgo.v6.i10.381 . PMC 4197429 . PMID 25320654.
- ^ "Causas del cáncer de páncreas". NHS Choices . Servicio Nacional de Salud, Inglaterra. 7 de octubre de 2014. Archivado desde el original el 6 de noviembre de 2014. Consultado el 5 de diciembre de 2014 .
- ^ Anderson LN, Cotterchio M, Gallinger S (agosto de 2009). "Factores de estilo de vida, dieta e historial médico asociados con el riesgo de cáncer de páncreas en Ontario, Canadá". Cancer Causes & Control . 20 (6): 825–834. doi :10.1007/s10552-009-9303-5. PMC 3907069 . PMID 19194662.
- ^ Bosetti C, Lucenteforte E, Silverman DT, Petersen G, Bracci PM, Ji BT, et al. (julio de 2012). "Fumar cigarrillos y cáncer de páncreas: un análisis del Consorcio Internacional de Casos y Controles de Cáncer de Páncreas (Panc4)". Anales de Oncología . 23 (7): 1880–88. doi :10.1093/annonc/mdr541. PMC 3387822 . PMID 22104574.
- ^ De Rubeis V, Cotterchio M, Smith BT, Griffith LE, Borgida A, Gallinger S, et al. (septiembre de 2019). "Trayectorias del índice de masa corporal, desde la adolescencia hasta la adultez avanzada, y riesgo de cáncer de páncreas; un estudio de casos y controles basado en la población en Ontario, Canadá". Cancer Causes & Control . 30 (9): 955–966. doi : 10.1007/s10552-019-01197-9 . PMC 6685923 . PMID 31230151.
- ^ Peters ML, Tseng JF, Miksad RA (julio de 2016). "Pruebas genéticas en el adenocarcinoma ductal pancreático: implicaciones para la prevención y el tratamiento". Clinical Therapeutics . 38 (7): 1622–35. doi : 10.1016/j.clinthera.2016.03.006 . PMID 27041411.
- ^ abc Reznik R, Hendifar AE, Tuli R (2014). "Determinantes genéticos y posibles dianas terapéuticas para el adenocarcinoma de páncreas". Frontiers in Physiology . 5 : 87. doi : 10.3389/fphys.2014.00087 . PMC 3939680 . PMID 24624093.
- ^ Greenhalf W, Grocock C, Harcus M, Neoptolemos J (mayo de 2009). "Detección de cáncer de páncreas en familias con alto riesgo". Pancreatología . 9 (3): 215–22. doi :10.1159/000210262. PMID 19349734. S2CID 29100310.
- ^ Venturi S (agosto de 2021). "El cesio en la biología, el cáncer de páncreas y la controversia sobre los daños causados por la exposición a la radiación alta y baja: aspectos científicos, ambientales, geopolíticos y económicos". Revista internacional de investigación ambiental y salud pública . 18 (17): 8934. doi : 10.3390/ijerph18178934 . PMC 8431133 . PMID 34501532.
 El texto fue copiado de esta fuente, que está disponible bajo una Licencia Creative Commons Atribución 4.0 Internacional.
El texto fue copiado de esta fuente, que está disponible bajo una Licencia Creative Commons Atribución 4.0 Internacional. - ^ ab "Datos y cifras sobre el cáncer 2014" (PDF) . Sociedad Estadounidense del Cáncer . Archivado (PDF) del original el 18 de diciembre de 2014 . Consultado el 5 de enero de 2015 ., p. 19, "Aunque aún se están acumulando evidencias, el consumo de carne roja o procesada, o de carne cocinada a temperaturas muy altas, puede aumentar levemente el riesgo".
- ^ ab Pericleous M, Rossi RE, Mandair D, Whyand T, Caplin ME (enero de 2014). "Nutrición y cáncer de páncreas". Anticancer Research . 34 (1): 9–21. PMID 24403441.
- ^ Hackeng WM, Hruban RH, Offerhaus GJ, Brosens LA (junio de 2016). "Patología quirúrgica y molecular de las neoplasias pancreáticas". Patología diagnóstica . 11 (1): 47. doi : 10.1186/s13000-016-0497-z . PMC 4897815 . PMID 27267993. (distribuida bajo los términos de la Licencia Creative Commons Attribution 4.0 International (http://creativecommons.org/licenses/by/4.0/)), Título de la imagen y optimización: Mikael Häggström, MD
- ^ Delpu Y, Hanoun N, Lulka H, Sicard F, Selves J, Buscail L, et al. (marzo de 2011). "Alteraciones genéticas y epigenéticas en la carcinogénesis pancreática". Current Genomics . 12 (1): 15–24. doi :10.2174/138920211794520132. PMC 3129039 . PMID 21886451.
- ^ Rooney SL, Shi J (octubre de 2016). "Neoplasia tubulopapilar intraductal del páncreas: una actualización desde la perspectiva de un patólogo". Archivos de patología y medicina de laboratorio . 140 (10): 1068–73. doi : 10.5858/arpa.2016-0207-RA . PMID 27684978.
- ^ ab "El proteoma patológico humano en el cáncer de páncreas – Atlas de proteínas humanas". www.proteinatlas.org . Consultado el 28 de septiembre de 2017 .
- ^ ab Uhlen M, Zhang C, Lee S, Sjöstedt E, Fagerberg L, Bidkhori G, et al. (Agosto de 2017). "Un atlas de patología del transcriptoma del cáncer humano". Ciencia . 357 (6352): ean2507. doi : 10.1126/ciencia.aan2507 . PMID 28818916.
- ^ ab Park W, Chawla A, O'Reilly EM (7 de septiembre de 2021). "Cáncer de páncreas: una revisión". JAMA . 326 (9): 851. doi :10.1001/jama.2021.13027.
- ^ ab Lewis MA, Yao JC (febrero de 2014). "Patología molecular y genética de los tumores neuroendocrinos gastrointestinales". Current Opinion in Endocrinology, Diabetes and Obesity . 21 (1): 22–27. doi :10.1097/MED.0000000000000033. PMID 24310147. S2CID 31094880.
- ^ Thakker RV, Newey PJ, Walls GV, Bilezikian J, Dralle H, Ebeling PR, et al. (septiembre de 2012). "Pautas de práctica clínica para la neoplasia endocrina múltiple tipo 1 (MEN1)". The Journal of Clinical Endocrinology and Metabolism . 97 (9): 2990–3011. doi : 10.1210/jc.2012-1230 . PMID 22723327.
- ^ Fitzgerald JE, White MJ, Lobo DN (abril de 2009). "Vesícula biliar de Courvoisier: ¿ley o signo?". Revista Mundial de Cirugía . 33 (4): 886–91. doi :10.1007/s00268-008-9908-y. PMID 19190960. S2CID 21799234.
- ^ Piraka C, Scheiman JM (septiembre de 2011). "Nuevas modalidades de diagnóstico por imágenes para la enfermedad pancreática". Current Opinion in Gastroenterology . 27 (5): 475–80. doi :10.1097/MOG.0b013e328349e30c. PMID 21743318. S2CID 38963685.
- ^ abcd Seufferlein T, Bachet JB, Van Cutsem E, Rougier P (octubre de 2012). "Adenocarcinoma de páncreas: pautas de práctica clínica de ESMO-ESDO para diagnóstico, tratamiento y seguimiento". Anales de oncología . 23 (Supl. 7): vii33–40. doi : 10.1093/annonc/mds224 . PMID 22997452.
- ^ abcd Imagen de Mikael Häggström, MD.
Referencias para artículos: Navale P, Savari O, Tomashefski Jr JF, Vyas M. "Neoplasia pseudopapilar sólida".Última actualización del autor: 4 de marzo de 2022 - ^ Skafida E, Grammatoglou X, Glava C, Zissis D, Paschalidis N, Katsamagkou E, et al. (febrero de 2010). "Carcinoma adenoescamoso de páncreas: reporte de un caso". Diario de Casos . 3 (1): 41. doi : 10.1186/1757-1626-3-41 . PMC 2825199 . PMID 20205828.
- ^ Agostini-Vulaj D. "Páncreas – Tumores exocrinos / carcinomas – Neoplasia mucinosa papilar intraductal (NMIP)". Esquemas de patología .Tema finalizado: 1 de julio de 2018. Revisado: 9 de marzo de 2020
- ^ Adsay V, Mino-Kenudson M, Furukawa T, Basturk O, Zamboni G, Marchegiani G, et al. (enero de 2016). "Evaluación patológica y notificación de neoplasias mucinosas papilares intraductales del páncreas y otras neoplasias intraepiteliales tumorales del tracto pancreatobiliar: recomendaciones de la reunión de consenso de Verona". Anales de cirugía . 263 (1): 162–77. doi :10.1097/SLA.0000000000001173. PMC 4568174 . PMID 25775066.
- ^ Cascinu S, Falconi M, Valentini V, Jelic S (mayo de 2010). "Cáncer de páncreas: pautas de práctica clínica de la ESMO para diagnóstico, tratamiento y seguimiento". Anales de oncología . 21 (suplemento 5): v55–58. doi : 10.1093/annonc/mdq165 . PMID 20555103.
- ^ abc «Estadificación del cáncer de páncreas». Sociedad Estadounidense del Cáncer . 11 de junio de 2014. Archivado desde el original el 10 de agosto de 2020. Consultado el 29 de septiembre de 2014 .
- ^ ab Zyromski NJ, Nakeeb A, Lillemoe KD (2010). "Capítulo 35: Cáncer de páncreas: tratamiento quirúrgico". En Silberman H, Silberman AW (eds.). Principios y práctica de la oncología quirúrgica: enfoque multidisciplinario para problemas difíciles (edición en línea). Filadelfia: Wolters Kluwer/Lippincott Williams & Wilkins. ISBN 978-0-7817-6546-6Archivado desde el original el 6 de febrero de 2015 . Consultado el 3 de noviembre de 2014 .
- ^ abcd "Tumores neuroendocrinos, Pautas de la NCCN versión 1.2015" (PDF) . National Comprehensive Cancer Network, Inc. (NCCN). 11 de noviembre de 2014. Consultado el 25 de diciembre de 2014 .
- ^ Instituto Nacional del Cáncer. Tumores neuroendocrinos pancreáticos (tumores de células de los islotes) Tratamiento (PDQ®) Incidencia y mortalidad "Tumores neuroendocrinos pancreáticos (tumores de células de los islotes) Tratamiento (PDQ®)–Versión para profesionales de salud". Archivado desde el original el 4 de enero de 2015 . Consultado el 29 de diciembre de 2014 .
- ^ "Factores de dieta y actividad que afectan los riesgos de ciertos tipos de cáncer: sección sobre cáncer de páncreas". Sociedad Estadounidense del Cáncer . 20 de agosto de 2012. Archivado desde el original el 4 de noviembre de 2014. Consultado el 4 de noviembre de 2014 .
- ^ Owens DK, Davidson KW, Krist AH, Barry MJ, Cabana M, Caughey AB, et al. (agosto de 2019). "Detección del cáncer de páncreas: declaración de recomendación reafirmada del grupo de trabajo de servicios preventivos de EE. UU." JAMA . 322 (5): 438–44. doi : 10.1001/jama.2019.10232 . PMID 31386141.
- ^ He XY, Yuan YZ (agosto de 2014). "Avances en la investigación del cáncer de páncreas: hacia la detección temprana". Revista Mundial de Gastroenterología . 20 (32): 11241–48. doi : 10.3748/wjg.v20.i32.11241 . PMC 4145762 . PMID 25170208.
- ^ ab Okano K, Suzuki Y (agosto de 2014). "Estrategias para la detección temprana del cáncer de páncreas resecable". Revista Mundial de Gastroenterología . 20 (32): 11230–40. doi : 10.3748/wjg.v20.i32.11230 . PMC 4145761 . PMID 25170207.
- ^ Goggins M, Overbeek KA, Brand R, Syngal S, Del Chiaro M, Bartsch DK, et al. (enero de 2020). "Manejo de pacientes con mayor riesgo de cáncer de páncreas familiar: recomendaciones actualizadas del Consorcio Internacional de Detección del Cáncer de Páncreas (CAPS)". Gut . 69 (1): 7–17. doi : 10.1136/gutjnl-2019-319352 . PMC 7295005 . PMID 31672839.
- ^ Sun J, Li Y, Liu L, Jiang Z, Liu G (diciembre de 2019). "Uso de aspirina y riesgo de cáncer de páncreas: una revisión sistemática de estudios observacionales". Medicina . 98 (51): e18033. doi :10.1097/MD.0000000000018033. PMC 6940047 . PMID 31860953.
- ^ Gurusamy KS, Kumar S, Davidson BR, Fusai G (febrero de 2014). "Resección versus otros tratamientos para el cáncer de páncreas localmente avanzado". Base de datos Cochrane de revisiones sistemáticas . 2014 (2): CD010244. doi :10.1002/14651858.CD010244.pub2. PMC 11095847. PMID 24578248 .
- ^ ab Mollberg N, Rahbari NN, Koch M, Hartwig W, Hoeger Y, Büchler MW, et al. (diciembre de 2011). "Resección arterial durante la pancreatectomía para el cáncer de páncreas: una revisión sistemática y un metanálisis". Anales de cirugía . 254 (6): 882–93. doi :10.1097/SLA.0b013e31823ac299. PMID 22064622. S2CID 42685174.
- ^ abc "Adenocarcinoma de páncreas. Pautas de la NCCN, versión 1.2015" (PDF) . Pautas de la NCCN . National Comprehensive Cancer Network, Inc. 4 de diciembre de 2014 . Consultado el 26 de diciembre de 2014 .
- ^ Alamo JM, Marín LM, Suarez G, Bernal C, Serrano J, Barrera L, et al. (octubre de 2014). "Mejora de los resultados en el cáncer de páncreas: puntos clave en el manejo perioperatorio". Revista Mundial de Gastroenterología . 20 (39): 14237–45. doi : 10.3748/wjg.v20.i39.14237 . PMC 4202352 . PMID 25339810.
- ^ Lopez NE, Prendergast C, Lowy AM (agosto de 2014). "Cáncer de páncreas resecable limítrofe: definiciones y tratamiento". Revista Mundial de Gastroenterología . 20 (31): 10740–51. doi : 10.3748/wjg.v20.i31.10740 . PMC 4138454 . PMID 25152577.
- ^ Polistina F, Di Natale G, Bonciarelli G, Ambrosino G, Frego M (julio de 2014). "Estrategias neoadyuvantes para el cáncer de páncreas". Revista Mundial de Gastroenterología . 20 (28): 9374–83. doi : 10.3748/wjg.v20.i28.9374 (inactivo el 12 de septiembre de 2024). PMC 4110569 . PMID 25071332.
{{cite journal}}: CS1 maint: DOI inactivo a partir de septiembre de 2024 ( enlace ) - ^ Gillen S, Schuster T, Meyer Zum Büschenfelde C, Friess H, Kleeff J (abril de 2010). "Terapia preoperatoria/neoadyuvante en cáncer de páncreas: una revisión sistemática y un metanálisis de los porcentajes de respuesta y resección". PLOS Medicine . 7 (4): e1000267. doi : 10.1371/journal.pmed.1000267 . PMC 2857873 . PMID 20422030.
- ^ Christians KK, Evans DB (junio de 2015). "Apoyo adicional para la terapia neoadyuvante en el tratamiento del cáncer de páncreas". Anales de oncología quirúrgica . 22 (6): 1755–58. doi : 10.1245/s10434-014-4307-0 . PMID 25519932.
- ^ Tsvetkova EV, Asmis TR (agosto de 2014). "El papel de la terapia neoadyuvante en el tratamiento del cáncer de páncreas: ¿ha llegado la era de la terapia dirigida por biomarcadores?". Oncología actual . 21 (4): e650–7. doi :10.3747/co.21.2006. PMC 4117630. PMID 25089113 .
- ^ Zhan HX, Xu JW, Wu D, Zhang TP, Hu SY (febrero de 2015). "Células madre del cáncer de páncreas: nueva perspectiva sobre una enfermedad persistente". Cancer Letters . 357 (2): 429–37. doi :10.1016/j.canlet.2014.12.004. PMID 25499079.
- ^ ab Tanase CP, Neagu AI, Necula LG, Mambet C, Enciu AM, Calenic B, et al. (agosto de 2014). "Células madre cancerosas: participación en la patogénesis del cáncer de páncreas y perspectivas sobre la terapéutica del cáncer". Revista mundial de gastroenterología . 20 (31): 10790–801. doi : 10.3748/wjg.v20.i31.10790 . PMC 4138459 . PMID 25152582.
- ^ Allen VB, Gurusamy KS, Takwoingi Y, Kalia A, Davidson BR (julio de 2016). "Precisión diagnóstica de la laparoscopia después de la tomografía computarizada (TC) para evaluar la resecabilidad con intención curativa en el cáncer de páncreas y periampular". Base de datos Cochrane de revisiones sistemáticas . 2016 (7): CD009323. doi :10.1002/14651858.CD009323.pub3. PMC 6458011. PMID 27383694.
- ^ Heinemann V, Haas M, Boeck S (octubre de 2013). "Tratamiento neoadyuvante del cáncer de páncreas resecable y no resecable en estadio límite". Anales de Oncología . 24 (10): 2484–92. doi : 10.1093/annonc/mdt239 . PMID 23852311.
- ^ abc Thota R, Pauff JM, Berlin JD (enero de 2014). "Tratamiento del adenocarcinoma pancreático metastásico: una revisión". Oncología . 28 (1): 70–74. PMID 24683721.
- ^ Ryan DP (8 de julio de 2014). "Quimioterapia para el cáncer de páncreas exocrino avanzado: Tema 2475, versión 46.0" (se requiere suscripción) . UpToDate . Wolters Kluwer Health . Archivado desde el original el 8 de diciembre de 2014. Consultado el 18 de noviembre de 2014 .
- ^ "Información sobre medicamentos contra el cáncer: aprobación de la FDA para el clorhidrato de erlotinib". Instituto Nacional del Cáncer . Institutos Nacionales de Salud. 3 de julio de 2013. Archivado desde el original el 29 de noviembre de 2014. Consultado el 5 de diciembre de 2014 .
- ^ Borazanci E, Von Hoff DD (septiembre de 2014). "Nab-paclitaxel y gemcitabina para el tratamiento de pacientes con cáncer de páncreas metastásico". Expert Review of Gastroenterology & Hepatology . 8 (7): 739–47. doi :10.1586/17474124.2014.925799. PMID 24882381. S2CID 31633898.
- ^ Neoptolemos JP, Dunn JA, Stocken DD, Almond J, Link K, Beger H, et al. (noviembre de 2001). "Quimiorradioterapia y quimioterapia adyuvantes en el cáncer de páncreas resecable: un ensayo controlado aleatorizado". Lancet . 358 (9293): 1576–1585. doi :10.1016/S0140-6736(01)06651-X. PMID 11716884. S2CID 23803289.
- ^ Neoptolemos JP, Stocken DD, Friess H, Bassi C, Dunn JA, Hickey H, et al. (marzo de 2004). "Un ensayo aleatorio de quimiorradioterapia y quimioterapia después de la resección del cáncer de páncreas". The New England Journal of Medicine . 350 (12): 1200–1210. doi : 10.1056/NEJMoa032295 . PMID 15028824.
- ^ Falconi M, Bartsch DK, Eriksson B, Klöppel G, Lopes JM, O'Connor JM, et al. (2012). "Directrices de consenso de ENETS para el tratamiento de pacientes con neoplasias neuroendocrinas digestivas del sistema digestivo: tumores pancreáticos no funcionantes bien diferenciados". Neuroendocrinología . 95 (2): 120–34. doi :10.1159/000335587. PMID 22261872. S2CID 6985904.
- ^ Jensen RT, Cadiot G, Brandi ML, de Herder WW, Kaltsas G, Komminoth P, et al. (2012). "Directrices de consenso de ENETS para el tratamiento de pacientes con neoplasias neuroendocrinas digestivas: síndromes de tumores endocrinos pancreáticos funcionales". Neuroendocrinología . 95 (2): 98–119. doi :10.1159/000335591. PMC 3701449 . PMID 22261919.
- ^ Pavel M, Baudin E, Couvelard A, Krenning E, Öberg K, Steinmüller T, et al. (2012). "Directrices de consenso de ENETS para el tratamiento de pacientes con metástasis hepáticas y otras metástasis distantes de neoplasias neuroendocrinas del intestino anterior, medio, posterior y primarias desconocidas". Neuroendocrinología . 95 (2): 157–76. doi :10.1159/000335597. PMID 22262022. S2CID 2097604.
- ^ Rossi RE, Massironi S, Conte D, Peracchi M (enero de 2014). "Terapia para tumores neuroendocrinos pancreáticos metastásicos". Annals of Translational Medicine . 2 (1): 8. doi :10.3978/j.issn.2305-5839.2013.03.01. PMC 4200651 . PMID 25332984.
- ^ Mulcahy N (17 de diciembre de 2014). "La FDA aprueba el uso de lanreótido para tumores neuroendocrinos". Medscape Medical News . WebMD LLC. Archivado desde el original el 18 de enero de 2015 . Consultado el 25 de diciembre de 2014 .
- ^ Aprobado el everolimus para los tumores neuroendocrinos pancreáticos Archivado el 16 de julio de 2016 en Wayback Machine The ASCO Post . 15 de mayo de 2011, Volumen 2, Número 8
- ^ Instituto Nacional del Cáncer. Información sobre medicamentos contra el cáncer. Aprobación de la FDA para el malato de sunitinib Archivado el 5 de enero de 2015 en Wayback Machine . Tumores neuroendocrinos pancreáticos
- ^ El texto está disponible en formato electrónico (pero puede requerir registro gratuito). Véase: Benson AB, Myerson RJ, Sasson AR (2010). Cánceres de páncreas, neuroendocrino, gastrointestinal y suprarrenales. Tratamiento del cáncer: un enfoque multidisciplinario (13.ª ed.). UBM Medica. ISBN 978-0-615-41824-7Archivado desde el original el 15 de mayo de 2011.
- ^ Gulenchyn KY, Yao X, Asa SL, Singh S, Law C (mayo de 2012). "Terapia con radionúclidos en tumores neuroendocrinos: una revisión sistemática". Oncología clínica . 24 (4): 294–308. doi :10.1016/j.clon.2011.12.003. PMID 22221516.
- ^ Vinik AI (noviembre de 2014). "Avances en el diagnóstico y tratamiento de tumores neuroendocrinos pancreáticos". Endocrine Practice . 20 (11): 1222–30. doi :10.4158/EP14373.RA. PMID 25297671.
- ^ Kwekkeboom DJ, de Herder WW, van Eijck CH, Kam BL, van Essen M, Teunissen JJ, et al. (Marzo de 2010). "Terapia con radionúclidos receptores de péptidos en pacientes con tumores neuroendocrinos gastroenteropancreáticos". Seminarios de Medicina Nuclear . 40 (2): 78–88. doi : 10.1053/j.semnuclmed.2009.10.004 . PMID 20113677.
- ^ Bodei L, Cremonesi M, Kidd M, Grana CM, Severi S, Modlin IM, et al. (agosto de 2014). "Terapia con radionúclidos de receptores peptídicos para tumores neuroendocrinos avanzados". Clínicas de cirugía torácica . 24 (3): 333–49. doi :10.1016/j.thorsurg.2014.04.005. hdl : 11392/2378236 . PMID: 25065935.
- ^ Castellano D, Grande E, Valle J, Capdevila J, Reidy-Lagunes D, O'Connor JM, et al. (junio de 2015). "Consenso de expertos para el manejo de tumores neuroendocrinos y carcinoides pancreáticos avanzados o metastásicos". Quimioterapia y farmacología del cáncer . 75 (6): 1099–114. doi :10.1007/s00280-014-2642-2. PMID 25480314. S2CID 39434924.
- ^ Singh S, Dey C, Kennecke H, Kocha W, Maroun J, Metrakos P, et al. (agosto de 2015). "Recomendaciones de consenso para el diagnóstico y el tratamiento de los tumores neuroendocrinos pancreáticos: directrices de un grupo nacional de expertos canadienses". Anales de oncología quirúrgica . 22 (8): 2685–99. doi :10.1245/s10434-014-4145-0. PMID 25366583. S2CID 8129133.
- ^ "Cuidado paliativo o de apoyo". Sociedad Estadounidense del Cáncer. 2014. Archivado desde el original el 21 de agosto de 2014. Consultado el 20 de agosto de 2014 .
- ^ Buanes TA (agosto de 2014). "Es posible mejorar la atención del cáncer de páncreas". Revista Mundial de Gastroenterología . 20 (30): 10405–18. doi : 10.3748/wjg.v20.i30.10405 . PMC 4130847 . PMID 25132756.
- ^ "Si el tratamiento del cáncer de páncreas deja de funcionar". Sociedad Estadounidense del Cáncer. 11 de junio de 2014. Archivado desde el original el 22 de octubre de 2014. Consultado el 20 de agosto de 2014 .
- ^ Arcidiacono PG, Calori G, Carrara S, McNicol ED, Testoni PA (marzo de 2011). Arcidiacono PG (ed.). "Bloqueo del plexo celíaco para el dolor por cáncer de páncreas en adultos". Base de Datos Cochrane de Revisiones Sistemáticas . 2019 (3): CD007519. doi : 10.1002 /14651858.CD007519.pub2. PMC 6464722. PMID 21412903.
- ^ "Datos y cifras sobre el cáncer 2014" (PDF) . Sociedad Estadounidense del Cáncer . Archivado (PDF) del original el 18 de diciembre de 2014 . Consultado el 5 de enero de 2015 ., Tabla, pág. 18, tasas ajustadas a la esperanza de vida normal
- ^ Jemal A, Siegel R, Ward E, Murray T, Xu J, Thun MJ (2007). "Estadísticas del cáncer, 2007". CA: A Cancer Journal for Clinicians . 57 (1): 43–66. doi : 10.3322/canjclin.57.1.43 . PMID 17237035. S2CID 22305510.
- ^ "¿Cuáles son las estadísticas clave sobre el cáncer de páncreas?". Sociedad Estadounidense del Cáncer . 11 de junio de 2014. Archivado desde el original el 11 de noviembre de 2014. Consultado el 11 de noviembre de 2014 .
- ^ "Estadísticas de cáncer de páncreas". Cancer Research UK . Archivado desde el original el 18 de diciembre de 2014. Consultado el 18 de diciembre de 2014 .; "En 2010, en el Reino Unido, el riesgo de desarrollar cáncer de páncreas a lo largo de la vida es de 1 en 73 para los hombres y de 1 en 74 para las mujeres", y se observa que "el riesgo a lo largo de la vida... se ha calculado... utilizando el método de 'probabilidad actual'; este es un método diferente al que se utiliza en la mayoría de los otros sitios de cáncer, ya que la posibilidad de tener más de un diagnóstico de cáncer de páncreas a lo largo de la vida es muy baja".
- ^ ab Busnardo AC, DiDio LJ, Tidrick RT, Thomford NR (noviembre de 1983). "Historia del páncreas". American Journal of Surgery . 146 (5): 539–50. doi : 10.1016/0002-9610(83)90286-6 . PMID 6356946.
- ^ abcd Are C, Dhir M, Ravipati L (junio de 2011). "Historia de la pancreatoduodenectomía: conceptos erróneos tempranos, hitos iniciales y pioneros". HPB . 13 (6): 377–84. doi :10.1111/j.1477-2574.2011.00305.x. PMC 3103093 . PMID 21609369.
- ^ ab Cameron JL, Riall TS, Coleman J, Belcher KA (julio de 2006). "Mil pancreatoduodenectomías consecutivas". Anales de Cirugía . 244 (1): 10–5. doi :10.1097/01.sla.0000217673.04165.ea. PMC 1570590 . PMID 16794383.
- ^ Fernández-del Castillo C, Morales-Oyarvide V, McGrath D, Wargo JA, Ferrone CR, Thayer SP, et al. (septiembre de 2012). "Evolución del procedimiento de Whipple en el Hospital General de Massachusetts". Surgery . 152 (3 Suppl 1): S56-63. doi :10.1016/j.surg.2012.05.022. PMC 3806095 . PMID 22770961.
- ^ abc "¿Qué hay de nuevo en la investigación y el tratamiento del cáncer de páncreas?". Sociedad Estadounidense del Cáncer . 2019. Consultado el 2 de mayo de 2019 .
- ^ "Investigación sobre el cáncer de páncreas". Cancer Research UK . Archivado desde el original el 18 de febrero de 2014. Consultado el 17 de julio de 2014 .
- ^ "Iniciativa australiana del genoma pancreático". Instituto Garvan. Archivado desde el original el 26 de julio de 2014. Consultado el 17 de julio de 2014 .
- ^ Biankin AV, Waddell N, Kassahn KS, Gingras MC, Muthuswamy LB, Johns AL, et al. (noviembre de 2012). "Los genomas del cáncer de páncreas revelan aberraciones en los genes de la vía de guía axonal". Nature . 491 (7424): 399–405. Bibcode :2012Natur.491..399.. doi :10.1038/nature11547. PMC 3530898 . PMID 23103869.
- ^ Feng HY, Chen YC (septiembre de 2016). "El papel de los ácidos biliares en la carcinogénesis del cáncer de páncreas: un tema antiguo con una nueva perspectiva". Revista Mundial de Gastroenterología . 22 (33): 7463–7477. doi : 10.3748/wjg.v22.i33.7463 . PMC 5011662 . PMID 27672269.
- ^ Sharma B, Twelker K, Nguyen C, Ellis S, Bhatia ND, Kuschner Z, et al. (junio de 2024). "Ácidos biliares en la carcinogénesis pancreática". Metabolitos . 14 (7): 348. doi : 10.3390/metabo14070348 . PMC 11278541 . PMID 39057671.
- ^ Graham JS, Jamieson NB, Rulach R, Grimmond SM, Chang DK, Biankin AV (septiembre de 2015). "Genómica del cáncer de páncreas: ¿hacia dónde nos puede llevar la ciencia?". Clinical Genetics . 88 (3): 213–9. doi :10.1111/cge.12536. PMID 25388820. S2CID 26414866.
- ^ Bruenderman EH, Martin RC (marzo de 2015). "Población de alto riesgo en adenocarcinoma de páncreas esporádico: pautas para la detección". The Journal of Surgical Research . 194 (1): 212–9. doi :10.1016/j.jss.2014.06.046. PMC 4559279 . PMID 25479908.
- ^ "Acerca de EUROPAC". Registro Europeo de Pancreatitis Hereditaria y Cáncer de Páncreas Familiar (EUROPAC) . Universidad de Liverpool. Archivado desde el original el 26 de julio de 2014. Consultado el 17 de julio de 2014 .
- ^ Subar D, Gobardhan PD, Gayet B (febrero de 2014). "Cirugía pancreática laparoscópica: una descripción general de la literatura y las experiencias de un solo centro". Mejores prácticas e investigación. Gastroenterología clínica . 28 (1): 123–32. doi :10.1016/j.bpg.2013.11.011. PMID 24485260.
- ^ Weiss MJ, Wolfgang CL (2013). "Electroporación irreversible: una nueva terapia contra el cáncer de páncreas". Problemas actuales en el cáncer . 37 (5): 262–5. doi :10.1016/j.currproblcancer.2013.10.002. PMID 24331180. S2CID 3137300.
- ^ Moir J, White SA, French JJ, Littler P, Manas DM (diciembre de 2014). "Revisión sistemática de la electroporación irreversible en el tratamiento del cáncer de páncreas avanzado". Revista Europea de Oncología Quirúrgica . 40 (12): 1598–604. doi :10.1016/j.ejso.2014.08.480. PMID 25307210.
- ^ Kleger A, Perkhofer L, Seufferlein T (julio de 2014). "Emergencia de fármacos más inteligentes en la terapia del cáncer de páncreas". Anales de Oncología . 25 (7): 1260–1270. doi : 10.1093/annonc/mdu013 . PMID 24631947.
- ^ ab Tang SC, Chen YC (agosto de 2014). "Nuevos objetivos terapéuticos para el cáncer de páncreas". Revista Mundial de Gastroenterología . 20 (31): 10825–44. doi : 10.3748/wjg.v20.i31.10825 . PMC 4138462 . PMID 25152585.
- ^ Rossi ML, Rehman AA, Gondi CS (agosto de 2014). "Opciones terapéuticas para el tratamiento del cáncer de páncreas". Revista Mundial de Gastroenterología . 20 (32): 11142–59. doi : 10.3748/wjg.v20.i32.11142 . PMC 4145755 . PMID 25170201.
- ^ Ady JW, Heffner J, Klein E, Fong Y (2014). "Terapia viral oncolítica para el cáncer de páncreas: investigación actual y direcciones futuras". Viroterapia oncolítica . 3 : 35–46. doi : 10.2147/OV.S53858 . PMC 4918362. PMID 27512661 .
- ^ Ren B, Cui M, Yang G, Wang H, Feng M, You L, et al. (julio de 2018). "El microambiente tumoral participa en la metástasis del cáncer de páncreas". Cáncer molecular . 17 (1): 108. doi : 10.1186 /s12943-018-0858-1 . PMC 6065152. PMID 30060755.
- ^ Das SS, Dubey AK, Singh N, Verma PR, Singh SK, Singh SK (9 de enero de 2023). "Tratamiento del cáncer de páncreas mediante el uso de nanopartículas terapéuticas". En Rahman M, Almalki HW, Alrobaian M, Beg S, Alharbi KS (eds.). Mecanismos y nanomedicinas relacionados con las hormonas del cáncer . Singapur: Springer. págs. 149–168. doi :10.1007/978-981-19-5558-7_8. ISBN 978-981-19-5557-0.