Hipertensión pulmonar
| Hipertensión pulmonar | |
|---|---|
| Otros nombres | Síndrome de Ayerza [1] |
 | |
| Hipertensión pulmonar | |
| Especialidad | Neumología , cardiología |
| Síntomas | Dolor en el pecho, fatiga [2] |
| Inicio habitual | 20 a 60 años [3] |
| Duración | A largo plazo [4] |
| Causas | Desconocido [4] |
| Factores de riesgo | Antecedentes familiares, embolia pulmonar , VIH/SIDA , enfermedad de células falciformes , consumo de cocaína , EPOC , apnea del sueño , vivir a grandes altitudes [5] [3] |
| Método de diagnóstico | Tras descartar otras posibles causas [4] |
| Tratamiento | Cuidados de apoyo , diversos medicamentos, trasplante de pulmón [4] [6] |
| Medicamento | Epoprostenol , treprostinil , iloprost , bosentan , ambrisentan , macitentan , sildenafil [4] |
| Frecuencia | 1.000 casos nuevos al año (EE.UU.) [1] |
La hipertensión pulmonar ( HP o HPTN ) es una afección en la que aumenta la presión arterial en las arterias de los pulmones . [7] Los síntomas incluyen dificultad para respirar , desmayos , cansancio, dolor en el pecho, hinchazón de las piernas y ritmo cardíaco acelerado . [7] [1] La afección puede dificultar el ejercicio. [7] El inicio suele ser gradual. [8] Según la definición del 6.º Simposio Mundial de Hipertensión Pulmonar en 2018, se considera que un paciente tiene hipertensión pulmonar si la presión arterial media pulmonar es superior a 20 mmHg en reposo, revisada a la baja desde un valor puramente arbitrario de 25 mmHg, y la resistencia vascular pulmonar (RVP) es superior a 3 unidades Wood.
La causa es a menudo desconocida. [4] Los factores de riesgo incluyen antecedentes familiares, embolia pulmonar previa (coágulos de sangre en los pulmones), VIH/SIDA , enfermedad de células falciformes , consumo de cocaína , enfermedad pulmonar obstructiva crónica , apnea del sueño , vivir a grandes altitudes y problemas con la válvula mitral . [5] [3] El mecanismo subyacente generalmente implica inflamación y posterior remodelación de las arterias en los pulmones . [5] El diagnóstico implica primero descartar otras causas potenciales. [4]
En 2022 [actualizar]no existía cura para la hipertensión pulmonar, [6] aunque se están realizando investigaciones para encontrar una cura. El tratamiento depende del tipo de enfermedad. [6] Se pueden utilizar varias medidas de apoyo , como oxigenoterapia , diuréticos y medicamentos para inhibir la coagulación sanguínea . [4] Los medicamentos que se utilizan específicamente para tratar la hipertensión pulmonar incluyen epoprostenol , treprostinil , iloprost , bosentán , ambrisentán , macitentan y sildenafil , tadalafil, selexipag, riociguat. [4] El trasplante de pulmón puede ser una opción en casos graves. [6]
La frecuencia de aparición se estima en 1.000 casos nuevos por año en los Estados Unidos. [3] [1] Afecta con mayor frecuencia a las mujeres que a los hombres. [1] La aparición suele darse entre los 20 y los 60 años de edad. [3] La hipertensión pulmonar fue identificada por Ernst von Romberg en 1891. [9] [4]
Clasificación
Según la clasificación de la OMS, existen 5 grupos de HP, donde el Grupo I (hipertensión arterial pulmonar) se subdivide a su vez en las clases Grupo I' y Grupo I''. [10] [11] El sistema de clasificación de la OMS en 2022 (con adaptaciones de las directrices ESC/ERS más recientes que se muestran en cursiva) se puede resumir de la siguiente manera: [11] [12]
Grupo I de la OMS – Hipertensión arterial pulmonar (HAP)
- Causada por el estrechamiento y engrosamiento de las pequeñas arterias del pulmón [13]
- Idiopática en la mayoría de los casos (hereditaria en algunos casos) [13]
- Hereditario ( mutaciones BMPR2 , ALK1 , SMAD9 , caveolina 1 , KCNK3 )
- Inducida por drogas y toxinas (por ejemplo, consumo de metanfetamina , anfetamina o cocaína [14] )
- Afecciones asociadas: Enfermedad del tejido conectivo , Infección por VIH , Hipertensión portal , Cardiopatías congénitas , Esquistosomiasis
Grupo I de la OMS : enfermedad venooclusiva pulmonar (EVP), hemangiomatosis capilar pulmonar (CHP)
- Idiopático
- Hereditario ( mutaciones EIF2AK4 )
- Drogas, toxinas y radiación inducida
- Afecciones asociadas: enfermedad del tejido conectivo, infección por VIH.
Grupo I de la OMS : Hipertensión pulmonar persistente del recién nacido
Grupo II de la OMS – Hipertensión pulmonar secundaria a cardiopatía izquierda
- Disfunción sistólica del ventrículo izquierdo
- Disfunción diastólica del ventrículo izquierdo
- Enfermedad cardíaca valvular
- Obstrucción congénita o adquirida del tracto de entrada y salida del corazón izquierdo y miocardiopatía congénita
- Estenosis venosa pulmonar congénita/adquirida
Grupo III de la OMS – Hipertensión pulmonar debida a enfermedad pulmonar , hipoxia crónica
- Enfermedad pulmonar obstructiva crónica (EPOC)
- Enfermedad pulmonar intersticial
- Enfermedades pulmonares de patrón mixto restrictivo y obstructivo
- Trastornos respiratorios del sueño
- Trastornos de hipoventilación alveolar
- Exposición crónica a grandes altitudes
- Anormalidades del desarrollo
Grupo IV de la OMS : obstrucción arterial crónica
- Hipertensión pulmonar tromboembólica crónica (HPTEC)
- Otras obstrucciones de la arteria pulmonar
- Angiosarcoma u otro tumor dentro de los vasos sanguíneos.
- Arteritis
- Estenosis congénita de la arteria pulmonar
- Infección parasitaria ( hidatidosis )
Grupo V de la OMS : Hipertensión pulmonar con mecanismos poco claros o multifactoriales
- Enfermedades hematológicas : anemia hemolítica crónica (incluida la enfermedad de células falciformes )
- Enfermedades sistémicas : sarcoidosis , histiocitosis pulmonar de células de Langerhans : linfangioleiomiomatosis , neurofibromatosis , vasculitis
- Trastornos metabólicos : enfermedad de almacenamiento de glucógeno , enfermedad de Gaucher , enfermedades de la tiroides
- Otros: microangiopatía trombótica tumoral pulmonar, mediastinitis fibrosante , insuficiencia renal crónica , hipertensión pulmonar segmentaria (hipertensión pulmonar restringida a uno o más lóbulos de los pulmones ).
Signos y síntomas
Los síntomas de la hipertensión pulmonar incluyen los siguientes: [2] [12] [15]
- Dificultad para respirar
- Fatiga
- Dolor en el pecho
- Palpitaciones ( aumento de la frecuencia cardíaca )
- Dolor abdominal en el lado derecho
- Falta de apetito
- Mareo
- Desmayo
- Hinchazón (piernas/tobillos)
- Cianosis
Los signos/síntomas menos comunes incluyen tos no productiva y náuseas y vómitos inducidos por el ejercicio. [12] La tos con sangre puede ocurrir en algunos pacientes, particularmente aquellos con subtipos específicos de hipertensión pulmonar, como hipertensión arterial pulmonar hereditaria, síndrome de Eisenmenger e hipertensión pulmonar tromboembólica crónica . [16] La hipertensión venosa pulmonar generalmente se presenta con dificultad para respirar al estar acostado o durmiendo ( ortopnea o disnea paroxística nocturna ), mientras que la hipertensión arterial pulmonar (HAP) generalmente no. [17]
Otros signos típicos de hipertensión pulmonar incluyen un componente pulmonar acentuado del segundo ruido cardíaco, un tercer ruido cardíaco ventricular derecho y un tirón paraesternal que indica un ventrículo derecho hipertrofiado . Los signos de congestión sistémica resultantes de la insuficiencia cardíaca derecha incluyen distensión venosa yugular , ascitis y reflujo hepatoyugular . [12] [15] [18] También se busca evidencia de insuficiencia tricuspídea y regurgitación pulmonar y, si está presente, es consistente con la presencia de hipertensión pulmonar. [12] [15] [19]
Causas
La hipertensión pulmonar es una afección fisiopatológica con muchas causas posibles. De hecho, esta afección acompaña con frecuencia a afecciones cardíacas o pulmonares graves. [12] Una reunión de la Organización Mundial de la Salud de 1973 fue el primer intento de clasificar la hipertensión pulmonar según su causa, y se hizo una distinción entre la HP primaria (resultante de una enfermedad de las arterias pulmonares) y la HP secundaria (resultante de otras causas no vasculares). Además, la HP primaria se dividió en las formas "plexiforme arterial", "venooclusiva" y "tromboembólica". [20] En 1998, una segunda conferencia en Évian-les-Bains abordó las causas de la HP secundaria. [21] Los simposios mundiales posteriores sobre HAP tercero, [22] cuarto, [10] y quinto (2013) [11] han definido con más detalle la clasificación de la HP. La clasificación continúa evolucionando en función de una mejor comprensión de los mecanismos de la enfermedad. [ cita requerida ]
Más recientemente, en 2015, la Sociedad Europea de Cardiología (ESC) y la Sociedad Respiratoria Europea (ERS) actualizaron las directrices de la OMS . [12] Estas directrices están avaladas por la Sociedad Internacional de Trasplante de Corazón y Pulmón y proporcionan el marco actual para la comprensión y el tratamiento de la hipertensión pulmonar. [23]
Genética
Las mutaciones en varios genes se han asociado con esta condición [24] [25] estos incluyen el receptor de proteína morfogenética ósea tipo 2 ( BMPR2 ) y el gen del factor de iniciación de traducción eucariota 2 alfa quinasa 4 ( EIF2AK4 ). El 80% de la hipertensión arterial pulmonar familiar y el 20% de las variantes esporádicas tienen mutaciones en BMPR2. [26] BMPR2 está involucrado en la proliferación y remodelación endotelial . Otras mutaciones asociadas con la HAP incluyen ACVRL1 (que codifica la quinasa similar al receptor de activina 1) y ENG que codifica endoglina, dos proteínas que también participan en la señalización de BMPR2. [26] La familia de factores de transcripción SMAD, que incluye SMAD1 , SMAD4 y SMAD9 , está involucrada en las vías de señalización posteriores a BMPR2 y también está implicada en el desarrollo de la hipertensión arterial pulmonar. [26]
Patogenesia

.jpg/440px-Pulmonary_hypertensive_arteriopathy_(4348170715).jpg)
La patogenia de la hipertensión arterial pulmonar (Grupo I de la OMS) implica el estrechamiento de los vasos sanguíneos conectados a los pulmones y dentro de ellos. Esto dificulta que el corazón bombee sangre a través de los pulmones , ya que es mucho más difícil hacer que el agua fluya a través de una tubería estrecha en comparación con una ancha. Con el tiempo, los vasos sanguíneos afectados se vuelven más rígidos y gruesos, en un proceso conocido como fibrosis . Los mecanismos involucrados en este proceso de estrechamiento incluyen vasoconstricción , trombosis y remodelación vascular (proliferación celular excesiva, fibrosis y apoptosis reducida/muerte celular programada en las paredes de los vasos, causada por inflamación , metabolismo desordenado y desregulación de ciertos factores de crecimiento ). [27] [28] Esto aumenta aún más la presión arterial dentro de los pulmones y perjudica su flujo sanguíneo. En común con otros tipos de hipertensión pulmonar, estos cambios resultan en una mayor carga de trabajo para el lado derecho del corazón. [15] [29] El ventrículo derecho normalmente forma parte de un sistema de baja presión, con presiones ventriculares sistólicas inferiores a las que normalmente encuentra el ventrículo izquierdo. Como tal, el ventrículo derecho no puede hacer frente tan bien a presiones más altas, y aunque las adaptaciones del ventrículo derecho ( hipertrofia y aumento de la contractilidad del músculo cardíaco) inicialmente ayudan a preservar el volumen sistólico , en última instancia estos mecanismos compensatorios son insuficientes; el músculo ventricular derecho no puede obtener suficiente oxígeno para satisfacer sus necesidades y se produce una insuficiencia cardíaca derecha . [15] [28] [29] A medida que disminuye la sangre que fluye a través de los pulmones, el lado izquierdo del corazón recibe menos sangre. Esta sangre también puede transportar menos oxígeno de lo normal. Por lo tanto, se vuelve cada vez más difícil para el lado izquierdo del corazón suministrar suficiente oxígeno al resto del cuerpo, especialmente durante la actividad física. [30] [31] [10] Durante la fase de volumen sistólico final del ciclo cardíaco, se encontró que la curvatura gaussiana y la curvatura media de la pared endocárdica del ventrículo derecho de los pacientes con HP eran significativamente diferentes en comparación con los controles. [32]
En la EVOP (grupo I de la OMS), el estrechamiento de los vasos sanguíneos pulmonares se produce preferentemente (aunque no exclusivamente) en los vasos sanguíneos venosos poscapilares. [33] La EVOP comparte varias características con la HAP, pero también existen algunas diferencias importantes, por ejemplo, diferencias en el pronóstico y la respuesta al tratamiento médico. [ cita requerida ]
La hipertensión pulmonar persistente del recién nacido ocurre cuando el sistema circulatorio de un bebé recién nacido no se adapta a la vida fuera del útero; se caracteriza por una alta resistencia al flujo sanguíneo a través de los pulmones, derivación cardíaca de derecha a izquierda e hipoxemia grave . [15]
La patogenia de la hipertensión pulmonar debida a la enfermedad cardíaca izquierda (Grupo II de la OMS) es completamente diferente, ya que la constricción o el daño de los vasos sanguíneos pulmonares no es el problema. En cambio, el corazón izquierdo no puede bombear sangre de manera eficiente, lo que lleva a la acumulación de sangre en los pulmones y a la contrapresión dentro del sistema pulmonar. Esto causa edema pulmonar y derrames pleurales . [34] En ausencia de estrechamiento de los vasos sanguíneos pulmonares, el aumento de la contrapresión se describe como "hipertensión pulmonar poscapilar aislada" (los términos más antiguos incluyen hipertensión pulmonar "pasiva" o "proporcionada" o "hipertensión venosa pulmonar"). Sin embargo, en algunos pacientes, la presión elevada en los vasos pulmonares desencadena un componente superpuesto de estrechamiento de los vasos, que aumenta aún más la carga de trabajo del lado derecho del corazón. Esto se conoce como "hipertensión pulmonar poscapilar con un componente precapilar" o "hipertensión pulmonar poscapilar y precapilar combinada" (los términos más antiguos incluyen hipertensión pulmonar "reactiva" o "desproporcionada"). [12] [17] [35]
En la hipertensión pulmonar debida a enfermedades pulmonares y/o hipoxia (Grupo III de la OMS), los niveles bajos de oxígeno en los alvéolos (debido a enfermedades respiratorias o vivir a gran altitud) causan constricción de las arterias pulmonares. Este fenómeno se llama vasoconstricción pulmonar hipóxica y es inicialmente una respuesta protectora para detener el flujo excesivo de sangre a las áreas del pulmón que están dañadas y no contienen oxígeno. Cuando la hipoxia alveolar es generalizada y prolongada, esta vasoconstricción mediada por hipoxia se produce en una gran parte del lecho vascular pulmonar y conduce a un aumento de la presión arterial pulmonar, con un engrosamiento de las paredes de los vasos pulmonares que contribuye al desarrollo de hipertensión pulmonar sostenida. [10] [36] [37] [38] La hipoxia prolongada también induce el factor de transcripción HIF1A , que activa directamente la señalización del factor de crecimiento descendente que causa la proliferación y remodelación irreversibles de las células endoteliales arteriales pulmonares, lo que conduce a la hipertensión arterial pulmonar crónica. [ cita requerida ]
En la hipertensión pulmonar tromboembólica crónica, o HPTEC (Grupo IV de la OMS), se cree que el evento desencadenante es el bloqueo o estrechamiento de los vasos sanguíneos pulmonares con coágulos sanguíneos no resueltos; estos coágulos pueden provocar un aumento de la presión y la tensión de corte en el resto de la circulación pulmonar, precipitando cambios estructurales en las paredes de los vasos (remodelación) similares a los observados en otros tipos de hipertensión pulmonar grave. Esta combinación de oclusión vascular y remodelación vascular aumenta una vez más la resistencia al flujo sanguíneo y, por lo tanto, aumenta la presión dentro del sistema. [39] [40]
Patología molecular
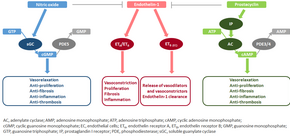
El mecanismo molecular de la hipertensión arterial pulmonar (HAP) no se conoce aún, pero se cree que la disfunción endotelial produce una disminución en la síntesis de vasodilatadores derivados del endotelio, como el óxido nítrico y la prostaciclina . [41] Además, hay una estimulación de la síntesis de vasoconstrictores como el tromboxano y el factor de crecimiento endotelial vascular (VEGF). Estos producen una vasoconstricción grave y una hipertrofia del músculo liso vascular y de la adventicia característica de los pacientes con HAP. [41]
Vía de la guanilato ciclasa soluble en óxido nítrico
En condiciones normales, la óxido nítrico sintasa endotelial vascular produce óxido nítrico a partir de L-arginina en presencia de oxígeno. [42]
Este óxido nítrico se difunde a las células vecinas (incluidas las células musculares lisas vasculares y las plaquetas), donde aumenta la actividad de la enzima guanilato ciclasa soluble , lo que conduce a una mayor formación de monofosfato de guanosina cíclico (cGMP) a partir del trifosfato de guanosina (GTP). [43] El cGMP luego activa la quinasa dependiente de cGMP o PKG (proteína quinasa G). La PKG activada promueve la vasorrelajación (a través de una reducción de los niveles intracelulares de calcio), altera la expresión de genes involucrados en la contracción, migración y diferenciación de las células musculares lisas e inhibe la activación plaquetaria . [44] La señalización de la guanilato ciclasa soluble de óxido nítrico también conduce a efectos antiinflamatorios. [45]
La fosfodiesterasa tipo 5 ( PDE5 ), abundante en el tejido pulmonar, hidroliza el enlace cíclico del cGMP. En consecuencia, la concentración de cGMP (y, por lo tanto, la actividad de PKG) disminuye. [46] [44]
Endotelina
La endotelina-1 es un péptido (que comprende 21 aminoácidos) que se produce en las células endoteliales. Actúa sobre los receptores de endotelina ETA y ETB en varios tipos de células, incluidas las células musculares lisas vasculares y los fibroblastos, lo que provoca vasoconstricción, hipertrofia, proliferación, inflamación y fibrosis. También actúa sobre los receptores ETB en las células endoteliales; esto conduce a la liberación de vasoconstrictores y vasodilatadores de esas células y elimina la endotelina-1 del sistema. [47] [48]
Prostaciclina y tromboxano
La prostaciclina se sintetiza a partir del ácido araquidónico en las células endoteliales. En las células musculares lisas vasculares, la prostaciclina se une principalmente al receptor de prostaglandina I. Esto envía una señal para aumentar la actividad de la adenilato ciclasa, lo que conduce a un aumento de la síntesis de monofosfato de adenosina cíclico (AMPc). Esto a su vez conduce a un aumento de la actividad de la proteína quinasa dependiente de AMPc o PKA (proteína quinasa A), que en última instancia promueve la vasodilatación e inhibe la proliferación celular. La señalización de la prostaciclina también conduce a efectos antitrombóticos, antifibróticos y antiinflamatorios. Los niveles de AMPc (que media la mayoría de los efectos biológicos de la prostaciclina) se reducen por las fosfodiesterasas 3 y 4. [49] [50] El vasoconstrictor tromboxano también se sintetiza a partir del ácido araquidónico. En la HAP, el equilibrio se desplaza desde la síntesis de prostaciclina hacia la síntesis de tromboxano. [49]
Otras vías
Las tres vías descritas anteriormente son el objetivo de las terapias médicas actualmente disponibles para la HAP. Sin embargo, se han identificado varias otras vías que también se alteran en la HAP y se están investigando como posibles objetivos para futuras terapias. Por ejemplo, la enzima mitocondrial piruvato deshidrogenasa quinasa (PDK) se activa patológicamente en la HAP, lo que provoca un cambio metabólico de la fosforilación oxidativa a la glucólisis y conduce a una mayor proliferación celular y una apoptosis deteriorada. [49] [51] La expresión del péptido intestinal vasoactivo, un potente vasodilatador con funciones antiinflamatorias e inmunomoduladoras, se reduce en la HAP, mientras que la expresión de su receptor aumenta. [49] [51] Los niveles plasmáticos de serotonina , que promueve la vasoconstricción, la hipertrofia y la proliferación, aumentan en pacientes con HAP, aunque el papel que desempeña la serotonina en la patogénesis de la HAP sigue siendo incierto. [15] [49] La expresión o actividad de varios factores de crecimiento (incluido el factor de crecimiento derivado de plaquetas , el factor de crecimiento básico de fibroblastos , el factor de crecimiento epidérmico y el factor de crecimiento endotelial vascular ) aumenta y contribuye a la remodelación vascular en la HAP. [49] Otros factores subyacentes al estado proliferativo de las células musculares lisas vasculares pulmonares incluyen OPG [52] y TRAIL . [53] Centrarse solo en la vasculatura pulmonar proporciona una imagen incompleta de la HAP; la capacidad del ventrículo derecho para adaptarse a la mayor carga de trabajo varía entre pacientes y es un determinante importante de la supervivencia. Por lo tanto, también se está investigando la patología molecular de la HAP en el ventrículo derecho, y la investigación reciente ha cambiado para considerar la unidad cardiopulmonar como un solo sistema en lugar de dos sistemas separados. Es importante destacar que la remodelación del ventrículo derecho se asocia con un aumento de la apoptosis; esto contrasta con la remodelación vascular pulmonar que implica la inhibición de la apoptosis. [28]
Aunque se desconoce la causa principal de la HAP, se ha demostrado que la inflamación y el estrés oxidativo tienen un papel clave en la remodelación vascular. [54] Se sabe que estos factores causan daño al ADN y también pueden promover el fenotipo proliferativo y resistente a la apoptosis que se observa en las células vasculares de la HAP. [54] Se ha informado que se producen niveles elevados de daño al ADN en pulmones y arterias remodeladas con HAP, y también en modelos animales de HP, lo que indica que el daño al ADN probablemente contribuye a la patogénesis de la HAP. [54]
Diagnóstico


.jpg/440px-Severe_tricuspid_regurgitation_E00572_(CardioNetworks_ECHOpedia).jpg)
En cuanto al diagnóstico de la hipertensión pulmonar, existen cinco tipos principales y se deben realizar una serie de pruebas para distinguir la hipertensión arterial pulmonar de la venosa, hipóxica, tromboembólica o de las variedades multifactoriales poco claras. La HAP se diagnostica tras la exclusión de otras posibles causas de hipertensión pulmonar. [15]
Examen físico
Se realiza un examen físico para buscar signos típicos de hipertensión pulmonar (descrita anteriormente), [55] y se establece una historia familiar detallada para determinar si la enfermedad podría ser hereditaria . [56] [57] [58] Se considera significativo un historial de exposición a drogas como benfluorex (un derivado de fenfluramina ), dasatinib , cocaína , metanfetamina , etanol que conduce a cirrosis y tabaco que conduce a enfisema . [15] [59] [11] El uso de inhibidores selectivos de la recaptación de serotonina durante el embarazo (particularmente al final del embarazo) se asocia con un mayor riesgo de que el bebé desarrolle hipertensión pulmonar persistente del recién nacido . [11]
Ecocardiografía
Si se sospecha hipertensión pulmonar con base en las evaluaciones anteriores, se realiza una ecocardiografía como siguiente paso. [12] [15] [58] Un metaanálisis de la ecocardiografía Doppler para predecir los resultados del cateterismo cardíaco derecho informó una sensibilidad y especificidad del 88% y 56%, respectivamente. [60] Por lo tanto, la ecocardiografía Doppler puede sugerir la presencia de hipertensión pulmonar, pero el cateterismo cardíaco derecho (descrito a continuación) sigue siendo el estándar de oro para el diagnóstico de HAP. [12] [15] La ecocardiografía también puede ayudar a detectar cardiopatías congénitas como causa de hipertensión pulmonar. [12]
Excluir otras enfermedades
Si el ecocardiograma es compatible con el diagnóstico de hipertensión pulmonar, se consideran las causas comunes de hipertensión pulmonar (enfermedad cardíaca izquierda y enfermedad pulmonar) y se realizan otras pruebas en consecuencia. Estas pruebas generalmente incluyen electrocardiografía (ECG), pruebas de función pulmonar que incluyen la capacidad de difusión pulmonar de monóxido de carbono y mediciones de gases en sangre arterial , radiografías de tórax y tomografía computarizada (TC) de alta resolución. [12] [15] [58] [61]
Gammagrafía de ventilación/perfusión
Si se han descartado cardiopatías y enfermedades pulmonares, se realiza una gammagrafía de ventilación/perfusión para descartar HPTEC. Si se encuentran defectos de perfusión no coincidentes, se realiza una evaluación adicional mediante angiografía pulmonar por TC, cateterismo cardíaco derecho y angiografía pulmonar selectiva. [12] [58]
Tomografía computarizada

Los signos de hipertensión pulmonar en la tomografía computarizada del tórax son:
- Agrandamiento del tronco pulmonar (medido en su bifurcación). Sin embargo, es un mal predictor de hipertensión pulmonar en pacientes con enfermedad pulmonar intersticial . [62]
- Se sugiere como punto de corte un diámetro de más de 27 mm para mujeres y 29 mm para hombres . [62]
- Un valor de corte de 31,6 mm puede ser estadísticamente más sólido en individuos sin enfermedad pulmonar intersticial . [62]
- Aumento de la relación entre el diámetro de la arteria pulmonar principal (tronco pulmonar) y la aorta ascendente (medida en su bifurcación).
- Se sugiere una relación de 1,0 como valor de corte en adultos. [62]
- Punto de corte ~1,09 en niños. [62]
- Aumento de la relación de diámetros entre las arterias segmentarias y los bronquios. Este hallazgo en tres o cuatro lóbulos, en presencia de un tronco pulmonar dilatado (≥29 mm) y ausencia de enfermedad pulmonar estructural significativa confiere una especificidad del 100% para la hipertensión pulmonar. [62]
- La calcificación mural en las arterias pulmonares centrales se observa con mayor frecuencia en pacientes con síndrome de Eisenmenger . [62]
Cateterismo cardíaco derecho
Aunque la presión arterial pulmonar (PAP) se puede estimar sobre la base de la ecocardiografía , [63] las mediciones de presión con un catéter de Swan-Ganz insertado a través del lado derecho del corazón proporcionan la evaluación más definitiva.[42] La hipertensión pulmonar se define como una PAP media de al menos 20 mmHg (3300 Pa) en reposo, y la HAP se define como hipertensión pulmonar precapilar (es decir, PAP media ≥ 20 mmHg con presión de oclusión arterial pulmonar [PAOP] ≤ 15 mmHg y resistencia vascular pulmonar [PVR] > 3 unidades Wood). [58] La PAOP y la PVR no se pueden medir directamente con ecocardiografía. Por lo tanto, el diagnóstico de HAP requiere cateterismo cardíaco del lado derecho. Un catéter de Swan-Ganz también puede medir el gasto cardíaco; esto se puede utilizar para calcular el índice cardíaco, que es mucho más importante para medir la gravedad de la enfermedad que la presión arterial pulmonar. [12] [64] La PAP media (mPAP) no debe confundirse con la PAP sistólica (sPAP), que suele informarse en los informes de ecocardiogramas. Una presión sistólica de 40 mmHg normalmente implica una presión media de más de 25 mmHg. Aproximadamente, mPAP = 0,61•sPAP + 2. [65] Debido a la naturaleza invasiva de este procedimiento, se ha postulado el uso de índices hemodinámicos basados en dinámica de fluidos computacional. [66] [67]
Otro
En el caso de las personas que se considera probable que tengan HAP según las pruebas anteriores, se determina la afección asociada específica en función del examen físico, los antecedentes médicos/familiares y otras pruebas diagnósticas específicas (por ejemplo, pruebas serológicas para detectar la enfermedad subyacente del tejido conectivo, infección por VIH o hepatitis, ecografía para confirmar la presencia de hipertensión portal, ecocardiografía/ resonancia magnética cardíaca para cardiopatía congénita, pruebas de laboratorio para esquistosomiasis y TC de alta resolución para EVOP y hemangiomatosis capilar pulmonar). Se desaconseja la biopsia pulmonar de rutina en pacientes con HAP debido al riesgo para el paciente y porque es poco probable que los hallazgos alteren el diagnóstico y el tratamiento. [12] [29] [58]
Tratamiento
El tratamiento de la hipertensión pulmonar se determina según si la HP es arterial, venosa, hipóxica, tromboembólica o miscelánea. Si es causada por una enfermedad cardíaca izquierda, el tratamiento consiste en optimizar la función ventricular izquierda mediante el uso de medicamentos o reparar/reemplazar la válvula mitral o la válvula aórtica . [68] Los pacientes con insuficiencia cardíaca izquierda o enfermedades pulmonares hipoxémicas (hipertensión pulmonar de los grupos II o III) no deben ser tratados de forma rutinaria con agentes vasoactivos, incluidos prostanoides, inhibidores de la fosfodiesterasa o antagonistas de la endotelina, ya que están aprobados para la afección diferente denominada hipertensión arterial pulmonar primaria. [69] Para hacer la distinción, los médicos, como mínimo, realizarán un cateterismo cardíaco del corazón derecho, una ecocardiografía, una TC de tórax, una prueba de caminata de siete minutos y una prueba de función pulmonar . [69] El uso de tratamientos para otros tipos de hipertensión pulmonar en pacientes con estas afecciones puede dañar al paciente y desperdiciar recursos médicos sustanciales. [69]
Los bloqueadores de los canales de calcio en dosis altas son útiles en solo el 5% de los pacientes con HAP que son vasorreactivos según el catéter de Swan-Ganz. Los bloqueadores de los canales de calcio se han utilizado incorrectamente en gran medida, y se han prescrito a muchos pacientes con HAP no vasorreactiva, lo que conduce a una morbilidad y mortalidad excesivas. [ 19 ] Los criterios de vasorreactividad han cambiado. Solo aquellos pacientes cuya presión arterial pulmonar media cae más de 10 mmHg a menos de 40 mmHg con un gasto cardíaco sin cambios o aumentado cuando se los estimula con adenosina , epoprostenol u óxido nítrico se consideran vasorreactivos. [70] De estos, solo la mitad de los pacientes responden a los bloqueadores de los canales de calcio a largo plazo. [71]
Recientemente se han introducido varios agentes para la HAP primaria y secundaria. Los ensayos que apoyan el uso de estos agentes han sido relativamente pequeños y la única medida utilizada de manera consistente para comparar su efectividad es la "prueba de la marcha de seis minutos". Muchos no tienen datos sobre el beneficio en la mortalidad o el tiempo hasta la progresión. [72]
Sotatercept (Winrevair) fue aprobado para uso médico en los Estados Unidos en marzo de 2024. [73]
Rehabilitación basada en ejercicios
Una revisión Cochrane de 2023 encontró que la rehabilitación basada en ejercicios puede conducir a un gran aumento en la capacidad de ejercicio y una mejora en la calidad de vida relacionada con la salud , sin aumentar significativamente los eventos adversos. [74]
Sustancias vasoactivas
En la proliferación y contracción anormal de las células musculares lisas de las arterias pulmonares en pacientes con hipertensión arterial pulmonar intervienen muchas vías . Tres de estas vías son importantes, ya que han sido blanco de fármacos: antagonistas del receptor de endotelina , inhibidores de la fosfodiesterasa tipo 5 (PDE-5) y derivados de la prostaciclina. [75]
Prostaglandinas
La prostaciclina ( prostaglandina I 2 ) se considera comúnmente el tratamiento más eficaz para la HAP. El epoprostenol (prostaciclina sintética) se administra mediante infusión continua que requiere un catéter venoso central semipermanente . Este sistema de administración puede causar sepsis y trombosis . La prostaciclina es inestable y, por lo tanto, debe mantenerse en hielo durante la administración. Dado que tiene una vida media de 3 a 5 minutos, la infusión debe ser continua y la interrupción puede ser fatal. [76] Por lo tanto, se han desarrollado otros prostanoides . El treprostinil se puede administrar por vía intravenosa o subcutánea, pero la forma subcutánea puede ser muy dolorosa. Los CDC han informado de un mayor riesgo de sepsis con Remodulin intravenoso . El iloprost también se usa en Europa por vía intravenosa y tiene una vida media más larga. El iloprost fue la única forma inhalada de prostaciclina aprobada para su uso en los EE. UU. y Europa, hasta que la FDA aprobó la forma inhalada de treprostinil en julio de 2009. [77]
Antagonistas del receptor de endotelina
Evidencias de calidad moderada sugieren que los antagonistas del receptor de endotelina mejoran la capacidad de ejercicio y disminuyen la gravedad de los síntomas. [78] El antagonista dual del receptor de endotelina (ET A y ET B ) bosentán fue aprobado en 2001. Macitentan es otro bloqueador dual del receptor de endotelina ET A y ET B que se utiliza. [26] Sitaxentan (Thelin) fue aprobado para su uso en Canadá, Australia y la Unión Europea, [79] pero no en los Estados Unidos. En 2010, Pfizer retiró el sitaxentan en todo el mundo debido a complicaciones hepáticas fatales. [80] Un fármaco similar, ambrisentán (que es un bloqueador del receptor de endotelina ET A ) se vende bajo la marca Letairis en los EE. UU. por Gilead Sciences . [81]
Inhibidores de la fosfodiesterasa tipo 5
La FDA de los EE. UU. aprobó el sildenafil , un inhibidor selectivo de la fosfodiesterasa tipo 5 (PDE5) específica de cGMP, para el tratamiento de la HAP en 2005. Se comercializa para la HAP como Revatio. En 2009, también aprobaron el tadalafil , otro inhibidor de la PDE5, comercializado bajo el nombre de Adcirca. [82] Se cree que los inhibidores de la PDE5 aumentan la vasodilatación de la arteria pulmonar e inhiben la remodelación vascular, reduciendo así la presión arterial pulmonar y la resistencia vascular pulmonar. [83]
El tadalafilo se toma por vía oral, al igual que el sildenafil, y se absorbe rápidamente (los niveles séricos son detectables a los 20 minutos). La T 1/2 ( vida media biológica ) ronda las 17,5 horas en sujetos sanos. [84] Además, si consideramos las implicaciones farmacoeconómicas, los pacientes que toman tadalafilo pagarían dos tercios del coste de la terapia con sildenafil. [85] Sin embargo, existen algunos efectos adversos de este fármaco como dolor de cabeza, diarrea, náuseas, dolor de espalda, dispepsia , sofocos y mialgia . [86]
El medicamento combinado macitentan/tadalafil (Opsynvi) fue aprobado para uso médico en Canadá en octubre de 2021, [87] y en los Estados Unidos en marzo de 2024. [88] [89]
Activadores de la guanilato ciclasa soluble
La guanilato ciclasa soluble (sGC) es el receptor intracelular del NO . En abril de 2009 [actualizar], los activadores de la sGC cinaciguat y riociguat estaban en fase de ensayos clínicos para el tratamiento de la HAP. [90]
Quirúrgico
La septostomía auricular es un procedimiento quirúrgico que crea una comunicación entre las aurículas derecha e izquierda . Alivia la presión en el lado derecho del corazón, pero a costa de niveles más bajos de oxígeno en la sangre ( hipoxemia ). El trasplante de pulmón reemplaza una condición crónica con la necesidad continua de tratamiento. [91] La supervivencia media posquirúrgica es de poco más de cinco años. [92]
La tromboendarterectomía pulmonar (TEP) es un procedimiento quirúrgico que se utiliza para la hipertensión pulmonar tromboembólica crónica. Es la extirpación quirúrgica de un trombo (coágulo) organizado junto con el revestimiento de la arteria pulmonar; es un procedimiento mayor y muy difícil que actualmente se realiza en unos pocos centros selectos. [93]
Escucha
Las pautas de práctica clínica establecidas dictan la frecuencia de evaluación y vigilancia de los nódulos pulmonares, [69] [94] los pacientes normalmente son monitoreados a través de pruebas comúnmente disponibles como: [ cita requerida ]
- Oximetría de pulso
- Pruebas de gases en sangre arterial
- Radiografías de tórax
- Pruebas de ECG seriadas
- Ecocardiografía seriada
- Espirometría o estudios más avanzados de la función pulmonar.
- Prueba de caminata de seis minutos [95]
Pronóstico
.jpg/440px-Heart_-_cor_pulmonale-_right_ventricular_hypertrophy_(4351912426).jpg)
La HAP se considera una enfermedad universalmente mortal, aunque el tiempo de supervivencia puede variar entre individuos. El pronóstico de la hipertensión arterial pulmonar (Grupo I de la OMS) tiene una supervivencia media sin tratamiento de 2 a 3 años desde el momento del diagnóstico, y la causa de muerte suele ser la insuficiencia ventricular derecha ( cor pulmonale ). [96] El tiempo de supervivencia es variable y depende de muchos factores. [97] Un estudio reciente de resultados de aquellos pacientes que habían comenzado el tratamiento con bosentán (Tracleer) mostró que el 89% de los pacientes estaban vivos a los 2 años. [98] Con las nuevas terapias, las tasas de supervivencia están aumentando. Para 2.635 pacientes inscritos en el Registro para evaluar el manejo temprano y a largo plazo de la enfermedad de hipertensión arterial pulmonar (Registro REVEAL) desde marzo de 2006 hasta diciembre de 2009, las tasas de supervivencia a 1, 3, 5 y 7 años fueron del 85%, 68%, 57% y 49%, respectivamente. En el caso de los pacientes con HAP idiopática/familiar, las tasas de supervivencia fueron del 91 %, 74 %, 65 % y 59 %. [99] Los niveles de mortalidad son muy elevados en las mujeres embarazadas con hipertensión arterial pulmonar grave (grupo I de la OMS). En ocasiones, se describe el embarazo como contraindicado en estas mujeres. [100] [101] [102]
Epidemiología
La epidemiología de la HAPI es de alrededor de 125 a 150 muertes por año en los EE. UU., y en todo el mundo la incidencia es similar en 4 casos por millón. Sin embargo, en partes de Europa (Francia), las indicaciones son 6 casos por millón de HAPI. Las mujeres tienen una tasa de incidencia más alta que los hombres (2-9:1). [103] Otras formas de HP son mucho más comunes. En la esclerodermia sistémica , la incidencia se ha estimado en un 8 a 12% de todos los pacientes; [104] en la artritis reumatoide es rara. [105] Sin embargo, en el lupus eritematoso sistémico es del 4 al 14%, [106] y en la enfermedad de células falciformes, varía del 20 al 40%. [107] Hasta el 4% de las personas que desarrollan una embolia pulmonar continúan desarrollando una enfermedad tromboembólica crónica, incluida la hipertensión pulmonar. [40] Un pequeño porcentaje de pacientes con EPOC desarrollan hipertensión pulmonar sin otra enfermedad que explique la presión alta. [108] Por otro lado, el síndrome de obesidad-hipoventilación se asocia muy comúnmente con insuficiencia cardíaca derecha debido a hipertensión pulmonar. [109]
Investigación
Para las personas que heredaron la enfermedad, se está estudiando la terapia genética. [110]
Cultura y sociedad
Casos notables
- Elaine Kaufman , restauradora estadounidense [111]
- Ina Balin , actriz estadounidense de Broadway y televisión [112]
- Chloe Temtchine , cantautora estadounidense [113] [114]
- Natalie Cole , cantante estadounidense [115]
Véase también
- Asociación de Hipertensión Pulmonar
- Revisión de resultados de hipertensión pulmonar de Cambridge (CAMPHOR)
Referencias
- ^ abcde «Hipertensión arterial pulmonar». Genetics Home Reference . Enero de 2016. Archivado desde el original el 28 de julio de 2017. Consultado el 30 de julio de 2017 .
- ^ ab "¿Cuáles son los signos y síntomas de la hipertensión pulmonar? – NHLBI, NIH". www.nhlbi.nih.gov . Archivado desde el original el 5 de enero de 2016 . Consultado el 30 de diciembre de 2015 .
- ^ abcde "¿Quién corre riesgo de sufrir hipertensión pulmonar?". NHLBI – NIH . 2 de agosto de 2011. Archivado desde el original el 31 de julio de 2017 . Consultado el 30 de julio de 2017 .
- ^ abcdefghij Humbert M, Kovacs G, Hoeper MM, Badagliacca R, Berger RM, Brida M, et al. (octubre de 2022). "Guía ESC/ERS 2022 para el diagnóstico y tratamiento de la hipertensión pulmonar". Revista Europea del Corazón . 43 (38): 3618–3731. doi :10.1093/eurheartj/ehac237. PMID 36017548.
- ^ abc "Causas y factores de riesgo". Temas de salud: Hipertensión pulmonar . Instituto Nacional del Corazón, los Pulmones y la Sangre. Biblioteca Nacional de Medicina. 24 de marzo de 2022.
- ^ abcd "Tratamiento". Temas de salud: Hipertensión pulmonar . Instituto Nacional del Corazón, los Pulmones y la Sangre. Biblioteca Nacional de Medicina. 24 de marzo de 2022.
- ^ abc NHLBI y ¿Qué es la hipertensión pulmonar? 2023
- ^ "Diagnóstico". Temas de salud: Hipertensión pulmonar . Instituto Nacional del Corazón, los Pulmones y la Sangre. Biblioteca Nacional de Medicina. 24 de marzo de 2022.
- ^ von Romberg E (1891-1892). "Über Sklerose der Lungenarterie". Dtsch Arch Klin Med (en alemán). 48 : 197-206.
- ^ abcd Simonneau G, Robbins IM, Beghetti M, Channick RN, Delcroix M, Denton CP, et al. (junio de 2009). "Clasificación clínica actualizada de la hipertensión pulmonar". Journal of the American College of Cardiology . 54 (1 Suppl): S43–S54. doi : 10.1016/j.jacc.2009.04.012 . PMID 19555858.
- ^ abcde Simonneau G, Gatzoulis MA, Adatia I, Celermajer D, Denton C, Ghofrani A, et al. (Diciembre de 2013). "Clasificación clínica actualizada de la hipertensión pulmonar". Revista del Colegio Americano de Cardiología . 62 (25 supl.): D34 – D41. doi : 10.1016/j.jacc.2013.10.029 . PMID 24355639.
- ^ abcdefghijklmno Galiè N, Humbert M, Vachiery JL, Gibbs S, Lang I, Torbicki A, et al. (ESC Scientific Document Group) (enero de 2016). "Guía ESC/ERS 2015 para el diagnóstico y tratamiento de la hipertensión pulmonar: Grupo de trabajo conjunto para el diagnóstico y tratamiento de la hipertensión pulmonar de la Sociedad Europea de Cardiología (ESC) y la Sociedad Respiratoria Europea (ERS): Aprobado por: Asociación Europea de Cardiología Pediátrica y Congénita (AEPC), Sociedad Internacional de Trasplante Cardíaco y Pulmonar (ISHLT)". Revista Europea del Corazón . 37 (1): 67–119. doi : 10.1093/eurheartj/ehv317 . PMID 26320113.
- ^ ab "Aprenda sobre la hipertensión arterial pulmonar". PAH . Asociación Estadounidense del Pulmón . Consultado el 1 de agosto de 2023 .
- ^ Kolaitis NA, Zamanian RT, de Jesus Perez VA, Badesch DB, Benza RL, Burger CD, et al. (abril de 2021). "Diferencias clínicas y resultados entre la hipertensión arterial pulmonar asociada a metanfetamina y la idiopática en el Registro de la Asociación de Hipertensión Pulmonar". Anales de la Sociedad Torácica Estadounidense . 18 (4): 613–622. doi : 10.1513/AnnalsATS.202007-774OC . PMC 8174020. PMID 33064950 .
- ^ abcdefghijkl McLaughlin VV, Archer SL, Badesch DB, Barst RJ, Farber HW, Lindner JR, et al. (abril de 2009). "Documento de consenso de expertos de la ACCF/AHA 2009 sobre hipertensión pulmonar: un informe del Grupo de trabajo sobre documentos de consenso de expertos de la Fundación del Colegio Americano de Cardiología y la Asociación Estadounidense del Corazón desarrollado en colaboración con el Colegio Americano de Médicos del Tórax, la Sociedad Torácica Estadounidense y la Asociación de Hipertensión Pulmonar". Revista del Colegio Americano de Cardiología . 53 (17): 1573–1619. doi : 10.1016/j.jacc.2009.01.004 . PMID 19389575.
- ^ Diller GP, Gatzoulis MA (febrero de 2007). "Enfermedad vascular pulmonar en adultos con cardiopatía congénita". Circulation . 115 (8): 1039–1050. doi : 10.1161/CIRCULATIONAHA.105.592386 . PMID 17325254.
- ^ ab Fang JC, DeMarco T, Givertz MM, Borlaug BA, Lewis GD, Rame JE, et al. (septiembre de 2012). "Grupo 2 de hipertensión pulmonar de la Organización Mundial de la Salud: hipertensión pulmonar debida a enfermedad cardíaca izquierda en adultos: una declaración resumida del Consejo de Hipertensión Pulmonar de la Sociedad Internacional de Trasplante de Corazón y Pulmón". The Journal of Heart and Lung Transplantation . 31 (9): 913–933. doi : 10.1016/j.healun.2012.06.002 . PMID 22884380.
- ^ Yusuf S, Cairns J, Camm J, Fallen EL, Gersh BJ (2011). Cardiología basada en la evidencia. John Wiley & Sons. pág. 70.3 (figura). ISBN 978-1-4443-5945-9. Archivado desde el original el 30 de abril de 2016.
- ^ ab "Presentación clínica de la hipertensión pulmonar primaria: antecedentes, exploración física, complicaciones". emedicine.medscape.com . Archivado desde el original el 2015-11-01 . Consultado el 2015-12-30 .
- ^ Hatano S, Strasser R (1975). Hipertensión pulmonar primaria . Ginebra: Organización Mundial de la Salud.
- ^ Rich S, Rubin LJ, Abenhail L, et al. (1998). Resumen ejecutivo del Simposio Mundial sobre Hipertensión Pulmonar Primaria (Evian, Francia, 6-10 de septiembre de 1998). Ginebra: Organización Mundial de la Salud. Archivado desde el original el 8 de abril de 2002.
- ^ Simonneau G, Galiè N, Rubin LJ, Langleben D, Seeger W, Domenighetti G, et al. (junio de 2004). "Clasificación clínica de la hipertensión pulmonar". Journal of the American College of Cardiology . 43 (12 Suppl S): 5S–12S. doi : 10.1016/j.jacc.2004.02.037 . PMID 15194173.
- ^ Galiè N, Humbert M, Vachiery JL, Gibbs S, Lang I, Torbicki A, et al. (enero de 2016). "Guía ESC/ERS 2015 para el diagnóstico y tratamiento de la hipertensión pulmonar: Grupo de trabajo conjunto para el diagnóstico y tratamiento de la hipertensión pulmonar de la Sociedad Europea de Cardiología (ESC) y la Sociedad Respiratoria Europea (ERS): Aprobado por: Asociación Europea de Cardiología Pediátrica y Congénita (AEPC), Sociedad Internacional de Trasplante Cardíaco y Pulmonar (ISHLT)". Revista Europea del Corazón . 37 (1): 67–119. doi : 10.1093/eurheartj/ehv317 . PMID 26320113.
- ^ Rabinovitch M (diciembre de 2012). "Patogénesis molecular de la hipertensión arterial pulmonar". The Journal of Clinical Investigation . 122 (12): 4306–4313. doi :10.1172/JCI60658. PMC 3533531 . PMID 23202738.
- ^ Hadinnapola C, Bleda M, Haimel M, Screaton N, Swift A, Dorfmüller P, et al. (noviembre de 2017). "Caracterización fenotípica de portadores de la mutación EIF2AK4 en una gran cohorte de pacientes diagnosticados clínicamente con hipertensión arterial pulmonar". Circulation . 136 (21): 2022–2033. doi :10.1161/CIRCULATIONAHA.117.028351. PMC 5700414 . PMID 28972005.
- ^ abcd Hassoun, Paul M. (16 de diciembre de 2021). "Hipertensión arterial pulmonar". New England Journal of Medicine . 385 (25): 2361–2376. doi :10.1056/NEJMra2000348. PMID 34910865.
- ^ Jacob AS, Nielsen DH, Gianelly RE (febrero de 1985). "Fibrilación ventricular fatal después de verapamilo en el síndrome de Wolff-Parkinson-White con fibrilación auricular". Anales de Medicina de Emergencia . 14 (2): 159–160. doi :10.1016/j.jacc.2013.10.025. PMC 3970402 . PMID 3970402.
- ^ abc Vonk-Noordegraaf A, Haddad F, Chin KM, Forfia PR, Kawut SM, Lumens J, et al. (Diciembre de 2013). "Adaptación del corazón derecho a la hipertensión arterial pulmonar: fisiología y patobiología". Revista del Colegio Americano de Cardiología . 62 (25 supl.): D22 – D33. doi : 10.1016/j.jacc.2013.10.027 . PMID 24355638.
- ^ abc Galiè N, Hoeper MM, Humbert M, Torbicki A, Vachiery JL, Barbera JA, et al. (diciembre de 2009). "Pautas para el diagnóstico y tratamiento de la hipertensión pulmonar". The European Respiratory Journal . 34 (6): 1219–1263. doi : 10.1183/09031936.00139009 . PMID 19749199.
- ^ Yuan JX, Rubin LJ (febrero de 2005). "Patogénesis de la hipertensión arterial pulmonar: la necesidad de múltiples impactos". Circulation . 111 (5): 534–538. doi : 10.1161/01.CIR.0000156326.48823.55 . PMID 15699271.
- ^ Tuder RM, Marecki JC, Richter A, Fijalkowska I, Flores S (marzo de 2007). "Patología de la hipertensión pulmonar". Clinics in Chest Medicine . 28 (1): 23–42, vii. doi :10.1016/j.ccm.2006.11.010. PMC 1924722 . PMID 17338926.
- ^ Bordones-Crom A, Patnaik SS, Menon PG, Murali S, Finol E (julio de 2021). "Análisis morfológico de la pared endocárdica del ventrículo derecho en la hipertensión pulmonar". Revista de ingeniería biomecánica . 143 (7). doi :10.1115/1.4050457. PMID 33704381. S2CID 232193407.
- ^ Montani D, Price LC, Dorfmuller P, Achouh L, Jaïs X, Yaïci A, et al. (enero de 2009). "Enfermedad venooclusiva pulmonar". The European Respiratory Journal . 33 (1): 189–200. doi : 10.1183/09031936.00090608 . PMID 19118230.
- ^ Guazzi M, Galiè N (diciembre de 2012). "Hipertensión pulmonar en la enfermedad cardíaca izquierda". European Respiratory Review . 21 (126): 338–346. doi : 10.1183/09059180.00004612 . PMC 9487233 . PMID 23204122.
- ^ Vachiéry JL, Adir Y, Barberà JA, Champion H, Coghlan JG, Cottin V, et al. (diciembre de 2013). "Hipertensión pulmonar debida a enfermedades del corazón izquierdo". Journal of the American College of Cardiology . 62 (25 Suppl): D100–D108. doi : 10.1016/j.jacc.2013.10.033 . hdl : 11585/534481 . PMID 24355634.
- ^ Shanks N, Macklin J, Coles S (2009). "Comparación de etilsuccinato de eritromicina oral y amoxicilina potenciada con clavulanato en el tratamiento de infecciones agudas del tracto respiratorio". Terapéutica clínica . 11 (6): 812–819. doi :10.1016/j.coph.2009.02.006. PMC 2692823 . PMID 2692823.
- ^ Sommer N, Dietrich A, Schermuly RT, Ghofrani HA, Gudermann T, Schulz R, et al. (diciembre de 2008). "Regulación de la vasoconstricción pulmonar hipóxica: mecanismos básicos". The European Respiratory Journal . 32 (6): 1639–1651. doi : 10.1183/09031936.00013908 . PMID 19043010.
- ^ Stenmark KR, Fagan KA, Frid MG (septiembre de 2006). "Remodelación vascular pulmonar inducida por hipoxia: mecanismos celulares y moleculares". Circulation Research . 99 (7): 675–691. doi : 10.1161/01.RES.0000243584.45145.3f . PMID 17008597.
- ^ McNeil K, Dunning J (septiembre de 2007). "Hipertensión pulmonar tromboembólica crónica (HPTEC)". Heart . 93 (9): 1152–1158. doi :10.1136/hrt.2004.053603. PMC 1955041 . PMID 17699182.
- ^ ab Hoeper MM, Mayer E, Simonneau G, Rubin LJ (abril de 2006). "Hipertensión pulmonar tromboembólica crónica". Circulation . 113 (16): 2011–2020. doi : 10.1161/CIRCULATIONAHA.105.602565 . PMID 16636189.
- ^ ab Budhiraja R, Tuder RM, Hassoun PM (enero de 2004). "Disfunción endotelial en la hipertensión pulmonar". Circulation . 109 (2): 159–165. doi : 10.1161/01.CIR.0000102381.57477.50 . PMID 14734504.
- ^ Förstermann U, Münzel T (abril de 2006). "Sintasa de óxido nítrico endotelial en la enfermedad vascular: de maravilla a amenaza". Circulation . 113 (13): 1708–1714. doi : 10.1161/CIRCULATIONAHA.105.602532 . PMID 16585403.
- ^ Murad F (noviembre de 2006). "Shattuck Lecture. Óxido nítrico y GMP cíclico en la señalización celular y el desarrollo de fármacos". The New England Journal of Medicine . 355 (19): 2003–2011. doi : 10.1056/NEJMsa063904 . PMID 17093251.
- ^ ab Francis SH, Busch JL, Corbin JD, Sibley D (septiembre de 2010). "Proteínas quinasas dependientes de cGMP y fosfodiesterasas de cGMP en la acción del óxido nítrico y cGMP". Pharmacological Reviews . 62 (3): 525–563. doi :10.1124/pr.110.002907. PMC 2964902 . PMID 20716671.
- ^ Zelia OP, Kovalenko FP (2011). "Eficiencia comparativa de la infección de animales de laboratorio mediante administración intravenosa y subcutánea de cercarias de Schistosoma mansoni". Parazitologiia . 20 (6): 461–465. PMID 3103045.
- ^ Ghofrani HA, Pepke-Zaba J, Barbera JA, Channick R, Keogh AM, Gomez-Sanchez MA, et al. (junio de 2004). "Vía del óxido nítrico e inhibidores de la fosfodiesterasa en la hipertensión arterial pulmonar". Journal of the American College of Cardiology . 43 (12 Suppl S): 68S–72S. doi : 10.1016/j.jacc.2004.02.031 . PMID 15194181.
- ^ McLaughlin VV, McGoon MD (septiembre de 2006). "Hipertensión arterial pulmonar". Circulation . 114 (13): 1417–1431. doi : 10.1161/CIRCULATIONAHA.104.503540 . PMID 17000921.
- ^ Fonseca C, Abraham D, Renzoni EA (enero de 2011). "Endotelina en la fibrosis pulmonar". American Journal of Respiratory Cell and Molecular Biology . 44 (1): 1–10. doi :10.1165/rcmb.2009-0388TR. PMID 20448055.
- ^ abcdef Wood SF (enero de 1986). "Astemizol y terfenadina comparados en la fiebre del heno". The Practitioner . 230 (1411): 41–44. doi : 10.1161/CIRCULATIONAHA.108.847707 . PMC 2869481 . PMID 2869481.
- ^ Gomberg-Maitland M, Olschewski H (abril de 2008). "Terapias con prostaciclina para el tratamiento de la hipertensión arterial pulmonar". The European Respiratory Journal . 31 (4): 891–901. doi : 10.1183/09031936.00097107 . PMID 18378784.
- ^ ab Lenfant M (2013). "[Fijación de dihidroestreptomicina en los ribosomas de E. coli]". Biochimie . 54 (2): 283–285. doi : 10.1016/j.jacc.2013.10.026 . PMC 4117578 . PMID 4117578.
- ^ Lawrie A (diciembre de 2014). "El papel del eje ligando inductor de apoptosis relacionado con osteoprotegerina/factor de necrosis tumoral en la patogénesis de la hipertensión arterial pulmonar". Farmacología vascular . 63 (3): 114–117. doi :10.1016/j.vph.2014.10.002. PMID 25446166.
- ^ Braithwaite AT, Marriott HM, Lawrie A (2018). "Roles divergentes de TRAIL en enfermedades pulmonares". Frontiers in Medicine . 5 : 212. doi : 10.3389/fmed.2018.00212 . PMC 6072839 . PMID 30101145.
- ^ abc Ranchoux B, Meloche J, Paulin R, Boucherat O, Provencher S, Bonnet S (junio de 2016). "Daños en el ADN e hipertensión pulmonar". Int J Mol Sci . 17 (6): 990. doi : 10.3390/ijms17060990 . PMC 4926518 . PMID 27338373.
- ^ "¿Cómo se diagnostica la hipertensión pulmonar? – NHLBI, NIH". www.nhlbi.nih.gov . Archivado desde el original el 5 de enero de 2016. Consultado el 30 de diciembre de 2015 .
- ^ Austin ED, Phillips III JA, Loyd JE (28 de diciembre de 2015). "Hipertensión arterial pulmonar". En Adam MP, Feldman J, Mirzaa GM, Pagon RA, Wallace SE, Bean LH, Gripp KW, Amemiya A (eds.). Referencia del hogar de genética . Archivado desde el original el 24 de diciembre de 2015 . Consultado el 30 de diciembre de 2015 .
- ^ Austin ED, Loyd JE, Phillips JA (enero de 1993). "Descripción general de la hipertensión arterial pulmonar hereditaria". En Pagon RA, Adam MP, Ardinger HH, Wallace SE, Amemiya A, Bean LJ, Bird TD, Fong C, Mefford HC (eds.). GeneReviews . Seattle (WA): Universidad de Washington, Seattle. PMID 20301658. NBK1485.
- ^ abcdef Hoeper MM, Bogaard HJ, Condliffe R, Frantz R, Khanna D, Kurzyna M, et al. (diciembre de 2013). "Definiciones y diagnóstico de la hipertensión pulmonar". Journal of the American College of Cardiology . 62 (25 Suppl): D42–D50. doi : 10.1016/j.jacc.2013.10.032 . PMID 24355641.
- ^ Klepper MJ, Cobert B (25 de octubre de 2010). Datos sobre seguridad de medicamentos: cómo analizarlos, resumirlos e interpretarlos para determinar el riesgo. Jones & Bartlett Learning. pág. 86. ISBN 978-0-7637-6912-3. Archivado desde el original el 4 de mayo de 2016.
- ^ Taleb M, Khuder S, Tinkel J, Khouri SJ (marzo de 2013). "La precisión diagnóstica de la ecocardiografía Doppler en la evaluación de la presión sistólica de la arteria pulmonar: un metaanálisis". Ecocardiografía . 30 (3): 258–265. doi :10.1111/echo.12061. PMID 23227919. S2CID 7460778.
- ^ "¿Cómo se diagnostica la hipertensión pulmonar?". Instituto Nacional del Corazón, los Pulmones y la Sangre.
- ^ abcdefg Gaillard F. «Hipertensión pulmonar». Radiopaedia . Consultado el 12 de marzo de 2018 .
- ^ Bossone E, D'Andrea A, D'Alto M, Citro R, Argiento P, Ferrara F, et al. (enero de 2013). "Ecocardiografía en hipertensión arterial pulmonar: del diagnóstico al pronóstico". Revista de la Sociedad Americana de Ecocardiografía . 26 (1): 1–14. doi :10.1016/j.echo.2012.10.009. PMID 23140849.
- ^ "Swan-Ganz: cateterismo cardíaco derecho". Enciclopedia Médica . MedlinePlus, Biblioteca Nacional de Medicina. 2022.
- ^ Khouri SJ, Pandya U (2012). "Hipertensión pulmonar". En Garcia MJ (ed.). Imágenes cardiovasculares no invasivas: un enfoque multimodal . Lippincott Williams & Wilkins. págs. 655–668.
- ^ Piskin S, Patnaik SS, Han D, Bordones AD, Murali S, Finol EA (marzo de 2020). "Un análisis de correlación canónica de la relación entre los atributos clínicos y los índices hemodinámicos específicos del paciente en la hipertensión pulmonar del adulto". Ingeniería médica y física . 77 : 1–9. doi :10.1016/j.medengphy.2020.01.006. PMC 7069525 . PMID 32007361.
- ^ Pillalamarri NR, Piskin S, Patnaik SS, Murali S, Finol EA (diciembre de 2021). "Análisis computacional específico del paciente de la hemodinámica en la hipertensión pulmonar del adulto". Anales de ingeniería biomédica . 49 (12): 3465–3480. doi :10.1007/s10439-021-02884-y. PMC 8684831 . PMID 34799807.
- ^ "¿Cómo se trata la hipertensión pulmonar? – NHLBI, NIH". www.nhlbi.nih.gov . Archivado desde el original el 5 de enero de 2016. Consultado el 30 de diciembre de 2015 .
- ^ abcd American College of Chest Physicians ; American Thoracic Society (septiembre de 2013), "Cinco cosas que los médicos y los pacientes deberían cuestionar", Choosing Wisely : una iniciativa de la ABIM Foundation , American College of Chest Physicians y American Thoracic Society, archivado desde el original el 3 de noviembre de 2013 , consultado el 6 de enero de 2013, que cita
- McLaughlin VV, Archer SL, Badesch DB, Barst RJ, Farber HW, Lindner JR, et al. (abril de 2009). "Documento de consenso de expertos de la ACCF/AHA 2009 sobre hipertensión pulmonar: un informe del Grupo de trabajo sobre documentos de consenso de expertos de la Fundación del Colegio Americano de Cardiología y la Asociación Estadounidense del Corazón: desarrollado en colaboración con el Colegio Americano de Médicos del Tórax, la Sociedad Torácica Estadounidense, Inc. y la Asociación de Hipertensión Pulmonar". Circulation . 119 (16): 2250–2294. doi : 10.1161/CIRCULATIONAHA.109.192230 . PMID 19332472.
- Galiè N, Hoeper MM, Humbert M, Torbicki A, Vachiery JL, Barbera JA, et al. (octubre de 2009). "Directrices para el diagnóstico y tratamiento de la hipertensión pulmonar: el Grupo de trabajo para el diagnóstico y tratamiento de la hipertensión pulmonar de la Sociedad Europea de Cardiología (ESC) y la Sociedad Respiratoria Europea (ERS), avalado por la Sociedad Internacional de Trasplante Cardíaco y Pulmonar (ISHLT)". Revista Europea del Corazón . 30 (20): 2493–2537. doi : 10.1093/eurheartj/ehp297 . PMID 19713419.
- Hoeper MM, Barberà JA, Channick RN, Hassoun PM, Lang IM, Manes A, et al. (junio de 2009). "Diagnóstico, evaluación y tratamiento de la hipertensión arterial no pulmonar e hipertensión pulmonar". Journal of the American College of Cardiology . 54 (1 Suppl): S85–S96. doi : 10.1016/j.jacc.2009.04.008 . PMID 19555862.
- ^ Barst RJ, McGoon M, Torbicki A, Sitbon O, Krowka MJ, Olschewski H, Gaine S (junio de 2004). "Diagnóstico y evaluación diferencial de la hipertensión arterial pulmonar". Journal of the American College of Cardiology . 43 (12 Suppl S): 40S–47S. doi : 10.1016/j.jacc.2004.02.032 . PMID 15194177.
- ^ Sitbon O, Humbert M, Jaïs X, Ioos V, Hamid AM, Provencher S, et al. (junio de 2005). "Respuesta a largo plazo a los bloqueadores de los canales de calcio en la hipertensión arterial pulmonar idiopática". Circulation . 111 (23): 3105–3111. doi : 10.1161/CIRCULATIONAHA.104.488486 . PMID 15939821.
- ^ Torres F (octubre de 2007). "Revisión sistemática de ensayos clínicos aleatorizados y doble ciego de agentes orales realizados en pacientes con hipertensión arterial pulmonar". Revista Internacional de Práctica Clínica . 61 (10): 1756–1765. doi : 10.1111/j.1742-1241.2007.01545.x . PMID 17877662. S2CID 1191543.
- ^ "La FDA aprueba Winrevair (sotatercept-csrk) de Merck, un tratamiento de primera clase para adultos con hipertensión arterial pulmonar (HAP, grupo 1 de la OMS*)" (Comunicado de prensa). Merck. 27 de marzo de 2024. Consultado el 27 de marzo de 2024 .
- ^ Morris NR, Kermeen FD, Jones AW, Lee JY, Holland AE, et al. (Grupo Cochrane de Vías Respiratorias) (marzo de 2023). "Programas de rehabilitación basados en ejercicios para la hipertensión pulmonar". Base de Datos Cochrane de Revisiones Sistemáticas . 2023 (3): CD011285. doi :10.1002/14651858.CD011285.pub3. PMC 10032353 . PMID 36947725.
- ^ Raja SG, Raja SM (noviembre de 2011). "Tratamiento de la hipertensión arterial pulmonar: tratamientos actuales y perspectivas futuras". Avances terapéuticos en enfermedades crónicas . 2 (6): 359–370. doi :10.1177/2040622311420773. PMC 3513893. PMID 23251761 .
- ^ Safdar Z (junio de 2011). "Tratamiento de la hipertensión arterial pulmonar: el papel de la prostaciclina y los análogos de la prostaglandina". Medicina respiratoria . 105 (6): 818–827. doi : 10.1016/j.rmed.2010.12.018 . PMID 21273054.
- ^ "Drugs@FDA: Medicamentos aprobados por la FDA".
- ^ Liu C, Chen J, Gao Y, Deng B, Liu K, et al. (Grupo Cochrane de Vías Respiratorias) (marzo de 2021). "Antagonistas del receptor de endotelina para la hipertensión arterial pulmonar". Base de Datos Cochrane de Revisiones Sistemáticas . 2021 (3): CD004434. doi :10.1002/14651858.CD004434.pub6. PMC 8094512 . PMID 33765691.
- ^ "ACTUALIZACIÓN 1: Encysive obtiene la aprobación canadiense para su uso como fármaco contra la hipertensión". Reuters . 2008-05-30. Archivado desde el original el 2007-07-04 . Consultado el 2007-07-08 .
- ^ "Pfizer retira Thelin por daños en el hígado - CBS Detroit". www.cbsnews.com . 10 de diciembre de 2010.
- ^ "La Administración de Alimentos y Medicamentos de Estados Unidos aprueba el tratamiento de la hipertensión arterial pulmonar con Letairis de Gilead" (Comunicado de prensa). Gilead Sciences . 15 de junio de 2007. Archivado desde el original el 27 de septiembre de 2007. Consultado el 16 de junio de 2007 .
- ^ "La FDA aprueba los comprimidos de Adcirca (tadalafil) para la hipertensión arterial pulmonar" (Nota de prensa). 2009-05-26. Archivado desde el original el 2010-12-03 . Consultado el 2010-12-06 .
- ^ Duarte JD, Hanson RL, Machado RF (mayo de 2013). "Tratamientos farmacológicos para la hipertensión pulmonar: exploración de la farmacogenómica". Future Cardiology . 9 (3): 335–349. doi :10.2217/fca.13.6. PMC 3864092 . PMID 23668740.
- ^ Forgue ST, Patterson BE, Bedding AW, Payne CD, Phillips DL, Wrishko RE, Mitchell MI (marzo de 2006). "Farmacocinética del tadalafilo en sujetos sanos". British Journal of Clinical Pharmacology . 61 (3): 280–288. doi :10.1111/j.1365-2125.2005.02553.x. PMC 1885023 . PMID 16487221.
- ^ Arif SA, Poon H (agosto de 2011). "Tadalafil: un inhibidor de la fosfodiesterasa-5 de acción prolongada para el tratamiento de la hipertensión arterial pulmonar". Clin Ther . 33 (8): 993–1004. doi :10.1016/j.clinthera.2011.06.008. PMID 21762988.
- ^ Galiè N, Brundage BH, Ghofrani HA, Oudiz RJ, Simonneau G, Safdar Z, et al. (junio de 2009). "Terapia con tadalafilo para la hipertensión arterial pulmonar". Circulación . 119 (22): 2894–2903. doi : 10.1161/circulaciónaha.108.839274 . PMID 19470885.
- ^ "Opsynvi (macitentan y tadalafil) se convierte en el primer y único tratamiento combinado de dosis fija una vez al día aprobado por Health Canada para pacientes con hipertensión arterial pulmonar (HAP)". Johnson & Johnson (Comunicado de prensa). 15 de octubre de 2021. Consultado el 25 de marzo de 2024 .
- ^ "Carta de aprobación: Opsynvi (macitentan y tadalafil)" (PDF) . Administración de Alimentos y Medicamentos de Estados Unidos.
- ^ "La FDA de EE. UU. aprueba Opsynvi (macitentan y tadalafil) como la primera y única terapia combinada de un solo comprimido de administración diaria para pacientes con hipertensión arterial pulmonar (HAP)". Johnson & Johnson (Comunicado de prensa). 22 de marzo de 2024. Consultado el 25 de marzo de 2024 .
- ^ Lasker GF, Maley JH, Pankey EA, Kadowitz PJ (abril de 2011). "Tratamiento de la guanilato ciclasa soluble para la hipertensión pulmonar". Expert Review of Respiratory Medicine . 5 (2): 153–161. doi :10.1586/ers.11.9. PMC 3108035 . PMID 21510726.
- ^ George MP, Champion HC, Pilewski JM (2011). "Trasplante de pulmón para hipertensión pulmonar". Circulación pulmonar . 1 (2): 182–191. doi : 10.4103/2045-8932.83455 . PMC 3198646 . PMID 22034605.
- ^ "Informe anual OPTN/SRTR 2006". Registro científico de receptores de trasplantes de EE. UU. 1 de mayo de 2006. Archivado desde el original el 5 de junio de 2010. Consultado el 28 de marzo de 2007 .
- ^ Cerveri I, D'Armini AM, Viganò M (abril de 2003). "Tromboendarterectomía pulmonar casi 50 años después de los primeros intentos quirúrgicos". Heart . 89 (4): 369–370. doi :10.1136/heart.89.4.369. PMC 1769265 . PMID 12639858.
- ^ Colegio Americano de Médicos de Tórax ; Sociedad Torácica Estadounidense (septiembre de 2013), "Cinco cosas que los médicos y los pacientes deberían cuestionar", Choosing Wisely : una iniciativa de la Fundación ABIM , Colegio Americano de Médicos de Tórax y Sociedad Torácica Estadounidense, archivado desde el original el 3 de noviembre de 2013 , consultado el 6 de enero de 2013
- ^ Pautas: Prueba de caminata de seis minutos. Consultado: 2015
- ^ "Hipertensión pulmonar. Acerca de la hipertensión pulmonar | Paciente". Paciente . Archivado desde el original el 2016-01-02 . Consultado el 2015-12-30 .
- ^ Mouratoglou SA, Bayoumy AA, Noordegraaf AV (2021). "Modelos de predicción y puntuaciones en hipertensión pulmonar: una revisión". Current Pharmaceutical Design . 27 (10): 1266–1276. doi :10.2174/1381612824999201105163437. PMID 33155897. S2CID 226272078.
- ^ McLaughlin VV, Sitbon O, Badesch DB, Barst RJ, Black C, Galiè N, et al. (febrero de 2005). "Supervivencia con bosentán de primera línea en pacientes con hipertensión pulmonar primaria". The European Respiratory Journal . 25 (2): 244–249. doi : 10.1183/09031936.05.00054804 . PMID 15684287.
- ^ Benza RL, Miller DP, Barst RJ, Badesch DB, Frost AE, McGoon MD (agosto de 2012). "Una evaluación de la supervivencia a largo plazo desde el momento del diagnóstico en la hipertensión arterial pulmonar del Registro REVEAL". Chest . 142 (2): 448–456. doi :10.1378/chest.11-1460. PMID 22281797.
- ^ Kaufman MH, Stead L, Feig R (2007). Primeros auxilios para el internado de obstetricia y ginecología . Nueva York: McGraw-Hill, Medical Pub. Division. p. 100. ISBN 978-0-07-144874-1.
- ^ Ghosh AK (2008). Mayo Clinic Internal Medicine Review (8.ª edición). Informa Healthcare. pág. 55. ISBN 978-1-4200-8478-8.
- ^ British Journal of Anaesthesia: "Hipertensión pulmonar primaria en el embarazo; un papel para los nuevos vasodilatadores" Archivado el 21 de enero de 2011 en Wayback Machine el 19 de marzo de 2011
- ^ Oudiz RJ (6 de febrero de 2023). «Hipertensión arterial pulmonar idiopática: aspectos prácticos, antecedentes y fisiopatología». Referencia de Medscape .
- ^ York M, Farber HW (noviembre de 2011). "Hipertensión pulmonar: detección y evaluación en la esclerodermia". Current Opinion in Rheumatology . 23 (6): 536–544. doi :10.1097/BOR.0b013e32834ba6a7. PMID 21934501. S2CID 19528958.
- ^ Nannini C. "Enfermedad pulmonar en la artritis reumatoide". MedScape.com . MedScape. Archivado desde el original el 8 de febrero de 2016 . Consultado el 31 de diciembre de 2015 .
- ^ Mittoo S, Fell CD (abril de 2014). "Pulmonary gestures of systemic lupus erythematosus" (Manifestaciones pulmonares del lupus eritematoso sistémico). Seminars in Respiratory and Critical Care Medicine (Seminarios en medicina respiratoria y de cuidados críticos ) . 35 (2). MedScape: 249–254. doi :10.1055/s-0034-1371537. PMID 24668539. S2CID 24654448. Archivado desde el original el 26 de octubre de 2015. Consultado el 31 de diciembre de 2015 .
- ^ Lee MT, Rosenzweig EB, Cairo MS (agosto de 2007). "Hipertensión pulmonar en la enfermedad de células falciformes". Avances clínicos en hematología y oncología . 5 (8): 585, 645–653. PMID 17982405.
- ^ Minai OA, Chaouat A, Adnot S (junio de 2010). "Hipertensión pulmonar en la EPOC: epidemiología, importancia y tratamiento: enfermedad vascular pulmonar: la perspectiva global". Chest . 137 (6 Suppl): 39S–51S. doi :10.1378/chest.10-0087. PMID 20522579.
- ^ Balachandran JS, Masa JF, Mokhlesi B (septiembre de 2014). "Epidemiología y diagnóstico del síndrome de hipoventilación por obesidad". Clínicas de Medicina del Sueño . 9 (3): 341–347. doi :10.1016/j.jsmc.2014.05.007. PMC 4210766 . PMID 25360072.
- ^ Reynolds PN (febrero de 2011). "Terapia génica para la hipertensión pulmonar: perspectivas y desafíos". Opinión de expertos sobre terapia biológica . 11 (2): 133–143. doi :10.1517/14712598.2011.542139. PMID 21219232. S2CID 23641857.
- ^ "Elaine Kaufman, famosa restauradora de Elaine's, muere a los 81 años". Daily News . 3 de diciembre de 2010. Archivado desde el original el 28 de agosto de 2016 . Consultado el 27 de septiembre de 2016 .
- ^ Folkart BA (21 de junio de 1990). «Ina Balin, 52; Actriz de cine y televisión busca implante de pulmón». Los Angeles Times . Archivado desde el original el 11 de septiembre de 2016. Consultado el 27 de septiembre de 2016 .
- ^ Phull H (26 de julio de 2016). "Está atada a un tanque de oxígeno, pero su carrera como cantante está en alza". New York Post . Archivado desde el original el 14 de agosto de 2016.
- ^ Insdorf A (10 de noviembre de 2013). "Los desafíos de Chloe Temtchine". The Huffington Post . Archivado desde el original el 18 de septiembre de 2016.
- ^ "Autopsia: Las últimas horas de Natalie Cole". Autopsia . Narrador: Eric Meyers. Producción ejecutiva: Ed Taylor y Michael Kelpie. Reelz, 27 de mayo de 2017. Televisión.
Lectura adicional
- "Hipertensión arterial pulmonar". Genética: afecciones genéticas . MedlinePlus, Biblioteca Nacional de Medicina. 2016.
- "¿Qué es la hipertensión pulmonar?". Temas de salud: Hipertensión pulmonar . Instituto Nacional del Corazón, los Pulmones y la Sangre. Biblioteca Nacional de Medicina. Mayo de 2023.
- Rubin LJ, Badesch DB (agosto de 2005). "Evaluación y manejo del paciente con hipertensión arterial pulmonar". Anales de Medicina Interna . 143 (4): 282–292. CiteSeerX 10.1.1.463.8466 . doi :10.7326/0003-4819-143-4-200508160-00009. PMID 16103472. S2CID 28841269.
- Abman SH, Hansmann G, Archer SL, Ivy DD, Adatia I, Chung WK, et al. (noviembre de 2015). "Hipertensión pulmonar pediátrica: directrices de la American Heart Association y la American Thoracic Society". Circulation . 132 (21): 2037–2099. doi : 10.1161/CIR.0000000000000329 . PMID 26534956. S2CID 7412370.
Enlaces externos
- Manual Merck Home Edition: Hipertensión pulmonar

