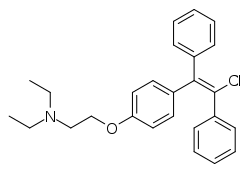
Clomifeno
 | |
 | |
| Datos clínicos | |
|---|---|
| Nombres comerciales | Clomid, Serophene, otros [1] |
| Otros nombres | Clomifeno; Cloramifeno; Cloramifeno; MRL-41; MRL/41; NSC-35770 |
| AHFS / Drogas.com | Monografía |
Categoría de embarazo |
|
| Vías de administración | Por la boca |
| Clase de droga | Modulador selectivo del receptor de estrógeno ; Progonadotropina |
| Código ATC |
|
| Estatus legal | |
| Estatus legal | |
| Datos farmacocinéticos | |
| Biodisponibilidad | Alto (>90%) |
| Metabolismo | CYP2D6 hepático (con circulación enterohepática ) [2] |
| Metabolitos | 4-Hidroxiclomifeno (4-OH-CLO), 4-Hidroxi-N-desetilclomifeno (4-OH-DE-CLO) |
| Vida media de eliminación | 4 – 7 días [2] [3] [4] metabolitos activos: |
| Excreción | Principalmente heces , algo en orina. |
| Identificadores | |
| |
| Número CAS | |
| Identificador de centro de PubChem |
|
| Unión Internacional para la Investigación y el Desarrollo (IUPHAR)/BPS |
|
| Banco de medicamentos | |
| Araña química | |
| UNIVERSIDAD |
|
| BARRIL | |
| EBICh | |
| Química biológica | |
| Panel de control CompTox ( EPA ) |
|
| Tarjeta informativa de la ECHA | 100.011.826 |
| Datos químicos y físicos | |
| Fórmula | C26H28ClNO |
| Masa molar | 405,97 g·mol −1 |
| Modelo 3D ( JSmol ) |
|
| |
 norte norte Y (¿que es esto?) (verificar) Y (¿que es esto?) (verificar) | |
El clomifeno , también conocido como clomifeno , es un medicamento utilizado para tratar la infertilidad en mujeres que no ovulan , incluidas aquellas con síndrome de ovario poliquístico . [5] Se toma por vía oral . [5]
Los efectos secundarios comunes incluyen dolor pélvico y sofocos . [5] Otros efectos secundarios pueden incluir cambios en la visión, vómitos, dificultad para dormir, cáncer de ovario y convulsiones . [5] [6] No se recomienda en personas con enfermedad hepática o sangrado vaginal anormal de causa desconocida o que estén embarazadas . [6] [7] El clomifeno pertenece a la familia de medicamentos moduladores selectivos del receptor de estrógeno (SERM) y es un medicamento no esteroide. [7] [8] Funciona provocando la liberación de GnRH por el hipotálamo y, posteriormente, gonadotropina de la pituitaria anterior . [6]
El clomifeno fue aprobado para uso médico en los Estados Unidos en 1967. [5] Está en la Lista de Medicamentos Esenciales de la Organización Mundial de la Salud , bajo la categoría "Inductores de la ovulación" (Lista complementaria). [9] Su introducción inició la era de la tecnología de reproducción asistida . [10]
También se ha descubierto que el clomifeno (en particular el isómero enclomifeno purificado) tiene una poderosa capacidad para aumentar o restaurar los niveles de testosterona en hombres hipogonadales . [11] Se puede utilizar para mejorar el rendimiento en los deportes y está prohibido por la Agencia Mundial Antidopaje .
Usos médicos
Medicina reproductiva
El clomifeno es una de las diversas alternativas para inducir la ovulación en mujeres infértiles debido a anovulación u oligoovulación . [12] No hay evidencia del uso de clomifeno en mujeres infértiles sin una razón conocida. [13] En tales casos, los estudios han observado una tasa de embarazo clínico del 5,6 % por ciclo con tratamiento con clomifeno frente al 1,3 %–4,2 % por ciclo sin tratamiento. [12] El clomifeno también se ha utilizado con otras tecnologías de reproducción asistida para aumentar las tasas de éxito de estas otras modalidades. [14]
El clomifeno se ha utilizado eficazmente para restaurar la espermatogénesis en mujeres trans que buscan tener hijos biológicos. [15] El efecto de la terapia hormonal feminizante sobre la fertilidad no está claro, pero se sabe que puede prevenir la producción de esperma. [16]
Terapia de reemplazo de testosterona
El clomifeno se utiliza a veces en el tratamiento del hipogonadismo masculino como una alternativa a la terapia de reemplazo de testosterona . [17] [ fuente no primaria necesaria ] Se ha descubierto que aumenta los niveles de testosterona de 2 a 2,5 veces en hombres hipogonadales en dichas dosis. [17] [18] A pesar de que se ha cuestionado el uso de cuestionarios en los ensayos comparativos de reemplazo de testosterona, se han observado el menor costo del clomifeno, los beneficios terapéuticos y el mayor valor para la mejora del hipogonadismo. [19] [ fuente no primaria necesaria ]
El clomifeno está formado por dos estereoisómeros en igual proporción: enclomifeno y zuclomifeno . El zuclomifeno tiene propiedades proestrogénicas, mientras que el enclomifeno es proandrogénico, es decir, promueve la producción de testosterona a través de la estimulación del eje HPG . Por esta razón, se ha descubierto que el isómero enclomifeno purificado es dos veces más eficaz para aumentar la testosterona en comparación con la mezcla estándar de ambos isómeros. [11] Además, el enclomifeno tiene una vida media de solo 10 horas, [4] pero el zuclomifeno tiene una vida media del orden de varios días a una semana, por lo que si el objetivo es aumentar la testosterona, tomar clomifeno regularmente puede producir efectos proestrogénicos mucho más duraderos que los efectos proandrogénicos. [20]
Ginecomastia
El clomifeno se ha utilizado en el tratamiento de la ginecomastia . [21] Se ha descubierto que es útil en el tratamiento de algunos casos de ginecomastia, pero no es tan eficaz como el tamoxifeno o el raloxifeno para esta indicación. [22] Ha mostrado resultados variables para la ginecomastia (probablemente porque el isómero zuclomifeno es estrogénico) y, por lo tanto, no se recomienda para el tratamiento de la afección. [23] Es probable que el isómero enclomifeno puro sea más eficaz que el clomifeno para tratar la ginecomastia, debido a la falta del isómero zuclomifeno (como se señaló anteriormente). [ cita médica necesaria ]
Debido a su larga vida media, el zuclomifeno puede detectarse en la orina durante al menos 261 días después de la interrupción [24] (261 días después de la interrupción con una vida media de 30 días, todavía se excreta el 0,24 % del nivel máximo de zuclomifeno, mientras que con una vida media de 10 horas, el enclomifeno alcanza el mismo nivel del 0,24 % en menos de 4 días [ cita médica necesaria ] ).
Uso prohibido en el deporte
La Agencia Mundial Antidopaje (AMA) prohíbe el clomifeno en la categoría S4 de moduladores hormonales y metabólicos. Puede estar presente como ingrediente no declarado en productos del mercado negro disponibles en línea para mejorar el rendimiento atlético. Al igual que otras sustancias con propiedades anabólicas , el clomifeno produce un aumento de la masa muscular en los hombres. [25]
Debido a que el clomifeno puede aumentar la producción de huevos en las gallinas , los atletas pueden consumir inadvertidamente la sustancia a través de alimentos contaminados. Un estudio de la AMA descubrió que el clomifeno administrado a las gallinas ponedoras migra a sus huevos, pero fue posible desarrollar un método para distinguir la ingestión de huevos del dopaje. [26]
Contraindicaciones
Las contraindicaciones incluyen alergia al medicamento, embarazo, problemas hepáticos previos, sangrado vaginal anormal de causa poco clara, quistes ováricos distintos de los debidos al síndrome de ovario poliquístico, problemas suprarrenales o tiroideos no controlados y tumores pituitarios . [7]
Efectos secundarios
La reacción adversa más común asociada con el uso de clomifeno (>10% de las personas) es el agrandamiento reversible de los ovarios. [7]
Los efectos menos comunes (1–10% de las personas) incluyen síntomas visuales (visión borrosa, visión doble , moscas volantes, sensibilidad ocular a la luz , escotomas ), dolores de cabeza, sofocos vasomotores (o sofocos ), sensibilidad a la luz y constricción pupilar, sangrado uterino anormal y/o malestar abdominal. [7]
Los eventos adversos raros (<1% de las personas) incluyen: niveles altos de triglicéridos en sangre , inflamación del hígado , calvicie reversible y/o síndrome de hiperestimulación ovárica . [7]
El clomifeno puede provocar ovulación múltiple, aumentando así las posibilidades de tener gemelos (un 10% de los nacimientos en lugar de aproximadamente un 1% en la población general) y trillizos . [ cita médica necesaria ]
Las tasas de defectos congénitos y abortos espontáneos no parecen cambiar con el uso de clomifeno para la fertilidad. [7] El clomifeno se ha asociado con anomalías hepáticas y un par de casos de hepatotoxicidad . [27]
Riesgo de cáncer
Algunos estudios han sugerido que el clomifeno, si se utiliza durante más de un año, puede aumentar el riesgo de cáncer de ovario . [13] Esto puede ser así sólo en aquellas mujeres que nunca han estado embarazadas ni quedan embarazadas. [28] Estudios posteriores no han podido respaldar esos hallazgos. [12] [29]
Se ha demostrado que el clomifeno está asociado con un mayor riesgo de melanomas malignos y cáncer de tiroides . [3] El riesgo de cáncer de tiroides no se asoció con el número de embarazos llevados a la viabilidad. [30]
Farmacología
Farmacodinamia
Actividad moduladora selectiva del receptor de estrógeno
El clomifeno es un derivado no esteroide del trifeniletileno que actúa como un modulador selectivo del receptor de estrógeno (SERM). [14] Consiste en una mezcla no racémica de zuclomifeno (~38%) y enclomifeno (~62%), cada uno de los cuales tiene propiedades farmacológicas únicas . [31] Es un agonista y antagonista mixto del receptor de estrógeno (ER). El clomifeno activa el ERα en el contexto de niveles basales bajos de estrógeno y bloquea parcialmente el receptor en el contexto de niveles basales altos de estrógeno. [18] Por el contrario, es un antagonista del ERβ . [18] El clomifeno tiene efectos antiestrogénicos en el útero . [32] Hay poca investigación clínica sobre la influencia del clomifeno en muchos tejidos diana, como los lípidos , el sistema cardiovascular y las mamas . [32] [33] Se han observado efectos positivos del clomifeno sobre los huesos . [18] [32] [33] Se ha descubierto que el clomifeno disminuye los niveles del factor de crecimiento similar a la insulina 1 (IGF-1) en mujeres. [34]
El clomifeno es un ligando de ER de acción prolongada , con una retención nuclear de más de 48 horas. [35] El clomifeno es un profármaco que se activa a través de vías metabólicas similares a las de los SERM de trifeniletileno relacionados, tamoxifeno y toremifeno . [36] [37] La afinidad del clomifeno por el ER en relación con el estradiol varía de 0,1 a 12% en diferentes estudios, que es similar al rango del tamoxifeno (0,06-16%). [38] [39] [40] El 4-hidroxiclomifeno, un metabolito activo principal del clomifeno, y el afimoxifeno (4-hidroxitamoxifeno), un metabolito activo principal del tamoxifeno, muestran un 89-251% y un 41-246% de la afinidad del estradiol por el ER en células de cáncer de mama MCF-7 humanas , respectivamente. [41] [42] Las afinidades de ER de los isómeros de 4-hidroxiclomifeno fueron 285% para ( E )-4-hidroxiclomifeno y 16% para ( Z )-4-hidroxiclomifeno en relación con el estradiol. [41] El 4-hidroxi- N -desmetilclomifeno tiene una afinidad similar al 4-hidroxiclomifeno para el ER. [37] En un estudio, las afinidades del clomifeno y sus metabolitos para el ERα fueron ~100 nM para el clomifeno, ~2,4 nM para el 4-hidroxiclomifeno, ~125 nM para el N -desmetilclomifeno y ~1,4 nM para el 4-hidroxi- N -desmetilclomifeno. [37]
Aunque el clomifeno tiene algún efecto estrogénico , se cree que la propiedad antiestrogénica es la fuente principal para estimular la ovulación . [5] El clomifeno parece actuar principalmente en el hipotálamo , donde agota los ER hipotalámicos y bloquea el efecto de retroalimentación negativa del estradiol endógeno circulante , lo que a su vez produce un aumento en la frecuencia del pulso de la hormona liberadora de gonadotropina (GnRH) hipotalámica y las concentraciones circulantes de la hormona folículo estimulante (FSH) y la hormona luteinizante (LH). [ cita médica necesaria ]
En el ciclo hormonal femenino fisiológico normal, siete días después de la ovulación , los altos niveles de estrógeno y progesterona producidos por el cuerpo lúteo inhiben la GnRH, FSH y LH en el hipotálamo y la hipófisis anterior. [ cita médica necesaria ] Si no se produce la fertilización en el período posterior a la ovulación, el cuerpo lúteo se desintegra debido a la falta de gonadotropina coriónica humana (hCG). [ cita médica necesaria ] Esto normalmente lo produciría el embrión en el esfuerzo por mantener los niveles de progesterona y estrógeno durante el embarazo. [ cita médica necesaria ]
Terapéuticamente, el clomifeno se administra temprano en el ciclo menstrual para producir folículos. [ cita médica necesaria ] Los folículos, a su vez, producen el estrógeno, que circula en el suero. [ cita médica necesaria ] En presencia de clomifeno, el cuerpo percibe un nivel bajo de estrógeno, similar al día 22 del ciclo anterior. [ cita médica necesaria ] Dado que el estrógeno ya no puede ejercer efectivamente una retroalimentación negativa sobre el hipotálamo, la secreción de GnRH se vuelve más rápidamente pulsátil, lo que resulta en una mayor liberación de gonadotropina pituitaria. [ cita médica necesaria ] (Los pulsos más rápidos y de menor amplitud de GnRH conducen a un aumento de la secreción de LH y FSH, mientras que los pulsos más irregulares y de mayor amplitud de GnRH conducen a una disminución en la proporción de LH a FSH. [ cita médica necesaria ] ) Los niveles aumentados de FSH causan el crecimiento de más folículos ováricos y, posteriormente, la ruptura de los folículos que resulta en la ovulación. La ovulación ocurre con mayor frecuencia entre 6 y 7 días después de un ciclo de clomifeno. [ cita médica necesaria ]
En hombres normales, se ha descubierto que 50 mg/día de clomifeno durante 8 meses aumenta los niveles de testosterona en alrededor de 870 ng/dL en hombres más jóvenes y en alrededor de 490 ng/dL en hombres mayores. [18] Los niveles de estradiol aumentaron en 62 pg/mL en hombres más jóvenes y en 40 pg/mL en hombres mayores. [18] Estos hallazgos sugieren que los efectos progonadotrópicos del clomifeno son más fuertes en hombres más jóvenes que en hombres mayores. [18] En hombres con hipogonadismo , se ha descubierto que el clomifeno aumenta los niveles de testosterona en 293 a 362 ng/dL y los niveles de estradiol en 5,5 a 13 pg/mL. [18] En un estudio clínico a gran escala de hombres con niveles bajos de testosterona (<400 ng/dL), 25 mg/día de clomifeno aumentaron los niveles de testosterona de 309 ng/dL a 642 ng/dL después de 3 meses de terapia. [43] No se observaron cambios significativos en los niveles de colesterol HDL , triglicéridos , glucosa en ayunas o prolactina , aunque los niveles de colesterol total disminuyeron significativamente. [18] [43]
| Medicamento | Mama | Hueso | Hígado | Útero | Vagina | Cerebro | ||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Lípidos | Coagulación | SHBGInformación sobre herramientas Globulina transportadora de hormonas sexuales | IGF-1Información sobre herramientas Factor de crecimiento similar a la insulina 1 | Sofocos | Gonadotropinas | |||||||||
| Estradiol | + | + | + | + | + | + | + | + | + | + | ||||
| "SERM ideal" | – | + | + | ± | ± | ± | – | + | + | ± | ||||
| Bazedoxifeno | – | + | + | + | + | ? | – | ± | – | ? | ||||
| Clomifeno | – | + | + | ? | + | + | – | ? | – | ± | ||||
| Lasofoxifeno | – | + | + | + | ? | ? | ± | ± | – | ? | ||||
| Ospemifeno | – | + | + | + | + | + | ± | ± | – | ± | ||||
| Raloxifeno | – | + | + | + | + | + | ± | – | – | ± | ||||
| Tamoxifeno | – | + | + | + | + | + | + | – | – | ± | ||||
| Toremifeno | – | + | + | + | + | + | + | – | – | ± | ||||
| Efecto: + = Estrogénico / agonista . ± = Mixto o neutro. – = Antiestrogénico / antagonista . Nota: Los SERM generalmente aumentan los niveles de gonadotropina en hombres hipogonadales y eugonadales, así como en mujeres premenopáusicas (antiestrogénicos), pero disminuyen los niveles de gonadotropina en mujeres posmenopáusicas (estrogénicos). Fuentes: Ver plantilla. | ||||||||||||||
Otras actividades
El clomifeno es un inhibidor de la conversión de desmosterol en colesterol por la enzima 24-dehidrocolesterol reductasa . [44] [45] Las preocupaciones sobre la posible inducción de desmosterolosis y síntomas asociados como cataratas e ictiosis con la exposición prolongada impidieron el uso de clomifeno en el tratamiento del cáncer de mama. [44] [45] Se ha descubierto que el uso continuo de clomifeno aumenta los niveles de desmosterol en un 10% y se ha informado que dosis altas continuas de clomifeno (200 mg/día) producen alteraciones visuales . [46] [47]
Farmacocinética
El clomifeno produce N- desmetilclomifeno, clomifenóxido (clomifeno N -óxido), 4-hidroxiclomifeno y 4-hidroxi- N -desmetilclomifeno como metabolitos . [2] [48] El clomifeno es un profármaco , principalmente de 4-hidroxiclomifeno y 4-hidroxi- N -desmetilclomifeno, que son los más activos de sus metabolitos. [36] [37] En un estudio, los niveles máximos después de una dosis única de 50 mg de clomifeno fueron 20,37 nmol/L para clomifeno, 0,95 nmol/L para 4-hidroxiclomifeno y 1,15 nmol/L para 4-hidroxi- N -desmetilclomifeno. [2]
El clomifeno comienza a actuar entre 5 y 10 días después del tratamiento y su semivida de eliminación es de entre 4 y 7 días. [2] [4] En un estudio, después de una dosis única de 50 mg de clomifeno, la semivida del clomifeno fue de 128 horas (5,3 días), la del 4-hidroxiclomifeno fue de 13 horas y la del 4-hidroxi- N -desmetilclomifeno fue de 15 horas. [2] Los individuos con el alelo CYP2D6*10 mostraron semividas más prolongadas para el 4-hidroxiclomifeno y el 4-hidroxi- N -desmetilclomifeno. [2] Debido principalmente a las diferencias en la genética del CYP2D6, las concentraciones en estado estacionario y la respuesta individual al clomifeno son muy variables. [49]
La mayor parte del metabolismo del clomifeno se produce en el hígado , donde sufre una recirculación enterohepática . El clomifeno y sus metabolitos se excretan principalmente a través de las heces (42 %), y la excreción puede producirse hasta 6 semanas después de la interrupción del tratamiento. [31]
Química
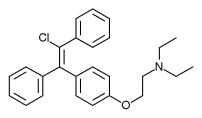
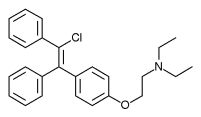
El clomifeno es un derivado del trifeniletileno . Es una mezcla de dos isómeros geométricos , la forma cis enclomifeno ( (E) -clomifeno) y la forma trans zuclomifeno ( (Z) -clomifeno). Estos dos isómeros contribuyen a las propiedades estrogénicas y antiestrogénicas mixtas del clomifeno. [10] La proporción típica de estos isómeros después de la síntesis es 38% de zuclomifeno y 62% de enclomifeno. [4] La Farmacopea de los Estados Unidos especifica que las preparaciones de clomifeno deben contener entre 30% y 50% de zuclomifeno. [4]
 |  |
Historia
Un equipo de la William S. Merrell Chemical Company dirigido por Frank Palopoli sintetizó clomifeno en 1956; después de que se confirmara su actividad biológica, se presentó una patente y se emitió en noviembre de 1959. [10] [50] Los científicos de Merrell habían sintetizado previamente clorotrianiseno y etamoxitrifetol . [10] El clomifeno se estudió en el tratamiento del cáncer de mama avanzado durante el período de 1964 a 1974 y se encontró que era eficaz, pero se abandonó debido a preocupaciones sobre la desmosterolosis con el uso prolongado. [44] [51] [52] El uso a corto plazo (por ejemplo, días a meses) no planteó las mismas preocupaciones y el clomifeno continuó siendo estudiado para otras indicaciones. [45] [46]
| Antiestrógeno | Dosificación | Años) | Tasa de respuesta | Efectos adversos |
|---|---|---|---|---|
| Etamoxitrifetol | 500–4.500 mg/día | 1960 | 25% | Episodios psicóticos agudos |
| Clomifeno | 100–300 mg/día | 1964–1974 | 34% | Riesgos de las cataratas |
| Nafoxidina | 180–240 mg/día | 1976 | 31% | Cataratas , ictiosis , fotofobia. |
| Tamoxifeno | 20–40 mg/día | 1971–1973 | 31% | Trombocitopenia transitoria a |
| Notas al pie: a = "La ventaja particular de este fármaco es la baja incidencia de efectos secundarios molestos (25)." "Los efectos secundarios fueron generalmente triviales (26)." Fuentes: [51] [53] | ||||
Los estudios clínicos se llevaron a cabo bajo una Solicitud de Nuevo Medicamento en Investigación ; el clomifeno fue el tercer fármaco para el cual se había presentado una Solicitud de Nuevo Medicamento en Investigación bajo la Enmienda Kefauver Harris de 1962 a la Ley Federal de Alimentos, Medicamentos y Cosméticos que se había aprobado en respuesta a la tragedia de la talidomida . [10] Fue aprobado para su comercialización en 1967 bajo la marca Clomid. [10] [54] Primero se utilizó para tratar casos de oligomenorrea , pero se amplió para incluir el tratamiento de la anovulación cuando las mujeres sometidas al tratamiento tenían tasas de embarazo más altas de lo esperado. [55]
Se considera ampliamente que el medicamento representó una revolución en el tratamiento de la infertilidad femenina, el comienzo de la era moderna de la tecnología de reproducción asistida y el comienzo de lo que, en palabras de Eli Y. Adashi , fue "el inicio de la epidemia de nacimientos múltiples en los EE. UU." [10] [56]
La compañía fue adquirida por Dow Chemical en 1980, [57] [58] y en 1989 Dow Chemical adquirió el 67 por ciento de las acciones de Marion Laboratories, que pasó a llamarse Marion Merrell Dow. [57] En 1995 Hoechst AG adquirió el negocio farmacéutico de Marion Merrell Dow. [59] Hoechst a su vez pasó a formar parte de Aventis en 1999, [60] : 9–11 y posteriormente de Sanofi . [61] Se convirtió en el fármaco más recetado para la inducción de la ovulación para revertir la anovulación u oligoovulación . [62]
Sociedad y cultura
Nombres de marca
El clomifeno se comercializa bajo muchas marcas en todo el mundo, entre ellas Beclom, Bemot, Biogen, Blesifen, Chloramiphene, Clofert, Clomene, ClomHEXAL, Clomi, Clomid, Clomidac, Clomifen, Clomifencitrat, Clomifene, Clomifène, Clomifene citrate, Clomifeni citras, Clomifeno, Clomifert, Clomihexal, Clomiphen, Clomiphene, Clomiphene Citrate, Cloninn, Clostil, Clostilbegyt, Clovertil, Clovul, Dipthen, Dufine, Duinum, Fensipros, Fertab, Fertec, Fertex, Ferticlo, Fertil, Fertilan, Fertilphen, Fertin, Fertomid, Ferton, Fertotab, Fertyl, Fetrop, Folistim, Genoclom, Genozym, Hete, I-Clom, Ikaclomin, Klofit, Klomen, Klomifen, Lomifen, MER 41, Milophene, Ofertil, Omifin, Ova-mit, Ovamit, Ovinum, Ovipreg, Ovofar, Ovuclon, Ovulet, Pergotime, Pinfetil, Profertil, Prolifen, Provula, Reomen, Serofene, Serophene, Serpafar, Serpafar, Surole, Tocofeno y Zimaquin. [1]
Regulación
El clomifeno está incluido en la lista de la Agencia Mundial Antidopaje de agentes dopantes ilegales en el deporte. [63] Está incluido en la lista porque es una "sustancia antiestrogénica". [ cita requerida ]
Investigación
El clomifeno se ha utilizado casi exclusivamente para la inducción de la ovulación en mujeres premenopáusicas y se ha estudiado muy limitadamente en mujeres posmenopáusicas . [64]
El clomifeno se estudió para el tratamiento y la prevención del cáncer de mama , pero los problemas de toxicidad llevaron al abandono de esta indicación, al igual que el descubrimiento del tamoxifeno . [65] Al igual que el fármaco estructuralmente relacionado triparanol , se sabe que el clomifeno inhibe la enzima 24-deshidrocolesterol reductasa y aumenta los niveles circulantes de desmosterol , lo que lo hace desfavorable para un uso prolongado en el cáncer de mama debido al riesgo de efectos secundarios como cataratas irreversibles . [66] [67]
Referencias
- ^ ab "Marcas internacionales de clomifeno -". Drugs.com. Archivado desde el original el 20 de septiembre de 2016. Consultado el 11 de septiembre de 2016 .
- ^ abcdefghi Kim MJ, Byeon JY, Kim YH, Kim SH, Lee CM, Jung EH, et al. (marzo de 2018). "Efecto del alelo CYP2D6*10 en la farmacocinética del clomifeno y sus metabolitos activos". Archivos de investigación farmacéutica . 41 (3): 347–353. doi :10.1007/s12272-018-1005-7. PMID 29516347. S2CID 4034257.
- ^ ab Yilmaz S, Yilmaz Sezer N, Gönenç İM, İlhan SE, Yilmaz E (abril de 2018). "Seguridad del citrato de clomifeno: una revisión de la literatura". Citotecnología . 70 (2): 489–495. doi :10.1007/s10616-017-0169-1. PMC 5851961 . PMID 29159661.
- ^ abcde Mikkelson TJ, Kroboth PD, Cameron WJ, Dittert LW, Chungi V, Manberg PJ (septiembre de 1986). "Farmacocinética de dosis única de citrato de clomifeno en voluntarios normales". Fertilidad y esterilidad . 46 (3): 392–396. doi :10.1016/S0015-0282(16)49574-9. PMID 3091405.
- ^ abcdef «Citrato de clomifeno». Sociedad Estadounidense de Farmacéuticos de Sistemas de Salud. Archivado desde el original el 14 de septiembre de 2017. Consultado el 8 de diciembre de 2016 .
- ^ abc Organización Mundial de la Salud (2009). Stuart MC, Kouimtzi M, Hill SR (eds.). Formulario Modelo de la OMS 2008. Organización Mundial de la Salud. págs. 385–386. hdl : 10665/44053 . ISBN. 9789241547659.
- ^ abcdefg "Etiqueta de comprimidos de citrato de clomifeno" (PDF) . FDA. Archivado (PDF) del original el 27 de septiembre de 2016 . Consultado el 11 de septiembre de 2016 .
- ^ Ghumman S (2015). Principios y práctica de la estimulación ovárica controlada en técnicas de reproducción asistida. Springer. pág. 65. ISBN 9788132216865Archivado desde el original el 27 de diciembre de 2016.
- ^ Organización Mundial de la Salud (2019). Lista modelo de medicamentos esenciales de la Organización Mundial de la Salud: 21.ª lista de 2019. Ginebra: Organización Mundial de la Salud. hdl : 10665/325771 . OMS/MVP/EMP/IAU/2019.06. Licencia: CC BY-NC-SA 3.0 IGO.
- ^ abcdefg Dickey RP, Holtkamp DE (1996). "Desarrollo, farmacología y experiencia clínica con citrato de clomifeno". Human Reproduction Update . 2 (6): 483–506. doi : 10.1093/humupd/2.6.483 . PMID 9111183.
- ^ ab Rodriguez KM, Pastuszak AW, Lipshultz LI (agosto de 2016). "Citrato de enclomifeno para el tratamiento del hipogonadismo masculino secundario". Opinión de expertos sobre farmacoterapia . 17 (11): 1561–7. doi :10.1080/14656566.2016.1204294. PMC 5009465. PMID 27337642 .
- ^ Comité de Práctica de la Sociedad Estadounidense de Medicina Reproductiva (agosto de 2013). "Uso de citrato de clomifeno en mujeres infértiles: opinión de un comité". Fertilidad y esterilidad . 100 (2): 341–8. doi : 10.1016/j.fertnstert.2013.05.033 . PMID 23809505.
- ^ ab Hughes E, Brown J, Collins JJ, Vanderkerchove P (enero de 2010). "Citrato de clomifeno para la subfertilidad inexplicada en mujeres". Base de datos Cochrane de revisiones sistemáticas . 2010 (1): CD000057. doi :10.1002/14651858.CD000057.pub2. PMC 7052733. PMID 20091498 .
- ^ ab Seli E, Arici A. "Inducción de la ovulación con citrato de clomifeno". UpToDate . Consultado el 30 de julio de 2019 .
- ^ Powers WJ, Costescu D, Massarella C, Gale J, Singh SS (marzo de 2024). "Un enfoque de afirmación de género para la atención de la fertilidad para pacientes transgénero y de género diverso" (PDF) . O&G Open . 1 (1): e002. doi :10.1097/og9.0000000000000002 . Consultado el 8 de julio de 2024 .
- ^ Schneider F, Neuhaus N, Wistuba J, Zitzmann M, Heß J, Mahler D, et al. (noviembre de 2015). "Funciones testiculares y caracterización clínica de pacientes con disforia de género (DG) sometidos a cirugía de reasignación de sexo (SRS)". The Journal of Sexual Medicine . 12 (11): 2190–2200. doi :10.1111/jsm.13022. PMID 26559385.
- ^ ab Bach PV, Najari BB, Kashanian JA (2016). "Tratamiento complementario del hipogonadismo masculino". Current Sexual Health Reports . 8 (4): 231–239. doi :10.1007/s11930-016-0089-7. ISSN 1548-3584. S2CID 79220716.
- ^ abcdefghi Trost LW, Khera M (julio de 2014). "Modalidades de tratamiento alternativas para el paciente hipogonadal". Current Urology Reports . 15 (7): 417. doi :10.1007/s11934-014-0417-2. PMID 24817260. S2CID 20304701.
- ^ DiGiorgio L, Sadeghi-Nejad H (diciembre de 2016). "Terapias fuera de etiqueta para el reemplazo de testosterona". Andrología y Urología Traslacional . 5 (6): 844–849. doi : 10.21037/tau.2016.08.15 . PMC 5182219 . PMID 28078215.
- ^ Helo S, Mahon J, Ellen J, Wiehle R, Fontenot G, Hsu K, et al. (enero de 2017). "Niveles séricos de enclomifeno y zuclomifeno en hombres con hipogonadismo en tratamiento a largo plazo con citrato de clomifeno". BJU International . 119 (1): 171–176. doi :10.1111/bju.13625. PMID 27511863. S2CID 5538782.
- ^ Becker KL (2001). Principios y práctica de endocrinología y metabolismo. Lippincott Williams & Wilkins. pp. 1206–. ISBN 978-0-7817-1750-2.
- ^ Agrawal S, Ganie MA, Nisar S (2017). "Ginecomastia". Fundamentos de la andrología humana . Springer. págs. 451–458. doi :10.1007/978-981-10-3695-8_26. ISBN . 978-981-10-3694-1.
- ^ Nordt CA, DiVasta AD (agosto de 2008). "Ginecomastia en adolescentes". Current Opinion in Pediatrics . 20 (4): 375–82. doi :10.1097/MOP.0b013e328306a07c. PMID 18622190. S2CID 205834072.
- ^ Miller GD, Moore C, Nair V, Hill B, Willick SE, Rogol AD, et al. (marzo de 2019). "Efectos del eje hipotálamo-hipofisario-testicular y detección urinaria tras la administración de clomifeno en varones". Revista de endocrinología clínica y metabolismo . 104 (3): 906–914. doi : 10.1210/jc.2018-01159 . PMID 30295816.
- ^ "Perfil de la sustancia: lo que los atletas deben saber sobre el clomifeno". USADA . 2 de febrero de 2017.
- ^ "¿Son las aves de corral y los huevos una fuente de cantidades minúsculas de clomifeno en las muestras de control de dopaje?". Agencia Mundial Antidopaje .
- ^ Cameron R, Feuer G, de la Iglesia F (6 de diciembre de 2012). Hepatotoxicidad inducida por fármacos. Springer Science & Business Media. pp. 565–. ISBN 978-3-642-61013-4.
- ^ Trabert B, Lamb EJ, Scoccia B, Moghissi KS, Westhoff CL, Niwa S, et al. (diciembre de 2013). "Fármacos inductores de la ovulación y riesgo de cáncer de ovario: resultados de un seguimiento prolongado de una gran cohorte de infertilidad de los Estados Unidos". Fertilidad y esterilidad . 100 (6): 1660–6. doi :10.1016/j.fertnstert.2013.08.008. PMC 3873340 . PMID 24011610.
- ^ Gadducci A, Guerrieri ME, Genazzani AR (enero de 2013). "Uso de fármacos para la fertilidad y riesgo de tumores ováricos: un desafío clínico debatido". Endocrinología ginecológica . 29 (1): 30–5. doi :10.3109/09513590.2012.705382. PMID 22946709. S2CID 1240526.
- ^ Yu Q, Lv X, Liu K, Ma D, Wu Y, Dai W, et al. (2018). "Medicamentos para la fertilidad asociados con el riesgo de cáncer de tiroides: una revisión sistemática y un metanálisis". BioMed Research International . 2018 : 7191704. doi : 10.1155/2018/7191704 . PMC 5971354. PMID 29862285 .
- ^ ab "ClomiFENO (Consejos profesionales para pacientes)". Drugs.com . Consultado el 30 de julio de 2019 .
- ^ abc Goldstein SR, Siddhanti S, Ciaccia AV, Plouffe L (2000). "Una revisión farmacológica de moduladores selectivos del receptor de estrógeno". Human Reproduction Update . 6 (3): 212–24. doi : 10.1093/humupd/6.3.212 . PMID 10874566.
- ^ ab Haskell SG (mayo de 2003). "Moduladores selectivos del receptor de estrógeno". Southern Medical Journal . 96 (5): 469–76. doi :10.1097/01.SMJ.0000051146.93190.4A. PMID 12911186. S2CID 40607634.
- ^ Duarte FH, Jallad RS, Bronstein MD (noviembre de 2016). "Estrógenos y moduladores selectivos del receptor de estrógeno en la acromegalia". Endocrine . 54 (2): 306–314. doi :10.1007/s12020-016-1118-z. PMID 27704479. S2CID 10136018.
- ^ Runnebaum B, Rabe T (17 de abril de 2013). Gynäkologische Endokrinologie und Fortpflanzungsmedizin: Banda 1: Gynäkologische Endokrinologie. Springer-Verlag. págs.88–. ISBN 978-3-662-07635-4.
- ^ ab Roche V, Zito WS, Lemke T, Williams DA (29 de julio de 2019). Principios de química medicinal de Foye. Wolters Kluwer Health. pp. 3010–. ISBN 978-1-4963-8587-1.
- ^ abcd Obach RS (abril de 2013). "Metabolitos farmacológicamente activos: impacto en el descubrimiento de fármacos y la farmacoterapia". Pharmacological Reviews . 65 (2): 578–640. doi :10.1124/pr.111.005439. PMID 23406671. S2CID 720243.
- ^ Wittliff JL, Kerr II DA, Andres SA (2005). "Estrógenos IV: fármacos similares a los estrógenos". En Wexler P (ed.). Enciclopedia de toxicología, 2.ª edición . Vol. Dib–L. Elsevier. págs. 254–258. ISBN 9780080548005.
- ^ Blair RM, Fang H, Branham WS, Hass BS, Dial SL, Moland CL, et al. (marzo de 2000). "Las afinidades de unión relativas al receptor de estrógeno de 188 sustancias naturales y xenoquímicas: diversidad estructural de ligandos". Toxicological Sciences . 54 (1): 138–53. doi : 10.1093/toxsci/54.1.138 . PMID 10746941.
- ^ Fang H, Tong W, Shi LM, Blair R, Perkins R, Branham W, et al. (marzo de 2001). "Relaciones estructura-actividad para un conjunto amplio y diverso de estrógenos naturales, sintéticos y ambientales". Chemical Research in Toxicology . 14 (3): 280–94. doi :10.1021/tx000208y. PMID 11258977.
- ^ ab Baumann RJ, Bush TL, Cross-Doersen DE, Cashman EA, Wright PS, Zwolshen JH, et al. (marzo de 1998). "Análogos de clomifeno con actividad in vitro e in vivo contra células de cáncer de mama humano". Farmacología bioquímica . 55 (6): 841–51. doi :10.1016/s0006-2952(97)00574-1. PMID 9586957.
- ^ Sutherland RL, Watts CK, Ruenitz PC (octubre de 1986). "Definición de dos mecanismos de acción distintos de los antiestrógenos sobre la proliferación de células de cáncer de mama humano utilizando hidroxitrifeniletilenos con alta afinidad por el receptor de estrógeno". Biochemical and Biophysical Research Communications . 140 (2): 523–9. doi :10.1016/0006-291x(86)90763-1. PMID 3778464.
- ^ ab Rambhatla A, Mills JN, Rajfer J (2016). "El papel de los moduladores de estrógeno en el hipogonadismo y la infertilidad masculinos". Reviews in Urology . 18 (2): 66–72. doi :10.3909/riu0711 (inactivo el 12 de septiembre de 2024). PMC 5010627 . PMID 27601965.
{{cite journal}}: CS1 maint: DOI inactivo a partir de septiembre de 2024 ( enlace ) - ^ abc Zhang X (16 de octubre de 2018). Receptor de estrógeno y cáncer de mama: celebración del 60.° aniversario del descubrimiento del receptor de estrógeno. Springer. pp. 153–. ISBN 978-3-319-99350-8.
- ^ abc Maximov PY, McDaniel RD, Jordan VC (23 de julio de 2013). Tamoxifeno: medicina pionera en el cáncer de mama. Springer Science & Business Media. pp. 34–. ISBN 978-3-0348-0664-0.
- ^ ab Harper MJ (21 de diciembre de 2013). "Control farmacológico de la reproducción en la mujer". En Jucker E (ed.). Progreso en la investigación de medicamentos / Fortschritte der Arzneimittelforschung / Progrès des recherches pharmaceutiques . Birkhäuser. págs.69–. ISBN 978-3-0348-7065-8.
- ^ Hormonas y cáncer de mama. Elsevier. 25 de junio de 2013. pp. 13–. ISBN 978-0-12-416676-9.
- ^ Perfiles analíticos de sustancias farmacológicas y excipientes. Academic Press. 20 de marzo de 1998. pp. 113–. ISBN 978-0-08-086120-3Archivado desde el original el 5 de noviembre de 2017.
- ^ Rostami-Hodjegan A, Lennard MS, Tucker GT, Ledger WL (mayo de 2004). "Monitoreo de las concentraciones plasmáticas para individualizar el tratamiento con citrato de clomifeno". Fertilidad y esterilidad . 81 (5): 1187–1193. doi : 10.1016/j.fertnstert.2003.07.044 . PMID 15136073.
- ^ US 2,914,563, Allen RE, Palopoli FP, Schumann EL, Van Campen Jr MG, "Composición terapéutica", expedida el 24 de noviembre de 1959, asignada a William S Merrill Company
- ^ ab Jensen EV, Jordan VC (junio de 2003). "El receptor de estrógeno: un modelo para la medicina molecular". Clin. Cancer Res . 9 (6): 1980–9. PMID 12796359.
- ^ Howell A, Jordan VC (2013). "Terapia antihormonal adyuvante". En Craig JV (ed.). Acción de los estrógenos, moduladores selectivos de los receptores de estrógenos y salud de la mujer: progreso y promesa . World Scientific. págs. 229–254. doi :10.1142/9781848169586_0010. ISBN . 978-1-84816-959-3.
- ^ Howell A, Jordan VC (2013). "Terapia antihormonal adyuvante". En Craig JV (ed.). Acción de los estrógenos, moduladores selectivos de los receptores de estrógenos y salud de la mujer: progreso y promesa. World Scientific. págs. 229–254. doi :10.1142/9781848169586_0010. ISBN 978-1-84816-959-3.
- ^ Holtkamp DE, Greslin JG, Root CA, Lerner LJ (octubre de 1960). "Inhibición de la gonadotropina y efectos antifecundidad del cloramifeno". Actas de la Sociedad de Biología y Medicina Experimental . 105 : 197–201. doi :10.3181/00379727-105-26054. PMID 13715563. S2CID 1448466.
- ^ Hughes E, Collins J, Vandekerckhove P (2000). "Citrato de clomifeno para la inducción de la ovulación en mujeres con oligoamenorrea". Base de datos Cochrane de revisiones sistemáticas (2): CD000056. doi :10.1002/14651858.CD000056. PMID 10796477.(Retractado, véase doi :10.1002/14651858.cd000056.pub2)
- ^ Adashi EY (otoño de 2014). "Iatrogenic Birth Plurality: The Challenge and Its Possible Solution" (PDF) . Harvard Health Policy Review . 14 (1): 9–10. Archivado desde el original (PDF) el 6 de octubre de 2016 . Consultado el 12 de septiembre de 2016 .
- ^ ab Lee P (18 de julio de 1989). "Dow Chemical obtendrá el control de Marion Labs: un acuerdo de más de 5.000 millones de dólares es un esfuerzo por diversificar". Los Angeles Times . Archivado desde el original el 29 de junio de 2016.
- ^ Williams W (11 de febrero de 1981). "Dow amplía sus líneas de productos". The New York Times . ISSN 0362-4331. Archivado desde el original el 6 de octubre de 2016.
- ^ "Hoechst AG comprará Marion Merrell Dow / Adquisición por valor de más de 7.000 millones de dólares". San Francisco Chronicle . Reuters. 5 de mayo de 1995. Archivado desde el original el 6 de octubre de 2016.
- ^ Arturo Bris y Christos Cabolis, Corporate Governance Convergence Through Cross-Border Mergers The Case of Aventis Archivado el 21 de abril de 2014 en Wayback Machine , Capítulo 4 en Corporate Governance and Regulatory Impact on Mergers and Acquisitions: Research and Analysis on Activity Worldwide Since 1990. Eds Greg N. Gregoriou, Luc Renneboog. Academic Press, 26 de julio de 2007
- ^ Timmons H, Bennhold K (27 de abril de 2004). "Francia ayudó a negociar el acuerdo Aventis-Sanofi". The New York Times . Archivado desde el original el 5 de noviembre de 2017.
- ^ Strauss JF, Barbieri RL (13 de septiembre de 2013). Yen and Jaffe's Reproductive Endocrinology. Elsevier Health Sciences. pp. 518–. ISBN 978-1-4557-2758-2Archivado desde el original el 5 de noviembre de 2017.
- ^ Lista de sustancias prohibidas de la AMA de 2016 (incluida como clomifeno) Archivado el 6 de marzo de 2016 en Wayback Machine.
- ^ Palacios S (marzo de 2007). "El futuro de los nuevos moduladores selectivos del receptor de estrógeno". Menopause International . 13 (1): 27–34. doi :10.1258/175404507780456791. PMID 17448265. S2CID 29053109.
- ^ Maximov PY, Lee TM, Jordan VC (mayo de 2013). "El descubrimiento y desarrollo de moduladores selectivos de los receptores de estrógeno (SERM) para la práctica clínica". Farmacología clínica actual . 8 (2): 135–55. doi :10.2174/1574884711308020006. PMC 3624793 . PMID 23062036.
- ^ Hormonas y cáncer de mama. Elsevier. 25 de junio de 2013. pp. 13–. ISBN 978-0-12-416676-9Archivado desde el original el 5 de noviembre de 2017.
- ^ Maximov PY, McDaniel RE, Jordan VC (2013). "El tamoxifeno avanza solo". Tamoxifen . Hitos en la farmacoterapia. Springer. págs. 31–46. doi :10.1007/978-3-0348-0664-0_2. ISBN 978-3-0348-0663-3. ISSN 2296-6064.
