Aféresis
| Aféresis | |
|---|---|
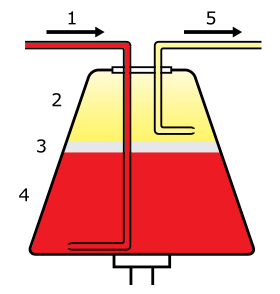 La sangre entera entra en la centrífuga (1) y se separa en plasma (2), leucocitos (3) y eritrocitos (4). A continuación, se extraen los componentes seleccionados (5). | |
| Malla | D016238 |
La aféresis (ἀφαίρεσις ( aphairesis , "quitar")) es una técnica médica en la que la sangre de una persona pasa por un aparato que separa un componente en particular y devuelve el resto a la circulación. Se trata, por tanto, de una terapia extracorpórea .
Uno de los usos de la aféresis es la recolección de células madre hematopoyéticas . [1]
Método
En función de la sustancia que se vaya a eliminar, en la aféresis se emplean distintos procesos. Si se requiere la separación por densidad , la centrifugación es el método más común. Otros métodos implican la absorción en perlas recubiertas con un material absorbente [2] y la filtración. [3]
El método de centrifugación se puede dividir en dos categorías básicas: [4]
Centrifugación de flujo continuo
Históricamente, la centrifugación de flujo continuo (CFC) requería dos venopunciones , ya que "continua" significa que la sangre se recolecta, se centrifuga y se devuelve simultáneamente. Los sistemas más nuevos pueden utilizar una sola venopunción al acumular sangre en un vaso y realizar un ciclo de extracción y devolución de sangre a través de la aguja mientras la centrífuga procesa continuamente la sangre restante en el vaso. [5] La principal ventaja de este sistema es el bajo volumen extracorpóreo (calculado por el volumen de la cámara de aféresis, el hematocrito del donante y el volumen total de sangre del donante) utilizado en el procedimiento, lo que puede ser ventajoso en ancianos y niños. [ cita requerida ]
Centrifugación de flujo intermitente
La centrifugación de flujo intermitente (IFC) funciona en ciclos: se extrae sangre, se centrifuga/procesa y luego se devuelven las partes no utilizadas al donante en un bolo . La principal ventaja es que se realiza en un solo sitio de venopunción. Requiere un mayor volumen extracorpóreo y lleva mucho más tiempo realizar el procedimiento mediante IFC. Por lo tanto, es menos probable que se utilice por razones terapéuticas y se observa a menudo en los centros de donación. [6] Para evitar que la sangre se coagule , se mezcla automáticamente un anticoagulante con la sangre a medida que se bombea desde el cuerpo hacia la máquina de aféresis. [7]
Variables de centrifugación
El proceso de centrifugación en sí tiene cuatro variables que se pueden controlar para eliminar selectivamente los componentes deseados. La primera es la velocidad de centrifugación y el diámetro del recipiente, la segunda es el "tiempo de reposo" en la centrífuga, la tercera son los solutos añadidos y la cuarta no es tan fácil de controlar: el volumen de plasma y el contenido celular del donante. El resultado en la mayoría de los casos es la clásica muestra de sangre sedimentada con los glóbulos rojos en la parte inferior, la capa leucocítica de plaquetas y glóbulos blancos ( linfocitos , granulocitos , monocitos ) en el medio y el plasma en la parte superior. [8]
Tipos

Existen numerosos tipos de aféresis.
Donación
La sangre extraída de un donante sano se puede separar en sus componentes durante la donación de sangre , donde se recolecta el componente necesario y los componentes no recolectados se devuelven al donante. Por lo general, no es necesario reponer líquidos en este tipo de recolección. En muchos países, los donantes de aféresis pueden donar plaquetas con mayor frecuencia que los que donan sangre completa. Existen varias categorías de recolección de componentes:
- Plasmaféresis : plasma sanguíneo . La plasmaféresis es útil para recolectar plasma fresco congelado (FFP) de un grupo ABO en particular. Los usos comerciales de este procedimiento, además del FFP, incluyen productos de inmunoglobulina, derivados del plasma y recolección de anticuerpos raros de glóbulos blancos y rojos.

- Eritrocitoféresis : glóbulos rojos . La eritrocitoféresis es la separación de los eritrocitos de la sangre entera. Se realiza más comúnmente mediante el método de sedimentación centrífuga. El procedimiento automatizado de recolección de glóbulos rojos para la donación de eritrocitos se conoce como "doble rojo" o "doble aféresis de glóbulos rojos". [9]
- Plaquetaféresis (trombaféresis, trombocitaféresis): plaquetas sanguíneas . La plaquetaféresis es la recolección de plaquetas por aféresis, mientras se recuperan los glóbulos rojos, los glóbulos blancos y el plasma componente. El rendimiento normalmente es el equivalente a entre seis y diez concentrados de plaquetas al azar. El control de calidad exige que las plaquetas de la aféresis sean iguales o mayores a 3,0 × 10 11 en número y tengan un pH igual o mayor a 6,2 en el 90% de los productos probados y deben usarse dentro de los cinco días.
- Leucoféresis : leucocitos (glóbulos blancos). La leucoféresis es la extracción de PMN , basófilos y eosinófilos para transfusión a pacientes cuyos PMN son ineficaces o en los que la terapia tradicional ha fallado. Hay datos limitados que sugieren el beneficio de la transfusión de granulocitos . Las complicaciones de este procedimiento son la dificultad en la recolección y la corta vida útil (24 horas a 20 a 24 °C). Dado que la capa de "capa leucocítica" se encuentra directamente sobre la capa de glóbulos rojos, se utiliza HES, un agente sedimentador, para mejorar el rendimiento y minimizar la recolección de glóbulos rojos. El control de calidad exige que el concentrado resultante sea de 1,0 × 10 10 granulocitos en el 75 % de las unidades analizadas y que el producto se irradie para evitar la enfermedad de injerto contra huésped (linfocitos inactivos). La irradiación no afecta la función de los PMN. Dado que generalmente se recolecta una pequeña cantidad de glóbulos rojos, se debe emplear la compatibilidad ABO cuando sea posible. [10]
- Recolección de células madre: células madre hematopoyéticas . Las células madre de sangre periférica circulantes (PBSC) se recolectan para su uso en el trasplante de células madre periféricas después de la administración de un agente movilizador, como el factor estimulante de colonias de granulocitos (G-CSF).
- Linfaféresis: linfocitos . Los linfocitos se recolectan para su uso en la fabricación de productos de células T CAR para inmunoterapias basadas en células T. [11]
Seguridad del donante
- Kits de un solo uso: la aféresis se realiza con kits de un solo uso, por lo que no existe riesgo de infección por tubos o centrífugas contaminados con sangre. La sangre no entra en contacto con el dispositivo y, durante la separación, la sangre no sale del kit. [12]
- Reinfusión – Al final del procedimiento, la sangre restante en el kit se devuelve al donante con un proceso llamado “reinfusión”.
- Efectos sobre el sistema inmunológico: “Las disminuciones inmediatas en el recuento de linfocitos en sangre y las concentraciones de inmunoglobulina sérica son de grado leve a moderado y no tienen efectos adversos conocidos. Hay menos información disponible sobre las alteraciones a largo plazo del sistema inmunológico”. [13]
Problemas con el kit
Los dos kits de aféresis retirados del mercado fueron:
- Baxter Healthcare Corporation (2005), en el que "se observaron fugas de pequeños orificios en el extremo de dos omega del ombligo (tubo multilumen), lo que provocó una fuga de sangre". [14]
- Fenwal Incorporated (2007), en el que hubo "dos casos en los que las líneas de anticoagulante citrato dextrosa (ACD) y solución salina se invirtieron en el proceso de ensamblaje. Las conexiones de las líneas invertidas pueden no ser visualmente evidentes en la caja del monitor y podrían resultar en una infusión excesiva de ACD y lesiones graves, incluida la muerte, al donante". [15]
Selección de donantes
Pueden ser donantes de aféresis las personas que no utilicen un fármaco que pueda impedir la donación de sangre, que no tengan el riesgo de ser portadores de una enfermedad y que tengan una estructura vascular adecuada. Para la donación de plaquetas por aféresis, el recuento de plaquetas previo del donante debe ser superior a 150 x 10^9/L. Para la donación de plasma por aféresis, el nivel de proteínas totales del donante debe ser superior a 60 g/L. Para la aféresis doble de glóbulos rojos, los donantes de ambos sexos requieren un nivel mínimo de hemoglobina de 14,0 g/dl. [16]
Exposición al plastificante
La aféresis utiliza plásticos y tubos que entran en contacto con la sangre. Los plásticos están hechos de PVC además de aditivos como un plastificante , a menudo DEHP . El DEHP se filtra del plástico a la sangre, y se han comenzado a estudiar los posibles efectos de este DEHP filtrado en los donantes, así como en los receptores de transfusiones. [17]
- "Los valores límite de riesgo o preventivos actuales para el DEHP, como la dosis de referencia de la EPA de EE. UU. (20 μg/kg/día) y la dosis diaria recomendada de la Unión Europea (20–48 μg/kg/día), pueden superarse el día de la plaquetoféresis... En particular, es necesario proteger a las mujeres en edad reproductiva de las exposiciones al DEHP que superen los valores límite preventivos mencionados anteriormente". [18]
- "Los productos desechables comerciales para plaquetasféresis liberan cantidades considerables de DEHP durante el procedimiento de aféresis, pero la dosis total de DEHP retenida por el donante está dentro del rango normal de exposición al DEHP de la población general". [19]
- La empresa Baxter fabricó bolsas de sangre sin DEHP , pero hubo poca demanda del producto en el mercado.
- "Las dosis medias de DEHP para ambas técnicas de plaquetoféresis (18,1 y 32,3 μg/kg/día) fueron cercanas o superiores a la dosis de referencia (DDR) de la EPA de EE. UU. y al valor de la ingesta diaria tolerable (IDT) de la UE el día de la aféresis. Por lo tanto, los márgenes de seguridad podrían ser insuficientes para proteger especialmente a los hombres y mujeres jóvenes en edad reproductiva de los efectos sobre la reproductividad. En la actualidad, se deberían preferir los dispositivos de flujo discontinuo para evitar posibles riesgos para la salud de los donantes de plaquetoféresis. Es necesario desarrollar estrategias para evitar la exposición de los donantes al DEHP durante la aféresis". [20]
Terapia

Las distintas técnicas de aféresis pueden emplearse siempre que el componente eliminado esté provocando síntomas graves de la enfermedad. Por lo general, la aféresis debe realizarse con bastante frecuencia y es un proceso invasivo. Por lo tanto, solo se emplea si otros medios para controlar una enfermedad en particular han fallado o si los síntomas son de tal naturaleza que esperar a que la medicación surta efecto causaría sufrimiento o riesgo de complicaciones. En el caso de las enfermedades autoinmunes en las que la aféresis es eficaz, no se utiliza como tratamiento independiente, sino más bien en combinación con terapias que reducen la producción de autoanticuerpos.
- Recambio de plasma : extracción de la parte líquida de la sangre para eliminar sustancias nocivas. El plasma se reemplaza por una solución de reemplazo.
- Aféresis de LDL : eliminación de lipoproteínas de baja densidad en pacientes con hipercolesterolemia familiar .
- Aféresis de lipoproteína(a) (Lp(a) [21]
- Fotoféresis : se utiliza para tratar la enfermedad de injerto contra huésped , el linfoma cutáneo de células T y el rechazo en el trasplante de corazón .
- Inmunoadsorción con columna de agarosa y proteína A de Staphylococcus aureus: eliminación de aloanticuerpos y autoanticuerpos (en enfermedades autoinmunes, rechazo de trasplantes, hemofilia) mediante la conducción del plasma a través de columnas de agarosa y proteína A. La proteína A es un componente de la pared celular producido por varias cepas de Staphylococcus aureus que se une a la región Fc de la IgG.
- Leucocitaféresis : eliminación de glóbulos blancos malignos en personas con leucemia y recuentos muy elevados de glóbulos blancos que causan síntomas.
- Eritrocitoféresis : extracción de eritrocitos (glóbulos rojos) en personas con sobrecarga de hierro como resultado de hemocromatosis hereditaria . Este proceso también se utiliza para la exanguinotransfusión en casos graves de malaria o en pacientes con anemia falciforme con indicaciones específicas, como síndrome torácico agudo o accidente cerebrovascular.
- Trombocitaféresis : extracción de plaquetas en personas con síntomas de elevaciones extremas en el recuento de plaquetas, como aquellas con trombocitemia esencial o policitemia vera .
Indicaciones

Categorías de ASFA
En 2023, [22] la Sociedad Estadounidense de Aféresis publicó la novena edición especial de las pautas basadas en evidencia para la práctica de la medicina de aféresis. Estas pautas se basan en una revisión sistemática de la literatura científica disponible. La utilidad clínica para una enfermedad determinada se denota mediante la asignación de una categoría ASFA (I – IV). La calidad y la solidez de la evidencia se denotan mediante recomendaciones GRADE estándar . Las categorías ASFA se definen de la siguiente manera:
- Categoría I para trastornos en los que la aféresis terapéutica se acepta como tratamiento de primera línea,
- Categoría II para trastornos en los que la aféresis terapéutica se acepta como tratamiento de segunda línea,
- Categoría III para trastornos en los que no está claramente establecido el papel óptimo de la aféresis terapéutica y
- Categoría IV para trastornos en los que la aféresis terapéutica se considera ineficaz o perjudicial.
Enfermedades y trastornos
Sólo las enfermedades (o las condiciones especiales mencionadas en ellas) con categoría I o II de ASFA se muestran en negrita , y además la categoría I aparece subrayada .
Reposición de líquidos durante la aféresis
Cuando se utiliza un sistema de aféresis para la terapia, el sistema elimina cantidades relativamente pequeñas de líquido (no más de 10,5 ml/kg de peso corporal). Ese líquido debe reemplazarse para mantener el volumen intravascular correcto. El líquido reemplazado es diferente en diferentes instituciones. Si se utiliza un cristaloide como la solución salina normal (NS), la cantidad de infusión debe ser el triple de lo que se elimina, ya que se necesita la proporción 3:1 de solución salina normal por plasma para mantener la presión oncótica . Algunas instituciones utilizan albúmina sérica humana , pero es costosa y puede ser difícil de encontrar. El uso rutinario de plasma fresco congelado (PFC) no suele ser apropiado debido a los peligros que conlleva, incluida la toxicidad del citrato (del anticoagulante), la incompatibilidad ABO , la infección y las reacciones alérgicas. Sin embargo, el PFC debe utilizarse en casos de púrpura trombocitopénica trombótica o en pacientes con alto riesgo de sangrado.
Véase también
Referencias
- ^ Katherine, Abel (2013). Guía oficial de estudio para la certificación CPC . Asociación Médica Estadounidense. pág. 128.
- ^ Fuchs K, Rummler S, Ries W, Helmschrott M, Selbach J, Ernst F, Morath C, Gauly A, Atiye S, Stauss-Grabo M, Giefer M. Rendimiento, eficacia clínica y seguridad de la inmunoadsorción en una amplia gama de indicaciones. Ther Apher Dial. Febrero de 2022;26(1):229-241. doi: 10.1111/1744-9987.13663. Publicación electrónica 6 de mayo de 2021. PMID: 33914397; PMCID: PMC9291474
- ^ Hirano R, Namazuda K, Hirata N. Plasmaféresis de doble filtración: revisión de las aplicaciones clínicas actuales. Ther Apher Dial. 2021 Abr;25(2):145-151. doi: 10.1111/1744-9987.13548. Publicación electrónica 6 de agosto de 2020. PMID: 32558286.
- ^ Lambert C, Gericke M, Smith R, Hermans C. Tasa de extracción de plasma y eficiencia de recolección durante el intercambio de plasma terapéutico con Spectra Optia en comparación con Haemonetics MCS+. J Clin Apher. 2011;26(1):17-22. doi: 10.1002/jca.20271. Publicación electrónica 17 de noviembre de 2010. PMID: 21312255.
- ^ Patente estadounidense 7108672, "Métodos y aparatos de procesamiento de sangre extracorpóreos"
- ^ "Aféresis" . Consultado el 24 de octubre de 2022 .
- ^ Vurro F, Merolle L, Marraccini C, Parisi M, Canovi L, Erta B, Santachiara A, Bonvicini L, Giorgi Rossi P, Baricchi R, Pertinhez TA. Evaluación cuantitativa del anticoagulante en unidades de plasma recogidas por plasmaféresis. Transfusión. Junio de 2019;59(6):2113-2120. doi: 10.1111/trf.15244. Publicación electrónica del 15 de marzo de 2019. PMID: 30875439.
- ^ Vrielink H, Neyrinck MM. Fundamentos de aféresis y equipamiento. Transfus Apher Sci. 2023 Abr;62(2):103671. doi: 10.1016/j.transci.2023.103671. Publicación electrónica 24 de febrero de 2023. PMID: 36870905.
- ^ dtm doble glóbulo rojo Archivado el 5 de julio de 2007 en Wayback Machine .
- ^ Lodermeier MA, Byrne KM, Flegel WA. Sedimentación de glóbulos rojos de granulocitos por aféresis. Transfusión. Octubre de 2017;57(10):2551-2552. doi: 10.1111/trf.14251. Publicación electrónica 16 de agosto de 2017. PMID: 28815621; PMCID: PMC5656404.
- ^ Yamanaka, I., Yamauchi, T., Henzan, T. et al. Optimización de la linfaféresis para la fabricación de células CAR-T autólogas. Int J Hematol 114, 449–458 (2021). https://doi.org/10.1007/s12185-021-03191-x
- ^ Vrielink H, Neyrinck MM. Fundamentos de aféresis y equipamiento. Transfus Apher Sci. 2023 Abr;62(2):103671. doi: 10.1016/j.transci.2023.103671. Publicación electrónica 24 de febrero de 2023. PMID: 36870905.
- ^ Strauss, Ronald G. (1984). "Seguridad del donante mediante aféresis: cambios en la inmunidad humoral y celular". Journal of Clinical Apheresis . 2 (1): 68–80. doi :10.1002/jca.2920020112. PMID 6536660. S2CID 25890912.
- ^ "Retirada de kits de aféresis Amicus de Baxter Healthcare Corporation". Administración de Alimentos y Medicamentos . Archivado desde el original el 17 de enero de 2009. Consultado el 20 de diciembre de 2008 ."Retirada del mercado de kits de aféresis Amicus de Baxter Healthcare Corporation", FDA de EE. UU., 31 de enero de 2005
- ^ "Retirada del mercado de los kits de aféresis CS3000". Administración de Alimentos y Medicamentos . 21 de junio de 2007.
- ^ Boulton F. La regla del 13%. Comentarios. Transfusion Today, 2007, 71:7–9.
- ^ Larsson L, Sandgren P, Ohlsson S, Derving J, Friis-Christensen T, Daggert F, Frizi N, Reichenberg S, Chatellier S, Diedrich B, Antovic J, Larsson S, Uhlin M. El plastificante sin ftalato DEHT preserva la calidad adecuada de los componentes sanguíneos durante el almacenamiento en bolsas de sangre de PVC. Vox Sang. Enero de 2021;116(1):60-70. doi: 10.1111/vox.12982. Publicación electrónica 12 de septiembre de 2020. PMID: 32918773.
- ^ Koch, Holger M.; Bolt, Hermann M.; Preuss, Ralf; Eckstein, Reinhold; Weisbach, Volker; Angerer, Jürgen (2005). "Exposición intravenosa a di(2-etilhexil)ftalato (DEHP): metabolitos de DEHP en orina después de una donación voluntaria de plaquetas". Archivos de toxicología . 79 (12): 689–93. doi :10.1007/s00204-005-0004-x. PMID 16059725. S2CID 743051.
- ^ Buchta, Christoph; Bittner, Claudia; Hocker, Paul; Macher, María; Schmid, Rainer; Seger, Christoph; Dettke, Markus (2003). "Exposición del donante al plastificante di (2-etilhexil) ftalato durante la plaquetoféresis". Transfusión . 43 (8): 1115–20. doi :10.1046/j.1537-2995.2003.00479.x. PMID 12869118. S2CID 34539126.
- ^ Koch, Holger M.; Angerer, Jürgen; Drexler, Hans; Eckstein, Reinhold; Weisbach, Volker (2005). "Exposición de donantes voluntarios de plasma y plaquetas al di(2-etilhexil)ftalato (DEHP)". Revista Internacional de Higiene y Salud Ambiental . 208 (6): 489–98. doi :10.1016/j.ijheh.2005.07.001. PMID 16325559.
- ^ "Lipoproteína (a)". Oficina de Ciencias (OS) de los CDC , Oficina de Genómica y Salud Pública de Precisión . Departamento de Salud y Servicios Humanos de EE. UU . . 5 de julio de 2022. Consultado el 14 de septiembre de 2022 .
- ^ Connelly-Smith, Laura; Alquist, Caroline; Aqui, Nicole; Hofmann, Jan; Klingel, Reinhard; et al. (2023). "Directrices sobre el uso de la aféresis terapéutica en la práctica clínica: enfoque basado en la evidencia del Comité de redacción de la Sociedad Estadounidense de Aféresis: Noveno número especial". The Journal of Clinical Apheresis . 38 (2): 77–278. doi :10.1002/jca.22043. PMID 37017433.
Enlaces externos
- NIH
- Sociedad Americana de Aféresis
- Página de aféresis de WebPath.
- Donación y procesamiento de sangre en WebPath
- Donación de plaquetas por aféresis: datos y preguntas frecuentes
{{ }}