1,1,1,2-Tetrafluoroetano
| |||
| Nombres | |||
|---|---|---|---|
| Nombre IUPAC preferido 1,1,1,2-Tetrafluoroetano | |||
| Otros nombres HFA-134a HFC-134a R-134a Norflurano | |||
| Identificadores | |||
Modelo 3D ( JSmol ) |
| ||
| Química biológica |
| ||
| Araña química | |||
| Banco de medicamentos |
| ||
| Tarjeta informativa de la ECHA | 100.011.252 | ||
| Número CE |
| ||
| BARRIL | |||
Identificador de centro de PubChem |
| ||
| Número RTECS |
| ||
| UNIVERSIDAD | |||
| Número de la ONU | 3159 | ||
Panel de control CompTox ( EPA ) |
| ||
| |||
| Propiedades | |||
| C2H2F4 | |||
| Masa molar | 102,032 g·mol −1 | ||
| Apariencia | Gas incoloro | ||
| Densidad | 0,00425 g/cm3 , gas | ||
| Punto de fusión | -103,3 °C (-153,9 °F; 169,8 K) | ||
| Punto de ebullición | -26,3 °C (-15,3 °F; 246,8 K) | ||
| 0,15 % en peso | |||
| Peligros | |||
| Seguridad y salud en el trabajo (SST/OHS): | |||
Principales peligros | Asfixiante | ||
| Etiquetado SGA : | |||
 | |||
| Advertencia | |||
| H280 | |||
| P410+P403 | |||
| NFPA 704 (rombo cortafuegos) | |||
| punto de inflamabilidad | 250 °C (482 °F; 523 K) | ||
| Compuestos relacionados | |||
Refrigerantes relacionados | Difluorometano Pentafluoroetano | ||
Compuestos relacionados | 1-Cloro-1,2,2,2-tetrafluoroetano 1,1,1-Tricloroetano | ||
| Página de datos complementarios | |||
| 1,1,1,2-Tetrafluoroetano (página de datos) | |||
Salvo que se indique lo contrario, los datos se proporcionan para los materiales en su estado estándar (a 25 °C [77 °F], 100 kPa). | |||
El 1,1,1,2-tetrafluoroetano (también conocido como norflurano ( DCI ), R-134a, Klea 134a , Freón 134a , Forane 134a , Genetron 134a , Green Gas , Florasol 134a , Suva 134a , HFA-134a o HFC-134a ) es un refrigerante de hidrofluorocarbono (HFC) y haloalcano con propiedades termodinámicas similares al R-12 (diclorodifluorometano) pero con un potencial insignificante de agotamiento de la capa de ozono y un potencial de calentamiento global a 100 años menor (1430, en comparación con el GWP del R-12 de 10 900). [1] Tiene la fórmula CF 3 CH 2 F y un punto de ebullición de −26,3 °C (−15,34 °F) a presión atmosférica. Los cilindros R-134a son de color azul claro . [2] En 2012, se inició en el mercado automotriz una eliminación gradual y una transición al HFO-1234yf y otros refrigerantes con potencial de calentamiento global similar al CO 2 . [3]
Usos
El 1,1,1,2-tetrafluoroetano es un gas no inflamable que se utiliza principalmente como refrigerante de "alta temperatura" para sistemas de refrigeración domésticos y aires acondicionados de automóviles . Estos dispositivos comenzaron a utilizar 1,1,1,2-tetrafluoroetano a principios de los años 90 como reemplazo del R-12 , que es más nocivo para el medio ambiente . Existen kits de actualización disponibles para convertir unidades que originalmente estaban equipadas con R-12.

Otros usos comunes incluyen el soplado de espuma plástica, como disolvente de limpieza, como propulsor para la administración de productos farmacéuticos (por ejemplo, botes de inhaladores como los de los broncodilatadores ), destapadores de corcho de vino, espolvoreadores de gas ("aire enlatado") y en secadores de aire para eliminar la humedad del aire comprimido . El 1,1,1,2-tetrafluoroetano también se ha utilizado para enfriar computadoras en algunos intentos de overclocking . Es el refrigerante utilizado en los kits de congelación de tuberías de plomería. También se utiliza comúnmente como propulsor para pistolas de aire comprimido Airsoft . El gas a menudo se mezcla con un lubricante a base de silicona.
Aplicaciones aspiracionales y de nicho
El 1,1,1,2-tetrafluoroetano también se considera un disolvente orgánico , tanto como líquido como fluido supercrítico . [4] [5] [6]
Se utiliza en los detectores de partículas de cámara de placa resistiva en el Gran Colisionador de Hadrones . [7] [8] También se utiliza para otros tipos de detectores de partículas, por ejemplo, algunos detectores de partículas criogénicas . [9] Se puede utilizar como una alternativa al hexafluoruro de azufre en la fundición de magnesio como gas protector . [10]
Historia e impactos ambientales
El 1,1,1,2-tetrafluoroetano se introdujo a principios de los años 1990 como sustituto del diclorodifluorometano (R-12) , que tiene enormes propiedades de agotamiento de la capa de ozono. [11] Aunque el 1,1,1,2-tetrafluoroetano tiene un potencial insignificante de agotamiento de la capa de ozono ( capa de ozono ) y un potencial de acidificación insignificante ( lluvia ácida ), tiene un potencial de calentamiento global (GWP) de 100 años de 1430 y una vida atmosférica aproximada de 14 años. [1] Su concentración en la atmósfera y su contribución al forzamiento radiativo han ido aumentando desde su introducción. Por ello, se incluyó en la lista del IPCC de gases de efecto invernadero . [12]
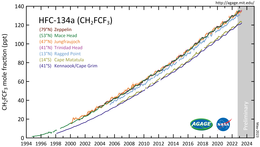

El R-134a comenzó a eliminarse gradualmente de su uso en la Unión Europea a partir de mediados de la década de 2010, mediante una directiva de 2006 que recomendaba la sustitución de gases en los sistemas de aire acondicionado con un PCA superior a 100. [13]
El 1,1,1,2-tetrafluoroetano está sujeto a restricciones de uso en los EE. UU. y otros países también. La Sociedad de Ingenieros Automotrices (SAE) ha propuesto que lo mejor sea reemplazarlo por un nuevo refrigerante fluoroquímico HFO-1234yf (CF 3 CF=CH 2 ) en los sistemas de aire acondicionado de los automóviles. [14] A partir del año modelo 2021, los vehículos ligeros de nueva fabricación en los Estados Unidos ya no utilizan R-134a. [3]
California también puede prohibir la venta de R-134a enlatado a particulares para evitar la recarga no profesional de los aparatos de aire acondicionado. [15] En Wisconsin había existido una prohibición desde octubre de 1994 en virtud de la ATCP 136 que prohibía las ventas de envases de menos de 15 libras de 1,1,1,2-tetrafluoroetano, pero esta restricción se aplicaba únicamente cuando el producto químico estaba destinado a ser un refrigerante. Sin embargo, la prohibición se levantó en Wisconsin en 2012. [16] Durante el tiempo en que estuvo vigente, esta prohibición específica de Wisconsin contenía lagunas. Por ejemplo, era legal que una persona comprara envases de gas para limpiar el polvo con cualquier cantidad del producto químico porque en ese caso el producto químico no está destinado a ser un refrigerante [16] ni el HFC-134a está incluido en la lista de sustancias de clase I y clase II del § 7671a. [17]
Producción y reacciones
El tetrafluoroetano se obtiene generalmente mediante la reacción del tricloroetileno con fluoruro de hidrógeno : [18]
- CHCl=CCl2 + 4HF → CF3CH2F + 3HCl
Reacciona con butillitio para dar trifluorovinil litio: [19]
- CF3CH2F + 2BuLi → CF2 = CFLi + LiF +2BuH
Seguridad

Las mezclas con aire del gas 1,1,1,2-tetrafluoroetano no son inflamables a presión atmosférica y temperaturas de hasta 100 °C (212 °F). Sin embargo, las mezclas con altas concentraciones de aire a presión y/o temperatura elevadas pueden encenderse . [20] El contacto del 1,1,1,2-tetrafluoroetano con llamas o superficies calientes a más de 250 °C (482 °F) puede causar descomposición del vapor y la emisión de gases tóxicos , incluidos fluoruro de hidrógeno y fluoruro de carbonilo , [21] sin embargo, se ha informado que la temperatura de descomposición es superior a 370 °C. [22] El propio 1,1,1,2-tetrafluoroetano tiene una LD 50 de 1500 g/m 3 en ratas, lo que lo hace relativamente no tóxico, aparte de los peligros inherentes al abuso de inhalantes . Su forma gaseosa es más densa que el aire y desplazará el aire en los pulmones. Esto puede provocar asfixia si se inhala en exceso. [23] [24] Esto contribuye a la mayoría de las muertes por abuso de inhalantes .
Las latas de aerosol que contienen 1,1,1,2-tetrafluoroetano, al invertirlas, se convierten en aerosoles congelantes eficaces. Bajo presión, el 1,1,1,2-tetrafluoroetano se comprime hasta convertirse en un líquido que, al vaporizarse, absorbe una cantidad significativa de energía térmica . Como resultado, reducirá en gran medida la temperatura de cualquier objeto con el que entre en contacto al evaporarse.
.jpg/440px-Freon_134a_refrigerant_for_car_AC_001_(cropped).jpg)
Uso médico
Por sus usos médicos, el 1,1,1,2-tetrafluoroetano tiene el nombre genérico de norflurano. Se utiliza como propulsor para algunos inhaladores de dosis medida . [25] Se considera seguro para este uso. [26] [27] [28] En combinación con pentafluoropropano , se utiliza como un aerosol tópico de enfriamiento para adormecer los furúnculos antes del legrado . [29] [30] También se ha estudiado como un posible anestésico por inhalación , [31] pero no es anestésico en las dosis utilizadas en inhaladores. [26]
Véase también
Referencias
- ^ ab "Tabla 2.14 (Fe de erratas). Duración de la vida, eficiencia radiativa y PCG directos (excepto para el CH4) en relación con el CO2". Archivado desde el original el 6 de julio de 2017 . Consultado el 11 de julio de 2017 .
- ^ "Imagen de ejemplo de una botella de R134a de 30 libras". budgetheating.com . Consultado el 26 de marzo de 2018 .
- ^ ab "Transición de refrigerantes e impactos ambientales". Agencia de Protección Ambiental de Estados Unidos. 6 de agosto de 2015. Consultado el 1 de octubre de 2020 .
- ^ Corr, Stuart (2005). "1,1,1,2-Tetrafluoroetano (R-134a): Un disolvente selectivo para la generación de ingredientes de aromas y fragancias". Sabores y fragancias naturales . Serie de simposios de la ACS. Vol. 908. pág. 41. doi :10.1021/bk-2005-0908.ch003. ISBN . 0-8412-3904-5.
- ^ Abbott, Andrew P.; Eltringham, Wayne; Hope, Eric G.; Nicola, Mazin (2005). "Solubilidad de ácidos carboxílicos insaturados en 1,1,1,2-tetrafluoroetano supercrítico (HFC 134a) y una metodología para la separación de mezclas ternarias". Química verde . 7 (4): 210. doi :10.1039/B412697A.
- ^ Abbott, Andrew P.; Eltringham, Wayne; Hope, Eric G.; Nicola, Mazin (2005). "Hidrogenación en 1,1,1,2 tetrafluoroetano supercrítico (HFC 134a)" (PDF) . Química verde . 7 (10): 721. doi :10.1039/B507554H. hdl : 2381/604 . Archivado desde el original (PDF) el 19 de julio de 2018 . Consultado el 18 de septiembre de 2019 .
- ^ Anushree Ghosh ESTUDIO DE CÁMARAS DE PLACAS RESISTIVAS DE VIDRIO (RPC) Y CÁLCULO DE EFICIENCIA Archivado el 7 de agosto de 2011 en Wayback Machine . Programa de capacitación de posgrado INO DHEP, TIFR, Mumbai.
- ^ M. Capeans, I. Glushkov, R. Guida, F. Hahn, S. Haider (CERN, Suiza) Operación de RPC en los experimentos del LHC en un sistema de gas de circuito cerrado optimizado. Medical Imaging Conference. 25–31 de octubre de 2009.
- ^ Norbeck, E.; Olson, JE; Moeller, A.; Onel, Y. (2006). "Rad Hard Active Media For Calorimeters" (PDF) . Actas de la conferencia AIP . 867 : 84. Bibcode :2006AIPC..867...84N. doi :10.1063/1.2396941. Archivado desde el original (PDF) el 23 de marzo de 2012.
- ^ Reciclaje de magnesio en Estados Unidos en 1998. (PDF). USGS. Consultado el 21 de agosto de 2011.
- ^ Franklin J (1993). "La degradación atmosférica y el impacto del 1,1,1,2-tetrafluoroetano (hidrofluorocarbono 134a)". Chemosphere . 27 (8): 1565–1601. Código Bibliográfico :1993Chmsp..27.1565F. doi :10.1016/0045-6535(93)90251-Y.
- ^ Forster, P.; et al. (2007). "Cambios en los componentes atmosféricos y en el forzamiento radiativo". (PDF) . Cambio climático 2007: la base científica física. Contribución del Grupo de trabajo I al Cuarto informe de evaluación del Grupo Intergubernamental de Expertos sobre el Cambio Climático . Archivado (PDF) desde el original el 24 de julio de 2010.
- ^ Directiva 2006/40/CE del Parlamento Europeo y del Consejo, de 17 de mayo de 2006, relativa a las emisiones procedentes de los sistemas de aire acondicionado de los vehículos de motor y por la que se modifica la Directiva 70/156/CEE del Consejo
- ^ HFO-1234yf Un refrigerante de bajo GWP para MAC Archivado el 27 de febrero de 2009 en Wayback Machine . Refrigerants.dupont.com (17 de agosto de 2011). Consultado el 21 de agosto de 2011.
- ^ California restringe el uso de HFC-134a en automóviles. 27 de junio de 2007. R744.com. Consultado el 21 de agosto de 2011.
- ^ ab Capítulo ATCP 136. ACONDICIONADORES DE AIRE MÓVILES; RECUPERACIÓN O RECICLAJE DE REFRIGERANTE. State.wi.us. (PDF). Consultado el 21 de agosto de 2011.
- ^ Sustancias que agotan la capa de ozono de clase I. EPA.gov. Consultado el 21 de agosto de 2011.
- ^ "Solvay en América del Norte | Solvay" (PDF) .
- ^ Burdon, James; Coe, Paul L.; Haslock, Iain B.; Powell, Richard L. (1996). "El hidrofluorocarbono 1,1,1,2-tetrafluoroetano (HFC-134a) como fuente de trifluorovinil-litio". Chemical Communications : 49. doi :10.1039/CC9960000049.
- ^ DuPont (2004). DuPont HFC-134a: propiedades, usos, almacenamiento y manipulación (PDF) (Informe). Archivado desde el original (PDF) el 4 de octubre de 2016 . Consultado el 5 de agosto de 2016 .
- ^ Honeywell Internacional (diciembre de 2005). "MSDS n.º GTRN-0047 para Genetron 134aUV".
- ^ "FICHA DE DATOS DE SEGURIDAD según Reglamento (UE) 2015/8301/7 Harp 134a" (PDF) . Consultado el 17 de noviembre de 2024 .
- ^ Alexander DJ; Libretto SE (1995). "Una visión general de la toxicología del HFA-134a (1,1,1,2-tetrafluoroetano)". Hum. Exp. Toxicol . 14 (9): 715–20. doi :10.1177/096032719501400903. PMID 8579881. S2CID 19669317.
- ^ GE Millward; E. Tschuikow-Roux (1972). "Análisis cinético de la descomposición por ondas de choque del 1,1,1,2-tetrafluoroetano". The Journal of Physical Chemistry . 76 (3): 292–298. doi :10.1021/j100647a002.
- ^ Sellers, William FS (2017). "Rendimiento del inhalador dosificador presurizado para el asma: estudios del efecto del propulsor en sistemas de administración". Allergy, Asthma & Clinical Immunology . 13 : 30. doi : 10.1186/s13223-017-0202-0 . PMC 5492461 . PMID 28670327.
- ^ ab Shah, S. B; Hariharan, U; Bhargava, A. K (2015). "Anestésico en la apariencia de un propelente". Indian Journal of Anaesthesia . 59 (4): 258–260. doi : 10.4103/0019-5049.155011 . PMC 4408662 . PMID 25937660.
Se ha demostrado que este propelente es seguro y no anestésico en dosis estándar para inhaladores.
- ^ Huchon, G; Hofbauer, P; Cannizzaro, G; Iacono, P; Wald, F (2000). "Comparación de la seguridad de la administración de fármacos a través de inhaladores de dosis medidas con HFA y CFC en CAO". The European Respiratory Journal . 15 (4): 663–9. doi : 10.1034/j.1399-3003.2000.15d07.x . PMID 10780756.
- ^ "1,1,1,2-Tetrafluoroetano". Administración de Seguridad y Salud Ocupacional . Archivado desde el original el 3 de febrero de 2018. Consultado el 3 de febrero de 2018 .
- ^ "Norflurano". DrugBank.
- ^ "Aerosol de norflurano-pentafluoropropano, pulverización". WebMD .
- ^ Shulman M, Sadove MS (1967). "1,1,1,2-tetrafluoroetano: un agente inhalatorio de potencia intermedia". Anestesia y analgesia . 46 (5): 629–635. doi : 10.1213/00000539-196709000-00029 . S2CID 5868484.
Enlaces externos
- Ficha internacional de seguridad química 1281
- Comité Técnico Europeo de Fluorocarbonos (EFCTC)
- Hojas de datos de seguridad de materiales en la Universidad de Oxford
- Documento de evaluación química internacional conciso n.º 11, en inchem.org
- Calculadora de presión y temperatura
- "La curva coexistente del refrigerante HFC 134a: algunos modelos de escala" (PDF) . Archivado desde el original (PDF) el 29 de septiembre de 2006 . Consultado el 11 de septiembre de 2007 .
- Refrigeración por ordenador bifásica con refrigerante R134a Archivado el 18 de junio de 2008 en Wayback Machine