Pseudorabia
| Herpesvirus alfa suidificado tipo 1 | |
|---|---|
| Clasificación de virus | |
| (sin clasificar): | Virus |
| Reino : | Duplodnaviria |
| Reino: | Virus de Heunggong |
| Filo: | Peploviricota |
| Clase: | Hervivircetes |
| Orden: | Virus del herpes |
| Familia: | Ortoherpesvirus |
| Género: | Varicelovirus |
| Especies: | Herpesvirus alfa suidificado tipo 1 |
| Sinónimos [1] | |
| |
La enfermedad de Aujeszky , generalmente llamada pseudorrabia en los Estados Unidos , es una enfermedad viral de los cerdos que es endémica en la mayor parte del mundo. Es causada por el herpesvirus suidiano 1 (SuHV-1). La enfermedad de Aujeszky se considera la enfermedad viral porcina de mayor importancia económica en las zonas donde se ha erradicado la peste porcina clásica ( cólera porcino ). [2] Otros mamíferos , como el ganado vacuno , las ovejas , las cabras , los gatos , los perros y los mapaches , también son susceptibles. La enfermedad suele ser mortal en estas especies animales.
La investigación sobre el SuHV-1 en cerdos ha sido pionera en el control de enfermedades animales con vacunas modificadas genéticamente. El SuHV-1 se utiliza ahora en estudios modelo de procesos básicos durante la infección por herpesvirus lítico y para desentrañar los mecanismos moleculares del neurotropismo del herpesvirus . [3] [4]
Historia
En 1902, un veterinario húngaro , Aladár Aujeszky , demostró la presencia de un nuevo agente infeccioso en un perro, un buey y un gato, y demostró que causaba la misma enfermedad en cerdos y conejos . En las décadas siguientes, la infección se encontró en varios países europeos, especialmente en el ganado, donde el prurito intenso local (picazón) es un síntoma característico. En los Estados Unidos, se concluyó que una enfermedad bien conocida en el ganado llamada "picor loco" era, de hecho, la enfermedad de Aujeszky. [5]
Descripción general de la enfermedad
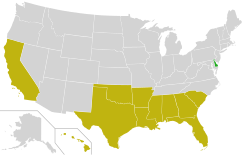
Presente
Ausente
El virus se excreta en la saliva y las secreciones nasales de los cerdos infectados por vía respiratoria. También puede producirse la aerosolización del virus y la transmisión por fómites . El virus puede sobrevivir potencialmente durante siete horas en aire húmedo y puede sobrevivir en agua de pozo hasta siete horas, en pasto verde, tierra y heces hasta dos días, en alimento contaminado hasta tres días y en lechos de paja hasta cuatro días. [6]
El diagnóstico se realiza principalmente mediante el aislamiento del virus en cultivos de tejidos o mediante pruebas ELISA o PCR. Existen vacunas disponibles para cerdos ( códigos ATCvet : QI09AA01 ( OMS ) inactivada, QI09AD01 ( OMS ) viva, más varias combinaciones). [7] La infección ha sido erradicada en varios países europeos. En los Estados Unidos, la población porcina doméstica en 2004 fue declarada libre de la enfermedad de Aujeszky, aunque la infección aún persiste en las poblaciones de cerdos salvajes. [8]
Signos clínicos
La infección respiratoria suele ser asintomática en cerdos de más de dos meses de edad, pero puede causar abortos, alta mortalidad en lechones y tos, estornudos, fiebre, estreñimiento, depresión, convulsiones, ataxia , movimientos circulares y exceso de salivación en lechones y cerdos adultos. La mortalidad en lechones de menos de un mes de edad es cercana al 100%, pero es inferior al 10% en cerdos de entre uno y seis meses de edad. Las cerdas preñadas pueden reabsorber sus camadas o dar a luz lechones momificados, nacidos muertos o debilitados. [9] En el ganado, los síntomas incluyen picor intenso seguido de signos neurológicos y muerte. En los perros, los síntomas incluyen picor intenso, parálisis de mandíbula y faringe , aullidos y muerte. [2] Cualquier huésped secundario infectado generalmente solo vive de dos a tres días. [6]
La infección genital parece haber sido común durante gran parte del siglo XX en muchos países europeos en explotaciones porcinas, donde se utilizaban verracos de centros de cría para la monta natural de cerdas o nulíparas. Esta manifestación de la enfermedad siempre ha sido asintomática en los cerdos afectados, y la presencia de la infección en una explotación se ha detectado únicamente debido a casos en bovinos que presentaban prurito en los cuartos traseros. [10]
En los animales susceptibles distintos de los cerdos, la infección suele ser mortal y los animales afectados suelen presentar un prurito intenso en una zona de la piel. El prurito en la enfermedad de Aujeszky se considera una sensación fantasma, ya que nunca se ha encontrado el virus en el lugar del prurito. [11]
Patogenicidad y virulencia del SuHV-1
Esta sección necesita citas adicionales para su verificación . ( Enero de 2021 ) |
La epidemiología de la enfermedad de Aujeszky varía según la patogenicidad o virulencia de la cepa del virus en cuestión. Esto se ilustra mejor con el desarrollo de la gravedad de la enfermedad en Dinamarca, donde la importación de cerdos estuvo prohibida durante décadas hasta 1972. Antes de 1964 sólo se propagaban cepas genitales, pero luego aparecieron cepas respiratorias, que posteriormente se propagaron rápidamente por todo el país, principalmente mediante el comercio de animales. A finales de la década de 1970 se desarrollaron cepas más virulentas. La enfermedad en los cerdos se volvió mucho más grave, los brotes de enfermedad respiratoria en el ganado aumentaron drásticamente y la infección se propagó por vía aérea a otras piaras de cerdos. La mayor virulencia de estas cepas del virus se asoció con una cierta capacidad para crear sincitios (fusión celular) en cultivos de tejidos (cepas del virus sincitial). Los análisis exhaustivos de patrones de fragmentos de restricción del ADN del virus han documentado que las cepas más virulentas no habían sido introducidas desde el extranjero, sino que se habían desarrollado en dos etapas a partir de las cepas danesas originales. La correlación entre la alta virulencia de las cepas del virus y la formación de sincitios en cultivos de tejidos fue confirmada por los exámenes de aislamientos de otros países. Este segundo paso en la evolución de la gravedad de la enfermedad en Dinamarca motivó la decisión de erradicarla. Los nuevos brotes después de la erradicación de la infección autóctona a finales de 1985 fueron causados por cepas sincitiales extranjeras altamente virulentas introducidas por transmisión aérea desde Alemania. [11]
En resumen, el SuHV-1 se transmite por vía genital o respiratoria. Se ha descubierto que las cepas genitales no son sincitiales. Las cepas respiratorias pueden tener una virulencia relativamente baja o alta. En Europa, se ha descubierto que las cepas sincitiales son muy virulentas.
Epidemiología
Las poblaciones de jabalíes o cerdos salvajes ( Sus scrofa ) en los EE. UU. suelen contraer y propagar el virus en toda su área de distribución. La mortalidad es mayor en los lechones jóvenes. Las cerdas preñadas a menudo abortan cuando se infectan. Los adultos machos (verracos) por lo demás sanos suelen ser portadores latentes, es decir, albergan y transmiten el virus sin mostrar síntomas ni experimentar discapacidad. [12]
Los cerdos (tanto domésticos como salvajes) son reservorios habituales de este virus, aunque afecta a otras especies. La enfermedad de Aujeszky se ha descrito en otros mamíferos, incluidos osos pardos y negros , panteras de Florida , mapaches , coyotes y venados de cola blanca. En la mayoría de los casos, se conocía o sospechaba que había contacto con cerdos o productos derivados del cerdo. Los brotes en especies de peletería de granja en Europa ( visones y zorros ) se han asociado con la alimentación con productos derivados del cerdo contaminados. Muchas otras especies pueden infectarse experimentalmente. Los humanos no son huéspedes potenciales. [13]
Se ha descubierto que el ganado bovino se infecta por vía respiratoria o vaginal ( no se tienen en cuenta los casos iatrogénicos ). La infección primaria de las membranas mucosas del tracto respiratorio superior se asocia con prurito en la cabeza, mientras que la infección pulmonar produce prurito en el pecho. Se ha descubierto que la infección vaginal de los bovinos, que regularmente presentan prurito en los cuartos traseros, está asociada con una infección genital concurrente en los cerdos en las mismas instalaciones, y las investigaciones han demostrado que la infección vaginal del ganado bovino había sido transmitida sexualmente por el hombre a partir de cerdas infectadas. [ cita requerida ] La infección genital en las piaras de cerdos se ha correlacionado estrechamente con el uso de verracos de centros de verracos para el servicio natural de las cerdas. [ 11 ]
Transmisión
La enfermedad de Aujeszky es muy contagiosa. Se considera que la infección se transmite entre cerdos por contacto nariz con nariz, ya que el virus se encuentra principalmente en las zonas nasal y oral. Sin embargo, esta idea se contradice con los resultados de estudios epidemiológicos, según los cuales la propagación decisiva dentro de las manadas se produce por corrientes de aire a lo largo de muchos metros. En consecuencia, se ha descubierto que el riesgo de transmisión aérea de cepas de virus altamente virulentas desde manadas con infección aguda a otras manadas de cerdos es muy alto. Se ha descubierto que la infección se transmite a distancias de muchos kilómetros. [11] De lo contrario, la infección se transmite con mayor frecuencia a las manadas por la introducción de cerdos con infección aguda o latente. En cuanto a la transmisión al ganado, véase la sección anterior.
Prevención
Aunque no existe un tratamiento específico para la infección aguda por SuHV-1, la vacunación puede aliviar los signos clínicos en cerdos de ciertas edades. Por lo general, se recomienda la vacunación masiva de todos los cerdos de la granja con una vacuna de virus vivo modificado. La vacunación intranasal de las cerdas y los lechones neonatos de uno a siete días de edad, seguida de la vacunación intramuscular (IM) de todos los demás cerdos de las instalaciones, ayuda a reducir la diseminación viral y mejora la supervivencia. El virus vivo modificado se replica en el sitio de la inyección y en los ganglios linfáticos regionales. El virus de la vacuna se disemina en niveles tan bajos que la transmisión mucosa a otros animales es mínima. En las vacunas con genes eliminados, también se ha eliminado el gen de la timidina quinasa; por lo tanto, el virus no puede infectar y replicarse en las neuronas. Se recomienda vacunar a los rebaños de cría trimestralmente y a los cerdos de engorde después de que disminuyan los niveles de anticuerpos maternos. La vacunación regular da como resultado un excelente control de la enfermedad. Se recomienda la terapia con antibióticos concurrente a través del alimento y la inyección IM para controlar los patógenos bacterianos secundarios. [14]
Aplicaciones en neurociencia
El SuHV-1 se puede utilizar para analizar circuitos neuronales en el sistema nervioso central (SNC). Para este propósito, se utiliza comúnmente la cepa atenuada (menos virulenta) SuHV-1 Bartha [15] y se emplea como un trazador transneuronal retrógrado [16] y anterógrado [17] . En la dirección retrógrada, SuHV-1-Bartha se transporta a un cuerpo celular neuronal a través de su axón, donde se replica y se dispersa por todo el citoplasma y el árbol dendrítico. El SuHV-1-Bartha liberado en la sinapsis puede cruzar la sinapsis para infectar las terminales axónicas de las neuronas conectadas sinápticamente, propagando así el virus; sin embargo, no se sabe en qué medida también puede ocurrir el transporte transneuronal no sináptico. Mediante estudios temporales y/o cepas modificadas genéticamente de SuHV-1-Bartha, se pueden identificar neuronas de segundo, tercer y orden superior en la red neuronal de interés.
Véase también
Referencias
- ^ "Historia de la taxonomía del ICTV: Suid alphaherpesvirus 1". Comité Internacional de Taxonomía de Virus (ICTV) . Consultado el 9 de enero de 2019 .
- ^ ab Fenner, Frank J.; Gibbs, E. Paul J.; Murphy, Frederick A.; Rott, Rudolph; Studdert, Michael J.; White, David O. (1993). Virología veterinaria (2.ª ed.) . Academic Press, Inc. ISBN 978-0-12-253056-2.
- ^ Mettenleiter (2008). "Biología molecular de los herpesvirus animales". Virus animales: biología molecular . Caister Academic Press. ISBN 978-1-904455-22-6.
- ^ Sandri-Goldin, RM, ed. (2006). Herpesvirus alfa: biología molecular y celular. Caister Academic Press. ISBN 978-1-904455-09-7.
- ^ Pomeranz L, Reynolds A, Hengartner C (2005). "Biología molecular del virus de la pseudorrabia: impacto en la neurovirología y la medicina veterinaria". Microbiol Mol Biol Rev . 69 (3): 462–500. doi :10.1128/MMBR.69.3.462-500.2005. PMC 1197806 . PMID 16148307.
- ^ ab "Pseudorabia: Introducción". Manual veterinario de Merck . 2006. Consultado el 31 de marzo de 2007 .
- ^ Pensaert M, Labarque G, Favoreel H, Nauwynck H (2004). "Vacunación contra la enfermedad de Aujeszky y diferenciación de cerdos vacunados e infectados". Dev Biol (Basilea) . 119 : 243–54. PMID 15742635.
- ^ Amass, SF (2006). "Enfermedades exóticas: ¿está preparado? ¿Está listo?". Actas de la Conferencia Veterinaria de América del Norte . Consultado el 31 de marzo de 2007 .
- ^ Carter, GR; Flores, EF; Wise, DJ (2006). "Herpesviridae" . Una revisión concisa de virología veterinaria . Consultado el 4 de junio de 2006 .
- ^ Bitsch, Viggo (2015). Principales características epidemiológicas de la enfermedad de Aujeszky en cerdos y ganado vacuno . ISBN 978-87-994685-1-5 .
- ^ abcd Bitsch, Viggo (2015)
- ^ Instituto Berryman: Manejo de cerdos salvajes Archivado el 5 de septiembre de 2011 en Wayback Machine.
- ^ Autoridad de Seguridad Alimentaria de Finlandia Evira: Aujeszkyn tauti (AD, pseudorabia) Archivado el 17 de julio de 2011 en Wayback Machine. (en finlandés)
- ^ "Manual Veterinario de Merck".
- ^ Barta A (1961). "Reducción experimental de la virulencia del virus de la enfermedad de Aujesky". Magyar Allatorvosok Lapja . 16 : 42–45.
- ^ Koyuncu OO, Perlman DH, Enquist LW (16 de enero de 2013). "El transporte retrógrado eficiente del virus de la pseudorrabia dentro de las neuronas requiere la síntesis local de proteínas en los axones". Cell Host Microbe . 13 (1): 54–66. doi :10.1016/j.chom.2012.10.021. PMC 3552305 . PMID 23332155.
- ^ Kratchmarov R, Taylor MP, Enquist LW (2013). "El papel de la fosforilación de us9 en la clasificación axonal y el transporte anterógrado del virus de la pseudorrabia". PLOS ONE . 8 (3): e58776. Bibcode :2013PLoSO...858776K. doi : 10.1371/journal.pone.0058776 . PMC 3602541 . PMID 23527020.
Enlaces externos
- Panorama del virus y sus aplicaciones en la neurociencia
- Virus animales


