Octreotida
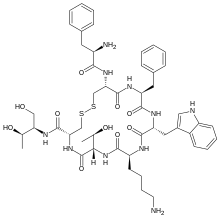 | |
 Estructura 3D del octreótido. PDB : 6VC1 | |
| Datos clínicos | |
|---|---|
| Nombres comerciales | Sandostatin, Bynfezia Pen, Mycapssa, otros |
| AHFS / Drogas.com | Monografía |
| MedlinePlus | a693049 |
| Datos de licencia |
|
Categoría de embarazo |
|
| Vías de administración | Subcutánea , intramuscular , intravenosa , por vía oral. |
| Código ATC |
|
| Estatus legal | |
| Estatus legal | |
| Datos farmacocinéticos | |
| Biodisponibilidad | 60% ( IM ), 100% ( SC ) |
| Unión de proteínas | 40–65% |
| Metabolismo | Hígado |
| Vida media de eliminación | 1,7–1,9 horas |
| Excreción | Orina (32%) |
| Identificadores | |
| |
| Número CAS |
|
| Identificador de centro de PubChem |
|
| Unión Internacional para la Investigación y el Desarrollo (IUPHAR)/BPS |
|
| Banco de medicamentos | |
| Araña química | |
| UNIVERSIDAD |
|
| BARRIL | |
| EBICh |
|
| Química biológica | |
| Panel de control CompTox ( EPA ) |
|
| Datos químicos y físicos | |
| Fórmula | C49H66N10O10S2 |
| Masa molar | 1 019 .25 g·mol −1 |
| Modelo 3D ( JSmol ) |
|
| |
| |
 norte norte Y (¿que es esto?) (verificar) Y (¿que es esto?) (verificar) | |
Octreotide , que se comercializa bajo la marca Sandostatin , entre otras, es un octapéptido que imita farmacológicamente a la somatostatina natural , aunque es un inhibidor más potente de la hormona del crecimiento , el glucagón y la insulina que la hormona natural. Se sintetizó por primera vez en 1979 y se une predominantemente a los receptores de somatostatina SSTR2 y SSTR5 . [5]
Fue aprobado para su uso en los Estados Unidos en 1988. [2] [1] La octreotida fue aprobada para uso médico en la Unión Europea en 2022. [4] A junio de 2020 [actualizar], la octreotida es el primer análogo oral de la somatostatina (SSA) aprobado por la FDA. [6] Está en la Lista de Medicamentos Esenciales de la Organización Mundial de la Salud . [7]
Usos médicos
Tumores
La octreotida se utiliza para el tratamiento de tumores productores de hormona de crecimiento ( acromegalia y gigantismo ), cuando la cirugía está contraindicada, tumores hipofisarios que secretan hormona estimulante de la tiroides (tirotropinoma), [ cita requerida ] diarrea y episodios de sofocos asociados con el síndrome carcinoide , y diarrea en personas con tumores secretores de péptidos intestinales vasoactivos ( VIPomas ). La octreotida también se utiliza en casos leves de glucagonoma cuando la cirugía no es una opción. [8] [9]
Varices esofágicas sangrantes
La octreótida se administra a menudo como infusión para el tratamiento de la hemorragia aguda de las várices esofágicas en la cirrosis hepática , sobre la base de que reduce la presión venosa portal , aunque la evidencia actual sugiere que este efecto es transitorio y no mejora la supervivencia. [10]
Marcaje radioactivo
La octreótida se utiliza en imágenes de medicina nuclear mediante el marcado con indio-111 (Octreoscan) para obtener imágenes no invasivas de tumores neuroendocrinos y otros tumores que expresan receptores de somatostatina. [11] Se ha marcado radiactivamente con carbono-11 [12] así como con galio-68 (usando edotreotida ), lo que permite obtener imágenes con tomografía por emisión de positrones (PET).
Acromegalia
En junio de 2020, el octreotida (Mycapssa) fue aprobado para uso médico en los Estados Unidos con una indicación para el tratamiento de mantenimiento a largo plazo en pacientes con acromegalia que han respondido y tolerado el tratamiento con octreotida o lanreotida . [13] [6] Mycapssa es el primer análogo de somatostatina oral (SSA) aprobado por la FDA. [6]
Hipoglucemia
La octreótida también se utiliza en el tratamiento de la hipoglucemia refractaria o el hiperinsulinismo congénito en neonatos [14] y la hipoglucemia inducida por sulfonilureas en adultos.
Contraindicaciones
La octreotida no se ha estudiado adecuadamente para el tratamiento de niños, mujeres embarazadas y lactantes. El medicamento se administra a estos grupos sólo si el análisis de riesgo-beneficio es positivo. [15] [16]
Efectos adversos
Los efectos adversos más comunes son dolor de cabeza, hipotiroidismo , cambios en la conducción cardíaca , reacciones gastrointestinales (incluyendo calambres, náuseas/vómitos y diarrea o estreñimiento), cálculos biliares , reducción de la liberación de insulina , hiperglucemia [17] o algunas veces hipoglucemia y reacciones en el lugar de la inyección (generalmente transitorias). La frecuencia cardíaca lenta , las reacciones cutáneas como prurito , hiperbilirrubinemia , hipotiroidismo , mareos y disnea también son bastante comunes (más del 1%). Los efectos secundarios raros incluyen reacciones anafilácticas agudas , pancreatitis y hepatitis . [15] [16]
Algunos estudios informaron alopecia en aquellos que fueron tratados con octreotida. [18] Las ratas que fueron tratadas con octreotida experimentaron disfunción eréctil en un estudio de 1998. [19]
Se ha observado un intervalo QT prolongado, pero no se sabe con certeza si se trata de una reacción a la medicación o del resultado de una enfermedad existente. [15]
Interacciones
La octreótida puede reducir la reabsorción intestinal de ciclosporina , posiblemente haciendo necesario aumentar la dosis. [20] Las personas con diabetes mellitus podrían necesitar menos insulina o antidiabéticos orales cuando son tratadas con octreótida, ya que inhibe la secreción de glucagón con mayor fuerza y durante un período de tiempo más prolongado que la secreción de insulina. [15] La biodisponibilidad de la bromocriptina aumenta; [16] además de ser un antiparkinsoniano , la bromocriptina también se utiliza para el tratamiento de la acromegalia.
Farmacología
Dado que el octreótido se parece a la somatostatina en sus actividades fisiológicas, puede:
- inhibe la secreción de muchas hormonas, como la gastrina , la colecistoquinina , el glucagón , la hormona del crecimiento , la insulina , la secretina , el polipéptido pancreático , la TSH y el péptido intestinal vasoactivo .
- reducir la secreción de líquidos por el intestino y el páncreas ,
- reducir la motilidad gastrointestinal e inhibir la contracción de la vesícula biliar ,
- inhibir la acción de ciertas hormonas de la hipófisis anterior ,
- Provoca vasoconstricción en los vasos sanguíneos y
- reducir las presiones de los vasos portales en las varices sangrantes.
También se ha demostrado que produce efectos analgésicos , probablemente actuando como un agonista parcial del receptor opioide mu . [21] [22]
Farmacocinética
La octreotida se absorbe rápidamente y completamente después de la aplicación subcutánea . La concentración plasmática máxima se alcanza después de 30 minutos. La semivida de eliminación es de 100 minutos (1,7 horas) en promedio cuando se aplica por vía subcutánea; después de la inyección intravenosa , la sustancia se elimina en dos fases con semividas de 10 y 90 minutos, respectivamente. [15] [16]
Historia
El acetato de octreótido fue aprobado para su uso en los Estados Unidos en 1988. [1] [2]
En enero de 2020, se otorgó la aprobación del acetato de octreotida en los Estados Unidos a Sun Pharmaceutical bajo la marca Bynfezia Pen para el tratamiento de: [2] [23] [24]
- la reducción de la hormona del crecimiento y del factor de crecimiento similar a la insulina 1 (somatomedina C) en adultos con acromegalia que han tenido una respuesta inadecuada o que no pueden ser tratados con resección quirúrgica, irradiación de la hipófisis y mesilato de bromocriptina en dosis máximas toleradas
- Episodios graves de diarrea y sofocos asociados con tumores carcinoides metastásicos en adultos
- Diarrea acuosa profusa asociada con tumores de péptidos intestinales vasoactivos (VIPomas) en adultos
Sociedad y cultura
Estatus legal
En septiembre de 2022, el Comité de Medicamentos de Uso Humano de la Agencia Europea de Medicamentos adoptó un dictamen positivo, recomendando la concesión de una autorización de comercialización para el medicamento Mycapssa, destinado al tratamiento de adultos con acromegalia. [25] El solicitante de este medicamento es Amryt Pharmaceuticals DAC. [25] Mycapssa fue aprobado para uso médico en la Unión Europea en diciembre de 2022. [4] [26]
Investigación
El octreotida también se ha utilizado fuera de indicación para el tratamiento de la diarrea grave y refractaria por otras causas. Se utiliza en toxicología para el tratamiento de la hipoglucemia recurrente prolongada después de una sobredosis de sulfonilurea y posiblemente meglitinida . También se ha utilizado con distintos grados de éxito en lactantes con nesidioblastosis para ayudar a disminuir la hipersecreción de insulina. Varios ensayos clínicos han demostrado el efecto del octreotida como tratamiento agudo (agente abortivo) en la cefalea en racimos , donde se ha demostrado que la administración de octreotida subcutánea es eficaz en comparación con placebo. [27]
También se ha investigado la octreotida en personas con dolor por pancreatitis crónica . [28]
Se ha utilizado en el tratamiento de la obstrucción intestinal maligna. [29]
La octreotida puede utilizarse junto con midodrina para revertir parcialmente la vasodilatación periférica en el síndrome hepatorrenal . Al aumentar la resistencia vascular sistémica, estos medicamentos reducen la derivación y mejoran la perfusión renal, prolongando la supervivencia hasta el tratamiento definitivo con trasplante de hígado. [30] De manera similar, la octreotida puede utilizarse para tratar la hipotensión crónica refractaria . [31] [ ¿ Fuente médica poco confiable? ]
Si bien se ha demostrado un tratamiento exitoso en informes de casos, [32] [33] estudios más amplios no han logrado demostrar eficacia en el tratamiento del quilotórax . [34]
Un pequeño estudio ha demostrado [ ¿cuándo? ] que el octreotido puede ser eficaz en el tratamiento de la hipertensión intracraneal idiopática . [35] [¿ fuente médica poco confiable? ] [36]
Obesidad
La octreótida se ha utilizado experimentalmente para tratar la obesidad , en particular la obesidad causada por lesiones en los centros del hambre y la saciedad del hipotálamo , una región del cerebro central para la regulación de la ingesta de alimentos y el gasto de energía. [37] El circuito comienza con un área del hipotálamo, el núcleo arqueado , que tiene salidas al hipotálamo lateral (LH) y al hipotálamo ventromedial (VMH), los centros de alimentación y saciedad del cerebro, respectivamente. [38] [39] El hipotálamo ventromedial a veces se lesiona por el tratamiento en curso para la leucemia linfoblástica aguda o la cirugía o la radiación para tratar los tumores de la fosa craneal posterior . [37] Con el hipotálamo ventromedial deshabilitado y ya no responde a las señales de equilibrio energético periférico, "la actividad simpática eferente disminuye, lo que resulta en malestar y reducción del gasto energético, y la actividad vagal aumenta, lo que resulta en un aumento de la secreción de insulina y la adipogénesis ". [40] "La disfunción del VMH promueve la ingesta calórica excesiva y la disminución del gasto calórico, lo que lleva a un aumento de peso continuo e implacable. Los intentos de restricción calórica o farmacoterapia con agentes adrenérgicos o serotoninérgicos anteriormente han tenido poco o solo un breve éxito en el tratamiento de este síndrome". [37] En este contexto, el octreótido suprime la liberación excesiva de insulina y puede aumentar su acción, inhibiendo así el almacenamiento adiposo excesivo. En un pequeño ensayo clínico en dieciocho sujetos pediátricos con aumento de peso intratable después de la terapia para leucemia linfoblástica aguda o tumores cerebrales y otra evidencia de disfunción hipotalámica, el octreótido redujo el índice de masa corporal (IMC) y la respuesta a la insulina durante la prueba de tolerancia a la glucosa , al tiempo que aumentó la actividad física informada por los padres y la calidad de vida (CdV) en relación con el placebo . [37] En un ensayo separado controlado con placebo de adultos obesos sin lesiones hipotalámicas conocidas, los sujetos obesos que recibieron octreótido de acción prolongada perdieron peso y redujeron su IMC en comparación con los sujetos que recibieron placebo; El análisis post hoc sugirió mayores efectos en los participantes que recibieron la dosis más alta del medicamento y entre " sujetos caucásicos que tenían una secreción de insulina mayor que la mediana de la cohorte". "No hubo cambios estadísticamente significativos en las puntuaciones de calidad de vida, la grasa corporal, la concentración de leptina y el Inventario de Depresión de Beck "., o ingesta de macronutrientes", aunque los sujetos que tomaron octreotida tuvieron niveles de glucosa en sangre más altos después de una prueba de tolerancia a la glucosa que los que recibieron placebo. [41]
Referencias
- ^ abc "Sandostatin Lar Depot- octreotide acetato kit". DailyMed . 11 de abril de 2019. Archivado desde el original el 24 de marzo de 2021 . Consultado el 16 de febrero de 2020 .
- ^ abcd "Bynfezia Pen- inyección de acetato de octreotida". DailyMed . 19 de febrero de 2020. Archivado desde el original el 19 de septiembre de 2022 . Consultado el 19 de abril de 2021 .
- ^ "Mycapssa-cápsula de octreotida de liberación retardada". DailyMed . 21 de agosto de 2024 . Consultado el 30 de septiembre de 2024 .
- ^ abc «Mycapssa EPAR». Agencia Europea de Medicamentos . 14 de septiembre de 2022. Consultado el 24 de diciembre de 2022 .El texto se ha copiado de esta fuente, cuyos derechos de autor pertenecen a la Agencia Europea de Medicamentos. Se autoriza la reproducción siempre que se cite la fuente.
- ^ Hofland LJ, Lamberts SW (enero de 1996). "Receptores de somatostatina y enfermedad: papel de los subtipos de receptores". Baillière's Clinical Endocrinology and Metabolism . 10 (1): 163–176. doi :10.1016/s0950-351x(96)80362-4. hdl : 1765/60433 . PMID 8734455.
- ^ abc "Chiasma anuncia la aprobación por parte de la FDA de las cápsulas Mycapssa (octreótido), el primer y único análogo oral de la somatostatina". Chiasma (nota de prensa). 26 de junio de 2020. Archivado desde el original el 30 de junio de 2020 . Consultado el 30 de junio de 2020 .
- ^ Organización Mundial de la Salud (2023). Selección y uso de medicamentos esenciales 2023: anexo web A: Lista modelo de medicamentos esenciales de la Organización Mundial de la Salud: 23.ª lista (2023) . Ginebra: Organización Mundial de la Salud. hdl : 10665/371090 . OMS/MHP/HPS/EML/2023.02.
- ^ Monografía de octreótido
- ^ Moattari AR, Cho K, Vinik AI (1990). "Análogo de la somatostatina en el tratamiento de glucagonoma coexistente y pseudoquiste pancreático: disociación de respuestas". Cirugía . 108 (3): 581–7. PMID 2168587.
- ^ Gøtzsche PC, Hróbjartsson A (julio de 2008). "Análogos de la somatostatina para el sangrado agudo de las varices esofágicas". Base de Datos Cochrane de Revisiones Sistemáticas . 2008 (3): CD000193. doi :10.1002/14651858.CD000193.pub3. PMC 7043291. PMID 18677774 .
- ^ "Medscape: revisión de Octreoscan". Archivado desde el original el 12 de febrero de 2017. Consultado el 28 de octubre de 2010 .
- ^ Chin J, Vesnaver M, Bernard-Gauthier V, Saucke-Lacelle E, Wängler B, Wängler C, et al. (noviembre de 2013). "Etiquetado directo en un solo paso de residuos de cisteína en péptidos con triflato de [(11)C]metilo para la síntesis de radiofármacos PET". Aminoácidos . 45 (5): 1097–108. doi :10.1007/s00726-013-1562-5. PMID 23921782. S2CID 16848582.
- ^ "Cápsulas de octreotida: nuestra investigación". Chiasma . 24 de enero de 2020. Archivado desde el original el 2 de julio de 2020 . Consultado el 30 de junio de 2020 .
- ^ McMahon AW, Wharton GT, Thornton P, De Leon DD (enero de 2017). "Uso y seguridad de octreotida en lactantes con hiperinsulinismo". Farmacoepidemiología y seguridad de fármacos . 26 (1): 26–31. doi :10.1002/pds.4144. PMC 5286465 . PMID 27910218.
- ^ abcde Haberfeld H, ed. (2009). Austria-Codex (en alemán) (edición 2009/2010). Viena: Österreichischer Apothekerverlag. ISBN 978-3-85200-196-8.
- ^ abcd Dinnendahl V, Fricke U, eds. (2010). Perfil Arzneistoff (en alemán). vol. 8 (23 ed.). Eschborn, Alemania: Govi Pharmazeutischer Verlag. ISBN 978-3-7741-9846-3.
- ^ Hovind P, Simonsen L, Bülow J (marzo de 2010). "La disminución de la captación de glucosa en las piernas durante el ejercicio contribuye al efecto hiperglucémico del octreotido". Fisiología clínica e imágenes funcionales . 30 (2): 141–5. doi :10.1111/j.1475-097X.2009.00917.x. PMID 20132129. S2CID 5303108.
- ^ van der Lely AJ, de Herder WW, Lamberts SW (noviembre de 1997). "Una evaluación de riesgo-beneficio de la octreotida en el tratamiento de la acromegalia". Drug Safety . 17 (5): 317–24. doi :10.2165/00002018-199717050-00004. PMID 9391775. S2CID 25405834.
- ^ Kapicioglu S, Mollamehmetoglu M, Kutlu N, Can G, Ozgur GK (enero de 1998). "Inhibición de la erección del pene en ratas por un análogo de la somatostatina de acción prolongada, octreótido (SMS 201-995)". British Journal of Urology . 81 (1): 142–5. doi :10.1046/j.1464-410x.1998.00520.x. PMID 9467491.
- ^ Klopp T, ed. (2010). Arzneimittel-Interaktionen (en alemán) (edición 2010/2011). Arbeitsgemeinschaft für Pharmazeutische Information. ISBN 978-3-85200-207-1.
- ^ Maurer R, Gaehwiler BH, Buescher HH, Hill RC, Roemer D (agosto de 1982). "Propiedades antagonistas de opiáceos de un análogo octapeptídico de la somatostatina". Actas de la Academia Nacional de Ciencias de los Estados Unidos de América . 79 (15): 4815–7. Bibcode :1982PNAS...79.4815M. doi : 10.1073/pnas.79.15.4815 . PMC 346769 . PMID 6126877.
- ^ Allen MP, Blake JF, Bryce DK, Haggan ME, Liras S, McLean S, et al. (marzo de 2000). "Diseño, síntesis y evaluación biológica de derivados de 3-amino-3-fenilpropionamida como nuevos ligandos del receptor opioide mu". Bioorganic & Medicinal Chemistry Letters . 10 (6): 523–6. doi :10.1016/s0960-894x(00)00034-2. PMID 10741545.
- ^ "Carta de Bynfezia Pen" (PDF) . Administración de Alimentos y Medicamentos de Estados Unidos (FDA). 28 de enero de 2020. Archivado (PDF) del original el 17 de febrero de 2020. Consultado el 16 de febrero de 2020 .
 Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público .
Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público . - ^ "Paquete de aprobación de medicamentos: Bynfezia". Administración de Alimentos y Medicamentos de Estados Unidos (FDA) . 1 de junio de 2020. Archivado desde el original el 30 de marzo de 2021. Consultado el 18 de abril de 2021 .
- ^ ab «Mycapssa: pendiente de decisión de la CE». Agencia Europea de Medicamentos . 16 de septiembre de 2022. Archivado desde el original el 19 de septiembre de 2022. Consultado el 18 de septiembre de 2022 .El texto se ha copiado de esta fuente, cuyos derechos de autor pertenecen a la Agencia Europea de Medicamentos. Se autoriza la reproducción siempre que se cite la fuente.
- ^ "Información del producto Mycapssa". Registro de medicamentos de la Unión . Consultado el 3 de marzo de 2023 .
- ^ Matharu MS, Levy MJ, Meeran K, Goadsby PJ (octubre de 2004). "Octreotida subcutánea en cefalea en racimos: estudio cruzado, doble ciego, aleatorizado y controlado con placebo". Anales de neurología . 56 (4): 488–94. doi :10.1002/ana.20210. PMID 15455406. S2CID 23879669.
- ^ Uhl W, Anghelacopoulos SE, Friess H, Büchler MW (1999). "El papel de la octreotida y la somatostatina en la pancreatitis aguda y crónica". Digestión . 60 (2): 23–31. doi :10.1159/000051477. PMID 10207228. S2CID 24011709.
- ^ Shima Y, Ohtsu A, Shirao K, Sasaki Y (mayo de 2008). "Eficacia clínica y seguridad de la octreotida (SMS201-995) en pacientes japoneses con cáncer terminal y obstrucción intestinal maligna". Revista japonesa de oncología clínica . 38 (5): 354–9. doi : 10.1093/jjco/hyn035 . PMID 18490369.
- ^ Skagen C, Einstein M, Lucey MR, Said A (agosto de 2009). "El tratamiento combinado con octreotida, midodrina y albúmina mejora la supervivencia en pacientes con síndrome hepatorrenal tipo 1 y tipo 2". Journal of Clinical Gastroenterology . 43 (7): 680–5. doi :10.1097/MCG.0b013e318188947c. PMID 19238094. S2CID 19747120.
- ^ Tidy C (febrero de 2013). Cox J (ed.). "Hipotensión". Patient.info . Archivado desde el original el 28 de agosto de 2021. Consultado el 26 de junio de 2015 .
- ^ Kilic D, Sahin E, Gulcan O, Bolat B, Turkoz R, Hatipoglu A (2005). "Octreotida para el tratamiento del quilotórax después de una cirugía cardíaca". Revista del Instituto del Corazón de Texas . 32 (3): 437–9. PMC 1336729 . PMID 16392238.
- ^ Siu SL, Lam DS (2006). "Quilotórax neonatal espontáneo tratado con octreotida". Revista de Pediatría y Salud Infantil . 42 (1–2): 65–7. doi :10.1111/j.1440-1754.2006.00788.x. PMID 16487393. S2CID 24561126.
- ^ Chan EH, Russell JL, Williams WG, Van Arsdell GS, Coles JG, McCrindle BW (noviembre de 2005). "Quilotórax posoperatorio después de cirugía cardiotorácica en niños". Anales de Cirugía Torácica . 80 (5): 1864–70. doi :10.1016/j.athoracsur.2005.04.048. PMID 16242470.
- ^ "Intracranial Hypertension Research Foundation". ihrfoundation.org . 17 de mayo de 2011. Archivado desde el original el 19 de diciembre de 2010 . Consultado el 30 de septiembre de 2024 .
- ^ Panagopoulos GN, Deftereos SN, Tagaris GA, Gryllia M, Kounadi T, Karamani O, et al. (julio de 2007). "Octreotida: una opción terapéutica para la hipertensión intracraneal idiopática". Neurología, neurofisiología y neurociencia : 1. PMID 17700925.
{{cite journal}}: Mantenimiento de CS1: configuración anulada ( enlace ) - ^ abcd Lustig RH, Hinds PS, Ringwald-Smith K, Christensen RK, Kaste SC, Schreiber RE, et al. (junio de 2003). "Terapia con octreotida para la obesidad hipotalámica pediátrica: un ensayo doble ciego controlado con placebo". The Journal of Clinical Endocrinology and Metabolism . 88 (6): 2586–92. doi : 10.1210/jc.2002-030003 . PMID 12788859.
{{cite journal}}: Mantenimiento de CS1: configuración anulada ( enlace ) - ^ Flier JS (enero de 2004). "Guerras de la obesidad: el progreso molecular confronta una epidemia en expansión". Cell . 116 (2): 337–50. doi : 10.1016/S0092-8674(03)01081-X . PMID 14744442.
- ^ Boulpaep EL, Boron WF (2003). Fisiología médica: un enfoque celular y molecular . Filadelfia: Saunders. p. 1227. ISBN 978-0-7216-3256-8.
- ^ Lustig RH (2011). "Obesidad hipotalámica después de craneofaringioma: mecanismos, diagnóstico y tratamiento". Frontiers in Endocrinology . 2 : 60. doi : 10.3389/fendo.2011.00060 . PMC 3356006 . PMID 22654817.
- ^ Lustig RH, Greenway F, Velasquez-Mieyer P, Heimburger D, Schumacher D, Smith D, et al. (febrero de 2006). "Un ensayo multicéntrico, aleatorizado, doble ciego, controlado con placebo, de búsqueda de dosis de una formulación de acción prolongada de octreotida para promover la pérdida de peso en adultos obesos con hipersecreción de insulina". Revista internacional de obesidad . 30 (2): 331–41. doi :10.1038/sj.ijo.0803074. PMC 1540404 . PMID 16158082.
{{cite journal}}: Mantenimiento de CS1: configuración anulada ( enlace )
