Vitamina D
| Vitamina D | |
|---|---|
| Clase de droga | |
 Colecalciferol ( D3 ) | |
| Identificadores de clase | |
| Sinónimos | Calciferoles |
| Usar | Raquitismo , osteoporosis , osteomalacia , deficiencia de vitamina D |
| Código ATC | A11CC |
| Objetivo biológico | receptor de vitamina D |
| Datos clínicos | |
| Drogas.com | Productos naturales MedFacts |
| Enlaces externos | |
| Malla | D014807 |
| Estatus legal | |
| En Wikidata | |
La vitamina D es un grupo de secosteroides liposolubles responsables de aumentar la absorción intestinal de calcio , magnesio y fosfato , junto con numerosas otras funciones biológicas. [1] [2] En los humanos, los compuestos más significativos dentro de este grupo son la vitamina D 3 ( colecalciferol ) y la vitamina D 2 ( ergocalciferol ). [2] [3]
La principal fuente natural de vitamina D es la síntesis de colecalciferol en las capas inferiores de la epidermis de la piel , desencadenada por una reacción fotoquímica con la radiación ultravioleta B (UV-B) de la luz solar o lámparas UV-B . [1] El colecalciferol y el ergocalciferol también se pueden obtener a través de la dieta y suplementos . [1] [2] Alimentos como la carne de pescado graso son buenas fuentes de vitamina D, aunque hay pocos otros alimentos donde aparece de forma natural en cantidades significativas. [2] [4] En los EE. UU. y otros países, la leche de vaca y los sustitutos de la leche de origen vegetal están fortificados con vitamina D, al igual que muchos cereales para el desayuno. [ 1] Los hongos expuestos a la luz ultravioleta también proporcionan cantidades útiles de vitamina D 2. [2] [5] Las recomendaciones dietéticas generalmente asumen que toda la vitamina D de una persona se toma por vía oral, dada la variabilidad en la exposición a la luz solar entre la población y las incertidumbres con respecto a los niveles seguros de exposición a la luz solar , particularmente debido al riesgo asociado de cáncer de piel . [2]
La vitamina D obtenida de la dieta o sintetizada en la piel es biológicamente inactiva. Se activa mediante dos pasos de hidroxilación enzimática , el primero que ocurre en el hígado y el segundo en los riñones . [1] [3] Dado que la mayoría de los mamíferos pueden sintetizar suficiente vitamina D con una exposición adecuada a la luz solar, técnicamente no es esencial en la dieta y, por lo tanto, no es una verdadera vitamina . En cambio, funciona como una hormona ; la activación de la prohormona de la vitamina D produce calcitriol , la forma activa. El calcitriol luego ejerce sus efectos a través del receptor de vitamina D , un receptor nuclear que se encuentra en varios tejidos en todo el cuerpo. [6]
El colecalciferol se convierte en el hígado en calcifediol (también conocido como calcidiol o 25-hidroxicolecalciferol), mientras que el ergocalciferol se convierte en ercalcidiol (25-hidroxiergocalciferol). [1] Estos dos metabolitos de la vitamina D, denominados colectivamente 25-hidroxivitamina D o 25(OH)D, se miden en suero para evaluar el estado de vitamina D de una persona. [7] [8] El calcifediol es hidroxilado aún más por los riñones y ciertas células inmunes para formar calcitriol (1,25-dihidroxicolecalciferol), la forma biológicamente activa de la vitamina D. [9] [10] El calcitriol circula en la sangre como una hormona, desempeñando un papel importante en la regulación de las concentraciones de calcio y fosfato , así como en la promoción de la salud ósea y la remodelación ósea . [1] Además, el calcitriol tiene otros efectos, incluida la influencia en la diferenciación celular, las funciones neuromusculares e inmunes y la reducción de la inflamación. [2]
La vitamina D tiene un papel importante en la homeostasis y el metabolismo del calcio. [1] Su descubrimiento se debió al esfuerzo por identificar la deficiencia dietética en niños con raquitismo , la forma infantil de osteomalacia . [11] Los suplementos de vitamina D se utilizan comúnmente para tratar o prevenir la osteomalacia y el raquitismo. [1] La evidencia de otros beneficios para la salud de la suplementación con vitamina D en personas que ya tienen suficiente vitamina D es inconsistente. [2] El efecto de la suplementación con vitamina D sobre la morbilidad y la mortalidad tampoco está claro, y un metanálisis encontró una pequeña disminución de la mortalidad en personas mayores. [12] A excepción de la prevención del raquitismo y la osteomalacia en grupos de alto riesgo, cualquier beneficio de los suplementos de vitamina D para la salud musculoesquelética o general puede ser pequeño y, en algunos casos, puede tener efectos adversos para la salud. [13] [14] [15]
Tipos
| Nombre | Composición química | Estructura |
|---|---|---|
| Vitamina D 1 | Mezcla de compuestos moleculares de ergocalciferol con lumisterol , 1:1 | |
| Vitamina D 2 | ergocalciferol (elaborado a partir de ergosterol ) | 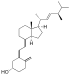 |
| Vitamina D3 | colecalciferol (elaborado a partir del 7-dehidrocolesterol presente en la piel). |  |
| Vitamina D 4 | 22-dihidroergocalciferol |  |
| Vitamina D 5 | sitocalciferol (elaborado a partir de 7-dehidrositosterol ) |  |
Existen varias formas ( vitámeros ) de vitamina D, siendo las dos formas principales la vitamina D 2 o ergocalciferol y la vitamina D 3 o colecalciferol. [1] El término "vitamina D" se refiere a D 2 o D 3 , o a ambas, y se conoce colectivamente como calciferol. [16]
La vitamina D 2 se caracterizó químicamente en 1931. En 1935, se definió la estructura química de la vitamina D 3 y se demostró que resultaba de la irradiación ultravioleta del 7-dehidrocolesterol. Aunque en 1981 se recomendó una nomenclatura química para las formas de vitamina D, [17] todavía se utilizan comúnmente nombres alternativos. [3]
Químicamente, las diversas formas de vitamina D son secoesteroides , lo que significa que uno de los enlaces en los anillos esteroides está roto. [18] La diferencia estructural entre la vitamina D 2 y la vitamina D 3 radica en la cadena lateral : la vitamina D 2 tiene un doble enlace entre los carbonos 22 y 23, y un grupo metilo en el carbono 24. [3] También se han sintetizado numerosos análogos de la vitamina D. [3]
Biología
El metabolito activo de la vitamina D, el calcitriol, ejerce sus efectos biológicos al unirse al receptor de vitamina D (VDR), que se encuentra principalmente en los núcleos de las células diana. [1] [18] Cuando el calcitriol se une al VDR, permite que el receptor actúe como un factor de transcripción , modulando la expresión génica de las proteínas de transporte involucradas en la absorción de calcio en el intestino, como TRPV6 y calbindina . [20] El VDR es parte de la superfamilia de receptores nucleares de receptores de hormonas esteroides , que son reguladores dependientes de hormonas de la expresión génica. Estos receptores se expresan en células de la mayoría de los órganos.
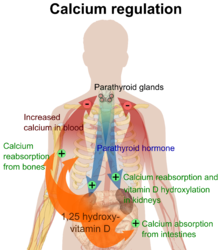
La activación del VDR en las células del intestino, los huesos, los riñones y las glándulas paratiroides desempeña un papel crucial en el mantenimiento de los niveles de calcio y fósforo en la sangre, un proceso que es asistido por la hormona paratiroidea y la calcitonina , lo que favorece la salud ósea . [1] [21]
Una de las funciones más importantes de la vitamina D es mantener el equilibrio del calcio esquelético promoviendo la absorción de calcio en los intestinos, promoviendo la resorción ósea al aumentar el número de osteoclastos , manteniendo los niveles de calcio y fosfato necesarios para la formación ósea y facilitando el funcionamiento adecuado de la hormona paratiroidea para mantener los niveles séricos de calcio. [1] La deficiencia de vitamina D puede conducir a una disminución de la densidad mineral ósea , aumentando el riesgo de osteoporosis y fracturas óseas debido a su impacto en el metabolismo mineral. [1] [22] En consecuencia, la vitamina D también es importante para la remodelación ósea , actuando como un potente estimulador de la resorción ósea. [22]
El VDR también regula la proliferación y diferenciación celular . Además, la vitamina D influye en el sistema inmunológico, ya que los VDR se expresan en varios glóbulos blancos, incluidos los monocitos y las células T y B activadas . [23] Los estudios in vitro indican que la vitamina D aumenta la expresión del gen de la tirosina hidroxilasa en las células medulares suprarrenales y afecta la síntesis de factores neurotróficos , óxido nítrico sintasa y glutatión , que pueden controlar la respuesta y la adaptación del cuerpo al estrés . [24]
La expresión de VDR disminuye con la edad. [1]
Deficiencia
Una dieta insuficiente en vitamina D, combinada con una exposición inadecuada a la luz solar, puede provocar una deficiencia de vitamina D, que se define como un nivel de 25-hidroxivitamina D o 25(OH)D en sangre inferior a 12 ng/ml (30 nmol/litro). La insuficiencia de vitamina D, por otro lado, se caracteriza por un nivel de 25(OH)D en sangre entre 12 y 20 ng/ml (30 a 50 nmol/litro). [2] [25] Se estima que mil millones de adultos en todo el mundo tienen insuficiencia o deficiencia de vitamina D, incluidos los de los países desarrollados de toda Europa. [26] La deficiencia grave de vitamina D en los niños, aunque es poco frecuente en el mundo desarrollado, puede provocar un ablandamiento y debilitamiento de los huesos en crecimiento, lo que lleva a una afección conocida como raquitismo . [27]
La deficiencia de vitamina D es prevalente a nivel mundial, particularmente entre los ancianos, y sigue siendo común tanto en niños como en adultos. [28] [29] [30] Esta deficiencia altera la mineralización ósea y causa daño óseo, lo que lleva a enfermedades que ablandan los huesos, como el raquitismo en niños y la osteomalacia en adultos. [31] Los niveles bajos de calcifediol (25-hidroxivitamina D 3 ) en sangre pueden ser resultado de una exposición solar limitada. [32] Cuando los niveles de vitamina D son deficientes, la absorción total de calcio dietético puede disminuir del rango normal de 60-80% a 15%. [21]
Las personas de piel oscura que viven en climas templados tienen más probabilidades de tener niveles bajos de vitamina D. [33] [34] [35] Esto se debe a que la melanina en la piel, que dificulta la síntesis de vitamina D, hace que las personas de piel oscura sean menos eficientes en la producción de vitamina D. [36] En los EE. UU., la deficiencia de vitamina D es particularmente común entre las poblaciones hispanas y afroamericanas, y los niveles disminuyen significativamente en el invierno debido al efecto protector de la melanina contra la exposición al sol. [25]
La deficiencia de vitamina D también se ha asociado con un mayor riesgo de desarrollar varios tipos de cáncer, incluido el melanoma . [37]
Salud ósea
Raquitismo
El raquitismo, una enfermedad infantil, se caracteriza por un retraso en el crecimiento y huesos largos blandos, débiles y deformados que se doblan y arquean bajo su peso cuando los niños comienzan a caminar. El raquitismo suele aparecer entre los 3 y los 18 meses de edad. [38] Se siguen notificando casos en América del Norte y otros países occidentales y se observa principalmente en bebés amamantados y en aquellos con tez más oscura. [38] Esta afección se caracteriza por piernas arqueadas, [31] que pueden ser causadas por deficiencia de calcio o fósforo, así como por falta de vitamina D; en el siglo XXI, se encuentra principalmente en países de bajos ingresos en África, Asia o Medio Oriente [39] y en personas con trastornos genéticos como el raquitismo por pseudodeficiencia de vitamina D. [40]
La deficiencia de vitamina D materna puede causar enfermedad ósea evidente desde antes del nacimiento y deterioro de la calidad ósea después del nacimiento. [41] [42] El raquitismo nutricional existe en países con luz solar intensa durante todo el año, como Nigeria, y puede ocurrir sin deficiencia de vitamina D. [43] [44]
Aunque el raquitismo y la osteomalacia son ahora poco frecuentes en el Reino Unido, se han producido brotes en algunas comunidades de inmigrantes en las que las personas con osteomalacia incluían mujeres con una exposición aparentemente adecuada a la luz del día al aire libre que vestían ropa occidental. [45] Tener la piel más oscura y una exposición reducida a la luz solar no produjo raquitismo a menos que la dieta se desviara de un patrón omnívoro occidental caracterizado por una alta ingesta de carne, pescado y huevos. [46] [47] [48] Los factores de riesgo dietéticos para el raquitismo incluyen la abstinencia de alimentos de origen animal. [45] [49]
La deficiencia de vitamina D sigue siendo la principal causa de raquitismo entre los lactantes en la mayoría de los países, ya que la leche materna tiene un bajo contenido de vitamina D y las costumbres sociales y las condiciones climáticas pueden impedir una exposición adecuada al sol. En países soleados como Nigeria, Sudáfrica y Bangladesh, donde el raquitismo se da entre los niños mayores y los niños pequeños, se ha atribuido a la baja ingesta de calcio en la dieta, característica de las dietas basadas en cereales con acceso limitado a los productos lácteos. [48]
El raquitismo era antiguamente un importante problema de salud pública entre la población estadounidense. En Denver , casi dos tercios de 500 niños tenían raquitismo leve a finales de la década de 1920. [50] Un aumento en la proporción de proteína animal [49] [51] en la dieta estadounidense del siglo XX junto con un mayor consumo de leche [52] [53] fortificada con cantidades relativamente pequeñas de vitamina D coincidió con una disminución drástica en el número de casos de raquitismo. [21] Además, en los Estados Unidos y Canadá, la leche fortificada con vitamina D, los suplementos vitamínicos infantiles y los suplementos vitamínicos han ayudado a erradicar la mayoría de los casos de raquitismo en niños con trastornos de malabsorción de grasas. [31]
Osteomalacia y osteoporosis
La osteomalacia es una enfermedad en adultos que resulta de la deficiencia de vitamina D. [1] Las características de esta enfermedad son el ablandamiento de los huesos, lo que lleva a la curvatura de la columna, debilidad muscular proximal , fragilidad ósea y mayor riesgo de fracturas. [1] La osteomalacia reduce la absorción de calcio y aumenta la pérdida de calcio del hueso, lo que aumenta el riesgo de fracturas óseas. La osteomalacia suele estar presente cuando los niveles de 25-hidroxivitamina D son inferiores a unos 10 ng/ml. [54] Aunque se cree que los efectos de la osteomalacia contribuyen al dolor musculoesquelético crónico , no hay evidencia convincente de niveles más bajos de vitamina D en personas con dolor crónico [55] o de que la suplementación alivie el dolor musculoesquelético crónico inespecífico. [56] La osteomalacia progresa a osteoporosis , una afección de densidad mineral ósea reducida con mayor fragilidad ósea y riesgo de fracturas óseas. La osteoporosis puede ser un efecto a largo plazo de la insuficiencia de calcio y/o vitamina D, esta última contribuyendo al reducir la absorción de calcio. [2]
Uso de suplementos
La suplementación con vitamina D es un método confiable para prevenir o tratar el raquitismo . [1] Por otra parte, los efectos de la suplementación con vitamina D sobre la salud no esquelética son inciertos. [57] [58] Una revisión no encontró ningún efecto de la suplementación sobre las tasas de enfermedad no esquelética, aparte de una disminución tentativa en la mortalidad en los ancianos. [59] Los suplementos de vitamina D no alteran los resultados de infarto de miocardio , accidente cerebrovascular o enfermedad cerebrovascular , cáncer, fracturas óseas u osteoartritis de rodilla . [14] [60]
Un informe del Instituto de Medicina de Estados Unidos (IOM) afirma: "Los resultados relacionados con el cáncer, las enfermedades cardiovasculares y la hipertensión , y la diabetes y el síndrome metabólico, las caídas y el rendimiento físico, el funcionamiento inmunológico y los trastornos autoinmunes , las infecciones, el funcionamiento neuropsicológico y la preeclampsia no se pudieron vincular de manera confiable con la ingesta de calcio o vitamina D, y a menudo fueron contradictorios". [61] : 5 Algunos investigadores afirman que el IOM fue demasiado definitivo en sus recomendaciones y cometió un error matemático al calcular el nivel sanguíneo de vitamina D asociado con la salud ósea. [62] Los miembros del panel del IOM sostienen que utilizaron un "procedimiento estándar para recomendaciones dietéticas" y que el informe se basa sólidamente en los datos. [62]
Mortalidad por todas las causas
Se ha descubierto tentativamente que la suplementación con vitamina D3 conduce a un menor riesgo de muerte en los ancianos, [12] [59] pero el efecto no se ha considerado pronunciado, o lo suficientemente seguro, como para recomendar la toma de suplementos. [14] Otras formas (vitamina D2 , alfacalcidol y calcitriol) no parecen tener ningún efecto beneficioso con respecto al riesgo de muerte. [12] Los niveles altos en sangre parecen estar asociados con un menor riesgo de muerte, pero no está claro si la suplementación puede resultar en este beneficio. [63] Tanto un exceso como una deficiencia de vitamina D parecen causar un funcionamiento anormal y envejecimiento prematuro. [64] [65] [66] La relación entre las concentraciones séricas de calcifediol y la mortalidad por todas las causas tiene "forma de U": la mortalidad es elevada en niveles altos y bajos de calcifediol, en relación con los niveles moderados. [61] El daño causado por la vitamina D parece ocurrir a un nivel más bajo de vitamina D en las poblaciones de piel oscura de Canadá y Estados Unidos que se han estudiado que en las poblaciones de piel clara de Canadá y Estados Unidos que se han estudiado. Se desconoce si esto sucede así en las poblaciones de piel oscura de otras partes del mundo. [61] : 435
Salud ósea
En general, no hay evidencia sólida que respalde la creencia generalizada de que los suplementos de vitamina D pueden ayudar a prevenir la osteoporosis . [14] Por lo tanto, es probable que no sea necesario su uso generalizado para la prevención de esta enfermedad en personas sin deficiencia de vitamina D. [13] Para las personas mayores con osteoporosis, tomar vitamina D con calcio puede ayudar a prevenir fracturas de cadera, pero también aumenta ligeramente el riesgo de problemas estomacales y renales. [67] Un estudio encontró que la suplementación con 800 UI o más al día, en personas mayores de 65 años, fue "algo favorable en la prevención de fracturas de cadera y fracturas no vertebrales". [68] El efecto es pequeño o nulo para las personas que viven de forma independiente. [69] [70] Los niveles bajos de vitamina D sérica se han asociado con caídas y baja densidad mineral ósea . [71] Sin embargo, tomar vitamina D adicional no parece cambiar el riesgo. [72]
Los deportistas con deficiencia de vitamina D tienen un mayor riesgo de sufrir fracturas por estrés o roturas importantes, en particular los que practican deportes de contacto. El mayor beneficio de la suplementación se observa en deportistas con deficiencia (niveles séricos de 25(OH)D <30 ng/ml) o deficiencia grave (niveles séricos de 25(OH)D <25 ng/ml). Se observan disminuciones progresivas de los riesgos con concentraciones séricas crecientes de 25(OH)D que se estabilizan en 50 ng/ml sin que se observen beneficios adicionales en niveles más allá de este punto. [73]
Una revisión sistemática Cochrane de 2020 encontró evidencia limitada de que la vitamina D más calcio , pero no de forma independiente, pueden mejorar la curación en niños con raquitismo nutricional , pero la evidencia no fue concluyente para reducir las fracturas. [74]
La Administración de Alimentos y Medicamentos de los Estados Unidos (FDA) exige a los fabricantes que declaren la cantidad de vitamina D en las etiquetas de información nutricional , como "nutrientes de importancia para la salud pública", desde mayo de 2016. Mediante una extensión propuesta de la fecha límite, algunos fabricantes tenían hasta el 1 de julio de 2021 para cumplir. [75]
Cáncer
Se han encontrado asociaciones potenciales entre niveles bajos de vitamina D y el riesgo de desarrollar varios tipos de cáncer. [37] [76] [77] Los metanálisis de estudios observacionales han encontrado un riesgo reducido de incidencia de cáncer relacionado con la ingesta de vitamina D y los niveles de 25(OH)D, particularmente para el cáncer colorrectal , aunque la fuerza de las asociaciones se clasificó como débil. [77] [78] Se encontró que el receptor de vitamina D y SNAI2 están involucrados en el proceso metastásico del osteosarcoma . [79] Si bien los ensayos controlados aleatorios no han confirmado que los suplementos de vitamina D reduzcan el riesgo de incidencia de cáncer, el riesgo relativo de muertes por cáncer fue menor hasta en un 16% en varios metanálisis. [80] [78]
Se ha sugerido que los niveles bajos de 25-hidroxivitamina D, un marcador de uso rutinario para la vitamina D, son un factor que contribuye a aumentar el riesgo de desarrollo y progresión de varios tipos de cáncer, incluido el melanoma . La vitamina D requiere la activación de las enzimas del citocromo P450 (CYP) para activarse y unirse al VDR. Específicamente, CYP27A1 , CYP27B1 y CYP2R1 están involucradas en la activación de la vitamina D, mientras que CYP24A1 y CYP3A4 son responsables de la degradación de la vitamina D activa. CYP24A1, la enzima catabólica primaria del calcitriol, se sobreexpresa en los tejidos y células del melanoma. Esta sobreexpresión podría conducir a niveles más bajos de vitamina D activa en los tejidos, lo que potencialmente promueve el desarrollo y la progresión del melanoma. Varias clases de medicamentos y productos naturales para la salud pueden modular las enzimas CYP relacionadas con la vitamina D, lo que potencialmente causa niveles más bajos de vitamina D y sus metabolitos activos en los tejidos, lo que sugiere que mantener niveles adecuados de vitamina D, es decir, evitar la deficiencia de vitamina D, ya sea a través de suplementos dietéticos o modulando el metabolismo del CYP, podría ser beneficioso para disminuir el riesgo de desarrollo de melanoma. [37]
Enfermedad cardiovascular
La suplementación con vitamina D no está asociada con un riesgo reducido de accidente cerebrovascular, enfermedad cerebrovascular , infarto de miocardio o enfermedad cardíaca isquémica . [14] [81] [82] La suplementación no reduce la presión arterial en la población general. [83] [84] [85]
Sistema inmunitario
Enfermedades infecciosas
En general, la vitamina D funciona para activar el sistema inmune innato y amortiguar el adaptativo con efectos antibacterianos, antivirales y antiinflamatorios. [86] [87] Los niveles bajos de vitamina D parecen ser un factor de riesgo para la tuberculosis , [88] e históricamente se ha utilizado como tratamiento. [89]
La suplementación con vitamina D en dosis bajas (400 a 1000 UI/día) puede reducir levemente el riesgo general de infecciones agudas del tracto respiratorio . [90] Los beneficios se encontraron en niños pequeños y adolescentes (de 1 a 16 años) y no se confirmaron con dosis más altas (>1000 UI por día o más). [90] La suplementación con vitamina D reduce sustancialmente la tasa de exacerbaciones moderadas o graves de la EPOC en personas con niveles basales de 25(OH)D por debajo de 25 nmol/L, pero no en aquellas con deficiencia menos grave. [91]
Asma
La suplementación con vitamina D no ayuda a prevenir los ataques de asma ni a aliviar sus síntomas. [92]
Enfermedad inflamatoria intestinal
Los niveles bajos de vitamina D se asocian con dos formas principales de enfermedad inflamatoria intestinal humana : la enfermedad de Crohn y la colitis ulcerosa . [93] Las deficiencias de vitamina D se han relacionado con la gravedad del caso de enfermedad inflamatoria intestinal, sin embargo, no está claro si la deficiencia de vitamina D causa enfermedad inflamatoria intestinal o es un síntoma de la enfermedad. [94]
Hay cierta evidencia de que la terapia de suplementación con vitamina D para personas con enfermedad inflamatoria intestinal puede estar asociada con mejoras en las puntuaciones de la actividad clínica de la enfermedad inflamatoria intestinal y los marcadores bioquímicos. [95] [94] El tratamiento con vitamina D puede estar asociado con una recaída menos frecuente de los síntomas en la EII. [94] No está claro si este tratamiento mejora la calidad de vida de la persona o la respuesta clínica al tratamiento con vitamina D. [94] El régimen de tratamiento ideal y la dosis de la terapia con vitamina D no se han estudiado lo suficientemente bien. [94]
Otras condiciones
Diabetes
Un metaanálisis informó que la suplementación con vitamina D redujo significativamente el riesgo de diabetes tipo 2 en personas no obesas con prediabetes . [96] Otro metaanálisis informó que la suplementación con vitamina D mejoró significativamente el control glucémico [evaluación del modelo homeostático de resistencia a la insulina (HOMA-IR)], la hemoglobina A1C (HbA1C) y la glucemia en ayunas (FBG) en personas con diabetes tipo 2. [97] En estudios prospectivos, un nivel alto versus bajo de vitamina D se asoció respectivamente con una disminución significativa del riesgo de diabetes tipo 2, diabetes tipo 2 combinada y prediabetes, y prediabetes. [98] Una revisión sistemática Cochrane de 2011 examinó un estudio que mostró que la vitamina D junto con la insulina mantenía los niveles de péptido C en ayunas después de 12 meses mejor que la insulina sola. Sin embargo, es importante destacar que los estudios disponibles para ser incluidos en esta revisión presentaron fallas considerables en calidad y diseño. [99]
Trastorno por déficit de atención e hiperactividad (TDAH)
Un metaanálisis de estudios observacionales mostró que los niños con TDAH tienen niveles más bajos de vitamina D y que había una pequeña asociación entre los niveles bajos de vitamina D al momento del nacimiento y el desarrollo posterior del TDAH. [100] Varios ensayos controlados aleatorizados pequeños de suplementación con vitamina D indicaron una mejora en los síntomas del TDAH, como la impulsividad y la hiperactividad. [101]
Depresión
Los ensayos clínicos de suplementación con vitamina D para los síntomas depresivos generalmente han sido de baja calidad y no muestran un efecto general, aunque el análisis de subgrupos mostró que la suplementación para los participantes con síntomas depresivos clínicamente significativos o trastorno depresivo tuvo un efecto moderado. [102]
Cognición y demencia
Una revisión sistemática de estudios clínicos encontró una asociación entre los niveles bajos de vitamina D y el deterioro cognitivo y un mayor riesgo de desarrollar la enfermedad de Alzheimer . Sin embargo, las concentraciones más bajas de vitamina D también se asocian con una mala nutrición y con pasar menos tiempo al aire libre. Por lo tanto, existen explicaciones alternativas para el aumento del deterioro cognitivo y, por lo tanto, no se pudo establecer una relación causal directa entre los niveles de vitamina D y la cognición . [103]
Esquizofrenia
Los ensayos han demostrado que los niveles más bajos de vitamina D son muy frecuentes en personas con esquizofrenia, particularmente en aquellas con episodios agudos. [104]
Embarazo
Los niveles bajos de vitamina D durante el embarazo se asocian con diabetes gestacional , preeclampsia y bebés pequeños (para la edad gestacional). [105] Aunque tomar suplementos de vitamina D durante el embarazo aumenta los niveles sanguíneos de vitamina D en la madre a término, [106] no está claro el alcance total de los beneficios para la madre o el bebé. [105] [106] [107] Las mujeres embarazadas que toman una cantidad adecuada de vitamina D durante la gestación pueden experimentar un menor riesgo de preeclampsia [108] y efectos inmunológicos positivos. [109] También es probable que la suplementación con vitamina D reduzca el riesgo de diabetes gestacional, bebés de tamaño insuficiente [108] y de su baja tasa de crecimiento. [110] Las mujeres embarazadas a menudo no toman la cantidad recomendada de vitamina D. [109]
Pérdida de peso
Aunque se planteó la hipótesis de que la suplementación con vitamina D puede ser un tratamiento eficaz para la obesidad , además de la restricción calórica , una revisión sistemática no encontró asociación entre la suplementación y el peso corporal o la masa grasa . [111] Un metanálisis de 2016 encontró que el estado de vitamina D circulante mejoraba con la pérdida de peso, lo que indica que la masa grasa puede estar inversamente asociada con los niveles sanguíneos de vitamina D. [112]
Declaraciones de propiedades saludables permitidas
Las agencias reguladoras gubernamentales estipulan para las industrias de alimentos y suplementos dietéticos ciertas declaraciones de propiedades saludables que están permitidas como declaraciones en los envases.
Autoridad Europea de Seguridad Alimentaria
- Función normal del sistema inmunológico [113]
- respuesta inflamatoria normal [113]
- Función muscular normal [113]
- riesgo reducido de caídas en personas mayores de 60 años [114]
Administración de Alimentos y Medicamentos de los Estados Unidos (FDA)
- “Un aporte adecuado de calcio y vitamina D, como parte de una dieta bien equilibrada, junto con la actividad física, puede reducir el riesgo de osteoporosis”. [115]
- “Una ingesta adecuada de calcio y ejercicio regular pueden ayudar a fortalecer los huesos en niños y adolescentes y pueden reducir el riesgo de osteoporosis en adultos mayores. También es necesaria una ingesta adecuada de vitamina D.” [116]
Otras posibles agencias con orientación sobre reclamaciones: FOSHU de Japón [117] y Australia-Nueva Zelanda [118] .
Ingesta dietética
| Reino Unido | ||
| Grupo de edad | Ingesta (μg/día) | Ingesta máxima (μg/día) [119] |
|---|---|---|
| Lactantes amamantados de 0 a 12 meses | 8,5 – 10 | 25 |
| Lactantes alimentados con fórmula (<500 ml/día) | 10 | 25 |
| Niños de 1 a 10 años | 10 | 50 |
| Niños >10 años y adultos | 10 | 100 |
| Estados Unidos | ||
| Grupo de edad | RDA (UI/día) | (μg/día) [61] |
| Bebés de 0 a 6 meses | 400* | 10 |
| Bebés de 6 a 12 meses | 400* | 10 |
| 1–70 años | 600 | 15 |
| Adultos > 70 años | 800 | 20 |
| Embarazada/Lactancia | 600 | 15 |
| Grupo de edad | Nivel máximo de ingesta tolerable (UI/día) | (μg/día) |
| Bebés de 0 a 6 meses | 1.000 | 25 |
| Bebés de 6 a 12 meses | 1.500 | 37.5 |
| 1–3 años | 2.500 | 62,5 |
| 4–8 años | 3.000 | 75 |
| 9+ años | 4.000 | 100 |
| Embarazada/lactante | 4.000 | 100 [61] |
| Canadá | ||
| Grupo de edad | RDA (UI) [120] | Ingesta máxima tolerable (UI) [120] |
| Bebés de 0 a 6 meses | 400* | 1.000 |
| Bebés de 7 a 12 meses | 400* | 1.500 |
| Niños de 1 a 3 años | 600 | 2.500 |
| Niños de 4 a 8 años | 600 | 3.000 |
| Niños y adultos de 9 a 70 años | 600 | 4.000 |
| Adultos > 70 años | 800 | 4.000 |
| Embarazo y lactancia | 600 | 4.000 |
| Australia y Nueva Zelanda | ||
| Grupo de edad | Ingesta adecuada (μg) [118] | Nivel máximo de ingesta (μg) [118] |
| Bebés de 0 a 12 meses | 5* | 25 |
| Niños de 1 a 18 años | 5* | 80 |
| Adultos de 19 a 50 años | 5* | 80 |
| Adultos de 51 a 70 años | 10* | 80 |
| Adultos > 70 años | 15* | 80 |
| Autoridad Europea de Seguridad Alimentaria | ||
| Grupo de edad | Ingesta adecuada (μg) [121] | Límite superior tolerable (μg) [122] |
| Bebés de 0 a 12 meses | 10 | 25 |
| Niños de 1 a 10 años | 15 | 50 |
| Niños de 11 a 17 años | 15 | 100 |
| Adultos | 15 | 100 |
| Embarazo y lactancia | 15 | 100 |
| * Ingesta adecuada, aún no se ha establecido RDA/RDI | ||
Niveles recomendados
Varias instituciones han propuesto diferentes recomendaciones sobre la cantidad de ingesta diaria [123] de vitamina D. Estas varían según la definición precisa, la edad, el embarazo o la lactancia, y el grado de suposiciones que se hacen sobre la síntesis cutánea de vitamina D. [61] [118] [119] [120] [121] Conversión: 1 μg (microgramo) = 40 UI (unidad internacional). [119]
Reino Unido
El Servicio Nacional de Salud del Reino Unido (NHS) recomienda que las personas con riesgo de deficiencia de vitamina D, los bebés amamantados, los bebés alimentados con fórmula que toman menos de 500 ml/día y los niños de 6 meses a 4 años, tomen suplementos diarios de vitamina D durante todo el año para asegurar una ingesta suficiente. [119] Esto incluye a las personas con síntesis cutánea limitada de vitamina D, que no suelen estar al aire libre, son frágiles, están confinadas en casa, viven en una residencia de ancianos o suelen llevar ropa que cubre la mayor parte de la piel, o tienen piel oscura, como las personas de origen africano, afrocaribeño o del sur de Asia. Otras personas pueden ser capaces de producir vitamina D adecuada a partir de la exposición a la luz solar de abril a septiembre. El NHS y Public Health England recomiendan que todas las personas, incluidas las embarazadas y las que están amamantando, consideren tomar un suplemento diario que contenga 10 μg (400 UI) de vitamina D durante el otoño y el invierno debido a la luz solar inadecuada para la síntesis de vitamina D. [124]
Estados Unidos
La ingesta dietética de referencia para la vitamina D emitida en 2010 por el Instituto de Medicina (IoM) (rebautizado como Academia Nacional de Medicina en 2015), reemplazó las recomendaciones anteriores que se expresaban en términos de ingesta adecuada. Las recomendaciones se formularon asumiendo que el individuo no tiene síntesis cutánea de vitamina D debido a una exposición solar inadecuada. La ingesta de referencia para la vitamina D se refiere a la ingesta total de alimentos, bebidas y suplementos, y supone que se están satisfaciendo los requerimientos de calcio. [61] : 5 El nivel máximo de ingesta tolerable (UL) [125] se define como "la ingesta diaria promedio más alta de un nutriente que probablemente no presente riesgo de efectos adversos para la salud para casi todas las personas de la población general". [61] : 403 Aunque se cree que los UL son seguros, la información sobre los efectos a largo plazo es incompleta y estos niveles de ingesta no se recomiendan para el consumo a largo plazo. [61] : 403 : 433
Para los fines del etiquetado de alimentos y suplementos dietéticos en los EE. UU., la cantidad en una porción se expresa como un porcentaje del valor diario (%VD). Para los fines del etiquetado de vitamina D, el 100 % del valor diario era de 400 UI (10 μg), pero en mayo de 2016, se revisó a 800 UI (20 μg) para que coincidiera con la ingesta diaria recomendada (IDR). [126] [127] El cumplimiento de las regulaciones de etiquetado actualizadas se exigió para el 1 de enero de 2020 para los fabricantes con US$10 millones o más en ventas anuales de alimentos, y para el 1 de enero de 2021 para los fabricantes con ventas de alimentos de menor volumen. [75] [128] Se proporciona una tabla de los valores diarios antiguos y nuevos para adultos en Ingesta diaria de referencia .
Canadá
Health Canada publicó las ingestas dietéticas recomendadas (IDR) y los niveles máximos de ingesta tolerables (NM) de vitamina D basados en el informe de 2010 encargado y financiado conjuntamente por el Instituto de Medicina. [61] [120]
Australia y Nueva Zelanda
En 2006, Australia y Nueva Zelanda publicaron valores de referencia de nutrientes que incluían pautas para la ingesta de vitamina D en la dieta. [118] Aproximadamente un tercio de los australianos tienen deficiencia de vitamina D. [129] [130]
unión Europea
En 2016, la Autoridad Europea de Seguridad Alimentaria (AESA) [121] revisó la evidencia actual y encontró que la relación entre la concentración sérica de 25(OH)D y los resultados de salud musculoesquelética es muy variable. Consideraron que no se pueden derivar los requerimientos promedio y los valores de referencia de ingesta poblacional para la vitamina D, y que una concentración sérica de 25(OH)D de 50 nmol/L era un valor objetivo adecuado. Para todas las personas mayores de 1 año, incluidas las mujeres embarazadas o en período de lactancia, establecieron una ingesta adecuada de 15 μg/día (600 UI). [121]
La EFSA revisó los niveles seguros de ingesta en 2012, [122] estableciendo el límite superior tolerable para adultos en 100 μg/día (4000 UI), una conclusión similar a la del IOM.
La Agencia Nacional de Alimentos de Suecia recomienda una ingesta diaria de 10 μg (400 UI) de vitamina D3 para niños y adultos de hasta 75 años, y 20 μg (800 UI) para adultos de 75 años o más. [131]
Las organizaciones no gubernamentales en Europa han hecho sus propias recomendaciones. La Sociedad Alemana de Nutrición recomienda 20 μg. [132] La Sociedad Europea de Menopausia y Andropausia recomienda que las mujeres posmenopáusicas consuman 15 μg (600 UI) hasta los 70 años y 20 μg (800 UI) a partir de los 71 años. Esta dosis debe aumentarse a 100 μg (4000 UI) en algunos pacientes con niveles muy bajos de vitamina D o en caso de comorbilidades. [133]
Fuentes
Aunque la vitamina D está presente de forma natural solo en unos pocos alimentos, [2] se suele añadir como fortificación a los alimentos procesados. En algunos países, los alimentos básicos se fortifican artificialmente con vitamina D. [134]
Fuentes naturales
| Fuentes animales | |||
| Fuente [135] | UI/g | Irregular | |
|---|---|---|---|
| Yema de huevo cocida | 0,7 | 44 UI por un huevo de 61 g | |
| Hígado de res, cocido, estofado | 0,5 | ||
| Aceites de hígado de pescado, como el aceite de hígado de bacalao | 100 | 450 UI por cucharadita (4,5 g) | |
| Especies de peces grasos | |||
| Salmón , rosado, cocido, calor seco | 5.2 | ||
| Caballa del Pacífico y jurel, especies mixtas, cocidas, calor seco | 4.6 | ||
| Atún enlatado en aceite | 2.7 | ||
| Sardinas enlatadas en aceite , escurridas | 1.9 | ||
| Fuentes de hongos | |||
| Fuente | microgramos por gramo | UI/g | |
|---|---|---|---|
| Cladonia arbuscula (liquen), talos , secos [136] | vitamina D3 | 0,67–2,04 | 27–82 |
| vitamina D2 | 0,22–0,55 | 8.8–22 | |
| Agaricus bisporus (hongo común): D 2 + D 3 | |||
| Portobello | Crudo | 0,003 | 0,1 |
| Expuesto a la luz ultravioleta | 0,11 | 4.46 | |
| Crímenes | Crudo | 0,001 | 0,03 |
| Expuesto a la luz ultravioleta | 0,32 | 12.8 | |
En general, la vitamina D 3 se encuentra en alimentos de origen animal , particularmente pescado, carne, vísceras , huevos y productos lácteos. [137] La vitamina D 2 se encuentra en hongos y se produce por irradiación ultravioleta de ergosterol . [138] El contenido de vitamina D 2 en hongos y Cladina arbuscula , un liquen, aumenta con la exposición a la luz ultravioleta, [136] [139] y es estimulado por lámparas ultravioleta industriales para fortificación. [138] El Departamento de Agricultura de los Estados Unidos informa el contenido de D 2 y D 3 combinados en un valor.
Fortificación de alimentos
Los alimentos elaborados fortificados con vitamina D incluyen algunos jugos de frutas y bebidas de jugo de frutas, barras energéticas de reemplazo de comidas , bebidas a base de proteína de soja , ciertos quesos y productos de queso, productos de harina, fórmulas infantiles , muchos cereales para el desayuno y leche. [140] [141]
En 2016, en los Estados Unidos, la Administración de Alimentos y Medicamentos (FDA) modificó las regulaciones de aditivos alimentarios para la fortificación de la leche, [142] indicando que los niveles de vitamina D 3 no deben exceder las 42 UI de vitamina D por cada 100 g (400 UI por cuarto de galón estadounidense ) de leche láctea, 84 UI de vitamina D 2 por cada 100 g (800 UI por cuarto de galón) de leches vegetales y 89 UI por cada 100 g (800 UI por cuarto de galón) en yogures vegetales o en productos de bebidas de soja. [143] [144] [145] Las leches vegetales se definen como bebidas elaboradas a partir de soja, almendras, arroz, entre otras fuentes vegetales, destinadas a ser alternativas a la leche láctea. [146]
Si bien algunos estudios han descubierto que la vitamina D3 aumenta los niveles de 25(OH)D en sangre más rápidamente y permanece activa en el cuerpo durante más tiempo, [147] [148] otros sostienen que las fuentes de vitamina D2 son igualmente biodisponibles y efectivas que la D3 para aumentar y mantener los niveles de 25(OH)D. [138] [149] [150]
Preparación de alimentos
El contenido de vitamina D en los alimentos típicos se reduce de forma variable con la cocción. Los alimentos hervidos, fritos y horneados conservan entre el 69 y el 89 % de la vitamina D original. [151]
Niveles séricos recomendados

Las recomendaciones sobre los niveles séricos recomendados de 25(OH)D varían según las autoridades y varían en función de factores como la edad. [2] Los laboratorios estadounidenses generalmente informan los niveles de 25(OH)D en ng/mL. [154] Otros países suelen utilizar nmol/L. [154] Un ng/mL es aproximadamente igual a 2,5 nmol/L. [155]
Una revisión de 2014 concluyó que los niveles séricos más ventajosos para 25(OH)D para todos los resultados parecían estar cerca de 30 ng/mL (75 nmol/L). [156] Los niveles óptimos de vitamina D aún son controvertidos y otra revisión concluyó que se debían recomendar rangos de 30 a 40 ng/mL (75 a 100 nmol/L) para los atletas. [157] Parte de la controversia se debe a que numerosos estudios han encontrado diferencias en los niveles séricos de 25(OH)D entre grupos étnicos; los estudios apuntan a razones genéticas y ambientales detrás de estas variaciones. [158] La suplementación para alcanzar estos niveles estándar podría causar calcificación vascular dañina . [35]
Un metaanálisis de 2012 mostró que el riesgo de enfermedades cardiovasculares aumenta cuando los niveles de vitamina D en sangre son más bajos, en un rango de 8 a 24 ng/mL (20 a 60 nmol/L), aunque los resultados entre los estudios analizados fueron inconsistentes. [159]
En 2011, un comité del IOM concluyó que es necesario un nivel sérico de 25(OH)D de 20 ng/mL (50 nmol/L) para la salud ósea y general. Las ingestas dietéticas de referencia para la vitamina D se eligen con un margen de seguridad y "sobrepasan" el valor sérico objetivo para asegurar que los niveles de ingesta especificados alcancen los niveles séricos deseados de 25(OH)D en casi todas las personas. No se supone que la exposición al sol contribuya al nivel sérico de 25(OH)D y las recomendaciones son totalmente aplicables a las personas de piel oscura o con una exposición insignificante a la luz solar. El Instituto descubrió que las concentraciones séricas de 25(OH)D superiores a 30 ng/mL (75 nmol/L) "no están asociadas de manera consistente con un mayor beneficio". Los niveles séricos de 25(OH)D superiores a 50 ng/mL (125 nmol/L) pueden ser motivo de preocupación. Sin embargo, algunas personas con niveles séricos de 25(OH)D entre 30 y 50 ng/mL (75 nmol/L-125 nmol/L) también tendrán niveles inadecuados de vitamina D. [61]
Exceso
La toxicidad de la vitamina D es poco frecuente. [30] Se produce por la administración de suplementos con dosis altas de vitamina D en lugar de la luz solar. No se ha establecido el umbral de toxicidad de la vitamina D; sin embargo, según algunas investigaciones:
- Se ha demostrado que 100 μg/día (4 k UI ) no causan niveles tóxicos. edades de 9 a 71 años [160]
- Se ha demostrado que una dosis de 240 μg/día (10 000 UI) durante 5 meses no causa toxicidad. [30]
- 1250 μg/día (50 000 UI) durante varios meses pueden aumentar los niveles séricos de 25-hidroxivitamina D a 150 ng/ml. [30] [161]
Las personas con ciertas afecciones médicas, como el hiperparatiroidismo primario , [162] son mucho más sensibles a la vitamina D y desarrollan hipercalcemia en respuesta a cualquier aumento en la nutrición con vitamina D, mientras que la hipercalcemia materna durante el embarazo puede aumentar la sensibilidad fetal a los efectos de la vitamina D y conducir a un síndrome de discapacidad intelectual y deformidades faciales. [162] [163]
La hipercalcemia infantil idiopática es causada por una mutación del gen CYP24A1 , que conduce a una reducción en la degradación de la vitamina D. Los bebés que tienen dicha mutación tienen una mayor sensibilidad a la vitamina D y, en caso de ingesta adicional, un riesgo de hipercalcemia . [164] [165] El trastorno puede continuar hasta la edad adulta. [166]
Una revisión publicada en 2015 señaló que solo se han informado efectos adversos en concentraciones séricas de 25(OH)D superiores a 200 nmol/L. [157]
Los casos publicados de toxicidad que involucran hipercalcemia en los que se conocen la dosis de vitamina D y los niveles de 25-hidroxi-vitamina D implican todos una ingesta de ≥40.000 UI (1.000 μg) por día. [162]
Las mujeres embarazadas o en período de lactancia deben consultar a un médico antes de tomar un suplemento de vitamina D. La FDA recomendó a los fabricantes de suplementos líquidos de vitamina D que los goteros que acompañan a estos productos deben estar marcados de forma clara y precisa para 400 unidades internacionales (1 UI es el equivalente biológico de 25 ng de colecalciferol/ergocalciferol). Además, para los productos destinados a bebés, la FDA recomienda que el gotero no contenga más de 400 UI. [167] Para los bebés (desde el nacimiento hasta los 12 meses), el límite superior tolerable (cantidad máxima que se puede tolerar sin sufrir daños) se establece en 25 μg/día (1000 UI). Mil microgramos por día en bebés han producido toxicidad en el plazo de un mes. [161] Tras recibir encargos de los gobiernos canadiense y estadounidense, el Instituto de Medicina (IOM), a partir del 30 de noviembre de 2010 [actualizar], ha aumentado el límite superior tolerable (UL) a 2500 UI por día para las edades de 1 a 3 años, 3000 UI por día para las edades de 4 a 8 años y 4000 UI por día para las edades de 9 a 71 años o más (incluidas las mujeres embarazadas o lactantes). [160]
El propio calcitriol se autorregula en un ciclo de retroalimentación negativa y también se ve afectado por la hormona paratiroidea , el factor de crecimiento de fibroblastos 23 , las citocinas , el calcio y el fosfato. [168]
Un estudio publicado en 2017 evaluó la prevalencia de niveles altos de ingesta diaria de vitamina D suplementaria entre adultos mayores de 20 años en los Estados Unidos, basándose en datos de NHANES disponibles públicamente desde 1999 hasta 2014. Sus datos muestran lo siguiente:
- Más del 18% de la población excede la dosis diaria recomendada ( RDA ) del NIH de 600 a 800 UI, [2] al tomar más de 1000 UI, lo que sugiere una ingesta intencional de suplementos. [169]
- Más del 3% de la población excede el nivel máximo de ingesta diaria tolerable ( UL ) de los NIH de 4000 UI, [2] por encima del cual aumenta el riesgo de efectos tóxicos. [170] [169]
- Según el análisis de tendencias, el porcentaje de la población que toma más de 1000 UI/día, así como el porcentaje que toma más de 4000 UI/día, han aumentado desde 1999. [169]
Efecto del exceso
La sobredosis de vitamina D causa hipercalcemia, que es un fuerte indicio de toxicidad por vitamina D; esto se puede notar con un aumento en la micción y la sed. Si la hipercalcemia no se trata, da como resultado depósitos excesivos de calcio en los tejidos blandos y órganos como los riñones, el hígado y el corazón, lo que provoca dolor y daño orgánico. [30] [31] [171]
Los principales síntomas de una sobredosis de vitamina D son la hipercalcemia, que incluye anorexia , náuseas y vómitos. A estos pueden seguirles poliuria , polidipsia , debilidad, insomnio, nerviosismo, prurito y, en última instancia, insuficiencia renal. Además, pueden desarrollarse proteinuria , cilindros urinarios , azotemia y calcificación metastásica (especialmente en los riñones). [161] Otros síntomas de toxicidad por vitamina D incluyen discapacidad intelectual en niños pequeños, crecimiento y formación anormal de los huesos, diarrea, irritabilidad, pérdida de peso y depresión grave. [30] [171]
La toxicidad por vitamina D se trata suspendiendo la suplementación con vitamina D y restringiendo la ingesta de calcio. El daño renal puede ser irreversible. La exposición a la luz solar durante períodos prolongados normalmente no causa toxicidad por vitamina D. Las concentraciones de precursores de vitamina D producidos en la piel alcanzan un equilibrio y cualquier vitamina D adicional producida se degrada. [162]
Biosíntesis
La síntesis de vitamina D en la naturaleza depende de la presencia de radiación UV y de su posterior activación en el hígado y los riñones. Muchos animales sintetizan vitamina D3 a partir del 7-dehidrocolesterol y muchos hongos sintetizan vitamina D2 a partir del ergosterol . [138] [172]
Ruta interactiva
Haga clic en el icono en la esquina inferior derecha para abrir.
Haga clic en los genes, proteínas y metabolitos que aparecen a continuación para acceder a los artículos correspondientes. [§ 1]
- ^ El mapa de ruta interactivo se puede editar en WikiPathways: "VitaminDSynthesis_WP1531".
Fotoquímica


La transformación que convierte el 7-deshidrocolesterol en vitamina D 3 ocurre en dos pasos. [173] [174] Primero, el 7-deshidrocolesterol es fotolizado por luz ultravioleta en una reacción electrocíclica de apertura de anillo conrotatorio de 6 electrones ; el producto es previtamina D 3 . Segundo, la previtamina D 3 se isomeriza espontáneamente a vitamina D 3 ( colecalciferol ) en un desplazamiento de hidruro sigmatrópico antarafacial [1,7] . A temperatura ambiente, la transformación de previtamina D 3 en vitamina D 3 en un solvente orgánico tarda unos 12 días en completarse. La conversión de previtamina D 3 en vitamina D 3 en la piel es aproximadamente 10 veces más rápida que en un solvente orgánico. [175]
La conversión de ergosterol a vitamina D 2 sigue un procedimiento similar, formándose previtamina D 2 por fotólisis, que se isomeriza a vitamina D 2 ( ergocalciferol ). [176] La transformación de previtamina D 2 a vitamina D 2 en metanol tiene una velocidad comparable a la de la previtamina D 3 . El proceso es más rápido en los champiñones blancos. [138] : fig. 3
Síntesis en la piel

La vitamina D 3 se produce fotoquímicamente a partir del 7-dehidrocolesterol en la piel de la mayoría de los animales vertebrados, incluidos los humanos. [177] El precursor de la vitamina D 3 , el 7-dehidrocolesterol, se produce en cantidades relativamente grandes. El 7-dehidrocolesterol reacciona con la luz UVB en longitudes de onda de 290 a 315 nm. [178] Estas longitudes de onda están presentes en la luz solar, así como en la luz emitida por las lámparas UV en las camas de bronceado (que producen ultravioleta principalmente en el espectro UVA , pero normalmente producen entre el 4% y el 10% de las emisiones UV totales como UVB, algunas camas de bronceado pueden usar solo bombillas de luz UVB separadas específicamente para la producción de vitamina D). La exposición a la luz a través de las ventanas es insuficiente porque el vidrio bloquea casi por completo la luz UVB. [179]
Se pueden producir cantidades adecuadas de vitamina D con una exposición moderada al sol en la cara, los brazos y las piernas (para quienes tienen menos melanina), con un promedio de 5 a 30 minutos dos veces por semana, o aproximadamente el 25% del tiempo para quemaduras solares mínimas. Cuanto más oscura sea la piel en la escala de Fitzpatrick y más débil la luz solar, más minutos de exposición se necesitan. También depende de las partes del cuerpo expuestas, los tres factores afectan la dosis mínima de eritema (MED). [180] La sobredosis de vitamina D por exposición a rayos UV es imposible: la piel alcanza un equilibrio donde la vitamina D se degrada tan rápido como se crea. [30] [181]
La piel consta de dos capas principales: la capa interna llamada dermis y la epidermis externa, más delgada . La vitamina D se produce en los queratinocitos de los dos estratos más internos de la epidermis, el estrato basal y el estrato espinoso, que también pueden producir calcitriol y expresar el VDR. [182]
Evolución
La vitamina D solo se puede sintetizar mediante un proceso fotoquímico. Su producción a partir de esteroles habría comenzado muy temprano en la evolución de la vida alrededor del origen de la fotosíntesis , posiblemente ayudando a prevenir el daño al ADN al absorber la radiación UVB, convirtiendo a la vitamina D en un producto final inactivo. La conocida maquinaria endocrina de la vitamina D que contiene el receptor de vitamina D (VDR), varias enzimas CYP450 para la activación e inactivación y una proteína de unión a la vitamina D (DBP) se encuentra solo en vertebrados . Se cree que los vertebrados marinos primitivos absorben calcio del océano en sus esqueletos y comen plancton rico en vitamina D, aunque la función en aquellos que no tienen un cartílago calcificado no está clara. [183] El fitoplancton en el océano (como el cocolitóforo y la Emiliania huxleyi ) ha estado fotosintetizando vitamina D durante más de 500 millones de años.
Los vertebrados terrestres necesitaban otra fuente de vitamina D además de las plantas para sus esqueletos calcificados. Tenían que ingerirla o exponerse a la luz solar para realizar la fotosíntesis en su piel. [172] [175] Los vertebrados terrestres han estado fotosintetizando vitamina D durante más de 350 millones de años. [184]
En las aves y los mamíferos con pelaje, el pelo o las plumas impiden que los rayos UV lleguen a la piel. En cambio, la vitamina D se crea a partir de secreciones oleosas de la piel depositadas sobre las plumas o el pelaje, y se obtiene por vía oral durante el acicalamiento. [185] Sin embargo, algunos animales, como la rata topo desnuda , tienen una deficiencia natural de colecalciferol, ya que los niveles séricos de 25-OH vitamina D son indetectables. [186] Los perros y los gatos son prácticamente incapaces de sintetizar vitamina D debido a la alta actividad de la 7-dehidrocolesterol reductasa , pero obtienen vitamina D de los animales de presa. [187]
Síntesis industrial
La vitamina D 3 (colecalciferol) se produce industrialmente mediante la exposición del 7-dehidrocolesterol a la luz UVB y UVC, seguida de una purificación. [188] [138] El 7-dehidrocolesterol es una sustancia natural presente en los órganos de los peces, especialmente el hígado, [189] en la grasa de lana ( lanolina ) de las ovejas y en algunas plantas, [190] y en el liquen ( Cladonia rangiferina ). [191] [192] La vitamina D 2 (ergocalciferol) se produce de forma similar utilizando ergosterol de levaduras o de hongos como material de partida. [188] [138]
Mecanismo de acción
Activación metabólica

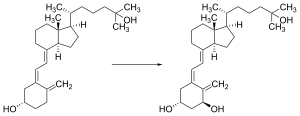
La vitamina D se transporta a través de la sangre hasta el hígado, donde se convierte en la prohormona calcifediol . El calcifediol circulante puede luego convertirse en calcitriol (la forma biológicamente activa de la vitamina D) en los riñones. [193]
Ya sea sintetizada en la piel o ingerida, la vitamina D se hidroxila en el hígado en la posición 25 (arriba a la derecha de la molécula) para formar 25-hidroxicolecalciferol (calcifediol o 25(OH)D). [3] Esta reacción es catalizada por la enzima microsomal vitamina D 25-hidroxilasa , el producto del gen humano CYP2R1 , y expresada por los hepatocitos . [194] Una vez elaborado, el producto se libera en el plasma , donde se une a una proteína transportadora de α-globulina llamada proteína de unión a la vitamina D. [ 195]
El calcifediol se transporta a los túbulos proximales de los riñones, donde se hidroxila en la posición 1-α (parte inferior derecha de la molécula) para formar calcitriol (1,25-dihidroxicolecalciferol, 1,25(OH) 2D ). [1] La conversión de calcifediol a calcitriol es catalizada por la enzima 25-hidroxivitamina D3 1 -alfa-hidroxilasa , que es el producto del gen humano CYP27B1 . [1] La actividad de CYP27B1 aumenta con la hormona paratiroidea y también con niveles bajos de calcio o fosfato. [1] Después del paso final de conversión en el riñón, el calcitriol se libera a la circulación. Al unirse a la proteína transportadora de vitamina D, el calcitriol se transporta por todo el cuerpo, incluido el intestino, los riñones y los huesos. [18] El calcitriol es el ligando natural más potente del receptor de vitamina D , que media la mayoría de las acciones fisiológicas de la vitamina D. [1] [193] Además de los riñones, el calcitriol también es sintetizado por ciertas otras células, incluidos los monocitos - macrófagos en el sistema inmunológico . Cuando es sintetizado por monocitos-macrófagos, el calcitriol actúa localmente como una citocina , modulando las defensas corporales contra invasores microbianos al estimular el sistema inmunológico innato . [193]
Inactivación
La actividad del calcifediol y del calcitriol puede reducirse por hidroxilación en la posición 24 por la vitamina D3 24-hidroxilasa , formando secalciferol y calcitetrol, respectivamente. [3]
Diferencia entre sustratos
La vitamina D 2 (ergocalciferol) y la vitamina D 3 (colecalciferol) comparten un mecanismo de acción similar al descrito anteriormente. [3] Los metabolitos producidos por la vitamina D 2 se nombran con un prefijo er- o ergo- para diferenciarlos de sus contrapartes basadas en D 3 (a veces con un prefijo chole- ). [17]
- Los metabolitos producidos a partir de la vitamina D2 tienden a unirse menos bien a la proteína transportadora de vitamina D. [3]
- La vitamina D 3 puede ser hidroxilada alternativamente a calcifediol por la esterol 27-hidroxilasa (CYP27A1), pero la vitamina D 2 no puede. [3]
- El ergocalciferol puede ser hidroxilado directamente en la posición 24 por CYP27A1 . [3] Esta hidroxilación también conduce a un mayor grado de inactivación: la actividad del calcitriol disminuye al 60% del original después de la 24-hidroxilación, [196] mientras que el ercalcitriol sufre una disminución de 10 veces en la actividad en la conversión a ercalcitetrol. [197]
Se discute si estas diferencias conducen a una caída mensurable de la eficacia (véase § Fortificación de alimentos).
Mecanismos intracelulares
El calcitriol entra en la célula diana y se une al receptor de vitamina D en el citoplasma. Este receptor activado entra en el núcleo y se une a los elementos de respuesta a la vitamina D (VDRE), que son secuencias de ADN específicas en los genes. [1] Se estimula la transcripción de estos genes y se producen mayores niveles de las proteínas que median los efectos de la vitamina D. [3]
Algunas reacciones de la célula al calcitriol parecen ser demasiado rápidas para la vía clásica de transcripción VDRE, lo que llevó al descubrimiento de varias acciones no genómicas de la vitamina D. El PDIA3 unido a la membrana probablemente sirva como un receptor alternativo en esta vía. [198] El VDR clásico todavía puede desempeñar un papel. [199]
Historia
La vitamina D fue descubierta en 1922 a raíz de investigaciones anteriores. [200] Los investigadores estadounidenses Elmer McCollum y Marguerite Davis en 1914 [11] descubrieron una sustancia en el aceite de hígado de bacalao que más tarde se llamó " vitamina A ". El médico británico Edward Mellanby notó que los perros alimentados con aceite de hígado de bacalao no desarrollaban raquitismo y concluyó que la vitamina A, o un factor estrechamente asociado, podía prevenir la enfermedad. En 1922, Elmer McCollum probó aceite de hígado de bacalao modificado en el que se había destruido la vitamina A. [11] El aceite modificado curó a los perros enfermos, por lo que McCollum concluyó que el factor en el aceite de hígado de bacalao que curaba el raquitismo era distinto de la vitamina A. Lo llamó vitamina D porque pensó que era la cuarta vitamina en ser nombrada. [201] [202] Inicialmente no se sabía que la vitamina D puede ser sintetizada por los humanos (en la piel) a través de la exposición a la luz ultravioleta y, por lo tanto, técnicamente no es una vitamina, sino que puede considerarse una hormona.
En 1925, [11] se estableció que cuando el 7-dehidrocolesterol se irradia con luz, se produce una forma de sustancia liposoluble (ahora conocida como D 3 ). Alfred Fabian Hess afirmó: "La luz es igual a vitamina D". [203] Adolf Windaus , de la Universidad de Göttingen en Alemania, recibió el Premio Nobel de Química en 1928 por su trabajo sobre la constitución de los esteroles y su conexión con las vitaminas. [204] En 1929, un grupo del NIMR en Hampstead, Londres, estaba trabajando en la estructura de la vitamina D, que todavía era desconocida, así como en la estructura de los esteroides. Se llevó a cabo una reunión con JBS Haldane , JD Bernal y Dorothy Crowfoot para discutir posibles estructuras, lo que contribuyó a formar un equipo. La cristalografía de rayos X demostró que las moléculas de esterol eran planas, no como lo propuso el equipo alemán dirigido por Windaus. En 1932, Otto Rosenheim y Harold King publicaron un artículo en el que proponían estructuras para esteroles y ácidos biliares que tuvo una aceptación inmediata. [205] La colaboración académica informal entre los miembros del equipo Robert Benedict Bourdillon , Otto Rosenheim, Harold King y Kenneth Callow fue muy productiva y condujo al aislamiento y caracterización de la vitamina D. [206] En ese momento, la política del Consejo de Investigación Médica era no patentar descubrimientos, creyendo que los resultados de la investigación médica deberían estar abiertos a todos. En la década de 1930, Windaus aclaró aún más la estructura química de la vitamina D. [207]
En 1923, el bioquímico estadounidense Harry Steenbock, de la Universidad de Wisconsin, demostró que la irradiación con luz ultravioleta aumentaba el contenido de vitamina D de los alimentos y otros materiales orgánicos. [208] Después de irradiar comida para roedores, Steenbock descubrió que los roedores se curaban del raquitismo. Con 300 dólares estadounidenses de su propio bolsillo, Steenbock patentó su invento. Su técnica de irradiación se utilizó para alimentos, sobre todo para la leche. Cuando expiró su patente en 1945, el raquitismo había sido prácticamente eliminado en los EE. UU. [209]
En 1969, se identificó una proteína de unión específica para la vitamina D llamada receptor de vitamina D. [210] Poco después, se confirmó la conversión de vitamina D en calcifediol y luego en calcitriol, la forma biológicamente activa. [9] [10] [211] La fotosíntesis de la vitamina D3 en la piel a través de la previtamina D3 y su posterior metabolismo se describió en 1980. [212]
Investigación
Existe evidencia contradictoria sobre los beneficios de las intervenciones con vitamina D. La suplementación de entre 800 y 1.000 UI es segura, pero niveles más altos que conducen a niveles sanguíneos de más de 50 ng/mL (125 nmol/L) pueden causar efectos adversos . [2] [213]
La Oficina de Suplementos Dietéticos de Estados Unidos estableció una Iniciativa de Vitamina D entre 2004 y 2018 para realizar un seguimiento de las investigaciones actuales y brindar educación a los consumidores. [214] A partir de 2022, el papel de la vitamina D en la prevención y el tratamiento de la diabetes , la intolerancia a la glucosa , la hipertensión , la esclerosis múltiple y otras afecciones médicas sigue siendo objeto de investigación preliminar. [2]
Algunos estudios preliminares vinculan los niveles bajos de vitamina D con enfermedades más adelante en la vida. [215] Un metanálisis encontró una disminución de la mortalidad en personas mayores. [12] Otro metanálisis que abarcó a más de 350.000 personas concluyó que la suplementación con vitamina D en individuos no seleccionados que viven en la comunidad no reduce los resultados esqueléticos (fractura total) o no esqueléticos (infarto de miocardio, cardiopatía isquémica, accidente cerebrovascular, enfermedad cerebrovascular, cáncer) en más del 15%, y que es poco probable que futuros ensayos de investigación con un diseño similar cambien estas conclusiones. [14] A partir de 2022, no hay evidencia suficiente de un efecto de la suplementación con vitamina D sobre el riesgo de cáncer. [2] [216] [217] Un metanálisis de 2019 encontró un pequeño aumento en el riesgo de accidente cerebrovascular cuando se tomaron suplementos de calcio y vitamina D juntos. [218]
COVID-19
A partir de septiembre de 2022, [actualizar]los Institutos Nacionales de Salud de EE. UU. afirman que no hay evidencia suficiente para recomendar o no el uso de suplementos de vitamina D para prevenir o tratar la COVID-19. [219] El Instituto Nacional para la Excelencia en la Salud y la Atención (NICE) del Reino Unido no recomienda ofrecer un suplemento de vitamina D a las personas únicamente para prevenir o tratar la COVID-19. [220] [221] Ambas organizaciones incluyeron recomendaciones para continuar con las recomendaciones establecidas previamente sobre la suplementación con vitamina D por otras razones, como la salud ósea y muscular, según corresponda. Ambas organizaciones señalaron que más personas pueden requerir suplementos debido a una menor cantidad de exposición al sol durante la pandemia. [219] [220]
Varias revisiones sistemáticas y metanálisis de múltiples estudios han descrito las asociaciones de la deficiencia de vitamina D con resultados adversos en COVID-19. [222] [223] [224] [225] [226] [227] En el análisis más grande, con datos de 76 estudios observacionales que incluyeron casi dos millones de adultos, la deficiencia o insuficiencia de vitamina D aumentó significativamente la susceptibilidad a infectarse con COVID-19 y tener COVID-19 grave, con razones de probabilidades de 1,5 y 1,9 respectivamente, pero estos hallazgos tuvieron un alto riesgo de sesgo y heterogeneidad. Se encontró una mortalidad dos veces mayor, pero este análisis fue menos sólido. [227] Estos hallazgos confirman análisis más pequeños y anteriores, [223] [224] [225] [226] uno de los cuales, al informar que las personas con COVID-19 tienden a tener niveles más bajos de 25(OH)D que los sujetos sanos, afirmó que la tendencia de las asociaciones con los resultados de salud estaba limitada por la baja calidad de los estudios y por la posibilidad de mecanismos de causalidad inversa. [225]
Un metaanálisis de tres estudios sobre el efecto de la suplementación oral con vitamina D o calcifediol indicó una tasa de admisión a la unidad de cuidados intensivos (UCI) más baja ( odds ratio : 0,36) en comparación con los que no recibieron suplementación, pero sin un cambio en la mortalidad. [228] Una revisión Cochrane, también de tres estudios, encontró que la evidencia de la efectividad de la suplementación con vitamina D para el tratamiento de COVID-19 es muy incierta. [229] Encontraron que había una heterogeneidad clínica y metodológica sustancial en los tres estudios que se incluyeron, principalmente debido a diferentes estrategias de suplementación, formulaciones de vitamina D (una que usa calcifediol), estado previo al tratamiento y resultados informados. [229] Otro metaanálisis afirmó que el uso de altas dosis de vitamina D en personas con COVID-19 no se basa en evidencia sólida, aunque la suplementación con calcifediol puede tener un efecto protector en las admisiones a la UCI. [225]
Otros animales
Pez
Los peces no sintetizan vitamina D en un entorno natural y dependen de fuentes dietéticas. Al igual que en los mamíferos, la vitamina D3 es más biodisponible que la vitamina D2 . [ 230] A diferencia de los mamíferos, ambos pasos de hidroxilación de la vitamina D3 a la forma activa 1,25 hidroxivitamina D3 ocurren en el hígado, por lo que los niveles plasmáticos de 25 hidroxivitamina D3 no son una medida precisa de los niveles de vitamina D3 . [ 230]
Referencias
- ^ abcdefghijklmnopqrstu vw «Vitamina D». Centro de Información sobre Micronutrientes, Instituto Linus Pauling, Universidad Estatal de Oregón, Corvallis. 11 de febrero de 2021. Archivado desde el original el 8 de abril de 2015. Consultado el 14 de marzo de 2022 .
- ^ abcdefghijklmnopq «Vitamina D». Oficina de Suplementos Dietéticos, Institutos Nacionales de Salud de EE. UU. 12 de agosto de 2022. Archivado desde el original el 9 de abril de 2021 . Consultado el 22 de febrero de 2022 .
- ^ abcdefghijkl Bikle DD (marzo de 2014). "Metabolismo de la vitamina D, mecanismo de acción y aplicaciones clínicas". Química y biología . 21 (3): 319–29. doi :10.1016/j.chembiol.2013.12.016. PMC 3968073 . PMID 24529992.
- ^ Lehmann U, Gjessing HR, Hirche F, Mueller-Belecke A, Gudbrandsen OA, Ueland PM, et al. (octubre de 2015). "Eficacia de la ingesta de pescado en el estado de vitamina D: un metaanálisis de ensayos controlados aleatorizados". The American Journal of Clinical Nutrition . 102 (4): 837–47. doi : 10.3945/ajcn.114.105395 . PMID 26354531.
- ^ Cardwell, Glenn et al. “Una revisión de los hongos como una fuente potencial de vitamina D en la dieta”. Nutrients vol. 10,10 1498. 13 de octubre de 2018, doi:10.3390/nu10101498
- ^ Norman AW (agosto de 2008). "De la vitamina D a la hormona D: fundamentos del sistema endocrino de la vitamina D esencial para una buena salud". The American Journal of Clinical Nutrition . 88 (2): 491S–9S. doi : 10.1093/ajcn/88.2.491S . PMID 18689389.
- ^ "Pruebas de vitamina D". Lab Tests Online (Estados Unidos) . Asociación Estadounidense de Química Clínica. Archivado desde el original el 7 de noviembre de 2017. Consultado el 23 de junio de 2013 .
- ^ Hollis BW (enero de 1996). "Evaluación del estado nutricional y hormonal de la vitamina D: qué medir y cómo hacerlo". Calcified Tissue International . 58 (1): 4–5. doi :10.1007/BF02509538. PMID 8825231. S2CID 35887181.
- ^ ab Holick MF, Schnoes HK, DeLuca HF (abril de 1971). "Identificación de 1,25-dihidroxicolecalciferol, una forma de vitamina D3 metabólicamente activa en el intestino". Actas de la Academia Nacional de Ciencias de los Estados Unidos de América . 68 (4): 803–4. Bibcode :1971PNAS...68..803H. doi : 10.1073/pnas.68.4.803 . PMC 389047 . PMID 4323790.
- ^ ab Norman AW, Myrtle JF, Midgett RJ, Nowicki HG, Williams V, Popják G (julio de 1971). "1,25-dihidroxicolecalciferol: identificación de la forma activa propuesta de vitamina D 3 en el intestino". Science . 173 (3991): 51–4. Bibcode :1971Sci...173...51N. doi :10.1126/science.173.3991.51. PMID 4325863. S2CID 35236666.
- ^ abcd Wolf G (junio de 2004). "El descubrimiento de la vitamina D: la contribución de Adolf Windaus". The Journal of Nutrition . 134 (6): 1299–302. doi : 10.1093/jn/134.6.1299 . PMID 15173387.
- ^ abcd Bjelakovic G, Gluud LL, Nikolova D, Whitfield K, Wetterslev J, Simonetti RG, et al. (enero de 2014). "Suplementación con vitamina D para la prevención de la mortalidad en adultos". Base de datos Cochrane de revisiones sistemáticas (revisión sistemática). 1 (1): CD007470. doi : 10.1002 /14651858.CD007470.pub3. PMC 11285307. PMID 24414552.
- ^ ab Reid IR, Bolland MJ, Grey A (enero de 2014). "Efectos de los suplementos de vitamina D en la densidad mineral ósea: una revisión sistemática y un metanálisis". Lancet . 383 (9912): 146–55. doi :10.1016/s0140-6736(13)61647-5. PMID 24119980. S2CID 37968189.
- ^ abcdef Bolland MJ, Grey A, Gamble GD, Reid IR (abril de 2014). "El efecto de la suplementación con vitamina D en los resultados óseos, vasculares o oncológicos: un metanálisis secuencial de ensayos". The Lancet. Diabetes & Endocrinology (Metaanálisis). 2 (4): 307–20. doi :10.1016/S2213-8587(13)70212-2. PMID 24703049.
- ^ "The Lancet Diabetes & Endocrinology: La suplementación con vitamina D en adultos no previene fracturas, caídas ni mejora la densidad mineral ósea". EurekAlert! . Archivado desde el original el 24 de marzo de 2022 . Consultado el 23 de febrero de 2022 .
Los autores concluyen que, por lo tanto, hay pocas razones para utilizar suplementos de vitamina D para mantener o mejorar la salud musculoesquelética, excepto para la prevención de enfermedades raras como el raquitismo y la osteomalacia en grupos de alto riesgo, que pueden ser causadas por la deficiencia de vitamina D después de una larga falta de exposición a la luz solar.
- ^ Alayed Albarri EM, Sameer Alnuaimi A, Abdelghani D (4 de agosto de 2022). "Eficacia de la terapia de reemplazo de vitamina D2 en comparación con la vitamina D3 en un entorno de atención primaria: un estudio de cohorte retrospectivo". Qatar Medical Journal . 2022 (3): 29. doi :10.5339/qmj.2022.35. ISSN 0253-8253. PMC 9372493 . PMID 35974883.
La vitamina D es una vitamina liposoluble que consta de vitamina D2 (ergocalciferol) y vitamina D3 (colecalciferol).
- ^ ab "IUPAC-IUB Joint Commission on Biochemical Nomenclature (JCBN): Nomenclatura de la vitamina D. Recomendaciones 1981". Revista Europea de Bioquímica . 124 (2): 223–7. Mayo de 1982. doi : 10.1111/j.1432-1033.1982.tb06581.x . PMID 7094913.
- ^ abc Fleet JC, Shapses SA (2020). "Vitamina D". En BP Marriott, DF Birt, VA Stallings, AA Yates (eds.). Present Knowledge in Nutrition, undécima edición . Londres, Reino Unido: Academic Press (Elsevier). págs. 93–114. ISBN 978-0-323-66162-1.
- ^ Boron WF, Boulpaep EL (29 de marzo de 2016). Fisiología médica, libro electrónico. Elsevier Health Sciences. ISBN 978-1-4557-3328-6Archivado desde el original el 19 de marzo de 2023 . Consultado el 9 de abril de 2017 .
- ^ Bouillon R, Van Cromphaut S, Carmeliet G (febrero de 2003). "Absorción intestinal de calcio: mecanismos mediados por la vitamina D molecular". Journal of Cellular Biochemistry . 88 (2): 332–9. doi :10.1002/jcb.10360. PMID 12520535. S2CID 9853381.
- ^ abc Holick MF (diciembre de 2004). "Luz solar y vitamina D para la salud ósea y la prevención de enfermedades autoinmunes, cánceres y enfermedades cardiovasculares". The American Journal of Clinical Nutrition . 80 (6 Suppl): 1678S–88S. doi : 10.1093/ajcn/80.6.1678S . PMID 15585788.
- ^ ab Bell TD, Demay MB, Burnett-Bowie SA (septiembre de 2010). "La biología y patología del control de la vitamina D en los huesos". Journal of Cellular Biochemistry . 111 (1): 7–13. doi :10.1002/jcb.22661. PMC 4020510 . PMID 20506379.
- ^ Watkins RR, Lemonovich TL, Salata RA (mayo de 2015). "Una actualización sobre la asociación de la deficiencia de vitamina D con enfermedades infecciosas comunes". Revista Canadiense de Fisiología y Farmacología . 93 (5): 363–8. doi :10.1139/cjpp-2014-0352. PMID 25741906.
- ^ Puchacz E, Stumpf WE, Stachowiak EK, Stachowiak MK (febrero de 1996). "La vitamina D aumenta la expresión del gen de la tirosina hidroxilasa en las células de la médula suprarrenal". Investigación cerebral. Investigación cerebral molecular . 36 (1): 193–6. doi :10.1016/0169-328X(95)00314-I. PMID 9011759.
- ^ ab Holick MF, Binkley NC, Bischoff-Ferrari HA, Gordon CM, Hanley DA, Heaney RP, et al. (julio de 2011). "Evaluación, tratamiento y prevención de la deficiencia de vitamina D: una guía de práctica clínica de la Endocrine Society". The Journal of Clinical Endocrinology and Metabolism . 96 (7): 1911–30. doi : 10.1210/jc.2011-0385 . PMID 21646368.
- ^ Cashman KD, Dowling KG, Škrabáková Z, Gonzalez-Gross M, Valtueña J, De Henauw S, et al. (abril de 2016). "Deficiencia de vitamina D en Europa: ¿pandemia?". The American Journal of Clinical Nutrition . 103 (4): 1033–44. doi :10.3945/ajcn.115.120873. PMC 5527850 . PMID 26864360.
- ^ "Raquitismo". Servicio Nacional de Salud . 8 de marzo de 2012. Archivado desde el original el 11 de octubre de 2017. Consultado el 9 de julio de 2012 .
- ^ Munns CF, Shaw N, Kiely M, Specker BL, Thacher TD, Ozono K, et al. (febrero de 2016). "Recomendaciones de consenso mundial sobre la prevención y el tratamiento del raquitismo nutricional". Revista de endocrinología clínica y metabolismo . 101 (2): 394–415. doi :10.1210/jc.2015-2175. PMC 4880117. PMID 26745253 .
- ^ Eriksen EF, Glerup H (2002). "Deficiencia de vitamina D y envejecimiento: implicaciones para la salud general y la osteoporosis". Biogerontología . 3 (1–2): 73–7. doi :10.1023/A:1015263514765. PMID 12014847. S2CID 22112344.
- ^ abcdefg Holick MF (julio de 2007). "Deficiencia de vitamina D". The New England Journal of Medicine . 357 (3): 266–81. doi :10.1056/NEJMra070553. PMID 17634462. S2CID 18566028.
- ^ abcd Brown JE, Isaacs J, Krinke B, Lechtenberg E, Murtaugh M (28 de junio de 2013). Nutrición a lo largo del ciclo vital. Aprendizaje Cengage. ISBN 978-1-285-82025-5Archivado desde el original el 19 de marzo de 2023 . Consultado el 9 de abril de 2017 .
- ^ Schoenmakers I, Goldberg GR, Prentice A (junio de 2008). "Abundante luz solar y deficiencia de vitamina D". The British Journal of Nutrition . 99 (6): 1171–3. doi :10.1017/S0007114508898662. PMC 2758994 . PMID 18234141.
- ^ Lowe NM, Bhojani I (junio de 2017). "Consideraciones especiales sobre la vitamina D en la población del sur de Asia en el Reino Unido". Avances terapéuticos en enfermedades musculoesqueléticas . 9 (6): 137–44. doi :10.1177/1759720X17704430. PMC 5466148. PMID 28620422 .
- ^ O'Connor MY, Thoreson CK, Ramsey NL, Ricks M, Sumner AE (2013). "El significado incierto de los niveles bajos de vitamina D en poblaciones de ascendencia africana: una revisión de la literatura sobre huesos y cardiometabólica". Progreso en enfermedades cardiovasculares . 56 (3): 261–9. doi :10.1016/j.pcad.2013.10.015. PMC 3894250 . PMID 24267433.
- ^ ab Freedman BI, Register TC (junio de 2012). "Efecto de la raza y la genética en el metabolismo de la vitamina D, la salud ósea y vascular". Nature Reviews. Nephrology . 8 (8): 459–66. doi :10.1038/nrneph.2012.112. PMC 10032380 . PMID 22688752. S2CID 29026212.
- ^ Khalid AT, Moore CG, Hall C, Olabopo F, Rozario NL, Holick MF, et al. (septiembre de 2017). "Utilidad de la tipificación de piel reactiva al sol y del índice de melanina para discernir la deficiencia de vitamina D". Pediatric Research . 82 (3): 444–51. doi :10.1038/pr.2017.114. PMC 5570640 . PMID 28467404.
- ^ abc Ben-Eltriki M, Gayle EJ, Paras JM, Nyame-Addo L, Chhabra M, Deb S (abril de 2024). "Vitamina D en el melanoma: posible función de las enzimas del citocromo P450". Life . 14 (4): 510. Bibcode :2024Life...14..510B. doi : 10.3390/life14040510 . PMC 11050855 . PMID 38672780. Este artículo incorpora texto de esta fuente, que está disponible bajo la licencia CC BY 4.0.
- ^ ab Wagner CL, Greer FR (noviembre de 2008). "Prevención del raquitismo y la deficiencia de vitamina D en lactantes, niños y adolescentes". Pediatría . 122 (5): 1142–52. doi :10.1542/peds.2008-1862. PMID 18977996. S2CID 342161.
- ^ Lerch C, Meissner T (octubre de 2007). Lerch C (ed.). "Intervenciones para la prevención del raquitismo nutricional en niños nacidos a término". Base de datos Cochrane de revisiones sistemáticas . 2010 (4): CD006164. doi :10.1002/14651858.CD006164.pub2. PMC 8990776. PMID 17943890 .
- ^ Zargar AH, Mithal A, Wani AI, Laway BA, Masoodi SR, Bashir MI, et al. (junio de 2000). "Raquitismo por deficiencia de pseudovitamina D: un informe del subcontinente indio". Revista Médica de Postgrado . 76 (896): 369–72. doi : 10.1136/pmj.76.896.369. PMC 1741602 . PMID 10824056.
- ^ Elidrissy AT (septiembre de 2016). "El regreso del raquitismo congénito: ¿estamos pasando por alto casos ocultos?". Calcified Tissue International (Revisión). 99 (3): 227–36. doi :10.1007/s00223-016-0146-2. PMID 27245342. S2CID 14727399.
- ^ Paterson CR, Ayoub D (octubre de 2015). "Raquitismo congénito debido a deficiencia de vitamina D en las madres". Nutrición clínica (revisión). 34 (5): 793–8. doi :10.1016/j.clnu.2014.12.006. PMID 25552383.
- ^ Oramasionwu GE, Thacher TD, Pam SD, Pettifor JM, Abrams SA (agosto de 2008). "Adaptación de la absorción de calcio durante el tratamiento del raquitismo nutricional en niños nigerianos" (PDF) . The British Journal of Nutrition . 100 (2): 387–92. doi : 10.1017/S0007114507901233 . PMID: 18197991. S2CID : 15406992.
- ^ Fischer PR, Rahman A, Cimma JP, Kyaw-Myint TO, Kabir AR, Talukder K, et al. (octubre de 1999). "Raquitismo nutricional sin deficiencia de vitamina D en Bangladesh". Journal of Tropical Pediatrics . 45 (5): 291–3. doi : 10.1093/tropej/45.5.291 . PMID 10584471.
- ^ ab Dunnigan MG, Henderson JB (noviembre de 1997). "Un modelo epidemiológico del raquitismo y la osteomalacia por privación". Actas de la Sociedad de Nutrición . 56 (3): 939–56. doi : 10.1079/PNS19970100 . PMID 9483661.
- ^ Robertson I, Ford JA, McIntosh WB, Dunnigan MG (enero de 1981). "El papel de los cereales en la etiología del raquitismo nutricional: la lección de la Encuesta Nacional de Nutrición Irlandesa 1943-8". The British Journal of Nutrition . 45 (1): 17–22. doi : 10.1079/BJN19810073 . PMID 6970590.
- ^ Clements MR (1989). "El problema del raquitismo en los asiáticos del Reino Unido". Revista de nutrición humana y dietética . 2 (2): 105–16. doi :10.1111/j.1365-277X.1989.tb00015.x.
- ^ ab Pettifor JM (diciembre de 2004). "Raquitismo nutricional: ¿deficiencia de vitamina D, calcio o ambos?". The American Journal of Clinical Nutrition . 80 (6 Suppl): 1725S–9S. doi : 10.1093/ajcn/80.6.1725S . PMID 15585795.
- ^ ab Dunnigan MG, Henderson JB, Hole DJ, Barbara Mawer E, Berry JL (diciembre de 2005). "El consumo de carne reduce el riesgo de raquitismo nutricional y osteomalacia". The British Journal of Nutrition . 94 (6): 983–91. doi : 10.1079/BJN20051558 . PMID 16351777.
- ^ Weick MT (noviembre de 1967). "Una historia del raquitismo en los Estados Unidos". The American Journal of Clinical Nutrition . 20 (11): 1234–41. doi : 10.1093/ajcn/20.11.1234 . PMID 4862158.
- ^ Garrison RH, Somer E (1997). Referencia nutricional. McGraw-Hill. ISBN 978-0-87983-826-3Archivado desde el original el 19 de marzo de 2023 . Consultado el 9 de abril de 2017 .
- ^ Dupuis EM (1 de febrero de 2002). El alimento perfecto de la naturaleza: cómo la leche se convirtió en la bebida de Estados Unidos. NYU Press. ISBN 978-0-8147-1938-1Archivado desde el original el 19 de marzo de 2023 . Consultado el 9 de abril de 2017 .
- ^ Teegarden D, Lyle RM, Proulx WR, Johnston CC, Weaver CM (mayo de 1999). "El consumo previo de leche se asocia con una mayor densidad ósea en mujeres jóvenes". The American Journal of Clinical Nutrition . 69 (5): 1014–7. doi : 10.1093/ajcn/69.5.1014 . PMID 10232644.
- ^ Holick MF (marzo de 2006). "Alta prevalencia de deficiencia de vitamina D e implicaciones para la salud". Mayo Clinic Proceedings . 81 (3): 353–73. doi : 10.4065/81.3.353 . PMID 16529140.
- ^ Straube S, Andrew Moore R, Derry S, McQuay HJ (enero de 2009). "Vitamina D y dolor crónico". Pain . 141 (1–2): 10–3. doi :10.1016/j.pain.2008.11.010. PMID 19084336. S2CID 17244398.
- ^ Gaikwad M, Vanlint S, Mittinity M, Moseley GL, Stocks N (mayo de 2017). "¿La suplementación con vitamina D alivia el dolor musculoesquelético crónico inespecífico? Una revisión sistemática y un metanálisis". Reumatología clínica . 36 (5): 1201–08. doi :10.1007/s10067-016-3205-1. PMID 26861032. S2CID 30189971.
- ^ Chung M, Balk EM, Brendel M, Ip S, Lau J, Lee J, et al. (agosto de 2009). "Vitamina D y calcio: una revisión sistemática de los resultados de salud". Informe de evidencia/evaluación de tecnología (183): 1–420. PMC 4781105 . PMID 20629479.
- ^ Theodoratou E, Tzoulaki I, Zgaga L, Ioannidis JP (abril de 2014). "Vitamina D y múltiples resultados de salud: revisión general de revisiones sistemáticas y metanálisis de estudios observacionales y ensayos aleatorizados". BMJ . 348 : g2035. doi :10.1136/bmj.g2035. PMC 3972415 . PMID 24690624.
- ^ ab Autier P, Boniol M, Pizot C, Mullie P (enero de 2014). "Estado de vitamina D y mala salud: una revisión sistemática". The Lancet. Diabetes & Endocrinology . 2 (1): 76–89. doi :10.1016/S2213-8587(13)70165-7. PMID 24622671.
- ^ Hussain S, Singh A, Akhtar M, Najmi AK (septiembre de 2017). "Suplementación con vitamina D para el tratamiento de la osteoartritis de rodilla: una revisión sistemática de ensayos controlados aleatorizados". Reumatología Internacional . 37 (9): 1489–98. doi :10.1007/s00296-017-3719-0. PMID 28421358. S2CID 23994681.
- ^ abcdefghijk Instituto de Medicina (2011). "8, Implicaciones y preocupaciones especiales". En Ross AC, Taylor CL, Yaktine AL, Del Valle HB (eds.). Ingesta dietética de referencia de calcio y vitamina D. Colección de las Academias Nacionales: informes financiados por los Institutos Nacionales de Salud. National Academies Press. doi :10.17226/13050. ISBN 978-0-309-16394-1. PMID 21796828. S2CID 58721779. Archivado desde el original el 26 de enero de 2021 . Consultado el 17 de septiembre de 2017 .
- ^ ab Maxmen A (julio de 2011). «Consejos nutricionales: el lema de la vitamina D» (PDF) . Nature . 475 (7354): 23–5. doi : 10.1038/475023a . PMID 21734684. Archivado (PDF) del original el 3 de agosto de 2020. Consultado el 17 de noviembre de 2011 .
- ^ Schöttker B, Jorde R, Peasey A, Thorand B, Jansen EH, Groot L, et al. (Consorcio sobre envejecimiento saludable: Red de cohortes en Europa y Estados Unidos) (junio de 2014). "Vitamina D y mortalidad: metaanálisis de datos de participantes individuales de un gran consorcio de estudios de cohorte de Europa y Estados Unidos". BMJ . 348 (junio de 2016): g3656. doi :10.1136/bmj.g3656. PMC 4061380 . PMID 24938302.
- ^ Tuohimaa P (marzo de 2009). "Vitamina D y envejecimiento". Revista de bioquímica de esteroides y biología molecular . 114 (1–2): 78–84. doi :10.1016/j.jsbmb.2008.12.020. PMID 19444937. S2CID 40625040.
- ^ Tuohimaa P, Keisala T, Minasyan A, Cachat J, Kalueff A (diciembre de 2009). "Vitamina D, sistema nervioso y envejecimiento". Psiconeuroendocrinología . 34 (Supl 1): S278–86. doi :10.1016/j.psyneuen.2009.07.003. PMID 19660871. S2CID 17462970.
- ^ Manya H, Akasaka-Manya K, Endo T (julio de 2010). "Deficiencia de proteína Klotho y envejecimiento". Geriatrics & Gerontology International . 10 (Supl 1): S80-7. doi : 10.1111/j.1447-0594.2010.00596.x . PMID 20590845. S2CID 36692930.
- ^ Avenell A, Mak JC, O'Connell D (abril de 2014). "Vitamina D y análogos de vitamina D para la prevención de fracturas en mujeres posmenopáusicas y hombres mayores". Base de datos Cochrane de revisiones sistemáticas . 4 (4): CD000227. doi :10.1002/14651858.CD000227.pub4. PMC 7032685. PMID 24729336 .
- ^ Bischoff-Ferrari HA, Willett WC, Orav EJ, Oray EJ, Lips P, Meunier PJ, et al. (julio de 2012). "Un análisis agrupado de los requisitos de dosis de vitamina D para la prevención de fracturas" (PDF) . The New England Journal of Medicine . 367 (1): 40–9. doi :10.1056/NEJMoa1109617. hdl :1871/48765. PMID 22762317. S2CID 24338997. Archivado (PDF) del original el 15 de diciembre de 2020 . Consultado el 17 de julio de 2019 .
- ^ Chung M, Lee J, Terasawa T, Lau J, Trikalinos TA (diciembre de 2011). "Vitamina D con o sin suplementos de calcio para la prevención del cáncer y las fracturas: un metanálisis actualizado para el Grupo de Trabajo de Servicios Preventivos de EE. UU." Anales de Medicina Interna . 155 (12): 827–38. doi :10.7326/0003-4819-155-12-201112200-00005. PMID 22184690. S2CID 22380502.
- ^ Zhao JG, Zeng XT, Wang J, Liu L (diciembre de 2017). "Asociación entre la suplementación con calcio o vitamina D y la incidencia de fracturas en adultos mayores que viven en la comunidad: una revisión sistemática y un metanálisis". JAMA . 318 (24): 2466–2482. doi :10.1001/jama.2017.19344. PMC 5820727 . PMID 29279934.
- ^ Cranney A, Horsley T, O'Donnell S, Weiler H, Puil L, Ooi D, et al. (agosto de 2007). "Eficacia y seguridad de la vitamina D en relación con la salud ósea". Informe de evidencia/evaluación tecnológica (158): 1–235. PMC 4781354. PMID 18088161 .
- ^ Bolland MJ, Grey A, Gamble GD, Reid IR (julio de 2014). "Suplementación con vitamina D y caídas: un metanálisis secuencial de ensayos". The Lancet. Diabetes & Endocrinology . 2 (7): 573–80. doi :10.1016/S2213-8587(14)70068-3. PMID 24768505.
- ^ Shuler FD, Wingate MK, Moore GH, Giangarra C (noviembre de 2012). "Beneficios de la vitamina D para la salud deportiva". Salud deportiva . 4 (6): 496–501. doi :10.1177/1941738112461621. PMC 3497950. PMID 24179588 .
- ^ Chibuzor MT, Graham-Kalio D, Osaji JO, Meremikwu MM, et al. (Grupo Cochrane de Trastornos Metabólicos y Endocrinos) (abril de 2020). "Vitamina D, calcio o una combinación de vitamina D y calcio para el tratamiento del raquitismo nutricional en niños". Base de Datos Cochrane de Revisiones Sistemáticas . 2020 (4): CD012581. doi :10.1002/14651858.CD012581.pub2. PMC 7164979. PMID 32303107 .
- ^ ab "Cambios en la etiqueta de información nutricional". Administración de Alimentos y Medicamentos de Estados Unidos (FDA) . 27 de mayo de 2016. Archivado desde el original el 6 de mayo de 2018. Consultado el 16 de mayo de 2020 .
 Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público .
Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público . - ^ Zhao Y, Chen C, Pan W, Gao M, He W, Mao R, et al. (mayo de 2016). "Eficacia comparativa del estado de vitamina D en la reducción del riesgo de cáncer de vejiga: una revisión sistemática y un metanálisis en red". Nutrition . 32 (5): 515–523. doi :10.1016/j.nut.2015.10.023. PMID 26822497.
- ^ ab Hernández-Alonso P, Boughanem H, Canudas S, Becerra-Tomás N, Fernández de la Puente M, Babio N, et al. (julio de 2021). "Niveles circulantes de vitamina D y riesgo de cáncer colorrectal: un metaanálisis y una revisión sistemática de estudios de casos y controles y de cohorte prospectiva". Critical Reviews in Food Science and Nutrition . 63 (1): 1–17. doi :10.1080/10408398.2021.1939649. hdl : 10609/136992 . PMID 34224246. S2CID 235746547.
- ^ ab Sluyter JD, Manson JE, Scragg R (enero de 2021). "Vitamina D y resultados clínicos del cáncer: una revisión de metanálisis". JBMR Plus . 5 (1): e10420. doi :10.1002/jbm4.10420. PMC 7839823 . PMID 33553987.
- ^ Seraphin G, Rieger S, Hewison M, Capobianco E, Lisse TS (julio de 2023). "El impacto de la vitamina D en el cáncer: una mini revisión". J Steroid Biochem Mol Biol . 231 : 106308. doi :10.1016/j.jsbmb.2023.106308. PMC 10330295. PMID 37054849 .
- ^ Keum N, Lee DH, Greenwood DC, Manson JE, Giovannucci E (mayo de 2019). "Suplementación con vitamina D e incidencia y mortalidad total por cáncer: un metaanálisis de ensayos controlados aleatorizados". Anales de Oncología . 30 (5): 733–743. doi :10.1093/annonc/mdz059. PMC 6821324 . PMID 30796437.
- ^ Barbarawi M, Kheiri B, Zayed Y, Barbarawi O, Dhillon H, Swaid B, et al. (agosto de 2019). "Suplementación con vitamina D y riesgos de enfermedad cardiovascular en más de 83 000 personas en 21 ensayos clínicos aleatorizados: un metanálisis". JAMA Cardiology . 4 (8): 765–76. doi :10.1001/jamacardio.2019.1870. PMC 6584896 . PMID 31215980.
- ^ Nudy M, Krakowski G, Ghahramani M, Ruzieh M, Foy AJ (2020). "Suplementación con vitamina D, eventos cardíacos y accidente cerebrovascular: una revisión sistemática y un análisis de metarregresión". Int J Cardiol Heart Vasc . 28 : 100537. doi :10.1016/j.ijcha.2020.100537. PMC 7240168 . PMID 32462077.
- ^ Beveridge LA, Struthers AD, Khan F, Jorde R, Scragg R, Macdonald HM, et al. (mayo de 2015). "Efecto de la suplementación con vitamina D en la presión arterial: una revisión sistemática y un metanálisis que incorpora datos de pacientes individuales". JAMA Internal Medicine . 175 (5): 745–54. doi :10.1001/jamainternmed.2015.0237. PMC 5966296 . PMID 25775274.
- ^ Zhang D, Cheng C, Wang Y, Sun H, Yu S, Xue Y, et al. (2020). "Efecto de la vitamina D sobre la presión arterial y la hipertensión en la población general: un metaanálisis actualizado de estudios de cohorte y ensayos controlados aleatorizados". Prev Chronic Dis . 17 : E03. doi :10.5888/pcd17.190307. PMC 6977781 . PMID 31922371.
- ^ Abboud M, Al Anouti F, Papandreou D (2021). "Estado de la vitamina D y presión arterial en niños y adolescentes: una revisión sistemática de estudios observacionales". Revisiones sistemáticas . 10 (1): 60. doi : 10.1186/s13643-021-01584-x . PMC 7898425 . PMID 33618764.
- ^ Hewison M (2011). "Vitamina D e inmunidad innata y adaptativa". Vitaminas y sistema inmunitario . Vitaminas y hormonas. Vol. 86. Academic Press. págs. 23–62. doi :10.1016/B978-0-12-386960-9.00002-2. ISBN . 978-0-12-386960-9. Número de identificación personal 21419266.
- ^ Bishop E, Ismailova A, Dimeloe SK, Hewison M, White JH (agosto de 2020). "Vitamina D y regulación inmunitaria: antibacteriana, antiviral, antiinflamatoria". JBMR Plus . 5 (1): e10405. doi :10.1002/jbm4.10405. PMC 7461279 . PMID 32904944.
- ^ Nnoaham KE, Clarke A (febrero de 2008). "Niveles séricos bajos de vitamina D y tuberculosis: una revisión sistemática y un metanálisis". Revista Internacional de Epidemiología . 37 (1): 113–9. CiteSeerX 10.1.1.513.3969 . doi :10.1093/ije/dym247. PMID 18245055.
- ^ Luong K, Nguyen LT (junio de 2011). "Impacto de la vitamina D en el tratamiento de la tuberculosis". The American Journal of the Medical Sciences . 341 (6): 493–8. doi :10.1097/MAJ.0b013e3182070f47. PMID 21289501. S2CID 18802134.
- ^ ab "Revisión rápida de SACN: vitamina D e infecciones agudas del tracto respiratorio". Public Health England . Archivado desde el original el 14 de enero de 2021. Consultado el 6 de enero de 2021 .
- ^ Jolliffe DA, Greenberg L, Hooper RL, Mathyssen C, Rafiq R, de Jongh RT, et al. (abril de 2019). "Vitamina D para prevenir las exacerbaciones de la EPOC: revisión sistemática y metanálisis de datos de participantes individuales de ensayos controlados aleatorizados". Thorax . 74 (4): 337–345. doi : 10.1136/thoraxjnl-2018-212092 . PMID 30630893. S2CID 58548871.
- ^ Williamson A, Martineau AR, Sheikh A, Jolliffe D, Griffiths CJ (febrero de 2023). "Vitamina D para el tratamiento del asma". Cochrane Database Syst Rev. 2023 ( 2): CD011511. doi :10.1002 / 14651858.CD011511.pub3. PMC 9899558. PMID 36744416.
- ^ Del Pinto R, Pietropaoli D, Chandar AK, Ferri C, Cominelli F (noviembre de 2015). "Asociación entre la enfermedad inflamatoria intestinal y la deficiencia de vitamina D: una revisión sistemática y un metanálisis". Enfermedades inflamatorias intestinales . 21 (11): 2708–2717. doi :10.1097/MIB.0000000000000546. PMC 4615394 . PMID 26348447.
- ^ abcde Wallace C, Gordon M, Sinopoulou V, Limketkai BN, et al. (Grupo Cochrane de Intestinos) (octubre de 2023). "Vitamina D para el tratamiento de la enfermedad inflamatoria intestinal". Base de Datos Cochrane de Revisiones Sistemáticas . 2023 (10): CD011806. doi :10.1002/14651858.CD011806.pub2. PMC 10542962. PMID 37781953 .
- ^ Guzman-Prado Y, Samson O, Segal JP, Limdi JK, Hayee B (mayo de 2020). "Terapia con vitamina D en adultos con enfermedad inflamatoria intestinal: una revisión sistemática y un metanálisis". Enfermedades inflamatorias intestinales . 26 (12): 1819–1830. doi :10.1093/ibd/izaa087. PMID 32385487.
- ^ Zhang Y, Tan H, Tang J, Li J, Chong W, Hai Y, et al. (julio de 2020). "Efectos de la suplementación con vitamina D en la prevención de la diabetes tipo 2 en pacientes con prediabetes: una revisión sistemática y un metanálisis". Diabetes Care . 43 (7): 1650–58. doi : 10.2337/dc19-1708 . PMID 33534730. S2CID 219897727.
- ^ Sahebi R, Rezayi M, Emadzadeh M, Salehi M, Tayefi M, Parizadeh SM, et al. (febrero de 2019). "Los efectos de la suplementación con vitamina D en los índices de control glucémico en diabéticos iraníes: una revisión sistemática y un metanálisis". Terapias complementarias en la práctica clínica . 34 : 294–304. doi :10.1016/j.ctcp.2018.12.009. PMID 30712741. S2CID 57479957.
- ^ Mohammadi S, Hajhashemy Z, Saneei P (junio de 2021). "Niveles séricos de vitamina D en relación con la diabetes tipo 2 y la prediabetes en adultos: una revisión sistemática y un metanálisis de dosis-respuesta de estudios epidemiológicos". Critical Reviews in Food Science and Nutrition . 2 (29): 8178–8198. doi :10.1080/10408398.2021.1926220. PMID 34076544. S2CID 235295924.
- ^ Brophy S, Davies H, Mannan S, Brunt H, Williams R (septiembre de 2011). "Intervenciones para la diabetes autoinmune latente (LADA) en adultos". Base de datos Cochrane de revisiones sistemáticas . 2011 (9): CD006165. doi :10.1002/14651858.cd006165.pub3. PMC 6486159. PMID 21901702 .
- ^ Khoshbakht Y, Bidaki R, Salehi-Abargouei A (enero de 2018). "Estado de vitamina D y trastorno por déficit de atención e hiperactividad: una revisión sistemática y un metaanálisis de estudios observacionales". Avances en nutrición . 9 (1): 9–20. doi : 10.1093/advances/nmx002 . PMC 6333940 . PMID 29438455.
- ^ Gan J, Galer P, Ma D, Chen C, Xiong T (noviembre de 2019). "El efecto de la suplementación con vitamina D en el trastorno por déficit de atención e hiperactividad: una revisión sistemática y un metaanálisis de ensayos controlados aleatorizados". Revista de psicofarmacología infantil y adolescente . 29 (9): 670–87. doi :10.1089/cap.2019.0059. PMID 31368773. S2CID 199054851.
- ^ Shaffer JA, Edmondson D, Wasson LT, Falzon L, Homma K, Ezeokoli N, et al. (abril de 2014). "Suplementación con vitamina D para los síntomas depresivos: una revisión sistemática y un metanálisis de ensayos controlados aleatorizados". Medicina Psicosomática . 76 (3): 190–6. doi :10.1097/psy.0000000000000044. PMC 4008710 . PMID 24632894.
- ^ Balion C, Griffith LE, Strifler L, Henderson M, Patterson C, Heckman G, et al. (septiembre de 2012). "Vitamina D, cognición y demencia: una revisión sistemática y un metanálisis". Neurología . 79 (13): 1397–405. doi :10.1212/WNL.0b013e31826c197f. PMC 3448747 . PMID 23008220.
- ^ Yüksel RN, Altunsoy N, Tikir B, Cingi Külük M, Unal K, Goka S, et al. (diciembre de 2014). "Correlación entre los niveles totales de vitamina D y la psicopatología psicótica en pacientes con esquizofrenia: implicaciones terapéuticas para el aumento de vitamina D adicional". Avances terapéuticos en psicofarmacología . 4 (6): 268–75. doi :10.1177/2045125314553612. PMC 4257987 . PMID 25489478.
- ^ ab Aghajafari F, Nagulesapillai T, Ronksley PE, Tough SC, O'Beirne M, Rabi DM (marzo de 2013). "Asociación entre el nivel de 25-hidroxivitamina D en suero materno y los resultados del embarazo y neonatales: revisión sistemática y metaanálisis de estudios observacionales". BMJ . 346 : f1169. doi : 10.1136/bmj.f1169 . PMID 23533188.
- ^ ab Palacios C, De-Regil LM, Lombardo LK, Peña-Rosas JP (noviembre de 2016). "Suplementación con vitamina D durante el embarazo: metaanálisis actualizado sobre los resultados maternos". The Journal of Steroid Biochemistry and Molecular Biology . 164 : 148–55. doi :10.1016/j.jsbmb.2016.02.008. PMC 5357731 . PMID 26877200.
- ^ Roth DE, Leung M, Mesfin E, Qamar H, Watterworth J, Papp E (noviembre de 2017). "Suplementación con vitamina D durante el embarazo: estado de la evidencia a partir de una revisión sistemática de ensayos aleatorizados". BMJ . 359 : j5237. doi :10.1136/bmj.j5237. PMC 5706533 . PMID 29187358.
- ^ ab Palacios C, Kostiuk LK, Peña-Rosas JP (julio 2019). "Suplementación con vitamina D para mujeres durante el embarazo". Base de Datos Cochrane de Revisiones Sistemáticas . 2019 (7): CD008873. doi : 10.1002/14651858.CD008873.pub4. PMC 3747784. PMID 31348529.
- ^ ab Wagner CL, Taylor SN, Dawodu A, Johnson DD, Hollis BW (marzo de 2012). "Vitamina D y su papel durante el embarazo para lograr una salud óptima de la madre y el feto". Nutrients . 4 (3): 208–30. doi : 10.3390/nu4030208 . PMC 3347028 . PMID 22666547.
- ^ Bi WG, Nuyt AM, Weiler H, Leduc L, Santamaria C, Wei SQ (julio de 2018). "Asociación entre la suplementación con vitamina D durante el embarazo y el crecimiento, la morbilidad y la mortalidad de la descendencia: una revisión sistemática y un metanálisis". JAMA Pediatrics . 172 (7): 635–45. doi :10.1001/jamapediatrics.2018.0302. PMC 6137512 . PMID 29813153.
- ^ Pathak K, Soares MJ, Calton EK, Zhao Y, Hallett J (junio de 2014). "Suplementación con vitamina D y estado de peso corporal: una revisión sistemática y metanálisis de ensayos controlados aleatorizados". Obesity Reviews . 15 (6): 528–37. doi :10.1111/obr.12162. PMID 24528624. S2CID 8660739.
- ^ Mallard SR, Howe AS, Houghton LA (octubre de 2016). "Estado de vitamina D y pérdida de peso: una revisión sistemática y metanálisis de ensayos controlados aleatorizados y no aleatorizados de pérdida de peso". The American Journal of Clinical Nutrition . 104 (4): 1151–1159. doi : 10.3945/ajcn.116.136879 . PMID 27604772.
- ^ abc Autoridad Europea de Seguridad Alimentaria (AESA) Panel de Productos Dietéticos, Nutrición y Alergias (NDA) (2010). «Dictamen científico sobre la justificación de las declaraciones de propiedades saludables relacionadas con la vitamina D y el funcionamiento normal del sistema inmunitario y la respuesta inflamatoria (ID 154, 159), el mantenimiento de la función muscular normal (ID 155) y el mantenimiento de la función cardiovascular normal (ID 159) de conformidad con el artículo 13(1) del Reglamento (CE) n.º 1924/2006». Revista de la EFSA . 8 (2): 1468–85. doi :10.2903/j.efsa.2010.1468.
- ^ Comisión Técnica de Productos Dietéticos, Nutrición y Alergias (NDA) de la Autoridad Europea de Seguridad Alimentaria (AESA) (2011). «Dictamen científico sobre la justificación de una declaración de propiedades saludables relacionada con la vitamina D y el riesgo de caídas de conformidad con el artículo 14 del Reglamento (CE) n.º 1924/2006» (PDF) . Revista de la EFSA . 9 (9): 2382–2400. doi : 10.2903/j.efsa.2011.2382 . Archivado (PDF) desde el original el 20 de agosto de 2019 . Consultado el 20 de agosto de 2019 .
- ^ "Guía para la industria: Guía de etiquetado de alimentos". Administración de Alimentos y Medicamentos (FDA). Enero de 2013. Archivado desde el original el 22 de diciembre de 2020. Consultado el 17 de julio de 2019 .
 Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público .
Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público . - ^ "Resumen científico de Health Canada sobre la afirmación de que los Estados Unidos tienen propiedades saludables en relación con el calcio y la osteoporosis". Dirección de Alimentos, División de Productos y Alimentos para la Salud de la Oficina de Ciencias de la Nutrición de Health Canada. 1 de mayo de 2000. Archivado desde el original el 3 de diciembre de 2016. Consultado el 29 de enero de 2012 .
- ^ "Sistemas reguladores de las declaraciones de propiedades saludables en Japón" (PDF) . Agencia de Asuntos del Consumidor de Japón, División de Etiquetado de Alimentos. 1 de junio de 2011. Archivado desde el original (PDF) el 6 de marzo de 2012. Consultado el 29 de enero de 2012 .
- ^ abcde Valores de referencia de nutrientes para Australia y Nueva Zelanda, incluidas las ingestas dietéticas recomendadas. Canberra: Consejo Nacional de Salud e Investigación Médica. 2006. ISBN 1-86496-243-7Archivado desde el original el 3 de marzo de 2023 . Consultado el 19 de marzo de 2023 .
- ^ abcd «Vitaminas y minerales – Vitamina D». Servicio Nacional de Salud . 3 de agosto de 2020. Archivado desde el original el 30 de octubre de 2017. Consultado el 15 de noviembre de 2020 .
- ^ abcd «Vitamina D y calcio: ingestas dietéticas de referencia actualizadas». Nutrición y alimentación saludable . Health Canada. 5 de diciembre de 2008. Archivado desde el original el 14 de junio de 2017. Consultado el 28 de abril de 2018 .
- ^ abcd Panel de la EFSA sobre productos dietéticos, nutrición y alergias (NDA) (29 de junio de 2016). «Valores dietéticos de referencia para la vitamina D». Revista de la EFSA . 14 (10): e04547. doi : 10.2903/j.efsa.2016.4547 . hdl : 11380/1228918 .
- ^ ab Panel de la EFSA sobre productos dietéticos, nutrición y alergias (NDA) (2012). "Opinión científica sobre el nivel máximo tolerable de ingesta de vitamina D". Revista de la EFSA (manuscrito enviado). 10 (7): 2813. doi : 10.2903/j.efsa.2012.2813 . hdl : 2434/257871 .
- ^ "Oficina de Suplementos Dietéticos – Vitamina D". Institutos Nacionales de Salud Oficina de Suplementos Dietéticos . Archivado desde el original el 23 de julio de 2020 . Consultado el 14 de abril de 2022 .
 Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público .
Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público . - ^ "PHE publica nuevos consejos sobre la vitamina D". Public Health England. 21 de julio de 2016. Archivado desde el original el 3 de enero de 2021. Consultado el 15 de noviembre de 2020 .
- ^ "Vitamina D". The Nutrition Source . 18 de septiembre de 2012. Archivado desde el original el 13 de abril de 2022. Consultado el 14 de abril de 2022 .
- ^ "Registro Federal 27 de mayo de 2016 Etiquetado de alimentos: Revisión de las etiquetas de información nutricional y de suplementos. Página FR 33982" (PDF) . Archivado (PDF) del original el 8 de agosto de 2016 . Consultado el 20 de agosto de 2019 .
 Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público .
Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público . - ^ "Daily Value Reference of the Dietary Supplement Label Database (DSLD)" ( Base de datos de etiquetas de suplementos dietéticos (DSLD)) . Archivado desde el original el 7 de abril de 2020. Consultado el 16 de mayo de 2020 .
- ^ "Recursos de la industria sobre los cambios en la etiqueta de información nutricional". Administración de Alimentos y Medicamentos de Estados Unidos (FDA) . 21 de diciembre de 2018. Archivado desde el original el 25 de diciembre de 2020. Consultado el 16 de mayo de 2020 .
 Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público .
Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público . - ^ Salleh A (12 de junio de 2012). «Fortificación de alimentos con vitamina D en la mesa». Australian Broadcasting Corporation. Archivado desde el original el 22 de diciembre de 2020. Consultado el 12 de junio de 2012 .
- ^ "Encuesta de salud australiana: resultados biomédicos sobre nutrientes, 2011-2012". Oficina de Estadísticas de Australia . 21 de diciembre de 2011. Archivado desde el original el 10 de marzo de 2023. Consultado el 19 de marzo de 2023 .
- ^ "Vitamina D (traducida)" (en sueco). Agencia Nacional de Alimentos de Suecia . Archivado desde el original el 26 de octubre de 2020. Consultado el 19 de octubre de 2018 .
- ^ Vitamin-D-Bedarf bei fehlender endogener Synthese Deutsche Gesellschaft für Ernährung, enero de 2012
- ^ Pérez-López FR, Brincat M, Erel CT, Tremollieres F, Gambacciani M, Lambrinoudaki I, et al. (Enero de 2012). "Declaración de posición de EMAS: vitamina D y salud posmenopáusica". Maturitas . 71 (1): 83–8. doi : 10.1016/j.maturitas.2011.11.002 . PMID 22100145.
- ^ Comité Permanente sobre la Evaluación Científica de las Ingestas Dietéticas de Referencia del Instituto de Medicina (EE. UU.) (1997). DRI, Ingestas dietéticas de referencia: para calcio, fósforo, magnesio, vitamina D y flúor. Washington, DC: National Academy Press. p. 250. doi :10.17226/5776. ISBN 978-0-309-06350-0. PMID 23115811. Archivado desde el original el 2 de abril de 2015 . Consultado el 11 de abril de 2010 .
- ^ "Búsqueda, Base de datos nacional de nutrientes para la publicación de referencia estándar 27". Departamento de Agricultura de los Estados Unidos, Servicio de Investigación Agrícola. 2014. Archivado desde el original el 19 de abril de 2014 . Consultado el 12 de junio de 2015 .
 Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público .
Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público . - ^ ab Wang T, Bengtsson G, Kärnefelt I, Björn LO (septiembre de 2001). "Provitaminas y vitaminas D2 y D3 en Cladina spp. en un gradiente latitudinal: posible correlación con los niveles de UV". Journal of Photochemistry and Photobiology B: Biology . 62 (1–2): 118–22. doi :10.1016/S1011-1344(01)00160-9. PMID 11693362. Archivado desde el original el 28 de mayo de 2020 . Consultado el 31 de octubre de 2018 .
- ^ Schmid A, Walther B (julio de 2013). "Contenido natural de vitamina D en productos animales". Advances in Nutrition . 4 (4): 453–62. doi :10.3945/an.113.003780. PMC 3941824 . PMID 23858093.
- ^ abcdefg Keegan RJ, Lu Z, Bogusz JM, Williams JE, Holick MF (enero de 2013). "Fotobiología de la vitamina D en hongos y su biodisponibilidad en humanos". Dermato-Endocrinology . 5 (1): 165–76. doi :10.4161/derm.23321. PMC 3897585 . PMID 24494050.
- ^ Haytowitz DB (2009). «Vitamina D en hongos» (PDF) . Laboratorio de Datos de Nutrientes, Departamento de Agricultura de los Estados Unidos. Archivado (PDF) del original el 1 de febrero de 2021. Consultado el 16 de abril de 2018 .
 Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público .
Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público . - ^ de Lourdes Samaniego-Vaesken M, Alonso-Aperte E, Varela-Moreiras G (2012). "La fortificación de alimentos con vitaminas hoy". Investigación sobre alimentación y nutrición . 56 : 5459. doi : 10.3402/fnr.v56i0.5459. PMC 3319130 . PMID 22481896.
- ^ Spiro A, Buttriss JL (diciembre de 2014). "Vitamina D: una descripción general del estado y la ingesta de vitamina D en Europa". Boletín de nutrición . 39 (4): 322–350. doi :10.1111/nbu.12108. PMC 4288313 . PMID 25635171.
- ^ "Vitamina D para la leche y las alternativas a la leche". Administración de Alimentos y Medicamentos (FDA). 15 de julio de 2016. Archivado desde el original el 22 de diciembre de 2020. Consultado el 22 de febrero de 2017 .
 Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público .
Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público . - ^ "Registro Federal: Aditivos alimentarios permitidos para su adición directa a alimentos para consumo humano; vitamina D2". Administración de Alimentos y Medicamentos, Departamento de Salud y Servicios Humanos de Estados Unidos. 18 de julio de 2016. Archivado desde el original el 22 de diciembre de 2020. Consultado el 22 de febrero de 2017 .
 Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público .
Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público . - ^ "§172.379 Vitamina D2". Código Electrónico de Reglamentos Federales. Archivado desde el original el 22 de diciembre de 2020. Consultado el 16 de julio de 2019 .
 Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público .
Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público . - ^ "§172.380 Vitamina D3". Código Electrónico de Reglamentos Federales. Archivado desde el original el 22 de diciembre de 2020. Consultado el 16 de julio de 2019 .
 Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público .
Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público . - ^ "Alternativa a la leche de vaca". osoblanco . 16 de enero de 2020. Archivado desde el original el 22 de diciembre de 2020 . Consultado el 20 de enero de 2020 .
- ^ Tripkovic L (2013). "Vitamina D 2 vs. vitamina D 3 : ¿Son lo mismo?". Boletín de nutrición . 38 (2): 243–248. doi :10.1111/nbu.12029.
- ^ Alshahrani F, Aljohani N (septiembre de 2013). "Vitamina D: deficiencia, suficiencia y toxicidad". Nutrients . 5 (9): 3605–16. doi : 10.3390/nu5093605 . PMC 3798924 . PMID 24067388.
- ^ Biancuzzo RM, Clarke N, Reitz RE, Travison TG, Holick MF (marzo de 2013). "Concentraciones séricas de 1,25-dihidroxivitamina D2 y 1,25-dihidroxivitamina D3 en respuesta a la suplementación con vitamina D2 y vitamina D3". The Journal of Clinical Endocrinology and Metabolism . 98 (3): 973–9. doi :10.1210/jc.2012-2114. PMC 3590486 . PMID 23386645.
- ^ Borel P, Caillaud D, Cano NJ (2015). "Biodisponibilidad de la vitamina D: estado del arte" (PDF) . Critical Reviews in Food Science and Nutrition . 55 (9): 1193–205. doi :10.1080/10408398.2012.688897. PMID 24915331. S2CID 9818323. Archivado (PDF) del original el 13 de julio de 2021 . Consultado el 27 de abril de 2021 .
- ^ Jakobsen J, Knuthsen P (abril de 2014). "Estabilidad de la vitamina D en alimentos durante la cocción". Química alimentaria . 148 : 170–5. doi :10.1016/j.foodchem.2013.10.043. PMID 24262542.
- ^ Wahl DA, Cooper C, Ebeling PR, Eggersdorfer M, Hilger J, Hoffmann K, et al. (29 de agosto de 2012). "Una representación global del estado de la vitamina D en poblaciones sanas" (PDF) . Archivos de Osteoporosis . 7 (1–2): 155–172. doi :10.1007/s11657-012-0093-0. hdl : 11343/220606 . PMID: 23225293. S2CID: 207300035. Archivado desde el original el 19 de marzo de 2023. Consultado el 20 de agosto de 2019 .
- ^ Wahl DA, Cooper C, Ebeling PR, Eggersdorfer M, Hilger J, Hoffmann K, et al. (1 de febrero de 2013). "Una representación global del estado de la vitamina D en poblaciones sanas: respuesta al comentario de Saadi". Archivos de Osteoporosis . 8 (1–2): 122. doi :10.1007/s11657-013-0122-7. PMID 23371520. S2CID 5929230.
- ^ ab "Niveles de 25(OH)D en ng/mL". health harvard edu/ . 19 de diciembre de 2016. Archivado desde el original el 2 de enero de 2020 . Consultado el 2 de enero de 2020 .
- ^ "convertidor nmol". endmemo . Archivado desde el original el 2 de febrero de 2020 . Consultado el 5 de enero de 2020 .
- ^ Bischoff-Ferrari HA (2008). "Niveles séricos óptimos de 25-hidroxivitamina D para múltiples resultados de salud". Luz solar, vitamina D y cáncer de piel (revisión). Avances en medicina experimental y biología. Vol. 810. Springer. págs. 500–25. doi :10.1007/978-0-387-77574-6_5. ISBN 978-0-387-77573-9. Número de identificación personal 25207384.
- ^ ab Dahlquist DT, Dieter BP, Koehle MS (2015). "Efectos ergogénicos plausibles de la vitamina D en el rendimiento atlético y la recuperación". Revista de la Sociedad Internacional de Nutrición Deportiva (Revisión). 12 : 33. doi : 10.1186/s12970-015-0093-8 . PMC 4539891. PMID 26288575 .
- ^ Engelman CD, Fingerlin TE, Langefeld CD, Hicks PJ, Rich SS, Wagenknecht LE, et al. (septiembre de 2008). "Determinantes genéticos y ambientales de los niveles de 25-hidroxivitamina D y 1,25-dihidroxivitamina D en hispanoamericanos y afroamericanos". The Journal of Clinical Endocrinology and Metabolism . 93 (9): 3381–8. doi :10.1210/jc.2007-2702. PMC 2567851 . PMID 18593774.
- ^ Wang L, Song Y, Manson JE, Pilz S, März W, Michaëlsson K, et al. (noviembre de 2012). "25-hidroxi-vitamina D circulante y riesgo de enfermedad cardiovascular: un metaanálisis de estudios prospectivos". Circulation: Cardiovascular Quality and Outcomes . 5 (6): 819–29. doi :10.1161/CIRCOUTCOMES.112.967604. PMC 3510675 . PMID 23149428.
- ^ ab Ross AC, Manson JE, Abrams SA, Aloia JF, Brannon PM, Clinton SK, et al. (enero de 2011). "El informe de 2011 sobre las ingestas dietéticas de referencia para calcio y vitamina D del Instituto de Medicina: lo que los médicos necesitan saber". The Journal of Clinical Endocrinology and Metabolism . 96 (1): 53–8. doi :10.1210/jc.2010-2704. PMC 3046611 . PMID 21118827.
- ^ abc Vitamina D en Manual Merck de Diagnóstico y Terapia Edición Profesional
- ^ abcd Vieth R (mayo de 1999). "Suplementación con vitamina D, concentraciones de 25-hidroxivitamina D y seguridad" (PDF) . The American Journal of Clinical Nutrition . 69 (5): 842–56. doi : 10.1093/ajcn/69.5.842 . PMID 10232622. Archivado (PDF) desde el original el 3 de julio de 2012. Consultado el 30 de enero de 2011 .
- ^ Límites máximos de ingesta tolerables de vitaminas y minerales (PDF) . Autoridad Europea de Seguridad Alimentaria . Diciembre de 2006. ISBN 978-92-9199-014-6. Archivado (PDF) del original el 6 de mayo de 2019 . Consultado el 27 de febrero de 2011 .
- ^ Schlingmann KP, Kaufmann M, Weber S, Irwin A, Goos C, John U, et al. (Agosto de 2011). "Mutaciones en CYP24A1 e hipercalcemia infantil idiopática". La Revista de Medicina de Nueva Inglaterra . 365 (5): 410–21. doi : 10.1056/NEJMoa1103864 . PMID 21675912.
- ^ De Paolis E, Scaglione GL, De Bonis M, Minucci A, Capoluongo E (octubre de 2019). "Defectos genéticos de CYP24A1 y SLC34A1 asociados con hipercalcemia infantil idiopática: del genotipo al fenotipo". Química clínica y medicina de laboratorio . 57 (11): 1650–1667. doi : 10.1515/cclm-2018-1208 . PMID 31188746.
- ^ Tebben PJ, Singh RJ, Kumar R (octubre de 2016). "Hipercalcemia mediada por vitamina D: mecanismos, diagnóstico y tratamiento". Endocrine Reviews . 37 (5): 521–547. doi :10.1210/er.2016-1070. PMC 5045493 . PMID 27588937.
- ^ "La FDA advierte sobre la necesidad de administrar suplementos de vitamina D a los bebés" (Comunicado de prensa). Administración de Alimentos y Medicamentos (FDA). 15 de junio de 2010. Archivado desde el original el 12 de enero de 2017.
 Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público .
Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público . - ^ Olmos-Ortiz A, Avila E, Durand-Carbajal M, Díaz L (enero de 2015). "Regulación de la biosíntesis y actividad del calcitriol: atención a la deficiencia gestacional de vitamina D y los resultados adversos del embarazo". Nutrients . 7 (1): 443–80. doi : 10.3390/nu7010443 . PMC 4303849 . PMID 25584965.
- ^ abc Rooney MR, Harnack L, Michos ED, Ogilvie RP, Sempos CT, Lutsey PL (junio de 2017). "Tendencias en el uso de suplementos de vitamina D en dosis altas superiores a 1000 o 4000 unidades internacionales diarias, 1999-2014". JAMA . 317 (23): 2448–2450. doi :10.1001/jama.2017.4392. PMC 5587346 . PMID 28632857.
- ^ Comité del Instituto de Medicina (EE. UU.) para revisar las ingestas dietéticas de referencia de vitamina D y calcio (2011). Ross AC, Taylor CL, Yaktine AL, Del Valle HB (eds.). Dietary Reference Intakes for Calcium and Vitamin D. The National Academies Collection: Reports funded by National Institutes of Health. Washington (DC): National Academies Press (EE. UU.). PMID 21796828. Archivado desde el original el 29 de enero de 2016. Consultado el 7 de julio de 2012 .
- ^ ab Insel P, Ross D, Bernstein M, McMahon K (18 de marzo de 2015). Descubriendo la nutrición. Jones & Bartlett Publishers. ISBN 978-1-284-06465-0Archivado desde el original el 19 de marzo de 2023 . Consultado el 9 de abril de 2017 .
- ^ ab Holick MF (1992). "Biología evolutiva y patología de la vitamina D". J Nutr Sci Vitaminol (Tokio) . N.º de especificación: 79–83. doi : 10.3177/jnsv.38.special_79 . PMID 1297827.
- ^ Holick MF (abril de 1987). "Fotosíntesis de vitamina D en la piel: efecto de variables ambientales y de estilo de vida". Actas de la Federación . 46 (5): 1876–82. PMID 3030826.
- ^ Deluca HF (enero de 2014). "Historia del descubrimiento de la vitamina D y sus metabolitos activos". BoneKEy Reports . 3 : 479. doi :10.1038/bonekey.2013.213. PMC 3899558 . PMID 24466410.
- ^ ab Holick MF (marzo de 2004). "Vitamina D: importancia en la prevención de cánceres, diabetes tipo 1, enfermedades cardíacas y osteoporosis". The American Journal of Clinical Nutrition . 79 (3): 362–71. doi : 10.1093/ajcn/79.3.362 . PMID 14985208.
- ^ Eyley SC, Williams DH (1975). "Producción fotolítica de vitamina D. El valor preparativo de un fotosensibilizador". Journal of the Chemical Society, Chemical Communications (20): 858a. doi :10.1039/C3975000858A.
- ^ Crissey SD, Ange KD, Jacobsen KL, Slifka KA, Bowen PE, Stacewicz-Sapuntzakis M, et al. (enero de 2003). "Concentraciones séricas de lípidos, metabolitos de vitamina D, retinol, ésteres de retinilo, tocoferoles y carotenoides seleccionados en doce especies de felinos salvajes en cautiverio en cuatro zoológicos". The Journal of Nutrition . 133 (1): 160–6. doi : 10.1093/jn/133.1.160 . PMID 12514284.
- ^ Holick MF (2018). "Capítulo 4: Fotobiología de la vitamina D". En Feldman D, Pike JW, Bouillon R, Giovannucci E, Goltzman D, Hewison M (eds.). Vitamina D: Volumen 1: Bioquímica, fisiología y diagnóstico (4.ª ed.). Londres, Reino Unido: Academic Press. ISBN 978-0-12-809965-0.
- ^ Holick MF (2020). "Luz solar, radiación ultravioleta, vitamina D y cáncer de piel: ¿cuánta luz solar necesitamos?". Luz solar, vitamina D y cáncer de piel . Avances en medicina experimental y biología. Vol. 1268. Springer. págs. 19–36. doi :10.1007/978-3-030-46227-7_2. ISBN . 978-3-030-46226-0. PMID 32918212. S2CID 221636019.
108 referencias
- ^ Young AR, Morgan KA, Harrison GI, Lawrence KP, Petersen B, Wulf HC, et al. (octubre de 2021). "Un espectro de acción revisado para la síntesis de vitamina D por exposición a la radiación UV suberitemal en humanos in vivo". Actas de la Academia Nacional de Ciencias de los Estados Unidos de América . 118 (40). Código Bibliográfico :2021PNAS..11815867Y. doi : 10.1073/pnas.2015867118 . PMC 8501902 . PMID 34580202.
- ^ Holick MF (febrero de 2002). "Vitamina D: la hormona D-light subestimada que es importante para la salud ósea y celular". Current Opinion in Endocrinology, Diabetes and Obesity . 9 (1): 87–98. doi :10.1097/00060793-200202000-00011. S2CID 87725403.
- ^ Bikle DD (marzo de 2010). "Vitamina D y la piel". Revista de metabolismo óseo y mineral . 28 (2): 117–30. doi :10.1007/s00774-009-0153-8. PMID 20107849. S2CID 6072459.
- ^ Bouillon R, Suda T (enero de 2014). "Vitamina D: calcio y homeostasis ósea durante la evolución". BoneKEy Reports . 3 : 480. doi :10.1038/bonekey.2013.214. PMC 3899559 . PMID 24466411.
- ^ Holick MF (1 de abril de 2010). La solución de la vitamina D: una estrategia de tres pasos para curar nuestros problemas de salud más comunes. Penguin Publishing Group. ISBN 978-1-101-22293-5Archivado desde el original el 19 de marzo de 2023 . Consultado el 19 de marzo de 2023 .
- ^ Agarwal SC, Stout SD (28 de junio de 2011). Pérdida ósea y osteoporosis: una perspectiva antropológica. Springer Science & Business Media. ISBN 978-1-4419-8891-1. Archivado (PDF) del original el 29 de enero de 2006.
Las altas concentraciones de 25(OH)D y los requerimientos relativamente altos de vitamina D de los simios y monos son comprensibles a la luz de su biología: su área de superficie corporal en relación con la masa es generalmente mayor que la de los humanos, y son inveterados acicaladores, que consumen por la boca la vitamina D generada a partir de los aceites secretados por la piel en el pelaje. Aunque gran parte de la vitamina D producida dentro de la piel humana se absorbe directamente, las aves y los animales con peletería adquieren la mayor parte de su vitamina D por vía oral, mientras se acicalan (Bicknell y Prescott, 1946; Carpenter y Zhao, 1999). La vitamina D se genera a partir de las secreciones aceitosas de la piel en el pelaje. El consumo oral de la excreción dérmica expuesta a los rayos UV es la forma en que muchos animales adquieren el "nutriente", la vitamina D. Aunque Fraser (1983) ha argumentado que la absorción dérmica de vitamina D puede ser más natural, lo que sabemos de los animales indica que el consumo oral es igualmente fisiológico. Dado que la vitamina D se puede extraer del sudor humano y de las secreciones de la piel expuestas a los rayos UV (Bicknell y Prescott, 1946), también es razonable pensar que los primeros humanos también obtenían parte de su vitamina D por vía oral, lamiéndose la piel.
- ^ Yahav S, Buffenstein R (enero de 1993). "La suplementación con colecalciferol altera la función intestinal y mejora la digestibilidad en un habitante subterráneo, la rata topo desnuda (Heterocephalus glaber), cuando se alimenta con una dieta de zanahoria". The British Journal of Nutrition . 69 (1): 233–41. doi : 10.1079/BJN19930025 . PMID 8384476.
- ^ Zafalon RV, Risolia LW, Pedrinelli V, Vendramini TH, Rodrigues RB, Amaral AR, et al. (enero de 2020). "Metabolismo de la vitamina D en perros y gatos y su relación con enfermedades no asociadas al metabolismo óseo". Journal of Animal Physiology and Animal Nutrition . 104 (1): 322–42. doi : 10.1111/jpn.13259 . PMID 31803981.
- ^ ab Holick MF (noviembre de 2005). "La epidemia de vitamina D y sus consecuencias para la salud" (PDF) . The Journal of Nutrition . 135 (11): 2739S–2748S. doi : 10.1093/jn/135.11.2739S . PMID 16251641. Archivado (PDF) del original el 18 de noviembre de 2017. Consultado el 24 de noviembre de 2011.
[La vitamina D3] se produce comercialmente mediante la extracción de 7-dehidrocolesterol de la grasa de lana, seguida de irradiación UVB y purificación [...] [La vitamina D2] se produce comercialmente mediante la irradiación y luego purificación del ergosterol extraído de la levadura.
- ^ Takeuchi A, Okano T, Sayamoto M, Sawamura S, Kobayashi T, Motosugi M, et al. (febrero de 1986). "Distribución tisular de 7-dehidrocolesterol, vitamina D3 y 25-hidroxivitamina D3 en varias especies de peces". Journal of Nutritional Science and Vitaminology . 32 (1): 13–22. doi : 10.3177/jnsv.32.13 . PMID 3012050. Archivado desde el original el 1 de noviembre de 2018 . Consultado el 20 de agosto de 2019 .
- ^ Jäpelt RB, Jakobsen J (mayo de 2013). "Vitamina D en plantas: una revisión de su aparición, análisis y biosíntesis". Frontiers in Plant Science . 4 : 136. doi : 10.3389/fpls.2013.00136 . PMC 3651966 . PMID 23717318.
- ^ Göring H (noviembre de 2018). "Vitamina D en la naturaleza: un producto de síntesis y/o degradación de componentes de la membrana celular". Bioquímica. Biokhimiia . 83 (11): 1350–1357. doi :10.1134/S0006297918110056. PMID 30482146. S2CID 53437216.
- ^ Björn LO, Wang T (2000). "Vitamina D en un contexto ecológico". Revista Internacional de Salud Circumpolar . 59 (1): 26–32. ISSN 1239-9736. PMID 10850004.
- ^ abc Adams JS, Hewison M (febrero de 2010). "Actualización en vitamina D". Revista de endocrinología clínica y metabolismo . 95 (2): 471–8. doi :10.1210/jc.2009-1773. PMC 2840860. PMID 20133466 .
- ^ Cheng JB, Levine MA, Bell NH, Mangelsdorf DJ, Russell DW (mayo de 2004). "Evidencia genética de que la enzima humana CYP2R1 es una vitamina D 25-hidroxilasa clave". Actas de la Academia Nacional de Ciencias de los Estados Unidos de América . 101 (20): 7711–5. Bibcode :2004PNAS..101.7711C. doi : 10.1073/pnas.0402490101 . PMC 419671 . PMID 15128933.
- ^ Laing CJ, Cooke NE (2004). "Sección I: Cap. 8: Proteína de unión a la vitamina D". En Feldman D, Glorieux FH, Pike JW (eds.). Vitamina D . Vol. 1 (2.ª ed.). Academic Press. págs. 117–134. ISBN 978-0-12-252687-9Archivado desde el original el 19 de marzo de 2023 . Consultado el 9 de abril de 2017 .
- ^ Holick MF, Kleiner-Bossaller A, Schnoes HK, Kasten PM, Boyle IT, DeLuca HF (octubre de 1973). "1,24,25-Trihidroxivitamina D3. Un metabolito de la vitamina D3 eficaz en el intestino". The Journal of Biological Chemistry . 248 (19): 6691–6. doi : 10.1016/S0021-9258(19)43408-X . PMID 4355503.
- ^ Horst RL, Reinhardt TA, Ramberg CF, Koszewski NJ, Napoli JL (julio de 1986). "24-Hidroxilación de 1,25-dihidroxiergocalciferol. Un proceso de desactivación inequívoco". The Journal of Biological Chemistry . 261 (20): 9250–6. doi : 10.1016/S0021-9258(18)67647-1 . PMID 3013880.
- ^ Doroudi M, Schwartz Z, Boyan BD (marzo de 2015). "Acciones mediadas por membrana de la 1,25-dihidroxivitamina D3: una revisión de las funciones de la proteína activadora de la fosfolipasa A2 y la proteína quinasa II dependiente de Ca(2+)/calmodulina". Revista de bioquímica de esteroides y biología molecular . 147 : 81–84. doi :10.1016/j.jsbmb.2014.11.002. PMC 4323845. PMID 25448737 .
- ^ Hii CS, Ferrante A (marzo de 2016). "Las acciones no genómicas de la vitamina D". Nutrients . 8 (3): 135. doi : 10.3390/nu8030135 . PMC 4808864 . PMID 26950144.
- ^ Jones G (abril de 2022). "100 AÑOS DE VITAMINA D: aspectos históricos de la vitamina D". Endocrine Connections . 11 (4). doi :10.1530/EC-21-0594. PMC 9066576 . PMID 35245207.
- ^ Carere S (25 de julio de 2007). "La enfermedad de los niños de muchos años vuelve a cobrar fuerza". Toronto Star . Archivado desde el original el 17 de mayo de 2008. Consultado el 24 de agosto de 2010 .
- ^ McClean FC, Budy AM (28 de enero de 1964). "Vitamina A, vitamina D, cartílago, huesos y dientes". Vitaminas y hormonas . Vol. 21. Academic Press. págs. 51–52. ISBN 978-0-12-709821-0Archivado desde el original el 19 de marzo de 2023 . Consultado el 19 de marzo de 2023 .
- ^ "Historia de la vitamina D". Universidad de California en Riverside. 2011. Archivado desde el original el 16 de octubre de 2017. Consultado el 9 de mayo de 2014 .
- ^ "Adolf Windaus – Biografía". Nobelprize.org. 25 de marzo de 2010. Archivado desde el original el 24 de julio de 2018. Consultado el 25 de marzo de 2010 .
- ^ Rosenheim O, King H (1932). "El sistema de anillos de esteroles y ácidos biliares. Parte II". J. Chem. Technol. Biotechnol . 51 (47): 954–7. doi :10.1002/jctb.5000514702.
- ^ Askew FA, Bourdillon RB, Bruce HM, Callow RK, St. L. Philpot J, Webster TA (1932). "Vitamina D cristalina". Actas de la Royal Society de Londres. Serie B, que contiene artículos de carácter biológico . 109 (764): 488–506. doi : 10.1098/rspb.1932.0008 . JSTOR 81571.
- ^ Hirsch AL (2011). "Aspectos industriales de la vitamina D". En Feldman DJ, Pike JW, Adams JS (eds.). Vitamina D . Academic Press. p. 73. ISBN 978-0-12-387035-3Archivado desde el original el 19 de marzo de 2023 . Consultado el 19 de marzo de 2023 .
- ^ Ziedonis AA, Mowery DC, Nelson RR, Bhaven NS (2004). Torre de marfil e innovación industrial: transferencia de tecnología universidad-industria antes y después de la Ley Bayh-Dole en los Estados Unidos. Stanford Business Books. pp. 39–40. ISBN 978-0-8047-4920-6Archivado desde el original el 19 de marzo de 2023 . Consultado el 19 de marzo de 2023 .
- ^ Marshall J (septiembre de 2010). Elbridge a Stuart: fundador de Carnation Company. Kessinger Publishing. ISBN 978-1-164-49678-6Archivado desde el original el 19 de marzo de 2023 . Consultado el 9 de abril de 2017 .
- ^ Haussler MR, Norman AW (enero de 1969). "Receptor cromosómico para un metabolito de la vitamina D". Actas de la Academia Nacional de Ciencias de los Estados Unidos de América . 62 (1): 155–62. Bibcode :1969PNAS...62..155H. doi : 10.1073/pnas.62.1.155 . PMC 285968 . PMID 5253652.
- ^ Holick MF, DeLuca HF, Avioli LV (enero de 1972). "Aislamiento e identificación de 25-hidroxicolecalciferol del plasma humano". Archivos de Medicina Interna . 129 (1): 56–61. doi :10.1001/archinte.1972.00320010060005. PMID 4332591.
- ^ Holick MF, MacLaughlin JA, Clark MB, Holick SA, Potts JT, Anderson RR, et al. (octubre de 1980). "Fotosíntesis de previtamina D3 en la piel humana y consecuencias fisiológicas". Science . 210 (4466): 203–5. Bibcode :1980Sci...210..203H. doi :10.1126/science.6251551. JSTOR 1685024. PMID 6251551.
- ^ Rizzoli R (enero de 2021). "Suplementación con vitamina D: ¿se ha revisado el límite superior de seguridad?". Aging Clin Exp Res (revisión). 33 (1): 19–24. doi :10.1007/s40520-020-01678-x. PMC 7897606. PMID 32857334 .
- ^ "Iniciativa de vitamina D de la ODS". Oficina de Suplementos Dietéticos, Institutos Nacionales de Salud de EE. UU. 2018. Archivado desde el original el 26 de enero de 2021. Consultado el 22 de febrero de 2023 .
- ^ Pyrżak B, Witkowska-Sędek E, Krajewska M, Demkow U, Kucharska AM (2015). "Consecuencias metabólicas e inmunológicas de la deficiencia de vitamina D en niños obesos". Metabolismo corporal y ejercicio . Avances en medicina experimental y biología. Vol. 840. Springer. págs. 13–9. doi :10.1007/5584_2014_81. ISBN. 978-3-319-10249-8. Número de identificación personal 25315624. Número de identificación personal 13296456.
- ^ "Vitamina D y prevención del cáncer". Instituto Nacional del Cáncer, Institutos Nacionales de Salud de EE. UU. 21 de octubre de 2013. Archivado desde el original el 13 de febrero de 2015 . Consultado el 15 de diciembre de 2016 .
- ^ Goulão, Beatriz, Stewart, Fiona, Ford, John A., MacLennan, Graeme, Avenell, Alison (2018). "Cáncer y suplementación con vitamina D: una revisión sistemática y metanálisis". The American Journal of Clinical Nutrition . 107 (4): 652–63. doi : 10.1093/ajcn/nqx047 . PMID 29635490.
- ^ Khan SU, Khan MU, Riaz H, Valavoor S, Zhao D, Vaughan L, et al. (agosto de 2019). "Efectos de los suplementos nutricionales y las intervenciones dietéticas en los resultados cardiovasculares: una revisión general y un mapa de evidencia". Anales de Medicina Interna . 171 (3): 190–98. doi :10.7326/m19-0341. PMC 7261374 . PMID 31284304.
- ^ ab "Vitamina D". Pautas para el tratamiento de la enfermedad por coronavirus 2019 (COVID-19) . Institutos Nacionales de Salud (NIH). 26 de septiembre de 2022. Consultado el 4 de julio de 2023 .
 Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público .
Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público . - ^ ab Guía rápida sobre la COVID-19: vitamina D (PDF) (Informe técnico). Instituto Nacional para la Excelencia en la Salud y la Atención (NICE). Diciembre de 2020. ISBN 978-1-4731-3942-8NG187. Archivado desde el original el 3 de diciembre de 2021. Consultado el 22 de febrero de 2021 .
- ^ Revisiones de evidencias sobre el uso de suplementos de vitamina D como prevención y tratamiento de la COVID-19 (PDF) (Informe). Instituto Nacional para la Excelencia en la Salud y la Atención (NICE). Diciembre de 2020. Archivado desde el original el 20 de octubre de 2021. Consultado el 22 de febrero de 2021 .
- ^ Liu N, Sun J, Wang X, Zhang T, Zhao M, Li H (marzo de 2021). "El bajo nivel de vitamina D se asocia con los resultados de la enfermedad por coronavirus 2019: una revisión sistemática y un metanálisis". Revista internacional de enfermedades infecciosas . 104 : 58–64. doi :10.1016/j.ijid.2020.12.077. PMC 7833186 . PMID 33401034.
- ^ ab Kazemi A, Mohammadi V, Aghababaee SK, Golzarand M, Clark CC, Babajafari S (octubre de 2021). "Asociación del estado de vitamina D con la infección por SARS-CoV-2 o la gravedad de la COVID-19: una revisión sistemática y un metanálisis". Avances en nutrición . 12 (5): 1636–58. doi : 10.1093/advances/nmab012 . PMC 7989595 . PMID 33751020.
- ^ ab Petrelli F, Luciani A, Perego G, Dognini G, Colombelli PL, Ghidini A (julio de 2021). "Función terapéutica y pronóstica de la vitamina D para la infección por COVID-19: una revisión sistemática y un metanálisis de 43 estudios observacionales". Revista de bioquímica de esteroides y biología molecular . 211 : 105883. doi : 10.1016/j.jsbmb.2021.105883. PMC 7997262. PMID 33775818 .
- ^ abcd Bassatne A, Basbous M, Chakhtoura M, El Zein O, Rahme M, El-Hajj Fuleihan G (junio de 2021). "El vínculo entre COVID-19 y vitamina D (VIVID): una revisión sistemática y un metanálisis". Metabolismo (revisión sistemática). 119 : 154753. doi :10.1016/j.metabol.2021.154753. PMC 7989070. PMID 33774074 .
- ^ ab Damascena AD, Azevedo LM, Oliveira TA, Santana JD, Pereira M (agosto de 2021). "La adición a la deficiencia de vitamina D agrava la COVID-19: revisión sistemática y metanálisis". Critical Reviews in Food Science and Nutrition . 63 (4): 557–62. doi :10.1080/10408398.2021.1951652. PMID 34384300. S2CID 236997712.
- ^ ab Dissanayake HA, de Silva NL, Sumanatilleke M, de Silva SD, Gamage KK, Dematapitiya C, et al. (abril de 2022). "Papel pronóstico y terapéutico de la vitamina D en la COVID-19: revisión sistemática y metanálisis". Revista de endocrinología clínica y metabolismo . 107 (5): 1484–502. doi :10.1210/clinem/dgab892. PMC 8689831. PMID 34894254 .
- ^ Shah K, Saxena D, Mavalankar D (enero de 2021). "Suplementación con vitamina D, COVID-19 y gravedad de la enfermedad: un metanálisis". QJM: Revista mensual de la Asociación de Médicos . 114 (3): 175–81. doi :10.1093/qjmed/hcab009. PMC 7928587. PMID 33486522 .
- ^ ab Stroehlein JK, Wallqvist J, Iannizzi C, Mikolajewska A, Metzendorf MI, Benstoem C, et al. (mayo de 2021). "Suplementación con vitamina D para el tratamiento de la COVID-19: una revisión sistemática activa". Base de datos Cochrane de revisiones sistemáticas . 2021 (5): CD015043. doi :10.1002/14651858.CD015043. PMC 8406457. PMID 34029377. S2CID 235202971 .
- ^ ab Cheng K, Huang Y, Wang C, Ali W, Karrow NA (septiembre de 2023). "Función fisiológica de la vitamina D 3 en peces". Reseñas en acuicultura . 15 (4): 1732–1748. Código Bibliográfico :2023RvAq...15.1732C. doi :10.1111/raq.12814. ISSN 1753-5123.

