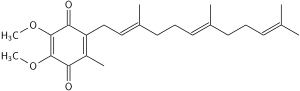
Coenzima Q10
 | |
| Nombres | |
|---|---|
| Nombre IUPAC preferido 2-[(2 mi ,6 mi ,10 mi ,14 mi ,18 mi ,22 mi ,26 mi ,30 mi ,34 mi )-3,7,11,15,19,23,27,31,35, 39-Decametiltetraconta-2,6,10,14,18,22,26,30,34,38-decaen-1-il]-5,6-dimetoxi-3-metilciclohexa-2,5-dieno-1,4 -diona | |
Otros nombres
Q 10 , CoQ 10 / ˌ k oʊ ˌ k juː ˈ t ɛ n / | |
| Identificadores | |
Modelo 3D ( JSmol ) |
|
| EBICh | |
| Química biológica | |
| Araña química | |
| Tarjeta informativa de la ECHA | 100.005.590 |
| BARRIL |
|
Identificador de centro de PubChem |
|
| UNIVERSIDAD | |
Panel de control CompTox ( EPA ) |
|
| |
| |
| Propiedades | |
| C59H90O4 | |
| Masa molar | 863,365 g·mol −1 |
| Apariencia | sólido amarillo o naranja |
| Punto de fusión | 48–52 °C (118–126 °F; 321–325 K) |
| insoluble | |
| Farmacología | |
| C01EB09 ( OMS ) | |
| Compuestos relacionados | |
Quinonas relacionadas | 1,4-Benzoquinona Plastoquinona Ubiquinol |
Salvo que se indique lo contrario, los datos se proporcionan para los materiales en su estado estándar (a 25 °C [77 °F], 100 kPa). | |
La coenzima Q 10 (CoQ 10 / ˌ k oʊ k j uː ˈ t ɛ n / ), también conocida como ubiquinona, es un cofactor bioquímico natural (coenzima) y un antioxidante producido por el cuerpo humano. [1] [2] [3] También se puede obtener de fuentes dietéticas, como carne, pescado, aceites de semillas, verduras y suplementos dietéticos . [1] [2] La CoQ 10 se encuentra en muchos organismos, incluidos animales y bacterias.
La CoQ 10 desempeña un papel en la fosforilación oxidativa mitocondrial , ayudando en la producción de trifosfato de adenosina (ATP), que está involucrado en la transferencia de energía dentro de las células. [1] La estructura de la CoQ 10 consta de una fracción de benzoquinona y una cadena lateral de isoprenoides, donde el "10" se refiere al número de subunidades químicas de isoprenilo en su cola. [4] [5] [6]
Aunque es una molécula omnipresente en los tejidos humanos, la CoQ 10 no es un nutriente dietético y no tiene un nivel de ingesta recomendado , y su uso como suplemento no está asociado ni aprobado para ningún efecto sobre la salud o contra las enfermedades. [1] [2]
Funciones biológicas
La CoQ 10 es un componente de la cadena de transporte de electrones mitocondrial (CTE), donde desempeña un papel en la fosforilación oxidativa, un proceso necesario para la biosíntesis del trifosfato de adenosina, la principal fuente de energía de las células. [1] [6] [7]
La CoQ 10 es una molécula lipofílica que se encuentra en todas las membranas biológicas del cuerpo humano y sirve como componente para la síntesis de ATP y es un cofactor vital para los tres complejos ( complejo I , complejo II y complejo III ) de la cadena de transporte de electrones en las mitocondrias. [1] [5] La CoQ 10 tiene un papel en el transporte de protones a través de las membranas lisosomales para regular el pH en las funciones de los lisosomas. [1]
El proceso de fosforilación oxidativa mitocondrial tiene lugar en la membrana mitocondrial interna de las células eucariotas. [1] Esta membrana está muy plegada en estructuras llamadas crestas, que aumentan la superficie disponible para la fosforilación oxidativa. La CoQ 10 desempeña un papel en este proceso como cofactor esencial de la cadena de transporte de electrones ubicada en la membrana mitocondrial interna y cumple las siguientes funciones: [1] [7]
- Transporte de electrones en la cadena de transporte de electrones mitocondrial, mediante el transporte de electrones desde complejos mitocondriales como el dinucleótido de nicotinamida y adenina (NADH), la ubiquinona reductasa (complejo I) y la succinato ubiquinona reductasa (complejo II), la oxidación de ácidos grasos y aminoácidos de cadena ramificada (a través de deshidrogenasas ligadas a flavina) a la ubiquinol-citocromo-c reductasa (complejo III) de la cadena de transporte de electrones: [1] [7] La CoQ 10 participa en el metabolismo de los ácidos grasos y la glucosa mediante la transferencia de electrones generados a partir de la reducción de los ácidos grasos y la glucosa a los aceptores de electrones; [8]
- Actividad antioxidante como antioxidante liposoluble junto con la vitamina E , eliminando especies reactivas de oxígeno y protegiendo las células contra el estrés oxidativo, [1] [6] inhibiendo la oxidación de proteínas, ADN y el uso de vitamina E. [1] [9]
La CoQ 10 también puede influir en la respuesta inmunitaria al modular la expresión de genes implicados en la inflamación . [10] [11] [12]
Bioquímica
Este artículo necesita la atención de un experto en bioquímica . Consulta la página de discusión para obtener más detalles. ( Abril de 2024 ) |
Las coenzimas Q son una familia de coenzimas que se encuentran en todas partes en los animales y en muchas Pseudomonadota , [13] un grupo de bacterias gramnegativas. El hecho de que la coenzima sea ubicua da origen a su otro nombre, ubiquinona. [1] [2] [14] En los seres humanos, la forma más común de las coenzimas Q es la coenzima Q 10 , también llamada CoQ 10 ( / ˌ k oʊ k j uː ˈ t ɛ n / ) o ubiquinona-10. [1]
La coenzima Q 10 es una 1,4-benzoquinona , en la que "Q" se refiere al grupo químico de la quinona y "10" se refiere al número de subunidades químicas de isoprenilo (mostradas entre paréntesis en el diagrama) en su cola. [1] En las ubiquinonas naturales, hay de seis a diez subunidades en la cola, y los humanos tienen una cola de 10 unidades de isopreno (50 átomos de carbono) conectadas a su "cabeza" de benzoquinona. [1]
Esta familia de sustancias liposolubles está presente en todas las células eucariotas que respiran , principalmente en las mitocondrias. [1] El noventa y cinco por ciento de la energía del cuerpo humano se genera de esta manera. [15] Los órganos con mayores requerimientos energéticos, como el corazón , el hígado y los riñones , tienen las mayores concentraciones de CoQ 10. [16] [17] [18] [19]
Existen tres estados redox de CoQ: completamente oxidado ( ubiquinona ), semiquinona ( ubisemiquinona ) y completamente reducido ( ubiquinol ). [1] La capacidad de esta molécula para actuar como transportador de dos electrones (moviéndose entre la forma quinona y quinol) y transportador de un electrón (moviéndose entre la semiquinona y una de estas otras formas) es fundamental para su papel en la cadena de transporte de electrones debido a los grupos de hierro-azufre que solo pueden aceptar un electrón a la vez, y como antioxidante eliminador de radicales libres. [1] [14]
Deficiencia
Existen dos vías principales de deficiencia de CoQ 10 en humanos: biosíntesis reducida y mayor uso por parte del cuerpo. [10] [20] La biosíntesis es la principal fuente de CoQ 10. La biosíntesis requiere al menos 15 genes , y las mutaciones en cualquiera de ellos pueden causar deficiencia de CoQ. [20] Los niveles de CoQ 10 también pueden verse afectados por otros defectos genéticos (como mutaciones del ADN mitocondrial , ETFDH , APTX , FXN y BRAF , genes que no están directamente relacionados con el proceso biosintético de CoQ 10 ). [20] Algunas de estas, como las mutaciones en COQ6 , pueden conducir a enfermedades graves como el síndrome nefrótico resistente a esteroides con sordera neurosensorial . [21] [22] [23]
Evaluación
Aunque la CoQ 10 se puede medir en el plasma sanguíneo , estas mediciones reflejan la ingesta dietética más que el estado del tejido. Actualmente, la mayoría de los centros clínicos miden los niveles de CoQ 10 en fibroblastos de piel cultivados , biopsias musculares y células mononucleares de la sangre. [ 24] Los fibroblastos cultivados también se pueden utilizar para evaluar la tasa de biosíntesis endógena de CoQ 10 , midiendo la captación de p -hidroxibenzoato marcado con 14 C. [ 25]
Estatinas
Aunque las estatinas pueden reducir la CoQ 10 en la sangre, no está claro si reducen la CoQ 10 en los músculos. [26] La evidencia no respalda que la suplementación mejore los efectos secundarios de las estatinas. [26] [27]
Propiedades químicas
La estructura oxidada de CoQ 10 se muestra a continuación. Los distintos tipos de coenzima Q se pueden distinguir por el número de subunidades isoprenoides en sus cadenas laterales . La coenzima Q más común en las mitocondrias humanas es CoQ 10. [1] Q se refiere a la cabeza de quinona y "10" se refiere al número de repeticiones de isopreno en la cola. La molécula que se muestra a continuación tiene tres unidades isoprenoides y se llamaría Q 3 .
En estado puro, es un polvo lipófilo de color naranja y no tiene sabor ni olor. [14]
Biosíntesis
La biosíntesis se produce en la mayoría de los tejidos humanos y consta de tres pasos principales:
- Creación de la estructura de la benzoquinona (utilizando fenilalanina o tirosina , mediante 4-hidroxibenzoato )
- Creación de la cadena lateral de isopreno (utilizando acetil-CoA )
- La unión o condensación de las dos estructuras anteriores.
Las dos reacciones iniciales ocurren en las mitocondrias , el retículo endoplásmico y los peroxisomas , lo que indica múltiples sitios de síntesis en las células animales. [28]
Una enzima importante en esta vía es la HMG-CoA reductasa , que suele ser un objetivo de intervención en las complicaciones cardiovasculares. La familia de medicamentos para reducir el colesterol, las "estatinas", inhibe la HMG-CoA reductasa. Un posible efecto secundario de las estatinas es la disminución de la producción de CoQ 10 , que puede estar relacionada con el desarrollo de miopatía y rabdomiólisis . Sin embargo, el papel que desempeñan las estatinas en la deficiencia de CoQ es controvertido. Aunque las estatinas reducen los niveles sanguíneos de CoQ, aún quedan estudios sobre los efectos de los niveles musculares de CoQ. La suplementación con CoQ tampoco reduce los efectos secundarios de los medicamentos con estatinas. [24] [26]
Los genes involucrados incluyen PDSS1 , PDSS2 , COQ2 y ADCK3 ( COQ8 , CABC1 ). [29]
Otros organismos, además de los humanos, producen las estructuras de benzoquinona e isopreno a partir de sustancias químicas de origen algo diferentes. Por ejemplo, la bacteria E. coli produce la primera a partir de corismato y la segunda a partir de una fuente distinta del mevalonato . Sin embargo, la levadura común S. cerevisiae obtiene la primera a partir de corismato o tirosina y la segunda a partir del mevalonato . La mayoría de los organismos comparten el intermediario común 4-hidroxibenzoato, pero nuevamente utilizan diferentes pasos para llegar a la estructura "Q". [30]
Suplemento dietético
Aunque no es un medicamento recetado ni un nutriente esencial , la CoQ 10 se usa comúnmente como un suplemento dietético con la intención de prevenir o mejorar enfermedades, como los trastornos cardiovasculares. [2] [31] La CoQ 10 es producida naturalmente por el cuerpo y juega un papel crucial en el crecimiento y la protección celular. [6] A pesar de su importante papel en el cuerpo, no se usa como medicamento para el tratamiento de ninguna enfermedad específica. [1] [2] [3]
Sin embargo, la CoQ 10 está ampliamente disponible como un suplemento dietético de venta libre y es recomendada por algunos profesionales de la salud, a pesar de la falta de evidencia científica definitiva que respalde estas recomendaciones, [1] [3] especialmente cuando se trata de enfermedades cardiovasculares. [32]
Reglamento y composición
La CoQ 10 no está aprobada por la Administración de Alimentos y Medicamentos de los Estados Unidos (FDA) para el tratamiento de ninguna condición médica. [33] [34] [35] [36] Sin embargo, se vende como un suplemento dietético que no está sujeto a las mismas regulaciones que los medicamentos y es un ingrediente en algunos cosméticos. [37] La fabricación de CoQ 10 no está regulada y los diferentes lotes y marcas pueden variar significativamente. [35]
Investigación
Una revisión Cochrane de 2014 no encontró evidencia suficiente para llegar a una conclusión sobre su uso para la prevención de enfermedades cardíacas. [38] Una revisión Cochrane de 2016 concluyó que la CoQ 10 no tenía efecto sobre la presión arterial . [39] Una revisión Cochrane de 2021 no encontró "evidencia convincente para apoyar o refutar" el uso de CoQ 10 para el tratamiento de la insuficiencia cardíaca. [40]
Un metaanálisis de 2017 de personas con insuficiencia cardíaca que tomaron 30–100 mg/día de CoQ10 encontró una mortalidad un 31% menor y una mayor capacidad de ejercicio, sin diferencias significativas en los puntos finales de la fracción de eyección del corazón izquierdo. [41] Un metaanálisis de 2021 encontró que la coenzima Q10 se asoció con una mortalidad por todas las causas un 31% menor en pacientes con IC. [42] En un metaanálisis de 2023 de personas mayores, la ubiquinona tuvo evidencia de un efecto cardiovascular, pero el ubiquinol no. [43]
Aunque se ha estudiado la CoQ 10 como un posible remedio para tratar los supuestos efectos secundarios musculares relacionados con las estatinas , los resultados fueron mixtos. Aunque un metanálisis de 2018 concluyó que existía evidencia preliminar de que la CoQ 10 oral reducía los síntomas musculares asociados a las estatinas, incluidos el dolor muscular, la debilidad muscular, los calambres musculares y el cansancio muscular, [44] los metanálisis de 2015 [45] y 2024 [32] encontraron que la CoQ 10 no tenía efecto sobre la miopatía por estatinas. [45] [32]
Farmacología
Absorción
La CoQ 10 en forma pura es un polvo cristalino insoluble en agua. La absorción como sustancia farmacológica sigue el mismo proceso que la de los lípidos; el mecanismo de captación parece ser similar al de la vitamina E , otro nutriente liposoluble. [19] Este proceso en el cuerpo humano implica la secreción en el intestino delgado de enzimas pancreáticas y bilis , lo que facilita la emulsificación y la formación de micelas necesarias para la absorción de sustancias lipofílicas . [46] La ingesta de alimentos (y la presencia de lípidos) estimula la excreción biliar corporal de ácidos biliares y mejora en gran medida la absorción de CoQ 10. La CoQ 10 exógena se absorbe en el intestino delgado y se absorbe mejor si se toma con una comida. La concentración sérica de CoQ 10 en condiciones de alimentación es mayor que en condiciones de ayuno. [47] [48]
Metabolismo
La CoQ10 se metaboliza en todos los tejidos y sus metabolitos se fosforilan en las células. [2] La CoQ10 se reduce a ubiquinol durante o después de su absorción en el intestino delgado . [2] Es absorbida por los quilomicrones y redistribuida en la sangre dentro de las lipoproteínas . [2] Su eliminación se produce por excreción biliar y fecal . [2]
Farmacocinética
Se han publicado algunos informes sobre la farmacocinética de la CoQ 10. El pico plasmático se puede observar entre 6 y 8 horas después de la administración oral cuando se toma como sustancia farmacológica. [2] En algunos estudios, también se observó un segundo pico plasmático aproximadamente 24 horas después de la administración, probablemente debido tanto al reciclaje enterohepático como a la redistribución desde el hígado a la circulación. [46]
Se utilizó CoQ 10 cristalino marcado con deuterio para investigar la farmacocinética en humanos y determinar un tiempo medio de eliminación de 33 horas. [49]
Biodisponibilidad
A diferencia de la ingesta de CoQ 10 como componente de los alimentos, como los frutos secos o la carne, de los que normalmente se absorbe, existe una preocupación sobre la biodisponibilidad de CoQ 10 cuando se toma como suplemento dietético. [50] [51] La biodisponibilidad de los suplementos de CoQ 10 puede verse reducida debido a la naturaleza lipofílica de su molécula y su gran peso molecular. [50]
Reducción del tamaño de partículas
Las nanopartículas se han explorado como un sistema de administración para varios fármacos, como mejorar la biodisponibilidad oral de fármacos con características de absorción deficientes. [52] Sin embargo, esto no ha demostrado ser exitoso con CoQ 10 , aunque los informes han diferido ampliamente. [53] [54] El uso de una suspensión acuosa de CoQ 10 finamente pulverizado en agua pura también revela solo un efecto menor. [55]
Solubilidad en agua
Facilitar la absorción de fármacos aumentando su solubilidad en agua es una estrategia farmacéutica común y también se ha demostrado que tiene éxito para la CoQ 10. Se han desarrollado varios enfoques para lograr este objetivo, y muchos de ellos producen resultados significativamente mejores que las cápsulas de gelatina blanda a base de aceite a pesar de los muchos intentos de optimizar su composición. [19] Ejemplos de dichos enfoques son el uso de la dispersión acuosa de CoQ 10 sólida con el polímero tiloxapol , [56] formulaciones basadas en varios agentes solubilizantes, como lecitina hidrogenada, [57] y la complejación con ciclodextrinas ; entre estas últimas, se ha descubierto que el complejo con β-ciclodextrina tiene una biodisponibilidad muy aumentada [58] [59] y también se utiliza en las industrias farmacéutica y alimentaria para la fortificación de CoQ 10. [19]
Efectos adversos y precauciones
En general, la suplementación oral con CoQ10 es bien tolerada. [1] Los efectos secundarios más comunes son síntomas gastrointestinales ( náuseas , vómitos, supresión del apetito y dolor abdominal ), erupciones cutáneas y dolores de cabeza. [60] Se han reportado algunos efectos adversos, principalmente gastrointestinales, con la ingesta. [2] Las dosis de 100 a 300 mg por día pueden inducir insomnio o elevar las enzimas hepáticas . [2] El método de evaluación de riesgos de nivel seguro observado indicó que la evidencia de seguridad es aceptable en ingestas de hasta 1200 mg por día. [61]
No se recomienda el uso de suplementos de CoQ10 en personas con enfermedades hepáticas o renales , durante el embarazo o la lactancia, ni en ancianos. [2]
Posibles interacciones farmacológicas
La CoQ 10 tomada como sustancia farmacológica tiene el potencial de inhibir los efectos de la teofilina , así como del anticoagulante warfarina ; la CoQ 10 puede interferir con las acciones de la warfarina al interactuar con las enzimas del citocromo p450, reduciendo así el INR , una medida de la coagulación sanguínea. [62] La estructura de la CoQ 10 es similar a la de la vitamina K , que compite con los efectos anticoagulantes de la warfarina y los contrarresta. No se recomienda la CoQ 10 en personas que toman warfarina debido al mayor riesgo de coagulación. [60]
Concentraciones dietéticas
En 2010 se publicaron revisiones detalladas sobre la aparición de CoQ 10 y la ingesta dietética . [63] Además de la síntesis endógena dentro de los organismos, la CoQ 10 también se suministra a través de varios alimentos. [1] Las concentraciones de CoQ 10 en varios alimentos son: [1]
| Alimento | Concentración de CoQ10 (mg/kg) | |
|---|---|---|
| Aceites vegetales | aceite de soja | 54–280 |
| aceite de oliva | 40–160 | |
| aceite de semilla de uva | 64–73 | |
| aceite de girasol | 4–15 | |
| aceite de canola | 64–73 | |
| Carne de res | corazón | 113 |
| hígado | 39–50 | |
| músculo | 26–40 | |
| Cerdo | corazón | 12–128 |
| hígado | 23–54 | |
| músculo | 14–45 | |
| Pollo | mama | 8–17 |
| hermético | 24–25 | |
| ala | 11 | |
| Pez | sardina | 5–64 |
| caballa – pulpa roja | 43–67 | |
| caballa – carne blanca | 11–16 | |
| salmón | 4–8 | |
| atún | 5 | |
| Cojones | maní | 27 |
| nuez | 19 | |
| semilla de sésamo | 18–23 | |
| pistacho | 20 | |
| avellana | 17 | |
| almendra | 5–14 | |
| Verduras | perejil | 8–26 |
| brócoli | 6–9 | |
| coliflor | 2–7 | |
| espinaca | hasta 10 | |
| col china | 2–5 | |
| Fruta | palta | 10 |
| grosella negra | 3 | |
| uva | 6–7 | |
| fresa | 1 | |
| naranja | 1–2 | |
| pomelo | 1 | |
| manzana | 1 | |
| banana | 1 | |
Los aceites vegetales, la carne y el pescado son bastante ricos en niveles de CoQ 10. [1] Los productos lácteos son fuentes mucho más pobres de CoQ 10 que los tejidos animales. Entre las verduras, el brócoli y la coliflor son buenas fuentes de CoQ 10. [1] La mayoría de las frutas y bayas son fuentes pobres de CoQ 10 , con la excepción de los aguacates , que tienen un contenido relativamente alto de aceite y CoQ 10. [63]
Consumo
En el mundo desarrollado, la ingesta diaria estimada de CoQ 10 se ha determinado en 3 a 6 mg por día, derivada principalmente de la carne. [63]
Los surcoreanos tienen una ingesta diaria promedio estimada de CoQ (Q 9 + Q 10 ) de 11,6 mg/d, derivada principalmente del kimchi . [64]
Efecto del calor y el procesamiento.
Cocinar mediante fritura reduce el contenido de CoQ 10 entre un 14 y un 32 %. [65]
Historia
En 1950, se aisló una pequeña cantidad de CoQ 10 del revestimiento del intestino de un caballo, un compuesto inicialmente llamado sustancia SA , pero que luego se consideró que era quinona que se encuentra en muchos tejidos animales. [66] En 1957, el mismo compuesto se aisló de las membranas mitocondriales del corazón de res, y las investigaciones demostraron que transportaba electrones dentro de las mitocondrias. Se llamó Q-275 como quinona. [66] [67] La Q-275/sustancia SA fue posteriormente rebautizada como ubiquinona , ya que era una quinona ubicua que se encuentra en todos los tejidos animales. [66] En 1958, se informó su estructura química completa. [66] [68] La ubiquinona fue posteriormente llamada mitoquinona o coenzima Q debido a su participación en la cadena de transporte de electrones mitocondrial. [66] En 1966, un estudio informó que la CoQ 6 reducida era un antioxidante eficaz en las células. [69]
Véase también
- Idebenona : análogo sintético con propiedades generadoras de oxidantes reducidas
- Mesilato de mitoquinona : análogo sintético con permeabilidad mitocondrial mejorada
Referencias
- ^ abcdefghijklmnopqrstu vwxyz aa «Coenzima Q10». Centro de Información sobre Micronutrientes, Instituto Linus Pauling, Universidad Estatal de Oregón. 2018. Archivado desde el original el 15 de marzo de 2024. Consultado el 13 de abril de 2024 .
- ^ abcdefghijklmn Sood B, Preeti Patel P, Keenaghan M (30 de enero de 2024). "Coenzima Q10". StatPearls, Biblioteca Nacional de Medicina de EE. UU. PMID 30285386. Archivado desde el original el 2 de octubre de 2023. Consultado el 17 de abril de 2024 .
- ^ abc «Coenzima Q10». Centro Nacional de Salud Complementaria e Integral, Institutos Nacionales de Salud de EE. UU. Enero de 2019. Archivado desde el original el 4 de abril de 2024. Consultado el 13 de abril de 2024 .
- ^ Mantle D, Lopez-Lluch G, Hargreaves IP (enero de 2023). "Metabolismo de la coenzima Q10: una revisión de cuestiones no resueltas". Revista internacional de ciencias moleculares . 24 (3): 2585. doi : 10.3390/ijms24032585 . PMC 9916783 . PMID 36768907. Este artículo incorpora texto de esta fuente, que está disponible bajo la licencia CC BY 4.0.
- ^ ab Kadian M, Sharma G, Pandita S, Sharma K, Shrivasatava K, Saini N, et al. (2022). "El impacto de la coenzima Q10 en la neurodegeneración: una revisión exhaustiva". Current Pharmacology Reports . 8 : 1–19. doi :10.1007/s40495-021-00273-6.
- ^ abcd Mantle D, Heaton RA, Hargreaves IP (mayo de 2021). "Coenzima Q10 y función inmunitaria: una descripción general". Antioxidantes . 10 (5): 759. doi : 10.3390/antiox10050759 . PMC 8150987 . PMID 34064686. Este artículo incorpora texto de esta fuente, que está disponible bajo la licencia CC BY 4.0.
- ^ abc Pradhan N, Singh C, Singh A (noviembre de 2021). "La coenzima Q10 es un restaurador mitocondrial para diversos trastornos cerebrales". Naunyn Schmiedebergs Arch Pharmacol . 394 (11): 2197–2222. doi :10.1007/s00210-021-02161-8. PMID 34596729.
- ^ Manzar H, Abdulhussein D, Yap TE, Cordeiro MF (diciembre de 2020). "Consecuencias celulares de la deficiencia de coenzima Q10 en la neurodegeneración de la retina y el cerebro". Int J Mol Sci . 21 (23): 9299. doi : 10.3390/ijms21239299 . PMC 7730520 . PMID 33291255. Este artículo incorpora texto de esta fuente, que está disponible bajo la licencia CC BY 4.0.
- ^ Di Lorenzo A, Iannuzzo G, Parlato A, Cuomo G, Testa C, Coppola M, et al. (abril de 2020). "Evidencia clínica de la suplementación con coenzima Q10 en la insuficiencia cardíaca: de la mejora energética a la funcional". J Clin Med . 9 (5): 1266. doi : 10.3390/jcm9051266 . PMC 7287951 . PMID 32349341. Este artículo incorpora texto de esta fuente, que está disponible bajo la licencia CC BY 4.0.
- ^ ab Hargreaves I, Heaton RA, Mantle D (septiembre de 2020). "Trastornos del metabolismo de la coenzima Q10 humana: una descripción general". Int J Mol Sci . 21 (18): 6695. doi : 10.3390/ijms21186695 . PMC 7555759 . PMID 32933108. Este artículo incorpora texto de esta fuente, que está disponible bajo la licencia CC BY 4.0.
- ^ Mantle D, Millichap L, Castro-Marrero J, Hargreaves IP (agosto de 2023). "Deficiencia primaria de coenzima Q10: una actualización". Antioxidantes . 12 (8): 1652. doi : 10.3390/antiox12081652 . PMC 10451954 . PMID 37627647. Este artículo incorpora texto de esta fuente, que está disponible bajo la licencia CC BY 4.0.
- ^ Barcelos IP, Haas RH (mayo de 2019). "CoQ10 y envejecimiento". Biología . 8 (2): 28. doi : 10.3390/biology8020028 . PMC 6627360 . PMID 31083534. Este artículo incorpora texto de esta fuente, que está disponible bajo la licencia CC BY 4.0.
- ^ Nowicka B, Kruk J (septiembre de 2010). "Presentación, biosíntesis y función de quinonas isoprenoides". Biochimica et Biophysica Acta (BBA) - Bioenergética . 1797 (9): 1587-1605. doi : 10.1016/j.bbabio.2010.06.007 . PMID 20599680.
- ^ abc
 Este artículo incorpora material de dominio público de "Ubidecarenona". PubChem . Biblioteca Nacional de Medicina de EE. UU. 30 de marzo de 2024 . Consultado el 4 de abril de 2024 .
Este artículo incorpora material de dominio público de "Ubidecarenona". PubChem . Biblioteca Nacional de Medicina de EE. UU. 30 de marzo de 2024 . Consultado el 4 de abril de 2024 . - ^ Ernster L, Dallner G (mayo de 1995). "Aspectos bioquímicos, fisiológicos y médicos de la función de la ubiquinona". Biochimica et Biophysica Acta (BBA) - Base molecular de la enfermedad . 1271 (1): 195–204. doi : 10.1016/0925-4439(95)00028-3 . PMID 7599208.
- ^ Okamoto T, Matsuya T, Fukunaga Y, Kishi T, Yamagami T (1989). "Niveles de ubiquinol-10 en suero humano y relación con los lípidos séricos". Revista internacional de investigación sobre vitaminas y nutrición. Internationale Zeitschrift Fur Vitamin- und Ernahrungsforschung. Revista Internacional de Vitaminología y Nutrición . 59 (3): 288–292. PMID 2599795.
- ^ Aberg F, Appelkvist EL, Dallner G, Ernster L (junio de 1992). "Distribución y estado redox de las ubiquinonas en tejidos humanos y de ratas". Archivos de bioquímica y biofísica . 295 (2): 230–234. doi :10.1016/0003-9861(92)90511-T. PMID 1586151.
- ^ Shindo Y, Witt E, Han D, Epstein W, Packer L (enero de 1994). "Antioxidantes enzimáticos y no enzimáticos en la epidermis y la dermis de la piel humana". The Journal of Investigative Dermatology . 102 (1): 122–124. doi :10.1111/1523-1747.ep12371744. PMID 8288904.
- ^ abcd Žmitek J, ŽMitek K, Pravs I (2008). "Mejora de la biodisponibilidad de la coenzima q10 de la teoría a la práctica". Industria agroalimentaria de alta tecnología . Archivado desde el original el 23 de abril de 2024. Consultado el 5 de abril de 2024 .
- ^ abc Desbats MA, Lunardi G, Doimo M, Trevisson E, Salviati L (enero de 2015). "Bases genéticas y manifestaciones clínicas de la deficiencia de coenzima Q10 (CoQ 10)". J Inherit Metab Dis . 38 (1): 145–56. doi :10.1007/s10545-014-9749-9. PMID 25091424.
- ^ Heeringa SF, Chernin G, Chaki M, Zhou W, Sloan AJ, Ji Z, et al. (2011). "Las mutaciones de COQ6 en pacientes humanos producen síndrome nefrótico con sordera neurosensorial". Journal of Clinical Investigation . 121 (5): 2013–2024. doi :10.1172/JCI45693. PMC 3083770 . PMID 21540551.
- ^ Justine Perrin R, Rousset-Rouvière C, Garaix F, Cano A, Conrath J, Boyer O, et al. (2020). "Mutación de COQ6 en pacientes con síndrome nefrótico, sordera neurosensorial y atrofia óptica". Jimd Reports . 54 (1): 37–44. doi :10.1002/jmd2.12068. PMC 7358665 . PMID 32685349.
- ^ "Síndrome nefrótico asociado a COQ6 (identificación conceptual: C4054393) - MedGen - NCBI". Archivado desde el original el 6 de abril de 2024. Consultado el 6 de abril de 2024 .
- ^ ab Trevisson E, DiMauro S, Navas P, Salviati L (octubre de 2011). "Deficiencia de coenzima Q en el músculo". Current Opinion in Neurology . 24 (5): 449–456. doi :10.1097/WCO.0b013e32834ab528. hdl : 10261/129020 . PMID 21844807.
- ^ Montero R, Sánchez-Alcázar JA, Briones P, Hernández AR, Cordero MD, Trevisson E, et al. (junio de 2008). "Análisis de la coenzima Q10 en músculo y fibroblastos para el diagnóstico de síndromes de deficiencia de CoQ 10 ". Bioquímica clínica . 41 (9): 697–700. doi :10.1016/j.clinbiochem.2008.03.007. hdl : 11577/2447079 . PMID 18387363.
- ^ abc Tan JT, Barry AR (junio de 2017). "Suplementación con coenzima Q10 en el tratamiento de la mialgia asociada a las estatinas". American Journal of Health-System Pharmacy . 74 (11): 786–793. doi : 10.2146/ajhp160714 . PMID 28546301. S2CID 3825396.
- ^ Kennedy C, Köller Y, Surkova E (1 de abril de 2020). "Efecto de la coenzima Q10 en la mialgia asociada a las estatinas y la adherencia a la terapia con estatinas: una revisión sistemática y un metanálisis". Aterosclerosis . 299 : 1–8. doi : 10.1016/j.atherosclerosis.2020.03.006 . PMID 32179207.
- ^ Bentinger M, Tekle M, Dallner G (mayo de 2010). "Coenzima Q: biosíntesis y funciones". Comunicaciones de investigación bioquímica y biofísica . 396 (1): 74–79. doi :10.1016/j.bbrc.2010.02.147. PMID 20494114.
- ^ Espinós C, Felipo V, Palau F (2009). Enfermedades neuromusculares hereditarias: traducción de los mecanismos patológicos a las terapias. Springer. pp. 122ff. ISBN 978-90-481-2812-9. Recuperado el 4 de enero de 2011 .
- ^ Meganathan R (septiembre de 2001). "Biosíntesis de ubiquinona en microorganismos". FEMS Microbiology Letters . 203 (2): 131–139. doi : 10.1111/j.1574-6968.2001.tb10831.x . PMID 11583838.
- ^ Arenas-Jal M, Suñé-Negre JM, García-Montoya E (marzo de 2020). "Suplementación con coenzima Q10: eficacia, seguridad y desafíos de formulación". Revisiones exhaustivas en ciencia y seguridad alimentaria . 19 (2): 574–594. doi :10.1111/1541-4337.12539. hdl : 2445/181270 . PMID: 33325173.
- ^ abc Bjørklund G, Semenova Y, Gasmi A, Indika NR, Hrynovets I, Lysiuk R, et al. (2024). "Coenzima Q10 para mejorar la actividad física y prolongar el ciclo de vida humano". Curr Med Chem . 31 (14): 1804–1817. doi :10.2174/0929867330666230228103913. PMID 36852817.
- ^
 Este artículo incorpora material de dominio público de Coenzima Q10. Instituto Nacional del Cáncer . Abril de 2022.
Este artículo incorpora material de dominio público de Coenzima Q10. Instituto Nacional del Cáncer . Abril de 2022. - ^ Consejo editorial del PDQ sobre terapias complementarias, alternativas e integrales (2002). Coenzima Q10: versión para profesionales de la salud . Consejo editorial del PDQ sobre terapias complementarias, alternativas e integrales. PMID 26389329.
- ^ ab
 Este artículo incorpora material de dominio público de White J (14 de mayo de 2014). PDQ Coenzima Q10. Instituto Nacional del Cáncer , Institutos Nacionales de Salud , Departamento de Salud y Servicios Humanos de EE. UU . . Consultado el 29 de junio de 2014 .
Este artículo incorpora material de dominio público de White J (14 de mayo de 2014). PDQ Coenzima Q10. Instituto Nacional del Cáncer , Institutos Nacionales de Salud , Departamento de Salud y Servicios Humanos de EE. UU . . Consultado el 29 de junio de 2014 . - ^ "Trastornos mitocondriales en niños: coenzima Q10". nice.org.uk . Reino Unido: Instituto Nacional para la Excelencia en la Salud y la Atención. 28 de marzo de 2017. Archivado desde el original el 10 de octubre de 2019 . Consultado el 10 de octubre de 2019 .
- ^ Hojerová J (mayo de 2000). "[Coenzima Q10: su importancia, propiedades y uso en nutrición y cosmética]". Ceska a Slovenska Farmacie . 49 (3): 119–123. PMID 10953455.
- ^ Flowers N, Hartley L, Todkill D, Stranges S, Rees K (4 de diciembre de 2014). "Suplementación con coenzima Q10 para la prevención primaria de la enfermedad cardiovascular". Base de datos Cochrane de revisiones sistemáticas . 2014 (12): CD010405. doi : 10.1002 /14651858.CD010405.pub2. PMC 9759150. PMID 25474484.
- ^ Ho MJ, Li EC, Wright JM (marzo de 2016). "Eficacia de la coenzima Q10 para reducir la presión arterial en la hipertensión primaria". Base de datos Cochrane de revisiones sistemáticas . 2016 (3): CD007435. doi : 10.1002/14651858.CD007435.pub3. PMC 6486033. PMID 26935713.
- ^ Al Saadi T, Assaf Y, Farwati M, Turkmani K, Al-Mouakeh A, Shebli B, et al. (Grupo Cochrane de Cardiología) (febrero de 2021). "Coenzima Q10 para la insuficiencia cardíaca". Base de datos Cochrane de revisiones sistemáticas . 2021 (2): CD008684. doi : 10.1002 /14651858.CD008684.pub3. PMC 8092430. PMID 35608922.
- ^ Lei L, Liu Y (julio de 2017). "Eficacia de la coenzima Q10 en pacientes con insuficiencia cardíaca: un metaanálisis de ensayos clínicos". BMC Cardiovascular Disorders . 17 (1): 196. doi : 10.1186/s12872-017-0628-9 . PMC 5525208 . PMID 28738783. Este artículo incorpora texto de esta fuente, que está disponible bajo la licencia CC BY 4.0.
- ^ Khan MS, Khan F, Fonarow GC, Sreenivasan J, Greene SJ, Khan SU, et al. (junio de 2021). «Intervenciones dietéticas y suplementos nutricionales para la insuficiencia cardíaca: una evaluación sistemática y un mapa de evidencia». Revista Europea de Insuficiencia Cardíaca . 23 (9): 1468–1476. doi :10.1002/ejhf.2278. ISSN 1388-9842. PMID 34173307. Archivado desde el original el 2 de enero de 2023 . Consultado el 10 de junio de 2024 .
- ^ Fladerer JP, Grollitsch S (diciembre de 2023). "Comparación de la coenzima Q10 (ubiquinona) y la coenzima Q10 reducida (ubiquinol) como suplemento para prevenir enfermedades cardiovasculares y reducir la mortalidad cardiovascular". Current Cardiology Reports . 25 (12): 1759–1767. doi : 10.1007/s11886-023-01992-6 . PMC 10811087 . PMID 37971634.
- ^ Qu H, Guo M, Chai H, Wang WT, Gao ZY, Shi DZ (octubre de 2018). "Efectos de la coenzima Q10 en la miopatía inducida por estatinas: un metaanálisis actualizado de ensayos controlados aleatorizados". Revista de la Asociación Estadounidense del Corazón . 7 (19): e009835. doi :10.1161/JAHA.118.009835. PMC 6404871. PMID 30371340 . Este artículo incorpora texto de esta fuente, que está disponible bajo la licencia CC BY 4.0.
- ^ ab Banach M, Serban C, Sahebkar A, Ursoniu S, Rysz J, Muntner P, et al. (enero de 2015). "Efectos de la coenzima Q10 en la miopatía inducida por estatinas: un metaanálisis de ensayos controlados aleatorizados". Mayo Clinic Proceedings (revisión sistemática y metaanálisis). 90 (1): 24–34. doi :10.1016/j.mayocp.2014.08.021. PMID 25440725.
- ^ ab Bhagavan HN, Chopra RK (mayo de 2006). "Coenzima Q10: absorción, captación tisular, metabolismo y farmacocinética". Free Radical Research . 40 (5): 445–453. doi :10.1080/10715760600617843. PMID 16551570. S2CID 39001523.
- ^ Bogentoft C, Edlund PO, Olsson B, Widlund L, Westensen K (1991). "Aspectos biofarmacéuticos de la administración intravenosa y oral de coenzima Q10". Aspectos biomédicos y clínicos de la coenzima Q. Vol. 6. págs. 215–224.
- ^ Ochiai A, Itagaki S, Kurokawa T, Kobayashi M, Hirano T, Iseki K (agosto de 2007). "Mejora de la absorción intestinal de la coenzima q10 mediante la ingesta de alimentos". Yakugaku Zasshi . 127 (8): 1251-1254. doi : 10.1248/yakushi.127.1251 . hdl : 2115/30144 . PMID 17666877.[ verificación necesaria ]
- ^ Tomono Y, Hasegawa J, Seki T, Motegi K, Morishita N (octubre de 1986). "Estudio farmacocinético de la coenzima Q10 marcada con deuterio en el hombre". Revista internacional de farmacología clínica, terapia y toxicología . 24 (10): 536–541. PMID 3781673.
- ^ ab Mantle D, Dybring A (2020). "Biodisponibilidad de la coenzima Q10: descripción general del proceso de absorción y metabolismo posterior". Antioxidantes . 9 (5): 386. doi : 10.3390/antiox9050386 . PMC 7278738 . PMID 32380795.
- ^ Martucci A, Reurean-Pintilei D, Manole A (2019). "Biodisponibilidad y concentraciones plasmáticas sostenidas de CoQ10 en voluntarios sanos mediante una nueva preparación oral de liberación controlada". Nutrients . 11 (3): 527. doi : 10.3390/nu11030527 . PMC 6471387 . PMID 30823449.
- ^ Mathiowitz E, Jacob JS, Jong YS, Carino GP, Chickering DE, Chaturvedi P, et al. (marzo de 1997). "Microesferas erosionables biológicamente como sistemas potenciales de administración oral de fármacos". Nature . 386 (6623): 410–414. Bibcode :1997Natur.386..410M. doi :10.1038/386410a0. PMID 9121559. S2CID 4324209.
- ^ Hsu CH, Cui Z, Mumper RJ, Jay M (2003). "Preparación y caracterización de nuevas nanopartículas de coenzima Q10 diseñadas a partir de precursores de microemulsión". AAPS PharmSciTech . 4 (3): E32. doi :10.1208/pt040332. PMC 2750625 . PMID 14621964. [ verificación necesaria ]
- ^ Joshi SS, Sawant SV, Shedge A, Halpner AD (enero de 2003). "Biodisponibilidad comparativa de dos nuevas preparaciones de coenzima Q10 en humanos". Revista internacional de farmacología clínica y terapéutica . 41 (1): 42–48. doi :10.5414/CPP41042. PMID 12564745.[ verificación necesaria ]
- ^ Ozawa Y, Mizushima Y, Koyama I, Akimoto M, Yamagata Y, Hayashi H, et al. (Abril de 1986). "Mejora de la absorción intestinal de la coenzima Q10 con una microesfera lipídica". Arzneimittel-Forschung . 36 (4): 689–690. PMID 3718593.
- ^ US 6197349, Westesen K, Siekmann B, "Partículas con propiedades fisicoquímicas modificadas, su preparación y usos", publicado en 2001
- ^ US 4483873, Ohashi H, Takami T, Koyama N, Kogure Y, Ida K, "Solución acuosa que contiene ubidecarenona", publicada en 1984
- ^ Zmitek J, Smidovnik A, Fir M, Prosek M, Zmitek K, Walczak J, et al. (2008). "Biodisponibilidad relativa de dos formas de una nueva coenzima Q10 soluble en agua". Anales de nutrición y metabolismo . 52 (4): 281–287. doi :10.1159/000129661. PMID 18645245. S2CID 825159.
- ^ Kagan D, Madhavi D (2010). "Un estudio sobre la biodisponibilidad de un nuevo complejo de coenzima Q 10 -β-ciclodextrina de liberación sostenida ". Medicina Integrativa . 9 (1).
- ^ ab Wyman M, Leonard M, Morledge T (julio de 2010). "Coenzima Q10: ¿una terapia para la hipertensión y la mialgia inducida por estatinas?". Cleveland Clinic Journal of Medicine . 77 (7): 435–442. doi : 10.3949/ccjm.77a.09078 . PMID 20601617. S2CID 26572524.
- ^ Hathcock JN, Shao A (agosto de 2006). "Evaluación de riesgos de la coenzima Q10 (ubiquinona)". Toxicología y farmacología regulatorias . 45 (3): 282–288. doi :10.1016/j.yrtph.2006.05.006. PMID 16814438.
- ^ Sharma A, Fonarow GC, Butler J, Ezekowitz JA, Felker GM (abril de 2016). "Coenzima Q10 e insuficiencia cardíaca: una revisión de vanguardia". Circulation: Heart Failure . 9 (4): e002639. doi : 10.1161/CIRCHEARTFAILURE.115.002639 . PMID 27012265. S2CID 2034503.
- ^ abcd Pravst I, Zmitek K, Zmitek J (abril de 2010). "Contenido de coenzima Q10 en alimentos y estrategias de fortificación". Critical Reviews in Food Science and Nutrition . 50 (4): 269–280. doi :10.1080/10408390902773037. PMID 20301015. S2CID 38779392.
- ^ Pyo Y, Oh H (2011). "Contenido de ubiquinona en alimentos fermentados coreanos e ingesta diaria promedio". Revista de composición y análisis de alimentos . 24 (8): 1123–1129. doi :10.1016/j.jfca.2011.03.018.
- ^ Weber C, Bysted A, Hłlmer G (1997). "El contenido de coenzima Q10 de la dieta danesa media". Revista internacional de investigación sobre vitaminas y nutrición. Internationale Zeitschrift Fur Vitamin- und Ernahrungsforschung. Revista Internacional de Vitaminología y Nutrición . 67 (2): 123-129. PMID 9129255.
- ^ abcde Morton RA (diciembre de 1958). "Ubiquinona". Nature . 182 (4652): 1764–1767. Bibcode :1958Natur.182.1764M. doi :10.1038/1821764a0. PMID 13622652.
- ^ Crane FL, Hatefi Y, Lester RL, Widmer C (julio de 1957). "Aislamiento de una quinona de mitocondrias de corazón de res". Biochimica et Biophysica Acta . 25 (1): 220–221. doi :10.1016/0006-3002(57)90457-2. PMID 13445756.
- ^ Wolf DE (1958). "Estudios de la estructura de la coenzima QI en el grupo de la coenzima Q". Revista de la Sociedad Química Americana . 80 (17): 4752. doi :10.1021/ja01550a096. ISSN 0002-7863.
- ^ Mellors A, Tappel AL (julio de 1966). "Quinonas y quinoles como inhibidores de la peroxidación lipídica". Lípidos . 1 (4): 282–284. doi :10.1007/BF02531617. PMID 17805631. S2CID 2129339.