Bcl-2
| BCL2 | |||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| Identificadores | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Alias | BCL2 , Bcl-2, PPP1R50, LCC/linfoma de células B 2, regulador de apoptosis, regulador de apoptosis BCL2, genes, bcl-2 | ||||||||||||||||||||||||||||||||||||||||||||||||||
| Identificaciones externas | OMIM : 151430; MGI : 88138; HomoloGene : 527; Tarjetas genéticas : BCL2; OMA :BCL2 - ortólogos | ||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| Wikidatos | |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
Bcl-2 , codificado en humanos por el gen BCL2 , es el miembro fundador de la familia Bcl-2 de proteínas reguladoras . BCL2 bloquea la muerte celular programada ( apoptosis ) [5] mientras que otros miembros de la familia BCL2 pueden inhibirla o inducirla. [6] [7] Fue el primer regulador de la apoptosis identificado en cualquier organismo. [8]
Bcl-2 deriva su nombre de B-cell lymphoma 2 , ya que es el segundo miembro de una gama de proteínas descritas inicialmente en translocaciones cromosómicas que involucran los cromosomas 14 y 18 en linfomas foliculares . Se han identificado ortólogos [9] (como Bcl2 en ratones) en numerosos mamíferos para los que se dispone de datos genómicos completos .
Al igual que BCL3 , BCL5, BCL6 , BCL7A, BCL9 y BCL10 , tiene importancia clínica en el linfoma .
Isoformas
Las dos isoformas de Bcl-2, la isoforma 1 y la isoforma 2, presentan un plegamiento similar. Sin embargo, los resultados en la capacidad de estas isoformas para unirse a las proteínas BAD y BAK , así como en la topología estructural y el potencial electrostático del surco de unión, sugieren diferencias en la actividad antiapoptótica de las dos isoformas . [10]
Función
BCL-2 se localiza en la membrana externa de las mitocondrias , donde desempeña un papel importante en la promoción de la supervivencia celular y la inhibición de las acciones de las proteínas proapoptóticas. Las proteínas proapoptóticas de la familia BCL-2, incluidas Bax y Bak , normalmente actúan sobre la membrana mitocondrial para promover la permeabilización y la liberación de citocromo c y ROS , que son señales importantes en la cascada de apoptosis. Estas proteínas proapoptóticas son activadas a su vez por proteínas exclusivas de BH3 y son inhibidas por la función de BCL-2 y su pariente BCL-Xl . [11]
Existen otras funciones no canónicas de BCL-2 que se están explorando. Se sabe que BCL-2 regula la dinámica mitocondrial y está involucrado en la regulación de la fusión y fisión mitocondrial. Además, en las células beta pancreáticas, se sabe que BCL-2 y BCL-Xl están involucrados en el control de la actividad metabólica y la secreción de insulina, y la inhibición de BCL-2/Xl muestra un aumento de la actividad metabólica [12] , pero también una producción adicional de ROS; esto sugiere que tiene un efecto metabólico protector en condiciones de alta demanda [13] .
Papel en la enfermedad
Se ha identificado el daño al gen Bcl-2 como causa de varios tipos de cáncer , entre ellos el melanoma , el cáncer de mama , el cáncer de próstata , la leucemia linfocítica crónica y el cáncer de pulmón , y como posible causa de esquizofrenia y autoinmunidad . También es causa de resistencia a los tratamientos contra el cáncer. [14]
Cáncer
El cáncer puede verse como una alteración en el equilibrio homeostático entre el crecimiento celular y la muerte celular. La sobreexpresión de genes antiapoptóticos y la subexpresión de genes proapoptóticos pueden dar como resultado la falta de muerte celular que es característica del cáncer. Un ejemplo puede verse en los linfomas . La sobreexpresión de la proteína antiapoptótica Bcl-2 en linfocitos por sí sola no causa cáncer. Pero la sobreexpresión simultánea de Bcl-2 y el protooncogén myc puede producir neoplasias malignas agresivas de células B, incluido el linfoma. [15] En el linfoma folicular , una translocación cromosómica ocurre comúnmente entre los cromosomas decimocuarto y decimoctavo - t(14;18) - que coloca el gen Bcl-2 del cromosoma 18 junto al locus de la cadena pesada de inmunoglobulina en el cromosoma 14. Este gen de fusión está desregulado, lo que lleva a la transcripción de niveles excesivamente altos de Bcl-2. [16] Esto disminuye la propensión de estas células a la apoptosis. La expresión de Bcl-2 es frecuente en el cáncer de pulmón de células pequeñas y representa el 76 % de los casos en un estudio. [17]
Enfermedades autoinmunes
La apoptosis desempeña un papel activo en la regulación del sistema inmunológico. Cuando es funcional, puede causar una falta de respuesta inmunológica a los autoantígenos a través de la tolerancia central y periférica. En el caso de una apoptosis defectuosa, puede contribuir a los aspectos etiológicos de las enfermedades autoinmunes. [18] La enfermedad autoinmune diabetes tipo 1 puede ser causada por una apoptosis defectuosa, que conduce a una AICD aberrante de células T y una tolerancia periférica defectuosa. Debido al hecho de que las células dendríticas son las células presentadoras de antígenos más importantes del sistema inmunológico , su actividad debe estar estrechamente regulada por mecanismos como la apoptosis. Los investigadores han descubierto que los ratones que contienen células dendríticas que son Bim -/-, por lo tanto incapaces de inducir una apoptosis efectiva, tienen enfermedades autoinmunes más que aquellos que tienen células dendríticas normales. [18] Otros estudios han demostrado que la vida útil de las células dendríticas puede estar controlada en parte por un temporizador dependiente de Bcl-2 antiapoptótico. [18]
Otro
La apoptosis desempeña un papel importante en la regulación de diversas enfermedades. Por ejemplo, la esquizofrenia es un trastorno psiquiátrico en el que una proporción anormal de factores proapoptóticos y antiapoptóticos puede contribuir a la patogénesis. [19] Algunas evidencias sugieren que esto puede ser resultado de la expresión anormal de Bcl-2 y el aumento de la expresión de caspasa-3 . [19]
Uso diagnóstico
Los anticuerpos contra Bcl-2 se pueden utilizar con inmunohistoquímica para identificar células que contienen el antígeno. En el tejido sano, estos anticuerpos reaccionan con las células B en la zona del manto , así como con algunas células T. Sin embargo, las células positivas aumentan considerablemente en el linfoma folicular , así como en muchas otras formas de cáncer. En algunos casos, la presencia o ausencia de tinción de Bcl-2 en las biopsias puede ser significativa para el pronóstico del paciente o la probabilidad de recaída . [20]
Terapias dirigidas
Los inhibidores selectivos y dirigidos de Bcl-2 que se encuentran en desarrollo o actualmente en uso clínico incluyen:
Oblimarse
Genta Incorporated desarrolló un fármaco oligonucleótido antisentido, el oblimersen (G3139), para atacar a Bcl-2. Una cadena de ADN o ARN antisentido no codifica y es complementaria a la cadena codificante (que es la plantilla para producir ARN o proteína respectivamente). Un fármaco antisentido es una secuencia corta de ARN que se hibrida con el ARNm y lo inactiva, impidiendo que se forme la proteína .
La proliferación de células de linfoma humano (con translocación t(14;18)) podría ser inhibida por el ARN antisentido dirigido a la región del codón de inicio del ARNm de Bcl-2 . Los estudios in vitro condujeron a la identificación de Genasense, que es complementario a los primeros 6 codones del ARNm de Bcl-2. [21]
Estos ensayos mostraron resultados exitosos en las fases I y II para el linfoma. En 2004 se lanzó un ensayo de fase III a gran escala. [22] En 2016, el fármaco no había sido aprobado y su desarrollador había cerrado el negocio. [23]
ABT-737 y navitoclax (ABT-263)
A mediados de la década de 2000, Abbott Laboratories desarrolló un nuevo inhibidor de Bcl-2, Bcl-xL y Bcl-w, conocido como ABT-737 . Este compuesto es parte de un grupo de inhibidores de moléculas pequeñas (SMI) miméticos de BH3 que se dirigen a estas proteínas de la familia Bcl-2, pero no a A1 o Mcl-1 . ABT-737 es superior a los inhibidores de BCL-2 anteriores debido a su mayor afinidad por Bcl-2, Bcl-xL y Bcl-w. Los estudios in vitro mostraron que las células primarias de pacientes con neoplasias malignas de células B son sensibles a ABT-737. [24]
En modelos animales, mejora la supervivencia, provoca regresión tumoral y cura un alto porcentaje de ratones. [25] En estudios preclínicos que utilizan xenoinjertos de pacientes , ABT-737 mostró eficacia para tratar el linfoma y otros cánceres de la sangre. [26] Debido a sus propiedades farmacológicas desfavorables, ABT-737 no es apropiado para ensayos clínicos, mientras que su derivado biodisponible por vía oral navitoclax (ABT-263) tiene una actividad similar en líneas celulares de cáncer de pulmón de células pequeñas (SCLC) y ha entrado en ensayos clínicos. [27] Si bien las respuestas clínicas con navitoclax fueron prometedoras, se observó trombocitopenia limitante de la dosis mecanística en pacientes bajo tratamiento debido a la inhibición de Bcl-xL en plaquetas . [28] [29] [30]
Venetoclax (ABT-199)
Debido a la trombocitopenia limitante de la dosis de navitoclax como resultado de la inhibición de Bcl-xL, Abbvie desarrolló con éxito el inhibidor altamente selectivo venetoclax (ABT-199), que inhibe Bcl-2, pero no Bcl-xL o Bcl-w. [31] Los ensayos clínicos estudiaron los efectos de venetoclax, un fármaco mimético de BH3 diseñado para bloquear la función de la proteína Bcl-2, en pacientes con leucemia linfocítica crónica (LLC). [32] [33] Se han informado buenas respuestas y ya no se observó trombocitopenia. [33] [34] Un ensayo de fase 3 comenzó en diciembre de 2015. [35] Fue aprobado por la FDA de EE. UU. en abril de 2016 como un tratamiento de segunda línea para la LLC asociada con la deleción de 17-p. [36] Esta fue la primera aprobación de la FDA de un inhibidor de BCL-2. [36] En junio de 2018, la FDA amplió la aprobación para cualquier persona con LLC o linfoma linfocítico pequeño, con o sin deleción de 17p, todavía como tratamiento de segunda línea. [37]
Sonrotoclax (BGB-11417)
Se ha observado resistencia al fármaco venetoclax con la mutación G101V en BCL-2 observada en pacientes con recaídas. [38] Sonrotoclax muestra una mayor inhibición del crecimiento tumoral en modelos tumorales hematológicos que venetoclax e inhibe las variantes de BCL-2 resistentes a venetoclax. Sonrotoclax está bajo investigación clínica como monoterapia y en combinación con otros agentes anticancerígenos. [39]
Interacciones
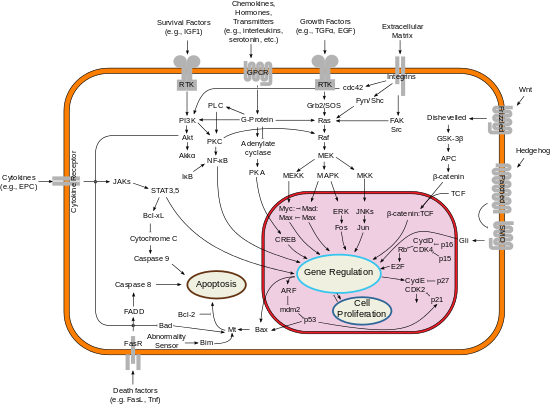
Se ha demostrado que Bcl-2 interactúa con:
- BAK1 , [40] [41]
- BCAP31 , [42]
- Similar a BCL2 1 , [40] [43]
- BCL2L11 , [44] [45] [46]
- BECN1 , [47]
- Oferta , [44] [48]
- BMF , [49]
- BNIP2 , [50] [51]
- BNIP3 , [51] [52]
- BNIPL , [50] [53]
- MALO [44] [54]
- BAX , [40] [55] [56] [57]
- BIK , [44] [58]
- C-Raf , [59]
- CAPN2 , [60]
- CASP8 , [61] [62]
- Cdk1 , [63] [64]
- República Checa , [44] [65]
- IRS1 , [66]
- Mi c , [67]
- NR4A1 , [40]
- Noxa , [44] [68]
- PPP2CA , [69]
- PSEN1 , [70]
- RAD9A , [55]
- RRAS , [71]
- RTN4 , [72]
- SMN1 , [73]
- SOD1 , [74] y
- TP53BP2 . [75]
Véase también
Referencias
- ^ abc GRCh38: Lanzamiento de Ensembl 89: ENSG00000171791 – Ensembl , mayo de 2017
- ^ abc GRCm38: Lanzamiento de Ensembl 89: ENSMUSG00000057329 – Ensembl , mayo de 2017
- ^ "Referencia de PubMed humana:". Centro Nacional de Información Biotecnológica, Biblioteca Nacional de Medicina de EE. UU .
- ^ "Referencia de PubMed sobre ratón". Centro Nacional de Información Biotecnológica, Biblioteca Nacional de Medicina de EE. UU .
- ^ Hockenbery D, Nuñez G, Milliman C, Schreiber RD, Korsmeyer SJ (noviembre de 1990). "Bcl-2 es una proteína de la membrana mitocondrial interna que bloquea la muerte celular programada". Nature . 348 (6299): 334–336. Bibcode :1990Natur.348..334H. doi :10.1038/348334a0. PMID 2250705.
- ^ Tsujimoto Y, Finger LR, Yunis J, Nowell PC, Croce CM (noviembre de 1984). "Clonación del punto de ruptura cromosómica de las células B neoplásicas con la translocación cromosómica t(14;18)". Science . 226 (4678): 1097–1099. Bibcode :1984Sci...226.1097T. doi :10.1126/science.6093263. PMID 6093263.
- ^ Cleary ML, Smith SD, Sklar J (octubre de 1986). "Clonación y análisis estructural de los ADNc para bcl-2 y un transcrito híbrido bcl-2/inmunoglobulina resultante de la translocación t(14;18)". Cell . 47 (1): 19–28. doi :10.1016/0092-8674(86)90362-4. PMID 2875799. S2CID 31493780.
- ^ Kelly GL, Strasser A (2020). "Hacia la focalización del MCL-1 antiapoptótico para la terapia del cáncer". Revisión anual de biología del cáncer . 4 : 299–313. doi : 10.1146/annurev-cancerbio-030419-033510 . hdl : 11343/252362 .
- ^ "Marcador filogenético OrthoMaM: secuencia codificante de Bcl-2". Archivado desde el original el 24 de septiembre de 2015. Consultado el 20 de diciembre de 2009 .
- ^ PDB : 1G5M ; Petros AM, Medek A, Nettesheim DG, Kim DH, Yoon HS, Swift K, et al. (marzo de 2001). "Estructura de la solución de la proteína antiapoptótica bcl-2". Actas de la Academia Nacional de Ciencias de los Estados Unidos de América . 98 (6): 3012–3017. Bibcode :2001PNAS...98.3012P. doi : 10.1073/pnas.041619798 . PMC 30598 . PMID 11248023.
- ^ Hardwick JM, Soane L (febrero de 2013). "Múltiples funciones de las proteínas de la familia BCL-2". Cold Spring Harbor Perspectives in Biology . 5 (2): a008722. doi :10.1101/cshperspect.a008722. PMC 3552500 . PMID 23378584.
- ^ Luciani DS, White SA, Widenmaier SB, Saran VV, Taghizadeh F, Hu X, et al. (enero de 2013). "Bcl-2 y Bcl-xL suprimen la señalización de glucosa en las células β pancreáticas". Diabetes . 62 (1): 170–182. doi :10.2337/db11-1464. PMC 3526034 . PMID 22933114.
- ^ Aharoni-Simon M, Shumiatcher R, Yeung A, Shih AZ, Dolinsky VW, Doucette CA, et al. (junio de 2016). "Bcl-2 regula la señalización de especies reactivas de oxígeno y una fuga de protones mitocondriales sensible al rédox en células β pancreáticas de ratón". Endocrinología . 157 (6): 2270–2281. doi : 10.1210/en.2015-1964 . PMID 27070098.
- ^ García-Aranda M, Pérez-Ruiz E, Redondo M (diciembre de 2018). "Inhibición de Bcl-2 para superar la resistencia a la quimio e inmunoterapia". Revista Internacional de Ciencias Moleculares . 19 (12): 3950. doi : 10.3390/ijms19123950 . PMC 6321604 . PMID 30544835.
- ^ Otake Y, Soundararajan S, Sengupta TK, Kio EA, Smith JC, Pineda-Roman M, et al. (abril de 2007). "La sobreexpresión de nucleolina en células de leucemia linfocítica crónica induce la estabilización del ARNm de bcl2". Blood . 109 (7): 3069–3075. doi :10.1182/blood-2006-08-043257. PMC 1852223 . PMID 17179226.
- ^ Vaux DL, Cory S, Adams JM (septiembre de 1988). "El gen Bcl-2 promueve la supervivencia de las células hematopoyéticas y coopera con c-myc para inmortalizar las células pre-B". Nature . 335 (6189): 440–442. Bibcode :1988Natur.335..440V. doi :10.1038/335440a0. PMID 3262202. S2CID 23593952.
- ^ Kaiser U, Schilli M, Haag U, Neumann K, Kreipe H, Kogan E, et al. (agosto de 1996). "Expresión de la proteína bcl-2 en el cáncer de pulmón de células pequeñas". Cáncer de pulmón . 15 (1): 31–40. doi :10.1016/0169-5002(96)00568-5. PMID 8865121.
- ^ abc Li A, Ojogho O, Escher A (2006). "Salvando la muerte: apoptosis para la intervención en trasplantes y autoinmunidad". Inmunología clínica y del desarrollo . 13 (2–4): 273–282. doi :10.1080/17402520600834704. PMC 2270759 . PMID 17162368.
- ^ ab Glantz LA, Gilmore JH, Lieberman JA, Jarskog LF (enero de 2006). "Mecanismos apoptóticos y patología sináptica de la esquizofrenia". Schizophrenia Research . 81 (1): 47–63. doi :10.1016/j.schres.2005.08.014. PMID 16226876. S2CID 22388783.
- ^ Chetty R, Cooper K, Gown AM, eds. (2016). "Sección 1 - Anticuerpos: Bcl-2". Manual de citología diagnóstica (2.ª ed.). Greenwich Medical Media, Ltd., págs. 23-24. doi :10.1017/9781139939508.013. ISBN 978-1-139-93950-8.
- ^ Dias N, Stein CA (noviembre de 2002). "Posibles funciones de los oligonucleótidos antisentido en la terapia del cáncer. El ejemplo de los oligonucleótidos antisentido Bcl-2". Revista Europea de Farmacia y Biofarmacia . 54 (3): 263–269. doi :10.1016/S0939-6411(02)00060-7. PMID 12445555.
- ^ Mavromatis BH, Cheson BD (junio de 2004). "Nuevas terapias para la leucemia linfocítica crónica". Blood Reviews . 18 (2): 137–148. doi :10.1016/S0268-960X(03)00039-0. PMID 15010151.
- ^ "Estado de aprobación de la FDA para Genasense (oblimersen sódico)". Drugs.com . Consultado el 11 de febrero de 2016 .
- ^ Vogler M, Dinsdale D, Dyer MJ, Cohen GM (marzo de 2009). "Inhibidores de Bcl-2: pequeñas moléculas con un gran impacto en la terapia del cáncer". Muerte celular y diferenciación . 16 (3): 360–367. doi : 10.1038/cdd.2008.137 . hdl : 2381/4756 . PMID: 18806758. S2CID : 24538054.
- ^ Oltersdorf T, Elmore SW, Shoemaker AR, Armstrong RC, Augeri DJ, Belli BA, et al. (junio de 2005). "Un inhibidor de las proteínas de la familia Bcl-2 induce la regresión de tumores sólidos". Nature . 435 (7042): 677–681. Bibcode :2005Natur.435..677O. doi :10.1038/nature03579. PMID 15902208. S2CID 4335635.
- ^ Hann CL, Daniel VC, Sugar EA, Dobromilskaya I, Murphy SC, Cope L, et al. (abril de 2008). "Eficacia terapéutica de ABT-737, un inhibidor selectivo de BCL-2, en el cáncer de pulmón de células pequeñas". Cancer Research . 68 (7): 2321–2328. doi :10.1158/0008-5472.can-07-5031. PMC 3159963 . PMID 18381439.
- ^ Hauck P, Chao BH, Litz J, Krystal GW (abril de 2009). "Las alteraciones en el eje Noxa/Mcl-1 determinan la sensibilidad del cáncer de pulmón de células pequeñas al mimético de BH3 ABT-737". Molecular Cancer Therapeutics . 8 (4): 883–892. doi :10.1158/1535-7163.MCT-08-1118. PMID 19372561. S2CID 19245418.
- ^ Gandhi L, Camidge DR, Ribeiro de Oliveira M, Bonomi P, Gandara D, Khaira D, et al. (marzo de 2011). "Estudio de fase I de Navitoclax (ABT-263), un nuevo inhibidor de la familia Bcl-2, en pacientes con cáncer de pulmón de células pequeñas y otros tumores sólidos". Journal of Clinical Oncology . 29 (7): 909–916. doi :10.1200/JCO.2010.31.6208. PMC 4668282 . PMID 21282543.
- ^ Rudin CM, Hann CL, Garon EB, Ribeiro de Oliveira M, Bonomi PD, Camidge DR, et al. (junio de 2012). "Estudio de fase II de navitoclax como agente único (ABT-263) y correlaciones de biomarcadores en pacientes con cáncer de pulmón de células pequeñas en recaída". Investigación clínica del cáncer . 18 (11): 3163–3169. doi :10.1158/1078-0432.CCR-11-3090. PMC 3715059. PMID 22496272 .
- ^ Kaefer A, Yang J, Noertersheuser P, Mensing S, Humerickhouse R, Awni W, et al. (septiembre de 2014). "Metaanálisis farmacocinético/farmacodinámico basado en el mecanismo de la trombocitopenia inducida por navitoclax (ABT-263)". Quimioterapia y farmacología del cáncer . 74 (3): 593–602. doi :10.1007/s00280-014-2530-9. PMID 25053389. S2CID 10685695.
- ^ Pan R, Hogdal LJ, Benito JM, Bucci D, Han L, Borthakur G, et al. (marzo de 2014). "La inhibición selectiva de BCL-2 por ABT-199 provoca la muerte celular en la leucemia mieloide aguda". Cancer Discovery . 4 (3): 362–375. doi :10.1158/2159-8290.CD-13-0609. PMC 3975047 . PMID 24346116.
- ^ Liao G (12 de agosto de 2011). "ABT-199 BH-3 Mimetic Enters Phase Ia Trial For Chronic Lymphocytic Leukemia". Científico asiático. Archivado desde el original el 18 de julio de 2012. Consultado el 11 de febrero de 2016 .
- ^ ab Roberts AW, Davids MS, Pagel JM, Kahl BS, Puvvada SD, Gerecitano JF, et al. (enero de 2016). "Dirigir BCL2 con Venetoclax en la leucemia linfocítica crónica recidivante". The New England Journal of Medicine . 374 (4): 311–322. doi : 10.1056/NEJMoa1513257 . PMC 7107002 . PMID 26639348.
- ^ "'¡Un fármaco milagroso me curó el cáncer!': Sorprendente recuperación en tres semanas de un paciente de Staffordshire". Stoke Sentinel . Archivado desde el original el 12 de mayo de 2014 . Consultado el 10 de mayo de 2014 .
- ^ Smith M (7 de diciembre de 2015). "La LLC difícil de tratar da lugar a un fármaco en investigación".
- ^ ab Bankhead C (11 de abril de 2016). "La FDA aprueba el fármaco dirigido a BCL-2 de AbbVie para la LLC". Medpage Today .
- ^ "La FDA aprueba venetoclax para la LLC o la LPP, con o sin deleción de 17p, después de una terapia previa". Administración de Alimentos y Medicamentos de Estados Unidos. 24 de marzo de 2020.
- ^ Blombery P, Anderson MA, Gong JN, Thijssen R, Birkinshaw RW, Thompson ER, et al. (marzo de 2019). "La adquisición de la mutación recurrente Gly101Val en BCL2 confiere resistencia a Venetoclax en pacientes con leucemia linfocítica crónica progresiva". Cancer Discovery . 9 (3): 342–353. doi :10.1158/2159-8290.CD-18-1119. PMID 30514704.
- ^ Liu J, Li S, Wang Q, Feng Y, Xing H, Yang X, et al. (mayo de 2024). "Sonrotoclax supera la resistencia a venetoclax inducida por la mutación BCL2 G101V en modelos preclínicos de malignidad hematológica". Blood . 143 (18): 1825–1836. doi :10.1182/blood.2023019706. PMC 11076911 . PMID 38211332.
- ^ abcd Lin B, Kolluri SK, Lin F, Liu W, Han YH, Cao X, et al. (febrero de 2004). "Conversión de Bcl-2 de protector a asesino por interacción con el receptor huérfano nuclear Nur77/TR3". Cell . 116 (4): 527–540. doi : 10.1016/s0092-8674(04)00162-x . PMID 14980220. S2CID 17808479.
- ^ Enyedy IJ, Ling Y, Nacro K, Tomita Y, Wu X, Cao Y, et al. (diciembre de 2001). "Descubrimiento de inhibidores de moléculas pequeñas de Bcl-2 mediante análisis informático basado en la estructura". Journal of Medicinal Chemistry . 44 (25): 4313–4324. doi :10.1021/jm010016f. PMID 11728179.
- ^ Ng FW, Nguyen M, Kwan T, Branton PE, Nicholson DW, Cromlish JA, et al. (octubre de 1997). "p28 Bap31, una proteína asociada a Bcl-2 / Bcl-XL y procaspasa-8 en el retículo endoplásmico". La revista de biología celular . 139 (2): 327–338. doi :10.1083/jcb.139.2.327. PMC 2139787 . PMID 9334338.
- ^ Zhang H, Nimmer P, Rosenberg SH, Ng SC, Joseph M (agosto de 2002). "Desarrollo de un ensayo de polarización de fluorescencia de alto rendimiento para Bcl-x(L)". Analytical Biochemistry . 307 (1): 70–75. doi :10.1016/s0003-2697(02)00028-3. PMID 12137781.
- ^ abcdef Chen L, Willis SN, Wei A, Smith BJ, Fletcher JI, Hinds MG, et al. (febrero de 2005). "La orientación diferencial de las proteínas prosupervivencia Bcl-2 por sus ligandos BH3-only permite una función apoptótica complementaria". Molecular Cell . 17 (3): 393–403. doi : 10.1016/j.molcel.2004.12.030 . PMID 15694340.
- ^ O'Connor L, Strasser A, O'Reilly LA, Hausmann G, Adams JM, Cory S, et al. (enero de 1998). "Bim: un nuevo miembro de la familia Bcl-2 que promueve la apoptosis". The EMBO Journal . 17 (2): 384–395. doi :10.1093/emboj/17.2.384. PMC 1170389 . PMID 9430630.
- ^ Hsu SY, Lin P, Hsueh AJ (septiembre de 1998). "BOD (gen de muerte ovárica relacionado con Bcl-2) es una proteína Bcl-2 proapoptótica que contiene el dominio BH3 ovárico capaz de dimerizarse con diversos miembros Bcl-2 antiapoptóticos". Endocrinología molecular . 12 (9): 1432–1440. doi : 10.1210/mend.12.9.0166 . PMID 9731710.
- ^ Liang XH, Kleeman LK, Jiang HH, Gordon G, Goldman JE, Berry G, et al. (noviembre de 1998). "Protección contra la encefalitis mortal por virus Sindbis mediante beclin, una nueva proteína que interactúa con Bcl-2". Revista de Virología . 72 (11): 8586–8596. doi :10.1128/JVI.72.11.8586-8596.1998. PMC 110269 . PMID 9765397.
- ^ Real PJ, Cao Y, Wang R, Nikolovska-Coleska Z, Sanz-Ortiz J, Wang S, et al. (noviembre de 2004). "Las células de cáncer de mama pueden evadir la muerte selectiva mediada por apoptosis mediante un nuevo inhibidor de molécula pequeña de Bcl-2". Cancer Research . 64 (21): 7947–7953. doi :10.1158/0008-5472.CAN-04-0945. PMID 15520201. S2CID 11807428.
- ^ Puthalakath H, Villunger A, O'Reilly LA, Beaumont JG, Coultas L, Cheney RE, et al. (septiembre de 2001). "Bmf: una proteína proapoptótica BH3-only regulada por interacción con el complejo motor de actina de miosina V, activado por anoikis". Science . 293 (5536): 1829–1832. Bibcode :2001Sci...293.1829P. doi :10.1126/science.1062257. PMID 11546872. S2CID 5638023.
- ^ ab Qin W, Hu J, Guo M, Xu J, Li J, Yao G, et al. (agosto de 2003). "BNIPL-2, un nuevo homólogo de BNIP-2, interactúa con Bcl-2 y Cdc42GAP en la apoptosis". Comunicaciones de investigación bioquímica y biofísica . 308 (2): 379–385. doi :10.1016/s0006-291x(03)01387-1. PMID 12901880.
- ^ ab Boyd JM, Malstrom S, Subramanian T, Venkatesh LK, Schaeper U, Elangovan B, et al. (octubre de 1994). "Las proteínas de adenovirus E1B 19 kDa y Bcl-2 interactúan con un conjunto común de proteínas celulares". Cell . 79 (2): 341–351. doi :10.1016/0092-8674(94)90202-X. PMID 7954800. S2CID 38609845.
- ^ Ray R, Chen G, Vande Velde C, Cizeau J, Park JH, Reed JC, et al. (enero de 2000). "BNIP3 heterodimeriza con Bcl-2/Bcl-X(L) e induce muerte celular independiente de un dominio de homología 3 (BH3) de Bcl-2 en sitios mitocondriales y no mitocondriales". The Journal of Biological Chemistry . 275 (2): 1439–1448. doi : 10.1074/jbc.275.2.1439 . PMID 10625696.
- ^ Yasuda M, Han JW, Dionne CA, Boyd JM, Chinnadurai G (febrero de 1999). "BNIP3alpha: un homólogo humano de la proteína proapoptótica mitocondrial BNIP3". Cancer Research . 59 (3): 533–537. PMID 9973195.
- ^ Yang E, Zha J, Jockel J, Boise LH, Thompson CB, Korsmeyer SJ (enero de 1995). "Bad, un socio heterodímero de Bcl-XL y Bcl-2, desplaza a Bax y promueve la muerte celular". Cell . 80 (2): 285–291. doi : 10.1016/0092-8674(95)90411-5 . PMID 7834748. S2CID 10343291.
- ^ ab Komatsu K, Miyashita T, Hang H, Hopkins KM, Zheng W, Cuddeback S, et al. (Enero de 2000). "El homólogo humano de S. pombe Rad9 interactúa con BCL-2/BCL-xL y promueve la apoptosis". Biología celular de la naturaleza . 2 (1): 1–6. doi :10.1038/71316. PMID 10620799. S2CID 52847351.
- ^ Hoetelmans RW (junio de 2004). "Socios nucleares de Bcl-2: Bax y PML". ADN y biología celular . 23 (6): 351–354. doi :10.1089/104454904323145236. PMID 15231068.
- ^ Oltvai ZN, Milliman CL, Korsmeyer SJ (agosto de 1993). "Bcl-2 heterodimeriza in vivo con un homólogo conservado, Bax, que acelera la muerte celular programada". Cell . 74 (4): 609–619. doi :10.1016/0092-8674(93)90509-O. PMID 8358790. S2CID 31151334.
- ^ Gillissen B, Essmann F, Graupner V, Stärck L, Radetzki S, Dörken B, et al. (julio de 2003). "La inducción de muerte celular por el homólogo de Bcl-2 Nbk/Bik, que solo contiene BH3, está mediada por una vía mitocondrial completamente dependiente de Bax". The EMBO Journal . 22 (14): 3580–3590. doi :10.1093/emboj/cdg343. PMC 165613 . PMID 12853473.
- ^ Wang HG, Rapp UR, Reed JC (noviembre de 1996). "Bcl-2 dirige la proteína quinasa Raf-1 a las mitocondrias". Cell . 87 (4): 629–638. doi : 10.1016/s0092-8674(00)81383-5 . PMID 8929532. S2CID 16559750.
- ^ Gil-Parrado S, Fernández-Montalván A, Assfalg-Machleidt I, Popp O, Bestvater F, Holloschi A, et al. (julio de 2002). "La calpaína activada por ionomicina desencadena la apoptosis. Un papel probable para los miembros de la familia Bcl-2". The Journal of Biological Chemistry . 277 (30): 27217–27226. doi : 10.1074/jbc.M202945200 . PMID 12000759.
- ^ Poulaki V, Mitsiades N, Romero ME, Tsokos M (junio de 2001). "La apoptosis mediada por Fas en el neuroblastoma requiere activación mitocondrial y es inhibida por la proteína inhibidora FLICE y Bcl-2". Cancer Research . 61 (12): 4864–4872. PMID 11406564.
- ^ Guo Y, Srinivasula SM, Druilhe A, Fernandes-Alnemri T, Alnemri ES (abril de 2002). "La caspasa-2 induce la apoptosis mediante la liberación de proteínas proapoptóticas de las mitocondrias". The Journal of Biological Chemistry . 277 (16): 13430–13437. doi : 10.1074/jbc.M108029200 . PMID 11832478.
- ^ Pathan N, Aime-Sempe C, Kitada S, Basu A, Haldar S, Reed JC (2001). "Los fármacos dirigidos a microtúbulos inducen la fosforilación de bcl-2 y la asociación con Pin1". Neoplasia . 3 (6): 550–559. doi :10.1038/sj.neo.7900213. PMC 1506558 . PMID 11774038.
- ^ Pathan N, Aime-Sempe C, Kitada S, Haldar S, Reed JC (2001). "Los fármacos dirigidos a los microtúbulos inducen la fosforilación de Bcl-2 y la asociación con Pin1". Neoplasia . 3 (1): 70–79. doi :10.1038/sj.neo.7900131. PMC 1505024 . PMID 11326318.
- ^ Inohara N, Ding L, Chen S, Núñez G (abril de 1997). "harakiri, un nuevo regulador de la muerte celular, codifica una proteína que activa la apoptosis e interactúa selectivamente con las proteínas promotoras de supervivencia Bcl-2 y Bcl-X(L)". The EMBO Journal . 16 (7): 1686–1694. doi :10.1093/emboj/16.7.1686. PMC 1169772 . PMID 9130713.
- ^ Ueno H, Kondo E, Yamamoto-Honda R, Tobe K, Nakamoto T, Sasaki K, et al. (febrero de 2000). "Asociación de proteínas sustrato del receptor de insulina con Bcl-2 y sus efectos sobre su fosforilación y función antiapoptótica". Biología molecular de la célula . 11 (2): 735–746. doi :10.1091/mbc.11.2.735. PMC 14806 . PMID 10679027.
- ^ Jin Z, Gao F, Flagg T, Deng X (septiembre de 2004). "La nitrosamina 4-(metilnitrosamino)-1-(3-piridil)-1-butanona, específica del tabaco, promueve la cooperación funcional de Bcl2 y c-Myc a través de la fosforilación en la regulación de la supervivencia y proliferación celular". The Journal of Biological Chemistry . 279 (38): 40209–40219. doi : 10.1074/jbc.M404056200 . PMID 15210690.
- ^ Oda E, Ohki R, Murasawa H, Nemoto J, Shibue T, Yamashita T, et al. (mayo de 2000). "Noxa, un miembro exclusivo de BH3 de la familia Bcl-2 y candidato a mediador de la apoptosis inducida por p53". Ciencia . 288 (5468): 1053–1058. Código Bib : 2000 Ciencia... 288.1053O. doi : 10.1126/ciencia.288.5468.1053. PMID 10807576.
- ^ Deng X, Ito T, Carr B, Mumby M, May WS (diciembre de 1998). "La fosforilación reversible de Bcl2 después de la interleucina 3 o la briostatina 1 está mediada por la interacción directa con la proteína fosfatasa 2A". The Journal of Biological Chemistry . 273 (51): 34157–34163. doi : 10.1074/jbc.273.51.34157 . PMID 9852076.
- ^ Alberici A, Moratto D, Benussi L, Gasparini L, Ghidoni R, Gatta LB, et al. (octubre de 1999). "La proteína presenilina 1 interactúa directamente con Bcl-2". La Revista de Química Biológica . 274 (43): 30764–30769. doi : 10.1074/jbc.274.43.30764 . PMID 10521466.
- ^ Fernandez-Sarabia MJ, Bischoff JR (noviembre de 1993). "Bcl-2 se asocia con la proteína relacionada con ras R-ras p23". Nature . 366 (6452): 274–275. Bibcode :1993Natur.366..274F. doi :10.1038/366274a0. PMID 8232588. S2CID 4312803.
- ^ Tagami S, Eguchi Y, Kinoshita M, Takeda M, Tsujimoto Y (noviembre de 2000). "Una nueva proteína, RTN-XS, interactúa con Bcl-XL y Bcl-2 en el retículo endoplasmático y reduce su actividad antiapoptótica". Oncogene . 19 (50): 5736–5746. doi : 10.1038/sj.onc.1203948 . PMID 11126360.
- ^ Iwahashi H, Eguchi Y, Yasuhara N, Hanafusa T, Matsuzawa Y, Tsujimoto Y (noviembre de 1997). "Actividad antiapoptótica sinérgica entre Bcl-2 y SMN implicada en la atrofia muscular espinal". Nature . 390 (6658): 413–417. Bibcode :1997Natur.390..413I. doi :10.1038/37144. PMID 9389483. S2CID 1936633.
- ^ Pasinelli P, Belford ME, Lennon N, Bacskai BJ, Hyman BT, Trotti D, et al. (julio de 2004). "Las proteínas mutantes de SOD1 asociadas a la esclerosis lateral amiotrófica se unen y se agregan con Bcl-2 en las mitocondrias de la médula espinal". Neuron . 43 (1): 19–30. doi : 10.1016/j.neuron.2004.06.021 . PMID 15233914. S2CID 18141051.
- ^ Naumovski L, Cleary ML (julio de 1996). "La proteína de unión a p53 53BP2 también interactúa con Bc12 e impide la progresión del ciclo celular en G2/M". Biología molecular y celular . 16 (7): 3884–3892. doi :10.1128/MCB.16.7.3884. PMC 231385 . PMID 8668206.
Enlaces externos
- Base de datos de la familia Bcl-2
- La familia Bcl-2 en celldeath.de
- Genes bcl-2+ en los encabezados de materias médicas (MeSH) de la Biblioteca Nacional de Medicina de EE. UU.
- Proteínas c-bcl-2+ en los encabezados de materias médicas (MeSH) de la Biblioteca Nacional de Medicina de EE. UU.
- Página de detalles del gen BCL2 y ubicación del genoma humano en el navegador de genomas de la UCSC .
- Resumen de toda la información estructural disponible en el PDB para UniProt : P10415 (regulador de la apoptosis humana Bcl-2) en el PDBe-KB .









