Ácido sulfúrico
| |||
 | |||
| Nombres | |||
|---|---|---|---|
| Nombre IUPAC Ácido sulfúrico | |||
Otros nombres
| |||
| Identificadores | |||
Modelo 3D ( JSmol ) |
| ||
| EBICh | |||
| Química biológica | |||
| Araña química | |||
| Tarjeta informativa de la ECHA | 100.028.763 | ||
| Número CE |
| ||
| Número E | E513 (reguladores de acidez, ...) | ||
| 2122 | |||
| BARRIL | |||
Identificador de centro de PubChem |
| ||
| Número RTECS |
| ||
| UNIVERSIDAD | |||
| Número de la ONU | 1830 | ||
Panel de control CompTox ( EPA ) |
| ||
| |||
| |||
| Propiedades | |||
| H 2 SO 4 , a veces expresado (HO) 2 SO 2 | |||
| Masa molar | 98,079 g/mol | ||
| Apariencia | Líquido viscoso incoloro | ||
| Olor | Inodoro | ||
| Densidad | 1,8302 g/cm 3 , líquido [1] | ||
| Punto de fusión | 10,31 [1] °C (50,56 °F; 283,46 K) | ||
| Punto de ebullición | 337 [1] °C (639 °F; 610 K) Cuando el ácido sulfúrico está por encima de 300 °C (572 °F; 573 K), se descompone gradualmente en SO 3 + H 2 O | ||
| miscible, exotérmico | |||
| Presión de vapor | 0,001 mmHg (20 °C) [2] | ||
| Acidez (p K a ) | pKa1 = −2,8 pKa2 = 1,99 | ||
| Base conjugada | Bisulfato | ||
| Viscosidad | 26,7 cP (20 °C) | ||
| Estructura [3] | |||
| monoclínico | |||
| C2/c | |||
a = 818,1(2) pm, b = 469,60(10) pm, c = 856,3(2) pm α = 90°, β = 111,39(3) °, γ = 90° | |||
Unidades de fórmula ( Z ) | 4 | ||
| Termoquímica | |||
Entropía molar estándar ( S ⦵ 298 ) | 157 J/(mol·K) [4] | ||
Entalpía estándar de formación (Δ f H ⦵ 298 ) | −814 kJ/mol [4] | ||
| Peligros | |||
| Etiquetado SGA : | |||
  | |||
| Peligro | |||
| H314 | |||
| P260 , P264 , P280 , P301+P330+P331 , P303+P361+P353 , P304+P340 , P305+P351+P338 , P310 , P321 , P363 , P405 , P501 | |||
| NFPA 704 (rombo cortafuegos) | |||
| punto de inflamabilidad | Ininflamable | ||
Valor límite umbral (TLV) | 15 mg/m3 ( IDLH), 1 mg/m3 ( TWA), 2 mg/m3 ( STEL) | ||
| Dosis o concentración letal (LD, LC): | |||
LD 50 ( dosis media ) | 2140 mg/kg (rata, oral) [5] | ||
LC 50 ( concentración media ) |
| ||
LC Lo ( valor más bajo publicado ) | 87 mg/m3 ( conejillo de indias, 2,75 h) [5] | ||
| NIOSH (límites de exposición a la salud en EE. UU.): | |||
PEL (Permisible) | TWA 1 mg/m3 [ 2] | ||
REL (recomendado) | TWA 1 mg/m3 [ 2] | ||
IDLH (Peligro inmediato) | 15 mg/m3 [ 2] | ||
| Ficha de datos de seguridad (FDS) | Hoja de datos de seguridad externa | ||
| Compuestos relacionados | |||
Ácidos fuertes relacionados | |||
Compuestos relacionados | |||
Salvo que se indique lo contrario, los datos se proporcionan para los materiales en su estado estándar (a 25 °C [77 °F], 100 kPa). | |||
El ácido sulfúrico ( ortografía estadounidense y el nombre preferido de la IUPAC ) o ácido sulfúrico ( ortografía de la Commonwealth ), conocido en la antigüedad como aceite de vitriolo , es un ácido mineral compuesto por los elementos azufre , oxígeno e hidrógeno , con la fórmula molecular H 2 SO 4 . Es un líquido incoloro, inodoro y viscoso que es soluble en agua. [6]

El ácido sulfúrico puro no se produce de forma natural debido a su fuerte afinidad con el vapor de agua ; es higroscópico y absorbe fácilmente el vapor de agua del aire . [6] El ácido sulfúrico concentrado es muy corrosivo para otros materiales, desde rocas hasta metales, ya que es un oxidante con potentes propiedades deshidratantes. El pentóxido de fósforo es una notable excepción, ya que no es deshidratado por el ácido sulfúrico sino que, por el contrario, deshidrata el ácido sulfúrico a trióxido de azufre . Al añadir ácido sulfúrico al agua, se libera una cantidad considerable de calor; por lo tanto, generalmente se evita el procedimiento inverso de agregar agua al ácido, ya que el calor liberado puede hervir la solución, rociando gotitas de ácido caliente durante el proceso. Al entrar en contacto con el tejido corporal, el ácido sulfúrico puede causar quemaduras químicas ácidas graves y quemaduras térmicas secundarias debido a la deshidratación. [7] [8] El ácido sulfúrico diluido es sustancialmente menos peligroso sin las propiedades oxidativas y deshidratantes; sin embargo, se maneja con cuidado por su acidez.
El ácido sulfúrico es un producto químico muy importante; la producción de ácido sulfúrico de un país es un buen indicador de su fortaleza industrial. [9] Se conocen muchos métodos para su producción, incluido el proceso de contacto , el proceso de ácido sulfúrico húmedo y el proceso de cámara de plomo . [10] El ácido sulfúrico también es una sustancia clave en la industria química . Se utiliza más comúnmente en la fabricación de fertilizantes [11] pero también es importante en el procesamiento de minerales , la refinación de petróleo , el procesamiento de aguas residuales y la síntesis química . Tiene una amplia gama de aplicaciones finales, incluso en limpiadores de desagües ácidos domésticos , [12] como electrolito en baterías de plomo-ácido , como compuesto deshidratante y en varios agentes de limpieza . El ácido sulfúrico se puede obtener disolviendo trióxido de azufre en agua.
Propiedades físicas
Grados de ácido sulfúrico
Aunque se pueden preparar soluciones de ácido sulfúrico casi al 100%, la pérdida posterior de SO3 en el punto de ebullición lleva la concentración al 98,3 % de ácido. El grado al 98,3%, que es más estable en el almacenamiento, es la forma habitual de lo que se describe como "ácido sulfúrico concentrado". Se utilizan otras concentraciones para diferentes fines. Algunas concentraciones comunes son: [13] [14]
| Fracción de masa H 2 SO 4 | Densidad (kg/L) | Concentración (mol/L) | Nombre común |
|---|---|---|---|
| <29% | 1,00-1,25 | <4.2 | ácido sulfúrico diluido |
| 29–32% | 1,25–1,28 | 4.2–5.0 | Ácido de batería (usado en baterías de plomo-ácido ) |
| 62–70% | 1,52–1,60 | 9.6–11.5 | cámara de ácido fertilizante ácido |
| 78–80% | 1,70–1,73 | 13,5–14,0 | Ácido de torre Ácido de Glover |
| 93,2% | 1.83 | 17.4 | Ácido 66 °Bé ("66 grados Baumé") |
| 98,3% | 1.84 | 18.4 | ácido sulfúrico concentrado |
"Ácido de cámara" y "ácido de torre" eran las dos concentraciones de ácido sulfúrico producidas por el proceso de cámara de plomo , siendo el ácido de cámara el ácido producido en la propia cámara de plomo (<70% para evitar la contaminación con ácido nitrosilsulfúrico ) y el ácido de torre el ácido recuperado del fondo de la torre Glover. [13] [14] Ahora están obsoletos como concentraciones comerciales de ácido sulfúrico, aunque se pueden preparar en el laboratorio a partir de ácido sulfúrico concentrado si es necesario. En particular, el ácido sulfúrico "10 M" (el equivalente moderno del ácido de cámara, utilizado en muchas titulaciones ), se prepara añadiendo lentamente ácido sulfúrico al 98% a un volumen igual de agua, con buena agitación: la temperatura de la mezcla puede subir a 80 °C (176 °F) o más. [14]
Ácido sulfúrico
El ácido sulfúrico no sólo contiene moléculas de H 2 SO 4 , sino que en realidad es un equilibrio de muchas otras especies químicas, como se muestra en la siguiente tabla.
| Especies | mMol/kg |
|---|---|
| HSO−4 | 15.0 |
| H3SO4+4 | 11.3 |
| H3O + | 8.0 |
| HS2O−7 | 4.4 |
| H2S2O7 | 3.6 |
| H2O | 0,1 |
El ácido sulfúrico es un líquido aceitoso incoloro y tiene una presión de vapor de <0,001 mmHg a 25 °C y 1 mmHg a 145,8 °C, [16] y el ácido sulfúrico al 98% tiene una presión de vapor de <1 mmHg a 40 °C. [17]
En estado sólido, el ácido sulfúrico es un sólido molecular que forma cristales monoclínicos con parámetros reticulares casi trigonales . La estructura consta de capas paralelas al plano (010), en las que cada molécula está conectada por enlaces de hidrógeno a otras dos. [3] Los hidratos H 2 SO 4 · n H 2 O son conocidos para n = 1, 2, 3, 4, 6,5 y 8, aunque la mayoría de los hidratos intermedios son estables frente a la desproporción . [18]
Polaridad y conductividad
El H 2 SO 4 anhidro es un líquido muy polar , con una constante dieléctrica de alrededor de 100. Tiene una alta conductividad eléctrica , consecuencia de la autoprotólisis , es decir, la autoprotonación : [ 15]
- 2H2SO4 ⇌ H3SO4+4+HSO4−4
La constante de equilibrio para la autoprotólisis (25 °C) es: [15]
- [ H3SO4 ] + [HSO4 ] − = 2,7 × 10 −4
La constante de equilibrio correspondiente para el agua , K w, es 10 −14 , un factor de 10 10 (10 mil millones) más pequeño.
A pesar de la viscosidad del ácido, las conductividades efectivas del H 3 SO+4y HSO−4Los iones son altos debido a un mecanismo de intercambio de protones intramolecular (análogo al mecanismo de Grotthuss en el agua), lo que hace que el ácido sulfúrico sea un buen conductor de electricidad. También es un excelente disolvente para muchas reacciones.
Propiedades químicas
Acidez

La reacción de hidratación del ácido sulfúrico es altamente exotérmica y dilutiva. [19]
Como lo indica su constante de disociación ácida , el ácido sulfúrico es un ácido fuerte:
- H2SO4 → H3O ++ HSO−4K a1 = 1000 (pKa1 = −3)
El producto de esta ionización es HSO−4, el anión bisulfato . El bisulfato es un ácido mucho más débil:
- HSO−4+ H2O → H3O + + SO2−4K a2 = 0,01 (pK a2 = 2) [20]
El producto de esta segunda disociación es SO2−4, el anión sulfato .
Deshidración
El ácido sulfúrico concentrado tiene una poderosa propiedad deshidratante , ya que elimina el agua ( H2O ) de otros compuestos químicos como el azúcar de mesa ( sacarosa ) y otros carbohidratos , para producir carbono , vapor y calor. La deshidratación del azúcar de mesa ( sacarosa) es una demostración común en laboratorio. [21] El azúcar se oscurece a medida que se forma el carbono, y puede surgir una columna rígida de carbono negro y poroso llamada serpiente de carbono . [22]
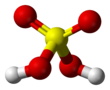
De manera similar, al mezclar almidón con ácido sulfúrico concentrado se obtiene carbono elemental y agua. El efecto de esto también se puede observar cuando se derrama ácido sulfúrico concentrado sobre papel. El papel está compuesto de celulosa , un polisacárido relacionado con el almidón. La celulosa reacciona para dar un aspecto quemado en el que el carbono se parece mucho al hollín que resulta del fuego. Aunque menos espectacular, la acción del ácido sobre el algodón , incluso en forma diluida, destruye la tela.
La reacción con sulfato de cobre (II) también puede demostrar la propiedad de deshidratación del ácido sulfúrico. Los cristales azules se transforman en polvo blanco a medida que se elimina el agua.
Reacciones con sales
El ácido sulfúrico reacciona con la mayoría de las bases para dar el sulfato o bisulfato correspondiente.
El ácido sulfúrico reacciona con el cloruro de sodio y produce gas cloruro de hidrógeno y bisulfato de sodio :
- NaCl + H2SO4 → NaHSO4 + HCl
El sulfato de aluminio , también conocido como alumbre para fabricación de papel, se obtiene tratando la bauxita con ácido sulfúrico:
- 2AlO( OH ) + 3H2SO4 → Al2 ( SO4 ) 3 + 4H2O
El ácido sulfúrico también se puede utilizar para desplazar ácidos más débiles de sus sales. La reacción con acetato de sodio , por ejemplo, desplaza el ácido acético , CH3COOH , y forma bisulfato de sodio :
- H 2 SO 4 + CH 3 CO 2 Na → NaHSO 4 + CH 3 COOH
De manera similar, el tratamiento del nitrato de potasio con ácido sulfúrico produce ácido nítrico .
Cuando se combina con ácido nítrico , el ácido sulfúrico actúa como ácido y como agente deshidratante, formando el ion nitronio NO+2, que es importante en las reacciones de nitración que implican sustitución aromática electrofílica . Este tipo de reacción, en la que se produce la protonación en un átomo de oxígeno , es importante en muchas reacciones de química orgánica , como la esterificación de Fischer y la deshidratación de alcoholes.
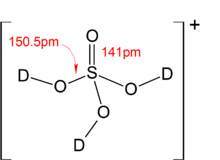
Cuando se le permite reaccionar con superácidos , el ácido sulfúrico puede actuar como una base y puede protonarse, formando el ion [H 3 SO 4 ] + . Se han preparado sales de [H 3 SO 4 ] + (por ejemplo, hexafluoroantimoniato de trihidroxioxosulfonio (V) [H 3 SO 4 ] + [SbF 6 ] − ) utilizando la siguiente reacción en HF líquido :
- [( CH3 ) 3SiO ] 2SO2 + 3HF + SbF5 → [ H3SO4 ] + [ SbF6 ] − + 2 ( CH3 ) 3SiF
La reacción anterior se ve favorecida termodinámicamente debido a la alta entalpía de enlace del enlace Si–F en el producto secundario. Sin embargo, la protonación utilizando simplemente ácido fluoroantimónico ha fracasado, ya que el ácido sulfúrico puro sufre autoionización para dar iones [H 3 O] + :
- 2H2SO4 ⇌ H3O ++ HS2O−7
que impide la conversión de H 2 SO 4 a [H 3 SO 4 ] + por el sistema HF/ SbF 5 . [23]
Reacciones con metales
Incluso el ácido sulfúrico diluido reacciona con muchos metales a través de una única reacción de desplazamiento, como otros ácidos típicos , produciendo gas hidrógeno y sales (el sulfato metálico). Ataca a los metales reactivos (metales en posiciones por encima del cobre en la serie de reactividad ) como el hierro , el aluminio , el zinc , el manganeso , el magnesio y el níquel .
- Fe + H2SO4 → H2 + FeSO4
El ácido sulfúrico concentrado puede servir como agente oxidante , liberando dióxido de azufre: [7]
- Cu + 2H2SO4 → SO2 + 2H2O + SO2−4+Cu2 +
Sin embargo, el plomo y el tungsteno son resistentes al ácido sulfúrico.
Reacciones con carbono y azufre
El ácido sulfúrico concentrado caliente oxida el carbono [24] (como el carbón bituminoso ) y el azufre :
- C + 2 H 2 SO 4 → CO 2 + 2 SO 2 + 2 H 2 O
- S + 2 H 2 SO 4 → 3 SO 2 + 2 H 2 O
Sustitución aromática electrofílica
El benceno y muchos derivados experimentan una sustitución aromática electrofílica con ácido sulfúrico para dar los ácidos sulfónicos correspondientes : [25]
Ciclo del azufre y el yodo
El ácido sulfúrico se puede utilizar para producir hidrógeno a partir del agua :
2I2 + 2SO2 + 4H2O → 4HI + 2H2SO4 (120 °C, reacción de Bunsen ) 2H2SO4 → 2SO2 + 2H2O + O2 (830 °C) 4HI → 2I2 + 2H2 (320 °C)
Los compuestos de azufre y yodo se recuperan y reutilizan, por lo que el proceso se llama ciclo azufre-yodo . Este proceso es endotérmico y debe ocurrir a altas temperaturas, por lo que se debe suministrar energía en forma de calor. El ciclo azufre-yodo se ha propuesto como una forma de suministrar hidrógeno para una economía basada en el hidrógeno . Es una alternativa a la electrólisis y no requiere hidrocarburos como los métodos actuales de reformado con vapor . Pero tenga en cuenta que toda la energía disponible en el hidrógeno así producido es suministrada por el calor utilizado para fabricarlo. [26] [27]
Aparición

El ácido sulfúrico rara vez se encuentra de forma natural en la Tierra en forma anhidra, debido a su gran afinidad por el agua . El ácido sulfúrico diluido es un componente de la lluvia ácida , que se forma por oxidación atmosférica del dióxido de azufre en presencia de agua , es decir, oxidación del ácido sulfuroso . Cuando se queman combustibles que contienen azufre, como el carbón o el petróleo, el dióxido de azufre es el principal subproducto (además de los productos principales óxidos de carbono y agua).
El ácido sulfúrico se forma naturalmente por la oxidación de minerales sulfurados, como la pirita :
- 2FeS2 (s) + 7O2 + 2H2O → 2Fe2 + + 4SO2−4+ 4H +
El agua altamente ácida resultante se llama drenaje ácido de minas (AMD) o drenaje ácido de rocas (ARD).
El Fe2 + puede oxidarse aún más a Fe3 + :
- 4Fe2 + + O2 + 4H + → 4Fe3 + + 2H2O
El Fe3 + producido se puede precipitar como hidróxido u óxido de hierro hidratado :
- Fe3 + + 3H2O → Fe(OH) 3 ↓ + 3H +
El ion hierro (III) ("hierro férrico") también puede oxidar la pirita:
- FeS2 (s) + 14 Fe3 + + 8 H2O → 15 Fe2 + + 2 SO2−4+ 16 horas +
Cuando se produce la oxidación del hierro (III) de la pirita, el proceso puede volverse rápido. Se han medido valores de pH por debajo de cero en el ARD producido por este proceso.
La ARD también puede producir ácido sulfúrico a un ritmo más lento, de modo que la capacidad de neutralización de ácidos (ANC) del acuífero pueda neutralizar el ácido producido. En tales casos, la concentración total de sólidos disueltos (TDS) del agua puede aumentar a partir de la disolución de minerales a partir de la reacción de neutralización de ácidos con los minerales.
El ácido sulfúrico es utilizado como defensa por ciertas especies marinas, por ejemplo, el alga feófita Desmarestia munda (orden Desmarestiales ) concentra ácido sulfúrico en las vacuolas celulares. [28]
Aerosol estratosférico
En la estratosfera , la segunda capa de la atmósfera que se encuentra generalmente entre 10 y 50 km por encima de la superficie de la Tierra, el ácido sulfúrico se forma por la oxidación del dióxido de azufre volcánico por el radical hidroxilo : [29]
- SO2 + HO • → HSO3
- HSO3 + O2 → SO3 + HO2
- SO3 + H2O → H2SO4
Debido a que el ácido sulfúrico alcanza la sobresaturación en la estratosfera, puede nuclear partículas de aerosol y proporcionar una superficie para el crecimiento de aerosoles a través de la condensación y coagulación con otros aerosoles de agua y ácido sulfúrico. Esto da como resultado la capa de aerosoles estratosféricos . [29]
Ácido sulfúrico extraterrestre
Las nubes permanentes de Venus producen una lluvia ácida concentrada, al igual que las nubes en la atmósfera de la Tierra producen lluvia de agua. [30] También se cree que la luna Europa de Júpiter tiene una atmósfera que contiene hidratos de ácido sulfúrico. [31]
Fabricación
El ácido sulfúrico se produce a partir de azufre , oxígeno y agua mediante el proceso de contacto convencional (DCDA) o el proceso de ácido sulfúrico húmedo (WSA).
Proceso de contacto
En el primer paso, se quema azufre para producir dióxido de azufre.
- S(s) + O2 → SO2
El dióxido de azufre se oxida a trióxido de azufre mediante oxígeno en presencia de un catalizador de óxido de vanadio (V) . Esta reacción es reversible y la formación del trióxido de azufre es exotérmica.
- 2SO2 + O2 ⇌ 2SO3
El trióxido de azufre se absorbe en H2SO4 al 97-98% para formar óleum ( H2S2O7 ) , también conocido como ácido sulfúrico fumante o ácido pirosulfúrico . Luego, el óleum se diluye con agua para formar ácido sulfúrico concentrado.
- H2SO4 + SO3 → H2S2O7
- H2S2O7 + H2O → 2H2SO4
La disolución directa de SO 3 en agua, denominada " proceso de ácido sulfúrico húmedo ", rara vez se practica porque la reacción es extremadamente exotérmica y da como resultado un aerosol caliente de ácido sulfúrico que requiere condensación y separación.
Proceso de ácido sulfúrico húmedo
En el primer paso, se quema el azufre para producir dióxido de azufre:
- S + O 2 → SO 2 (−297 kJ/mol)
o, alternativamente, se incinera gas de sulfuro de hidrógeno ( H2S ) para formar gas SO2 :
- 2H2S + 3O2 → 2H2O + 2SO2 ( −1036 kJ/mol )
Luego, el dióxido de azufre se oxida a trióxido de azufre usando oxígeno con óxido de vanadio (V) como catalizador .
- 2 SO 2 + O 2 ⇌ 2 SO 3 (−198 kJ/mol) (la reacción es reversible)
El trióxido de azufre se hidrata en ácido sulfúrico H 2 SO 4 :
- SO3 + H2O → H2SO4 (g) ( −101 kJ/ mol )
El último paso es la condensación del ácido sulfúrico a H2SO4 líquido al 97–98 % :
- H2SO4 ( g ) → H2SO4 ( l ) ( −69 kJ/mol )
Otros métodos
Un método menos conocido es el método del metabisulfito, en el que se coloca metabisulfito en el fondo de un vaso de precipitados y se añade ácido clorhídrico de concentración 12,6 molar . El gas resultante se burbujea a través de ácido nítrico , que liberará vapores marrones/rojos de dióxido de nitrógeno a medida que avanza la reacción. La finalización de la reacción se indica mediante el cese de los vapores. Este método no produce una niebla inseparable, lo que resulta bastante conveniente.
- 3SO2 + 2HNO3 + 2H2O → 3H2SO4 + 2NO
Históricamente se ha utilizado la quema de azufre junto con salitre ( nitrato de potasio , KNO3 ), en presencia de vapor. A medida que el salitre se descompone, oxida el azufre a SO3 , que se combina con agua para producir ácido sulfúrico.
Alternativamente, disolver dióxido de azufre en una solución acuosa de una sal metálica oxidante como cloruro de cobre (II) o de hierro (III):
- 2 FeCl3 + 2 H2O + SO2 → 2 FeCl2 + H2SO4 + 2 HCl
- 2CuCl2 + 2H2O + SO2 → 2CuCl + H2SO4 + 2HCl
Dos métodos de laboratorio menos conocidos para producir ácido sulfúrico, aunque en forma diluida y que requieren un esfuerzo adicional para su purificación. Una solución de sulfato de cobre (II) se puede electrolizar con un cátodo de cobre y un ánodo de platino/grafito para dar cobre esponjoso en el cátodo y evolución de gas oxígeno en el ánodo; la solución de ácido sulfúrico diluido indica que la reacción se ha completado cuando cambia de azul a transparente (la producción de hidrógeno en el cátodo es otra señal):
- 2 CuSO 4 + 2 H 2 O → 2 Cu + 2 H 2 SO 4 + O 2
El método de electrobromo es más costoso, peligroso y problemático, pero novedoso, y emplea una mezcla de azufre , agua y ácido bromhídrico como solución electrolítica. El azufre se empuja hacia el fondo del recipiente bajo la solución ácida. Luego se utilizan el cátodo de cobre y el ánodo de platino/grafito con el cátodo cerca de la superficie y el ánodo se coloca en el fondo del electrolito para aplicar la corriente. Este proceso puede llevar más tiempo y emite vapores tóxicos de bromo /bromuro de azufre, pero el ácido reactivo es reciclable. En general, solo el azufre y el agua se convierten en ácido sulfúrico e hidrógeno (omitiendo las pérdidas de ácido en forma de vapores):
- 2 HBr → H 2 + Br 2 (electrólisis de bromuro de hidrógeno acuoso)
- Br2 + Br − ↔ Br−3(producción inicial de tribromuro , que finalmente se revierte a medida que se agota el Br − )
- 2 S + Br 2 → S 2 Br 2 (el bromo reacciona con el azufre para formar dibromuro de disulfuro )
- S 2 Br 2 + 8 H 2 O + 5 Br 2 → 2 H 2 SO 4 + 12 HBr (oxidación e hidratación del dibromuro de disulfuro)
Antes de 1900, la mayor parte del ácido sulfúrico se fabricaba mediante el proceso de cámara de plomo . [32] Incluso en 1940, hasta el 50% del ácido sulfúrico fabricado en los Estados Unidos se producía mediante plantas de proceso de cámara.
A principios y mediados del siglo XIX existían plantas de "vitriolo", entre otros lugares, en Prestonpans en Escocia, Shropshire y el valle de Lagan en el condado de Antrim, Irlanda, donde se utilizaba como blanqueador para el lino. El blanqueo primitivo del lino se hacía con ácido láctico de leche agria, pero era un proceso lento y el uso de vitriolo aceleraba el proceso de blanqueo. [33]
Usos

El ácido sulfúrico es un producto químico muy importante y, de hecho, la producción de ácido sulfúrico de una nación es un buen indicador de su fortaleza industrial. [9] La producción mundial en el año 2004 fue de aproximadamente 180 millones de toneladas , con la siguiente distribución geográfica: Asia 35%, América del Norte (incluido México) 24%, África 11%, Europa Occidental 10%, Europa del Este y Rusia 10%, Australia y Oceanía 7%, América del Sur 7%. [34] La mayor parte de esta cantidad (≈60%) se consume para fertilizantes, particularmente superfosfatos, fosfato de amonio y sulfatos de amonio. Aproximadamente el 20% se utiliza en la industria química para la producción de detergentes, resinas sintéticas, colorantes, productos farmacéuticos, catalizadores de petróleo, insecticidas y anticongelantes , así como en varios procesos como la acidificación de pozos petrolíferos, la reducción de aluminio, el encolado de papel y el tratamiento de agua. Alrededor del 6% de los usos están relacionados con pigmentos e incluyen pinturas, esmaltes , tintas de impresión, tejidos recubiertos y papel, mientras que el resto se distribuye en una multitud de aplicaciones como la producción de explosivos, celofán , acetato y textiles de viscosa, lubricantes, metales no ferrosos y baterías. [35]
Producción industrial de productos químicos
El uso predominante del ácido sulfúrico es en el "método húmedo" para la producción de ácido fosfórico , que se utiliza para la fabricación de fertilizantes fosfatados . En este método, se utiliza roca fosfórica y se procesan más de 100 millones de toneladas al año. Esta materia prima se muestra a continuación como fluorapatita , aunque la composición exacta puede variar. Esta se trata con ácido sulfúrico al 93% para producir sulfato de calcio , fluoruro de hidrógeno (HF) y ácido fosfórico . El HF se elimina como ácido fluorhídrico . El proceso general se puede representar como:
El sulfato de amonio , un importante fertilizante nitrogenado, se produce habitualmente como subproducto de las plantas de coquización que abastecen a las plantas siderúrgicas. La reacción del amoníaco producido en la descomposición térmica del carbón con ácido sulfúrico residual permite que el amoníaco se cristalice en forma de sal (que a menudo adquiere un color marrón debido a la contaminación con hierro) y se venda a la industria agroquímica.
El ácido sulfúrico también es importante en la fabricación de soluciones de colorantes .
Agente de limpieza industrial
El ácido sulfúrico se utiliza en la fabricación de acero y otras industrias metalúrgicas como agente decapante para eliminar el óxido y las incrustaciones . [36] El ácido usado se recicla a menudo utilizando una planta de regeneración de ácido gastado (SAR). Estas plantas queman el ácido gastado [ aclaración necesaria ] con gas natural, gas de refinería, fueloil u otras fuentes de combustible. Este proceso de combustión produce dióxido de azufre gaseoso ( SO2 ) y trióxido de azufre ( SO3 ) que luego se utilizan para fabricar ácido sulfúrico "nuevo".
El peróxido de hidrógeno (H2O2 ) se puede agregar al ácido sulfúrico para producir una solución de piraña , una solución de limpieza potente pero muy tóxica con la que se pueden limpiar las superficies de los sustratos. La solución de piraña se usa normalmente en la industria de la microelectrónica y también en entornos de laboratorio para limpiar material de vidrio.
Catalizador
El ácido sulfúrico se utiliza para una variedad de otros propósitos en la industria química. Por ejemplo, es el catalizador ácido habitual para la conversión de oxima de ciclohexanona en caprolactama , que se utiliza para fabricar nailon . Se utiliza para fabricar ácido clorhídrico a partir de sal mediante el proceso de Mannheim . Gran parte del H 2 SO 4 se utiliza en la refinación del petróleo , por ejemplo, como catalizador para la reacción del isobutano con isobutileno para dar isooctano , un compuesto que aumenta el índice de octano de la gasolina . El ácido sulfúrico también se utiliza a menudo como agente deshidratante u oxidante en reacciones industriales, como la deshidratación de varios azúcares para formar carbono sólido.
Electrólito
.jpg/440px-Acidic_drain_cleaner_containing_sulfuric_acid_(sulphuric_acid).jpg)
El ácido sulfúrico actúa como electrolito en las baterías de plomo-ácido (acumulador de plomo-ácido):
En el ánodo :
- Pb + SO2−4⇌ PbSO4 + 2 e−
En el cátodo :
- PbO2 + 4H ++ SO2−4+ 2 e − ⇌ PbSO4 + 2 H2O

En general:
- Pb + PbO2 + 4 H + + 2 SO2−4⇌ 2 PbSO4 + 2 H2O
Usos domésticos
El ácido sulfúrico en altas concentraciones es frecuentemente el ingrediente principal en los limpiadores de desagües ácidos domésticos [12] que se utilizan para eliminar grasa , cabello , papel tisú , etc. De manera similar a sus versiones alcalinas , estos destapadores de desagües pueden disolver grasas y proteínas mediante hidrólisis . Además, como el ácido sulfúrico concentrado tiene una fuerte propiedad deshidratante, también puede eliminar el papel tisú mediante un proceso de deshidratación. Dado que el ácido puede reaccionar con el agua de manera vigorosa, estos destapadores de desagües ácidos deben agregarse lentamente a la tubería que se va a limpiar.
Historia

Vitriolos
El estudio de los vitriolos ( sulfatos hidratados de varios metales que forman minerales vítreos de los que se puede derivar el ácido sulfúrico) comenzó en la antigüedad . Los sumerios tenían una lista de tipos de vitriolo que clasificaban según el color de las sustancias. Algunas de las primeras discusiones sobre el origen y las propiedades del vitriolo se encuentran en las obras del médico griego Dioscórides (siglo I d. C.) y del naturalista romano Plinio el Viejo (23-79 d. C.). Galeno también discutió su uso médico. Los usos metalúrgicos de las sustancias vitriólicas se registraron en las obras alquímicas helenísticas de Zósimo de Panópolis , en el tratado Phisica et Mystica y en el papiro X de Leyden . [37] Los químicos islámicos medievales como los autores que escribieron bajo el nombre de Jabir ibn Hayyan (fallecido c. 806 – c. 816 d. C., conocido en latín como Geber), Abu Bakr al-Razi (865 – 925 d. C., conocido en latín como Rhazes), Ibn Sina (980 – 1037 d. C., conocido en latín como Avicena) y Muhammad ibn Ibrahim al-Watwat (1234 – 1318 d. C.) incluyeron el vitriolo en sus listas de clasificación de minerales. [38]
Jabir ibn Hayyan, Abu Bakr al-Razi, Ibn Sina, et al.
Los autores jabirianos y al-Razi experimentaron extensamente con la destilación de varias sustancias, incluidos los vitriolos. [39] En una receta registrada en su Kitāb al-Asrār ( 'Libro de los secretos' ), al-Razi puede haber creado ácido sulfúrico sin ser consciente de ello: [40]
Tome alumbre blanca (yemení) , disuélvalo y purifíquelo por filtración. Luego destile el vitriolo (¿verde?) con el verde cobre (el acetato) y mezcle (el destilado) con la solución filtrada del alumbre purificado, luego déjelo solidificar (o cristalizar) en el vaso de vidrio. Obtendrá el mejor qalqadis (alumbre blanca) que se pueda conseguir. [41]
— Abu Bakr al-Razi, Kitāb al-Asrār
En una obra latina anónima atribuida a Aristóteles (bajo el título Liber Aristotilis , 'Libro de Aristóteles'), [42] a al-Razi (bajo el título Lumen luminum magnum , 'Gran Luz de Luces'), o a Ibn Sina, [43] el autor habla de un 'aceite' ( oleum ) obtenido a través de la destilación de sulfato de hierro (II) (vitriolo verde), que probablemente era 'aceite de vitriolo' o ácido sulfúrico. [44] La obra se refiere varias veces al Libro de los Setenta de Jabir ibn Hayyan ( Liber de septuaginta ), una de las pocas obras árabes de Jabir que se tradujeron al latín. [45] El autor de la versión atribuida a al-Razi también se refiere al Liber de septuaginta como su propia obra, mostrando que creía erróneamente que el Liber de septuaginta era una obra de al-Razi. [46] Hay varios indicios de que la obra anónima fue una composición original en latín, [47] aunque según un manuscrito fue traducida por un tal Raimundo de Marsella, lo que significa que también pudo haber sido una traducción del árabe. [48]
Según Ahmad Y. al-Hassan , hay tres recetas de ácido sulfúrico en un manuscrito anónimo de Karshuni que contiene una compilación tomada de varios autores y que data de antes de c. 1100 d . C. [49] Una de ellas dice lo siguiente:
El agua de vitriolo y azufre que se usa para regar las drogas: vitriolo amarillo tres partes, azufre amarillo una parte, se muelen y se destilan a la manera del agua de rosas. [50]
En Risālat Jaʿfar al-Sādiq fī ʿilm al-ṣanʿa , un tratado árabe falsamente atribuido al imán chií Ja'far al-Sadiq (fallecido en 765), se menciona una receta para la preparación de ácido sulfúrico. Julius Ruska fechó este tratado en el siglo XIII, pero según Ahmad Y. al-Hassan es probable que sea de un período anterior: [51]
Luego destila el vitriolo verde en una cucurbitácea y en un alambique, usando fuego medio; toma lo que obtengas del destilado y lo encontrarás claro con un tinte verdoso. [50]
Vicente de Beauvais, Alberto Magno y el pseudo-Geber
Los alquimistas medievales europeos llamaban al ácido sulfúrico «aceite de vitriolo» porque se preparaba calcinando sulfato de hierro (II) o vitriolo verde en una retorta de hierro . Las primeras alusiones a él en obras de origen europeo aparecen en el siglo XIII d. C., como por ejemplo en las obras de Vicente de Beauvais , en el Compositum de Compositis atribuido a Alberto Magno y en la Summa perfectionis de pseudo-Geber . [52]
Producción de ácido sulfúrico a partir de azufre
En el siglo XVI se conocía un método para producir oleum sulphuris per campanam, o "aceite de azufre por la campana": implicaba quemar azufre bajo una campana de vidrio en tiempo húmedo (o, más tarde, bajo una campana humedecida). Sin embargo, era muy ineficiente (según Gesner , 5 libras (2,3 kg) de azufre se convertían en menos de 1 onza (0,03 kg) de ácido), y el producto resultante estaba contaminado con ácido sulfuroso (o más bien, solución de dióxido de azufre ), por lo que la mayoría de los alquimistas (incluido, por ejemplo, Isaac Newton) no lo consideraban equivalente al "aceite de vitriolo".
En el siglo XVII, Johann Glauber descubrió que la adición de salitre ( nitrato de potasio , KNO3 ) mejora significativamente el rendimiento, sustituyendo además la humedad por vapor. A medida que el salitre se descompone, oxida el azufre a SO3 , que se combina con agua para producir ácido sulfúrico. En 1736, Joshua Ward , un farmacéutico de Londres, utilizó este método para iniciar la primera producción a gran escala de ácido sulfúrico.
Proceso de cámara de plomo
En 1746, en Birmingham, John Roebuck adaptó este método para producir ácido sulfúrico en cámaras revestidas de plomo , que eran más resistentes, menos costosas y podían fabricarse de mayor tamaño que los recipientes de vidrio utilizados anteriormente. Este proceso permitió la industrialización efectiva de la producción de ácido sulfúrico. Después de varias mejoras, este método, llamado proceso de cámara de plomo o "proceso de cámara", siguió siendo el estándar para la producción de ácido sulfúrico durante casi dos siglos. [4]
Destilación de pirita
El ácido sulfúrico creado por el proceso de John Roebuck se acercaba a una concentración del 65%. Los refinamientos posteriores del proceso de la cámara de plomo por el químico francés Joseph Louis Gay-Lussac y el químico británico John Glover mejoraron la concentración al 78%. Sin embargo, la fabricación de algunos tintes y otros procesos químicos requieren un producto más concentrado. A lo largo del siglo XVIII, esto solo podía hacerse mediante la destilación en seco de minerales en una técnica similar a los procesos alquímicos originales. La pirita (disulfuro de hierro, FeS 2 ) se calentaba en aire para producir sulfato de hierro (II), FeSO 4 , que se oxidaba mediante un calentamiento adicional en aire para formar sulfato de hierro (III) , Fe 2 (SO 4 ) 3 , que, cuando se calentaba a 480 °C, se descomponía en óxido de hierro (III) y trióxido de azufre, que podían pasarse a través del agua para producir ácido sulfúrico en cualquier concentración. Sin embargo, el costo de este proceso impidió el uso a gran escala de ácido sulfúrico concentrado. [4]
Proceso de contacto
En 1831, el comerciante de vinagre británico Peregrine Phillips patentó el proceso de contacto , que era un proceso mucho más económico para producir trióxido de azufre y ácido sulfúrico concentrado. Hoy en día, casi todo el ácido sulfúrico del mundo se produce utilizando este método. [53]
Seguridad
Peligros de laboratorio



El ácido sulfúrico es capaz de causar quemaduras muy graves, especialmente cuando se encuentra en altas concentraciones . Al igual que otros ácidos corrosivos y álcalis , descompone fácilmente las proteínas y los lípidos a través de la hidrólisis de amidas y ésteres al entrar en contacto con tejidos vivos , como la piel y la carne . Además, exhibe una fuerte propiedad deshidratante de los carbohidratos , liberando calor adicional y causando quemaduras térmicas secundarias . [7] [8] En consecuencia, ataca rápidamente la córnea y puede inducir ceguera permanente si salpica los ojos . Si se ingiere, daña los órganos internos de forma irreversible e incluso puede ser mortal. [6] Por lo tanto, siempre se debe utilizar equipo de protección al manipularlo. Además, su fuerte propiedad oxidante lo hace altamente corrosivo para muchos metales y puede extender su destrucción a otros materiales. [7] Debido a estas razones, el daño provocado por el ácido sulfúrico es potencialmente más grave que el de otros ácidos fuertes comparables , como el ácido clorhídrico y el ácido nítrico .
El ácido sulfúrico debe almacenarse con cuidado en recipientes fabricados con material no reactivo (como vidrio). Las soluciones con una concentración igual o superior a 1,5 M se etiquetan como "CORROSIVAS", mientras que las soluciones con una concentración superior a 0,5 M pero inferior a 1,5 M se etiquetan como "IRRITANTES". Sin embargo, incluso la solución "diluida" normal de laboratorio (aproximadamente 1 M, 10 %) carbonizará el papel si se deja en contacto durante un tiempo suficiente.
El tratamiento estándar de primeros auxilios para los derrames de ácido sobre la piel es, al igual que para otros agentes corrosivos , la irrigación con grandes cantidades de agua. El lavado se continúa durante al menos diez a quince minutos para enfriar el tejido que rodea la quemadura de ácido y evitar daños secundarios. La ropa contaminada se quita inmediatamente y la piel subyacente se lava a fondo.
Peligros de dilución
La preparación de ácido diluido puede ser peligrosa debido al calor que se libera en el proceso de dilución. Para evitar salpicaduras, normalmente se añade el ácido concentrado al agua y no al revés. Un dicho que se utiliza para recordar esto es "Haz lo que debes hacer, añade el ácido al agua". [54] [ Se necesita una mejor fuente ] El agua tiene una mayor capacidad calorífica que el ácido, por lo que un recipiente con agua fría absorberá calor a medida que se añade ácido.
| Propiedad física | H2SO4 | Agua | Unidades |
|---|---|---|---|
| Densidad | 1.84 | 1.0 | kilogramo/litro |
| Capacidad calorífica volumétrica | 2.54 | 4.18 | kilojulios/litro |
| Punto de ebullición | 337 | 100 | °C |
Además, como el ácido es más denso que el agua, se hunde hasta el fondo. El calor se genera en la interfaz entre el ácido y el agua, que se encuentra en el fondo del recipiente. El ácido no hierve debido a su punto de ebullición más alto. El agua caliente cerca de la interfaz sube debido a la convección , que enfría la interfaz y evita que hierva tanto el ácido como el agua.
Por el contrario, la adición de agua al ácido sulfúrico concentrado da como resultado una fina capa de agua sobre el ácido. El calor generado en esta fina capa de agua puede hervir, lo que provoca la dispersión de un aerosol de ácido sulfúrico o, peor aún, una explosión .
La preparación de soluciones con una concentración superior a 6 M (35 %) es peligrosa, a menos que el ácido se agregue con la suficiente lentitud para permitir que la mezcla se enfríe. De lo contrario, el calor producido puede ser suficiente para hacer hervir la mezcla. Es esencial una agitación mecánica eficiente y un enfriamiento externo (como un baño de hielo).
La velocidad de reacción se duplica por cada aumento de 10 grados Celsius en la temperatura . [55] Por lo tanto, la reacción se volverá más violenta a medida que avanza la dilución, a menos que se le dé tiempo a la mezcla para que se enfríe. Agregar ácido al agua tibia provocará una reacción violenta.
A escala de laboratorio, el ácido sulfúrico se puede diluir vertiendo ácido concentrado sobre hielo triturado elaborado con agua desionizada. El hielo se derrite en un proceso endotérmico mientras se disuelve el ácido. La cantidad de calor necesaria para derretir el hielo en este proceso es mayor que la cantidad de calor que se desprende al disolver el ácido, de modo que la solución permanece fría. Una vez que se ha derretido todo el hielo, se puede realizar una dilución adicional utilizando agua.
Riesgos industriales
El ácido sulfúrico no es inflamable.
Los principales riesgos laborales que plantea este ácido son el contacto con la piel que produce quemaduras (véase más arriba) y la inhalación de aerosoles. La exposición a aerosoles en altas concentraciones produce una irritación inmediata y grave de los ojos, las vías respiratorias y las mucosas: esta irritación cesa rápidamente tras la exposición, aunque existe el riesgo de edema pulmonar posterior si el daño tisular ha sido más grave. En concentraciones más bajas, el síntoma más común de exposición crónica a aerosoles de ácido sulfúrico es la erosión de los dientes, que se encuentra en prácticamente todos los estudios: los indicios de un posible daño crónico de las vías respiratorias no son concluyentes a fecha de 1997. La exposición ocupacional repetida a nieblas de ácido sulfúrico puede aumentar la probabilidad de cáncer de pulmón hasta en un 64 por ciento. [56] En los Estados Unidos, el límite de exposición permisible (PEL) para el ácido sulfúrico está fijado en 1 mg/m3 : los límites en otros países son similares. Se han notificado casos de ingestión de ácido sulfúrico que han provocado deficiencia de vitamina B12 con degeneración combinada subaguda. La médula espinal es la más frecuentemente afectada en estos casos, pero los nervios ópticos pueden presentar desmielinización , pérdida de axones y gliosis .
Restricciones legales
El comercio internacional de ácido sulfúrico está controlado por la Convención de las Naciones Unidas contra el Tráfico Ilícito de Estupefacientes y Sustancias Sicotrópicas, de 1988 , que incluye el ácido sulfúrico en el Cuadro II de la Convención como una sustancia química frecuentemente utilizada en la fabricación ilícita de estupefacientes o sustancias sicotrópicas. [57]
Véase también
- Agua regia
- Éter dietílico : también conocido como “aceite dulce de vitriolo”
- Solución piraña
- Oxoácido de azufre
- Intoxicación por ácido sulfúrico
Referencias
- ^ abc Haynes, William M. (2014). Manual de química y física del CRC (95.ª edición). CRC Press. págs. 4–92. ISBN 9781482208689. Recuperado el 18 de noviembre de 2018 .
- ^ abcd Guía de bolsillo del NIOSH sobre peligros químicos. "#0577". Instituto Nacional de Seguridad y Salud Ocupacional (NIOSH).
- ^ ab Kemnitz, E.; Werner, C.; Trojanov, S. (15 de noviembre de 1996). "Reinvestigación del ácido sulfúrico cristalino y el hidrogenosulfato de oxonio". Acta Crystallographica Sección C Crystal Structure Communications . 52 (11): 2665–2668. Bibcode :1996AcCrC..52.2665K. doi :10.1107/S0108270196006749.
- ^ abcd Zumdahl, Steven S. (2009). Principios químicos, sexta edición . Houghton Mifflin Company. pág. A23. ISBN 978-0-618-94690-7.
- ^ abc "Ácido sulfúrico". Concentraciones inmediatamente peligrosas para la vida o la salud (IDLH) . Instituto Nacional de Seguridad y Salud Ocupacional (NIOSH).
- ^ abc "Hoja de datos de seguridad del ácido sulfúrico" (PDF) . arkema-inc.com . Archivado desde el original (PDF) el 17 de junio de 2012.
Líquido transparente a turbio, aceitoso, inodoro, incoloro a ligeramente amarillento.
- ^ abcd «Ácido sulfúrico: usos». dynamicscience.com.au . Archivado desde el original el 9 de mayo de 2013.
- ^ ab "Directrices médicas de emergencia química de BASF: ácido sulfúrico (H2SO4)" (PDF) . BASF Chemical Company. 2012. Archivado desde el original (PDF) el 14 de junio de 2019 . Consultado el 18 de diciembre de 2014 .
- ^ ab Chenier, Philip J. (1987). Encuesta sobre química industrial. Nueva York: John Wiley & Sons. págs. 45-57. ISBN 978-0-471-01077-7.
- ^ Hermann Müller "Ácido sulfúrico y trióxido de azufre" en Ullmann's Encyclopedia of Industrial Chemistry , Wiley-VCH, Weinheim. 2000 doi :10.1002/14356007.a25_635
- ^ "Ácido sulfúrico". essentialchemicalindustry.org .
- ^ ab "Desatascador de desagües con ácido sulfúrico" (PDF) . herchem.com. Archivado desde el original (PDF) el 29 de octubre de 2013.
- ^ ab "Ácido sulfúrico". The Columbia Encyclopedia (6.ª ed.). 2009. Consultado el 16 de marzo de 2010 .
- ^ abc "Ácido sulfúrico". Encyclopædia Britannica . Vol. 26 (11.ª ed.). 1910–1911. págs. 65–69.Tenga en cuenta que no hay ningún enlace wiki de EB1911 disponible para este artículo.
- ^ abc Greenwood, Norman N. ; Earnshaw, Alan (1997). Química de los elementos (2.ª ed.). Butterworth-Heinemann . ISBN 978-0-08-037941-8.
- ^ "Ácido sulfúrico" (PDF) . Determinación de los niveles de exposición crónica de referencia no cancerígena Lote 2B Diciembre de 2001 . 2001. Archivado desde el original (PDF) el 22 de mayo de 2003 . Consultado el 1 de octubre de 2012 .
- ^ "Ácido sulfúrico al 98%" (PDF) . rhodia.com. 2009. Archivado desde el original (PDF) el 7 de enero de 2011 . Consultado el 2 de julio de 2014 .
- ^ Giauque, WF; Hornung, EW; Kunzler, JE; Rubin, TR (enero de 1960). "Propiedades termodinámicas de soluciones acuosas de ácido sulfúrico e hidratos de 15 a 300 K. 1". Revista de la Sociedad Química Americana . 82 (1): 62–70. doi :10.1021/ja01486a014.
- ^ "Consorcio de autoridades educativas locales para la provisión de equipos científicos - HOJAS DE SEGURIDAD PARA ALUMNOS 22 Ácido sulfúrico (VI)" (PDF) . Archivado desde el original (PDF) el 31 de marzo de 2013.
- ^ "Constantes de ionización de ácidos inorgánicos". .chemistry.msu.edu . Consultado el 30 de mayo de 2011 .
- ^ Dolson, David A.; et al. (1995). "Demostraciones de deshidratación de carbohidratos". J. Chem. Educ . 72 (10): 927. Bibcode :1995JChEd..72..927D. doi :10.1021/ed072p927. ISSN 0021-9584.
- ^ Helmenstine, Anne (18 de febrero de 2020). "Demostración de la serpiente de carbono (azúcar y ácido sulfúrico)". Notas y proyectos científicos . Consultado el 5 de julio de 2022 .
- ^ Housecroft, Catherine E.; Sharpe, Alan G. (2008). "Capítulo 16: Los elementos del grupo 16". Química inorgánica, 3.ª edición . Pearson. pág. 523. ISBN 978-0-13-175553-6.
- ^ Kinney, Corliss Robert; Grey, VE (1959). Reacciones de un carbón bituminoso con ácido sulfúrico (PDF) . Universidad Estatal de Pensilvania. Archivado desde el original (PDF) el 28 de abril de 2017.
- ^ Carey, FA "Reacciones de arenos. Sustitución aromática electrofílica". Centro de aprendizaje en línea de química orgánica . Universidad de Calgary . Archivado desde el original el 6 de julio de 2008. Consultado el 27 de enero de 2008 .
{{cite web}}: CS1 maint: unfit URL (link) - ^ Ngo, Christian; Natowitz, Joseph (2016). Nuestro futuro energético: recursos, alternativas y medio ambiente. John Wiley & Sons. págs. 418–419. ISBN 9781119213369.
- ^ Pickard, Paul (25 de mayo de 2005). "Revisión del programa de hidrógeno del Departamento de Energía de 2005: ciclo termoquímico del azufre y el yodo" (PDF) . Sandia National Labs . Consultado el 8 de octubre de 2021 .
- ^ Pelletreau, K.; Muller-Parker, G. (2002). "El ácido sulfúrico en el alga feófita Desmarestia munda impide que el erizo de mar Strongylocentrotus droebachiensis se alimente". Biología marina . 141 (1): 1–9. Bibcode :2002MarBi.141....1K. doi :10.1007/s00227-002-0809-6. S2CID 83697676.
- ^ ab Kremser, S.; Thomson, LW (2016). "Aerosol estratosférico: observaciones, procesos e impacto en el clima" (PDF) . Reseñas de Geofísica . 54 (2): 278–335. Bibcode :2016RvGeo..54..278K. doi : 10.1002/2015RG000511 .
- ^ Krasnopolsky, Vladimir A. (2006). "Composición química de la atmósfera y las nubes de Venus: algunos problemas sin resolver". Ciencia planetaria y espacial . 54 (13–14): 1352–1359. Código Bibliográfico :2006P&SS...54.1352K. doi :10.1016/j.pss.2006.04.019.
- ^ Orlando, TM; McCord, TB; Grieves, GA (2005). "La naturaleza química del material de la superficie de Europa y su relación con un océano subterráneo". Icarus . 177 (2): 528–533. Bibcode :2005Icar..177..528O. doi :10.1016/j.icarus.2005.05.009.
- ^ Jones, Edward M. (1950). "Fabricación de ácido sulfúrico mediante proceso de cámara". Química industrial e ingeniería . 42 (11): 2208–2210. doi :10.1021/ie50491a016.
- ^ (Harm), Benninga, H. (1990). Una historia de la producción de ácido láctico: un capítulo en la historia de la biotecnología . Dordrecht [Países Bajos]: Kluwer Academic Publishers. p. 4. ISBN 9780792306252.OCLC 20852966 .
{{cite book}}: CS1 maint: multiple names: authors list (link) - ^ Davenport, William George; King, Matthew J. (2006). Fabricación de ácido sulfúrico: análisis, control y optimización. Elsevier. pp. 8, 13. ISBN 978-0-08-044428-4. Recuperado el 23 de diciembre de 2011 .
- ^ Greenwood, Norman N. ; Earnshaw, Alan (1997). Química de los elementos (2.ª ed.). Butterworth-Heinemann . pág. 653. ISBN 978-0-08-037941-8.
- ^ Müller, Hermann (2012). "Ácido sulfúrico y trióxido de azufre". Ullmann's Encyclopedia of Industrial Chemistry . Weinheim: Wiley-VCH. doi :10.1002/14356007.a25_635. ISBN 978-3527306732.
- ^ Karpenko, Vladimír; Norris, John A. (2002). "Vitriolo en la Historia de la Química". Lista química . 96 (12): 997–1005.
- ^ Karpenko y Norris 2002, págs. 999-1000.
- ^ Multhauf, Robert P. (1966). Los orígenes de la química . Londres: Oldbourne.págs. 140-142.
- ^ Needham, Joseph ; Ping-Yü, Ho; Gwei-Djen, Lu; Sivin, Nathan (1980). Ciencia y civilización en China. Volumen 5, Química y tecnología química. Parte IV, Descubrimiento e invención espagíricos: aparatos, teorías y dones. Cambridge: Cambridge University Press. ISBN 978-0-521-08573-1.pag. 195, nota d. Stapleton, Henry E .; Azo, RF; Hidayat Husain, M. (1927). "Química en Irak y Persia en el siglo X d. C." Memorias de la Sociedad Asiática de Bengala . VIII (6): 317–418. OCLC 706947607.pp. 333 (sobre el Liber Bubacaris , cf. p. 369, nota 3), 393. Cita de la p. 393: "Es sumamente curioso ver lo cerca que estuvo ar-Rāzī del descubrimiento del ácido sulfúrico, sin reconocer realmente las poderosas propiedades disolventes del destilado de vitriolos y alumbre. Esto es aún más sorprendente, ya que se dio cuenta plenamente de los poderes reactivos tanto del sulfuro de arsénico como del sal-amoniaco, los 'espíritus' con los que debe haber asociado el destilado de alumbre".
- ^ Needham et al. 1980, pág. 195, nota d.
- ^ Pattin, Adriaan (1972). "Un recueil alchimique: le manuscrit Firenze, Bibl. Riccardiana, L. III. 13. 119 - Descripción y documentación". Boletín de Filosofía Médiévale . 14 : 89-107. doi :10.1484/J.BPM.3.143.págs. 93–94.
- ^ Moureau, Sébastien (2020). «Min al-kīmiyāʾ ad alchimiam. La transmisión de la alquimia desde el mundo árabe-musulmán al Occidente latino en la Edad Media». Micrologus . 28 : 87–141. hdl :2078.1/211340.pag. 114 (núm. 20). Moureau menciona que el trabajo también se realiza a veces de forma anónima. Da su incipit como " cum de sublimiori atque precipuo rerum effectum... ". Algunas partes han sido publicadas por Ruska, Julius (1939). "Pseudepigraphe Rasis-Schriften". Osiris . 7 : 31–94. doi :10.1086/368502. S2CID 143373785.págs. 56–65.
- ^ Hoefer, Fernando (1866). Historia de la chimenea (2ª ed.). París: Librairie de Firmin Didot.pág. 341.
- ^ Ruska 1939, pág. 58; Pattin 1972, pág. 93; Halleux, Robert (1996). "La recepción de la alquimia árabe en Occidente". En Rashed, Roshdi (ed.). Enciclopedia de la historia de la ciencia árabe . Vol. 3. Londres: Routledge. págs. 886–902. ISBN. 9780415020633.p. 892. Sobre el Liber de septuaginta latino y las otras dos traducciones latinas conocidas de las obras árabes de Jabir, véase Moureau 2020, pp. 111-112.
- ^ Ruska 1939, pág. 58.
- ^ Ruska 1939, págs. 58–61.
- ↑ Halleux 1996, p. 892; Moureau 2020, p. 114. Moureau menciona que 'Raymond de Marsella' puede ser el astrónomo con ese nombre (fl. 1141). Hoefer 1866, p. 343 todavía creía firmemente que la obra pertenecía a al-Razi, pero esta opinión ha sido abandonada desde los estudios realizados por Ruska 1939; cf. Moureau 2020, p. 117, cita "aunque muchos textos alquímicos latinos se atribuyen a Rāzı̄, solo uno es, en el estado actual de la investigación, conocido como una traducción del famoso médico y alquimista" (es decir, el Liber secretorum Bubacaris , una paráfrasis del Kitāb al-asrār de al-Razi ); Ferrario, Gabriele (2009). "Un diccionario árabe de términos alquímicos técnicos: MS Sprenger 1908 de la Staatsbibliothek zu Berlin (fols. 3r–6r)". Ambix . 56 (1): 36–48. doi :10.1179/174582309X405219. PMID 19831258. S2CID 41045827.p. 42, cita "Una crítica fuerte y aún no refutada de esta atribución tradicional fue propuesta por Ruska [...]".
- ^ Al-Hassan 2001, págs. 60, 63. Sobre la datación de este manuscrito, véase también Berthelot, Marcellin ; Houdas, Octava V. (1893). La Chimie au MoyenÂge . París: Imprimerie nationale.vol. II, pág. xvii.
- ^Ab Al-Hassan 2001, pág. 60.
- ^ Williams, Alan (2012). La espada y el crisol: una historia de la metalurgia de las espadas europeas hasta el siglo XVI. Leiden: Brill. ISBN 978-90-04-22783-5.pág. 104. Al-Hassan, Ahmad Y. (2001). Ciencia y tecnología en el Islam: tecnología y ciencias aplicadas. UNESCO. ISBN 978-92-3-103831-0.pág. 60.
- ^ Karpenko y Norris 2002, págs. 1002-1004.
- ^ Philip J. Chenier (1 de abril de 2002). Encuesta sobre química industrial. Springer. pp. 28–. ISBN 978-0-306-47246-6. Recuperado el 23 de diciembre de 2011 .
- ^ Snyder, Lucy A. (4 de noviembre de 2005). "Haz lo que debes hacer, agrega ácido al agua". Lucy A. Snyder . Consultado el 23 de enero de 2022 .
- ^ Pauling, LC (1988) Química general , Publicaciones de Dover
- ^ Beaumont, JJ; Leveton, J; Knox, K; Bloom, T; McQuiston, T; Young, M; Goldsmith, R; Steenland, NK; Brown, DP; Halperin, WE (1987). "Mortalidad por cáncer de pulmón en trabajadores expuestos a nieblas de ácido sulfúrico y otras nieblas ácidas". J Natl Cancer Inst . 79 (5): 911–21. doi :10.1093/jnci/79.5.911. PMID 3479642.
- ^ "Anexo al Formulario D ("Lista Roja"), 11ª Edición" (PDF) . Viena, Austria: Junta Internacional de Fiscalización de Estupefacientes . Enero de 2007. pág. 4. Archivado (PDF) desde el original el 27 de febrero de 2008.
Enlaces externos
- Ficha internacional de seguridad química 0362
- Ácido sulfúrico en la Tabla Periódica de Vídeos (Universidad de Nottingham)
- Guía de bolsillo del NIOSH sobre peligros químicos
- CDC – Ácido sulfúrico – Tema de seguridad y salud en el trabajo de NIOSH
- Calculadoras: tensiones superficiales, densidades, molaridades y molalidades de ácido sulfúrico acuoso






![{\displaystyle {\underset {\text{polisacárido}}{{\ce {[C6H10O5]}}_{n}}}\longrightarrow 6n\ {\ce {C}}+5n\ {\ce {H2O}} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/fc5b432fe56cddc7fd4e08fda4502ba801cd3d07)





