Prostaciclina
 | |
 | |
| Datos clínicos | |
|---|---|
| Nombres comerciales | Flolan, Veletri |
| AHFS / Drogas.com | Monografía |
| Datos de licencia |
|
Categoría de embarazo |
|
| Código ATC |
|
| Estatus legal | |
| Estatus legal | |
| Datos farmacocinéticos | |
| Vida media de eliminación | 42 segundos |
| Identificadores | |
| |
| Número CAS | |
| Identificador de centro de PubChem |
|
| Unión Internacional para la Investigación y el Desarrollo (IUPHAR)/BPS |
|
| Banco de medicamentos | |
| Araña química | |
| UNIVERSIDAD |
|
| BARRIL |
|
| Química biológica | |
| Panel de control CompTox ( EPA ) |
|
| Datos químicos y físicos | |
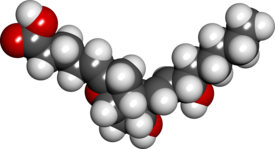
| Fórmula | C20H32O5 |
| Masa molar | 352,471 g·mol −1 |
| Modelo 3D ( JSmol ) |
|
| |
 norte norte Y (¿que es esto?) (verificar) Y (¿que es esto?) (verificar) | |
La prostaciclina (también llamada prostaglandina I 2 o PGI 2 ) es una prostaglandina que pertenece a la familia de las moléculas lipídicas de los eicosanoides . Inhibe la activación plaquetaria y también es un vasodilatador eficaz.
Cuando se utiliza como fármaco, también se conoce como epoprostenol . [1] A veces, los términos se utilizan indistintamente. [2]
Función
La prostaciclina previene principalmente la formación del tapón plaquetario que interviene en la hemostasia primaria (una parte de la formación del coágulo sanguíneo ). Lo hace inhibiendo la activación plaquetaria. [3] También es un vasodilatador eficaz . Las interacciones de la prostaciclina contrastan con las del tromboxano (TXA 2 ), otro eicosanoide. Ambas moléculas se derivan del ácido araquidónico y trabajan juntas con efectos agregadores plaquetarios opuestos. Estos sugieren firmemente un mecanismo de homeostasis cardiovascular entre estas dos hormonas en relación con el daño vascular .
Usos médicos
Se utiliza para tratar la hipertensión arterial pulmonar (HAP), [4] [5] [6] la fibrosis pulmonar , [7] así como la aterosclerosis . [7] Las prostaciclinas se administran a personas con HAP de clase III o clase IV. [8]
Degradación
La prostaciclina, que tiene una vida media de 42 segundos, [9] se descompone en 6-ceto-PGF 1 , que es un vasodilatador mucho más débil. Una forma de estabilizar la prostaciclina en su forma activa, especialmente durante la administración del fármaco, es prepararla en un tampón alcalino. Incluso a pH fisiológico, la prostaciclina puede formar rápidamente el producto de hidratación inactivo 6-ceto-prostaglandina F1α. [10]
Mecanismo
Efecto de la prostaciclina Mecanismo Respuesta celular
Funciones clásicasTono del buque ↑cAMP, ↓ET-1
↓Ca 2+ , ↑K +↓Proliferación de células SMC
↑VosodilataciónAntiproliferativo ↑AMPc
↑PPARgamma↓Crecimiento de fibroblastos
↑ApoptosisAntitrombótico ↓Tromboxano-A2
↓PDGF↓Agregación plaquetaria
↓Adherencia de plaquetas a la pared vascular
Funciones novedosasAntiinflamatorio ↓IL-1, IL-6
↑IL-10↓Citocinas proinflamatorias
↑Citocinas antiinflamatoriasAntimitogénico ↓FCEV
↓FCE-β↓Angiogénesis
↑Remodelación de la matriz extracelular
Como se mencionó anteriormente, la prostaciclina (PGI 2 ) es liberada por células endoteliales sanas y realiza su función a través de una cascada de señalización paracrina que involucra receptores acoplados a proteína G en plaquetas y células endoteliales cercanas. El receptor acoplado a proteína Gs de plaquetas ( receptor de prostaciclina ) se activa cuando se une a PGI 2 . Esta activación, a su vez, envía señales a la adenilil ciclasa para que produzca AMPc . El AMPc continúa inhibiendo cualquier activación plaquetaria indebida (para promover la circulación) y también contrarresta cualquier aumento en los niveles de calcio citosólico que resultaría de la unión del tromboxano A2 (TXA 2 ) (lo que conduce a la activación plaquetaria y la coagulación posterior ). PGI 2 también se une a los receptores de prostaciclina endoteliales y, de la misma manera, aumenta los niveles de AMPc en el citosol. Este AMPc luego activa la proteína quinasa A (PKA). La PKA luego continúa la cascada al promover la fosforilación de la quinasa de la cadena ligera de miosina , que la inhibe y conduce a la relajación del músculo liso y la vasodilatación . Se puede observar que la PGI 2 y el TXA 2 funcionan como antagonistas fisiológicos.
Miembros[11]
| PROSTACICLINAS | |||
|---|---|---|---|
| Flolan (epoprostenol sódico) inyectable | Infusión continua | 2 ng/kg/min para comenzar, aumentar 2 ng/kg/min cada 15 minutos o más hasta lograr un equilibrio adecuado de eficacia/tolerabilidad | Clase III Clase IV |
| Veletri (epoprostenol) para inyección | Infusión continua | 2 ng/kg/min para comenzar, aumentar 2 ng/kg/min cada 15 minutos o más hasta lograr un equilibrio adecuado de eficacia/tolerabilidad | Clase III Clase IV |
| Remodulin SC§ ( treprostinil sódico) Inyección | Infusión continua | 1,25 ng/kg/min para comenzar, aumentar hasta 1,25 ng/kg/min por semana durante 4 semanas, luego hasta 2,5 ng/kg/min por semana hasta lograr un equilibrio adecuado entre eficacia y tolerabilidad | Clase II Clase III Clase IV |
| Ventavis ( iloprost ) Solución para inhalación | Inhalado 6–9 veces al día | 2,5 μg 6 a 9 veces al día para comenzar, aumentar a 5,0 μg 6 a 9 veces al día si se tolera bien | Clase III Clase IV |
Farmacología

Los análogos sintéticos de prostaciclina ( iloprost , cisaprost) se utilizan por vía intravenosa, subcutánea o por inhalación:
- como vasodilatador en el fenómeno de Raynaud severo o en la isquemia de una extremidad;
- en hipertensión pulmonar .
- en la hipertensión pulmonar primaria (HPP)
La producción de prostaciclina se inhibe por la acción de los AINE sobre las enzimas ciclooxigenasas COX1 y COX2, que convierten el ácido araquidónico en prostaglandina H2 (PGH 2 ), precursora inmediata de la prostaciclina. Como el tromboxano (un eicosanoide estimulador de la agregación plaquetaria) también se encuentra aguas abajo de las enzimas COX, se podría pensar que el efecto de los AINE actuaría para equilibrar. Sin embargo, las concentraciones de prostaciclina se recuperan mucho más rápido que los niveles de tromboxano, por lo que la administración de aspirina inicialmente tiene poco o ningún efecto, pero finalmente previene la agregación plaquetaria (el efecto de las prostaglandinas predomina a medida que se regeneran). Esto se explica al comprender las células que producen cada molécula, TXA 2 y PGI 2 . Dado que la PGI 2 se produce principalmente en una célula endotelial nucleada, la inhibición de la COX por los AINE puede superarse con el tiempo mediante el aumento de la activación del gen COX y la posterior producción de más enzimas COX para catalizar la formación de PGI 2 . Por el contrario, el TXA 2 es liberado principalmente por plaquetas anucleadas, que no pueden responder a la inhibición de la COX por los AINE con la transcripción adicional del gen COX porque carecen del material de ADN necesario para realizar dicha tarea. Esto permite que los AINE resulten en el predominio de la PGI 2 que promueve la circulación y retarda la trombosis .
En pacientes con hipertensión pulmonar , el epoprostenol inhalado reduce la presión pulmonar y mejora el volumen sistólico del ventrículo derecho en pacientes sometidos a cirugía cardíaca. Una dosis de 60 μg es hemodinámicamente segura y su efecto se revierte completamente después de 25 minutos. No se ha encontrado evidencia de disfunción plaquetaria o un aumento del sangrado quirúrgico después de la administración de epoprostenol inhalado. [12] Se sabe que el fármaco causa sofocos, dolores de cabeza e hipotensión. [13]
Síntesis
Biosíntesis
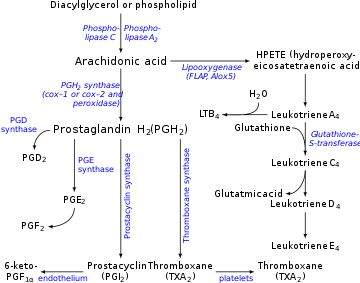
La prostaciclina se produce en las células endoteliales , que recubren las paredes de las arterias y las venas, [14] a partir de la prostaglandina H 2 (PGH 2 ) por la acción de la enzima prostaciclina sintasa . Aunque la prostaciclina se considera un mediador independiente, se llama PGI 2 (prostaglandina I 2 ) en la nomenclatura de los eicosanoides, y es un miembro de los prostanoides (junto con las prostaglandinas y el tromboxano ). La PGI 2 , derivada principalmente de la COX-2 en humanos, es el principal metabolito araquidonato liberado del endotelio vascular. Este es un punto controvertido, algunos asignan a la COX 1 como la principal ciclooxigenasa productora de prostaciclina en las células endoteliales de los vasos sanguíneos. [15]
La prostaglandina de serie 3 PGH 3 también sigue la vía de la prostaciclina sintasa, produciendo otra prostaciclina, PGI 3 . [16] El término no calificado "prostaciclina" generalmente se refiere a PGI 2 . PGI 2 se deriva del ácido araquidónico ω-6 . PGI 3 se deriva del ω-3 EPA .
Síntesis artificial
La prostaciclina se puede sintetizar a partir del éster metílico de la prostaglandina F 2α . [17] Después de su síntesis, el fármaco se reconstituye en solución salina y glicerina. [18]
Debido a que la prostaciclina es tan químicamente lábil, se utiliza la cuantificación de sus metabolitos inactivos, en lugar de los compuestos activos, para evaluar su tasa de síntesis. [19]
Historia
Durante la década de 1960, un equipo de investigación del Reino Unido, encabezado por el profesor John Vane , comenzó a explorar el papel de las prostaglandinas en la anafilaxia y las enfermedades respiratorias. Trabajando con un equipo del Royal College of Surgeons , Vane descubrió que la aspirina y otros antiinflamatorios orales actúan inhibiendo la síntesis de prostaglandinas. Este hallazgo crucial abrió la puerta a una comprensión más amplia del papel de las prostaglandinas en el cuerpo.
Un equipo de la Wellcome Foundation dirigido por Salvador Moncada había identificado un mediador lipídico al que llamaron "PG-X", que inhibe la agregación plaquetaria. El PG-X, más tarde conocido como prostaciclina, es 30 veces más potente que cualquier otro agente antiagregante conocido en ese momento. Lo hicieron mientras buscaban una enzima que genera un prostanoide inestable, el tromboxano A2 [20].
En 1976, Vane y sus colegas investigadores Salvador Moncada , Ryszard Gryglewski y Stuart Bunting publicaron el primer artículo sobre la prostaciclina en Nature . [21] La colaboración produjo una molécula sintetizada, que se denominó epoprostenol. Pero, al igual que con la prostaciclina nativa, la molécula de epoprostenol es inestable en solución y propensa a una rápida degradación. [ cita requerida ] Esto presentó un desafío tanto para los experimentos in vitro como para las aplicaciones clínicas.
Para superar este desafío, el equipo de investigación que descubrió la prostaciclina continuó con la investigación y sintetizó casi 1000 análogos. [ cita requerida ]
Referencias
- ^ "epoprostenol" en el Diccionario médico de Dorland
- ^ Kermode J, Butt W, Shann F (agosto de 1991). "Comparación entre prostaglandina E1 y epoprostenol (prostaciclina) en lactantes después de una cirugía cardíaca". British Heart Journal . 66 (2): 175–178. doi :10.1136/hrt.66.2.175. PMC 1024613 . PMID 1883670.
- ^ Base patológica de la enfermedad , Robbins y Cotran, 8.ª ed. Saunders, Filadelfia, 2010
- ^ Ruopp NF, Cockrill BA (abril de 2022). "Diagnóstico y tratamiento de la hipertensión arterial pulmonar: una revisión". JAMA . 327 (14): 1379–1391. doi :10.1001/jama.2022.4402. PMID 35412560.
- ^ "Monografía de epoprostenol sódico para profesionales". Drugs.com . AHFS. 6 de abril de 2020 . Consultado el 22 de octubre de 2020 .
- ^ "Flolan - inyección de epoprostenol sódico, polvo, liofilizado, para solución Diluyente - solución acuosa". DailyMed . 15 de noviembre de 2019 . Consultado el 22 de octubre de 2020 .
- ^ ab Stitham J, Midgett C, Martin KA, Hwa J (13 de mayo de 2011). "Prostaciclina: una paradoja inflamatoria". Frontiers in Pharmacology . 2 . Frontiers Media SA: 24. doi : 10.3389/fphar.2011.00024 . PMC 3108482 . PMID 21687516.
- ^ Hassoun PM (diciembre de 2021). «Hipertensión arterial pulmonar». The New England Journal of Medicine . 385 (25): 2361–2376. doi :10.1056/NEJMra2000348. PMID 34910865.
- ^ Cawello W, Schweer H, Müller R, Bonn R, Seyberth HW (1994). "Metabolismo y farmacocinética de la prostaglandina E1 administrada por infusión intravenosa en sujetos humanos". Revista Europea de Farmacología Clínica . 46 (3): 275–277. doi :10.1007/BF00192562. PMID 8070511. S2CID 25410558.
- ^ Lewis PJ, Dollery CT (julio de 1983). "Farmacología clínica y potencial de la prostaciclina". British Medical Bulletin . 39 (3): 281–4. doi :10.1093/oxfordjournals.bmb.a071834. PMID 6354353.
- ^ ^ REM_RefGuideWC_AUG07v.1
- ^ Haché M, Denault A, Bélisle S, Robitaille D, Couture P, Sheridan P, et al. (marzo de 2003). "Epoprostenol inhalado (prostaciclina) e hipertensión pulmonar antes de la cirugía cardíaca". The Journal of Thoracic and Cardiovascular Surgery . 125 (3): 642–649. doi : 10.1067/mtc.2003.107 . PMID 12658208.
- ^ Nickson, C. (28 de octubre de 2015). Prostaciclina o epoprostenol. Recuperado el 16 de noviembre de 2015 de http://lifeinthefastlane.com/ccc/prostacyclin-or-epoprostenol/
- ^ prostaciclina. (sin fecha) Miller-Keane Encyclopedia and Dictionary of Medicine, Nursing, and Allied Health, séptima edición. (2003). Consultado el 17 de noviembre de 2015 en http://medical-dictionary.thefreedictionary.com/prostacyclin
- ^ Kirkby NS, Lundberg MH, Harrington LS, Leadbeater PD, Milne GL, Potter CM, et al. (octubre de 2012). "La ciclooxigenasa-1, no la ciclooxigenasa-2, es responsable de la producción fisiológica de prostaciclina en el sistema cardiovascular". Actas de la Academia Nacional de Ciencias de los Estados Unidos de América . 109 (43): 17597–17602. Bibcode :2012PNAS..10917597K. doi : 10.1073/pnas.1209192109 . PMC 3491520 . PMID 23045674.
- ^ Fischer S, Weber PC (septiembre de 1985). "El tromboxano (TX)A3 y la prostaglandina (PG)I3 se forman en el hombre después de la ingesta de ácido eicosapentaenoico: identificación y cuantificación mediante cromatografía de gases capilar-espectrometría de masas por impacto electrónico". Espectrometría de masas biomédica . 12 (9): 470–476. doi :10.1002/bms.1200120905. PMID 2996649.
- ^ Johnson RA, Lincoln FH, Nidy EG, Schneider WP, Thompson JL, Axen U (1978). "Síntesis y caracterización de prostaciclina, 6-ketoprostaglandina F1.alpha., prostaglandina I1 y prostaglandina I3". Revista de la Sociedad Química Americana . 100 (24): 7690–7705. doi :10.1021/ja00492a043.
- ^ Nickson C (15 de octubre de 2015). «Prostaciclina o epoprostenol». La vida en el carril rápido . Archivado desde el original el 28 de marzo de 2015. Consultado el 16 de noviembre de 2015 .
- ^ Collins PW, Djuric SW (1993). "Síntesis de análogos de prostaglandinas y prostaciclinas terapéuticamente útiles". Chemical Reviews . 03 (4): 1533–1564. doi :10.1021/cr00020a007.
- ^ Kermode J, Butt W, Shann F (agosto de 1991). "Comparación entre prostaglandina E1 y epoprostenol (prostaciclina) en lactantes después de una cirugía cardíaca". British Heart Journal . 66 (2): 175–178. doi :10.1016/s0002-9149(99)80377-4. PMC 1024613 . PMID 1883670.
- ^ Moncada S, Gryglewski R, Bunting S, Vane JR (octubre de 1976). "Una enzima aislada de las arterias transforma los endoperóxidos de prostaglandina en una sustancia inestable que inhibe la agregación plaquetaria". Nature . 263 (5579): 663–665. Bibcode :1976Natur.263..663M. doi :10.1038/263663a0. PMID 802670. S2CID 4279030.
Enlaces externos
- "Epoprostenol". Portal de información sobre medicamentos . Biblioteca Nacional de Medicina de EE. UU.
- "Epoprostenol sódico". Portal de información sobre medicamentos . Biblioteca Nacional de Medicina de EE. UU.
