Formaldehído
| |||
 | |||
| Nombres | |||
|---|---|---|---|
| Nombre IUPAC preferido Formaldehído [1] | |||
| Nombre sistemático de la IUPAC Metanal [1] | |||
Otros nombres
| |||
| Identificadores | |||
Modelo 3D ( JSmol ) |
| ||
| 3DMet |
| ||
| 1209228 | |||
| EBICh | |||
| Química biológica | |||
| Araña química | |||
| Banco de medicamentos | |||
| Tarjeta informativa de la ECHA | 100.000.002 | ||
| Número CE |
| ||
| Número E | E240 (conservantes) | ||
| 445 | |||
| |||
| BARRIL | |||
| Malla | Formaldehído | ||
Identificador de centro de PubChem |
| ||
| Número RTECS |
| ||
| UNIVERSIDAD | |||
| Número de la ONU | 2209 | ||
Panel de control CompTox ( EPA ) |
| ||
| |||
| |||
| Propiedades [7] | |||
| C2O | |||
| Masa molar | 30,026 g·mol −1 | ||
| Apariencia | Gas incoloro | ||
| Densidad | 0,8153 g/cm 3 (−20 °C) [2] (líquido) | ||
| Punto de fusión | -92 °C (-134 °F; 181 K) | ||
| Punto de ebullición | -19 °C (-2 °F; 254 K) [2] | ||
| 400 g/l | |||
| registro P | 0.350 | ||
| Presión de vapor | > 1 atm [3] | ||
| Acidez (p K a ) | 13,27 (hidrato) [4] [5] | ||
| −18,6·10 −6 cm3 / mol | |||
| 2.330 D [6] | |||
| Estructura | |||
| C2v | |||
| Trigonal plana | |||
| Termoquímica [8] | |||
Capacidad calorífica ( C ) | 35,387 J·mol −1 ·K −1 | ||
Entropía molar estándar ( S ⦵ 298 ) | 218,760 J·mol −1 ·K −1 | ||
Entalpía estándar de formación (Δ f H ⦵ 298 ) | −108,700 kJ·mol −1 | ||
Energía libre de Gibbs (Δ f G ⦵ ) | −102,667 kJ·mol −1 | ||
Entalpía estándar de combustión (Δ c H ⦵ 298 ) | 571 kJ·mol −1 | ||
| Farmacología | |||
| QP53AX19 ( OMS ) | |||
| Peligros | |||
| Etiquetado SGA : | |||
   [9] [9] | |||
| Peligro | |||
| H301+H311+H331 , H314 , H317 , H335 , H341 , H350 , H370 [9] | |||
| P201 , P280 , P303+P361+P353 , P304+P340+P310 , P305+P351+P338 , P308+P310 [9] | |||
| NFPA 704 (rombo cortafuegos) | |||
| punto de inflamabilidad | 64 °C (147 °F; 337 K) | ||
| 430 °C (806 °F; 703 K) | |||
| Límites de explosividad | 7–73% | ||
| Dosis o concentración letal (LD, LC): | |||
LD 50 ( dosis media ) | 100 mg/kg (oral, rata) [12] | ||
LC 50 ( concentración media ) | 333 ppm (ratón, 2 h ) 815 ppm (rata, 30 min) [13] | ||
LC Lo ( valor más bajo publicado ) | 333 ppm (cat., 2 h ) [13] | ||
| NIOSH (límites de exposición a la salud en EE. UU.): | |||
PEL (Permisible) | TWA 0,75 ppm ST 2 ppm (como formaldehído y formalina) [10] [11] | ||
REL (recomendado) | Ca TWA 0,016 ppm C 0,1 ppm [15 minutos] [10] | ||
IDLH (Peligro inmediato) | Ca [20 ppm] [10] | ||
| Ficha de datos de seguridad (FDS) | MSDS (archivada) | ||
| Compuestos relacionados | |||
Aldehídos relacionados | |||
Compuestos relacionados | |||
Salvo que se indique lo contrario, los datos se proporcionan para los materiales en su estado estándar (a 25 °C [77 °F], 100 kPa). | |||
Formaldehído ( / f ɔːr ˈ m æ l d ɪ h aɪ d / para-MAL-di-hide,EE.UU.también/ f ə r -/ formaldehído(nombresistemático metanal) es uncompuesto orgánicocon lafórmula química CH2Oyla estructuraH−CHO, más precisamenteH2C=O. El compuesto es un gas picante e incoloro quepolimerizaespontáneamente enparaformaldehído. Se almacena como soluciones acuosas (formalina), que consiste principalmente en el hidrato CH2(OH)2. Es el más simple de losaldehídos(R−CHO). Como precursor de muchos otros materiales y compuestos químicos, en 2006 la producción mundial de formaldehído se estimó en 12 millones de toneladas por año.[14]Se utiliza principalmente en la producción deresinas, por ejemplo, paratableros de partículasyrevestimientos. También se producen pequeñas cantidades de forma natural.
El formaldehído está clasificado como carcinógeno [nota 1] y puede causar irritación respiratoria y cutánea en caso de exposición. [15]
Formularios
El formaldehído es más complejo que muchos compuestos de carbono simples, ya que adopta diversas formas. Estos compuestos a menudo se pueden utilizar indistintamente y pueden interconvertirse. [ cita requerida ]
- Formaldehído molecular. Gas incoloro con un olor característico, penetrante e irritante. Es estable a unos 150 °C, pero se polimeriza cuando se condensa en líquido.
- 1,3,5-Trioxano , de fórmula (CH2O ) 3 . Es un sólido blanco que se disuelve sin degradarse en disolventes orgánicos. Es un trímero del formaldehído molecular.
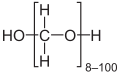
- Paraformaldehído , con la fórmula HO(CH 2 O) n H. Es un sólido blanco insoluble en la mayoría de los disolventes.
- Metanodiol , de fórmula CH2 ( OH) 2 . Este compuesto también existe en equilibrio con diversos oligómeros (polímeros cortos), dependiendo de la concentración y la temperatura. Una solución saturada de agua, de aproximadamente 40% de formaldehído en volumen o 37% en masa, se denomina "formalina al 100%.
Generalmente se añade una pequeña cantidad de estabilizador , como metanol , para suprimir la oxidación y la polimerización . Una formalina comercial típica puede contener entre un 10 y un 12 % de metanol además de varias impurezas metálicas.
"Formaldehído" se utilizó por primera vez como marca genérica en 1893 después de un nombre comercial anterior, "formalina". [16]
- Principales formas de formaldehído
- Formaldehído monomérico (tema de este artículo)
- El trioxano es un trímero cíclico estable de formaldehído.
- El paraformaldehído es una forma común de formaldehído para aplicaciones industriales.
- Metanodiol, la especie predominante en soluciones acuosas diluidas de formaldehído.
Estructura y unión
El formaldehído molecular contiene un átomo de carbono central con un doble enlace al átomo de oxígeno y un enlace sencillo a cada átomo de hidrógeno . Esta estructura se resume en la fórmula condensada H 2 C=O. [17] La molécula es plana, tiene forma de Y y su simetría molecular pertenece al grupo puntual C 2v . [18] La geometría molecular precisa del formaldehído gaseoso se ha determinado mediante difracción de electrones de gas [17] [19] y espectroscopia de microondas . [20] [21] Las longitudes de enlace son 1,21 Å para el enlace carbono-oxígeno [17] [19] [20] [21] [22] y alrededor de 1,11 Å para el enlace carbono-hidrógeno , [17] [19] [20] [21] mientras que el ángulo de enlace H–C–H es de 117°, [20] [21] cercano al ángulo de 120° encontrado en una molécula plana trigonal ideal . [17] Algunos estados electrónicos excitados del formaldehído son piramidales en lugar de planos como en el estado fundamental . [22]
Aparición
Los procesos en la atmósfera superior contribuyen con más del 80% del formaldehído total en el medio ambiente. [23] El formaldehído es un intermediario en la oxidación (o combustión ) del metano , así como de otros compuestos de carbono, por ejemplo, en los incendios forestales , los escapes de los automóviles y el humo del tabaco . Cuando se produce en la atmósfera por la acción de la luz solar y el oxígeno sobre el metano atmosférico y otros hidrocarburos , se convierte en parte del smog . El formaldehído también se ha detectado en el espacio exterior.
El formaldehído y sus aductos son omnipresentes en la naturaleza. Los alimentos pueden contener formaldehído en niveles de 1 a 100 mg/kg. [24] El formaldehído, formado en el metabolismo de los aminoácidos serina y treonina , se encuentra en el torrente sanguíneo de los humanos y otros primates en concentraciones de aproximadamente 50 micromolar . [25] Los experimentos en los que los animales están expuestos a una atmósfera que contiene formaldehído marcado isotópicamente han demostrado que incluso en animales expuestos deliberadamente, la mayoría de los aductos de formaldehído-ADN encontrados en tejidos no respiratorios se derivan de formaldehído producido endógenamente. [26]
El formaldehído no se acumula en el medio ambiente, ya que se descompone en pocas horas por la acción de la luz solar o de las bacterias presentes en el suelo o el agua. Los seres humanos metabolizan el formaldehído rápidamente, convirtiéndolo en ácido fórmico , por lo que no se acumula. [27] [28] No obstante, presenta importantes problemas de salud, como contaminante .
Formaldehído interestelar
El formaldehído parece ser una sonda útil en astroquímica debido a la prominencia de las transiciones de dobletes K 1 10 ←1 11 y 2 11 ←2 12 . Fue la primera molécula orgánica poliatómica detectada en el medio interestelar . [29] Desde su detección inicial en 1969, se ha observado en muchas regiones de la galaxia . Debido al interés generalizado en el formaldehído interestelar, se ha estudiado ampliamente, lo que ha producido nuevas fuentes extragalácticas. [30] Un mecanismo propuesto para la formación es la hidrogenación del hielo de CO: [31]
- H + CO → HCO
- HCO2 + H → CH2O
También se han observado HCN , HNC , H 2 CO y polvo dentro de las comas de los cometas C/2012 F6 (Lemmon) y C/2012 S1 (ISON) . [32] [33]
Síntesis y producción industrial
Síntesis de laboratorio
El formaldehído fue reportado por primera vez en 1859 por el químico ruso Aleksandr Butlerov (1828-1886). [34] En su artículo, Butlerov se refirió al formaldehído como "dioximetileno" (dióxido de metileno) porque su fórmula empírica para él era incorrecta (C 4 H 4 O 4 ). Fue identificado de manera concluyente por August Wilhelm von Hofmann , quien anunció por primera vez la producción de formaldehído al pasar vapor de metanol en el aire sobre un alambre de platino caliente. [35] [36] Con modificaciones, el método de Hoffmann sigue siendo la base de la ruta industrial actual.
Las rutas de solución al formaldehído también implican la oxidación de metanol o yodometano . [37]
Industria
El formaldehído se produce industrialmente mediante la oxidación catalítica del metanol . Los catalizadores más comunes son el metal plata , el óxido de hierro (III) , [38] los óxidos de hierro y molibdeno (por ejemplo, el molibdato de hierro (III) ) con una superficie enriquecida con molibdeno , [39] o los óxidos de vanadio . En el proceso formox , que se utiliza habitualmente , el metanol y el oxígeno reaccionan a una temperatura de entre 250 y 400 °C en presencia de óxido de hierro en combinación con molibdeno y/o vanadio para producir formaldehído según la ecuación química : [40]
- 2CH3OH + O2 → 2CH2O + 2H2O
El catalizador a base de plata suele funcionar a una temperatura más alta, de unos 650 °C. En él se producen simultáneamente dos reacciones químicas que producen formaldehído: la que se muestra arriba y la reacción de deshidrogenación :
- CH3OH → CH2O + H2
En principio, el formaldehído podría generarse mediante la oxidación del metano , pero esta ruta no es industrialmente viable porque el metanol se oxida más fácilmente que el metano. [40]
Bioquímica
El formaldehído se produce a través de varias vías catalizadas por enzimas. [41] Los seres vivos, incluidos los humanos, producen formaldehído como parte de su metabolismo. El formaldehído es clave para varias funciones corporales (por ejemplo, la epigenética [25] ), pero su cantidad también debe controlarse estrictamente para evitar el envenenamiento. [42]
- La serina hidroximetiltransferasa puede descomponer la serina en formaldehído y glicina , según esta reacción: HOCH 2 CH(NH 2 )CO 2 H → CH 2 O + H 2 C(NH 2 )CO 2 H.
- Los microbios metilotróficos convierten el metanol en formaldehído y energía a través de la metanol deshidrogenasa : CH 3 OH → CH 2 O + 2e − + 2H +
- Otras rutas hacia el formaldehído incluyen desmetilaciones oxidativas , aminooxidasas sensibles a semicarbazida , dimetilglicina deshidrogenasas , peroxidasas lipídicas , oxidasas P450 y desmetilasas del grupo N -metilo. [41]
El formaldehído es catabolizado por la alcohol deshidrogenasa ADH5 y la aldehído deshidrogenasa ALDH2 . [43]
Química orgánica
El formaldehído es un componente básico en la síntesis de muchos otros compuestos de importancia industrial y especializada. Presenta la mayoría de las propiedades químicas de otros aldehídos, pero es más reactivo. [ cita requerida ]
Polimerización e hidratación
El CH 2 O monomérico es un gas y rara vez se encuentra en el laboratorio. El formaldehído acuoso, a diferencia de otros aldehídos pequeños (que necesitan condiciones específicas para oligomerizarse mediante condensación aldólica ), oligomeriza espontáneamente en un estado común. El trímero 1,3,5-trioxano , (CH 2 O) 3 , es un oligómero típico. Se han aislado muchos oligómeros cíclicos de otros tamaños. De manera similar, el formaldehído se hidrata para dar el diol geminal metanodiol , que se condensa aún más para formar oligómeros con terminación hidroxi HO(CH 2 O) n H. El polímero se llama paraformaldehído . Cuanto mayor sea la concentración de formaldehído, más se desplaza el equilibrio hacia la polimerización. Diluir con agua o aumentar la temperatura de la solución, así como agregar alcoholes (como metanol o etanol) reduce esa tendencia.
El formaldehído gaseoso se polimeriza en sitios activos en las paredes de los vasos, pero se desconoce el mecanismo de la reacción. [44] Pequeñas cantidades de cloruro de hidrógeno , trifluoruro de boro o cloruro estánnico presentes en el formaldehído gaseoso proporcionan el efecto catalítico y hacen que la polimerización sea rápida. [45]
Reticulaciónreacciones
El formaldehído forma enlaces cruzados al combinarse primero con una proteína para formar metilol , que pierde una molécula de agua para formar una base de Schiff . [46] La base de Schiff puede luego reaccionar con ADN o proteína para crear un producto reticulado. [46] Esta reacción es la base del proceso más común de fijación química .
Oxidación y reducción
El formaldehído se oxida fácilmente con el oxígeno atmosférico y se transforma en ácido fórmico . Por este motivo, el formaldehído comercial suele estar contaminado con ácido fórmico. El formaldehído se puede hidrogenar y transformar en metanol .
En la reacción de Cannizzaro , el formaldehído y la base reaccionan para producir ácido fórmico y metanol, una reacción de desproporción .
Hidroximetilación y clorometilación
El formaldehído reacciona con muchos compuestos, lo que da lugar a la hidroximetilación :
- XH + CH 2 O → X-CH 2 OH (X = R 2 N, RC(O)NR', SH).
Los derivados de hidroximetilo resultantes suelen reaccionar posteriormente. Así, las aminas dan lugar a hexahidro-1,3,5-triazinas :
- 3 RNH 2 + 3 CH 2 O → (RNCH 2 ) 3 + 3 H 2 O
De manera similar, cuando se combina con sulfuro de hidrógeno , forma tritiano : [47]
- 3CH2O + 3H2S → ( CH2S ) 3 + 3H2O
En presencia de ácidos, participa en reacciones de sustitución aromática electrófila con compuestos aromáticos dando lugar a derivados hidroximetilados:
- ArH + CH2O → ArCH2OH
Cuando se lleva a cabo en presencia de cloruro de hidrógeno, el producto es el compuesto clorometilado, como se describe en la clorometilación de Blanc . Si el areno es rico en electrones, como en los fenoles, se producen condensaciones elaboradas. Con fenoles 4-sustituidos se obtienen calixarenos . [48] El fenol da lugar a polímeros.
Otras reacciones
Muchos aminoácidos reaccionan con el formaldehído. [41] La cisteína se convierte en tioprolina .
Usos
Aplicaciones industriales
El formaldehído es un precursor común de compuestos y materiales más complejos. En orden aproximado de consumo decreciente, los productos generados a partir del formaldehído incluyen resina de urea formaldehído , resina de melamina , resina de fenol formaldehído , plásticos de polioximetileno , 1,4-butanodiol y diisocianato de metileno difenilo . [40] La industria textil utiliza resinas a base de formaldehído como acabados para hacer que las telas sean resistentes a las arrugas. [49]

Cuando se condensa con fenol , urea o melamina , el formaldehído produce, respectivamente, resina de fenol formaldehído termoendurecible, resina de urea formaldehído y resina de melamina. Estos polímeros son adhesivos permanentes que se utilizan en madera contrachapada y alfombras . También se espuman para fabricar aislamientos o se vierten en productos moldeados. La producción de resinas de formaldehído representa más de la mitad del consumo de formaldehído.
El formaldehído también es un precursor de alcoholes polifuncionales como el pentaeritritol , que se utiliza para fabricar pinturas y explosivos . Otros derivados del formaldehído incluyen el diisocianato de metileno difenilo, un componente importante en las pinturas y espumas de poliuretano , y la hexamina , que se utiliza en resinas de fenol-formaldehído, así como en el explosivo RDX .
La condensación con acetaldehído produce pentaeritritol , una sustancia química necesaria para sintetizar PETN , un alto explosivo: [50]

Usos de nicho
Desinfectante y biocida
Una solución acuosa de formaldehído puede ser útil como desinfectante, ya que mata la mayoría de las bacterias y hongos (incluidas sus esporas). Se utiliza como aditivo en la fabricación de vacunas para inactivar toxinas y patógenos. [51] Los liberadores de formaldehído se utilizan como biocidas en productos de cuidado personal, como los cosméticos. Aunque están presentes en niveles que normalmente no se consideran nocivos, se sabe que causan dermatitis alérgica de contacto en ciertas personas sensibilizadas. [52]
Los acuaristas utilizan formaldehído como tratamiento para los parásitos Ichthyophthirius multifiliis y Cryptocaryon irritans . [53] El formaldehído es uno de los principales desinfectantes recomendados para destruir el ántrax . [54]
El formaldehído también está aprobado para su uso en la fabricación de alimentos para animales en los EE. UU. Es un agente antimicrobiano que se utiliza para mantener los alimentos para animales completos o los ingredientes de los alimentos libres de Salmonella durante hasta 21 días. [55]
Agente fijador de tejidos y embalsamador

El formaldehído conserva o fija tejidos o células. El proceso implica la reticulación de grupos amino primarios . La Unión Europea ha prohibido el uso de formaldehído como biocida (incluido el embalsamamiento ) en virtud de la Directiva sobre productos biocidas (98/8/CE) debido a sus propiedades cancerígenas. [56] [57] Los países con una fuerte tradición de embalsamar cadáveres, como Irlanda y otros países de clima más frío, han expresado su preocupación. A pesar de los informes en sentido contrario, [58] hasta septiembre de 2009 no se había tomado ninguna decisión sobre la inclusión del formaldehído en el Anexo I de la Directiva sobre productos biocidas para el tipo de producto 22 (líquidos para embalsamar y taxidermizar) [actualizar]. [59]
La reticulación basada en formaldehído se aprovecha en experimentos genómicos ChIP-on-chip o ChIP-sequencing , donde las proteínas de unión al ADN se reticulan con sus sitios de unión afines en el cromosoma y se analizan para determinar qué genes están regulados por las proteínas. El formaldehído también se utiliza como agente desnaturalizante en la electroforesis en gel de ARN , evitando que el ARN forme estructuras secundarias. Una solución de formaldehído al 4% fija muestras de tejido patológico a aproximadamente un mm por hora a temperatura ambiente.
Prueba de drogas
El formaldehído y el ácido sulfúrico 18 M (concentrado) forman el reactivo Marquis , que puede identificar alcaloides y otros compuestos.
Fotografía
En fotografía, el formaldehído se utiliza en bajas concentraciones para el estabilizador del proceso C-41 (película negativa en color) en el paso de lavado final, [60] así como en el paso de preblanqueo del proceso E-6 , para que no sea necesario en el lavado final. Debido a las mejoras en la química del acoplador de colorantes, las películas E-6 y C-41 más modernas (2006 o posteriores) no necesitan formaldehído, ya que sus colorantes ya son estables.
Seguridad
En vista de su uso generalizado, su toxicidad y su volatilidad, el formaldehído representa un peligro significativo para la salud humana. [61] [62] En 2011, el Programa Nacional de Toxicología de los EE. UU. describió al formaldehído como "conocido por ser un carcinógeno humano". [63] [64] [65]
Inhalación crónica
Es posible que sea necesario limpiar esta sección para cumplir con los estándares de calidad de Wikipedia . El problema específico es: Está demasiado dispersa entre los diferentes tipos de riesgos. Necesita una reorganización. ( Noviembre de 2023 ) |
Las preocupaciones están asociadas con la exposición crónica (a largo plazo) por inhalación, como puede suceder por la descomposición térmica o química de resinas a base de formaldehído y la producción de formaldehído resultante de la combustión de una variedad de compuestos orgánicos (por ejemplo, gases de escape). Como las resinas de formaldehído se utilizan en muchos materiales de construcción , es uno de los contaminantes del aire interior más comunes . [66] En concentraciones superiores a 0,1 ppm en el aire, el formaldehído puede irritar los ojos y las membranas mucosas . [67] El formaldehído inhalado a esta concentración puede causar dolores de cabeza, una sensación de ardor en la garganta y dificultad para respirar, y puede desencadenar o agravar los síntomas del asma. [68] [69]
Los CDC consideran que el formaldehído es un veneno sistémico. La intoxicación por formaldehído puede provocar cambios permanentes en las funciones del sistema nervioso . [70]
Un estudio canadiense de 1988 sobre casas con aislamiento de espuma de urea-formaldehído encontró que niveles de formaldehído tan bajos como 0,046 ppm estaban correlacionados positivamente con la irritación ocular y nasal. [71] Una revisión de estudios de 2009 ha demostrado una fuerte asociación entre la exposición al formaldehído y el desarrollo de asma infantil . [72]
En 1978 se propuso una teoría sobre la carcinogénesis del formaldehído. [73] En 1987, la Agencia de Protección Ambiental de los Estados Unidos (EPA) lo clasificó como un probable carcinógeno humano , y después de más estudios, la Agencia Internacional para la Investigación sobre el Cáncer (IARC) de la OMS en 1995 también lo clasificó como un probable carcinógeno humano . Información adicional y la evaluación de todos los datos conocidos llevaron a la IARC a reclasificar el formaldehído como un carcinógeno humano conocido [74] asociado con el cáncer de los senos nasales y el cáncer nasofaríngeo . [75] Los estudios de 2009 y 2010 también han demostrado una correlación positiva entre la exposición al formaldehído y el desarrollo de leucemia , particularmente leucemia mieloide . [76] [77] Los cánceres nasofaríngeos y sinonasales son relativamente raros, con una incidencia anual combinada en los Estados Unidos de < 4000 casos. [78] [79] Cada año se producen alrededor de 30.000 casos de leucemia mieloide en los Estados Unidos. [80] [81] Algunas pruebas sugieren que la exposición al formaldehído en el lugar de trabajo contribuye a los cánceres sinonasales. [82] Los profesionales expuestos al formaldehído en su ocupación, como los trabajadores de la industria funeraria y los embalsamadores , mostraron un mayor riesgo de leucemia y cáncer cerebral en comparación con la población general. [83] Otros factores son importantes para determinar el riesgo individual de desarrollar leucemia o cáncer nasofaríngeo. [82] [84] [85] En la levadura, se ha descubierto que el formaldehído perturba las vías de reparación del ADN y el ciclo celular. [86]
En el entorno residencial, la exposición al formaldehído proviene de varias vías; el formaldehído puede ser emitido por productos de madera tratada , como madera contrachapada o tableros de partículas , pero también lo producen pinturas, barnices , acabados para pisos y el tabaquismo . [87] En julio de 2016, la EPA de EE. UU. publicó una versión previa a la publicación de su norma final sobre estándares de emisión de formaldehído para productos de madera compuesta. [88] Estas nuevas reglas afectan a los fabricantes, importadores, distribuidores y minoristas de productos que contienen madera compuesta, incluidos tableros de fibra, tableros de partículas y varios productos laminados, que deben cumplir con requisitos de etiquetado y mantenimiento de registros más estrictos. [89]
| Videos externos | |
|---|---|
 | |
 ¿A dónde se han ido todos los trailers?, video de Mariel Carr (videógrafa) y Nick Shapiro (investigador), 2015, Science History Institute ¿A dónde se han ido todos los trailers?, video de Mariel Carr (videógrafa) y Nick Shapiro (investigador), 2015, Science History Institute |
La EPA de los Estados Unidos no permite más de 0,016 ppm de formaldehído en el aire en los edificios nuevos construidos para esa agencia. [90] [ verificación fallida ] Un estudio de la EPA de los Estados Unidos encontró que una casa nueva medía 0,076 ppm cuando era nueva y 0,045 ppm después de 30 días. [91] La Agencia Federal para el Manejo de Emergencias (FEMA) también ha anunciado límites en los niveles de formaldehído en los remolques comprados por esa agencia. [92] La EPA recomienda el uso de productos de madera prensada "de grado exterior" con fenol en lugar de resina de urea para limitar la exposición al formaldehído, ya que los productos de madera prensada que contienen resinas de formaldehído son a menudo una fuente importante de formaldehído en los hogares. [75]
Los ojos son los más sensibles a la exposición al formaldehído: el nivel más bajo en el que muchas personas pueden empezar a percibir el olor oscila entre 0,05 y 1 ppm. El valor máximo de concentración en el lugar de trabajo es de 0,3 ppm. [93] [ necesita citar para verificar ] En estudios en cámaras controladas, las personas empiezan a sentir irritación ocular a alrededor de 0,5 ppm; entre el 5 y el 20 por ciento informan irritación ocular a niveles de 0,5 a 1 ppm; y se produce una mayor certeza de irritación sensorial a niveles de 1 ppm y superiores. Si bien algunas agencias han utilizado un nivel tan bajo como 0,1 ppm como umbral de irritación, el panel de expertos determinó que un nivel de 0,3 ppm protegería contra casi toda irritación. De hecho, el panel de expertos determinó que un nivel de 1,0 ppm evitaría la irritación ocular (el punto final más sensible) en el 75-95% de todas las personas expuestas. [94]

Los niveles de formaldehído en los ambientes de construcción se ven afectados por una serie de factores. Estos incluyen la potencia de los productos emisores de formaldehído presentes, la relación entre el área de superficie de los materiales emisores y el volumen del espacio, factores ambientales, la antigüedad del producto, las interacciones con otros materiales y las condiciones de ventilación. El formaldehído emite desde una variedad de materiales de construcción, muebles y productos de consumo. Los tres productos que emiten las concentraciones más altas son los tableros de fibra de densidad media , los contrachapados de madera dura y los tableros de partículas. Los factores ambientales como la temperatura y la humedad relativa pueden elevar los niveles porque el formaldehído tiene una alta presión de vapor. Los niveles de formaldehído de los materiales de construcción son los más altos cuando un edificio se abre por primera vez porque los materiales tendrían menos tiempo para liberar gases. Los niveles de formaldehído disminuyen con el tiempo a medida que las fuentes se suprimen.
En los quirófanos , el formaldehído se produce como subproducto de la electrocirugía y está presente en el humo quirúrgico, exponiendo a los cirujanos y al personal sanitario a concentraciones potencialmente peligrosas. [95]
Los niveles de formaldehído en el aire se pueden muestrear y analizar de varias maneras, incluidos los impactadores, los absorbentes tratados y los monitores pasivos. [96] El Instituto Nacional de Seguridad y Salud Ocupacional (NIOSH) tiene métodos de medición numerados 2016, 2541, 3500 y 3800. [97]
En junio de 2011, la duodécima edición del Informe sobre carcinógenos (RoC) del Programa Nacional de Toxicología (NTP) cambió el estado de inclusión del formaldehído de "razonablemente previsto como carcinógeno humano" a "conocido como carcinógeno humano". [63] [64] [65] Al mismo tiempo, se convocó un comité de la Academia Nacional de Ciencias (NAS) y emitió una revisión independiente del borrador de la evaluación IRIS de la EPA de EE. UU. sobre el formaldehído, proporcionando una evaluación integral de los efectos sobre la salud y estimaciones cuantitativas de los riesgos humanos de efectos adversos. [98]
Irritación aguda y reacción alérgica.

Para la mayoría de las personas, la irritación causada por el formaldehído es temporal y reversible, aunque el formaldehído puede causar alergias y es parte de la serie estándar de pruebas de parche. En 2005-06, fue el séptimo alérgeno más frecuente en las pruebas de parche (9,0%). [99] A las personas con alergia al formaldehído también se les recomienda evitar los liberadores de formaldehído (p. ej., Quaternium-15 , imidazolidinil urea y diazolidinil urea ). [100] Las personas que sufren reacciones alérgicas al formaldehído tienden a presentar lesiones en la piel en las áreas que han tenido contacto directo con la sustancia, como el cuello o los muslos (a menudo debido al formaldehído liberado por la ropa con acabado de planchado permanente) o dermatitis en la cara (normalmente por los cosméticos). [52] El formaldehído ha sido prohibido en los cosméticos tanto en Suecia [101] como en Japón . [102]
Otras rutas
El formaldehído se encuentra en la naturaleza y es "un intermediario esencial en el metabolismo celular de los mamíferos y los seres humanos". [40] Según el American Chemistry Council , "el formaldehído se encuentra en todos los sistemas vivos, desde las plantas hasta los animales y los seres humanos. Se metaboliza rápidamente en el cuerpo, se descompone rápidamente, no es persistente y no se acumula en el cuerpo". [103]
La duodécima edición del Informe sobre carcinógenos del NTP señala que "los alimentos y el agua contienen concentraciones mensurables de formaldehído, pero la importancia de la ingestión como fuente de exposición al formaldehído para la población general es cuestionable". El formaldehído de los alimentos generalmente se presenta en forma ligada y es inestable en una solución acuosa. [65]
En los seres humanos, la ingestión de tan sólo 30 mililitros (1,0 onza líquida estadounidense) de una solución de formaldehído al 37 % puede causar la muerte. Otros síntomas asociados con la ingestión de dicha solución incluyen daño gastrointestinal (vómitos, dolor abdominal) y daño sistémico (mareos). [70] La prueba de formaldehído se realiza mediante cromatografía de gases-espectrometría de masas en sangre y/o orina . Otros métodos incluyen la detección por infrarrojos, tubos detectores de gases, etc., de los cuales la cromatografía líquida de alto rendimiento es la más sensible. [104]
Regulación
Varios artículos web [¿ como quién? ] afirman que se ha prohibido la fabricación o importación de formaldehído en la Unión Europea (UE) según la legislación REACH (Registro, Evaluación, Autorización y Restricción de Sustancias Químicas). Se trata de un error, ya que el formaldehído no figura en el Anexo I del Reglamento (CE) nº 689/2008 (reglamento sobre exportación e importación de productos químicos peligrosos), ni en una lista de prioridades para la evaluación de riesgos. Sin embargo, el formaldehído está prohibido para su uso en determinadas aplicaciones (conservantes para sistemas de refrigeración y procesamiento de líquidos, antimoho , conservantes de fluidos para trabajar metales y productos antiincrustantes) según la Directiva sobre productos biocidas. [105] [106] En la UE, la concentración máxima permitida de formaldehído en productos terminados es del 0,2%, y cualquier producto que supere el 0,05% tiene que incluir una advertencia de que el producto contiene formaldehído. [52]
En los Estados Unidos, el Congreso aprobó un proyecto de ley el 7 de julio de 2010, relativo al uso de formaldehído en madera contrachapada de madera dura , tableros de partículas y tableros de fibra de densidad media . El proyecto de ley limitaba la cantidad permitida de emisiones de formaldehído de estos productos de madera a 0,09 ppm, y exigía a las empresas que cumplieran esta norma antes de enero de 2013. [107] La norma final de la EPA de los EE. UU. especificaba emisiones máximas de "0,05 ppm de formaldehído para madera contrachapada de madera dura, 0,09 ppm de formaldehído para tableros de partículas, 0,11 ppm de formaldehído para tableros de fibra de densidad media y 0,13 ppm de formaldehído para tableros de fibra de densidad media finos". [108]
El formaldehído fue declarado una sustancia tóxica por la Ley de Protección Ambiental de Canadá de 1999. [ 109]
La FDA está proponiendo la prohibición de los relajantes capilares con formaldehído debido a preocupaciones sobre el riesgo de cáncer. [110]
Contaminante en los alimentos
En 2005, en Indonesia, y en 2007, en Vietnam, estallaron escándalos relacionados con la adición de formaldehído a los alimentos para prolongar su vida útil. En 2011, tras cuatro años de ausencia, las autoridades indonesias encontraron alimentos con formaldehído en los mercados de varias regiones del país. [111] En agosto de 2011, al menos en dos supermercados Carrefour , el Subdepartamento Central de Ganadería y Pesca de Yakarta encontró cendol que contenía 10 partes por millón de formaldehído. [112] En 2014, el propietario de dos fábricas de fideos en Bogor (Indonesia) fue arrestado por utilizar formaldehído en los fideos. Se confiscaron 50 kg de formaldehído. [113] Entre los alimentos que se sabía que estaban contaminados se encontraban los fideos, el pescado salado y el tofu. También se rumoreaba que el pollo y la cerveza estaban contaminados. En algunos lugares, como China, los fabricantes todavía utilizan formaldehído ilegalmente como conservante en alimentos, lo que expone a las personas a la ingestión de formaldehído. [114] A principios de la década de 1900, las plantas lecheras estadounidenses lo añadían con frecuencia a las botellas de leche como método de pasteurización debido a la falta de conocimiento y la preocupación [115] con respecto a la toxicidad del formaldehído. [116] [117]
En 2011, en Nakhon Ratchasima (Tailandia), camiones cargados de pollo podrido fueron tratados con formaldehído para su venta, en lo que estuvo implicada "una gran red", incluidos 11 mataderos dirigidos por una banda criminal. [118] En 2012, se encontraron 1.000 millones de rupias (casi 100.000 dólares estadounidenses) de pescado importado de Pakistán a Batam (Indonesia) mezclado con formaldehído. [119]
En Bangladesh se ha informado de la contaminación de alimentos con formalina , y en las tiendas y supermercados se venden frutas, pescados y verduras que han sido tratados con formalina para mantenerlos frescos. [120] Sin embargo, en 2015, el Parlamento de Bangladesh aprobó un proyecto de ley de control de la formalina que establece la cadena perpetua como castigo máximo, así como una multa máxima de 2.000.000 BDT pero no menos de 500.000 BDT por importar, producir o acaparar formalina sin licencia. [121]
El formaldehído fue uno de los productos químicos utilizados en la producción industrial de alimentos del siglo XIX que investigó el Dr. Harvey W. Wiley con su famoso "Escuadrón de venenos" como parte del Departamento de Agricultura de los EE. UU . Esto condujo a la Ley de Alimentos y Medicamentos Puros de 1906 , un evento histórico en la historia temprana de la regulación de los alimentos en los Estados Unidos . [122]
Véase también
- Los complejos de metales de transición de aldehídos y cetonas incluyen varios complejos de formaldehído.
- 1,3-dioxetano
- DMDM hidantoína
- Aserrín | Impactos del aserrín en la salud
- Sulfófobos
- Pegamento para madera
- Conservante de madera
Referencias
- ^ ab "Front Matter". Nomenclatura de la química orgánica: recomendaciones de la IUPAC y nombres preferidos 2013 (Libro azul) . Cambridge: The Royal Society of Chemistry . 2014. p. 908. doi :10.1039/9781849733069-FP001. ISBN 978-0-85404-182-4.
- ^ ab "SIDS Initial Assessment Report" (PDF) . Programa Internacional de Seguridad Química. Archivado desde el original (PDF) el 2019-03-28 . Consultado el 2019-04-21 .
- ^ Spence, Robert; Wild, William (1935). "114. La curva de presión de vapor del formaldehído y algunos datos relacionados". Journal of the Chemical Society (Resumen) : 506–509. doi :10.1039/jr9350000506.
- ^ "Base de datos de compuestos de PubChem; CID=712". Centro Nacional de Información Biotecnológica. Archivado desde el original el 12 de abril de 2019. Consultado el 8 de julio de 2017 .
- ^ "Acidez de los aldehídos". Chemistry Stack Exchange. Archivado desde el original el 2018-09-01 . Consultado el 2019-04-21 .
- ^ Nelson, RD Jr.; Lide, DR; Maryott, AA (1967). "Valores seleccionados de momentos dipolares eléctricos para moléculas en fase gaseosa (NSRDS-NBS10)" (PDF) . Archivado (PDF) desde el original el 8 de junio de 2018. Consultado el 21 de abril de 2019 .
- ^ Weast, Robert C., ed. (1981). Manual de química y física del CRC (62.ª edición). Boca Raton, Florida: CRC Press. pp. C–301, E–61. ISBN 0-8493-0462-8.
- ^ Manual de química y física del CRC: un libro de referencia rápida de datos químicos y físicos. William M. Haynes, David R. Lide, Thomas J. Bruno (2016-2017, 97.ª ed.). Boca Raton, Florida. 2016. ISBN 978-1-4987-5428-6. OCLC 930681942. Archivado desde el original el 4 de mayo de 2022. Consultado el 12 de abril de 2022 .
{{cite book}}: CS1 maint: falta la ubicación del editor ( enlace ) CS1 maint: otros ( enlace ) - ^ abc Registro de formaldehído en la base de datos de sustancias GESTIS del Instituto de Seguridad y Salud Ocupacional , consultado el 13 de marzo de 2020.
- ^ abc Guía de bolsillo del NIOSH sobre peligros químicos. "#0293". Instituto Nacional de Seguridad y Salud Ocupacional (NIOSH).
- ^ Guía de bolsillo del NIOSH sobre peligros químicos. "#0294". Instituto Nacional de Seguridad y Salud Ocupacional (NIOSH).
- ^ "Nombre de la sustancia: Formaldehído [USP]". ChemlDplus . Biblioteca Nacional de Medicina de EE. UU. Archivado desde el original el 18 de septiembre de 2017.
- ^ ab "Formaldehído". Concentraciones inmediatamente peligrosas para la vida o la salud (IDLH) . Instituto Nacional de Seguridad y Salud Ocupacional (NIOSH).
- ^ Humanos, Grupo de trabajo del IARC sobre la evaluación de los riesgos carcinógenos (2006). Resumen de los datos notificados y la evaluación. Agencia Internacional para la Investigación sobre el Cáncer. Archivado desde el original el 2024-02-02 . Consultado el 2023-03-06 .
- ^ ab "Formaldehído y riesgo de cáncer". 10 de junio de 2011. Archivado desde el original el 2023-09-20 . Consultado el 2023-09-21 .
- ^ Formalin, Merriam-Webster, Inc., 15 de enero de 2020, archivado desde el original el 18 de abril de 2020 , consultado el 18 de febrero de 2020
- ^ abcde Wells, AF (1984). Química inorgánica estructural (5.ª ed.). Oxford University Press. págs. 915–917, 926. ISBN 978-0-19-965763-6.
- ^ Greenwood, Norman N. ; Earnshaw, Alan (1997). Química de los elementos (2.ª ed.). Butterworth-Heinemann . p. 1291. ISBN 978-0-08-037941-8.
- ^ abcChuichi , Kato; Shigehiro, Konaka; Takao, Iijima; Masao, Kimura (1969). "Estudios de difracción de electrones de formaldehído, acetaldehído y acetona". Toro. Química. Soc. Japón. 42 (8): 2148–2158. doi : 10.1246/bcsj.42.2148 .
- ^ abcd William M. Haynes, ed. (2012). Manual de química y física del CRC (93.ª edición). CRC Press . pp. 9–39. ISBN 978-1439880500.
- ^ abcd Duncan, JL (1974). "Estructuras de equilibrio y promedio del estado fundamental del formaldehído y el etileno". Mol. Phys. 28 (5): 1177–1191. Bibcode :1974MolPh..28.1177D. doi :10.1080/00268977400102501.
- ^ ab Smith, Michael B.; March, Jerry (2007). Química orgánica avanzada de March (6.ª ed.). John Wiley & Sons. págs. 24-25, 335. ISBN 978-0-471-72091-1.
- ^ Luecken, DJ; Hutzell, WT; Strum, ML; Pouliot, GA (1 de febrero de 2012). "Fuentes regionales de formaldehído y acetaldehído atmosféricos, e implicaciones para el modelado atmosférico". Atmospheric Environment . 47 : 477–490. Bibcode :2012AtmEn..47..477L. doi :10.1016/j.atmosenv.2011.10.005. ISSN 1352-2310.
- ^ "Capítulo 5.8 Formaldehído" (PDF) . Guías de calidad del aire (2.ª ed.). Copenhague (Dinamarca): Oficina Regional de la OMS para Europa. 2001. Archivado (PDF) desde el original el 18 de febrero de 2023. Consultado el 18 de febrero de 2023 .
- ^ ab Pham, Vanha N.; Bruemmer, Kevin J.; Toh, Joel DW; Ge, Eva J.; Tenney, Logan; Ward, Carl C.; Dingler, Felix A.; Millington, Christopher L.; Garcia-Prieto, Carlos A.; Pulos-Holmes, Mia C.; Ingolia, Nicholas T.; Pontel, Lucas B.; Esteller, Manel; Patel, Ketan J.; Nomura, Daniel K.; Chang, Christopher J. (2023). "El formaldehído regula la biosíntesis de S -adenosilmetionina y el metabolismo de un carbono". Science . 382 (6670): eabp9201. Bibcode :2023Sci...382P9201P. doi :10.1126/science.abp9201. Número de modelo: PMID 37917677. Número de modelo: S2CID 264935787.
- ^ Swenberg, JA; Lu, K.; Moeller, BC; Gao, L.; Upton, PB; Nakamura, J.; Starr, TB (2011). "Aductos de ADN endógenos versus exógenos: su papel en la carcinogénesis, la epidemiología y la evaluación de riesgos". Toxicological Sciences . 120 (Supl 1): S130–S145. doi :10.1093/toxsci/kfq371. PMC 3043087 . PMID 21163908.
- ^ "El formaldehído es biodegradable y se descompone rápidamente en el aire por la luz del sol o por las bacterias del suelo o el agua" (Comunicado de prensa). Panel de formaldehído del Consejo Estadounidense de Química. 2014-01-29. Archivado desde el original el 2019-03-28 . Consultado el 2017-04-22 .
- ^ . 2019-03-28 https://web.archive.org/web/20190328010414/https://www.atsdr.cdc.gov/ToxProfiles/tp111.pdf. Archivado desde el original (PDF) el 2019-03-28 . Consultado el 2023-02-18 .
{{cite web}}: Falta o está vacío|title=( ayuda ) - ^ Zuckerman, B.; Buhl, D.; Palmer, P.; Snyder, LE (1970). "Observación de formaldehído interestelar". Astrophys. J . 160 : 485–506. Código Bibliográfico :1970ApJ...160..485Z. doi :10.1086/150449.
- ^ Mangum, Jeffrey G.; Darling, Jeremy; Menten, Karl M.; Henkel, Christian (2008). "Densitometría de formaldehído en galaxias con formación de estrellas". Astrophys. J . 673 (2): 832–46. arXiv : 0710.2115 . Código Bibliográfico :2008ApJ...673..832M. doi :10.1086/524354. S2CID 14035123.
- ^ Woon, David E. (2002). "Modelado de la química de granos de gas con cálculos de clústeres químicos cuánticos. I. Hidrogenación heterogénea de CO y H2CO en mantos de granos helados". Astrophys. J . 569 (1): 541–48. Bibcode :2002ApJ...569..541W. doi : 10.1086/339279 .
- ^ Zubritsky, Elizabeth; Neal-Jones, Nancy (11 de agosto de 2014). "RELEASE 14-038 - NASA's 3-D Study of Comets Reveals Chemical Factory at Work". NASA . Archivado desde el original el 12 de agosto de 2014. Consultado el 12 de agosto de 2014 .
- ^ Cordiner, MA; et al. (11 de agosto de 2014). "Mapeo de la liberación de volátiles en las comas internas de los cometas C/2012 F6 (Lemmon) y C/2012 S1 (ISON) utilizando el Atacama Large Millimeter/Submillimeter Array". The Astrophysical Journal . 792 (1): L2. arXiv : 1408.2458 . Código Bibliográfico :2014ApJ...792L...2C. doi :10.1088/2041-8205/792/1/L2. S2CID 26277035.
- ^ Butlerow, A (1859). Ueber einige Derivate des Jodmethylens [ Sobre algunos derivados del yoduro de metileno ]. Vol. 111. págs. 242–252. Archivado desde el original el 12 de enero de 2023. Consultado el 27 de junio de 2015 .
{{cite book}}:|work=ignorado ( ayuda ) - ^ Ver: AW Hofmann (14 de octubre de 1867) "Zur Kenntnis des Methylaldehyds" ([Contribuciones] a nuestro conocimiento del metilaldehído), Monatsbericht der Königlich Preussischen Akademie der Wissenschaften zu Berlin (Informe mensual de la Real Academia de Ciencias de Prusia en Berlín), vol. 8, páginas 665–669. Reimpreso en:
- AW Hofmann, (1868) "Zur Kenntnis des Methylaldehyds", Annalen der Chemie und Pharmacie (Anales de química y farmacia), vol. 145, núm. 3, páginas 357–361.
- AW Hofmann (1868) "Zur Kenntnis des Methylaldehyds", Journal für praktische Chemie (Revista de química práctica), vol. 103, núm. 1, páginas 246–250.
- Hofmann, AW (1869). "Beiträge zur Kenntnis des Methylaldehyds". Revista para la química práctica . 107 (1): 414–424. doi :10.1002/prac.18691070161.
- AW Hofmann (1869) "Beiträge zur Kenntnis des Methylaldehyds", Berichte der Deutschen Chemischen Gesellschaft (Informes de la Sociedad Química Alemana), vol. 2, páginas 152-159.
- ^ Read, J. (1935). Libro de texto de química orgánica . Londres: G Bell & Sons.
- ^ Hooker, Jacob M.; Schönberger, Matthias; Schieferstein, Hanno; Fowler, Joanna S. (2008). "Un método simple y rápido para la preparación de [11C]formaldehído". Angewandte Chemie International Edition . 47 (32): 5989–5992. doi :10.1002/anie.200800991. PMC 2522306. PMID 18604787 .
- ^ Wang, Chien-Tsung; Ro, Shih-Hung (10 de mayo de 2005). "Catalizadores de aerogel de sílice y óxido de hierro de nanocluster para la oxidación parcial del metanol". Catálisis Aplicada A: General . 285 (1): 196–204. doi :10.1016/j.apcata.2005.02.029. ISSN 0926-860X.
- ^ Días, Ana Paula Soares; Montemor, Fátima ; Portela, Manuel Farinha; Kiennemann, Alain (1 de febrero de 2015). "El papel del molibdeno supraestequiométrico durante la oxidación de metanol a formaldehído sobre óxidos mixtos de Mo-Fe". Revista de Catálisis Molecular A: Química . 397 : 93–98. doi :10.1016/j.molcata.2014.10.022. ISSN 1381-1169.
- ^ abcd Reuss, Günther; Disteldorf, Walter; Jugador, Armin Otto; Empuñadura, Albrecht (2000). "Formaldehído". Enciclopedia de química industrial de Ullmann . Weinheim: Wiley-VCH. doi :10.1002/14356007.a11_619. ISBN 3527306730.
- ^ abc Kamps, Jos JAG; Hopkinson, Richard J.; Schofield, Christopher J.; Claridge, Timothy DW (2019). "Cómo reacciona el formaldehído con los aminoácidos". Química de las comunicaciones . 2 . doi : 10.1038/s42004-019-0224-2 . S2CID 207913561.
- ^ Chen, J; Chen, W; Zhang, J; Zhao, H; Cui, J; Wu, J; Shi, A (27 de septiembre de 2023). "Efectos duales del formaldehído endógeno en el organismo y fármacos para su eliminación". Revista de toxicología aplicada . 44 (6): 798–817. doi :10.1002/jat.4546. PMID 37766419. S2CID 263125399.
- ^ Nakamura, Jun; Holley, Darcy W.; Kawamoto, Toshihiro; Bultman, Scott J. (diciembre de 2020). "La falla de dos enzimas principales del catabolismo del formaldehído (ADH5 y ALDH2) conduce a una letalidad sintética parcial en ratones C57BL/6". Genes and Environment . 42 (1): 21. Bibcode :2020GeneE..42...21N. doi : 10.1186/s41021-020-00160-4 . PMC 7268536 . PMID 32514323.
- ^ Boyles, James G.; Toby, Sidney (junio de 1966). "El mecanismo de la polimerización del formaldehído gaseoso". Journal of Polymer Science Part B: Polymer Letters . 4 (6): 411–415. Código Bibliográfico :1966JPoSL...4..411B. doi :10.1002/pol.1966.110040608. Archivado desde el original el 20 de abril de 2023 . Consultado el 20 de abril de 2023 .
- ^ Bevington, JC; Norrish, RGW (7 de marzo de 1951). "La polimerización catalizada de formaldehído gaseoso". Actas de la Royal Society de Londres. Serie A. Ciencias matemáticas y físicas . 205 (1083): 516–529. Código Bibliográfico : 1951RSPSA.205..516B. doi : 10.1098/rspa.1951.0046. ISSN 0080-4630. S2CID 95395629. Archivado desde el original el 25 de octubre de 2019. Consultado el 20 de abril de 2023 .
- ^ ab Hoffman EA, Frey BL, Smith LM, Auble DT (2015). "Entrecruzamiento de formaldehído: una herramienta para el estudio de complejos de cromatina". Journal of Biological Chemistry . 290 (44): 26404–26411. doi : 10.1074/jbc.R115.651679 . PMC 4646298 . PMID 26354429.
- ^ Bost, RW; Constable, EW (1936). "Sim-tritiano". Síntesis orgánicas . 16 : 81; Volúmenes recopilados , vol. 2, pág. 610.
- ^ Gutsche, CD ; Iqbal, M. (1993). "p-tert-Butylcalix[4]arene". Síntesis orgánicas; Volúmenes recopilados , vol. 8, pág. 75.
- ^ "Ficha técnica sobre formaldehído en prendas de vestir y textiles". NICNAS . Esquema nacional australiano de notificación y evaluación de productos químicos industriales. 2013-05-01. Archivado desde el original el 2019-03-19 . Consultado el 2014-11-12 .
- ^ Schurink, HBJ (1925). "Pentaeritritol". Síntesis orgánicas . 4 : 53; Volúmenes recopilados , vol. 1, pág. 425.
- ^ "Ingredientes de las vacunas - Hoja informativa". Centro para el Control y Prevención de Enfermedades. Archivado desde el original el 21 de abril de 2019. Consultado el 4 de agosto de 2018.
El formaldehído se utiliza para inactivar productos bacterianos para las vacunas toxoides (estas son vacunas que utilizan una toxina bacteriana inactiva para producir inmunidad). También se utiliza para matar virus y bacterias no deseados que podrían contaminar la vacuna durante la producción. La mayor parte del formaldehído se elimina de la vacuna antes de envasarla.
- ^ abc De Groot, Anton C; Flyvholm, Mari-Ann; Lensen, Gerda; Menné, Torkil; Coenraads, Pieter-Jan (2009). "Liberadores de formaldehído: relación con la alergia de contacto al formaldehído. Alergia de contacto al formaldehído e inventario de liberadores de formaldehído". Dermatitis de contacto . 61 (2): 63–85. doi :10.1111/j.1600-0536.2009.01582.x. hdl : 11370/c3ff7adf-9f21-4564-96e0-0b9c5d025b30 . PMID 19706047. S2CID 23404196. Archivado desde el original el 2020-03-13 . Recuperado el 8 de julio de 2019 .
- ^ Francis-Floyd, Ruth (abril de 1996). "Uso de formalina para controlar los parásitos de los peces". Instituto de Ciencias Agrícolas y Alimentarias, Universidad de Florida. Archivado desde el original el 27 de mayo de 2012.
- ^ "Desinfección, descontaminación, fumigación, incineración", Ántrax en humanos y animales. 4.ª edición , Organización Mundial de la Salud, 2008, archivado desde el original el 6 de julio de 2022 , consultado el 20 de noviembre de 2023
- ^ "§573.460 Formaldehído". Oficina de Publicaciones del Gobierno de los Estados Unidos. 19 de abril de 2019. Archivado desde el original el 5 de mayo de 2017. Consultado el 9 de julio de 2016 .
- ^ Directiva 98/8/CE del Parlamento Europeo y del Consejo, de 16 de febrero de 1998, relativa a la comercialización de biocidas Archivado el 19 de febrero de 2008 en Wayback Machine . DOUE L 123, 24.04.1998, pp. 1–63. (versión consolidada al 26 de septiembre de 2008 (PDF) Archivado el 27 de enero de 2010 en Wayback Machine )
- ^ Reglamento (CE) nº 2032/2003 de la Comisión, de 4 de noviembre de 2003, relativo a la segunda fase del programa de trabajo de diez años contemplado en el artículo 16, apartado 2, de la Directiva 98/8/CE del Parlamento Europeo y del Consejo relativa a la comercialización de biocidas y por el que se modifica el Reglamento (CE) nº 1896/2000 Archivado el 12 de junio de 2011 en Wayback Machine . DOUE L 307, 24.11.2003, págs. 1–96. (versión consolidada hasta el 4 de enero de 2007 (PDF) Archivado el 14 de junio de 2011 en Wayback Machine )
- ^ Patel, Alkesh (4 de julio de 2007). "Prohibición del formaldehído fijada para el 22 de septiembre de 2007". WebWire. Archivado desde el original el 12 de diciembre de 2018. Consultado el 19 de mayo de 2012 .
- ^ "Entrada del Sistema Europeo de Información sobre Sustancias Químicas (ESIS) para el formaldehído". Archivado desde el original el 1 de enero de 2014. Consultado el 1 de septiembre de 2009 .
- ^ "Proceso C-41 con productos químicos Kodak Flexicolor - Publicación Z-131". Kodak. Archivado desde el original el 15 de junio de 2016. Consultado el 1 de septiembre de 2009 .
- ^ "Formaldehído", Formaldehído, 2-butoxietanol y 1-terc-butoxipropan-2-ol (PDF) , IARC Monographs on the Evaluation of Carcinogenic Risks to Humans 88, Lyon, Francia: Agencia Internacional para la Investigación sobre el Cáncer, 2006, págs. 39-325, ISBN 978-92-832-1288-1, archivado (PDF) del original el 4 de marzo de 2012 , consultado el 1 de septiembre de 2009
- ^ "Formaldehído (gas)", Informe sobre carcinógenos, undécima edición Archivado el 6 de agosto de 2019 en Wayback Machine (PDF), Departamento de Salud y Servicios Humanos de los EE. UU., Servicio de Salud Pública, Programa Nacional de Toxicología, 2005
- ^ ab Harris, Gardiner (10 de junio de 2011). "El gobierno dice que dos materiales comunes presentan riesgo de cáncer". The New York Times . Archivado desde el original el 28 de marzo de 2019. Consultado el 11 de junio de 2011 .
- ^ ab Programa Nacional de Toxicología (10 de junio de 2011). «12.º informe sobre carcinógenos». Programa Nacional de Toxicología . Archivado desde el original el 8 de junio de 2011. Consultado el 11 de junio de 2011 .
- ^ abc Programa Nacional de Toxicología (10 de junio de 2011). "Informe sobre carcinógenos - Duodécima edición - 2011" (PDF) . Programa Nacional de Toxicología . Archivado desde el original el 12 de junio de 2011. Consultado el 11 de junio de 2011 .
- ^ "Contaminación del aire en interiores en California" (PDF) . Air Resources Board, California Environmental Protection Agency. Julio de 2005. págs. 65–70. Archivado desde el original (PDF) el 2019-03-01 . Consultado el 2012-05-19 .
- ^ "Formaldehído". Administración de Seguridad y Salud Ocupacional. Agosto de 2008. Archivado desde el original el 2019-04-11 . Consultado el 2009-09-01 .
- ^ "Niveles de referencia de exposición al formaldehído". Oficina de evaluación de riesgos para la salud de California. Diciembre de 2008. Archivado desde el original ( PDF ) el 23 de marzo de 2019 . Consultado el 19 de mayo de 2012 .
- ^ "Formaldehído y aire interior". Health Canada. 29 de marzo de 2012. Archivado desde el original el 23 de abril de 2019. Consultado el 23 de abril de 2019 .
- ^ ab "Formaldehído | Pautas de manejo médico | Portal de sustancias tóxicas | ATSDR". Centros para el Control y la Prevención de Enfermedades. Archivado desde el original el 2021-08-25 . Consultado el 2021-08-25 .
- ^ Broder, I; Corey, P; Brasher, P; Lipa, M; Cole, P (1991). "Exposición al formaldehído y estado de salud en los hogares". Environmental Health Perspectives . 95 : 101–4. doi :10.1289/ehp.9195101. PMC 1568408 . PMID 1821362.
- ^ McGwin, G; Lienert, J; Kennedy, JI (noviembre de 2009). "Exposición al formaldehído y asma en niños: una revisión sistemática". Environmental Health Perspectives . 118 (3): 313–7. doi :10.1289/ehp.0901143. PMC 2854756 . PMID 20064771.
- ^ Lobachev, AN (1978). "РОЛЬ МИТОХОНДРИАЛЬНЫХ ПРОЦЕССОВ В РАЗВИТИИ И СТАРЕНИИ ОРГАНИЗМА. СТ АРЕНИЕ И РАК" [Papel de los procesos mitocondriales en el desarrollo y envejecimiento del organismo. Envejecimiento y cáncer] (PDF) (en ruso). VINITI. Archivado desde el original (PDF) el 6 de junio de 2013 . Consultado el 1 de agosto de 2012 .
- ^ Grupo de trabajo del IARC sobre la evaluación de los riesgos carcinógenos para los seres humanos (2006). Monografías del IARC sobre la evaluación de los riesgos carcinógenos para los seres humanos - VOLUMEN 88 - Formaldehído, 2-butoxietanol y 1-terc-butoxipropan-2-ol (PDF) . Prensa de la OMS. ISBN 92-832-1288-6Archivado desde el original (PDF) el 12 de julio de 2018. Consultado el 23 de abril de 2019 .
- ^ ab "Formaldehído y riesgo de cáncer". Instituto Nacional del Cáncer. 10 de junio de 2011. Archivado desde el original el 23 de enero de 2019.
- ^ Zhang, Luoping; Steinmaus, Craig; Eastmond, Eastmond; Xin, Xin; Smith, Smith (marzo-junio de 2009). "Exposición al formaldehído y leucemia: un nuevo metaanálisis y mecanismos potenciales" (PDF) . Mutation Research . 681 (2–3): 150–168. Bibcode :2009MRRMR.681..150Z. doi :10.1016/j.mrrev.2008.07.002. PMID 18674636. Archivado desde el original (PDF) el 27 de marzo de 2014.
- ^ Zhang, Luoping; Freeman, Laura E. Beane; Nakamura, Jun; Hecht, Stephen S.; Vandenberg, John J.; Smith, Martyn T.; Sonawane, Babasaheb R. (2010). "Formaldehído y leucemia: epidemiología, mecanismos potenciales e implicaciones para la evaluación de riesgos". Mutagénesis ambiental y molecular . 51 (3): 181–191. Bibcode :2010EnvMM..51..181Z. doi :10.1002/em.20534. PMC 2839060 . PMID 19790261.
- ^ "Estadísticas clave para el cáncer de nasofaringe". Sociedad Estadounidense del Cáncer. Archivado desde el original el 11 de enero de 2019. Consultado el 22 de abril de 2019 .
- ^ Turner JH, Reh DD (junio de 2012). "Incidencia y supervivencia en pacientes con cáncer nasosinusal: un análisis histórico de datos poblacionales". Cabeza y cuello . 34 (6): 877–85. doi :10.1002/hed.21830. PMID 22127982. S2CID 205857872.
- ^ "Estadísticas clave para la leucemia mieloide crónica". Sociedad Estadounidense del Cáncer. Archivado desde el original el 23 de abril de 2019. Consultado el 22 de abril de 2019 .
- ^ "¿Cuáles son las estadísticas clave sobre la leucemia mieloide aguda? Estadísticas clave para la leucemia mieloide aguda (LMA)". Sociedad Estadounidense del Cáncer. Archivado desde el original el 23 de abril de 2019. Consultado el 22 de abril de 2019 .
- ^ ab "Factores de riesgo del cáncer de nasofaringe". Sociedad Estadounidense del Cáncer . 24 de septiembre de 2018. Archivado desde el original el 10 de diciembre de 2016. Consultado el 17 de septiembre de 2019 .
- ^ Butticè, Claudio (2015). "Disolventes". En Colditz, Graham A. (ed.). The SAGE Encyclopedia of Cancer and Society (Segunda edición). Thousand Oaks: SAGE Publications. págs. 1089–1091. doi :10.4135/9781483345758.n530. ISBN 9781483345734Archivado del original el 14 de octubre de 2021. Consultado el 27 de octubre de 2015 .
- ^ "Factores de riesgo de leucemia mieloide aguda (LMA)". Sociedad Estadounidense del Cáncer. 21 de agosto de 2018. Archivado desde el original el 23 de abril de 2019.
- ^ "Factores de riesgo de leucemia mieloide crónica". Sociedad Estadounidense del Cáncer. 19 de junio de 2018. Archivado desde el original el 12 de diciembre de 2018.
- ^ Ogbede, JU, Giaever, G. y Nislow, C. (2021). Un retrato de todo el genoma de los contaminantes generalizados de los fármacos. Scientific reports, 11(1), 12487. https://doi.org/10.1038/s41598-021-91792-1 Archivado el 4 de diciembre de 2021 en Wayback Machine.
- ^ Dales, R; Liu, L; Wheeler, AJ; Gilbert, NL (julio de 2008). "Calidad del aire interior residencial y salud". Revista de la Asociación Médica Canadiense . 179 (2): 147–52. doi :10.1503/cmaj.070359. PMC 2443227 . PMID 18625986.
- ^ "Estándares de emisión de formaldehído para productos de madera compuesta". EPA. 8 de julio de 2016. Archivado desde el original el 24 de diciembre de 2018. Consultado el 24 de abril de 2019 .
- ^ Passmore, Whitney; Sullivan, Michael J. (4 de agosto de 2016). "La EPA emite una norma definitiva sobre los estándares de emisión de formaldehído para productos de madera compuesta". The National Law Review . Womble Carlyle Sandridge & Rice, PLLC. Archivado desde el original el 19 de junio de 2018. Consultado el 24 de agosto de 2016 a través de Google News.
- ^ "Pruebas de calidad del aire interior, calidad del aire interior de referencia y materiales". Agencia de Protección Ambiental. Archivado desde el original el 15 de octubre de 2006.
- ^ M. Koontz, H. Rector, D. Cade, C. Wilkes y L. Niang. 1996. Residential Indoor Air Formaldehyde Testing Program: Pilot Study. Informe n.º IE-2814, preparado por GEOMET Technologies, Inc. para la Oficina de Prevención de la Contaminación y Sustancias Tóxicas de la USEPA, de conformidad con el contrato n.º 68-D3-0013 de la EPA, Washington, DC
- ^ Evans, Ben (11 de abril de 2008). "FEMA limita el formaldehído en los remolques". The Boston Globe . Archivado desde el original el 15 de junio de 2010. Consultado el 4 de septiembre de 2008 .
- ^ "Formaldehído CAS 50-00-0" (PDF) . Programa de las Naciones Unidas para el Medio Ambiente . Archivado desde el original (PDF) el 2019-03-28 . Consultado el 2019-04-25 .
- ^ Formaldehyde Epidemiology, Toxicology and Environmental Group, Inc (agosto de 2002). "Formaldehído y datos sobre sus efectos en la salud" (PDF) . Archivado desde el original (PDF) el 11 de mayo de 2011.
{{cite web}}: CS1 maint: varios nombres: lista de autores ( enlace ) - ^ Carroll, Gregory T.; Kirschman, David L. (2023). "La unidad de filtración catalítica de humo quirúrgico reduce los niveles de formaldehído en un entorno de quirófano simulado". ACS Chemical Health & Safety . 30 (1): 21–28. doi :10.1021/acs.chas.2c00071. ISSN 1871-5532. S2CID 255047115. Archivado desde el original el 2023-05-14 . Consultado el 2023-05-17 .
- ^ "Al tomar muestras de formaldehído, el medio es importante". Galson Labs. Archivado desde el original el 23 de marzo de 2011.
- ^ "Guía de bolsillo de NIOSH sobre peligros químicos: formaldehído". Instituto Nacional de Seguridad y Salud Ocupacional, CDC. 2018-11-29. Archivado desde el original el 2019-03-28.
- ^ Adenda al 12.º Informe sobre carcinógenos (PDF) Archivado el 8 de junio de 2011 en Wayback Machine . Programa Nacional de Toxicología, Departamento de Salud y Servicios Humanos de los Estados Unidos. Consultado el 13 de junio de 2011.
- ^ Zug KA, Warshaw EM, Fowler JF, Maibach HI, Belsito DL, Pratt MD, Sasseville D, Storrs FJ, Taylor JS, Mathias CG, Deleo VA, Rietschel RL, Marks J (2009). "Resultados de las pruebas de parche del Grupo de Dermatitis de Contacto de América del Norte 2005-2006". Dermatitis . 20 (3): 149–60. doi :10.2310/6620.2009.08097. PMID 19470301. S2CID 24088485.
- ^ "Alergia al formaldehído". DermNet NZ. Sociedad Dermatológica de Nueva Zelanda. 2002. Archivado desde el original el 23 de septiembre de 2018. Consultado el 25 de abril de 2019 .
- ^ "Formaldehído y conservantes que liberan formaldehído". Cosméticos seguros . Consultado el 3 de junio de 2024 .
- ^ Hayashida, Mike. "La regulación de los cosméticos en Japón" (PDF) . Archivado desde el original (PDF) el 14 de abril de 2019. Consultado el 25 de abril de 2019 .
- ^ "El formaldehído se produce de forma natural y está a nuestro alrededor" (PDF) . Archivado (PDF) del original el 20 de enero de 2022 . Consultado el 31 de diciembre de 2021 .
- ^ Ngwa, Moise (25 de octubre de 2010). «formaldehyde testing» (PDF) . Cedar Rapids Gazette . Archivado desde el original (PDF) el 25 de octubre de 2018. Consultado el 19 de mayo de 2012 .
- ^ "La Unión Europea prohíbe el formaldehído/formalina en Europa" (PDF) . Dirección General de Medio Ambiente de la Comisión Europea. 22 de junio de 2007. pp. 1–3. Archivado desde el original (PDF) el 27 de abril de 2013.
- ^ "ESIS (Sistema Europeo de Información sobre Sustancias Químicas)". Instituto de Salud y Protección del Consumidor del Centro Común de Investigación de la Comisión Europea. Febrero de 2009. Archivado desde el original el 1 de enero de 2014. Consultado el 19 de mayo de 2012 .
- ^ "S.1660 - Ley de normas sobre formaldehído para productos de madera compuesta". GovTrack . 25 de agosto de 2010. Archivado desde el original el 29 de abril de 2019.
- ^ "Estándares de emisión de formaldehído para productos de madera compuesta". Regulations.gov . Registro Federal de los Estados Unidos. 12 de diciembre de 2016. Archivado desde el original el 10 de agosto de 2019 . Consultado el 21 de diciembre de 2019 .
Los estándares de emisión serán 0,05 ppm de formaldehído para madera contrachapada de madera dura, 0,09 ppm de formaldehído para tableros de partículas, 0,11 ppm de formaldehído para tableros de fibra de densidad media y 0,13 ppm de formaldehído para tableros de fibra de densidad media delgados.
- ^ "Health Canada - Propuesta de directrices para la calidad del aire en interiores residenciales en relación con el formaldehído". Health Canada. Abril de 2007. Archivado desde el original el 30 de mayo de 2013.
- ^ "Ver regla". www.reginfo.gov . Archivado desde el original el 20 de octubre de 2023 . Consultado el 21 de octubre de 2023 .
- ^ "Los alimentos contaminados con formaldehído vuelven a aparecer en los mercados de Indonesia". antaranews.com . 2011-08-10. Archivado desde el original el 2018-10-25.
- ^ "Encuentran bebidas de arroz contaminadas con formaldehído en supermercados Carrefour". Jakarta Globe . 22 de agosto de 2011. Archivado desde el original el 28 de septiembre de 2012.
- ^ "BPOM descubre dos fábricas de fideos contaminadas con formaldehído en Bogor". Jakarta Globe . 12 de octubre de 2014. Archivado desde el original el 1 de agosto de 2015.
- ^
- Tang, Xiaojiang; Bai, Yang; Duong, Anh; Smith, Martyn T.; Li, Laiyu; Zhang, Luoping (2009). "Formaldehído en China: producción, consumo, niveles de exposición y efectos sobre la salud". Environment International . 35 (8): 1210–1224. Bibcode :2009EnInt..35.1210T. doi :10.1016/j.envint.2009.06.002. ISSN 0160-4120. PMID 19589601.
- Ver referencias citadas en la pág. 1216 supra.
- "El municipio se pone rojo por el mal manejo de la sangre". China Daily . 18 de marzo de 2011. Archivado desde el original el 24 de octubre de 2018.
- ^ Blum, Deborah, 1954- (2018-09-25). El escuadrón antienvenenamiento: la cruzada decidida de un químico por la seguridad alimentaria a principios del siglo XX . Go Big Read (Programa). Nueva York, Nueva York. ISBN 9781594205149.OCLC 1024107182 .
{{cite book}}: CS1 maint: location missing publisher (link) CS1 maint: multiple names: authors list (link) CS1 maint: numeric names: authors list (link) - ^ "¿Había muerte en la leche?". The Indianapolis News . 31 de julio de 1900. pág. 5. Archivado desde el original el 17 de noviembre de 2018. Consultado el 20 de agosto de 2014 a través de Newspapers.com.

- ^ "Quiere que se promulgue una nueva ley. El inspector de alimentos Farnsworth quiere que se detenga el uso de formaldehído en la leche". The Topeka Daily Capital . 1903-08-30. p. 8. Archivado desde el original el 2018-11-17 . Consultado el 20 de agosto de 2014 – vía Newspapers.com.

- ^ "Negocio ilegal 'gestionado por una pandilla'". The Nation . 16 de junio de 2011. Archivado desde el original el 16 de junio de 2011.
- ^ "Frustrada en Batam la importación de pescado con formaldehído procedente de Pakistán". The Jakarta Post . 23 de febrero de 2012. Archivado desde el original el 16 de diciembre de 2018.
- ^ "Multan a comerciante por vender pescado tratado con formalina". The Daily Star . 31 de agosto de 2009. Archivado desde el original el 29 de abril de 2019.
- ^ "Se aprobó el proyecto de ley de control de formalina de 2015". ntv online . 2015-02-16. Archivado desde el original el 2018-03-23 . Consultado el 2015-03-04 .
- ^ Meadows, Michelle (enero de 2006). "Un siglo garantizando la seguridad de los alimentos y los cosméticos" (PDF) . FDA Consumer . 40 (1): 6–13. PMID 16528821.
Notas
- ^ El formaldehído está clasificado como carcinógeno, según la Agencia de Protección Ambiental , la Agencia Internacional para la Investigación sobre el Cáncer (IARC) y el Programa Nacional de Toxicología de EE. UU. [15]
Enlaces externos
- Ficha internacional de seguridad química 0275 ( gas )
- Ficha internacional de seguridad química 0695 ( solución )
- Guía de bolsillo del NIOSH sobre peligros químicos. "#0293". Instituto Nacional de Seguridad y Salud Ocupacional (NIOSH).
- Entrada de "formaldehído" en el Inventario Nacional de Contaminantes de Australia
- Formaldehído de ChemSub Online
- Guía de prevención: Formaldehído en el lugar de trabajo (PDF) del IRSST
- Formaldehído del Instituto Nacional de Seguridad y Salud Ocupacional
- Guía de salud y seguridad del IPCS n.° 57: Formaldehído
- Criterios de salud ambiental del IPCS 89: Formaldehído
- Informe de evaluación inicial de los pequeños Estados insulares en desarrollo sobre formaldehído de la Organización para la Cooperación y el Desarrollo Económicos (OCDE)
- "El formaldehído se añade a la lista de 'carcinógenos conocidos' a pesar del lobby de la industria química"—informe en video de Democracy Now!
- ¿Tiene un remolque FEMA posterior al huracán Katrina? Verifique su número de VIN
- Entonces estás viviendo en uno de los remolques Katrina de FEMA... ¿Qué puedes hacer?
- El formaldehído en la base de datos de propiedades de los pesticidas (PPDB)