Mielina
| Mielina | |
|---|---|
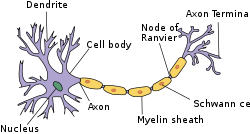 Estructura simplificada de una neurona en el SNP | |
 Neurona con oligodendrocito y vaina de mielina en el SNC | |
| Detalles | |
| Sistema | Sistema nervioso |
| Identificadores | |
| FMA | 62977 |
| Terminología anatómica [editar en Wikidata] | |
La mielina ( / ˈm aɪ . ə l ɪ n / MY -ə-lin ) es un material rico en lípidos que rodea los axones de las células nerviosas (los cables eléctricos del sistema nervioso) para aislarlos y aumentar la velocidad a la que los impulsos eléctricos (llamados potenciales de acción ) pasan a lo largo del axón. [1] [2] El axón mielinizado puede compararse con un cable eléctrico (el axón) con material aislante (mielina) a su alrededor. Sin embargo, a diferencia de la cubierta plástica de un cable eléctrico, la mielina no forma una única vaina larga en toda la longitud del axón. En cambio, la mielina envuelve el axón segmentariamente: en general, cada axón está envuelto en múltiples vainas largas con espacios cortos entre ellas, llamadas nódulos de Ranvier . En los nódulos de Ranvier, que tienen aproximadamente una milésima de mm de longitud, la membrana del axón está desnuda de mielina.
La función más conocida de la mielina es aumentar la velocidad a la que la información, codificada como cargas eléctricas, pasa a lo largo del axón. La mielina logra esto al provocar la conducción saltatoria . [1] La conducción saltatoria se refiere al hecho de que los impulsos eléctricos "saltan" a lo largo del axón, sobre largas vainas de mielina, de un nódulo de Ranvier al siguiente. Por lo tanto, la información se transmite alrededor de 100 veces más rápido a lo largo de un axón mielinizado que de uno no mielinizado.
A nivel molecular, la vaina de mielina aumenta la distancia entre los iones extracelulares e intracelulares, reduciendo la acumulación de cargas eléctricas. La estructura discontinua de la vaina de mielina da como resultado que el potencial de acción "salte" de un nódulo de Ranvier a lo largo de un tramo mielinizado largo (c. 0,1 mm – >1 mm, o 100–1000 micrones) del axón llamado segmento internodal o "entrenudo", antes de "recargarse" en el siguiente nódulo de Ranvier. Este "salto" continúa hasta que el potencial de acción alcanza la terminal del axón . [3] [4] [5] Una vez allí, la señal eléctrica provoca la liberación de neurotransmisores químicos a través de la sinapsis , que se unen a los receptores en la célula postsináptica (p. ej., otra neurona, miocito o célula secretora ).
La mielina está formada por células gliales , que son células no neuronales que proporcionan soporte nutricional y homeostático a los axones. Esto se debe a que los axones, al ser estructuras alargadas, están demasiado lejos del soma para ser sostenidos por las propias neuronas. En el sistema nervioso central ( cerebro , médula espinal y nervios ópticos ), la mielinización está formada por células gliales especializadas llamadas oligodendrocitos , cada una de las cuales envía prolongaciones (extensiones similares a extremidades desde el cuerpo celular) para mielinizar múltiples axones cercanos; mientras que en el sistema nervioso periférico , la mielina está formada por neurolemmocitos ( células de Schwann ), que solo mielinizan una sección de un axón. En el SNC, los axones transportan señales eléctricas de un cuerpo celular nervioso a otro. [6] [7] La función "aislante" de la mielina es esencial para la función motora eficiente (es decir, el movimiento como caminar), la función sensorial (por ejemplo, la vista , la audición , el olfato , la sensación del tacto o el dolor ) y la cognición (por ejemplo, la adquisición y el recuerdo de conocimientos), como lo demuestra la consecuencia de los trastornos que afectan la mielinización, como las leucodistrofias determinadas genéticamente ; [8] el trastorno desmielinizante inflamatorio adquirido , la esclerosis múltiple ; [9] y las neuropatías periféricas desmielinizantes inflamatorias . [10] Debido a su alta prevalencia, la esclerosis múltiple, que afecta específicamente al sistema nervioso central (cerebro, médula espinal y nervio óptico), es el trastorno más conocido de la mielina.
Desarrollo
El proceso de generación de mielina se denomina mielinización o mielinogénesis . En el SNC, las células progenitoras de oligodendrocitos (OPC) se diferencian en oligodendrocitos maduros, que forman la mielina. En los seres humanos, la mielinización comienza a principios del tercer trimestre, [11] aunque solo hay poca mielina presente en el SNC o el SNP en el momento del nacimiento. Durante la infancia, la mielinización progresa rápidamente, con un número cada vez mayor de axones que adquieren vainas de mielina. Esto se corresponde con el desarrollo de las habilidades cognitivas y motoras, incluida la comprensión del lenguaje, la adquisición del habla , el gateo y la marcha. La mielinización continúa durante la adolescencia y la adultez temprana y, aunque en gran parte se completa en este momento, se pueden agregar vainas de mielina en regiones de materia gris como la corteza cerebral , a lo largo de la vida. [12] [13] [14]
Distribución de especies
Vertebrados
La mielina se considera una característica definitoria de los vertebrados con mandíbulas ( gnatóstomos ), aunque los axones están envueltos por un tipo de células, llamadas células gliales, en los invertebrados. [15] [16] Estas envolturas gliales son bastante diferentes de la mielina compacta de los vertebrados, formada, como se indicó anteriormente, por la envoltura concéntrica del proceso de células mielinizantes varias veces alrededor del axón. La mielina fue descrita por primera vez en 1854 por Rudolf Virchow , [17] aunque fue más de un siglo después, tras el desarrollo de la microscopía electrónica, que su origen en las células gliales y su ultraestructura se hicieron evidentes. [18]
En los vertebrados, no todos los axones están mielinizados. Por ejemplo, en el SNP, una gran proporción de axones no están mielinizados. En cambio, están envueltos por células de Schwann no mielinizadas conocidas como células madre de Remak y dispuestas en haces de Remak . [19] En el SNC, los axones no mielinizados (o axones intermitentemente mielinizados, es decir, axones con largas regiones no mielinizadas entre segmentos mielinizados) se entremezclan con los mielinizados y están entrelazados, al menos parcialmente, por los procesos de otro tipo de célula glial , el astrocito . [ cita requerida ] [20]
Invertebrados
Se encuentran vainas similares a la mielina funcionalmente equivalentes en varios taxones de invertebrados, incluidos los anélidos oligoquetos y los taxones de crustáceos como los peneidos , los palemónidos y los calanoides . Estas vainas similares a la mielina comparten varias características estructurales con las vainas que se encuentran en los vertebrados, incluidas la multiplicidad de membranas, la condensación de la membrana y los nódulos. [15] Sin embargo, los nódulos en los vertebrados son anulares; es decir, rodean el axón. Por el contrario, los nódulos que se encuentran en las vainas de los invertebrados son anulares o fenestrados; es decir, están restringidos a "puntos". La velocidad de conducción más rápida registrada (tanto en vertebrados como en invertebrados) se encuentra en los axones envainados del camarón Kuruma , un invertebrado, [15] oscilando entre 90 y 200 m/s [16] ( cf. 100–120 m/s para el axón mielinizado más rápido de los vertebrados).
Composición


- Axón
- Núcleo de la célula de Schwann
- Célula de Schwann
- Vaina de mielina
- Neurilema
La mielina del SNC difiere ligeramente en composición y configuración de la mielina del SNP, pero ambas realizan la misma función "aislante" (ver arriba). Al ser rica en lípidos, la mielina parece blanca, de ahí el nombre dado a la " materia blanca " del SNC. Tanto los tractos de materia blanca del SNC (por ejemplo, el nervio óptico , el tracto corticoespinal y el cuerpo calloso ) como los nervios del SNP (por ejemplo, el nervio ciático y el nervio auditivo , que también aparecen blancos) comprenden cada uno de miles a millones de axones, en gran parte alineados en paralelo. Los vasos sanguíneos proporcionan la ruta para que el oxígeno y los sustratos energéticos como la glucosa lleguen a estos tractos de fibras, que también contienen otros tipos de células, incluidos astrocitos y microglia en el SNC y macrófagos en el SNP.
En términos de masa total, la mielina comprende aproximadamente un 40% de agua; la masa seca comprende entre un 60% y un 75% de lípidos y entre un 15% y un 25% de proteínas . El contenido proteico incluye la proteína básica de mielina (MBP), [21] que es abundante en el SNC donde desempeña un papel crítico y no redundante en la formación de mielina compacta; la glucoproteína de oligodendrocitos de mielina (MOG), [22] que es específica del SNC; y la proteína proteolipídica (PLP), [23] que es la proteína más abundante en la mielina del SNC, pero solo un componente menor de la mielina del SNP. En el SNP, la proteína cero de mielina (MPZ o P0) tiene un papel similar al de la PLP en el SNC, ya que participa en mantener unidas las múltiples capas concéntricas de la membrana de las células gliales que constituyen la vaina de mielina. El lípido primario de la mielina es un glucolípido llamado galactocerebrósido . Las cadenas de hidrocarburos entrelazadas de la esfingomielina fortalecen la vaina de mielina. El colesterol es un componente lipídico esencial de la mielina, sin el cual la mielina no se forma. [24]
Función

El objetivo principal de la mielina es aumentar la velocidad a la que los impulsos eléctricos (conocidos como potenciales de acción ) se propagan a lo largo de la fibra mielinizada. En las fibras amielínicas, los potenciales de acción viajan como ondas continuas, pero, en las fibras mielinizadas, "saltan" o se propagan por conducción saltatoria . Esta última es notablemente más rápida que la primera, al menos para los axones de un cierto diámetro. La mielina disminuye la capacitancia y aumenta la resistencia eléctrica a través de la membrana axonal (el axolema ). Se ha sugerido que la mielina permite un mayor tamaño corporal al mantener una comunicación ágil entre partes corporales distantes. [15]
Las fibras mielinizadas carecen de canales de sodio dependientes de voltaje a lo largo de los entrenudos mielinizados, exponiéndolos solo en los nódulos de Ranvier . Aquí, son muy abundantes y densamente empaquetados. [25] Los iones de sodio cargados positivamente pueden ingresar al axón a través de estos canales dependientes de voltaje, lo que lleva a la despolarización del potencial de membrana en el nódulo de Ranvier. El potencial de membrana en reposo luego se restaura rápidamente debido a los iones de potasio cargados positivamente que salen del axón a través de los canales de potasio . Los iones de sodio dentro del axón luego se difunden rápidamente a través del axoplasma ( citoplasma axonal ), al entrenudo mielinizado adyacente y finalmente al siguiente nódulo de Ranvier ( distal ), lo que desencadena la apertura de los canales de sodio dependientes de voltaje y la entrada de iones de sodio en este sitio. Aunque los iones de sodio se difunden a través del axoplasma rápidamente, la difusión es decremental por naturaleza, por lo que los nódulos de Ranvier tienen que estar (relativamente) estrechamente espaciados, para asegurar la propagación del potencial de acción. [26] El potencial de acción se "recarga" en nodos consecutivos de Ranvier a medida que el potencial de membrana axolemal se despolariza a aproximadamente +35 mV. [25] A lo largo del entrenudo mielinizado, las bombas de sodio/potasio dependientes de energía bombean los iones de sodio fuera del axón y los iones de potasio dentro del axón para restablecer el equilibrio de iones entre los fluidos intracelulares (dentro de la célula, es decir, el axón en este caso) y extracelulares (fuera de la célula).
Si bien el papel de la mielina como "aislante axonal" está bien establecido, otras funciones de las células mielinizantes son menos conocidas o se establecieron recientemente. La célula mielinizante "esculpe" el axón subyacente al promover la fosforilación de neurofilamentos , lo que aumenta el diámetro o el grosor del axón en las regiones internodales; ayuda a agrupar moléculas en el axolema (como los canales de sodio dependientes del voltaje) en el nódulo de Ranvier; [27] y modula el transporte de estructuras citoesqueléticas y orgánulos como las mitocondrias , a lo largo del axón. [28] En 2012, salió a la luz evidencia que apoya el papel de la célula mielinizante en la "alimentación" del axón. [29] [30] En otras palabras, la célula mielinizante parece actuar como una "estación de combustible" local para el axón, que utiliza una gran cantidad de energía para restablecer el equilibrio normal de iones entre él y su entorno, [31] [32] después de la generación de potenciales de acción.
Cuando se corta una fibra periférica, la vaina de mielina proporciona una vía a lo largo de la cual puede producirse el recrecimiento. Sin embargo, la capa de mielina no garantiza una regeneración perfecta de la fibra nerviosa. Algunas fibras nerviosas regeneradas no encuentran las fibras musculares correctas y algunas neuronas motoras dañadas del sistema nervioso periférico mueren sin recrecimiento. El daño a la vaina de mielina y a la fibra nerviosa a menudo se asocia con un aumento de la insuficiencia funcional.
Las fibras amielínicas y los axones mielinizados del sistema nervioso central de los mamíferos no se regeneran. [33]
Importancia clínica
Desmielinización
La desmielinización es la pérdida de la vaina de mielina que aísla los nervios y es el sello distintivo de algunas enfermedades autoinmunes neurodegenerativas , entre ellas la esclerosis múltiple , la encefalomielitis diseminada aguda , la neuromielitis óptica , la mielitis transversa , la polineuropatía desmielinizante inflamatoria crónica , el síndrome de Guillain-Barré , la mielinosis pontina central , las enfermedades desmielinizantes hereditarias como la leucodistrofia y la enfermedad de Charcot-Marie-Tooth . Las personas con anemia perniciosa también pueden desarrollar daño nervioso si la afección no se diagnostica rápidamente. La degeneración combinada subaguda de la médula espinal secundaria a la anemia perniciosa puede provocar desde un daño leve de los nervios periféricos hasta un daño grave del sistema nervioso central, afectando el habla, el equilibrio y la conciencia cognitiva . Cuando la mielina se degrada, la conducción de señales a lo largo del nervio puede verse afectada o perderse, y el nervio finalmente se marchita. [ aclaración necesaria ] Un caso más grave de deterioro de la mielina se llama enfermedad de Canavan .
El sistema inmunológico puede desempeñar un papel en la desmielinización asociada con dichas enfermedades, incluida la inflamación que causa desmielinización por sobreproducción de citocinas a través de la regulación positiva del factor de necrosis tumoral [34] o interferón . La resonancia magnética muestra que el éster etílico del ácido docosahexaenoico (DHA) mejora la mielinización en los trastornos peroxisomales generalizados. [35]
Síntomas
La desmielinización produce diversos síntomas que dependen de las funciones de las neuronas afectadas. Altera las señales entre el cerebro y otras partes del cuerpo; los síntomas difieren de un paciente a otro y tienen diferentes presentaciones en la observación clínica y en los estudios de laboratorio.
Los síntomas típicos incluyen visión borrosa en el campo visual central que afecta solo a un ojo, puede ir acompañada de dolor al mover los ojos, visión doble, pérdida de visión/audición, sensación extraña en piernas, brazos, pecho o cara, como hormigueo o entumecimiento ( neuropatía ), debilidad en brazos o piernas, alteración cognitiva, incluyendo deterioro del habla y pérdida de memoria, sensibilidad al calor (los síntomas empeoran o reaparecen con la exposición al calor, como una ducha caliente), pérdida de destreza, dificultad para coordinar el movimiento o trastorno del equilibrio, dificultad para controlar los movimientos intestinales o la micción, fatiga y tinnitus. [36]
Reparación de mielina
La investigación para reparar las vainas de mielina dañadas está en curso. Las técnicas incluyen la implantación quirúrgica de células precursoras de oligodendrocitos en el sistema nervioso central y la inducción de la reparación de la mielina con ciertos anticuerpos . Si bien los resultados en ratones han sido alentadores (a través del trasplante de células madre ), aún se desconoce si esta técnica puede ser efectiva para reemplazar la pérdida de mielina en humanos. [37] Los tratamientos colinérgicos , como los inhibidores de la acetilcolinesterasa (AChEI), pueden tener efectos beneficiosos sobre la mielinización, la reparación de la mielina y la integridad de la mielina. El aumento de la estimulación colinérgica también puede actuar a través de efectos tróficos sutiles en los procesos de desarrollo cerebral y, en particular, en los oligodendrocitos y el proceso de mielinización de por vida que apoyan. El aumento de la estimulación colinérgica de los oligodendrocitos , los AChEI y otros tratamientos colinérgicos, como la nicotina , posiblemente podrían promover la mielinización durante el desarrollo y la reparación de la mielina en la vejez. [38] Se ha descubierto que los inhibidores de la glucógeno sintasa quinasa 3β, como el cloruro de litio , promueven la mielinización en ratones con nervios faciales dañados. [39] El colesterol es un nutriente necesario para la vaina de mielina, junto con la vitamina B12 . [40] [41]
Desmielinización
La dismielinización se caracteriza por una estructura y función defectuosas de las vainas de mielina; a diferencia de la desmielinización, no produce lesiones . Estas vainas defectuosas a menudo surgen de mutaciones genéticas que afectan la biosíntesis y la formación de mielina. El ratón Shiverer representa un modelo animal de dismielinización. Las enfermedades humanas en las que se ha implicado la dismielinización incluyen leucodistrofias ( enfermedad de Pelizaeus-Merzbacher , enfermedad de Canavan , fenilcetonuria ) y esquizofrenia . [42] [43] [44]
Véase también
- Desmielinizaciones lesionales del sistema nervioso central
- Glicoproteína asociada a la mielina
- Incisión de mielina
- Proyecto Mielina , proyecto para regenerar la mielina
- Myelin Repair Foundation , una fundación de investigación médica sin fines de lucro para el descubrimiento de fármacos para la esclerosis múltiple .
- Mielinoide , un modelo in vitro para estudiar la mielinización humana y las enfermedades de la sustancia blanca
Referencias
- ^ ab Bean, Bruce P. (junio de 2007). "El potencial de acción en las neuronas centrales de los mamíferos". Nature Reviews Neuroscience . 8 (6): 451–65. doi :10.1038/nrn2148. ISSN 1471-0048. PMID 17514198. S2CID 205503852.
- ^ Morell, Pierre; Quarles, Richard H. (1999). "La vaina de mielina". Neuroquímica básica: aspectos moleculares, celulares y médicos. 6.ª edición . Lippincott-Raven . Consultado el 15 de diciembre de 2023 .
- ^ Carroll, SL (2017). "Las estructuras moleculares y morfológicas que hacen posible la conducción saltatoria en el nervio periférico". Revista de neuropatología y neurología experimental . 76 (4): 255–57. doi : 10.1093/jnen/nlx013 . PMID 28340093.
- ^ Keizer J, Smith GD, Ponce-Dawson S, Pearson JE (agosto de 1998). "Propagación saltatoria de ondas de Ca2+ mediante chispas de Ca2+". Revista biofísica . 75 (2): 595–600. Código Bibliográfico :1998BpJ....75..595K. doi :10.1016/S0006-3495(98)77550-2. PMC 1299735 . PMID 9675162.
- ^ Dawson SP, Keizer J, Pearson JE (mayo de 1999). "Modelo de fuego-difusión-fuego de la dinámica de las ondas de calcio intracelular". Actas de la Academia Nacional de Ciencias de los Estados Unidos de América . 96 (11): 6060–63. Bibcode :1999PNAS...96.6060D. doi : 10.1073/pnas.96.11.6060 . PMC 26835 . PMID 10339541.
- ^ Stassart, Ruth M.; Möbius, Wiebke; Nave, Klaus-Armin; Edgar, Julia M. (2018). "La unidad axón-mielina en el desarrollo y la enfermedad degenerativa". Frontiers in Neuroscience . 12 : 467. doi : 10.3389/fnins.2018.00467 . ISSN 1662-4548. PMC 6050401 . PMID 30050403.
- ^ Stadelmann, Christine; Timmler, Sebastian; Barrantes-Freer, Alonso; Simons, Mikael (1 de julio de 2019). "Mielina en el sistema nervioso central: estructura, función y patología". Physiological Reviews . 99 (3): 1381–431. doi : 10.1152/physrev.00031.2018 . ISSN 1522-1210. PMID 31066630.
- ^ van der Knaap MS, Bugiani M (septiembre de 2017). "Leucodistrofias: un sistema de clasificación propuesto basado en cambios patológicos y mecanismos patogénicos". Acta Neuropathologica . 134 (3): 351–82. doi :10.1007/s00401-017-1739-1. PMC 5563342 . PMID 28638987.
- ^ Compston A, Coles A (octubre de 2008). "Esclerosis múltiple". Lancet . 372 (9648): 1502–17. doi :10.1016/S0140-6736(08)61620-7. PMID 18970977. S2CID 195686659.
- ^ Lewis RA (octubre de 2017). "Polineuropatía desmielinizante inflamatoria crónica". Current Opinion in Neurology . 30 (5): 508–12. doi :10.1097/WCO.0000000000000481. PMID 28763304. S2CID 4961339.
- ^ "Videos y descripciones de exámenes neurológicos pediátricos: anatomía del desarrollo". library.med.utah.edu . Consultado el 20 de agosto de 2016 .
- ^ Swire M, French-Constant C (mayo de 2018). "Ver para creer: dinámica de la mielina en el sistema nervioso central adulto". Neuron . 98 (4): 684–86. doi : 10.1016/j.neuron.2018.05.005 . PMID 29772200.
- ^ Hill RA, Li AM, Grutzendler J (mayo de 2018). "Plasticidad de la mielina cortical a lo largo de la vida y degeneración relacionada con la edad en el cerebro de mamíferos vivos". Nature Neuroscience . 21 (5): 683–95. doi :10.1038/s41593-018-0120-6. PMC 5920745 . PMID 29556031.
- ^ Hughes EG, Orthmann-Murphy JL, Langseth AJ, Bergles DE (mayo de 2018). "Remodelación de la mielina a través de la oligodendrogénesis dependiente de la experiencia en la corteza somatosensorial adulta". Nature Neuroscience . 21 (5): 696–706. doi :10.1038/s41593-018-0121-5. PMC 5920726 . PMID 29556025.
- ^ abcd Hartline DK (mayo de 2008). "¿Qué es la mielina?". Neuron Glia Biology . 4 (2): 153–63. doi :10.1017/S1740925X09990263. PMID 19737435. S2CID 33164806.
- ^ ab Salzer JL, Zalc B (octubre de 2016). "Mielination" (PDF) . Current Biology . 26 (20): R971–75. Bibcode :2016CBio...26.R971S. doi : 10.1016/j.cub.2016.07.074 . PMID 27780071.
- ^ Virchow R (1854). "Ueber das ausgebreitete Vorkommen einer dem Nervenmark analogen Substanz in den thierischen Geweben". Archiv für Pathologische Anatomie und Physiologie und für Klinische Medicin (en alemán). 6 (4): 562–72. doi :10.1007/BF02116709. S2CID 20120269.
- ^ Boullerne AI (septiembre de 2016). "La historia de la mielina". Neurología experimental . 283 (Pt B): 431–45. doi :10.1016/j.expneurol.2016.06.005. PMC 5010938 . PMID 27288241.
- ^ Monk KR, Feltri ML, Taveggia C (agosto de 2015). "Nuevos conocimientos sobre el desarrollo de las células de Schwann". Glia . 63 (8): 1376–93. doi :10.1002/glia.22852. PMC 4470834 . PMID 25921593.
- ^ Wang, Doris D.; Bordey, Angélique (11 de diciembre de 2008). "La odisea de los astrocitos". Progress in Neurobiology . 86 (4): 342–67. doi :10.1016/j.pneurobio.2008.09.015. PMC 2613184 . PMID 18948166 – vía Elsevier Science Direct.
- ^ Steinman L (mayo de 1996). "Esclerosis múltiple: un ataque inmunológico coordinado contra la mielina en el sistema nervioso central". Cell . 85 (3): 299–302. doi : 10.1016/S0092-8674(00)81107-1 . PMID 8616884. S2CID 18442078.
- ^ Mallucci G, Peruzzotti-Jametti L, Bernstock JD, Pluchino S (abril de 2015). "El papel de las células inmunes, la glía y las neuronas en la patología de la materia blanca y gris en la esclerosis múltiple". Progreso en neurobiología . 127–128: 1–22. doi :10.1016/j.pneurobio.2015.02.003. PMC 4578232 . PMID 25802011.
- ^ Greer JM, Lees MB (marzo de 2002). "Proteína proteolipídica de mielina: los primeros 50 años". The International Journal of Biochemistry & Cell Biology . 34 (3): 211–15. doi :10.1016/S1357-2725(01)00136-4. PMID 11849988.
- ^ Saher G, Brügger B, Lappe-Siefke C, Möbius W, Tozawa R, Wehr MC, Wieland F, Ishibashi S, Nave KA (abril de 2005). "Un nivel alto de colesterol es esencial para el crecimiento de la membrana de mielina". Nature Neuroscience . 8 (4): 468–75. doi :10.1038/nn1426. PMID 15793579. S2CID 9762771.
- ^ ab Saladin KS (2012). Anatomía y fisiología: la unidad de forma y función (6.ª ed.). Nueva York: McGraw-Hill.[ página necesaria ]
- ^ Raine CS (1999). "Características de la neuroglia". En Siegel GJ, Agranoff BW, Albers RW, Fisher SK, Uhler MD (eds.). Neuroquímica básica: aspectos moleculares, celulares y médicos (6.ª ed.). Filadelfia: Lippincott-Raven.
- ^ Brivio V, Faivre-Sarrailh C, Peles E, Sherman DL, Brophy PJ (abril de 2017). "El ensamblaje de los nódulos del sistema nervioso central de Ranvier en los nervios mielinizados es promovido por el citoesqueleto axonal". Current Biology . 27 (7): 1068–73. Bibcode :2017CBio...27.1068B. doi :10.1016/j.cub.2017.01.025. PMC 5387178 . PMID 28318976.
- ^ Stassart RM, Möbius W, Nave KA, Edgar JM (2018). "La unidad axón-mielina en el desarrollo y la enfermedad degenerativa". Frontiers in Neuroscience . 12 : 467. doi : 10.3389/fnins.2018.00467 . PMC 6050401 . PMID 30050403.
- ^ Fünfschilling U, Supplie LM, Mahad D, Boretius S, Saab AS, Edgar J, Brinkmann BG, Kassmann CM, Tzvetanova ID, Möbius W, Diaz F, Meijer D, Suter U, Hamprecht B, Sereda MW, Moraes CT, Frahm J, Goebbels S, Nave KA (abril de 2012). "Los oligodendrocitos glucolíticos mantienen la mielina y la integridad axonal a largo plazo". Nature . 485 (7399): 517–21. Bibcode :2012Natur.485..517F. doi :10.1038/nature11007. PMC 3613737 . PMID 22622581.
- ^ Lee Y, Morrison BM, Li Y, Lengacher S, Farah MH, Hoffman PN, Liu Y, Tsingalia A, Jin L, Zhang PW, Pellerin L, Magistretti PJ, Rothstein JD (julio de 2012). "La oligodendroglia apoya metabólicamente a los axones y contribuye a la neurodegeneración". Nature . 487 (7408): 443–48. Bibcode :2012Natur.487..443L. doi :10.1038/nature11314. PMC 3408792 . PMID 22801498.
- ^ Engl E, Attwell D (agosto de 2015). "Uso de energía no señalizadora en el cerebro". The Journal of Physiology . 593 (16): 3417–329. doi :10.1113/jphysiol.2014.282517. PMC 4560575 . PMID 25639777.
- ^ Attwell D, Laughlin SB (octubre de 2001). "Un presupuesto energético para la señalización en la materia gris del cerebro". Journal of Cerebral Blood Flow and Metabolism . 21 (10): 1133–45. doi : 10.1097/00004647-200110000-00001 . PMID 11598490.
- ^ Huebner, Eric A.; Strittmatter, Stephen M. (2009). "Regeneración axonal en los sistemas nerviosos periférico y central". Resultados y problemas en la diferenciación celular . 48 : 339–51. doi :10.1007/400_2009_19. ISBN. 978-3-642-03018-5. ISSN 0080-1844. PMC 2846285. PMID 19582408 .
- ^ Ledeen RW, Chakraborty G (marzo de 1998). "Citocinas, transducción de señales y desmielinización inflamatoria: revisión e hipótesis". Neurochemical Research . 23 (3): 277–89. doi :10.1023/A:1022493013904. PMID 9482240. S2CID 7499162.
- ^ Martinez, Manuela; Vazquez, Elida (1 de julio de 1998). "Evidencias de resonancia magnética de que el éster etílico del ácido docosahexaenoico mejora la mielinización en trastornos peroxisomales generalizados". Neurología . 51 (1): 26–32. doi :10.1212/wnl.51.1.26. PMID 9674774. S2CID 21929640.
- ^ Mayo Clinic 2007 y Estudios clínicos de la Universidad de Leicester, 2014 [ cita completa necesaria ]
- ^ Windrem MS, Nunes MC, Rashbaum WK, Schwartz TH, Goodman RA, McKhann G, Roy NS, Goldman SA (enero de 2004). "Aislamientos de células progenitoras de oligodendrocitos humanos fetales y adultos mielinizan el cerebro congénitamente desmielinizado". Nature Medicine . 10 (1): 93–97. doi :10.1038/nm974. PMID 14702638. S2CID 34822879.
- "La terapia con células madre reemplaza la mielina faltante en los cerebros de ratones". FuturePundit . 20 de enero de 2004. Archivado desde el original el 14 de junio de 2011 . Consultado el 22 de marzo de 2007 .
- ^ Bartzokis G (agosto de 2007). "Los inhibidores de la acetilcolinesterasa pueden mejorar la integridad de la mielina". Biological Psychiatry . 62 (4): 294–301. doi :10.1016/j.biopsych.2006.08.020. PMID 17070782. S2CID 2130691.
- ^ Makoukji J, Belle M, Meffre D, Stassart R, Grenier J, Shackleford G, Fledrich R, Fonte C, Branchu J, Goulard M, de Waele C, Charbonnier F, Sereda MW, Baulieu EE, Schumacher M, Bernard S, Massaad C (marzo de 2012). "El litio mejora la remielinización de los nervios periféricos". Actas de la Academia Nacional de Ciencias de los Estados Unidos de América . 109 (10): 3973–78. Bibcode :2012PNAS..109.3973M. doi : 10.1073/pnas.1121367109 . PMC 3309729 . PMID 22355115.
- ^ Petrov AM, Kasimov MR, Zefirov AL (2016). "Metabolismo del colesterol cerebral y sus defectos: vínculo con enfermedades neurodegenerativas y disfunción sináptica". Acta Naturae . 8 (1): 58–73. doi :10.32607/20758251-2016-8-1-58-73. PMC 4837572 . PMID 27099785.
- ^ Miller A, Korem M, Almog R, Galboiz Y (junio de 2005). "Vitamina B12, desmielinización, remielinización y reparación en la esclerosis múltiple". Revista de Ciencias Neurológicas . 233 (1–2): 93–97. doi :10.1016/j.jns.2005.03.009. PMID 15896807. S2CID 6269094.
- ^ Krämer-Albers EM, Gehrig-Burger K, Thiele C, Trotter J, Nave KA (noviembre de 2006). "Interacciones perturbadas de la proteína proteolipídica mutante/DM20 con el colesterol y las balsas lipídicas en la oligodendroglia: implicaciones para la desmielinización en la paraplejía espástica". The Journal of Neuroscience . 26 (45): 11743–52. doi :10.1523/JNEUROSCI.3581-06.2006. PMC 6674790 . PMID 17093095.
- ^ Matalon R, Michals-Matalon K, Surendran S, Tyring SK (2006). "Enfermedad de Canavan: estudios en ratones knock-out". N-Acetilaspartato . Avances en medicina experimental y biología. Vol. 576. págs. 77–93, discusión 361–63. doi :10.1007/0-387-30172-0_6. ISBN 978-0-387-30171-6. Número de identificación personal 16802706.
- ^ Tkachev D, Mimmack ML, Huffaker SJ, Ryan M, Bahn S (agosto de 2007). "Más evidencia de biosíntesis de mielina alterada y disfunción glutamatérgica en la esquizofrenia". The International Journal of Neuropsychopharmacology . 10 (4): 557–63. doi : 10.1017/S1461145706007334 . PMID 17291371.
Lectura adicional
- Fields, R. Douglas, "El cerebro aprende de maneras inesperadas: los neurocientíficos han descubierto un conjunto de mecanismos celulares desconocidos para crear recuerdos nuevos", Scientific American , vol. 322, núm. 3 (marzo de 2020), págs. 74-79. "La mielina, considerada durante mucho tiempo como un aislante inerte en los axones , ahora se considera que contribuye al aprendizaje al controlar la velocidad a la que las señales viajan a lo largo del cableado neuronal". (pág. 79) .
- Swire M, Ffrench-Constant C (mayo de 2018). "Ver para creer: dinámica de la mielina en el sistema nervioso central adulto". Neuron . 98 (4): 684–86. doi : 10.1016/j.neuron.2018.05.005 . PMID 29772200.
- Waxman SG (octubre de 1977). "Conducción en fibras mielinizadas, no mielinizadas y desmielinizadas". Archivos de neurología . 34 (10): 585–89. doi :10.1001/archneur.1977.00500220019003. PMID 907529.
Enlaces externos
- El libro de fuentes de información sobre EM, Mielina
- Histología H&E
- Luxol Fast Blue: método de Kluver modificado para teñir la vaina de mielina