Sistema de cristal cúbico



En cristalografía , el sistema cristalino cúbico (o isométrico ) es un sistema cristalino en el que la celda unitaria tiene forma de cubo . Esta es una de las formas más comunes y simples que se encuentran en los cristales y minerales .
Hay tres variedades principales de estos cristales:
- Cúbica primitiva (abreviada cP y llamada alternativamente cúbica simple )
- Cúbica centrada en el cuerpo (abreviada cI o bcc )
- Cúbica centrada en las caras (abreviada cF o fcc )
Nota: el término fcc se utiliza a menudo como sinónimo de la estructura cúbica compacta o ccp que se da en los metales. Sin embargo, fcc representa una red Bravais cúbica centrada en las caras, que no está necesariamente compacta cuando se coloca un motivo sobre las puntas de la red. Por ejemplo, las redes de diamante y de blenda de cinc son fcc pero no compactas. Cada una se subdivide en otras variantes que se enumeran a continuación. Aunque las celdas unitarias de estos cristales se consideran convencionalmente cubos, las celdas unitarias primitivas a menudo no lo son.
Celosías de Bravais
Los tres reticulados de Bravais en el sistema cristalino cúbico son:
| Celosía de Bravais | Cúbico primitivo | Cúbico centrado en el cuerpo | Cúbico centrado en las caras |
|---|---|---|---|
| Símbolo de Pearson | cP | yo | cF |
| Celda unitaria | 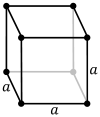 | 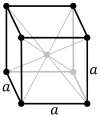 | 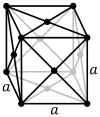 |
La red cúbica primitiva (cP) consta de un punto de red en cada esquina del cubo; esto significa que cada celda unitaria cúbica simple tiene en total un punto de red. Cada átomo en un punto de red se comparte de manera igualitaria entre ocho cubos adyacentes y, por lo tanto, la celda unitaria contiene en total un átomo ( 1 ⁄ 8 × 8). [1]
La red cúbica centrada en el cuerpo (cI) tiene un punto de red en el centro de la celda unitaria además de los ocho puntos de esquina. Tiene un total neto de dos puntos de red por celda unitaria ( 1 ⁄ 8 × 8 + 1). [1]
La red cúbica centrada en las caras (cF) tiene puntos de red en las caras del cubo, cada uno de los cuales da exactamente la mitad de la contribución, además de los puntos de red de las esquinas, lo que da un total de cuatro puntos de red por celda unitaria ( 1 ⁄ 8 × 8 de las esquinas más 1 ⁄ 2 × 6 de las caras).
La red cúbica centrada en las caras está estrechamente relacionada con el sistema hexagonal compacto (hcp), en el que dos sistemas difieren únicamente en la ubicación relativa de sus capas hexagonales. El plano [111] de una red cúbica centrada en las caras es una cuadrícula hexagonal.
Al intentar crear una red cúbica centrada en la base (es decir, colocar un punto de red adicional en el centro de cada cara horizontal), se obtiene una red de Bravais tetragonal simple .
El número de coordinación (CN) es el número de vecinos más cercanos de un átomo central en la estructura. [1] Cada esfera en una red cP tiene un número de coordinación 6, en una red cI 8 y en una red cF 12.
El factor de empaquetamiento atómico (FPA) es la fracción de volumen que ocupan los átomos. La red cP tiene un FPA de aproximadamente 0,524, la red cI un FPA de aproximadamente 0,680 y la red cF un FPA de aproximadamente 0,740.
Clases de cristales
En la siguiente tabla se enumeran los nombres de las clases de sistemas cristalinos isométricos , los grupos puntuales (en notación de Schönflies , notación de Hermann–Mauguin , orbifold y notación de Coxeter ), el tipo, los ejemplos, las tablas internacionales para el número de grupo espacial de cristalografía [2] y los grupos espaciales . Hay un total de 36 grupos espaciales cúbicos.
| No. | Grupo de puntos | Tipo | Ejemplo | Grupos espaciales | ||||||
|---|---|---|---|---|---|---|---|---|---|---|
| Nombre [3] | Hermoso. | Internacional | Orbe. | Timonel. | Primitivo | Centrado en la cara | Centrado en el cuerpo | |||
| 195–197 | Tetartoidal | yo | 23 | 332 | [3,3] + | enantiomórfico | Ullmannita , clorato de sodio | P23 | F23 | I23 |
| 198–199 | P2 1 3 | yo2 1 3 | ||||||||
| 200–204 | Diploide | El | 2/ m3 ( m3 ) | 3*2 | [3 + ,4] | centrosimétrico | Pirita | Pm3, Pn3 | Fm3 , Fd3 | Yo 3 |
| 205–206 | Pa 3 | Yo 3 | ||||||||
| 207–211 | Giroidal | Oh | 432 | 432 | [3,4] + | enantiomórfico | Petzita | P432 , P4232 | F432 , F4132 | I432 |
| 212–214 | P4 3 32, P4 1 32 | yo4132 | ||||||||
| 215–217 | Hextetraédrico | T.D. | 4 3 m | *332 | [3,3] | Esfalrita | P4 3m | F43m | Yo 4 3m | |
| 218–220 | P43n | F43c | Yo 4 3d | |||||||
| 221–230 | Hexoctaédrico | Oh | 4/m3 2 /m ( m3m ) | *432 | [3,4] | centrosimétrico | Galena , Halita | Pm3m , Pn3n , Pm3n , Pn3m | Fm3m , Fm3c , Fd3m , Fd3c | Tengo 3 meses y yo 3 días |
Otros términos para hexoctaédrico son: clase normal, holoédrico, clase central ditesseral, tipo galena .
Estructuras de un solo elemento

Como regla general, dado que los átomos en un sólido se atraen entre sí, las disposiciones de átomos más estrechamente empaquetados tienden a ser más comunes. (Sin embargo, se producen disposiciones de empaquetamiento débil, por ejemplo, si la hibridación orbital exige ciertos ángulos de enlace ). En consecuencia, la estructura cúbica primitiva, con un factor de empaquetamiento atómico especialmente bajo, es rara en la naturaleza, pero se encuentra en el polonio . [4] [5] El bcc y el fcc , con sus densidades más altas, son bastante comunes en la naturaleza. Los ejemplos de bcc incluyen hierro , cromo , tungsteno y niobio . Los ejemplos de fcc incluyen aluminio , cobre , oro y plata .
Otra estructura cristalina cúbica importante es la estructura cúbica del diamante , que puede aparecer en el carbono , el silicio , el germanio y el estaño . A diferencia de fcc y bcc, esta estructura no es una red, ya que contiene múltiples átomos en su celda primitiva . Otras estructuras elementales cúbicas incluyen la estructura A15 que se encuentra en el tungsteno y la estructura extremadamente complicada del manganeso .
Estructuras multielementos
Los compuestos que constan de más de un elemento (por ejemplo, compuestos binarios ) suelen tener estructuras cristalinas basadas en el sistema cristalino cúbico. Aquí se enumeran algunos de los más comunes. Estas estructuras pueden considerarse como dos o más subredes interpenetrantes, donde cada subred ocupa los sitios intersticiales de las otras.
Estructura del cloruro de cesio

Una de estas estructuras es la "estructura cúbica primitiva interpenetrante", también llamada "cloruro de cesio" o estructura B2. Esta estructura suele confundirse con una estructura cúbica centrada en el cuerpo porque la disposición de los átomos es la misma. Sin embargo, la estructura del cloruro de cesio tiene una base compuesta por dos especies atómicas diferentes. En una estructura cúbica centrada en el cuerpo, habría simetría traslacional a lo largo de la dirección [111]. En la estructura del cloruro de cesio, la traslación a lo largo de la dirección [111] da como resultado un cambio de especie. La estructura también puede considerarse como dos estructuras cúbicas simples separadas, una de cada especie, que se superponen una dentro de la otra. La esquina del cubo de cloruro es el centro del cubo de cesio y viceversa. [6]

Funciona de la misma manera para la estructura de NaCl que se describe en la siguiente sección. Si se eliminan los átomos de Cl, los átomos de Na restantes aún forman una estructura FCC, no una estructura cúbica simple.
En la celda unitaria del CsCl, cada ion está en el centro de un cubo de iones de tipo opuesto, por lo que el número de coordinación es ocho. El catión central está coordinado con 8 aniones en las esquinas de un cubo como se muestra y, de manera similar, el anión central está coordinado con 8 cationes en las esquinas de un cubo. Alternativamente, se podría ver esta red como una estructura cúbica simple con un átomo secundario en su vacío cúbico .
Además del cloruro de cesio en sí, la estructura también aparece en ciertos otros haluros alcalinos cuando se preparan a bajas temperaturas o altas presiones. [7] Generalmente, es más probable que esta estructura se forme a partir de dos elementos cuyos iones son aproximadamente del mismo tamaño (por ejemplo, radio iónico de Cs + = 167 pm y Cl − = 181 pm).
El grupo espacial de la estructura del cloruro de cesio (CsCl) se denomina Pm 3 m (en la notación de Hermann-Mauguin ) o "221" (en las Tablas Internacionales de Cristalografía). La designación Strukturbericht es "B2". [8]
Existen casi cien compuestos intermetálicos de tierras raras que cristalizan en la estructura CsCl, incluidos muchos compuestos binarios de tierras raras con magnesio , [9] y con elementos de los grupos 11 , 12 , [10] [11] y 13. Otros compuestos que muestran una estructura similar al cloruro de cesio son CsBr , CsI , RbCl de alta temperatura , AlCo, AgZn, BeCu, MgCe, RuAl y SrTl. [ cita requerida ]
Estructura de sal de roca

El grupo espacial de la estructura de la sal de roca o de la halita (cloruro de sodio) se denota como Fm 3 m (en la notación de Hermann-Mauguin ), o "225" (en las Tablas Internacionales de Cristalografía). La designación Strukturbericht es "B1". [12]
En la estructura de la sal de roca, cada uno de los dos tipos de átomos forma una red cúbica centrada en las caras separada, con las dos redes interpenetrándose de manera que forman un patrón de tablero de ajedrez en 3D. La estructura de la sal de roca tiene coordinación octaédrica : los vecinos más cercanos de cada átomo consisten en seis átomos del tipo opuesto, ubicados como los seis vértices de un octaedro regular . En el cloruro de sodio hay una proporción de 1:1 de átomos de sodio a cloro. La estructura también se puede describir como una red FCC de sodio con cloro ocupando cada vacío octaédrico o viceversa. [6]
Entre los ejemplos de compuestos con esta estructura se incluyen el propio cloruro de sodio, junto con casi todos los demás haluros alcalinos y "muchos óxidos de metales divalentes, sulfuros, seleniuros y telururos". [7] Según la regla de la relación de radios , es más probable que se forme esta estructura si el catión es algo más pequeño que el anión (una relación de radio catión/anión de 0,414 a 0,732).
La distancia interatómica (distancia entre catión y anión, o la mitad de la longitud de la celda unitaria a ) en algunos cristales con estructura de sal de roca son: 2,3 Å (2,3 × 10 −10 m) para NaF, [13] 2,8 Å para NaCl, [14] y 3,2 Å para SnTe. [15] La mayoría de los hidruros y haluros de metales alcalinos tienen la estructura de sal de roca, aunque algunos tienen la estructura de cloruro de cesio .
| Hidruros | Fluoruros | Cloruros | Bromuros | Yoduros | |
|---|---|---|---|---|---|
| Litio | Hidruro de litio | Fluoruro de litio [16] | Cloruro de litio | Bromuro de litio | Yoduro de litio |
| Sodio | Hidruro de sodio | Fluoruro de sodio [16] | Cloruro de sodio | Bromuro de sodio | Yoduro de sodio |
| Potasio | Hidruro de potasio | Fluoruro de potasio [16] | Cloruro de potasio | Bromuro de potasio | Yoduro de potasio |
| Rubidio | Hidruro de rubidio | Fluoruro de rubidio | Cloruro de rubidio | Bromuro de rubidio | Yoduro de rubidio |
| Cesio | Hidruro de cesio | Fluoruro de cesio | (Estructura de CsCl) | ||
| Óxidos | Sulfuros | Seleniuros | Telururos | Polónidas | |
|---|---|---|---|---|---|
| Magnesio | Óxido de magnesio | Sulfuro de magnesio | Seleniuro de magnesio [17] | Telururo de magnesio [18] | (Estructura de NiAs) |
| Calcio | Óxido de calcio | Sulfuro de calcio | Seleniuro de calcio [19] | Telururo de calcio | Polonuro de calcio [20] |
| Estroncio | Óxido de estroncio | Sulfuro de estroncio | Seleniuro de estroncio | Telururo de estroncio | Polonuro de estroncio [20] |
| Bario | Óxido de bario | Sulfuro de bario | Seleniuro de bario | Telururo de bario | Polonuro de bario [20] |
| Nitruros | Fosfuros | Arseniuros | Antimonuros | Bismuthuros | |
|---|---|---|---|---|---|
| Escandio | Nitruro de escandio | Fosfuro de escandio | Arseniuro de escandio [22] | Antimonuro de escandio [23] | Bismuthuro de escandio [24] |
| Itrio | Nitruro de itrio | Fosfuro de itrio | Arseniuro de itrio [25] | Antimonuro de itrio | Bismuthuro de itrio [26] |
| Lantano | Nitruro de lantano [27] | Fosfuro de lantano [28] | Arseniuro de lantano [25] | Antimonuro de lantano | Bismuthuro de lantano [29] |
| Cerio | Nitruro de cerio [27] | Fosfuro de cerio [28] | Arseniuro de cerio [25] | Antimonuro de cerio | Bismuthuro de cerio [29] |
| Praseodimio | Nitruro de praseodimio [27] | Fosfuro de praseodimio [28] | Arseniuro de praseodimio [25] | Antimonuro de praseodimio [30] | Bismuthuro de praseodimio [29] |
| Neodimio | Nitruro de neodimio [27] | Fosfuro de neodimio [28] | Arseniuro de neodimio [25] | Antimonuro de neodimio [30] | Bismuthuro de neodimio [29] |
| Prometeo | ? | ? | ? | ? | ? |
| Samario | Nitruro de samario [27] | Fosfuro de samario [28] | Arseniuro de samario [25] | Antimonuro de samario [30] | Bismuthuro de samario [29] |
| Europio | Nitruro de europio [27] | Fosfuro de europio | ( Estructura Na2O2 ) [ 31 ] | (inestable) [32] | |
| Gadolinio | Nitruro de gadolinio [27] | Fosfuro de gadolinio | Arseniuro de gadolinio [25] | Antimonuro de gadolinio [30] | Bismuthuro de gadolinio [29] |
| Terbio | Nitruro de terbio [27] | Fosfuro de terbio | Arseniuro de terbio [25] | Antimonuro de terbio [30] | Bismuthuro de terbio [29] |
| Disprosio | Nitruro de disprosio [27] | Fosfuro de disprosio | Arseniuro de disprosio | Antimonuro de disprosio | Bismuthuro de disprosio [29] |
| Holmio | Nitruro de holmio [27] | Fosfuro de holmio | Arseniuro de holmio [25] | Antimonuro de holmio | Bismuthuro de holmio [29] |
| Erbio | Nitruro de erbio [27] | Fosfuro de erbio | Arseniuro de erbio [25] | Antimonuro de erbio | Bismuthuro de erbio [29] |
| Tulio | Nitruro de tulio [27] | Fosfuro de tulio | Arseniuro de tulio | Antimonuro de tulio | Bismuthuro de tulio [29] |
| Iterbio | Nitruro de iterbio [27] | Fosfuro de iterbio | Arseniuro de iterbio [25] | Antimonuro de iterbio | (inestable) [33] [34] |
| Lutecio | Nitruro de lutecio [27] | Fosfuro de lutecio | Arseniuro de lutecio | Antimonuro de lutecio | Bismuthuro de lutecio |
| Actinio | ? | ? | ? | ? | ? |
| Torio | Nitruro de torio [35] | Fosfuro de torio [35] | Arseniuro de torio [35] | Antimonuro de torio [35] | (Estructura de CsCl) |
| Protactinio | ? | ? | ? | ? | ? |
| Uranio | Nitruro de uranio [35] | Monofosfuro de uranio [35] | Arseniuro de uranio [35] | Antimonuro de uranio [35] | Bismuthuro de uranio [36] |
| Neptunio | Nitruro de neptunio | Fosfuro de neptunio | Arseniuro de neptunio | Antimonuro de neptunio | Bismuthuro de neptunio [36] |
| Plutonio | Nitruro de plutonio [35] | Fosfuro de plutonio [35] | Arseniuro de plutonio [35] | Antimonuro de plutonio [35] | Bismuthuro de plutonio [36] |
| Americio | Nitruro de americio [36] | Fosfuro de americio [36] | Arseniuro de americio [36] | Antimonuro de americio [36] | Bismuthuro de americio [36] |
| Curio | Nitruro de curio [37] | Fosfuro de curio [37] | Arseniuro de curio [37] | Antimonuro de curio [37] | Bismuthuro de curio [37] |
| Berkelio | Nitruro de berkelio [37] | Fosfuro de berkelio [37] | Arseniuro de berkelio [37] | ? | Bismuthuro de berkelio [37] |
| Californio | ? | ? | Arseniuro de californio [37] | ? | Bismuthuro de californio [37] |
| Óxidos | Sulfuros | Seleniuros | Telururos | Polónidas | |
|---|---|---|---|---|---|
| Escandio | (inestable) [38] | Monosulfuro de escandio | |||
| Itrio | Monosulfuro de itrio [39] | ||||
| Lantano | Monosulfuro de lantano [40] | ||||
| Cerio | Monosulfuro de cerio [40] | Monoseleniuro de cerio [41] | Monotelururo de cerio [41] | ||
| Praseodimio | Monosulfuro de praseodimio [40] | Monoseleniuro de praseodimio [41] | Monotelururo de praseodimio [41] | ||
| Neodimio | Monosulfuro de neodimio [40] | Monoseleniuro de neodimio [41] | Monotelururo de neodimio [41] | ||
| Prometeo | ? | ? | ? | ? | |
| Samario | Monosulfuro de samario [40] | Monoseleniuro de samario | Monotelururo de samario | Monopolio de samario [42] | |
| Europio | Monóxido de europio | Monosulfuro de europio [40] | Monoseleniuro de europio [43] | Monotelururo de europio [43] | Monopolio de europio [42] |
| Gadolinio | (inestable) [38] | Monosulfuro de gadolinio [40] | |||
| Terbio | Monosulfuro de terbio [40] | Monopolio de terbio [42] | |||
| Disprosio | Monosulfuro de disprosio [40] | Monopolio de disprosio [42] | |||
| Holmio | Monosulfuro de holmio [40] | Monopolio de holmio [42] | |||
| Erbio | Monosulfuro de erbio [40] | ||||
| Tulio | Monosulfuro de tulio [40] | Monopolio de tulio [42] | |||
| Iterbio | Monóxido de iterbio | Monosulfuro de iterbio [40] | Monopolio de iterbio [42] | ||
| Lutecio | (inestable) [38] [44] | Monosulfuro de lutecio [40] | Monopolio de lutecio [42] | ||
| Actinio | ? | ? | ? | ? | |
| Torio | Monosulfuro de torio [35] | Monoseleniuro de torio [35] | (Estructura de CsCl) [45] | ||
| Protactinio | ? | ? | ? | ? | |
| Uranio | Monosulfuro de uranio [35] | Monoseleniuro de uranio [35] | Monotelururo de uranio [35] | ||
| Neptunio | Monosulfuro de neptunio | Monoseleniuro de neptunio | Monotelururo de neptunio | ||
| Plutonio | Monosulfuro de plutonio [35] | Monoseleniuro de plutonio [35] | Monotelururo de plutonio [35] | ||
| Americio | Monosulfuro de americio [36] | Monoseleniuro de americio [36] | Monotelururo de americio [36] | ||
| Curio | Monosulfuro de curio [37] | Monoseleniuro de curio [37] | Monotelururo de curio [37] |
| Carburos | Nitruros | |
|---|---|---|
| Titanio | Carburo de titanio | Nitruro de titanio |
| Circonio | Carburo de circonio | Nitruro de circonio |
| Hafnio | Carburo de hafnio | Nitruro de hafnio [46] |
| Vanadio | Carburo de vanadio | Nitruro de vanadio |
| Niobio | Carburo de niobio | Nitruro de niobio |
| Tantalio | Carburo de tantalio | (Estructura de CoSn) |
| Cromo | (inestable) [47] | Nitruro de cromo |
Muchos monóxidos de metales de transición también tienen la estructura de sal de roca ( TiO , VO , CrO , MnO , FeO , CoO , NiO , CdO ). Los primeros monocarburos actinoides también tienen esta estructura ( ThC , PaC, UC , NpC, PuC ). [37]
Estructura de fluorita
Al igual que la estructura de la sal de roca, la estructura de fluorita (AB 2 ) también es una estructura Fm 3 m pero tiene una proporción de iones de 1:2. La estructura de antifluorita es casi idéntica, excepto que las posiciones de los aniones y cationes están intercambiadas en la estructura. Se designan como posiciones de Wyckoff 4a y 8c, mientras que las posiciones de la estructura de sal de roca son 4a y 4b. [48] [49]
Estructura de la blenda de zinc

El grupo espacial de la estructura de Zincblenda se llama F 4 3m (en notación Hermann–Mauguin ), o 216. [50] [51] La designación Strukturbericht es "B3". [52]
La estructura de la blenda de cinc (también escrita "blenda de cinc") recibe su nombre del mineral blenda de cinc ( esfalrita ), una forma de sulfuro de cinc (β-ZnS). Al igual que en la estructura de sal de roca, los dos tipos de átomos forman dos redes cúbicas interpenetrantes centradas en las caras. Sin embargo, difiere de la estructura de sal de roca en cómo se posicionan las dos redes una con respecto a la otra. La estructura de la blenda de cinc tiene coordinación tetraédrica : los vecinos más cercanos de cada átomo consisten en cuatro átomos del tipo opuesto, posicionados como los cuatro vértices de un tetraedro regular . En el sulfuro de cinc, la relación de cinc a azufre es 1:1. [6] En conjunto, la disposición de los átomos en la estructura de la blenda de cinc es la misma que la estructura cúbica del diamante , pero con tipos de átomos alternados en los diferentes sitios de la red. La estructura también se puede describir como una red FCC de cinc con átomos de azufre que ocupan la mitad de los huecos tetraédricos o viceversa. [6]
Los ejemplos de compuestos con esta estructura incluyen la propia blenda de zinc, el nitrato de plomo (II) , muchos semiconductores compuestos (como el arseniuro de galio y el telururo de cadmio ) y una amplia gama de otros compuestos binarios. [ cita requerida ] Los pnictogenuros del grupo del boro suelen tener una estructura de blenda de zinc, aunque los nitruros son más comunes en la estructura de wurtzita , y sus formas de blenda de zinc son polimorfos menos conocidos . [ 53 ] [ 54 ]
| Fluoruros | Cloruros | Bromuros | Yoduros | |
|---|---|---|---|---|
| Cobre | Fluoruro de cobre (I) | Cloruro de cobre (I) | Bromuro de cobre (I) | Yoduro de cobre (I) |
| Sulfuros | Seleniuros | Telururos | Polónidas | |
|---|---|---|---|---|
| Berilio | Sulfuro de berilio | Seleniuro de berilio | Telururo de berilio | Polonuro de berilio [55] [56] |
| Zinc | Sulfuro de zinc | Seleniuro de zinc | Telururo de zinc | Polonuro de zinc |
| Cadmio | Sulfuro de cadmio | Seleniuro de cadmio | Telururo de cadmio | Polonuro de cadmio |
| Mercurio | Sulfuro de mercurio | Seleniuro de mercurio | Telururo de mercurio | – |
Este grupo también se conoce como la familia de compuestos II-VI , la mayoría de los cuales pueden prepararse tanto en forma de blenda de zinc (cúbica) como de wurtzita (hexagonal).
| Nitruros | Fosfuros | Arseniuros | Antimonuros | |
|---|---|---|---|---|
| Boro | Nitruro de boro * | Fosfuro de boro | Arseniuro de boro | Antimonuro de boro |
| Aluminio | Nitruro de aluminio * | Fosfuro de aluminio | Arseniuro de aluminio | Antimonuro de aluminio |
| Galio | Nitruro de galio * | Fosfuro de galio | Arseniuro de galio | Antimonuro de galio |
| Indio | Nitruro de indio * | Fosfuro de indio | Arseniuro de indio | Antimonuro de indio |
Este grupo también se conoce como la familia de compuestos III-V .

Estructura de Heusler
La estructura de Heusler, basada en la estructura de Cu2MnAl , es una estructura común para los compuestos ternarios que involucran metales de transición . Tiene el grupo espacial Fm3m ( No. 225), y la designación Strukturbericht es L21 . Junto con los compuestos de semi-Heusler y de Huesler inverso estrechamente relacionados, hay cientos de ejemplos.
Estructura de monosiliciuro de hierro

El grupo espacial de la estructura del monosiliciuro de hierro es P2 1 3 (n.º 198) y la designación Strukturbericht es B20. Se trata de una estructura quiral y, a veces, se asocia con propiedades helimagnéticas . Hay cuatro átomos de cada elemento, lo que hace un total de ocho átomos en la celda unitaria.
Se encuentran ejemplos de ellos entre los siliciuros y germanuros de metales de transición, así como algunos otros compuestos como el paladuro de galio .
| Siliciuros | Germánicas | |
|---|---|---|
| Manganeso | Monosiliciuro de manganeso | Germanuro de manganeso |
| Hierro | Monosiliciuro de hierro | Germanuro de hierro |
| Cobalto | Monosiliciuro de cobalto | Germanuro de cobalto |
| Cromo | Siliciuro de cromo (IV) | Germanuro de cromo (IV) |
Estructura de Weaire-Phelan

Una estructura de Weaire-Phelan tiene simetría Pm 3 n (223).
Tiene tres orientaciones de tetradecaedros apilados con celdas piritoédricas en los huecos. Se encuentra como una estructura cristalina en química, donde generalmente se la conoce como " estructura de clatrato de tipo I ". Los hidratos de gas formados por metano, propano y dióxido de carbono a bajas temperaturas tienen una estructura en la que las moléculas de agua se encuentran en los nodos de la estructura de Weaire-Phelan y están unidas por enlaces de hidrógeno , y las moléculas de gas más grandes quedan atrapadas en las jaulas poliédricas.
Véase también
- Atomium : edificio que es un modelo de una celda unitaria bcc , con cuerpo vertical en diagonal.
- Empaquetamiento compacto
- Dislocaciones
- Red recíproca
Referencias
- ^ abc De Wolff, PM; Belov, NV; Bertaut, EF; Buerger, MJ; Donnay, JDH; Fischer, W.; Hahn, Th.; Koptsik, VA; MacKay, AL; Wondratschek, H.; Wilson, AJC; Abrahams, SC (1985). "Nomenclatura para familias de cristales, tipos de red de Bravais y clases aritméticas. Informe del Comité Ad Hoc de la Unión Internacional de Cristalografía sobre la Nomenclatura de la Simetría". Acta Crystallographica Sección A . 41 (3): 278. doi : 10.1107/S0108767385000587 .
- ^ Prince, E., ed. (2006). Tablas internacionales de cristalografía . doi :10.1107/97809553602060000001. ISBN 978-1-4020-4969-9.S2CID146060934 .
- ^ Cristalografía y minerales ordenados por forma cristalina, Webmineral
- ^ Greenwood, Norman N. ; Earnshaw, Alan (1997). Química de los elementos (2.ª ed.). Butterworth-Heinemann . ISBN 978-0-08-037941-8.
- ^ El descubrimiento original fue en J. Chem. Phys. 14 , 569 (1946).
- ^ abcd "Redes cúbicas y empaquetamiento compacto". 3 de octubre de 2013. Archivado desde el original el 1 de noviembre de 2020.
- ^ ab Seitz, Teoría moderna de los sólidos (1940), pág. 49
- ^ La estructura del CsCl (B2) Archivado el 15 de septiembre de 2008 en Wayback Machine.
- ^ Saccone, A.; Delfino, S.; Macció, D.; Ferro, R. (1993). "Diagramas de fases de magnesio y tierras raras: investigación experimental del sistema Ho-Mg". Journal of Phase Equilibria . 14 (3): 280–287. doi :10.1007/bf02668225. S2CID 95011597.
- ^ Kanematu, K; T. Alfieri, G.; Banks, E. (1969). "Estudios magnéticos de compuestos de zinc de tierras raras con estructura CsCl". Revista de la Sociedad de Física de Japón . 26 (2): 244–248. Código Bibliográfico :1969JPSJ...26..244K. doi :10.1143/jpsj.26.244.
- ^ Buschow, KHJ (1974). "Propiedades magnéticas de compuestos de cadmio de tierras raras de tipo CsCl". The Journal of Chemical Physics . 61 (11): 4666–4670. Código Bibliográfico :1974JChPh..61.4666B. doi :10.1063/1.1681788.
- ^ La estructura del NaCl (B1) Archivado el 19 de octubre de 2008 en Wayback Machine.
- ^ Sundquist, JJ; Lin, CC (1981). "Estructura electrónica del centro F en un cristal de fluoruro de sodio". Journal of Physics C: Solid State Physics . 14 (32): 4797–4805. Bibcode :1981JPhC...14.4797S. doi :10.1088/0022-3719/14/32/016.
- ^ Abrahams, SC; Bernstein, JL (1965). "Precisión de un difractómetro automático. Medición de los factores estructurales del cloruro de sodio". Acta Crystallogr. 18 (5): 926–932. doi :10.1107/S0365110X65002244.
- ^ Kao, W.; Peretti, E. (1970). "El subsistema ternario Sn4As3-SnAs-SnTe". Revista de metales menos comunes . 22 : 39–50. doi :10.1016/0022-5088(70)90174-8.
- ^ abc J. Aigueperse, P. Mollard, D. Devilliers, M. Chemla, R. Faron, R. Romano, JP Cuer, "Compuestos de flúor inorgánicos" (sección 4) en Ullmann's Encyclopedia of Industrial Chemistry, Wiley-VCH, Weinheim, 2005. doi :10.1002/14356007.a11_307.
- ^ Broch, Einar (1 de junio de 1927). "Präzisionsbestimmungen der Gitterkonstanten der Verbindungen MgO, MgS, MgSe, MnO y MnSe". Zeitschrift für Physikalische Chemie (en alemán). 127U (1): 446–454. doi :10.1515/zpch-1927-12724. S2CID 100227546.
- ^ Mir, Showkat H.; Jha, Prakash C.; Dabhi, Shweta; Jha, Prafulla K. (2016). " Estudio ab initio de la estabilidad de fase, dinámica de red y propiedades termodinámicas de calcogenuros de magnesio". Química y física de materiales . 175 : 54–61. doi :10.1016/j.matchemphys.2016.02.066.
- ^ Louail, L.; Haddadi, K.; Maouche, D.; Ali Sahraoui, F.; Hachemi, A. (2008). "Estructura de banda electrónica del seleniuro de calcio bajo presión". Physica B: Condensed Matter . 403 (18): 3022–3026. Bibcode :2008PhyB..403.3022L. doi :10.1016/j.physb.2008.03.009.
- ^ abc Brown, SA; Brown, PL (2019). La química acuosa del polonio y la aplicación práctica de su termoquímica. Elsevier Science. pág. 25. ISBN 978-0-12-819309-9.
- ^ Hulliger, F. (1979). "Capítulo 33 Pnictides de tierras raras". Manual de física y química de tierras raras . Vol. 4. Elsevier. págs. 153–236. doi :10.1016/s0168-1273(79)04006-x. ISBN. 9780444852168.
- ^ Gschneidner, KA; Calderwood, FW (1986). "El sistema As−Sc (arsénico-escandio)". Boletín de diagramas de fases de aleación . 7 (4): 348–349. doi :10.1007/bf02873011.
- ^ Hayashi, J; Shirotani, I; Hirano, K; Ishimatsu, N; Shimomura, O; Kikegawa, T (2003). "Transición de fase estructural de ScSb y YSb con una estructura de tipo NaCl a altas presiones". Solid State Communications . 125 (10): 543–546. Bibcode :2003SSCom.125..543H. doi :10.1016/s0038-1098(02)00889-x.
- ^ Horovitz, CT (2012). El escandio: su aparición, química, física, metalurgia, biología y tecnología. Elsevier Science. pág. 273. ISBN 978-0-323-14451-3.
- ^ abcdefghijk Ono, S.; Despault, JG; Calvert, LD; Taylor, JB (1970). "Arsenuros de tierras raras". Revista de metales menos comunes . 22 (1): 51–59. doi :10.1016/0022-5088(70)90175-x.
- ^ Schmidt, FA; McMasters, OD; Lichtenberg, RR (1969). "El sistema de aleación de itrio-bismuto". Revista de metales menos comunes . 18 (3): 215–220. doi :10.1016/0022-5088(69)90159-3.
- ^ abcdefghijklmn Natali, F.; Ruck, BJ; Plank, NOV; Trodahl, HJ; Granville, S.; Meyer, C.; Lambrecht, WRL (2013). "Mononitruros de tierras raras". Progreso en la ciencia de los materiales . 58 (8): 1316–1360. arXiv : 1208.2410 . doi :10.1016/j.pmatsci.2013.06.002. S2CID 118566136.
- ^ abcde Ono, S.; Nomura, K.; Hayakawa, H. (1974). "Síntesis de nuevos fosfuros de tierras raras". Journal of the Less Common Metals . 38 (2–3): 119–130. doi :10.1016/0022-5088(74)90055-1.
- ^ abcdefghijk Yoshihara, K.; Taylor, JB; Calvert, LD; Despault, JG (1975). "Bismutos de tierras raras". Revista de metales menos comunes . 41 (2): 329–337. doi :10.1016/0022-5088(75)90038-7.
- ^ abcde Hayashi, J.; Shirotani, I.; Tanaka, Y.; Adachi, T.; Shimomura, O.; Kikegawa, T. (2000). "Transiciones de fase de LnSb (Ln=lantánido) con estructura de tipo NaCl a altas presiones". Solid State Communications . 114 (11): 561–565. Bibcode :2000SSCom.114..561H. doi :10.1016/s0038-1098(00)00113-7.
- ^ Gschneidner, KA; Calderwood, FW (1986). "El sistema As−Eu (arsénico-europio)". Boletín de diagramas de fases de aleación . 7 (3): 279–283. doi :10.1007/bf02869009.
- ^ Taylor, JB; Calvert, LD; Wang, Y. (1979). "Datos en polvo para algunos nuevos antimonuros y bismutos de europio". Journal of Applied Crystallography . 12 (2): 249–251. doi :10.1107/s0021889879012309.
- ^ Okamoto, H. (1999). "Bi-Yb (bismuto-iterbio)". Revista de equilibrios de fases . 20 (4): 453. doi :10.1361/105497199770335640.
- ^ Duan, Xu; Wu, Fan; Chen, Jia; Zhang, Peiran; Liu, Yang; Yuan, Huiqiu; Cao, Chao (2018). "Estructura electrónica ajustable y propiedades topológicas de LnPn (Ln=Ce, Pr, Sm, Gd, Yb; Pn=Sb, Bi)". Física de las comunicaciones . 1 (1): 71. arXiv : 1802.04554 . Código Bibliográfico :2018CmPhy...1...71D. doi : 10.1038/s42005-018-0074-8 .
- ^ abcdefghijklmnopqrst Kruger, OL; Moser, JB (1967). "Constantes de red y puntos de fusión de compuestos IVA-VIA del grupo actínido con estructuras de tipo NaCl". Revista de Física y Química de Sólidos . 28 (11): 2321–2325. Código Bibliográfico :1967JPCS...28.2321K. doi :10.1016/0022-3697(67)90257-0.
- ^ abcdefghijk Vogt, O.; Mattenberger, K. (1995). "El magnetismo de capas 4f y 5f localizadas o casi localizadas". Journal of Alloys and Compounds . 223 (2): 226–236. doi :10.1016/0925-8388(94)09005-x.
- ^ abcdefghijklmno Benedict, U.; Holzapfel, WB (1993). "Capítulo 113 Estudios de alta presión: aspectos estructurales". Lantánidos/actínidos: Física I. Manual sobre la física y la química de tierras raras. Vol. 17. Elsevier. págs. 245–300. doi :10.1016/s0168-1273(05)80030-3. ISBN 9780444815026.
- ^ abc Leger, JM; Yacoubi, N.; Loriers, J. (1981). "Síntesis de monóxidos de tierras raras". Journal of Solid State Chemistry . 36 (3): 261–270. Bibcode :1981JSSCh..36..261L. doi :10.1016/0022-4596(81)90436-9.
- ^ Roedhammer, P.; Reichardt, W.; Holtzberg, F. (1978). "Comportamiento en modo suave en la dispersión de fonones de YS". Physical Review Letters . 40 (7): 465–468. Código Bibliográfico :1978PhRvL..40..465R. doi :10.1103/physrevlett.40.465.
- ^ abcdefghijklmn Didchenko, R.; Gortsema, FP (1963). "Algunas propiedades eléctricas y magnéticas de monosulfuros y nitruros de tierras raras". Revista de Física y Química de Sólidos . 24 (7): 863–870. Código Bibliográfico :1963JPCS...24..863D. doi :10.1016/0022-3697(63)90062-3.
- ^ abcdef Smolensky, GA; Adamjan, VE; Loginov, GM (1968). "Propiedades antiferromagnéticas de monocalcogenuros de tierras raras ligeras". Revista de Física Aplicada . 39 (2): 786–790. Bibcode :1968JAP....39..786S. doi :10.1063/1.2163619.
- ^ abcdefgh Kershner, CJ; DeSando, RJ; Heidelberg, RF; Steinmeyer, RH (1966). "Polónidos de tierras raras". Revista de química inorgánica y nuclear . 28 (8): 1581–1588. doi :10.1016/0022-1902(66)80054-4.
- ^ ab Wachter, P. (1972). "Propiedades ópticas, eléctricas y magnéticas de los calcogenuros de europio y los pnictidos de tierras raras". CRC Critical Reviews in Solid State Sciences . 3 (2): 189–241. doi :10.1080/10408437208244865.
- ^ Meyer, G (1991). Síntesis de compuestos lantánidos y actínidos . Dordrecht: Springer Netherlands. p. 237. ISBN. 978-94-011-3758-4.OCLC 840310000 .
- ^ D'Eye, RWM; Sellman, PG (1954). "El sistema torio-telurio". J. Chem. Soc. : 3760–3766. doi :10.1039/jr9540003760.
- ^ Friedrich, Alexandra; Winkler, Björn; Juarez-Arellano, Erick A.; Bayarjargal, Lkhamsuren (2011). "Síntesis de nitruros, carburos y boruros de metales de transición binarios a partir de los elementos en la celda de yunque de diamante calentada por láser y sus relaciones estructura-propiedad". Materiales . 4 (10): 1648–1692. Bibcode :2011Mate....4.1648F. doi : 10.3390/ma4101648 . PMC 5448873 . PMID 28824101.
- ^ Venkatraman, M.; Neumann, JP (1990). "El sistema C-Cr (carbono-cromo)". Boletín de diagramas de fases de aleación . 11 (2): 152–159. doi :10.1007/bf02841701.
- ^ "Fluorita". aflow.org . Consultado el 22 de mayo de 2020 .
- ^ "Sal de roca". aflow.org . Consultado el 22 de mayo de 2020 .
- ^ Kantorovich, L. (2004). Teoría cuántica del estado sólido. Springer. pág. 32. ISBN 1-4020-2153-4.
- ^ Birkbeck College, Universidad de Londres
- ^ La estructura de la Zincblenda (B3). Laboratorio de Investigación Naval, EE. UU. Archivado el 19 de octubre de 2008 en Wayback Machine.
- ^ Wang, LD; Kwok, HS (2000). "Películas delgadas de nitruro de aluminio cúbico y nitruro de galio preparadas mediante deposición por láser pulsado". Applied Surface Science . 154–155 (1–4): 439–443. Bibcode :2000ApSS..154..439W. doi :10.1016/s0169-4332(99)00372-4.
- ^ Oseki, Masaaki; Okubo, Kana; Kobayashi, Atsushi; Ohta, Jitsuo; Fujioka, Hiroshi (2014). "Transistores de efecto de campo basados en nitruro de indio cúbico". Scientific Reports . 4 (1): 3951. Bibcode :2014NatSR...4E3951O. doi :10.1038/srep03951. PMC 3912472 . PMID 24492240.
- ^ Greenwood, Norman N. ; Earnshaw, Alan (1984). Química de los elementos. Oxford: Pergamon Press . p. 899. ISBN 978-0-08-022057-4..
- ^ Moyer, Harvey V. (1956). "Propiedades químicas del polonio". En Moyer, Harvey V. (ed.). Polonio (informe). Oak Ridge, Tennessee: Comisión de Energía Atómica de los Estados Unidos. págs. 33–96. doi : 10.2172/4367751 . TID-5221..
Lectura adicional
- Hurlbut, Cornelius S.; Klein, Cornelis, 1985, Manual de mineralogía , 20.ª edición, Wiley, ISBN 0-471-80580-7
Enlaces externos
- Simulaciones JMol de la Universidad de Graz :
- Cúbico simple
- BCC
- Comisión Federal de Comunicaciones (FCC)
- Profesional de la salud
- Elaboración de estructuras cristalinas con Molview