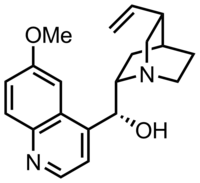
Quinina
 | |
 | |
| Datos clínicos | |
|---|---|
| Pronunciación | EE. UU .: / ˈ k w aɪ n aɪ n / , / k w ɪ ˈ n iː n / o Reino Unido : / ˈ k w ɪ n iː n / KWIN -een |
| Nombres comerciales | Qualaquin, Quinbisul, otros [1] |
| AHFS / Drogas.com | Monografía |
| MedlinePlus | a682322 |
| Datos de licencia | |
Categoría de embarazo |
|
| Vías de administración | Por vía oral , intramuscular , intravenosa , rectal. |
| Código ATC | |
| Estatus legal | |
| Estatus legal |
|
| Datos farmacocinéticos | |
| Unión de proteínas | 70–95% [4] |
| Metabolismo | Hígado (principalmente mediado por CYP3A4 y CYP2C19 ) |
| Vida media de eliminación | 8–14 horas (adultos), 6–12 horas (niños) [4] |
| Excreción | Riñón (20%) |
| Identificadores | |
| |
| Número CAS | |
| Identificador de centro de PubChem |
|
| Unión Internacional para la Investigación y el Desarrollo (IUPHAR)/BPS |
|
| Banco de medicamentos | |
| Araña química | |
| UNIVERSIDAD |
|
| BARRIL | |
| EBICh | |
| Química biológica | |
| Panel de control CompTox ( EPA ) |
|
| Tarjeta informativa de la ECHA | 100.004.550 |
| Datos químicos y físicos | |
| Fórmula | C20H24N2O2 |
| Masa molar | 324,424 g·mol −1 |
| Modelo 3D ( JSmol ) |
|
| Punto de fusión | 177 °C (351 °F) |
| |
 norte norte Y (¿que es esto?) (verificar) Y (¿que es esto?) (verificar) | |
La quinina es un medicamento que se utiliza para tratar la malaria y la babesiosis . [5] Esto incluye el tratamiento de la malaria causada por Plasmodium falciparum , que es resistente a la cloroquina cuando no se dispone de artesunato . [5] [6] Aunque a veces se utiliza para los calambres nocturnos en las piernas , no se recomienda la quinina para este propósito debido al riesgo de efectos secundarios graves . [5] Se puede tomar por vía oral o intravenosa . [5] La resistencia de la malaria a la quinina ocurre en ciertas áreas del mundo. [7] La quinina también se utiliza como ingrediente en el agua tónica y otras bebidas para impartir un sabor amargo. [8]
Los efectos secundarios comunes incluyen dolor de cabeza, zumbido en los oídos , problemas de visión y sudoración . [5] Los efectos secundarios más graves incluyen sordera , plaquetas bajas y ritmo cardíaco irregular . [5] El uso puede hacer que uno sea más propenso a las quemaduras solares . [5] Si bien no está claro si el uso durante el embarazo conlleva potencial de daño fetal, aún se recomienda tratar la malaria durante el embarazo con quinina cuando sea apropiado. [5] La quinina es un alcaloide , un compuesto químico natural. [5] No está del todo claro cómo funciona como medicamento. [5]
La quinina fue aislada por primera vez en 1820 de la corteza de un árbol de quina , que es originario de Perú , [5] [9] [10] y su fórmula molecular fue determinada por Adolph Strecker en 1854. [11] La clase de compuestos químicos a la que pertenece se llama alcaloides de la quina. Los extractos de corteza se habían utilizado para tratar la malaria desde al menos 1632 y fue introducida en España ya en 1636 por misioneros jesuitas que regresaban del Nuevo Mundo . [12] Está en la Lista de Medicamentos Esenciales de la Organización Mundial de la Salud . [13] [14] El tratamiento de la malaria con quinina marca el primer uso conocido de un compuesto químico para tratar una enfermedad infecciosa. [15]
Usos
Médico
A partir de 2006, la Organización Mundial de la Salud (OMS) ya no recomienda la quinina como tratamiento de primera línea para la malaria , porque existen otras sustancias que son igualmente eficaces y tienen menos efectos secundarios. Recomiendan que se utilice solo cuando no se disponga de artemisininas . [ ¿Por qué? ] [16] [17] [18] [19] La quinina también se utiliza para tratar el lupus y la artritis .
La quinina se recetaba con frecuencia como tratamiento no indicado en la etiqueta para los calambres en las piernas durante la noche , pero esto se ha vuelto menos común desde 2010 debido a una advertencia de la Administración de Alimentos y Medicamentos de los Estados Unidos (FDA) de que dicha práctica está asociada con efectos secundarios potencialmente mortales. [20] [21] [22] La quinina también puede actuar como un inhibidor competitivo de la monoaminooxidasa (MAO), una enzima que elimina los neurotransmisores del cerebro. Como inhibidor de la MAO , tiene el potencial de servir como tratamiento para personas con trastornos psicológicos, similar a los antidepresivos que inhiben la MAO. [23]
Formularios disponibles
La quinina es una amina básica y se presenta habitualmente en forma de sal. Entre las preparaciones existentes se encuentran el clorhidrato , el diclorhidrato, el sulfato , el bisulfato y el gluconato . En Estados Unidos, el sulfato de quinina se comercializa en comprimidos de 324 mg con la marca Qualaquin.
Todas las sales de quinina pueden administrarse por vía oral o intravenosa (IV); el gluconato de quinina también puede administrarse por vía intramuscular (IM) o rectal (PR). [24] [25] El principal problema con la administración rectal es que la dosis puede expulsarse antes de que se absorba por completo; en la práctica, esto se corrige administrando otra media dosis. En los EE. UU. no se ha autorizado ninguna preparación inyectable de quinina; en su lugar se utiliza quinidina . [26] [27]
| Nombre | Cantidad equivalente a 100 mg de quinina base |
|---|---|
| Base de quinina | 100 mg |
| Bisulfato de quinina | 169 mg |
| Diclorhidrato de quinina | 122 mg |
| Gluconato de quinina | 160 mg |
| Clorhidrato de quinina | 111 mg |
| Sulfato de quinina dihidrato [(quinina) 2 H 2 SO 4 ∙2H 2 O] | 121 mg |
Bebidas

La quinina es un componente del sabor de las bebidas con tónica y limón amargo . En la pistola de refrescos que se encuentra detrás de muchos bares, el agua tónica se designa con la letra "Q", que representa la quinina. [28]
El agua tónica se comercializó inicialmente como un medio para suministrar quinina a los consumidores con el fin de ofrecer protección contra la malaria. Según la tradición, debido al sabor amargo de la quinina tónica contra la malaria , los colonos británicos en la India la mezclaron con ginebra para hacerla más agradable al paladar, creando así el cóctel gin-tonic , que sigue siendo popular hoy en día. [29] Si bien es posible beber suficiente agua tónica para alcanzar temporalmente niveles de quinina que ofrezcan protección contra la malaria, no es un medio de protección sostenible a largo plazo. [30]
En Francia, la quinina es un ingrediente de un aperitivo conocido como quinquina , o "Cap Corse" , y del aperitivo a base de vino Dubonnet . En España, la quinina (también conocida como "corteza peruana" por su origen del árbol nativo de la quina) a veces se mezcla con el vino dulce de Málaga , que luego se llama "Málaga Quina" . En Italia, el vino aromatizado tradicional Barolo Chinato se infunde con quinina y hierbas locales, y se sirve como digestivo . En Gran Bretaña, la empresa AG Barr utiliza la quinina como ingrediente de la bebida carbonatada y con cafeína Irn-Bru . En Uruguay y Argentina, la quinina es un ingrediente de un agua tónica de PepsiCo llamada Paso de los Toros . En Dinamarca, se utiliza como ingrediente de la bebida deportiva carbonatada Faxe Kondi elaborada por Royal Unibrew .
Como agente aromatizante en bebidas, la quinina está limitada a 83 ppm ( 100 mg/L ) en los Estados Unidos y en la Unión Europea. [31] [32] [33]
Científico
La quinina (y la quinidina ) se utilizan como la fracción quiral para los ligandos utilizados en la dihidroxilación asimétrica de Sharpless , así como para muchas otras cadenas principales de catalizadores quirales. Debido a su rendimiento cuántico de fluorescencia relativamente constante y bien conocido , la quinina se utiliza en fotoquímica como un estándar de fluorescencia común . [34] [35]
Contraindicaciones
Debido a la estrecha diferencia entre sus efectos terapéuticos y tóxicos, la quinina es una causa común de trastornos inducidos por fármacos, incluyendo trombocitopenia y microangiopatía trombótica . [36] Incluso a partir de niveles menores presentes en bebidas comunes, la quinina puede tener efectos adversos graves que afectan a múltiples sistemas orgánicos, entre los que se encuentran efectos sobre el sistema inmunológico y fiebre , hipotensión , anemia hemolítica , lesión renal aguda , toxicidad hepática y ceguera. [36] En personas con fibrilación auricular , defectos de conducción o bloqueo cardíaco , la quinina puede causar arritmias cardíacas y debe evitarse. [37] [ verificación fallida ]
La quinina puede causar hemólisis en caso de deficiencia de G6PD (una deficiencia hereditaria), pero este riesgo es pequeño y el médico no debe dudar en utilizar quinina en personas con deficiencia de G6PD cuando no hay alternativa. [38]
Si bien no es necesariamente una contraindicación absoluta, la administración concomitante de quinina con fármacos metabolizados principalmente por CYP2D6 puede conducir a concentraciones plasmáticas del fármaco más altas de lo esperado, debido a la fuerte inhibición de la enzima por parte de la quinina. [39]
Efectos adversos
La quinina puede causar reacciones sanguíneas y cardiovasculares impredecibles, graves y potencialmente mortales, incluyendo recuento bajo de plaquetas y síndrome hemolítico-urémico / púrpura trombocitopénica trombótica (SHU/PTT), síndrome de QT largo y otras arritmias cardíacas graves, incluyendo torsades de pointes , fiebre de aguas negras , coagulación intravascular diseminada , leucopenia y neutropenia . [5] Algunas personas que han desarrollado PTT debido a la quinina han desarrollado insuficiencia renal . [5] [38] También puede causar reacciones de hipersensibilidad graves, incluyendo choque anafiláctico, urticaria , erupciones cutáneas graves, incluyendo síndrome de Stevens-Johnson y necrólisis epidérmica tóxica , angioedema , edema facial, broncoespasmo , hepatitis granulomatosa y picazón. [5] [38]
Los efectos adversos más comunes involucran un grupo de síntomas llamados cinconismo , que pueden incluir dolor de cabeza, vasodilatación y sudoración, náuseas, tinnitus , pérdida de audición, vértigo o mareos, visión borrosa y alteración en la percepción del color. [5] [36] [38] El cinconismo más severo incluye vómitos, diarrea, dolor abdominal, sordera, ceguera y alteraciones en el ritmo cardíaco. [38] El cinconismo es mucho menos común cuando la quinina se administra por vía oral, pero la quinina oral no se tolera bien (la quinina es excesivamente amarga y muchas personas vomitan después de ingerir tabletas de quinina). [5] Otros medicamentos, como Fansidar ( sulfadoxina con pirimetamina ) o Malarone ( proguanil con atovacuona ), a menudo se usan cuando se requiere terapia oral. El carbonato de etilo de quinina es insípido e inodoro, [40] pero está disponible comercialmente solo en Japón. No es necesario controlar los niveles de glucosa en sangre, los electrolitos ni la frecuencia cardíaca cuando se administra quinina por vía oral.
La quinina tiene diversas interacciones no deseadas con numerosos medicamentos recetados , como la potenciación de los efectos anticoagulantes de la warfarina . [5] Es un potente inhibidor de CYP2D6 , [39] una enzima implicada en el metabolismo de muchos fármacos.
Mecanismo de acción
En esta sección falta información sobre el mecanismo de los calambres y la acción de los IMAO antes mencionada. ( Diciembre de 2022 ) |
La quinina se utiliza por su toxicidad para el patógeno de la malaria, Plasmodium falciparum , al interferir con su capacidad para disolver y metabolizar la hemoglobina . [5] [41] Al igual que con otros fármacos antipalúdicos a base de quinolina, el mecanismo de acción preciso de la quinina no se ha resuelto por completo, aunque los estudios in vitro indican que inhibe la síntesis de ácidos nucleicos y proteínas, e inhibe la glucólisis en P. falciparum . [5] La hipótesis más aceptada de su acción se basa en el fármaco quinolínico muy estudiado y estrechamente relacionado, la cloroquina . Este modelo implica la inhibición de la biocristalización de la hemozoína en la vía de desintoxicación del hemo , lo que facilita la agregación del hemo citotóxico . [ cita médica necesaria ] El hemo citotóxico libre se acumula en los parásitos, provocando su muerte. [42] La quinina puede dirigirse a la enzima purina nucleósido fosforilasa de la malaria . [43]
Química
La absorción UV de la quinina alcanza su pico alrededor de los 350 nm (en UVA ). La emisión fluorescente alcanza su pico alrededor de los 460 nm (tono azul/cian brillante). [44] La quinina es altamente fluorescente ( rendimiento cuántico ~0,58) en solución de ácido sulfúrico 0,1 M. [34] [35]
Síntesis
Los árboles de quina siguen siendo la única fuente económicamente práctica de quinina. Sin embargo, bajo la presión de la guerra durante la Segunda Guerra Mundial, se emprendieron investigaciones para su producción sintética. Una síntesis química formal se logró en 1944 por los químicos estadounidenses RB Woodward y WE Doering . [45] Desde entonces, se han logrado varias síntesis totales de quinina más eficientes, [46] pero ninguna de ellas puede competir en términos económicos con el aislamiento del alcaloide de fuentes naturales. El primer tinte orgánico sintético , la malva , fue descubierto por William Henry Perkin en 1856 mientras intentaba sintetizar quinina.
Biosíntesis

En el primer paso de la biosíntesis de quinina , la enzima estrictosidina sintasa cataliza una reacción estereoselectiva de Pictet-Spengler entre triptamina y secologanina para producir estrictosidina . [47] [48] La modificación adecuada de estrictosidina conduce a un aldehído. La hidrólisis y la descarboxilación eliminarían inicialmente un carbono de la porción iridoide y producirían corinanteal. Luego, la cadena lateral de triptamina se escindió adyacente al nitrógeno, y este nitrógeno se unió a la función acetaldehído para producir cinchonaminal. La apertura del anillo heterocíclico de indol podría generar nuevas funciones amina y ceto. El nuevo heterociclo de quinolina se formaría luego combinando esta amina con el aldehído producido en la escisión de la cadena lateral de triptamina , dando cinconidinona. Para el último paso, la hidroxilación y la metilación dan quinina. [49] [50]
Catálisis
La quinina y otros alcaloides de Cinchona se pueden utilizar como catalizadores para reacciones estereoselectivas en síntesis orgánica . [51] : Tabla 3B Lámina 560 Por ejemplo, la adición de Michael catalizada por quinina de un malononitrilo a α,β-enonas proporciona un alto grado de control estereoquímico. [51]
Historia

La quinina era utilizada como relajante muscular por los quechuas , indígenas de Perú , Bolivia y Ecuador , para detener los temblores. [52] Los quechuas mezclaban la corteza molida de los árboles de quina con agua azucarada para compensar el sabor amargo de la corteza, produciendo así algo similar al agua tónica . [53]
Los misioneros jesuitas españoles fueron los primeros en traer la quina a Europa. Los españoles habían observado el uso que hacían los quechuas de la quina y conocían las propiedades medicinales de su corteza hacia la década de 1570 o antes: Nicolás Monardes (1571) y Juan Fragoso (1572) describieron un árbol, que posteriormente se identificó como el árbol de la quina, cuya corteza se utilizaba para producir una bebida para tratar la diarrea . [54] La quinina ha sido utilizada en forma no extraída por los europeos desde al menos principios del siglo XVII. [55]
Una historia popular sobre cómo llegó a Europa de la mano de la condesa de Chinchón fue desacreditada por el historiador médico Alec Haggis alrededor de 1941. [56] Durante el siglo XVII, la malaria era endémica de los pantanos y marismas que rodeaban la ciudad de Roma . Había causado la muerte de varios papas , muchos cardenales e innumerables ciudadanos romanos comunes. La mayoría de los sacerdotes católicos formados en Roma habían visto a pacientes con malaria y estaban familiarizados con los escalofríos provocados por la fase febril de la enfermedad.
El jesuita Agostino Salumbrino (1564-1642), [57] boticario de formación que vivió en Lima (hoy en el Perú ), observó que los quechuas usaban la corteza del árbol de la quina para tratar esos temblores. Si bien su efecto en el tratamiento de la malaria (y los temblores inducidos por la malaria) no estaba relacionado con su efecto en el control de los temblores provocados por los escalofríos , fue un medicamento exitoso contra la malaria. En la primera oportunidad, Salumbrino envió una pequeña cantidad a Roma para probarla como tratamiento contra la malaria. [58] En los años siguientes, la corteza de quina, conocida como corteza de jesuita o corteza peruana, se convirtió en uno de los productos más valiosos enviados desde Perú a Europa. Cuando el rey Carlos II se curó de la malaria a fines del siglo XVII con quinina, se hizo popular en Londres . [59] Siguió siendo el fármaco antipalúdico de elección hasta la década de 1940, cuando otros medicamentos tomaron el relevo. [60]
La forma de quinina más eficaz para tratar la malaria fue descubierta por Charles Marie de La Condamine en 1737. [61] [62] En 1820, los investigadores franceses Pierre Joseph Pelletier y Joseph Bienaimé Caventou aislaron por primera vez la quinina de la corteza de un árbol del género Cinchona , probablemente Cinchona pubescens , y posteriormente bautizaron la sustancia. [63] El nombre se deriva de la palabra quechua (inca) original para la corteza del árbol de quina, quina o quina-quina , que significa "corteza de corteza" o "corteza sagrada". Antes de 1820, la corteza se secaba, se molía hasta obtener un polvo fino y se mezclaba con un líquido (comúnmente vino) para beber. El uso a gran escala de la quinina como profilaxis de la malaria comenzó alrededor de 1850. En 1853, Paul Briquet publicó una breve historia y discusión de la literatura sobre la "quinquina". [64]
La quinina desempeñó un papel importante en la colonización de África por los europeos. Se ha dicho que la disponibilidad de quinina para el tratamiento fue la principal razón por la que África dejó de ser conocida como la "tumba del hombre blanco". Un historiador dijo que "fue la eficacia de la quinina lo que dio a los colonos nuevas oportunidades de invadir la Costa de Oro , Nigeria y otras partes de África occidental". [65]
Para mantener su monopolio sobre la corteza de quina, Perú y los países vecinos comenzaron a prohibir la exportación de semillas y plantones de quina a principios del siglo XIX. En 1865, Manuel Incra Mamani recolectó semillas de una planta particularmente rica en quinina y se las proporcionó a Charles Ledger . Ledger se las envió a su hermano, quien las vendió al gobierno holandés. Mamani fue arrestado en un viaje de recolección de semillas en 1871 y golpeado tan severamente, probablemente por proporcionar las semillas a extranjeros, que murió poco después. [66]
A finales del siglo XIX, los holandeses cultivaban las plantas en plantaciones de Indonesia y pronto se convirtieron en los principales proveedores del árbol. En 1913 crearon el Kina Bureau , un cártel de productores de quina encargado de controlar el precio y la producción. [67] En la década de 1930, las plantaciones holandesas en Java producían 22 millones de libras de corteza de quina, o el 97% de la producción mundial de quinina. [65] Los intentos de Estados Unidos de enjuiciar al Kina Bureau resultaron infructuosos. [67]
Durante la Segunda Guerra Mundial , las potencias aliadas se quedaron sin suministro de quinina cuando Alemania conquistó los Países Bajos y Japón controló Filipinas e Indonesia . Estados Unidos había obtenido cuatro millones de semillas de quina de Filipinas y comenzó a operar plantaciones de quina en Costa Rica . Además, comenzaron a cosechar corteza de quina silvestre durante las Misiones Cinchona . Dichos suministros llegaron demasiado tarde. Decenas de miles de tropas estadounidenses en África y el Pacífico Sur murieron de malaria debido a la falta de quinina. [65] A pesar de controlar el suministro, los japoneses no hicieron un uso efectivo de la quinina y, como resultado, miles de tropas japonesas en el suroeste del Pacífico murieron. [68] [69] [70] [71]
La quinina siguió siendo el fármaco antipalúdico de elección hasta después de la Segunda Guerra Mundial. Desde entonces, otros fármacos con menos efectos secundarios, como la cloroquina , la han sustituido en gran medida. [72]
Las pastillas para el resfriado con marca comercial Bromo Quinine contenían quinina y estaban fabricadas por Grove Laboratories. Se comercializaron por primera vez en 1889 y estuvieron disponibles al menos hasta la década de 1960. [73]
En su investigación en el centro de Misuri, John S. Sappington desarrolló de forma independiente una píldora antipalúdica a partir de quinina. Sappington comenzó a importar corteza de quina de Perú en 1820. En 1832, utilizando la quinina derivada de la corteza de quina, Sappington desarrolló una píldora para tratar una variedad de fiebres, como la escarlatina, la fiebre amarilla y la gripe, además de la malaria. Estas enfermedades estaban muy extendidas en los valles de Misuri y Misisipi. Fabricó y vendió las "píldoras antifebriles del Dr. Sappington" en todo Misuri. La demanda se volvió tan grande que en tres años, Sappington fundó una empresa conocida como Sappington and Sons para vender sus píldoras en todo el país. [74]
Sociedad y cultura
Ocurrencia natural
La corteza de Remijia contiene entre un 0,5 y un 2 % de quinina. La corteza es más barata que la corteza de Cinchona . Como tiene un sabor intenso, se utiliza para hacer agua tónica . [75]
Regulación en los EE.UU.
Entre 1969 y 1992, la Administración de Alimentos y Medicamentos de los Estados Unidos (FDA) recibió 157 informes de problemas de salud relacionados con el uso de quinina, incluidos 23 que habían resultado en muerte. [76] En 1994, la FDA prohibió la comercialización de quinina sin receta como tratamiento para los calambres nocturnos en las piernas. Pfizer Pharmaceuticals había estado vendiendo la marca Legatrin para este propósito. También se vende como cápsula blanda (por SmithKlineBeecham) como Q-vel. [ cita requerida ] Los médicos aún pueden recetar quinina, pero la FDA ha ordenado a las empresas que dejen de comercializar productos farmacéuticos no aprobados que contengan quinina. La FDA también está advirtiendo a los consumidores sobre el uso no aprobado de quinina para tratar calambres en las piernas. [20] [21] La quinina está aprobada para el tratamiento de la malaria, pero también se prescribía comúnmente para tratar calambres en las piernas y afecciones similares. Debido a que la malaria es potencialmente mortal, los riesgos asociados con el uso de quinina se consideran aceptables cuando se usa para tratar esa afección. [77]
Aunque la FDA prohibió el uso de Legatrin para el tratamiento de los calambres en las piernas, el fabricante de medicamentos URL Mutual ha comercializado un medicamento que contiene quinina llamado Qualaquin. Se comercializa como tratamiento para la malaria y se vende en los Estados Unidos sólo con receta médica. En 2004, los CDC informaron de sólo 1.347 casos confirmados de malaria en los Estados Unidos. [78]
Interrupción del embarazo
Durante gran parte del siglo XX, el uso de una sobredosis de quinina por parte de las mujeres para interrumpir deliberadamente un embarazo fue un método de aborto relativamente común en varias partes del mundo, incluida China. [79]
Agente de corte
La quinina a veces se detecta como agente de corte en drogas callejeras como la cocaína y la heroína . [80]
Otros animales
La quinina se utiliza como tratamiento para la infección por Cryptocaryon irritans (comúnmente conocida como mancha blanca, cripto o punto blanco marino) de los peces de acuario marino . [81]
Referencias
- ^ "Quinine International". Drugs.com . 2 de noviembre de 2020 . Consultado el 8 de noviembre de 2020 .
- ^ ab "Uso de quinina durante el embarazo". Drugs.com . 25 de marzo de 2020 . Consultado el 13 de agosto de 2020 .
- ^ "Lista de todos los medicamentos con advertencias de recuadro negro obtenida por la FDA (use los enlaces Descargar resultados completos y Ver consulta)". nctr-crs.fda.gov . FDA . Consultado el 22 de octubre de 2023 .
- ^ ab "Dosis, indicaciones, interacciones, efectos adversos y más de Qualaquin (quinina)". Referencia de Medscape . WebMD. Archivado desde el original el 2 de febrero de 2014. Consultado el 29 de enero de 2014 .
- ^ abcdefghijklmnopqrs «Sulfato de quinina». Drugs.com. 20 de febrero de 2020. Consultado el 14 de mayo de 2020 .
- ^ Esu EB, Effa EE, Opie ON, Meremikwu MM (junio de 2019). "Arteméter para la malaria grave". Base de datos Cochrane de revisiones sistemáticas . 6 (6): CD010678. doi :10.1002/14651858.CD010678.pub3. PMC 6580442. PMID 31210357 .
- ^ Foley M, Tilley L (febrero de 1997). "Antimaláricos a base de quinolina: mecanismos de acción y resistencia". Revista Internacional de Parasitología . 27 (2): 231–240. doi :10.1016/s0020-7519(96)00152-x. PMID 9088993.
- ^ Olmsted J, Williams GM (1997). Química: la ciencia molecular. Jones & Bartlett Learning. pág. 137. ISBN 978-0-815-18450-8Archivado desde el original el 15 de septiembre de 2016.
- ^ Willcox M (28 de junio de 2004). Plantas medicinales tradicionales y malaria. CRC Press. pág. 231. ISBN 9780203502327.
- ^ Cechinel-Filho V (2012). Bioactivos vegetales y descubrimiento de fármacos: principios, práctica y perspectivas. Hoboken, NJ: John Wiley & Sons. p. 2. ISBN 9780470582268Archivado desde el original el 4 de marzo de 2016.
- ^ Strecker A (1854). "Ueber einen neuen aus Aldehyd - Ammoniak und Blausäure entstehenden Körper". Liebigs Ann. química . 91 (3): 349–351. doi :10.1002/jlac.18540910309.
- ^ Staines HM, Krishna S (2011). Tratamiento y prevención de la malaria: química, acción y uso de los fármacos antipalúdicos. [Sl]: Springer Verlag. p. 45. ISBN 9783034604796.
- ^ Organización Mundial de la Salud (2019). Lista modelo de medicamentos esenciales de la Organización Mundial de la Salud: 21.ª lista , 2019. Ginebra: Organización Mundial de la Salud. hdl : 10665/325771 . OMS/MVP/EMP/IAU/2019.06. Licencia: CC BY-NC-SA 3.0 IGO.
- ^ Organización Mundial de la Salud (2021). Lista modelo de medicamentos esenciales de la Organización Mundial de la Salud: 22.ª lista (2021) . Ginebra: Organización Mundial de la Salud. hdl : 10665/345533 . OMS/MHP/HPS/EML/2021.02.
- ^ "Quinina". Enciclopedia Británica . Consultado el 12 de noviembre de 2021 .
- ^ Organización Mundial de la Salud (2006). «Directrices para el tratamiento de la malaria» (PDF) . Organización Mundial de la Salud. Archivado desde el original (PDF) el 5 de agosto de 2009. Consultado el 10 de agosto de 2009 .
- ^ Dondorp A, Nosten F, Stepniewska K, Day N, White N (2005). "Artesunato versus quinina para el tratamiento de la malaria falciparum grave: un ensayo aleatorizado". Lancet . 366 (9487): 717–725. doi : 10.1016/S0140-6736(05)67176-0 . PMID 16125588. S2CID 173027.
- ^ Reyburn H, Mtove G, Hendriksen I, von Seidlein L (julio de 2009). "Quinina oral para el tratamiento de la malaria no complicada" (PDF) . BMJ . 339 : b2066. doi :10.1136/bmj.b2066. PMID 19622550. S2CID 206891479.
- ^ Achan J, Tibenderana JK, Kyabayinze D, Wabwire Mangen F, Kamya MR, Dorsey G, et al. (Julio de 2009). "Efectividad de la quinina versus arteméter-lumefantrina para el tratamiento de la malaria falciparum no complicada en niños de Uganda: ensayo aleatorizado". BMJ . 339 : b2763. doi :10.1136/bmj.b2763. PMC 2714631 . PMID 19622553.
- ^ ab "Comunicado de seguridad de medicamentos de la FDA: Nuevo plan de gestión de riesgos y guía de medicación para pacientes para Qualaquin (sulfato de quinina)". Administración de Alimentos y Medicamentos de los Estados Unidos (FDA). 7 de agosto de 2010. Archivado desde el original el 19 de febrero de 2011. Consultado el 21 de febrero de 2011 .
- ^ ab "Riesgos graves asociados con el uso de quinina para prevenir o tratar los calambres nocturnos en las piernas (septiembre de 2012)". Administración de Alimentos y Medicamentos de Estados Unidos (FDA) . 31 de agosto de 2012. Archivado desde el original el 22 de octubre de 2016. Consultado el 19 de enero de 2020 .
- ^ "Quinina para los calambres nocturnos en las piernas". Consumer Reports . Consultado el 20 de enero de 2020 .
- ^ Mitsui N, Noro T, Kuroyanagi M, Miyase T, Umehara K, Ueno A (febrero de 1989). "Inhibidores de la monoaminooxidasa de la corteza de Cinchonae". Chemical & Pharmaceutical Bulletin . 37 (2): 363–366. doi : 10.1248/cpb.37.363 . PMID 2743481.
- ^ Barennes H, Pussard E, Mahaman Sani A, Clavier F, Kahiatani F, Granic G, et al. (mayo de 1996). "Eficacia y farmacocinética de una nueva formulación de quinina intrarrectal en niños con malaria por Plasmodium falciparum". British Journal of Clinical Pharmacology . 41 (5): 389–395. doi :10.1046/j.1365-2125.1996.03246.x. PMC 2042609 . PMID 8735679.
- ^ Barennes H, Balima-Koussoubé T, Nagot N, Charpentier JC, Pussard E (mayo de 2006). "Seguridad y eficacia de la quinina rectal en comparación con la intramuscular para el tratamiento temprano de la malaria moderadamente grave en niños: ensayo clínico aleatorizado". BMJ . 332 (7549): 1055–1059. doi :10.1136/bmj.332.7549.1055. PMC 1458599 . PMID 16675812.
- ^ Centros para el Control y la Prevención de Enfermedades (abril de 1991). "Tratamiento con gluconato de quinidina de personas con infección grave por Plasmodium falciparum: interrupción de la quinina parenteral por parte del Servicio de Medicamentos de los CDC". MMWR. Recomendaciones e informes . 40 (RR-4): 21–23. PMID 1850497.
- ^ Magill A, Panosian C (julio de 2005). "Hacer que los agentes antimaláricos estén disponibles en los Estados Unidos". The New England Journal of Medicine . 353 (4): 335–337. doi : 10.1056/NEJMp058167 . PMID 16000347.
- ^ Charming C (2006). Guía de la señorita Charming para camareros de moda y aspirantes a camareros de lujo . Estados Unidos: Sourcebooks, Inc., pág. 189. ISBN 978-1-4022-0804-1.
- ^ Khosla S (17 de marzo de 2017). «Gin and Tonic: La fascinante historia detrás de la invención del clásico cóctel inglés». India.com . Consultado el 8 de junio de 2019 .
- ^ Meyer CG, Marks F, May J (diciembre de 2004). "Editorial: El gin tonic revisitado". Medicina tropical y salud internacional . 9 (12): 1239–1240. doi : 10.1111/j.1365-3156.2004.01357.x . PMID 15598254. S2CID 24261782.
- ^ Ballestero JA, Plazas PV, Kracun S, Gómez-Casati ME, Taranda J, Rothlin CV, et al. (septiembre de 2005). "Efectos de la quinina, la quinidina y la cloroquina en los receptores colinérgicos nicotínicos alfa9alfa10". Farmacología molecular . 68 (3): 822–829. doi :10.1124/mol.105.014431. PMID 15955868. S2CID 26907917.
- ^ "Lista de estados de aditivos alimentarios". Administración de Alimentos y Medicamentos de EE. UU. . Departamento de Salud y Servicios Humanos de EE. UU . . Consultado el 9 de octubre de 2017 .
- ^ «REGLAMENTO DE EJECUCIÓN (UE) N.º 872/2012 DE LA COMISIÓN». EUR-Lex . Diario Oficial de la Unión Europea . Consultado el 9 de octubre de 2017 .
- ^ ab Lakowicz JR (2006). "2. Instrumentación para espectroscopia de fluorescencia". Principios de espectroscopia de fluorescencia (3.ª ed.). Springer Science & Business Media. pág. 54. ISBN 978-0-387-46312-4.
- ^ ab Prahl S. "Sulfato de quinina". OMLC . Consultado el 16 de agosto de 2013 .
- ^ abc Liles NW, Page EE, Liles AL, Vesely SK, Raskob GE, George JN (mayo de 2016). "Diversidad y gravedad de las reacciones adversas a la quinina: una revisión sistemática". American Journal of Hematology . 91 (5): 461–466. doi : 10.1002/ajh.24314 . PMID 26822544.
- ^ "Se debe evitar el uso de sildenafil fuera de indicación en la enfermedad cardíaca valvular". Clinical Pharmacist . 2017. doi :10.1211/cp.2017.20203778. ISSN 2053-6178.
- ^ abcde «Etiqueta estadounidense: sulfato de quinina» (PDF) . FDA. Abril de 2013. Archivado (PDF) del original el 20 de enero de 2017.
- ^ ab Fasinu PS, Tekwani BL, Avula B, Chaurasiya ND, Nanayakkara NP, Wang YH, et al. (septiembre de 2016). "Inhibición de la vía específica del metabolismo de la primaquina por cloroquina / quinina". Revista de malaria . 15 (1): 466. doi : 10.1186/s12936-016-1509-x . PMC 5020452 . PMID 27618912.
- ^ Jamaludin A, Mohamad M, Navaratnam V, Selliah K, Tan SC, Wernsdorfer WH, et al. (febrero de 1988). "Biodisponibilidad relativa de las sales de clorhidrato, sulfato y carbonato de etilo de la quinina". British Journal of Clinical Pharmacology . 25 (2): 261–263. doi :10.1111/j.1365-2125.1988.tb03299.x. PMC 1386482 . PMID 3358888.
- ^ Wishart DS , Djombou Feunang Y, Guo AC, Lo EJ, Marcu A, Grant JR, et al. "Quinina | DrugBank Online". Banco de medicamentos . 5.0.
- ^ Foley M, Tilley L (febrero de 1997). "Antimaláricos a base de quinolina: mecanismos de acción y resistencia". Revista Internacional de Parasitología . 27 (2): 231–240. doi :10.1016/s0020-7519(96)00152-x. PMID 9088993.
- ^ Lowe D (22 de enero de 2019). «El objetivo de la quinina». Science . Consultado el 28 de enero de 2019 .
- ^ "Conceptos básicos de fluorescencia". Archivado desde el original el 13 de septiembre de 2012.
- ^ Woodward R, Doering W (1944). "La síntesis total de la quinina". J Am Chem Soc . 66 (849): 849. doi :10.1021/ja01233a516.
- ^ Kaufman TS, Rúveda EA (2005). "Die Jagd auf Chinin: Etappenerfolge und Gesamtsiege". Edición internacional Angewandte Chemie (en alemán). 117 (6): 876–907. Código Bib : 2005AngCh.117..876K. doi : 10.1002/ange.200400663.
- ^ Treimer JF, Zenk MH (noviembre de 1979). "Purificación y propiedades de la estrictósidina sintasa, la enzima clave en la formación de alcaloides indólicos". Revista Europea de Bioquímica . 101 (1): 225–233. doi : 10.1111/j.1432-1033.1979.tb04235.x . PMID 510306.
- ^ Mizukami H, Nordlöv H, Lee SL, Scott AI (agosto de 1979). "Purificación y propiedades de la estrictósidina sintetasa (una enzima que condensa triptamina y secologanina) a partir de células cultivadas de Catharanthus roseus". Bioquímica . 18 (17): 3760–3763. doi :10.1021/bi00584a018. PMID 476085.
- ^ Productos naturales medicinales: un enfoque biosintético (3.ª edición). Wiley. pp. 380–381. ISBN 9780470742761.
- ^ O'Connor SE, Maresh JJ (agosto de 2006). "Química y biología de la biosíntesis de alcaloides indólicos monoterpénicos". Natural Product Reports . 23 (4): 532–547. doi :10.1039/b512615k. PMID 16874388.
- ^ ab Reyes E, Uria U, Vicario JL, Carrillo L (13 de septiembre de 2016), "La reacción catalítica y enantioselectiva de Michael", Organic Reactions , Hoboken , Nueva Jersey, EE. UU.: John Wiley & Sons, Inc., págs. 1–898, doi :10.1002/0471264180.or090.01, ISBN 978-0-471-26418-7
- ^ Flückiger FA , Hanbury D (1874). "Cortex Cinchonæ". Pharmacographia: Una historia de los principales fármacos de origen vegetal encontrados en Gran Bretaña y la India británica . Londres: Macmillan and Co., págs. 302–331.
- ^ Hobbs K, West D (2020). La historia de los árboles: y cómo cambiaron nuestra forma de vida . Ilustrado por Thibaud Hérem. Londres: Laurence King. Pág. 148. ISBN. 978-1-7862-7522-6.
- ^ Ver:
- Ortiz Crespo FI (1995). "Fragoso, Monardes y el conocimiento prechinchoniano de Cinchona". Archivos de Historia Natural . 22 (2): 169–181. doi :10.3366/anh.1995.22.2.169. ISSN 0260-9541.
- Stuart DC (2004). Dangerous Garden: The Quest for Plants to Change Our Lives [Jardín peligroso: la búsqueda de plantas que cambien nuestras vidas]. Cambridge, MA: Harvard University Press. pág. 28. ISBN 978-0-674-01104-5.
- Monardes N (1580). Primera y segunda y tercera partes de la Historia medicinal, de las cosas que se traen de nuestras Indias Occidentales, que sirven en Medicina utilizado en Medicina ] (en español). Sevilla, España: Fernando Díaz. págs. 74–75.
Del nuevo Reyno, trae una corteza, que dizen ser de un árbol, que es de mucha grandeza: el qual dizen que lleva unas hojas en forma de corazón, y que no lleva fruto. Este árbol tiene una corteza gruessa, muy solida y dura, que en esto y en el color parece mucho a la corteza del palo que llaman Guayacan: en la superficie tiene una película delgada blanquisca, quebrada por toda ella: tiene la corteza mas de un dedo de gruesso, solida y pesada: la qual gustada tiene notable amargor, como el de la Genciana: tiene en el gusto notable astriction, con alguna aromaticidad, porque al fin de mascar la respica della buen olor. Tienen los indios esta corteza en mucho, y usan della en todo genero de camaras, que sean con sangre, o sin ella. Los españoles fatigados de esta enfermedad, por aviso de los Indios, han usado de esta corteza y han sanado muchos dellos con ella.
grande: se dice que tiene hojas en forma de corazón, y que no da fruto. Este árbol tiene una corteza gruesa, muy sólida y dura, que en esto y en su color se parece mucho a la corteza del árbol que se llama guayacán : en la superficie, tiene una película blanquecina delgada y discontinua en toda su extensión: tiene corteza de más de un dedo de espesor, sólida y pesada: la cual, al probarla, tiene un amargor considerable, como el de la genciana: tiene en su gusto una astringencia considerable, con cierta aromaticidad, porque al final Al masticarlo se respira un olor dulce. Los indios tienen en gran estima esta corteza y la usan para toda clase de diarreas, con sangre o sin ella. Los españoles, cansados de esta enfermedad, por consejo de los indios, han Usaron esta corteza y curaron a muchos de los que la usaban. Toman hasta un frijol pequeño, lo hacen polvo, lo toman con vino tinto o en agua apropiada, si tienen fiebre o enfermedad: debe tomarse en por la mañana en ayunas, tres o cuatro veces; en lo demás, seguir el orden y régimen que convenga a los que tienen diarrea.]
Toman della tanto como una pequeña había hecha polvos, tómase en vino tinto, o en agua apropiada, como tienen la calentura, o mal: hase de tomar por la mañana en ayunas, tres o cuatro veces: usando en lo demás, la orden y Del nuevo reino se trae una corteza, que se dice que es de un árbol, que es muy - Fragoso J (1572). Discursos de las cosas aromáticas, arboles y frutales, y de otras muchas medicinas simples que se traen de la India Oriental y que sirven al uso de medicina traídos de la India y Oriente y son de utilidad para la medicina ] (en español). Madrid, España: Francisco Sánchez. pag. 35.
En el nuevo mundo hay un gran árbol que lleva las hojas en forma de corazón, y carece de fruto. Tiene dos cortezas, la una gruessa muy solida y dura, que assi en la sustancia como en el color es muy semejante al Guayacán: la otra es más delgada y blanquezina, la cual es amarga con alguna estipticidad: y demas desto es aromática.
Tienenla en muchosnuestros Indios, porque la usan contra cualesquiera cámaras, tomando del polvo peso de una drama o poco más, desatado en agua azerada, o vino tinto.
de corazón, y le falta fruto. Tiene dos cortezas, una [es] gruesa, muy sólida, [y] dura, que en sustancia así como en color se parece mucho al guayacán [es decir, lignum vitae ]: la otra es más delgada y blanquecino, que es amargo con alguna cualidad astringente; y además de esto, es aromático. Nuestros indios lo tienen en gran estima, porque lo usan contra cualquier diarrea, tomando un peso de una dracma o un poco más de la [polvo, mezclándolo con agua mineral o vino tinto.]
- ^ Achan J, Talisuna AO, Erhart A, Yeka A, Tibenderana JK, Baliraine FN y col. (mayo de 2011). "Quinina, un antiguo fármaco contra la malaria en un mundo moderno: papel en el tratamiento de la malaria". Revista de malaria . 10 : 144. doi : 10.1186/1475-2875-10-144 . PMC 3121651 . PMID 21609473.
- ^ Pain S (15 de septiembre de 2001). "La condesa y la cura". New Scientist .
- ^ de Andrade A (3 de agosto de 1642). "Vida del Devoto Hermano Agustin Salumbrino" [La vida del devoto Hermano Agustin Salumbrino]. Varones ilustres en santidad, letras y zelo de las almas de la Compañía de Jesús . Varones ilustres de la Compañía de Jesús (en español). vol. 5. Serie original de Juan Eusebio Nieremberg . Madrid, España: José Fernández de Buendía (publicado en 1666). págs. 612–628. pag. 612:
Naciò el Hermano Agustin Salumbrino el año de mil y quinientos y sesenta y quatro en la Ciudad de Fḷọṛi en la Rumania […]
[El Hermano Agustino Salumbrino nació en el año 1564 en la ciudad de Forlì en Romaña ] - ^ Ver:
- Medina Rodríguez F, Aceves Ávila FJ, Moreno Rodríguez J (2007). "Precisiones sobre la historia de la quinina". Reumatología Clínica . Cartas al Editor. 3 (4): 194–196. doi :10.1016/S2173-5743(07)70246-0. ISSN 2173-5743.
De hecho, aunque aún no se ha dicho la última palabra al respecto, hay textos jesuitas que mencionan que la quinina llegó a Roma en 1632, siendo su introductor el provincial de las misiones jesuitas en el Perú, padre Alonso Messia Venegas, cuando trajo una muestra de la corteza para presentarla como primado, y que había salido de Lima 2 años antes, pues se ha registrado constancia de su estancia en Sevilla 1632, publicando allí uno de sus libros y siguiendo su camino a Roma como procurador.
- Torres Saldamando E (junio de 1882). "El P. Diego de Torres Vázquez". Los antiguos jesuitas del Perú (en español). Lima, Perú: Imprenta Liberal. págs. 180-181. pag. 181:
Al año siguiente se dirigieron á Europa los Procuradores P. Alonso Messía Venegas y P. Hernando de León Garavito, llevando gran cantidad de la corteza de la quina, cuyo conocimiento se extendió por el mundo los jesuitas.
[Al año siguiente [es decir, 1631] fueron a Europa los procuradores Padre Alonso Messia Venegas y Padre Hernando de León Garavito, llevándose una gran cantidad de corteza de quina, cuyo conocimiento los jesuitas difundieron por todo el mundo.] - Bailetti A. "Capítulo 10: La Condesa de Chinchón". LA MISIÓN DEL JESUITA AGUSTÍN SALUMBRINO, la malaria y el árbol de quina .
A últimas horas de la tarde del treinta y uno de mayo de 1631 se hizo a la vela la Armada Real con dirección a Panamá llevando el precioso cargamento de oro y plata.
[A última hora de la tarde del 31 de mayo de 1631, la armada real zarpó rumbo a Panamá, llevando consigo su carga multimillonaria de oro y plata.
En una de las naves viajaban los procuradores jesuitas padres Alonso Messia y Hernando León Garavito custodiando los fardos con la corteza de quina en polvo preparada por Salumbrino. Después de casi veinte días de navegación el inapreciable medicamento llegó a la ciudad de Panamá, donde fue descargado para cruzar en mulas el agreste camino del itsmo palúdico hasta Portobelo para seguir a Cartagena y la Habana, cruzar el Atlántico y llegar a Sanlúcar de Barrameda en Sevilla. […] Finalmente siguió su camino a Roma ya su destino final el Hospital del Espíritu Santo.
En uno de los barcos viajaban los procuradores jesuitas, los padres Alonso Messia y Hernando León Garavito, guardando las cajas de polvo de quina, preparadas por Salumbrino. Después de casi 20 días de navegación, la medicina llegó a la ciudad de Panamá, donde fue trasbordada en mulas. Luego recorrió el istmo palúdico hasta Portobelo, de allí a Cartagena [en Colombia] y La Habana. Luego viajó a Sanlúcar de Barrameda en Sevilla, [España]. […] Finalmente siguió el camino hacia Roma y hasta su destino final, el Hospital del Espíritu Santo]
- Medina Rodríguez F, Aceves Ávila FJ, Moreno Rodríguez J (2007). "Precisiones sobre la historia de la quinina". Reumatología Clínica . Cartas al Editor. 3 (4): 194–196. doi :10.1016/S2173-5743(07)70246-0. ISSN 2173-5743.
- ^ Rocco F (2004). Quinina: malaria y la búsqueda de una cura que cambió el mundo . Nueva York, NY: Perennial.
- ^ Humphrey L (2000). Quinina y cuarentena . Columbia, Missouri: University of Missouri Press.
- ^ Marie de la Condamine C (29 de mayo de 1737). "Sur el árbol de la quinquina". Historia de la Academia Real de Ciencias . Imprimerie Royale (publicado en 1740). págs. 226–243.
- ^ De Jussieu acompañó a de la Condamine en la expedición de este último al Perú: de Jussieu J (1737). Descripción del árbol de quinquina. París: Société dutreatmentement des quinquinas (publicado en 1934).
- ^ Pelletier PJ, Caventou JB (1820). "Recherches Chimiques sur les Quinquinas" [Continuación: Investigación química sobre las Quinquinas]. Annales de Chimie et de Physique (en francés). 15 . Crochard: 337–365.
Los autores nombran la quinina en la página 348:
"..., nous avons cru devoir la nommer
quinine
, pour la distinguir de la cinchonine par un nom qui indica également son origine".
[…, pensamos que deberíamos llamarla "quinina" para distinguirla de la cinconina mediante un nombre que también indique su origen.] - ^ Briqueta P (1853). Traité thérapeutique du quinone et de ses préparations (en francés). París: L. Martinet.
- ^ abc Conner CD (2005). Una historia popular de la ciencia: mineros, parteras y "mecánicos de bajo nivel" . Nueva York: Nation Books. págs. 95-96. ISBN 978-1-56025-748-6.También cita a Porter R (1998). El mayor beneficio para la humanidad: una historia médica de la humanidad. Nueva York: WW Norton. pp. 465–466. ISBN. 978-0-393-04634-2.
- ^ Canales NA (7 de abril de 2022). «En busca de plantas perdidas en colecciones botánicas». Wellcome Collection . Consultado el 9 de mayo de 2022 .
- ^ ab Shah S (2010). La fiebre: cómo la malaria ha dominado a la humanidad durante 500.000 años . Farrar, Straus y Giroux. pág. 94.
- ^ Morton L (1953). "29". La caída de Filipinas . Washington, DC: Ejército de los Estados Unidos. p. 524. Archivado desde el original el 25 de mayo de 2017.
- ^ Hawk A. "Recordando la guerra en Nueva Guinea: Cuerpo Médico Japonés – malaria". Archivado desde el original el 22 de noviembre de 2011.
- ^ Heaton LD, ed. (1963). "8". Medicina preventiva en la Segunda Guerra Mundial: Volumen VI, Enfermedades transmisibles: malaria . Washington, DC: Departamento del Ejército. págs. 401 y 434. Archivado desde el original el 29 de enero de 2012.
- ^ "Notas sobre los servicios médicos japoneses". Tactical and Technical Trends (36). 1943. Archivado desde el original el 14 de octubre de 2011.
- ^ Shah S (2010). La fiebre: cómo la malaria ha dominado a la humanidad durante 500.000 años . Farrar, Straus y Giroux. pág. 102.
- ^ "Medicina: ¿Qué es bueno para un resfriado?". Time . 22 de febrero de 1960. Archivado desde el original el 26 de julio de 2010. Consultado el 27 de abril de 2010 .
- ^ "John. S Sappington". Habitantes históricos de Missouri . Sociedad Histórica del Estado de Missouri.
- ^ Hobhouse H (2004). Šest rostlin, které změnily svět (en checo). Praga: Akademie věd České republiky. pag. 59.ISBN 978-80-200-1179-4.
- ^ "La FDA ordena detener la comercialización de quinina para los calambres nocturnos en las piernas". Revista de consumidores de la FDA . Administración de Alimentos y Medicamentos de los Estados Unidos (FDA). Julio-agosto de 1995. Archivado desde el original el 15 de enero de 2008. Consultado el 31 de julio de 2009 .
- ^ "La FDA ordena que se retiren del mercado medicamentos a base de quinina no aprobados y advierte a los consumidores sobre el uso no autorizado de quinina para tratar calambres en las piernas" (Comunicado de prensa). Administración de Alimentos y Medicamentos de los Estados Unidos (FDA). 11 de diciembre de 2006. Archivado desde el original el 28 de julio de 2009. Consultado el 31 de julio de 2009 .
- ^ Skarbinski J, James EM, Causer LM, Barber AM, Mali S, Nguyen-Dinh P, et al. (mayo de 2006). "Vigilancia de la malaria: Estados Unidos, 2004" (PDF) . Informe semanal de morbilidad y mortalidad. Resúmenes de vigilancia . 55 (4): 23–37. PMID 16723971.
- ^ Rodríguez SM (2023). Realidades reproductivas en la China moderna: control de la natalidad y aborto, 1911-2021 . Cambridge, Reino Unido: Cambridge University Press . p. 1. ISBN. 978-1-009-02733-5.OCLC 1366057905 .
- ^ "Tabletas que imitan la dimetiltriptamina y el éxtasis (que en realidad contienen 5-metoxi-metilisopropiltriptamina) en Oregón" (PDF) . Administración para el Control de Drogas, Departamento de Justicia de los Estados Unidos. Octubre de 2009. p. 79. Archivado desde el original (PDF) el 17 de octubre de 2012. Consultado el 22 de septiembre de 2012 .
- ^ Porritt M. "Cryptocaryon irritans". Revista Reef Culture (1.ª ed.). Archivado desde el original el 24 de octubre de 2009. Consultado el 9 de julio de 2009 .
Lectura adicional
- Schroeder-Lein G (2008). La enciclopedia de la medicina de la Guerra Civil . Armonk, NY: Sharpe, Inc.
- Hobhouse H (2005) [1986]. Semillas de cambio: seis plantas que transformaron a la humanidad . Berkeley, CA: Counterpoint. ISBN 978-1-59376-049-6.
- Stockwell JR (octubre de 1982). "Consideraciones aeromédicas de la profilaxis de la malaria con clorhidrato de mefloquina" . Medicina aeronáutica, espacial y medioambiental . 53 (10): 1011–1013. PMID 6983345.
- Wolff RS, Wirtschafter D, Adkinson C (junio de 1997). «Toxicidad ocular por quinina tratada con oxígeno hiperbárico». Undersea & Hyperbaric Medicine . 24 (2): 131–134. PMID 9171472. Archivado desde el original el 11 de agosto de 2011. Consultado el 13 de agosto de 2008 .
{{cite journal}}: CS1 maint: URL no apta ( enlace ) - Slater L (2009). Guerra y enfermedad: investigación biomédica sobre la malaria en el siglo XX . New Brunswick, NJ: Rutgers University Press.
- Lloyd HD (junio de 1884). "Los señores de la industria". The North American Review . 138 (331). Universidad del Norte de Iowa: 535–553. ISSN 0029-2397. JSTOR 25118388.
- Organización Mundial de la Salud (2015). Guías para el tratamiento de la malaria (3.ª ed.). Organización Mundial de la Salud (OMS). hdl :10665/162441. ISBN 9789241549127.
Enlaces externos
- Quinina en el Portal de Información sobre Medicamentos
- La quinina en el Programa Internacional de Seguridad Química
- "Quinina". Centro de recursos . Chemwatch.


