Cáncer orofaríngeo con VPH positivo
| Cáncer orofaríngeo positivo al virus del papiloma humano | |
|---|---|
| Otros nombres | Cáncer orofaríngeo HPV16+, HPV16+OPC |
 | |
| Imagen microscópica de un tumor que muestra positividad para VPH mediante hibridación in situ | |
| Especialidad | Oncología |
| Síntomas | Llaga o ampolla en la parte posterior de la boca, dificultad para hablar, tragar o respirar, hinchazón en el cuello, pérdida de apetito, pérdida de peso y debilidad. |
| Causas | Virus del papiloma humano |
| Factores de riesgo | contacto sexual oral |
| Método de diagnóstico | Endoscopia , biopsia , tinción para p16 , tomografía computarizada , |
| Diagnóstico diferencial | Cáncer orofaríngeo asociado al tabaco |
| Prevención | Vacunación |
| Tratamiento | Cirugía , radiación , quimioterapia. |
| Frecuencia | 22.000 casos a nivel mundial (2008) [1] [2] |
El cáncer orofaríngeo positivo al virus del papiloma humano ( OPC positivo al VPH o OPC VPH+ ) es un cáncer ( carcinoma de células escamosas ) de la garganta causado por el virus del papiloma humano tipo 16 (VPH16). En el pasado, el cáncer de la orofaringe (garganta) se asociaba con el uso de alcohol o tabaco o ambos, pero la mayoría de los casos ahora están asociados con el virus VPH , que se adquiere al tener contacto oral con los genitales ( sexo oral-genital ) de una persona que tiene una infección genital por VPH. Los factores de riesgo incluyen tener un gran número de parejas sexuales, antecedentes de sexo oral-genital o sexo anal-oral , tener una pareja femenina con antecedentes de un frotis de Papanicolaou anormal o displasia cervical , tener periodontitis crónica y, entre los hombres, una edad más joven en la primera relación sexual y antecedentes de verrugas genitales . El OPC HPV positivo se considera una enfermedad separada del cáncer orofaríngeo HPV negativo (también llamado OPC HPV negativo y OPC HPV).
El OPC positivo para VPH se presenta de una de cuatro maneras: como una anomalía asintomática en la boca detectada por el paciente o un profesional de la salud como un dentista; con síntomas locales como dolor o infección en el sitio del tumor; con dificultades para hablar, tragar y/o respirar; o como una hinchazón en el cuello si el cáncer se ha propagado a los ganglios linfáticos locales. La detección de una proteína supresora de tumores , conocida como p16 , se utiliza comúnmente para diagnosticar un OPC asociado a VPH. La extensión de la enfermedad se describe en el sistema estándar de estadificación del cáncer , utilizando el sistema TNM del AJCC , basado en el estadio T (tamaño y extensión del tumor), el estadio N (extensión de la afectación de los ganglios linfáticos regionales ) y el estadio M (si hay propagación de la enfermedad fuera de la región o no), y se combinan en un estadio general de I a IV. En 2016, se desarrolló un sistema de estadificación separado para el OPC con VPH+, distinto del OPC con VPH-.
Mientras que la mayoría de los cánceres de cabeza y cuello han ido disminuyendo a medida que se han reducido las tasas de tabaquismo, el cáncer orofaríngeo positivo al VPH ha ido aumentando. En comparación con los pacientes con cáncer orofaríngeo positivo al VPH, los pacientes con cáncer orofaríngeo positivo al VPH tienden a ser más jóvenes, tienen un nivel socioeconómico más alto y tienen menos probabilidades de fumar. Además, tienden a tener tumores más pequeños, pero es más probable que se vean afectados los ganglios linfáticos cervicales. En los Estados Unidos y otros países, el número de casos de cáncer orofaríngeo ha ido aumentando de forma constante, y la incidencia de cáncer orofaríngeo positivo al VPH aumenta más rápido que la disminución de cáncer orofaríngeo negativo al VPH. El aumento se observa especialmente en los hombres jóvenes de los países desarrollados , y el cáncer orofaríngeo positivo al VPH representa ahora la mayoría de todos los casos de cáncer orofaríngeo. Se están realizando esfuerzos para reducir la incidencia de cáncer orofaríngeo positivo al VPH introduciendo la vacunación que incluye los tipos 16 y 18 del VPH, presentes en el 95% de estos cánceres, antes de la exposición al virus. Los primeros datos sugieren una reducción de las tasas de infección.
En el pasado, el tratamiento del OPC era la cirugía radical, con un abordaje a través del cuello y la división del hueso maxilar , lo que resultó en morbilidad y bajas tasas de supervivencia. Más tarde, la radioterapia con o sin la adición de quimioterapia , proporcionó una alternativa menos desfigurante, pero con resultados comparables. Ahora, las técnicas quirúrgicas mínimamente invasivas más nuevas a través de la boca han mejorado los resultados; en casos de alto riesgo, esta cirugía a menudo se sigue de radiación y/o quimioterapia. En ausencia de evidencia de alta calidad con respecto a qué tratamiento proporciona los mejores resultados, las decisiones de manejo a menudo se basan en uno o más de los siguientes: factores técnicos, probable pérdida funcional y preferencia del paciente. La presencia de VPH en el tumor se asocia con una mejor respuesta al tratamiento y un mejor resultado, independientemente de los métodos de tratamiento utilizados, y una reducción de casi el 60% del riesgo de morir por cáncer. La mayoría de las recurrencias se producen localmente y dentro del primer año después del tratamiento. El uso de tabaco disminuye las posibilidades de supervivencia.
Signos y síntomas
El HPV+OPC se presenta de una de cuatro maneras: como una anomalía asintomática en la boca detectada por el paciente o un profesional de la salud como un dentista; con síntomas locales como dolor o infección en el sitio del tumor; con dificultades para hablar, tragar y/o respirar; o como una hinchazón en el cuello (si el cáncer se ha propagado a los ganglios linfáticos). Estos pueden estar acompañados de síntomas más generales como pérdida de apetito, pérdida de peso y debilidad. [3]
Causa
_EM_(new_version).jpg/440px-Papilloma_Virus_(HPV)_EM_(new_version).jpg)
La mayoría de los cánceres de células escamosas de cabeza y cuello de las mucosas , incluido el cáncer orofaríngeo (OPC), se han atribuido históricamente al consumo de tabaco y alcohol. Sin embargo, este patrón ha cambiado considerablemente desde la década de 1980. Se advirtió que algunos cánceres ocurren en ausencia de estos factores de riesgo y una asociación entre el virus del papiloma humano (VPH) y varios cánceres de células escamosas, incluido el OPC, se describió por primera vez en 1983. [4] [5] Desde entonces , se han acumulado evidencias tanto moleculares como epidemiológicas , y la Agencia Internacional para la Investigación sobre el Cáncer (IARC) declaró que los tipos 16 y 18 de VPH de alto riesgo son cancerígenos en humanos, en 1995, [6] y en 2007 que el VPH era una causa de cánceres orales. [7] [8] La incidencia de cáncer positivo al virus del papiloma humano (VPH) (VPH+OPC) ha aumentado, mientras que la incidencia de cáncer negativo al VPH (VPH-OPC) está disminuyendo, una tendencia que se estima que aumentará aún más en los próximos años. [9] Dado que existen marcadas diferencias en la presentación clínica y el tratamiento en relación con el estado del VPH, el VPH+OPC ahora se considera una condición biológica y clínica distinta. [10] [11] [12]
El VPH humano ha estado implicado durante mucho tiempo en la patogénesis de varios cánceres anogenitales, incluidos los de ano , vulva , vagina , cuello uterino y pene . [13] En 2007, también se lo implicó, mediante evidencia molecular y epidemiológica, en cánceres que surgen fuera del tracto anogenital, a saber, cánceres orales. La infección por VPH es común entre individuos sanos y se adquiere a través del sexo oral . Aunque hay menos datos disponibles, la prevalencia de la infección por VPH es al menos tan común entre hombres como entre mujeres, con estimaciones de 2004 de alrededor del 27% entre mujeres estadounidenses de 14 a 59 años. [8]
La infección oral por VPH precede al desarrollo de OPC VPH+. [8] [5] Las lesiones leves en la membrana mucosa sirven como puerta de entrada para el VPH, que así trabaja en la capa basal del epitelio . [14] [15] Las personas que dan positivo en la prueba de infección oral por el virus VPH tipo 16 (VPH16) tienen un riesgo 14 veces mayor de desarrollar OPC VPH+. [14] La inmunosupresión parece ser un factor de riesgo aumentado para OPC VPH+. [5] Los individuos con variaciones genéticas de TGF-β1 , especialmente T869C, tienen más probabilidades de tener OPC VPH16+. [16] El TGF-β1 juega un papel importante en el control del sistema inmunológico. En 1993 se observó que los pacientes con cánceres anogenitales asociados al virus del papiloma humano (VPH) tenían un riesgo 4 veces mayor de carcinoma de células escamosas amigdalino. [17] Aunque la evidencia sugiere que el VPH16 es la principal causa de OPC en humanos no expuestos al tabaco y al alcohol, el grado en el que el uso de tabaco y/o alcohol puede contribuir a aumentar el riesgo de OPC HPV+ no siempre ha sido claro [5] pero parece que tanto el tabaquismo como la infección por VPH son factores de riesgo independientes y aditivos para desarrollar OPC. [18] La conexión entre la infección por VPH y el cáncer orofaríngeo es más fuerte en las regiones de tejido linfoepitelial (base de la lengua y amígdalas palatinas) que en las regiones de epitelio escamoso estratificado (paladar blando y úvula). [19] La infección por el virus del herpes humano-8 puede potenciar los efectos del VPH-16. [20]
Factores de riesgo
Los factores de riesgo incluyen un alto número de parejas sexuales (aumento del 25% >= 6 parejas), antecedentes de sexo oral-genital (125% >= 4 parejas) o sexo anal-oral , una pareja femenina con antecedentes de una prueba de Papanicolaou anormal o displasia cervical , [21] periodontitis crónica , [22] [23] y, entre los hombres, disminución de la edad de la primera relación sexual y antecedentes de verrugas genitales . [24] [25] [26] [27]
Patología

Los cánceres de la orofaringe surgen principalmente en el tejido linfoide de las amígdalas linguales y palatinas , que está revestido por epitelio mucoso escamoso respiratorio, que puede estar invaginado dentro del tejido linfoide. Por lo tanto, el tumor surge primero en criptas ocultas. El OPC se clasifica en función del grado de diferenciación escamosa y de queratina en grados bien, moderados o pobremente diferenciados (alto). Otras características patológicas incluyen la presencia de invasión en forma de dedo, invasión perineural , profundidad de invasión y distancia del tumor desde los márgenes de resección. Las variantes fenotípicas incluyen carcinoma escamoso basaloide , una forma de alto grado ( ver Chung Fig. 35-3(C) [28] e ilustración aquí). Lo más común es que no sean queratinizantes. El OPC HPV+ también se diferencia del OPC HPV- en que es focal en lugar de multifocal y no está asociado con displasia premaligna . Por lo tanto, los pacientes HPV+OPC tienen un menor riesgo de desarrollar otras neoplasias malignas en la región de cabeza y cuello, a diferencia de otros tumores primarios de cabeza y cuello que pueden tener segundas neoplasias asociadas, que pueden ocurrir al mismo tiempo (sincrónicas) o en un momento distante (metacrónicas), tanto dentro de la región de cabeza y cuello como más distantes. Esto sugiere que las alteraciones oncogénicas producidas por el virus están limitadas espacialmente en lugar de estar relacionadas con un defecto de campo. [29] [28] [30]
Anatomía
La orofaringe , en la parte posterior de la boca , forma un círculo e incluye la base de la lengua (tercio posterior) por debajo, las amígdalas a cada lado y el paladar blando por encima, junto con las paredes de la faringe , incluida la epiglotis anterior , las valléculas epiglóticas y la hendidura branquial en su base. La orofaringe es una de las tres divisiones del interior de la faringe según su relación con las estructuras adyacentes (faringe nasal ( nasofaringe ), faringe oral (orofaringe) y faringe laríngea ( laringofaringe , también conocida como hipofaringe), de arriba a abajo). La faringe es un tubo fibromuscular semicircular que une las cavidades nasales por encima con la laringe (caja de la voz) y el esófago (garganta), por debajo, donde la laringe está situada delante del esófago. [31]
La orofaringe se encuentra entre la boca (cavidad bucal) por delante, y la laringofaringe por debajo, que la separa de la laringe. El límite superior de la orofaringe está marcado por el paladar blando, y su límite inferior por la epiglotis y la raíz de la lengua. La orofaringe se comunica con la boca, por delante a través de lo que se conoce como istmo orofaríngeo, o istmo de las fauces . El istmo (es decir, la conexión) está formado por encima por el paladar blando, por debajo por el tercio posterior de la lengua, y a los lados por los arcos palatoglosos . El tercio posterior de la lengua, o base de la lengua, contiene numerosos folículos de tejido linfático que forman las amígdalas linguales . Adyacente a la base de la lengua, la superficie lingual de la epiglotis, que se curva hacia delante, está unida a la lengua por los pliegues glosoepiglóticos medio y lateral . Los pliegues forman pequeños surcos conocidos como valéculas epiglóticas. Las paredes laterales están marcadas por dos pilares verticales a cada lado, los pilares de las fauces o arcos palatoglosos. Más apropiadamente se los llama por separado arco palatogloso anteriormente y arco palatofaríngeo posteriormente. El arco anterior recibe su nombre del músculo palatogloso que se encuentra en su interior, que va desde el paladar blando hasta la lengua ( gloso ), mientras que el arco posterior contiene de manera similar el músculo palatofaríngeo que va desde el paladar blando hasta la faringe lateral. Entre los arcos se encuentra un espacio triangular, la fosa amigdalina, en la que se encuentra la amígdala palatina , otro órgano linfoide. [32]
Las paredes faríngeas externas, formadas por los cuatro músculos constrictores, forman parte del mecanismo de la deglución . La anatomía microscópica se compone de cuatro capas, que son, desde el lumen hacia afuera, la mucosa , la submucosa , los músculos y la fibrosa o capa fibrosa. La mucosa está formada por epitelio escamoso estratificado, que generalmente no está queratinizado, excepto cuando está expuesto a irritantes crónicos como el humo del tabaco. La submucosa contiene agregados de tejido linfoide. [32] [33]
Patrones de propagación
Los cánceres que surgen en la fosa amigdalina se propagan a los ganglios linfáticos cervicales , principalmente a los ganglios linfáticos subdigástricos (yugulares superiores) (nivel II), con afectación secundaria de los ganglios yugulares medios (nivel III) e inferiores (nivel IV) y, a veces, de los ganglios cervicales posteriores (nivel V). Los cánceres de la base de la lengua se propagan a los ganglios subdigástricos y yugulares medios, y ocasionalmente a los ganglios cervicales posteriores, pero al estar más cerca de la línea media, es más probable que presenten enfermedad ganglionar bilateral. Los cánceres amigdalinos rara vez se propagan al lado contralateral, a menos que afecten la línea media. [34]
Mecanismo
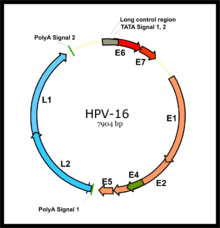
Virología
Los cánceres asociados al VPH son causados por cepas de alto riesgo del VPH, principalmente el VPH-16 y el VPH-18. [35] El VPH es un pequeño virus de ADN sin envoltura de la familia del virus del papiloma . Su genoma codifica las oncoproteínas tempranas (E) E5, E6 y E7 y las proteínas tardías (L) de la cápside L1 y L2. El virus accede a la mucosa a través de microlesiones, donde infecta la capa basal de células, que aún pueden proliferar. Si bien el virus no se replica en estas células, la expresión de sus genes tempranos estimula la proliferación y la expansión lateral de las células basales. A medida que esto mueve las partículas del virus hacia las capas suprabasales suprayacentes, se produce la expresión tardía del gen viral, lo que permite la replicación del genoma viral circular ( ver figura) y las proteínas estructurales. A medida que estos son empujados hacia las capas mucosas más superficiales, las partículas virales completas se ensamblan y liberan. [36]
Oncogénesis
Se observa un mayor riesgo de HPV+OPC más de 15 años después de la exposición al HPV, [8] lo que indica un desarrollo lento de la enfermedad, similar al observado en el cáncer de cuello uterino. En relación con HPV-OPC, la progresión molecular oncogénica de HPV+OPC es poco conocida. [28] Las dos principales oncoproteínas virales de los tipos de HPV de alto riesgo son E6 y E7. Estas se expresan consistentemente en líneas celulares malignas, y si su expresión se inhibe, el fenotipo maligno de las células cancerosas se bloquea. Cualquiera de estas oncoproteínas puede inmortalizar líneas celulares, [37] pero son más eficientes cuando se expresan ambas, ya que sus funciones moleculares separadas son sinérgicas . [35] [36] Los oncogenes E6 y E7 se integran en el ADN de la célula huésped, y las oncoproteínas que expresan interfieren con una variedad de mecanismos reguladores celulares predominantemente antiproliferativos . Se unen a los mecanismos más conocidos, las proteínas supresoras de tumores p53 y la proteína del retinoblastoma pRB (pRb), y los inactivan, lo que conduce a la inestabilidad genómica y luego a la desregulación del ciclo celular ( véase Chung et al., 2016, figura 35.2). [28] Además, se requieren mecanismos aún por determinar para los pasos finales de la transformación maligna de las células infectadas por el VPH. [28]
El HPV- y el HPV+OPC se pueden distinguir a nivel molecular. El p53 natural ( tipo salvaje ) está ampliamente involucrado en procesos celulares , incluyendo la autofagia , la respuesta al daño del ADN, la regulación del ciclo celular y la senescencia , la apoptosis y la generación de trifosfato de adenosina (ATP) a través de la fosforilación oxidativa . [38] El gen que codifica p53 es inactivado por E6 a nivel proteico y se encuentra como el tipo salvaje en HPV+OPC pero mutado en HPV-OPC. En HPV+OPC la proteína p53 sufre una degradación acelerada por E6, reduciendo drásticamente sus niveles, mientras que en HPV-OPC sufre una mutación genética , que puede resultar en la síntesis de una proteína p53 anormal, que no solo puede ser inactiva como supresor tumoral, sino que también puede unirse e inactivar cualquier p53 de tipo salvaje no mutado, con un aumento de la actividad oncogénica. [39] Aunque las mutaciones de p53 ocurren en el HPV+OPC, son mucho menos comunes que en el HPV-OPC (26% vs 48%) y no parecen afectar el resultado clínico. [40]
La proteína pRb es inactivada por E7 en HPV+OPC, pero en HPV-OPC es la parte supresora de tumores p16 de la red supresora de tumores pRb la que es inactivada. También la vía pRb es inactivada por E7 en lugar de la amplificación de Ciclina D1 . [8] [41] CDKN2A es un gen supresor de tumores que codifica una proteína supresora de tumores, p16 (inhibidor de la quinasa dependiente de ciclina 2A) e inhibe la actividad quinasa de las quinasas dependientes de ciclina CDK4 y CDK6 , que a su vez inducen la detención del ciclo celular. [38] La expresión de p16 depende del ciclo celular y se expresa focalmente en solo alrededor del 5-10% del epitelio escamoso normal. Al igual que la mayoría de los cánceres HPV+, las células OPC HPV+ expresan p16, pero esta última no funciona como un supresor tumoral, porque el mecanismo por el cual esto se logra, pRb, ha sido inactivado por E7. p16 se regula al alza (sobreexpresado) debido a la pérdida de pRB relacionada con E7 con retroalimentación negativa reducida, [39] [42] mientras que se regula a la baja en hasta el 90% de las células OPC HPV-. [43] Esta sobreexpresión difusa en las células tumorales proporciona un marcador diagnóstico para la participación del VPH. [44] [45] Aunque las células E6 y E7 del VPH reducen la actividad supresora tumoral, lo hacen menos que los procesos genéticos y epigenéticos en las células OPC HPV-. [46] [47] [11]
Los epitelios amigdalinos ( palatino y lingual ) comparten características similares de no queratinización con el cuello uterino , donde la infección por VPH desempeña el papel principal en los casos de cáncer de cuello uterino . [14] [48] Además, E6 y E7 pueden hacer que el OPC HPV+ sea más inmunogénico que el OPC HPV-, ya que se pueden detectar anticuerpos anti-E6 y E7 en estos pacientes. Esto a su vez podría restringir el comportamiento maligno del OPC HPV+ y la presencia de anticuerpos se ha asociado con un mejor pronóstico, mientras que el tratamiento puede mejorar la inmunogenicidad del tumor y, por lo tanto, mejorar la respuesta, aunque no está claro en qué medida. [49] [11] Los resultados también se asocian con una mejor inmunidad adaptativa . [50]
Diagnóstico


Biopsia
El diagnóstico inicial requiere la visualización del tumor a través de la boca o endoscópicamente a través de la nariz utilizando un rinoscopio , ilustrado a la derecha, seguido de una biopsia . [ cita requerida ]
Diferenciación entre HPV+OPC y HPV-OPC
El HPV+OPC suele diagnosticarse en una etapa más avanzada que el HPV-OPC, [8] con un 75-90% con afectación de ganglios linfáticos regionales. [51] Además, es más probable que el HPV+OPC esté poco diferenciado con células no queratinizadas o basaloides. [52] [53] [54]
Las firmas genéticas de OPC HPV+ y HPV- son diferentes. [55] [56] [57] [58] [59] El OPC HPV+ está asociado con el nivel de expresión de los ARNm E6/E7 y de p16 . [60] Los casos HPV16 E6/E7-positivos se caracterizan histopatológicamente por su estructura verrugosa o papilar ( similar a un pezón ) y coilocitosis de la mucosa adyacente. Aproximadamente el 15% de los HNSCC son causados por la infección HPV16 y la posterior expresión constitutiva de E6 y E7, y algunos tumores iniciados por HPV pueden perder sus características originales durante la progresión del tumor . [61] Los tipos de HPV de alto riesgo pueden estar asociados con el carcinoma oral, por la desregulación del control del ciclo celular , contribuyendo a la carcinogénesis oral y la sobreexpresión de mdm2, p27 y catepsina B. [62]
El HPV+OPC no se caracteriza únicamente por la presencia de HPV-16: solo la expresión de oncogenes virales dentro de las células tumorales más la presencia sérica de anticuerpos E6 o E7 es inequívocamente concluyente para el HPV+OPC. [14]
No existe un método estándar de prueba de VPH en cánceres de cabeza y cuello, [63] tanto la hibridación in situ (ISH) como la reacción en cadena de la polimerasa (PCR) se utilizan comúnmente. [44] [64] Ambos métodos tienen un rendimiento comparable para la detección de VPH, sin embargo, es importante utilizar controles de sensibilidad adecuados . [65] La tinción inmunohistoquímica (IHC) del tejido para p16 se utiliza con frecuencia como un sustituto rentable para el VPH en OPC, en comparación con ISH o PCR [66] [67] [68] pero hay una pequeña incidencia de enfermedad p16 positiva-negativa-VPH que representa aproximadamente el 5% de OPC-VPH. [66]
Puesta en escena
La estadificación se realiza generalmente mediante el sistema TNM (tumor, ganglios linfáticos, metástasis) de la UICC / AJCC . [68] La estadificación se basa en el examen clínico , el diagnóstico por imágenes y la patología. En las imágenes, los ganglios linfáticos afectados pueden parecer quísticos , una característica del HPV+OPC. [69]
El OPC HPV+ se ha tratado de manera similar al OPC no relacionado con el VPH con estadio y sitio coincidentes, pero sus características únicas, que contrastan con los cánceres de cabeza y cuello HPV-OPC relacionados con el tabaquismo, para los cuales la demografía, las comorbilidades, los factores de riesgo y la carcinogénesis de los pacientes difieren notablemente, sugieren que se desarrolle un sistema de estadificación distinto para representar de manera más apropiada la gravedad de la enfermedad y su pronóstico. [70] La estadificación TNM estándar del AJCC, como la séptima edición (2009) [71] , si bien es predictiva para el OPC HPV-OPC, no tiene valor pronóstico en el OPC HPV+. [72] [73] [67] [70] La octava edición del Manual de estadificación TNM del AJCC (2016) [74] incorpora esta estadificación específica para el OPC HPV+. [75] A partir de 2018, las pautas de tratamiento están evolucionando para tener en cuenta los diferentes resultados observados en el OPC HPV+. En consecuencia, se está investigando un uso menos intensivo (desintensificación) de radioterapia o quimioterapia, [76] así como una terapia específica, inscribiendo HPV+OPC en ensayos clínicos para preservar el control de la enfermedad y minimizar la morbilidad en grupos seleccionados según la estadificación TNM modificada y el estado de tabaquismo. [77] [78] [79] [80] [81]
El cáncer de orofaringe HPV+ se clasifica como (AJCC 8.ª ed. 2016): [75] Estadio del tumor
- T0 no se identificó ningún primario
- T1 2 cm o menos en su mayor dimensión
- T2 2–4 cm
- T3 >4 cm, o extensión a la superficie lingual de la epiglotis
- Enfermedad local moderadamente avanzada T4, que invade la laringe, el músculo extrínseco de la lengua, el pterigoideo medial, el paladar duro o la mandíbula o más allá
Etapa nodal
- No se pueden evaluar los ganglios linfáticos regionales Nx
- N0 no hay ganglios linfáticos regionales afectados
- N1 uno o más ganglios ipsilaterales afectados, de menos de 6 cm
- N2 ganglios linfáticos contralaterales o bilaterales, menores de 6 cm
- Ganglio(s) linfático(s) N3 mayores de 6 cm
Estadio clínico
- Estadio I: T0N1, T1–2N0–1
- Estadio II: T0N2, T1–3N2, T3N0–2
- Estadio III: T0–3N3, T4N0-3
- Estadio IV: cualquier metástasis (M1)
Sin embargo, la literatura publicada y los ensayos clínicos en curso utilizan la séptima edición anterior que no distingue entre HPV+OPC y HPV-OPC – ver Cáncer orofaríngeo – Estadios . [82] [83] Los estadios T son esencialmente similares entre AJCC 7 y AJCC 8, con dos excepciones. Tis ( carcinoma in situ ) se ha eliminado y la división de T4 en subestadios (p. ej., T4a) se ha eliminado. Los principales cambios están en los estadios N y, por lo tanto, en el estadio clínico general. N0 sigue siendo el mismo, pero al igual que con el estadio T, se han eliminado los subestadios como N2a. La extensión extracapsular (ECE), también conocida como extensión extranodal (ENE), que es la invasión del tumor más allá de la cápsula del ganglio linfático, se ha eliminado como criterio de estadificación. [a]
Esto hace que un tumor HPV+OPC reciba una etapa más baja que si fuera HPV-OPC. Por ejemplo, un tumor de 5 cm con un ganglio ipsilateral afectado que mide 5 cm pero tiene ECE se consideraría T3N3bM0 Etapa IVB si es HPV-, pero T3N1M0 Etapa II si es HPV+. [75]
Prevención

Evitar la exposición
La prevención del VPH+OPC implica evitar o reducir la exposición a los factores de riesgo siempre que sea posible. [ cita requerida ]
Vacunación
Alrededor del 90% de los pacientes con VPH+OPC son portadores del virus de papiloma humano tipo 16 y otro 5% del tipo 18. Estos dos tipos son el objetivo de las vacunas disponibles. Las vacunas contra el VPH administradas antes de la exposición pueden prevenir la infección genital persistente y el estado precanceroso consecuente. [11] Por lo tanto, tienen un potencial teórico para prevenir la infección oral por VPH. [8] Un estudio de revisión de 2010 encontró que la infección oral por VPH16 era rara (1,3%) entre los 3.977 sujetos sanos analizados. [84]
Tratamiento
Los objetivos del tratamiento son optimizar la supervivencia y el control locoregional de la enfermedad, y prevenir la propagación a áreas distantes del cuerpo ( metástasis ), mientras se minimiza la morbilidad a corto y largo plazo . [85] No hay evidencia de Nivel I de alta calidad de ensayos clínicos prospectivos en HPV+OPC, por lo tanto, las pautas de tratamiento deben basarse en datos del tratamiento de OPC en general y de algún subconjunto retrospectivo no planificado de esos estudios, junto con datos para cáncer de cabeza y cuello en general. [68] El tratamiento para OPC tradicionalmente se ha basado en radioterapia , quimioterapia y/u otros tratamientos sistémicos, y resección quirúrgica. Dependiendo del estadio y otros factores, el tratamiento puede incluir una combinación de modalidades . [86] El pilar ha sido la radioterapia en la mayoría de los casos. [67] un análisis agrupado de estudios publicados sugirió un control de la enfermedad comparable entre la radiación y la cirugía, pero tasas de complicaciones más altas para la cirugía +/− radiación. [86] [87] Lo ideal es un enfoque de modalidad única, ya que la modalidad triple se asocia con mucha más toxicidad, y se recomienda un equipo multidisciplinario en un centro grande con un gran volumen de pacientes. [68] [88] [12]
Las diferencias en la respuesta al tratamiento entre HPV-OPC y HPV+OPC pueden incluir diferencias en la extensión y manera en que se alteran las vías de regulación del crecimiento celular en las dos formas de OPC. Por ejemplo, en HPV+OPC, los oncogenes HPV E6 y E7 simplemente vuelven latentes las vías p53 y pRb, dejando abierta la posibilidad de reactivación de estas vías mediante la regulación negativa (reducción) de la expresión de los oncogenes. Esto contrasta con la forma mutante de p53 encontrada en HPV-OPC que está asociada con la resistencia al tratamiento. [11] Además, se sugiere que los efectos de E6 y E7 en estas vías hacen que el tumor sea más radiosensible, posiblemente por interferencia con mecanismos como la reparación del ADN , la señalización de repoblación y la redistribución del ciclo celular. [89] [90] El microambiente también es importante, ya que la radiación aumenta la respuesta inmunitaria del huésped a los antígenos virales expresados en el tumor. [50] [49] Además, existe una asociación entre un aumento de los linfocitos infiltrantes de tumores y de los glóbulos blancos circulantes en pacientes con OPC por VPH+ y un mejor pronóstico. Esto implica un papel del sistema inmunitario adaptativo en la supresión de la progresión tumoral . [91] [92] [90]
Cirugía
Históricamente, la cirugía era el único abordaje para el cáncer de cabeza y cuello. El manejo quirúrgico del OPC conllevaba una morbilidad significativa con un abordaje transcervical (a través del cuello), que a menudo implicaba una mandibulotomía, en la que se divide el hueso maxilar ( mandíbula ). Esto se conoce como una técnica quirúrgica abierta. En consecuencia, los abordajes quirúrgicos declinaron en favor de la radiación. En los Estados Unidos, el uso de la cirugía disminuyó del 41% de los casos en 1998 al 30% en 2009, año en que la Administración de Alimentos y Medicamentos aprobó el uso de las técnicas más nuevas. [93]
Estas mejoras en las técnicas quirúrgicas han permitido que muchos tumores se resequen (eliminen) mediante abordajes quirúrgicos transorales (a través de la boca) (TOS), utilizando cirugía endoscópica transoral de cabeza y cuello (HNS). [94] En consecuencia, la cirugía se utilizó más, aumentando al 35% de los casos en 2012. [93] Este enfoque ha demostrado seguridad, eficacia y tolerabilidad, e incluye dos técnicas mínimamente invasivas principales, cirugía robótica transoral (TORS) [95] [96 ] [97 ] [98] [99] [100] y microcirugía láser transoral (TLM). [101] [102] [103] No se han realizado comparaciones directas de estas dos técnicas, y los ensayos clínicos en cáncer de cabeza y cuello como ECOG 3311 permiten cualquiera de las dos. Se asocian con una morbilidad postoperatoria sustancial, dependiendo de la extensión de la resección, pero en comparación con las técnicas más antiguas, tienen una estancia hospitalaria más corta, una recuperación más rápida, menos dolor y menos necesidad de gastrostomía o traqueotomía , y menos efectos a largo plazo, que son mínimos en ausencia de radiación postoperatoria (RT) o quimiorradiación (CRT). [104] [105] La TORS tiene la ventaja práctica de que los telescopios en ángulo y los brazos quirúrgicos robóticos giratorios proporcionan una mejor línea de visión. Los resultados de los procedimientos mínimamente invasivos también se comparan favorablemente con los más invasivos. En la enfermedad en etapa temprana, incluida la afectación de los ganglios del cuello, la TORS produce una supervivencia a los 2 años del 80-90%. [106] De manera similar, se informa que la TLM tiene una supervivencia a cinco años del 78% y tasas de control local del 85-97%. [107] [108] Además de la enfermedad temprana, la cirugía mínimamente invasiva se ha utilizado en casos avanzados, con hasta un 90% de control local y supervivencia específica de la enfermedad. [95] [108] La deglución posoperatoria fue excelente en el 87%, pero la disfagia a largo plazo se asoció con cánceres más grandes (T4), especialmente si afectaban la base de la lengua. [108] [12]
Los detalles del abordaje quirúrgico dependen de la ubicación y el tamaño del tumor primario y su estadio N. La disección del cuello para examinar los ganglios linfáticos de drenaje se puede realizar simultáneamente o como un segundo procedimiento de estadificación. Para los tumores de la amígdala y la pared faríngea lateral, y la enfermedad clínicamente no relacionada con los ganglios linfáticos (N0), la disección del cuello generalmente involucra los niveles 2 a 4 ( ver diagrama en Dubner 2017 ) ipsilateralmente . Cuando los ganglios están clínicamente involucrados, la disección dependerá de la ubicación y el tamaño del ganglio o ganglios. En el caso de los tumores primarios de la base de la lengua, cerca de la línea media , se recomienda la disección bilateral. [12]
Estadificación patológica
Una ventaja de un abordaje quirúrgico primario es la cantidad de información patológica disponible, incluyendo grado, estado del margen y grado de afectación de los ganglios linfáticos. Esto puede cambiar la estadificación, ya que hasta el 40% de los pacientes pueden tener un estadio patológico posoperatorio diferente en comparación con su estadio clínico preoperatorio. En un estudio, al 24% se le redujo el estadio (downstaged), lo que puede afectar la toma de decisiones posterior, incluida la reducción de la intensidad y la morbilidad. [109] [12] En el Reino Unido, el Royal College of Pathologists (1998) [110] [b] ha estandarizado el informe de los márgenes quirúrgicos, con dos categorías, "mucoso" y "profundo", y para cada uno creó grupos basados en la distancia microscópica desde el cáncer invasivo hasta el margen, de la siguiente manera: más de 5 mm (limpio), 1–5 mm (cercano) y menos de 1 mm (afectado). [111]
Terapia postoperatoria adyuvante
Los datos sobre el uso de radioterapia postoperatoria (PORT) se limitan en gran medida a estudios históricos o retrospectivos en lugar de ensayos clínicos aleatorizados de alta calidad y se basan en la población general de pacientes con cáncer de cabeza y cuello, en lugar de estudios específicos de HPV + OPC, que habrían formado una proporción muy pequeña de la población estudiada. [12] A pesar de la escisión quirúrgica, en los casos más avanzados, la recurrencia local y regional del cáncer, junto con la propagación fuera de la región de cabeza y cuello ( metástasis ) son frecuentes. El riesgo de enfermedad recurrente posterior se ha considerado más alto en aquellos tumores donde la patología muestra tumor en los márgenes de la resección (márgenes positivos), múltiples ganglios linfáticos regionales afectados y extensión del tumor fuera de la cápsula del ganglio linfático (extensión extracapsular), según la experiencia histórica con el cáncer de cabeza y cuello. [112] PORT se introdujo en la década de 1950 en un intento de reducir el fracaso del tratamiento de la cirugía sola. [113] Aunque nunca se probó en un entorno controlado, PORT ha sido ampliamente adoptado para este propósito. [114] En un análisis del fracaso del tratamiento quirúrgico en el Memorial Sloan-Kettering Cancer Center , los pacientes tratados solo con cirugía entre 1960 y 1970 tuvieron tasas de fracaso del 39 y 73% para aquellos con márgenes quirúrgicos negativos y positivos respectivamente. Estos se compararon con aquellos que recibieron PORT (con o sin quimioterapia) de 1975 a 1980. El último grupo tuvo tasas de fracaso más bajas del 2% y 11% respectivamente. [115] Además, un estudio aleatorizado de la década de 1970 (RTOG 73–03) comparó la radiación preoperatoria con PORT, y encontró tasas de fracaso más bajas con este último. [114] [116]
La adición de otra modalidad de tratamiento se denomina terapia adyuvante (que literalmente ayuda), en comparación con su uso como terapia inicial (primaria), también conocida como terapia radical. En consecuencia, muchos de estos pacientes han sido tratados con radiación adyuvante, con o sin quimioterapia. En la serie de informes anteriores de cirugía mínimamente invasiva, muchos pacientes (30-80%) recibieron radiación adyuvante. Sin embargo, los resultados funcionales fueron peores si se agregó radiación a la cirugía y peores si se utilizaron tanto radiación como quimioterapia. [12] La dosis de radiación ha seguido en gran medida la derivada para todos los cánceres de cabeza y cuello, en este contexto, en función del riesgo. Históricamente, solo un ensayo clínico aleatorizado ha abordado la dosis óptima, asignó a los pacientes a dos niveles de dosis, estratificados por riesgo, pero no mostró diferencias en el control del cáncer entre las dosis bajas y altas (63 y 68,4 Gy), pero sí una mayor incidencia de complicaciones en las dosis más altas. En consecuencia, se recomendó la dosis más baja de 57,6 Gy . [117] [118] Debido a que los autores utilizaron un esquema de fraccionamiento de 1,8 Gy por tratamiento, esta dosis no fue ampliamente adoptada, los médicos prefirieron una fracción mayor de 2 Gy para producir un tiempo de tratamiento más corto, y una dosis ligeramente mayor de 60 Gy en fracciones de 2 Gy (30 tratamientos diarios). [41] Sin embargo, 57,6 Gy en fracciones de 1,8 Gy es equivalente (dosis isoefectiva) a solo 56 Gy en fracciones de 2 Gy. [119] 60 Gy corresponde a los 63 Gy utilizados como dosis baja en el grupo de alto riesgo. 60 Gy también fue la dosis utilizada en RTOG 73–03. Posteriormente, hubo una tendencia a intensificar el tratamiento en el cáncer de cabeza y cuello, y varios centros adoptaron una dosis de 66 Gy, al menos para aquellos pacientes con características tumorales adversas. [120] La efectividad de PORT en HPV+OPC recibe cierto respaldo de un estudio de cohorte (Nivel 2b), aunque el número de pacientes fue bajo y el número de eventos (enfermedad recurrente o muerte) solo del 7%. [121] Otro estudio retrospectivo a nivel de población (Nivel 4) de la base de datos SEER (1998-2011) concluyó que hubo un efecto de supervivencia general pero no de supervivencia específica de la enfermedad de la radiación en 410 pacientes con un solo ganglio linfático afectado, pero utilizó solo un análisis estadístico univariado y no contenía información sobre el estado del VPH. [122] Un estudio posterior mucho más grande en una población similar en la Base de Datos Nacional del Cáncer (2004-2013) de más de 9000 pacientes encontró una ventaja de supervivencia pero esta fue solo en HPV-OPC, no en 410 pacientes HPV+OPC, [123] y un estudio posterior de 2500 pacientes HPV+OPC de riesgo bajo e intermedio mostró una supervivencia general similar independientemente de si se administró PORT o no. [124]
Desintensificación
Aunque se han completado menos estudios que examinan la desintensificación (desescalada) en este entorno, que en la radiación radical primaria para este cáncer (ver a continuación), es un área de investigación activa. [125] En un estudio de una sola institución, se tomó la decisión de reducir la dosis de radiación en pacientes de alto riesgo con HPV+OPC de 66 a 60 Gy, lo que corresponde a la evidencia real, y el seguimiento no ha mostrado una disminución en el control del cáncer. [120] Los ensayos actuales, tanto en América del Norte como en Europa (como ECOG 3311 [c] y PATHOS [d] ) utilizan 50 Gy como brazo de comparación. [127] El comparador de 50 Gy se eligió sobre la base de (i) la exquisita sensibilidad de HPV+OPC a la radiación, tanto in vitro como in vivo ; ECOG 1308 que muestra un excelente control de la enfermedad a 54 Gy; y datos [128] que sugieren que 50 Gy en 1,43 Gy (dosis isoefectiva 43 Gy en 2,0 Gy) fue suficiente para tratar electivamente el cuello. [126] Otros estudios, como MC1273 y DART-HPV han evaluado dosis tan bajas como 30-36 Gy. [129] La reducción de la dosis de radiación a 54 Gy fue identificada como uno de los avances clínicos importantes en cáncer de 2018 por la Sociedad Estadounidense de Oncología Clínica , bajo el tema general de "Menos es más: preservar la calidad de vida con menos tratamiento". [130] La quimioterapia se ha utilizado simultáneamente con la radiación en este entorno, como en el tratamiento primario con radiación radical, particularmente donde las características patológicas indicaban un mayor riesgo de recurrencia del cáncer. Varios estudios han sugerido que esto no mejora el control local, aunque agrega toxicidad. [131]
Radioterapia

Las preocupaciones sobre la morbilidad asociada con la resección quirúrgica en bloque abierta tradicional llevaron a explorar enfoques alternativos con radiación. [121] La radioterapia de intensidad modulada ( IMRT ) puede proporcionar un buen control de los tumores primarios al mismo tiempo que preserva excelentes tasas de control, con una toxicidad reducida para las estructuras salivales y faríngeas en relación con la tecnología anterior. HPV+OPC ha demostrado una mayor sensibilidad a la radiación con una regresión más rápida, en comparación con HPV-OPC. [132] En general, la radiación se puede administrar de manera segura solo al lado afectado (ipsilateral), debido a la baja tasa de cáncer recurrente en el lado opuesto (contralateral) y una toxicidad significativamente menor en comparación con el tratamiento bilateral. [e] [134] [133] La IMRT tiene una supervivencia libre de enfermedad a dos años de entre el 82 y el 90%, y una supervivencia específica de la enfermedad a dos años de hasta el 97% para la etapa I y II. [135] [136]
Las toxicidades notificadas incluyen sequedad de boca ( xerostomía ) debido a daño en las glándulas salivales , 18% (grado 2); [f] dificultad para tragar ( disfagia ) debido a daño en los músculos constrictores, laringe y esfínter esofágico, 15% (grado 2); aspiración subclínica hasta 50% (incidencia notificada de neumonía por aspiración de aproximadamente 14%); hipotiroidismo 28–38% a los tres años (puede ser hasta 55% dependiendo de la cantidad de glándula tiroides expuesta a más de 45 Gy de radiación; estenosis esofágica 5%; osteonecrosis de la mandíbula 2,5%; y necesidad de colocar una sonda de gastrostomía en algún momento durante o hasta un año después del tratamiento 4% (hasta 16% con un seguimiento más prolongado). [12] [138] [136] [139] [140] Se han expresado inquietudes con respecto a la toxicidad excesiva a corto y largo plazo, especialmente disfagia y xerostomía, [141] [142] [143] y, por lo tanto, si las dosis estándar exponen a los pacientes con mejores pronósticos a un tratamiento excesivo y efectos secundarios innecesarios. [144] [90]
Dosimetría
La probabilidad de xerostomía al año aumenta un 5% por cada aumento de 1 Gy en la dosis a la glándula parótida . Las dosis superiores a 25-30 Gy se asocian con xerostomía moderada a severa. Consideraciones similares se aplican a la glándula submandibular , pero la xerostomía es menos común si solo se incluye una glándula parótida en el campo irradiado [145] y se preserva la glándula submandibular contralateral (menos de 39 Gy) [146] De la misma manera, la dosis de radiación a los músculos constrictores faríngeos , la laringe y la entrada cricofaríngea determinan el riesgo de disfagia (y, por lo tanto, la dependencia de la alimentación por sonda de gastrostomía ). El umbral para esta toxicidad depende del volumen a 55-60 Gy, [147] [148] [149] [90] con deterioro moderado a grave de la deglución, incluyendo aspiración, estenosis y dependencia de la sonda de alimentación por encima de una dosis media de 47 Gy, con una dosis recomendada para el constrictor inferior de menos de 41 Gy. [150] [151] Las relaciones dosis-toxicidad para los constrictores superior y medio son pronunciadas, con un aumento del 20% en la probabilidad de disfagia por cada 10 Gy. [152] Para la disfagia tardía, las dosis totales medias umbral de constrictor, para limitar las tasas mayores o iguales a grado 2 y 3 por debajo del 5% fueron 58 y 61 Gy respectivamente. Para la disfagia de grado 2, la tasa aumentó un 3,4% por Gy. [153] Las dosis superiores a 30 Gy para la tiroides se asocian con hipotiroidismo moderado a grave. [154] Los resultados subjetivos de calidad de vida informados por los pacientes también se correlacionan con la dosis de radiación recibida. [142]
Los esquemas de fraccionamiento modificados , como RTOG 9003 [g] [141] y RTOG 0129 [h] no han conferido un beneficio adicional. [155] [156] Las recomendaciones de dosis de radiación se determinaron en gran medida de manera empírica en estudios clínicos con pocos pacientes con HPV+OPC, y se han mantenido sin cambios durante medio siglo, [90] lo que dificulta determinar la dosis óptima para este subgrupo. Un enfoque común utiliza 70 Gy bilateralmente y anteriormente, como RTOG 9003 (1991-1997) [141] [155] y RTOG 0129 (2002-2005). [157] [156] Para el cáncer de amígdala lateralizado, generalmente se prescribe radiación unilateral en el cuello, pero para los primarios de la base de la lengua, la radiación bilateral en el cuello es más común, pero la radiación unilateral puede usarse cuando las lesiones de la base de la lengua están lateralizadas. [12]
Desintensificación
Se han expresado inquietudes con respecto a la toxicidad excesiva a corto y largo plazo, especialmente disfagia y xerostomía, [141] [142] [143] y, por lo tanto, si las dosis estándar exponen a los pacientes con mejores pronósticos a un tratamiento excesivo y efectos secundarios innecesarios. [144] [90] Las toxicidades actuales se han descrito como "no tolerables", [158] y, por lo tanto, un intenso interés en la desescalada. [127]
Aunque la comparación con controles históricos tiene un valor limitado en comparación con los ensayos clínicos aleatorizados ( fase III ), se han llevado a cabo estudios de fase II que utilizan dosis reducidas de radiación en comparación con el estándar histórico de 70 Gy. Un estudio que utilizó 54-60 Gy (una reducción del 15-20%, estratificada por respuesta a la quimioterapia de inducción inicial) demostró niveles comparables de control de la enfermedad con tasas de complicaciones mucho más bajas, [90] en comparación con estudios similares, utilizando 70 Gy, como ECOG 2399. [159] [160] El porcentaje de pacientes vivos después de 2 años fue del 95% con la dosis más alta y del 98% con la dosis más baja. De manera similar para el porcentaje libre de enfermedad (86 y 92%). Las toxicidades se redujeron en gran medida de una incidencia de disfagia y mucositis de grado 3 o mayor del 54 y 53% respectivamente, al 9%. Una menor incidencia y gravedad de la disfagia también significa que menos pacientes requieren alimentación por gastrostomía. [90] Se puede hacer una comparación similar con los datos agrupados de dos estudios RTOG que utilizaron 70 Gy (0129 y 0522). [161]
Aún no se han desarrollado nuevas pautas que aborden específicamente el HPV+OPC, fuera de los ensayos clínicos. Los datos indirectos sugieren la eficacia de un tratamiento menos intenso. Un análisis retrospectivo del HPV+OPC avanzado (N+) sugirió un control local del 96% a 5 años con radiación desintensificada de 54 Gy y quimioterapia concurrente basada en cisplatino . [162] Las conclusiones del par de ensayos de fase II similares anteriores han sido respaldadas por varios otros ensayos de fase II. Un ensayo prospectivo ( ECOG 1308) demostró un control locoregional similar con 54 Gy, [144] y otro estudio, una alta tasa de respuesta patológica completa a 60 Gy. [163] El ensayo Quarterback [i] mostró resultados comparables entre 56 y 70 Gy. [164] y fue seguido por Quarterback 2, comparando 50 a 56 Gy. [j] De manera similar, el ensayo Optima mostró un buen control de la enfermedad con dosis entre 45 y 50 Gy. [165] Estudios en curso, siguiendo la experiencia del ensayo de la Clínica Mayo (MC1273), [129] como el del Centro Oncológico Memorial Sloan Kettering están explorando dosis tan bajas como 30 Gy. [k] Todos estos estudios utilizaron dosis muy por debajo de la dosis estándar anterior de 70 Gy. Dado que la toxicidad a largo plazo está asociada con la dosis de radiación, determinar la eficacia de dosis de radiación más bajas y, por lo tanto, menos mórbidas es una prioridad, ya que se puede esperar que muchos pacientes HPV+ tengan una supervivencia a largo plazo. [12]
La radiación se utiliza comúnmente en combinación con quimioterapia, pero también puede usarse como una modalidad única, especialmente en etapas tempranas, por ejemplo, T1-T2, N0-1, y su uso en etapas posteriores se está explorando en ensayos clínicos como RTOG 1333 que compara la radiación sola con la radiación con quimioterapia reducida, en fumadores no fumadores o fumadores leves. [12]
Quimioterapia
Al igual que con los datos de radioterapia, la mayor parte del conocimiento disponible sobre la eficacia de la quimioterapia se deriva del tratamiento del cáncer avanzado de cabeza y cuello en lugar de estudios específicos de HPV + OPC. Desde 1976, muchos estudios clínicos han comparado la CRT con la RT sola en el tratamiento primario de cánceres de cabeza y cuello localmente avanzados y han demostrado una ventaja de la CRT tanto en la supervivencia como en el control locorregional. [166] [167] El cisplatino se considera el agente estándar, y se observó una ventaja de supervivencia para aquellos pacientes que recibieron radiación con cisplatino concurrente. [168] A pesar de esto, no se han realizado ensayos que comparen directamente el cisplatino con otros agentes en este contexto. El otro agente que se usa ampliamente es Cetuximab , un anticuerpo monoclonal dirigido al receptor del factor de crecimiento epidérmico (EGFR). Se observó una ventaja de supervivencia del 10% a los tres años cuando cetuximab se administró simultáneamente con radiación (biorradiación). [169] Los ensayos de cetuximab se completaron antes del conocimiento del estado del VPH. [170] Los estudios de laboratorio y clínicos sobre la utilidad de cetuximab en este contexto son contradictorios. La principal toxicidad es una erupción acneiforme , pero no se había comparado directamente con cisplatino en HPV+OPC, hasta que RTOG 1016 ( ver Discusión ) abordó esta cuestión. [12] [164] El análisis de los resultados tres años después de que se completó el ensayo demuestra que cetuximab es inferior al cisplatino. [171] La quimioterapia concurrente también es superior a la quimioterapia sola ( quimioterapia de inducción ) seguida de radiación. [166] [12] El cetuximab no muestra ninguna ventaja cuando se agrega al cisplatino en combinación con radiación. [143] Aunque la quimiorradiación se convirtió en un estándar de tratamiento basado en ensayos clínicos y, en particular, metaanálisis , un estudio posterior basado en la población de pacientes con OPC, no indicó ninguna ventaja en la adición de quimioterapia a la radiación ni en HPV+OPC ni en HPV-OPC, [172] y preocupaciones significativas sobre la toxicidad agregada. [173]
La quimioterapia también tiene un papel, combinada con la radiación, en el contexto postoperatorio (terapia adyuvante). [174] Generalmente se utiliza cuando la patología de la muestra resecada indica características asociadas con un alto riesgo de recurrencia locorregional (por ejemplo, extensión extracapsular a través de los ganglios linfáticos afectados o márgenes muy cercanos). Ha demostrado una mejor supervivencia libre de enfermedad y control locorregional en dos ensayos clínicos muy similares en pacientes de alto riesgo, EORTC 22931 (1994-2000) [112] y RTOG 9501 (1995-2000). [l] [m] [n] [175] [176] [177] Sin embargo, para los pacientes HPV+OPC, dicha propagación extracapsular no parece ser un factor adverso [178] [179] [180] y la adición de quimioterapia a la radiación en este grupo no proporcionó ninguna ventaja adicional. [179] Dado que el tamaño de la muestra para detectar una ventaja de supervivencia es grande, dada la pequeña cantidad de eventos en este grupo, estos estudios pueden haber tenido poca potencia y la cuestión de la utilidad de agregar quimioterapia se está abordando en un ensayo clínico aleatorizado (ADEPT) con control locoregional de dos años y supervivencia libre de enfermedad como punto final. [o] La adición de quimioterapia a la radiación aumenta la toxicidad aguda y tardía. En el ensayo GORTEC, la quimioterapia con docetaxel proporcionó una mejor supervivencia y control locoregional en OPC localmente avanzado, pero se asoció con un aumento de la mucositis y la necesidad de alimentación por gastrostomía. [181] La quimioterapia y la radiación se asocian con un riesgo de muerte del 3-4% en este contexto. [182] No está claro si la toxicidad agregada de agregar quimioterapia a la radiación se compensa con un beneficio clínico significativo en el control de la enfermedad y la supervivencia. [12]
Se cree que los pacientes con HPV+OPC se benefician más de la radioterapia y el tratamiento concurrente con cetuximab que los pacientes con HPV-OPC que reciben el mismo tratamiento, [183] y que la radiación y el cisplatino inducen una respuesta inmune contra un tumor antigénico que mejora su efecto sobre las células cancerosas. [49] Aunque la incidencia de positividad de HPV es baja (10-20%), se observó una ventaja para HPV+OPC en ensayos tanto de cetuximab como de panitumumab , un agente anti-EGFR similar, pero no una interacción consistente con el tratamiento, aunque HPV+OPC parece no beneficiarse en la misma medida que HPV-OPC con la terapia anti-EGFR de segunda línea, posiblemente debido a una menor expresión de EGFR en HPV+OPC. [170]
Elección del enfoque de tratamiento
In the absence of high quality evidence comparing a primary surgical approach to other modalities, decisions are based on consideration of factors such as adequate surgical exposure and anatomically favourable features for adequate resection, post treatment function and quality of life. Such patient selection may enable them to avoid the morbidity of additional adjuvant treatment. In the absence of favourable surgical features the primary treatment of choice remains radiation with or without chemotherapy. Tumor characteristics which favour a non-surgical approach include invasion of the base of the tongue to the extent of requiring resection of 50% or more of the tongue, pterygoid muscle involvement, extension into the parapharyngeal fat abutting the carotid, involvement of the mandible or maxilla or invasion of the prevertebral space.[12]
The adequacy of surgical resection is a major factor in determining the role of postoperative adjuvant therapy. In the presence of a positive margin on pathological examination, most radiation oncologists recommend radiation to the primary site, and concurrent chemotherapy. A negative margin is more likely to be treated with lower doses and a smaller treatment volume. Also the removal of a bulky tumour may allow reduced dosage to adjacent uninvolved pharyngeal structures and hence less effect on normal swallowing.[76][12]
The cancer outcomes (local control, regional control, and survival) for transoral resection followed by adjuvant therapy are comparable to primary chemoradiation,[102][98][139] so that treatment decisions depend more on treatment-related morbidity, functional outcome, and quality of life. Patient factors also need to be taken into account, including general baseline functionality, smoking history, anesthesia risk, oropharyngeal function, swallowing and airway protection and potential for rehabilitation. Patient preference is equally important. Many clinical trials are under way focussing on deintensification, often with risk stratification, e.g. Low, Intermediate and High risk (see Fundakowski and Lango, Table I).[12][p]
Las decisiones clínicas también tienen en cuenta las morbilidades, en particular si los resultados del cáncer son comparables, por ejemplo, la cirugía se asocia con un riesgo de sangrado entre el 5 y el 10% y un riesgo del 0,3% de hemorragia posoperatoria mortal. [103] [184] [99] [100] La cirugía también puede complicarse por la disfagia , y aunque la mayoría de los pacientes pueden tolerar una dieta el primer día posoperatorio, se ha informado que el uso a largo plazo de una sonda de alimentación es tan alto como el 10%. [108] [99] [100] Los pacientes con tumores más grandes, afectación de la base de la lengua y que requieren terapia adyuvante posoperatoria tienen más probabilidades de requerir una sonda de alimentación a largo plazo. [185] [186] En general, la función y la calidad de vida parecen relativamente similares entre la cirugía con radiación posoperatoria y la quimiorradiación primaria, [187] [188] [12] pero los pacientes con VPH+OPC tienden a tener una mejor calidad de vida en el momento del diagnóstico que los pacientes con VPH-OPC, pero pueden sufrir una mayor pérdida después del tratamiento. [189]
Las consideraciones anatómicas también pueden dictar la preferencia por abordajes quirúrgicos o no quirúrgicos. Por ejemplo, el trismo , una lengua voluminosa, una extensión limitada del cuello, dientes prominentes, torus mandibular (un crecimiento óseo en la mandíbula) o un ancho limitado de la mandíbula serían todas contraindicaciones relativas a la cirugía. [101] Las consideraciones relacionadas con el tumor incluyen la invasión de la mandíbula, la base del cráneo y la afectación extensa de la laringe o más de la mitad de la base de la lengua. [102] Las consideraciones técnicas al ofrecer la cirugía como modalidad primaria incluyen la presunta capacidad de lograr márgenes adecuados en la muestra resecada y el grado de defecto resultante, ya que los márgenes cercanos o positivos probablemente resulten en una terapia adyuvante posterior para lograr el control de la enfermedad, con el aumento resultante de la morbilidad. Los costos son difíciles de estimar, pero un estudio estadounidense, basado en estimaciones del 25% de todos los pacientes con OPC que recibieron cirugía sola y el 75% cirugía seguida de terapia adyuvante, utilizando los criterios del NCCN , encontró que este enfoque era menos costoso que la quimiorradiación primaria. [190] [191] [192]
La enfermedad en etapa temprana [q] se asocia con un resultado relativamente favorable, para el cual se recomienda una terapia de modalidad única, cuya elección depende de la ubicación del tumor y la accesibilidad. Por ejemplo, los tumores unilaterales de las amígdalas o de la base de la lengua generalmente se tratarán con resección transoral y disección selectiva del cuello ipsilateral. Por otro lado, una lesión grande en la línea media de la lengua requeriría una disección bilateral del cuello, pero en ausencia de lo que se considera una patología adversa (márgenes positivos, extensión extracapsular) probablemente se tratará solo con cirugía o radiación que incluya campos de radiación ipsilaterales o bilaterales en el cuello, con cirugía para aquellos casos en los que la probabilidad de terapia adyuvante sea baja. [12]
Pero muchos HPV+OPC presentan afectación de los ganglios linfáticos del cuello y, por lo tanto, una etapa más avanzada de la enfermedad, generalmente denominada enfermedad localmente avanzada. Este grupo se trata principalmente con terapia multimodal, con la excepción de uno de los subgrupos más favorables con tumores primarios pequeños y afectación de los ganglios linfáticos confinada a un solo ganglio no mayor de 3 cm de tamaño, que como se señaló se consideran enfermedad en etapa temprana. Las tres opciones principales para la enfermedad localmente avanzada pero operable son la resección, la disección del cuello y la terapia adyuvante; la quimiorradiación (con posible cirugía de rescate ); la quimioterapia de inducción seguida de radiación o quimiorradiación. Sin embargo, la última opción no ha sido apoyada en los ensayos clínicos que la probaron. [r] La consideración principal de la cirugía para la enfermedad localmente avanzada es obtener márgenes negativos adecuados y ahorrarle al paciente la quimiorradiación posoperatoria. Pero esto debe equilibrarse con la morbilidad y la pérdida funcional de la resección extensa, en particular cuando está involucrada la base de la lengua. Para evitar dicha morbilidad, se prefiere la quimiorradiación primaria. En el tratamiento de la enfermedad localmente avanzada, se debe tener en cuenta el manejo de la enfermedad dentro de los ganglios linfáticos cervicales. Las pautas para todos los ganglios linfáticos cervicales indican que se debe administrar quimiorradiación postoperatoria a la extensión ectracapsular. Cuando la enfermedad cervical macroscópica es evidente inicialmente, generalmente se administra quimiorradiación primaria. [12]
Preferencias del paciente
Las directrices actuales se basan en datos de la OPC en su conjunto, de modo que los pacientes generalmente reciben tratamiento independientemente del estado de VPH, aunque muchos médicos e investigadores están considerando la desintensificación. [195] Es probable que el tratamiento de esta afección continúe evolucionando en la dirección de la desintensificación, con el fin de minimizar la pérdida de función pero mantener el control de la enfermedad. [196] En ausencia de ensayos clínicos y directrices específicas, es necesario tener en cuenta las preferencias de los pacientes para minimizar la toxicidad a corto y largo plazo y la pérdida funcional y optimizar la calidad de vida, dada la supervivencia prolongada que se observa con frecuencia. [12] Esto puede implicar explorar los valores de los pacientes con respecto a las compensaciones del control de la enfermedad frente a los efectos adversos del tratamiento. Los pacientes que han recibido CRT como tratamiento primario para OPC valoran mucho la supervivencia y, aunque están de acuerdo en que la desintensificación es deseable, se mostraron reacios a sacrificar mucha ventaja de supervivencia por una menor toxicidad, aunque es más probable que renuncien a la quimioterapia que a aceptar una radiación reducida. [197]
Carcinoma de origen primario desconocido
En algunas situaciones, el carcinoma escamocelular de origen primario desconocido (T0 N1–3) puede presentarse con ganglios linfáticos cervicales, pero sin enfermedad evidente de un tumor primario, por lo que se clasifica como carcinoma escamocelular de origen primario desconocido . Esto ocurre en el 2–4% de los pacientes que presentan cáncer metastásico en los ganglios cervicales. La incidencia de positividad para el VPH está aumentando a un ritmo similar al observado en el carcinoma escamocelular de origen primario desconocido. En tales situaciones, la resección de las amígdalas linguales y palatinas junto con la disección del cuello puede ser diagnóstica y constituir una intervención suficiente, ya que las tasas de recurrencia son bajas. [198] [199] [200] [201] [202] [12] [ citas excesivas ]
Pronóstico
Desde la década de 1990 se ha reconocido que la presencia de VPH dentro del tumor es un factor importante para predecir la supervivencia. [203]
Comparación con el cáncer orofaríngeo HPV-negativo

Tumor HPV status is strongly associated with positive therapeutic response and survival compared with HPV-negative cancer, independent of the treatment modality chosen and even after adjustment for stage.[204] While HPV+OPC patients have a number of favourable demographic features compared to HPV-OPC patients, such differences account for only about ten per cent of the survival difference seen between the two groups.[11] Response rates of over 80% are reported in HPV+ cancer and three-year progression free survival has been reported as 75–82% and 45–57%, respectively, for HPV+ and HPV- cancer, and improving over increasing time.[12][205][206][207] It is likely that HPV+OPC is inherently less malignant than HPV-OPC, since patients treated by surgery alone have a better survival after adjustment for stage.[11]
HPV is tested for by the presence of the biomarker p16, which normally increases in the presence of HPV. Some people can have elevated levels of p16 but test negative for HPV and vice versa. This is known as discordant cancer. The 5-year survival for people who test positive for HPV and p16 is 81%, for discordant cancer it is 53 – 55%, and 40% for those who test negative for p16 and HPV.[208][209]
Determinants of survival
In RTOG clinical trial 0129,[s] in which all patients with advanced disease received radiation and chemotherapy, a retrospective analysis (recursive-partitioning analysis, or RPA) at three years identified three risk groups for survival (low, intermediate, and high) based on HPV status, smoking, T stage and N stage (see Ang et al., Fig. 2).[157] HPV status was the major determinant of survival, followed by smoking history and stage. 64% were HPV+ and all were in the low and intermediate risk group, with all non-smoking HPV+ patients in the low risk group. 82% of the HPV+ patients were alive at three years compared to 57% of the HPV- patients, a 58% reduction in the risk of death.[t][157] Locoregional failure is also lower in HPV+, being 14% compared to 35% for HPV-.[160]
Determinants of disease progression
La positividad del VPH confiere un riesgo de progresión de la enfermedad y muerte entre un 50 y un 60 % menor, pero el uso de tabaco es un factor pronóstico negativo independiente. [157] [210] Un análisis agrupado de pacientes con VPH+OPC y VPH-OPC con progresión de la enfermedad en los ensayos RTOG 0129 y 0522 mostró que, aunque menos pacientes con VPH+OPC experimentaron progresión de la enfermedad (23 frente a 40 %), el tiempo medio hasta la progresión de la enfermedad después del tratamiento fue similar (8 meses). La mayoría (65 %) de las recurrencias en ambos grupos se produjeron durante el primer año después del tratamiento y fueron locorregionales. Aunque la tasa de fracaso en el cuello opuesto después del tratamiento de un solo lado es del 2,4 %, la tasa de una recurrencia aislada en el cuello opuesto es del 1,7 % y se produjo principalmente cuando el tumor primario afectaba la línea media. Sin embargo, la tasa de fracaso en el cuello contralateral también es mayor para los pacientes con VPH+. [211] De aquellos que recurrieron en este sitio, casi todos fueron tratados exitosamente (salvados) mediante un tratamiento local adicional en el cuello opuesto. [133]
Determinantes de las tasas de metástasis
El VPH+ no redujo la tasa de metástasis (alrededor del 45% de los pacientes experimentan progresión), que son predominantemente en los pulmones (70%), aunque algunos estudios han informado una tasa menor. [212] [161] con tasas de recurrencia distante a 3 años de alrededor del 10% para pacientes tratados con radiación primaria o quimiorradiación. [213] Incluso si ocurre recurrencia o metástasis, la positividad del VPH aún confiere una ventaja. [12] [212] [214] Por el contrario, el uso de tabaco es un factor pronóstico negativo independiente, con una respuesta reducida a la terapia, [157] [210] mayores tasas de recurrencia de la enfermedad y disminución de la supervivencia. [215] Los efectos negativos del tabaquismo aumentan con la cantidad fumada, particularmente si es mayor a 10 paquetes-año . [157] [210]
Predictores de supervivencia
Después de la quimiorradiación
Para pacientes como los tratados con RTOG 0129 con quimiorradiación primaria, se han derivado nomogramas detallados de ese conjunto de datos combinado con RTOG 0522, lo que permite la predicción del resultado en función de una gran cantidad de variables . Por ejemplo, un graduado de la escuela secundaria no fumador, casado, de 71 años con un estado funcional (PS) de 0, sin pérdida de peso ni anemia y un HPV+OPC T3N1 esperaría tener una supervivencia libre de progresión del 92 % a los 2 años y del 88 % a los 5 años. Un graduado de la escuela secundaria no fumador, soltero, de 60 años con un PS de 1, pérdida de peso y anemia y un HPV+OPC T4N2 esperaría tener una supervivencia del 70 % a los dos años y del 48 % a los cinco años. [216]
Después de la cirugía
Se dispone de información menos detallada para aquellos tratados principalmente con cirugía, para quienes hay menos pacientes disponibles, [121] así como bajas tasas de recurrencia (7-10%), pero las características que tradicionalmente han sido útiles para predecir el pronóstico en otros cánceres de cabeza y cuello, parecen ser menos útiles en HPV+OPC. [51] Estos pacientes se estratifican con frecuencia en tres grupos de riesgo: [93]
- Riesgo bajo: Sin características patológicas adversas
- Riesgo intermedio: T3-T4 primaria, invasión perineural o linfovascular, N2 (AJCC 7) [a]
- Alto riesgo: Márgenes positivos, ECE
Desarrollo de otros tipos de cáncer
Los pacientes con OPC HPV+ tienen menos probabilidades de desarrollar otros tipos de cáncer, en comparación con otros pacientes con cáncer de cabeza y cuello. [30] Una posible explicación del impacto favorable del HPV+ es "la menor probabilidad de ocurrencia de la amplificación del gen 11q13, que se considera un factor subyacente a una recurrencia más rápida y frecuente de la enfermedad" [14] La presencia de mutaciones TP53, un marcador para el OPC HPV-, se asocia con un peor pronóstico. [8] Se cree que un alto grado de tinción p16 es mejor que el análisis de PCR de HPV para predecir la respuesta a la radioterapia. [64]
Recidiva regional después de la cirugía
El riesgo de recurrencia regional del cáncer después de una disección de cuello se estima a menudo [164] a partir de una serie amplia basada en todos los cánceres de células escamosas de las vías aerodigestivas superiores. En esta serie, los riesgos generales a los tres años por estadio patológico (AJCC 7) fueron: [217]
- pN0 4,7%
- pN1 4,9%
- pN2 12,1%
Epidemiología
En 2015, el cáncer de células escamosas de la región de cabeza y cuello fue el quinto cáncer más común aparte del cáncer de piel, a nivel mundial, con una incidencia anual de 600.000 casos y alrededor de 60.000 casos anualmente en los Estados Unidos y Europa. [218] La incidencia global de cáncer de faringe en 2013 se estimó en 136.000 casos. [12] [219] [220] Para 2008, la carga global de enfermedad por OPC en 2008 se estima en 85.000 casos, de los cuales 22.000 fueron atribuibles al VPH, una fracción atribuible poblacional (PAF) del 26%. De estos, 17.000 eran hombres y 4.400 mujeres, 13.000 (60%) tenían entre 50 y 69 años de edad, y la mayoría de los casos (15.000) estaban en regiones desarrolladas en comparación con las regiones en desarrollo (6.400). [221] [2] Las tasas de incidencia estandarizadas por edad (ASR) difieren considerablemente según la región y el país ( véase de Martel et al., 2017 Fig. 2b). [221] Las ASR para 2012 fueron más altas en Europa (Hungría 3,0) y América del Norte (Estados Unidos 1,7) pero mucho más bajas en África (≤ 0,3), Asia (≤ 0,6), América Latina (≤ 0,4) y Oceanía (≤ 0,2) (excepto Australasia , Australia 0,9). [222] [221] El número promedio estimado de casos y de ASR para los EE. UU. en el período 2008-2012 fue de 15 738 y 4,5 respectivamente. El VPH+OPC fue mucho más común en hombres que en mujeres (12 638, 7,6 y 3100, 1,7). El grupo de edad de mayor incidencia fue el de 60 a 69 años, y fue mayor en los caucásicos que en otras razas. [223]
Los pacientes con cáncer de cabeza y cuello HPV+ tienden a ser más jóvenes que los pacientes con HPV- en general. [224] La presentación clínica también está cambiando del paciente "típico" con cáncer de cabeza y cuello con edad avanzada y consumo importante de sustancias . [12] Por el contrario, los pacientes con cáncer HPV+ son más jóvenes (4.ª a 6.ª décadas), hombres (ratio 8:1) sin antecedentes de tabaquismo o con antecedentes mínimos de tabaquismo, generalmente caucásicos, han alcanzado niveles de educación más altos, están casados y tienen mayores ingresos. [225] Los factores de riesgo para el cáncer de cabeza y cuello HPV- y el cáncer de cabeza y cuello HPV+ tienden a ser independientes, con la excepción del tabaquismo que tiene un efecto adverso en ambos. [11] Las características de presentación también son diferentes entre el cáncer de cabeza y cuello HPV+. Los tumores HPV+ tienen lesiones primarias más pequeñas (menos de 4 cm) pero enfermedad ganglionar más avanzada que resulta en una estadificación TNM más alta. Esto a su vez puede sobrestimar la gravedad del estado de la enfermedad. [226] [227]
Tendencias
Ha habido una tendencia global en el aumento de la incidencia de OPC, particularmente en América del Norte y el norte de Europa, pero incluso en Taiwán, que tiene una tasa muy alta para todos los cánceres de la región de cabeza y cuello, las tasas de OPC aumentaron más rápidamente entre 1995 y 2009 que cualquier otro sitio de cáncer. [228] [229] La carga global de HPV+OPC aumentó de 22.000 en 2008 a 29.000 en 2012, y la PAF del 26% al 31%, [221] y se considera una epidemia . [44] En los Estados Unidos, el número estimado de casos fue de 12 410 en 2008, [230] 13 930 en 2013 [231] y 17 000 para 2017. [232] De estos casos, el cáncer HPV+ ha aumentado en comparación con el cáncer HPV-, pero el aumento en HPV+OPC supera la disminución en HPV-OPC, lo que resulta en un aumento general en OPC. [11] El aumento en la incidencia del cáncer de faringe contrasta con una disminución marginal en otros cánceres de cabeza y cuello. [233] Como resultado, el cáncer de cabeza y cuello más común ha pasado de la laringe a la orofaringe. [121] Una encuesta de 23 países entre 1983 y 2002 mostró un aumento en el carcinoma de células escamosas orofaríngeo que fue particularmente notable en hombres jóvenes en países económicamente desarrollados . [220] [12] En el Reino Unido la incidencia de cáncer oral y orofaríngeo en hombres aumentó un 51%, de 7/100.000 a 11/100.000 entre 1989 y 2006. [233] En los EE. UU. hay una creciente incidencia de cánceres orofaríngeos asociados al VPH, [234] A principios de la década de 1980, el VPH+ representaba solo el 7,5% de los casos en los EE. UU., pero en 2016 era del 70%, [12] [235] [236] [237] quizás como resultado de cambios en los comportamientos sexuales, menor popularidad de las amigdalectomías, mejor evaluación radiológica y patológica y cambios en la clasificación. [238] [239] [240] Los cánceres de amígdalas y orofaringe aumentaron en predominio masculino entre 1975 y 2004, a pesar de las reducciones en el tabaquismo. [241] El OPC-VPH disminuyó con la disminución de las tasas de tabaquismo entre 1988 y 2004, mientras que el OPC+VPH aumentó casi un 7,5% por año, desde aproximadamente el 16% de todos los casos de OPC a principios de los años 1980 hasta casi el 70% en 2004. [225] [242] La disminución del tabaquismo puede estar vinculada a la proporción decreciente de cánceres negativos al VPH, mientras que los cambios en la actividad sexual pueden reflejarse en una proporción creciente de cánceres positivos al VPH. [225] Recientemente, en los EE. UU., el OPC asociado al VPH representa aproximadamente el 60% de los casos de OPC [160] [243] en comparación con el 40% en la década anterior.[233] En 2007, en los EE. UU., la incidencia de OPC general, incluido el no asociado al VPH, es de 3,2 casos por cada 100 000 hombres/año y de 1,9 por cada 100 000 de todos los sexos/año. [244] Esto hace que el VPH+OPC sea uno de los únicos cinco tipos de cáncer cuya incidencia ha aumentado en los EE. UU. desde 1975. [245] El mayor aumento de incidencia se ha producido en pacientes menores de 50 años. [246]
El aumento de la incidencia de OPC asociado a VPH también se observa en otros países, como Suecia , con una incidencia en 2007 de más del 80% para cáncer en las amígdalas, [247] [248] Finlandia [249] y la República Checa . [250] Las parejas de pacientes con cáncer orofaríngeo positivo al VPH no parecen tener una infección oral por VPH elevada en comparación con la población general. [251] En Australia, la incidencia de OPC asociado a VPH fue de 1,56 casos por 100 000 hombres/año (2001-2005), aumentando del 19 % (1987-90) al 47 % (2001-05) y al 63,5 % (2006-2010). [252] [253] En Canadá, el porcentaje de casos de OPC atribuibles al VPH aumentó del 47% en 2000 al 74% en 2012. [254]
Véase también
Notas
- ^ ab N etapa, AJCC 7.ª ed. [75]
N1: un ganglio ipsilateral afectado, de 3 cm o menos, ECE negativo (ECE−)
N2a: un ganglio ipsilateral de 3 a 6 cm, ECE−
N2b: más de un ganglio ipsilateral, de menos de 6 cm, ECE−
N2c: ganglios bilaterales, de menos de 6 cm, ECE−
N3a: cualquier ganglio linfático de más de 6 cm, ECE−
N3b: cualquier ganglio linfático ECE+ - ^ Tercera edición revisada, 2013
- ^ ECOG 3311 (NCT01706939) se activó en 2013 y completó la acumulación de 511 pacientes y ahora se encuentra en seguimiento; consulte Discusión
- ^ La incorporación planificada de 242 pacientes a PATHOS comenzó a fines de 2014; consulte la charla [126]
- ^ La recurrencia contralateral después del tratamiento unilateral se ha reportado solo en el 2,4% de los casos [133]
- ^ Los efectos adversos se informan generalmente en grados 0 a 5, donde 0 representa ninguno y 5 representa la muerte, lo que corresponde a 1. leve, 2. moderado, 3. grave y 4. potencialmente mortal. Estos están estandarizados como Criterios Terminológicos Comunes para Eventos Adversos (CTCAE) [137]
- ^ RTOG 9003 – ver Discusión
- ^ RTOG0129 – ver Discusión
- ^ NCT01706939 – ver Discusión
- ^ NCT02945631 – ver Discusión
- ^ NCT03323463 – ver Discusión
- ^ RTOG 9501 aleatorizó a 459 pacientes con cáncer de cabeza y cuello y cualquiera o todas las siguientes características de alto riesgo identificadas sobre la base de ensayos previos: evidencia histológica de invasión de dos o más ganglios linfáticos regionales, extensión extracapsular de la enfermedad ganglionar y márgenes de resección de la mucosa afectados microscópicamente, entre la radiación y la quimiorradiación con cisplatino en el posoperatorio. A los cinco años, el control locorregional mejoró con la quimioterapia, pero los eventos adversos fueron mayores. Las metástasis distantes no se vieron afectadas. Un seguimiento más prolongado de hasta diez años mostró que estas diferencias solo se observaron en dos subgrupos de alto riesgo, aquellos con márgenes positivos y aquellos con extensión extracapsular.
- ^ :EORC 22931, también publicado en 2004, utilizó un diseño similar pero una definición diferente de alto riesgo. Demostró una ventaja temprana similar para la terapia combinada
- ^ RTOG 9501 – ver Discusión
- ^ ADEPT – ver Discusión
- ^ Por ejemplo, ECOG 3311 estratifica HPV+OPC con AJCC 7 Estadios III y IV 1–2, N1–2b en tres grupos de riesgo posoperatorios. El riesgo bajo es T1–T2 N0–N1 con márgenes negativos. El riesgo intermedio son márgenes limpios o cercanos con la presencia de características adversas en la patología como invasión perineural o invasión linfovascular, <1 mm ECE o 2–4 ganglios afectados. El riesgo alto son márgenes positivos o mayor a 1 mm ECE o al menos 5 ganglios afectados.
- ^ La enfermedad en etapa temprana se considera según AJCC 7 como T1–22 N0–1 M0, aproximadamente equivalente a T1–2 N0–2 M0 según AJCC 8
- ^ Ensayos clínicos, como PARADIGM [193] y DeCIDE [194]
- ^ RTOG 0129 - ver Discusión
- ^ En RTOG 0129 los tres grupos pronósticos fueron;
- Riesgo bajo: VPH-, y había fumado menos de 10 paquetes-año o más de 10 paquetes-año pero tenía un estado ganglionar bajo (limitado a un solo ganglio, >3 cm pero ≤6 cm en su mayor dimensión)
- Riesgo intermedio: HPV+ con tabaquismo de >10 paquetes-año y estado ganglionar más avanzado, o HPV-, <10 paquetes-año y estadio tumoral T2-T3
- Alto riesgo: todos los demás (incluidos el resto de pacientes con VPH, <10 paquetes-año con tumores T4 y todos con >10 paquetes-año)
Referencias
- ^ de Martel et al 2012.
- ^ desde Forman et al 2012.
- ^ Vokes y otros 2015.
- ^ Syrjänen y otros 1983.
- ^ abcd Mannarini y otros 2009.
- ^ CIIC 1995.
- ^ CIIC 2007.
- ^ abcdefgh Chaturvedi y Gillison 2010.
- ^ Gillison y otros 2000.
- ^ Ostras 2009.
- ^ abcdefghi Lowy y Munger 2010.
- ^ abcdefghijklmnopqrstu vwxyz aa ab Fundakowski & Lango 2016.
- ^ Ramqvist y Dalianis 2010.
- ^ abcde Michl y otros 2010.
- ^ Vidal y Gillison 2008.
- ^ Guan y otros 2010.
- ^ Frisch y otros 1999.
- ^ Anantharaman y otros 2016.
- ^ Haeggblom y otros 2017.
- ^ Underbrink y otros 2008.
- ^ Hemminki y otros 2000.
- ^ Tezal y otros 2009.
- ^ Tezal y otros 2009a.
- ^ Smith y otros 2004.
- ^ Schwartz y otros 1998.
- ^ D'Souza y otros 2007.
- ^ Heck y otros 2010.
- ^ abcde Chung y otros 2016.
- ^ Gillison 2006.
- ^ desde Martel et al 2017.
- ^ Enséñame 2017.
- ^ desde Joshi et al 2013.
- ^ McHanwell 2015.
- ^ Lindberg 1972.
- ^ desde agosto de 2006.
- ^ desde zur Hausen 2002.
- ^ Smeets y otros 2010.
- ^ por Maslon y Hupp 2010.
- ^ por Chung y Gillison 2009.
- ^ Hong y otros 2016a.
- ^ desde An et al 2016.
- ^ Lawrence y otros 2015.
- ^ Ha y Califano 2006.
- ^ abc Marur y otros 2010.
- ^ Caza 2010.
- ^ Howard y Chung 2012.
- ^ Licitra y otros 2006.
- ^ Salem 2010.
- ^ abc Spanos y otros 2009.
- ^ desde Wansom et al 2010.
- ^Ab Sinha et al. 2015.
- ^ Chernock y otros 2009.
- ^ Elmofty y Patil 2006.
- ^ S. Elrefaey; MA Massaro; S. Chiocca; F. Chiesa; M. Ansarin (2014). "HPV en cáncer orofaríngeo: aspectos básicos que se deben conocer en la práctica clínica". Acta Otorhinolaryngologica Italica . 34 (5): 299–309. PMC 4299160 . PMID 25709145.
- ^ Klussmann y otros 2009.
- ^ Lohavanichbutr y otros 2009.
- ^ Schlecht y otros 2007.
- ^ Weinberger y otros 2009.
- ^ Martínez et al 2007.
- ^ Jung y otros 2009.
- ^ Yamakawa-Kakuta y otros 2009.
- ^ Cristina Mazón 2011.
- ^ Robinson y otros 2010.
- ^ ab Munck-Wikland, Hammarstedt y Dahlstrand 2010.
- ^ Agoston y otros 2010.
- ^ por Seiwert 2014.
- ^ abc O'Sullivan y col. 2016.
- ^ abcd NCCN 2018.
- ^ Goldenberg y otros 2008.
- ^ desde Porceddu 2016.
- ^ TNM 7 2010.
- ^ Keane y otros 2015.
- ^ Huang y otros 2015a.
- ^ TNM 8 2017.
- ^ abcd Lydiatt y otros 2017.
- ^Ab Quon y Richmon 2012.
- ^ Psyrri, Gouveris y Vermorken 2009.
- ^ Lassen 2010.
- ^ Fakhry y Gillison 2006.
- ^ Brockstein y Vokes 2011.
- ^ Givens y otros 2009.
- ^ Instituto Nacional del Cáncer 2016.
- ^ Instituto Nacional del Cáncer 2016a.
- ^ Kreimer y otros 2010.
- ^ Posner y otros 2011.
- ^ desde Parsons et al 2002.
- ^ Bourhis y otros 2006.
- ^ Corry y otros 2015.
- ^ Dok y otros 2014.
- ^ abcdefgh Chen y otros 2017.
- ^ Huang y otros 2015b.
- ^ Ward y otros 2014.
- ^ abc Routman y otros 2017.
- ^ Adelstein y otros 2012.
- ^ desde Cohen et al 2011.
- ^ Genden y otros 2011.
- ^ White y otros 2010.
- ^ desde Rinaldi et al 2013.
- ^ abc Weinstein y otros 2012.
- ^ abc Chia y col. 2013.
- ^ desde Rich et al 2009.
- ^ abc Moore y Hinni 2013.
- ^ desde Canis et al 2012.
- ^ Moore y otros 2012.
- ^ Choby y otros 2015.
- ^ Dowthwaite y otros 2012.
- ^ Steiner y otros 2003.
- ^ abcd Haughey y otros 2011.
- ^ Walvekar y otros 2008.
- ^ Helliwell y Woolgar 1998.
- ^ Woolgar y Triantafyllou 2005.
- ^ desde Bernier et al 2004.
- ^ Maccomb y Fletcher 1957.
- ^ desde Kramer et al 1987.
- ^ Vikram y otros 1984.
- ^ Tupchong y otros 1991.
- ^ Peters y otros 1993.
- ^ Rosenthal y otros 2017.
- ^ ASTRO 2017.
- ^ desde Chin et al 2016.
- ^ abcd Haughey y Sinha 2012.
- ^ Monroe y otros 2017.
- ^ Olson y Clayburgh 2017, pág. 99.
- ^ Cramer y otros 2018.
- ^ Kelly y otros 2016.
- ^ desde Owadally et al 2015.
- ^ desde Masterson et al 2014.
- ^ Bedi y otros 2012.
- ^ ab Ma y col. 2017.
- ^ Heymach y otros 2018.
- ^ Su y otros 2016.
- ^ Chen y otros 2013.
- ^ abc Al-Mamgani y otros 2017.
- ^ O'Sullivan y otros 2001.
- ^ Maxwell y otros 2014.
- ^ desde Hunter et al 2013.
- ^ Centro de Investigación Científica y Tecnológica de la Universidad de California en Berkeley (CSIC) 2010.
- ^ Forastiere y otros 2013.
- ^ desde Almeida et al 2014.
- ^ Al-Mamgani y otros 2013.
- ^ abcd Fu y otros 2000.
- ^ abc Langendijk y otros 2008.
- ^ abc Ang y otros 2014.
- ^ abc Marur y otros 2017.
- ^ Deasy y otros 2010.
- ^ Robin y otros 2016.
- ^ Feng y otros 2007.
- ^ Li y otros 2009.
- ^ Caudell y otros 2010.
- ^ Eisbruch y otros 2004.
- ^ Vlacich y otros 2014.
- ^ Levendag y otros 2007.
- ^ Tsai y otros 2017.
- ^ Díaz et al 2010.
- ^ desde Beitler et al 2014.
- ^ desde Nguyen-Tan et al 2014.
- ^ abcdef Ang y otros 2010.
- ^ Baño 2017.
- ^ Cmelak y otros 2007.
- ^ abc Fakhry y otros 2008.
- ^ desde Fakhry y col. 2014.
- ^ Woody y otros 2016.
- ^ Chera y otros 2015.
- ^ abc Mirghani y otros 2018.
- ^ Seiwert y otros 2018.
- ^ desde Blanchard et al 2011.
- ^ Pignon y otros 2007.
- ^ Adelstein y otros 2003.
- ^ Bonner y otros 2010.
- ^ desde Szturz et al 2017.
- ^ NIH 2018.
- ^ Hall y otros 2017.
- ^ Hall y otros 2015.
- ^ Bachaud y otros 1996.
- ^ Cooper y otros 2004.
- ^ Cooper y otros 2012.
- ^ Bernier y otros 2005.
- ^ Lewis y otros 2011.
- ^Ab Sinha et al. 2012.
- ^ Maxwell y otros 2013.
- ^ Calais y otros 2004.
- ^ Machtay y otros 2008.
- ^ Erikson y otros 2010.
- ^ Pollei y otros 2013.
- ^ Sinclair y otros 2011.
- ^ Dziegielewski y otros 2013.
- ^ Más et al 2013.
- ^ Chen y otros 2015.
- ^ Sharma y otros 2012.
- ^ Moore y otros 2009.
- ^ Moore y otros 2009a.
- ^ Moore y otros 2012a.
- ^ Haddad y otros 2013.
- ^ Cohen y otros 2014.
- ^ Mehanna y otros 2016.
- ^ Mirghani y otros 2015.
- ^ Brotherston y otros 2013.
- ^ Durmus y otros 2014.
- ^ Graboyes y otros 2015.
- ^ Mehta y otros 2013.
- ^ Patel y otros 2013.
- ^ Galloway y Ridge 2015.
- ^ Rischin y otros 2010.
- ^ Mehanna 2017.
- ^ Dayyani y otros 2010.
- ^ de Jong et al 2010.
- ^ Ragin y Taioli 2007.
- ^ Mehanna, Hisham; Taberna, Miren; von Buchwald, cristiano; Todos, Sara; Brooks, Jill; Mena, Marisa; Morey, Francisca; Grønhøj, cristiano; Rasmussen, Jacob Hoygaard; Garset-Zamani, Martín; Bruni, Laia; Batis, Nicolás; Brakenhoff, Ruud H; Leemans, C René; Baatenburg de Jong, Robert J (1 de marzo de 2023). "Implicaciones pronósticas de la discordancia de p16 y VPH en el cáncer de orofaringe (HNCIG-EPIC-OPC): un análisis de datos de pacientes individuales, multinacionales y multicéntricos". Oncología de The Lancet . 24 (3): 239–251. doi :10.1016/s1470-2045(23)00013-x. hdl : 2445/198366 . ISSN 1470-2045. PMID 36796393.
- ^ Mehanna, Hisham; et al. (12 de septiembre de 2023). "Las pruebas de detección de VPH y p16 pueden proporcionar pronósticos más precisos en el cáncer orofaríngeo (de garganta)". NIHR Evidence . 24 (3): 239–251. doi :10.1016/S1470-2045(23)00013-X. hdl : 2445/198366 . PMID 36796393.
- ^ abc Gillison y otros 2012.
- ^ Kato y otros 2018.
- ^ desde Trosman et al 2015.
- ^ O'Sullivan y otros 2013.
- ^ Sinha y otros 2014.
- ^ Maxwell y otros 2010.
- ^ Fakhry y otros 2017.
- ^ Ambrosch y otros 2001.
- ^ Siegel y otros 2015.
- ^ Myers y Sturgis 2013.
- ^ desde Chaturvedi et al 2013.
- ^ abcd de Martel et al 2017.
- ^ Johnson y Chaturvedi 2016.
- ^ Viens y col. 2016.
- ^ Lajer y otros 2010.
- ^ abc Chaturvedi y otros 2011.
- ^ Fischer y otros 2010.
- ^ Hafkamp y otros 2008.
- ^ Hwang y otros 2015.
- ^ Gillison y otros 2015.
- ^ Jemal y otros 2008.
- ^ Siegel y otros 2013.
- ^ Siegel y otros 2017.
- ^ abc Mehanna y otros 2010.
- ^ Chenevert y Chiosea 2012.
- ^ Sturgis y Cinciripini 2007.
- ^ Ernster y otros 2007.
- ^ Hammarstedt y otros 2006.
- ^ Chenevert y otros 2012.
- ^ Chaturvedi y otros 2008.
- ^ Nguyen y otros 2009.
- ^ Cook y otros 2009.
- ^ Sturgis y Ang 2011.
- ^ Adelstein y Rodríguez 2010.
- ^ VIDENTE 2010.
- ^ Wirth 2016.
- ^ Nguyen y otros 2010.
- ^ Nasman y otros 2009.
- ^ Hammarstedt 2008.
- ^ Syrjänen 2004.
- ^ Tachezy 2005.
- ^ D'Souza y otros 2014.
- ^ Hong y otros 2010.
- ^ Hong y otros 2016b.
- ^ Habbous y otros 2017.
Bibliografía
- "Criterios terminológicos comunes para eventos adversos (CTCAE) Versión 4.0 Publicado: 28 de mayo de 2009 (v4.03)" (PDF) . CTCAE . Instituto Nacional del Cáncer . 14 de junio de 2010. Archivado desde el original (PDF) el 30 de agosto de 2017 . Consultado el 3 de agosto de 2017 .
Artículos
- Fakhry, Carole; Gillison, Maura L. (10 de junio de 2006). "Implicaciones clínicas del virus del papiloma humano en los cánceres de cabeza y cuello". Journal of Clinical Oncology (Revisión). 24 (17): 2606–2611. doi :10.1200/JCO.2006.06.1291. PMC 4696042. PMID 16763272 .
- Lindberg, Robert (junio de 1972). "Distribución de las metástasis de los ganglios linfáticos cervicales del carcinoma de células escamosas de las vías respiratorias superiores y digestivas". Cancer . 29 (6): 1446–1449. doi : 10.1002/1097-0142(197206)29:6<1446::AID-CNCR2820290604>3.0.CO;2-C . PMID 5031238. S2CID 11167436.
- Mehanna, H.; Jones, TM; Gregoire, V.; Ang, KK (24 de abril de 2010). "Carcinoma orofaríngeo relacionado con el virus del papiloma humano". BMJ (Editorial). 340 (7752): 879–880. doi :10.1136/bmj.c1439. JSTOR 40701677. PMID 20339160. S2CID 27997605.
- Nguyen, NP; Chi, A.; Nguyen, LM; Ly, BH; Karlsson, U.; Vinh-Hung, V. (2009). "Cáncer orofaríngeo asociado al virus del papiloma humano: una nueva entidad clínica". QJM (Revisión). 103 (4): 229–236. doi : 10.1093/qjmed/hcp176 . PMID 20015950.
- Psyrri, A.; Gouveris, P.; Vermorken, JB (2009). "Tumores de cabeza y cuello relacionados con el virus del papiloma humano: implicancias clínicas y de investigación". Current Opinion in Oncology (Revisión). 21 (3): 201–205. doi :10.1097/CCO.0b013e328329ab64. PMID 19370803. S2CID 35188456.
- Ramqvist, Torbjörn; Dalianis, Tina (noviembre de 2010). "Epidemia de cáncer orofaríngeo y virus del papiloma humano". Enfermedades infecciosas emergentes (revisión). 16 (11): 1671–1677. doi :10.3201/eid1611.100452. PMC 3294514. PMID 21029523 .
- Westra, WH (2009). "El rostro cambiante del cáncer de cabeza y cuello en el siglo XXI: el impacto del VPH en la epidemiología y patología del cáncer oral". Patología de cabeza y cuello (revisión). 3 (1): 78–81. doi :10.1007/s12105-009-0100-y. PMC 2807531 . PMID 20596995.
El virus del papiloma humano (VPH) y la biología molecular
- Adelstein, DJ; Rodriguez, Cristina P. (3 de febrero de 2010). "Virus del papiloma humano: cambios de paradigmas en el cáncer orofaríngeo". Current Oncology Reports . 12 (2): 115–120. doi :10.1007/s11912-010-0084-5. PMID 20425596. S2CID 11091993.
- Agoston, E. .; Robinson, S. .; Mehra, K. .; et al. (2010). "Detección de VPH mediante reacción en cadena de la polimerasa en carcinoma escamoso de orofaringe". American Journal of Clinical Pathology . 134 (1): 36–41. doi : 10.1309/AJCP1AAWXE5JJCLZ . PMID 20551264.
- Ault, KA (2006). "Epidemiología e historia natural de las infecciones por virus del papiloma humano en el tracto genital femenino". Enfermedades infecciosas en obstetricia y ginecología . 2006 : 1–5. doi : 10.1155/IDOG/2006/40470 . PMC: 1581465. PMID: 16967912 .
- Chung, CH; Gillison, ML (27 de octubre de 2009). "Virus del papiloma humano en el cáncer de cabeza y cuello: su papel en la patogénesis y las implicaciones clínicas". Clinical Cancer Research . 15 (22): 6758–6762. doi : 10.1158/1078-0432.CCR-09-0784 . PMID 19861444.
- Cristina Mazón, Renata; Rovigatti Gerbelli, Thaís; Benatti Neto, Carlos; et al. (febrero de 2011). "Expresión anormal del ciclo celular de las proteínas p27, mdm2 y catepsina B en el carcinoma oral de células escamosas infectado con el virus del papiloma humano". Acta Histoquímica . 113 (2): 109-116. doi :10.1016/j.acthis.2009.08.008. PMID 19811804.
- D'Souza, Gypsyamber; Gross, Neil D.; Pai, Sara I.; Haddad, Robert; Anderson, Karen S.; Rajan, Shirani; Gerber, Jennifer; Gillison, Maura L.; Posner, Marshall R. (10 de agosto de 2014). "Infección oral por virus del papiloma humano (VPH) en pacientes con VPH positivo con cáncer orofaríngeo y sus parejas". Journal of Clinical Oncology . 32 (23): 2408–2415. doi :10.1200/JCO.2014.55.1341. PMC 4263818 . PMID 24778397.
- Elmofty, S.; Patil, S. (2006). "Carcinoma de células escamosas no queratinizante orofaríngeo relacionado con el virus del papiloma humano (VPH): caracterización de un fenotipo distinto". Cirugía oral, medicina oral, patología oral, radiología oral y endodoncia . 101 (3): 339–345. doi :10.1016/j.tripleo.2005.08.001. PMID 16504868.
- Frisch, M.; Biggar, R. (1999). "Paralelismo etiológico entre carcinomas de células escamosas anogenitales y amigdalinos". The Lancet (manuscrito enviado). 354 (9188): 1442–1443. doi :10.1016/S0140-6736(99)92824-6. PMID 10543674. S2CID 33391604.
- Gillison, ML; Koch, WM; Capone, RB; et al. (mayo de 2000). "Evidencia de una asociación causal entre el virus del papiloma humano y un subconjunto de cánceres de cabeza y cuello". Journal of the National Cancer Institute . 92 (9): 709–720. doi : 10.1093/jnci/92.9.709 . ISSN 0027-8874. PMID 10793107.
- Guan, X.; Sturgis, E.; Lei, D.; Liu, Z.; Dahlstrom, K.; Wei, Q.; Li, G. (2010). "Asociación de variantes genéticas de TGF-beta1 con cáncer orofaríngeo HPV16-positivo". Investigación clínica del cáncer . 16 (5): 1416–1422. doi :10.1158/1078-0432.CCR-09-2877. PMC 2831118. PMID 20179236 .
- Ha, Patrick K; Califano, Joseph A (enero de 2006). "Metilación del promotor e inactivación de genes supresores de tumores en el carcinoma oral de células escamosas". The Lancet Oncology . 7 (1): 77–82. doi :10.1016/S1470-2045(05)70540-4. PMID 16389187.
- Haeggblom, Linnea; Ramqvist, Torbjörn; Tommasino, Massimo; Dalianis, Tina; Näsman, Anders (diciembre de 2017). "Es hora de cambiar las perspectivas sobre el VPH en el cáncer orofaríngeo. Una revisión sistemática de la prevalencia del VPH por subsitio orofaríngeo en los últimos 3 años". Papillomavirus Research . 4 : 1–11. doi :10.1016/j.pvr.2017.05.002. PMC 5883233 . PMID 29179862.
- Hong, Angela; Zhang, Xiaoying; Jones, Deanna; Veillard, Anne-Sophie; Zhang, Mei; Martin, Andrew; Lyons, J. Guy; Lee, C. Soon; Rose, Barbara (febrero de 2016a). "Relaciones entre la mutación p53, el estado del VPH y el pronóstico en el carcinoma de células escamosas orofaríngeo". Radioterapia y oncología . 118 (2): 342–349. doi :10.1016/j.radonc.2016.02.009. PMID 26952933.
- Howard, Jason D.; Chung, Christine H. (julio de 2012). "Biología del cáncer orofaríngeo relacionado con el virus del papiloma humano". Seminarios en oncología radioterápica . 22 (3): 187–193. doi :10.1016/j.semradonc.2012.03.002. PMC 3715056. PMID 22687942 .
- Jung, A.; Briolat, J.; Millon, R.; De Reyniès, A.; Rickman, D.; Thomas, E.; Abecassis, J.; Clavel, C.; Wasylyk, B. (2009). "Relevancia biológica y clínica de la infección por el virus del papiloma humano (VPH) transcripcionalmente activo en el carcinoma de células escamosas de orofaringe". Revista Internacional de Cáncer . 126 (8): 1882–1894. doi : 10.1002/ijc.24911 . PMID 19795456. S2CID 3441257.
- Klussmann, J.; Mooren, J.; Lehnen, M.; et al. (marzo de 2009). "Firmas genéticas del carcinoma orofaríngeo relacionado y no relacionado con el VPH y sus implicaciones pronósticas". Clinical Cancer Research . 15 (5): 1779–1786. doi : 10.1158/1078-0432.CCR-08-1463 . ISSN 1078-0432. PMID 19223504.
- Kreimer, Aimée R.; Bhatia, Rohini K.; Messeguer, Andrea L.; González, Paula; Herrero, Rolando; Giuliano, Anna R. (enero de 2010). "Virus del papiloma humano oral en individuos sanos: una revisión sistemática de la literatura". Enfermedades de Transmisión Sexual . 37 (6): 386–91. doi : 10.1097/OLQ.0b013e3181c94a3b . PMID 20081557. S2CID 32378293.
- Lajer, CB; Buchwald, CV (2010). "El papel del virus del papiloma humano en el cáncer de cabeza y cuello". APMIS . 118 (6–7): 510–519. doi : 10.1111/j.1600-0463.2010.02624.x . PMID 20553531. S2CID 7199240.
- Lassen, P. (2010). "El papel del virus del papiloma humano en el cáncer de cabeza y cuello y su impacto en los resultados de la radioterapia". Radioterapia y oncología . 95 (3): 371–380. doi :10.1016/j.radonc.2010.04.022. PMID 20493569.
- Lawrence MS, Sougnez C, Lichtenstein L, et al. (28 de enero de 2015). "Caracterización genómica integral de carcinomas de células escamosas de cabeza y cuello". Nature . 517 (7536): 576–582. Bibcode :2015Natur.517..576T. doi :10.1038/nature14129. PMC 4311405 . PMID 25631445.
- Lohavanichbutr, P.; Houck, J.; Fan, W.; et al. (febrero de 2009). "Perfiles de expresión génica en todo el genoma del cáncer orofaríngeo con y sin VPH: posibles implicaciones para las opciones de tratamiento". Archivos de otorrinolaringología y cirugía de cabeza y cuello . 135 (2): 180–188. doi :10.1001/archoto.2008.540. ISSN 0886-4470. PMC 2761829. PMID 19221247 .
- Mannarini, L.; Kratochvil, V.; Calabrese, L.; Gomes Silva, L.; Morbini, P.; Betka, J.; Benazzo, M. (2009). "Virus del papiloma humano (VPH) en la región de cabeza y cuello: revisión de la literatura". Acta Otorhinolaryngologica Italica . 29 (3): 119–126. PMC 2815356 . PMID 20140157.
- Martínez, I.; Wang, J.; Hobson, K.; Ferris, R.; Khan, S. (enero de 2007). "Identificación de genes expresados diferencialmente en carcinomas de células escamosas orofaríngeos positivos y negativos al VPH". Revista Europea del Cáncer . 43 (2): 415–432. doi :10.1016/j.ejca.2006.09.001. ISSN 0959-8049. PMC 1847595 . PMID 17079134.
- Maslon, Magda M.; Hupp, Ted R. (septiembre de 2010). "Descubrimiento de fármacos y p53 mutante". Tendencias en biología celular . 20 (9): 542–555. doi :10.1016/j.tcb.2010.06.005. PMID 20656489.
- Michl, P; Pazdera, J; Prochazka, M; Pink, R; Stosova, T (2010). "Virus del papiloma humano en la etiología de carcinomas de cabeza y cuello" (PDF) . Artículos biomédicos de la Facultad de Medicina de la Universidad Palacky, Olomouc, Checoslovaquia . 154 (1): 9–12. doi : 10.5507/bp.2010.004 . PMID 20445705.
- Robinson, M.; Sloan, P.; Shaw, R. (2010). "Refinamiento del diagnóstico del carcinoma de células escamosas orofaríngeo mediante pruebas del virus del papiloma humano". Oral Oncology . 46 (7): 492–496. doi :10.1016/j.oraloncology.2010.02.013. PMID 20227331.
- Schlecht, N.; Burk, R.; Adrien, L.; et al. (noviembre de 2007). "Perfiles de expresión génica en cáncer de cabeza y cuello infectado por VPH". The Journal of Pathology . 213 (3): 283–293. doi :10.1002/path.2227. ISSN 0022-3417. PMID 17893858. S2CID 11205618.
- Seiwert, Tanguy Y. (10 de diciembre de 2014). "Lazos que unen: p16 como biomarcador pronóstico y la necesidad de pruebas de alta precisión para el virus del papiloma humano". Journal of Clinical Oncology . 32 (35): 3914–3916. doi : 10.1200/JCO.2014.57.9268 . PMID 25366683.
- Smeets, S.; Van Der Plas, M.; Schaaij-Visser, T.; Van Veen, E.; Van Meerloo, J.; Braakhuis, B.; Steenbergen, R.; Brakenhoff, R. (2010). "Inmortalización de queratinocitos orales mediante inactivación funcional de las vías p53 y pRb". Revista Internacional de Cáncer . 128 (7): 1596–605. doi : 10.1002/ijc.25474 . PMID 20499310. S2CID 21846809.
- Syrjänen, S. (2004). "Infecciones por VPH y carcinoma amigdalino". Revista de patología clínica . 57 (5): 449–455. doi :10.1136/jcp.2003.008656. PMC 1770289 . PMID 15113849.
- Syrjänen, Kari; Syrjänen, Stina; Lamberg, Matti; Pyrhönen, Seppo; Nuutinen, Juhant (diciembre de 1983). "Evidencia morfológica e inmunohistoquímica que sugiere la participación del virus del papiloma humano (VPH) en la carcinogénesis oral de células escamosas". Revista Internacional de Cirugía Bucal . 12 (6): 418–424. doi :10.1016/S0300-9785(83)80033-7. PMID 6325356.
- Underbrink, M.; Hoskins, S.; Pou, A.; Albrecht, T. (2008). "Interacción viral: un posible factor contribuyente a la progresión del cáncer de cabeza y cuello". Acta Oto-Laryngologica . 128 (12): 1361–1369. doi :10.1080/00016480801965001. PMID 18607925. S2CID 205395382.
- Vidal, L.; Gillison, M. (2008). "Virus del papiloma humano en carcinoma espinocelular de cabeza y cuello: reconocimiento de un tipo de enfermedad distinto". Clínicas de Hematología y Oncología de Norteamérica . 22 (6): 1125–1142, vii. doi :10.1016/j.hoc.2008.08.006. PMID 19010263.
- Vokes, EE; Agrawal, N; Seiwert, TY (diciembre de 2015). "Cáncer de cabeza y cuello asociado al VPH". Revista del Instituto Nacional del Cáncer . 107 (12): djv344. doi : 10.1093/jnci/djv344 . PMID 26656751.
- Weinberger, P.; Yu, Z.; Kountourakis, P.; Sasaki, C.; Haffty, B.; Kowalski, D.; Merkley, M.; Rimm, D.; Camp, R.; Psyrri, A. (septiembre de 2009). "Definición de fenotipos moleculares del carcinoma de células escamosas orofaríngeo asociado al virus del papiloma humano: validación de la hipótesis de tres clases". Otorrinolaringología–Cirugía de cabeza y cuello . 141 (3): 382–389.e1. doi :10.1016/j.otohns.2009.04.014. ISSN 0194-5998. PMID 19716018. S2CID 207300943.
- Yamakawa-Kakuta, Y; Kawamata, H; Doi, Y; Fujimori, T; Imai, Y (15 de septiembre de 2009). "¿La expresión de HPV16/18 E6/E7 en carcinomas de células escamosas de cabeza y cuello se relaciona con sus características clinicopatológicas?". Revista Internacional de Oncología . 35 (5): 983–988. doi : 10.3892/ijo_00000412 . PMID 19787251.
- zur Hausen, Harald (1 de mayo de 2002). "Virus de papiloma y cáncer: de estudios básicos a aplicación clínica". Nature Reviews Cancer . 2 (5): 342–350. doi : 10.1038/nrc798 . PMID 12044010. S2CID 4991177.
Diagnóstico y estadificación
- Chenevert, J; Seethala, RR; Barnes, EL; Chiosea, SI (abril de 2012). "Carcinoma de células escamosas metastásico en el cuello a partir de un tumor primario desconocido: el posible impacto de la evaluación patológica moderna en la incidencia percibida del carcinoma orofaríngeo positivo al virus del papiloma humano antes de 1970". The Laryngoscope . 122 (4): 793–796. doi :10.1002/lary.21899. PMID 22252715. S2CID 25749527.
- Goldenberg, David; Begum, Shahnaz; Westra, William H.; Khan, Zubair; Sciubba, James; Pai, Sara I.; Califano, Joseph A.; Tufano, Ralph P.; Koch, Wayne M. (julio de 2008). "Metástasis quística de ganglios linfáticos en pacientes con cáncer de cabeza y cuello: un fenómeno asociado al VPH" (PDF) . Head & Neck . 30 (7): 898–903. doi :10.1002/hed.20796. PMID 18383529. S2CID 32614424. Archivado desde el original (PDF) el 2010-11-26 . Consultado el 2018-07-08 .
- Huang, Shao Hui; Xu, Wei; Waldron, John; et al. (10 de marzo de 2015). "Refinamiento del estadio TNM y los grupos pronósticos del Comité Conjunto Estadounidense sobre Cáncer/Unión para el Control Internacional del Cáncer para los carcinomas orofaríngeos relacionados con el virus del papiloma humano". Journal of Clinical Oncology . 33 (8): 836–845. doi : 10.1200/JCO.2014.58.6412 . PMID 25667292.
- Keane, Florence K.; Chen, Yui-Hui; Neville, Bridget A.; Tishler, Roy B.; Schoenfeld, Jonathan D.; Catalano, Paul J.; Margalit, Danielle N. (1 de agosto de 2015). "Cambio de la importancia pronóstica del estadio tumoral y del estadio ganglionar en pacientes con carcinoma de células escamosas de la orofaringe en la era del virus del papiloma humano". Cáncer . 121 (15): 2594–2602. doi : 10.1002/cncr.29402 . PMID 25873094. S2CID 205670627.
- Lydiatt, William M.; Patel, Snehal G.; O'Sullivan, Brian; Brandwein, Margaret S.; Ridge, John A.; Migliacci, Jocelyn C.; Loomis, Ashley M.; Shah, Jatin P. (marzo de 2017). "Cánceres de cabeza y cuello: cambios importantes en el manual de estadificación del cáncer de la octava edición del Comité Conjunto Estadounidense sobre el Cáncer". CA: A Cancer Journal for Clinicians . 67 (2): 122–137. doi : 10.3322/caac.21389 . PMID 28128848.
- O'Sullivan, Brian; Huang, Shao Hui; Su, Jie; et al. (abril de 2016). "Desarrollo y validación de un sistema de estadificación para el cáncer orofaríngeo relacionado con el VPH por parte de la Red de Colaboración Internacional para la Estadificación del Cáncer Orofaríngeo (ICON-S): un estudio de cohorte multicéntrico". The Lancet Oncology . 17 (4): 440–451. doi :10.1016/S1470-2045(15)00560-4. PMID 26936027.
- Porceddu, Sandro V (abril de 2016). "Una clasificación TNM para el cáncer orofaríngeo HPV+". The Lancet Oncology (Editorial). 17 (4): 403–404. doi :10.1016/S1470-2045(15)00611-7. PMID 26936026.
Tratamiento
- Brockstein, Bruce E.; Vokes, Everett E. (febrero de 2011). "Cáncer de cabeza y cuello en 2010: maximizar la supervivencia y minimizar la toxicidad". Nature Reviews Clinical Oncology . 8 (2): 72–74. doi :10.1038/nrclinonc.2010.226. PMID 21278773. S2CID 1347226.
- Corry, June; Peters, Lester J.; Rischin, Danny (10 de enero de 2015). "Impacto del tamaño y la experiencia del centro en los resultados del cáncer de cabeza y cuello". Journal of Clinical Oncology . 33 (2): 138–140. doi : 10.1200/JCO.2014.58.2239 . PMID 25488964.
- Fakhry, C.; Westra, W.; Li, S.; Cmelak, A.; Ridge, J.; Pinto, H.; Forastiere, A.; Gillison, M. (febrero de 2008). "Mejora de la supervivencia de pacientes con carcinoma de células escamosas de cabeza y cuello positivo al virus del papiloma humano en un ensayo clínico prospectivo". Journal of the National Cancer Institute . 100 (4): 261–269. doi : 10.1093/jnci/djn011 . ISSN 0027-8874. PMID 18270337.
- Fakhry, Carole; Zhang, Qiang; Nguyen-Tan, Phuc Felix; et al. (20 de octubre de 2014). "Virus del papiloma humano y supervivencia general después de la progresión del carcinoma de células escamosas orofaríngeo". Journal of Clinical Oncology . 32 (30): 3365–3373. doi :10.1200/JCO.2014.55.1937. PMC 4195851 . PMID 24958820.
- Fundakowski, Christopher E.; Lango, Miriam (11 de julio de 2016). "Consideraciones en el tratamiento quirúrgico versus no quirúrgico del cáncer orofaríngeo positivo para VPH". Cánceres de cabeza y cuello (revisión). 1 (1): 6. doi : 10.1186/s41199-016-0007-8 . PMC 6457136. PMID 31093336 .
- Galloway, TJ; Ridge, JA (10 de octubre de 2015). "Manejo del cáncer escamoso metastásico a ganglios cervicales con un sitio primario desconocido". Journal of Clinical Oncology (Revisión). 33 (29): 3328–3337. CiteSeerX 10.1.1.1029.7347 . doi :10.1200/JCO.2015.61.0063. PMID 26351351.
- Maxwell, Jessica H.; Mehta, Vikas; Wang, Hong; Cunningham, Diana; Duvvuri, Umamaheswar; Kim, Seungwon; Johnson, Jonas; Ferris, Robert L. (julio de 2014). "Calidad de vida en pacientes con cáncer de cabeza y cuello: impacto del VPH y modalidad de tratamiento primario". The Laryngoscope . 124 (7): 1592–1597. doi :10.1002/lary.24508. PMID 24353066. S2CID 8040452.
- Mehanna, H; Evans, M; Beasley, M; Chatterjee, S; Dilkes, M; Homer, J; O'Hara, J; Robinson, M; Shaw, R; Sloan, P (12 de mayo de 2016). "Cáncer orofaríngeo: directrices nacionales multidisciplinarias del Reino Unido". The Journal of Laryngology & Otology . 130 (S2): S90–S96. doi :10.1017/S0022215116000505. PMC 4873902 . PMID 27841123.
- More, Yogesh I.; Tsue, Terance T.; Girod, Douglas A.; Harbison, John; Sykes, Kevin J.; Williams, Carson; Shnayder, Yelizaveta (1 de enero de 2013). "Resultados de la deglución funcional después de la cirugía robótica transoral frente a la quimiorradioterapia primaria en pacientes con cánceres de orofaringe y supraglotis en estadio avanzado". JAMA Otolaryngology–Head & Neck Surgery . 139 (1): 43–48. doi : 10.1001/jamaoto.2013.1074 . PMID 23247974.
- Sharma, Arun; Méndez, Eduardo; Yueh, Bevan; Lohavanichbutr, Pawadee; Houck, John; Doody, David R.; Futran, Neal D.; Upton, Melissa P.; Schwartz, Stephen M.; Chen, Chu (24 de enero de 2012). "Los pacientes con cáncer orofaríngeo y de cavidad oral con virus del papiloma humano positivos no tienen mejores trayectorias de calidad de vida". Otorrinolaringología–Cirugía de cabeza y cuello . 146 (5): 739–745. doi :10.1177/0194599811434707. PMC 3535430 . PMID 22275190.
- Spanos, William C.; Nowicki, Paul; Lee, Dong Wook; Hoover, Andrew; Hostager, Bruce; Gupta, Anjali; Anderson, Mary E.; Lee, John H. (1 de noviembre de 2009). "Respuesta inmunitaria durante la terapia con cisplatino o radiación para el cáncer de cabeza y cuello relacionado con el virus del papiloma humano". Archivos de otorrinolaringología y cirugía de cabeza y cuello . 135 (11): 1137–46. doi : 10.1001/archoto.2009.159 . PMID 19917928.
- Wansom, Derrick; Light, Emily; Worden, Frank; et al. (20 de diciembre de 2010). "Correlación de la inmunidad celular con el estado del virus del papiloma humano 16 y el resultado en pacientes con cáncer orofaríngeo avanzado". Archivos de otorrinolaringología y cirugía de cabeza y cuello . 136 (12): 1267–73. doi :10.1001/archoto.2010.211. PMC 3342998 . PMID 21173378.
Cirugía
- Adelstein, David J.; Ridge, John A.; Brizel, David M.; et al. (diciembre de 2012). "Resección transoral del cáncer faríngeo: Resumen de una reunión de planificación de ensayos clínicos del Comité Directivo de Cáncer de Cabeza y Cuello del Instituto Nacional del Cáncer, 6 y 7 de noviembre de 2011, Arlington, Virginia". Cabeza y cuello . 34 (12): 1681–1703. doi :10.1002/hed.23136. hdl : 2027.42/94490 . PMC 7721598 . PMID 23015475. S2CID 542440.
- de Almeida, John R.; Byrd, James K.; Wu, Rebecca; Stucken, Chaz L.; Duvvuri, Uma; Goldstein, David P.; Miles, Brett A.; Teng, Marita S.; Gupta, Vishal; Genden, Eric M. (septiembre de 2014). "Una revisión sistemática de la cirugía robótica transoral y la radioterapia para el cáncer de orofaringe en etapa temprana: una revisión sistemática". The Laryngoscope . 124 (9): 2096–2102. doi :10.1002/lary.24712. PMID 24729006. S2CID 20283441.
- Ambrosch, Petra; Kron, Martina; Pradier, O.; Steiner, W. (2001). "Eficacia de la disección selectiva del cuello: una revisión de 503 casos de tratamiento electivo y terapéutico del cuello en el carcinoma de células escamosas del tracto aerodigestivo superior". Otorrinolaringología–Cirugía de cabeza y cuello . 124 (2): 180–187. doi :10.1067/mhn.2001.111598. PMID 11226954. S2CID 25298496.
- Canis, Martin; Martin, Alexios; Kron, Martina; Konstantinou, Alexandra; Ihler, Friedrich; Wolff, Hendrik A.; Matthias, Christoph; Steiner, Wolfgang (29 de diciembre de 2012). "Resultados de la microcirugía láser transoral en 102 pacientes con carcinoma de células escamosas de la amígdala". Archivos europeos de otorrinolaringología . 270 (8): 2299–2306. doi :10.1007/s00405-012-2335-6. PMC 3699702 . PMID 23274878.
- Chen, Allen M.; Daly, Megan E.; Luu, Quang; Donald, Paul J.; Farwell, D. Gregory (marzo de 2015). "Comparación de los resultados funcionales y la calidad de vida entre la cirugía transoral y la quimiorradioterapia definitiva para el cáncer orofaríngeo". Cabeza y cuello . 37 (3): 381–385. doi :10.1002/hed.23610. PMID 24431059. S2CID 28264800.
- Chia, Stanley H.; Gross, Neil D.; Richmon, Jeremy D. (diciembre de 2013). "Experiencia del cirujano y complicaciones con la cirugía robótica transoral (TORS)". Otorrinolaringología–Cirugía de cabeza y cuello . 149 (6): 885–892. doi :10.1177/0194599813503446. PMID 24013139. S2CID 3339804.
- Choby, Garret W.; Kim, Jeehong; Ling, Diane C.; Abberbock, Shira; Mandal, Rajarsi; Kim, Seungwon; Ferris, Robert L.; Duvvuri, Umamaheswar (1 de junio de 2015). "Cirugía robótica transoral sola para el cáncer orofaríngeo". JAMA Otolaryngology–Head & Neck Surgery . 141 (6): 499–504. doi : 10.1001/jamaoto.2015.0347 . PMID 25834991.
- Cohen, Marc A.; Weinstein, Gregory S.; O'Malley, Bert W.; Feldman, Michael; Quon, Harry (abril de 2011). "Cirugía robótica transoral y estado del virus del papiloma humano: resultados oncológicos". Cabeza y cuello . 33 (4): 573–580. doi :10.1002/hed.21500. PMID 21425382. S2CID 24704123.
- Durmus, K; Rangarajan, SV; Viejo, MO; Agrawal, A; Teknos, Tennessee; Ozer, E (junio de 2014). "Abordaje robótico transoral del carcinoma de primario desconocido". Cabeza y cuello . 36 (6): 848–52. doi :10.1002/hed.23385. PMC 4266274 . PMID 23720223.
- Dziegielewski, Peter T.; Teknos, Theodoros N.; Durmus, Kasim; Old, Matthew; Agrawal, Amit; Kakarala, Kiran; Marcinow, Anna; Ozer, Enver (1 de noviembre de 2013). "Cirugía robótica transoral para el cáncer orofaríngeo". JAMA Otolaryngology–Head & Neck Surgery . 139 (11): 1099–108. doi :10.1001/jamaoto.2013.2747. PMC 4274181 . PMID 23576186.
- Dowthwaite, Samuel A.; Franklin, Jason H.; Palma, David A.; Fung, Kevin; Yoo, John; Nichols, Anthony C. (2012). "El papel de la cirugía robótica transoral en el tratamiento del cáncer orofaríngeo: una revisión de la literatura". ISRN Oncology . 2012 : 945162. doi : 10.5402/2012/945162 . PMC 3347745 . PMID 22606380.
- Genden, Eric M.; Kotz, Tamar; Tong, Charles CL; Smith, Claris; Sikora, Andrew G.; Teng, Marita S.; Packer, Stuart H.; Lawson, William L.; Kao, Johnny (agosto de 2011). "Resección y reconstrucción robótica transoral para el cáncer de cabeza y cuello". El laringoscopio . 121 (8): 1668–1674. doi :10.1002/lary.21845. PMID 21792953. S2CID 25175486.
- Graboyes, EM; Sinha, P; Thorstad, WL; Rich, JT; Haughey, BH (noviembre de 2015). "Manejo de tumores primarios desconocidos relacionados con el virus del papiloma humano en cabeza y cuello con un abordaje quirúrgico transoral". Cabeza y cuello . 37 (11): 1603–11. doi :10.1002/hed.23800. PMID 24931847. S2CID 33000811.
- Haughey, Bruce H.; Hinni, Michael L.; Salassa, John R.; Hayden, Richard E.; Grant, David G.; Rich, Jason T.; Milov, Simon; Lewis, James S.; Krishna, Murli (diciembre de 2011). "Microcirugía láser transoral como tratamiento primario para el cáncer orofaríngeo en etapa avanzada: un estudio multicéntrico en Estados Unidos". Cabeza y cuello . 33 (12): 1683–1694. doi :10.1002/hed.21669. PMID 21284056. S2CID 10611085.
- Mehta, V; Johnson, P; Tassler, A; Kim, S; Ferris, RL; Nance, M; Johnson, JT; Duvvuri, U (enero de 2013). "Un nuevo paradigma para el diagnóstico y el tratamiento de tumores primarios desconocidos de cabeza y cuello: un papel para la cirugía robótica transoral". The Laryngoscope . 123 (1): 146–151. doi : 10.1002/lary.23562 . PMID 23154813. S2CID 321364.
- Moore, Eric J.; Hinni, Michael L.; Olsen, Kerry D.; Price, Daniel L.; Laborde, Rebecca R.; Inman, Jared C. (junio de 2012). "Consideraciones de costos en el tratamiento del carcinoma escamocelular orofaríngeo". Otorrinolaringología–Cirugía de cabeza y cuello . 146 (6): 946–951. doi :10.1177/0194599812437534. PMID 22344182. S2CID 40004254.
- Moore, Eric J.; Henstrom, Doug K.; Olsen, Kerry D.; Kasperbauer, Jan L.; McGree, Michaela E. (marzo de 2009). "Resección transoral del carcinoma de células escamosas amigdalinas". The Laryngoscope . 119 (3): 508–515. doi :10.1002/lary.20124. PMID 19235742. S2CID 26256802.
- Moore, Eric J.; Olsen, Kerry D.; Kasperbauer, Jan L. (noviembre de 2009). "Cirugía robótica transoral para el carcinoma de células escamosas orofaríngeo: un estudio prospectivo de viabilidad y resultados funcionales". The Laryngoscope . 119 (11): 2156–2164. doi :10.1002/lary.20647. PMID 19824067. S2CID 20097467.
- Moore, Eric J.; Olsen, Steven M.; Laborde, Rebecca R.; García, Joaquín J.; Walsh, Francis J.; Price, Daniel L.; Janus, Jeffrey R.; Kasperbauer, Jan L.; Olsen, Kerry D. (marzo de 2012). "Resultados funcionales y oncológicos a largo plazo de la cirugía robótica transoral para el carcinoma de células escamosas orofaríngeo". Mayo Clinic Proceedings . 87 (3): 219–225. doi :10.1016/j.mayocp.2011.10.007. PMC 3538408 . PMID 22386176.
- Moore, Eric J.; Hinni, Michael L. (abril de 2013). "Revisión crítica: microcirugía láser transoral y cirugía asistida por robot para el cáncer de orofaringe, incluido el cáncer relacionado con el virus del papiloma humano". Revista internacional de oncología radioterápica, biología y física (revisión). 85 (5): 1163–1167. doi :10.1016/j.ijrobp.2012.08.033. PMID 23182390.
- Patel, SA; Magnuson, JS; Holsinger, FC; et al. (noviembre de 2013). "Cirugía robótica para el carcinoma escamocelular primario de cabeza y cuello de sitio desconocido". JAMA Otolaryngology–Head & Neck Surgery . 139 (11): 1203–1211. doi : 10.1001/Jamaoto.2013.5189 . PMID 24136446.
- Pollei, Taylor R.; Hinni, Michael L.; Moore, Eric J.; Hayden, Richard E.; Olsen, Kerry D.; Casler, John D.; Walter, Logan C. (1 de noviembre de 2013). "Análisis del sangrado posoperatorio y los factores de riesgo en la cirugía transoral de la orofaringe". JAMA Otolaryngology–Head & Neck Surgery . 139 (11): 1212–8. doi : 10.1001/jamaoto.2013.5097 . PMID 24113922.
- Rinaldi, V; Pagani, D; Torretta, S; Pignataro, L (26 de septiembre de 2013). "Cirugía robótica transoral en el tratamiento de tumores de cabeza y cuello". Ecancermedicalscience . 7 : 359. doi :10.3332/ecancer.2013.359. PMC 3782590 . PMID 24073017.
- Sinclair, CF; McColloch, NL; Carroll, WR; Rosenthal, EL; Desmond, RA; Magnuson, JS (November 2011). "Patient-perceived and objective functional outcomes following transoral robotic surgery for early oropharyngeal carcinoma". Archives of Otolaryngology–Head & Neck Surgery. 137 (11): 1112–6. doi:10.1001/archoto.2011.172. PMID 22106235.
- Steiner, Wolfgang; Fierek, Oliver; Ambrosch, Petra; Hommerich, Christian P.; Kron, Martina (1 January 2003). "Transoral Laser Microsurgery for Squamous Cell Carcinoma of the Base of the Tongue". Archives of Otolaryngology–Head & Neck Surgery. 129 (1): 36–43. doi:10.1001/archotol.129.1.36. PMID 12525192.
- Walvekar, Rohan R.; Li, Ryan J.; Gooding, William E.; Gibson, Michael K.; Heron, Dwight; Johnson, Jonas T.; Ferris, Robert L. (December 2008). "Role of Surgery in Limited (T1–2, N0–1) Cancers of the Oropharynx". The Laryngoscope. 118 (12): 2129–2134. doi:10.1097/MLG.0b013e3181857950. PMID 18948826. S2CID 8072424.
- Weinstein, Gregory S.; O'Malley, Bert W.; Magnuson, J. Scott; Carroll, William R.; Olsen, Kerry D.; Daio, Lixia; Moore, Eric J.; Holsinger, F. Christopher (August 2012). "Transoral robotic surgery: A multicenter study to assess feasibility, safety, and surgical margins". The Laryngoscope. 122 (8): 1701–1707. doi:10.1002/lary.23294. PMID 22752997. S2CID 30048884.
- White, Hilliary N.; Moore, Eric J.; Rosenthal, Eben L.; Carroll, William R.; Olsen, Kerry D.; Desmond, Reneé A.; Magnuson, J. Scott (20 December 2010). "Transoral Robotic-Assisted Surgery for Head and Neck Squamous Cell Carcinoma". Archives of Otolaryngology–Head & Neck Surgery. 136 (12): 1248–52. doi:10.1001/archoto.2010.216. PMID 21173375.
- Woolgar, Julia Anne; Triantafyllou, Asterios (November 2005). "A histopathological appraisal of surgical margins in oral and oropharyngeal cancer resection specimens". Oral Oncology. 41 (10): 1034–1043. doi:10.1016/j.oraloncology.2005.06.008. PMID 16129652.
Radiation
- Adelstein, David J.; Li, Yi; Adams, George L.; Wagner, Henry; Kish, Julie A.; Ensley, John F.; Schuller, David E.; Forastiere, Arlene A. (enero de 2003). "Una comparación intergrupal de fase III de radioterapia estándar y dos esquemas de quimiorradioterapia concurrente en pacientes con cáncer de cabeza y cuello de células escamosas irresecable". Journal of Clinical Oncology . 21 (1): 92–98. doi :10.1200/JCO.2003.01.008. PMID 12506176.
- Al-Mamgani, Abrahim; van Rooij, Peter; Verduijn, Gerda M.; Mehilal, Robert; Kerrebijn, Jeroen D.; Levendag, Peter C. (febrero de 2013). "El impacto de la modalidad de tratamiento y la técnica de radiación en los resultados y la toxicidad de los pacientes con cáncer orofaríngeo localmente avanzado". The Laryngoscope . 123 (2): 386–393. doi :10.1002/lary.23699. PMID 23404489. S2CID 37351159.
- Bedi, Meena; Firat, Selim; Semenenko, Vladimir A.; Schultz, Christopher; Tripp, Patrick; Byhardt, Roger; Wang, Dian (mayo de 2012). "Irradiación electiva de ganglios linfáticos con radioterapia de intensidad modulada: ¿es necesaria la fraccionación de dosis convencional?". Revista internacional de oncología radioterápica, biología y física . 83 (1): e87–e92. doi :10.1016/j.ijrobp.2011.12.016. PMID 22516389.
- Beitler, Jonathan J.; Zhang, Qiang; Fu, Karen K.; Trotti, Andy; Spencer, Sharon A.; Jones, Christopher U.; Garden, Adam S.; Shenouda, George; Harris, Jonathan; Ang, Kian K. (mayo de 2014). "Resultados finales del control local-regional y la toxicidad tardía de RTOG 9003: un ensayo aleatorio de radiación fraccionada alterada para el cáncer de cabeza y cuello localmente avanzado". Revista internacional de oncología radioterápica, biología y física . 89 (1): 13–20. doi :10.1016/j.ijrobp.2013.12.027. PMC 4664465. PMID 24613816 .
- Bourhis, Jean; Overgaard, Jens; Audry, Hélène; et al. (septiembre de 2006). "Radioterapia hiperfraccionada o acelerada en cáncer de cabeza y cuello: un metaanálisis". The Lancet . 368 (9538): 843–854. doi :10.1016/S0140-6736(06)69121-6. PMID 16950362. S2CID 20670949.
- Caudell, Jimmy J.; Schaner, Philip E.; Desmond, Renee A.; Meredith, Ruby F.; Spencer, Sharon A.; Bonner, James A. (febrero de 2010). "Factores dosimétricos asociados con disfagia a largo plazo después de la radioterapia definitiva para el carcinoma de células escamosas de cabeza y cuello". Revista internacional de oncología radioterápica, biología y física . 76 (2): 403–409. doi :10.1016/j.ijrobp.2009.02.017. PMID 19467801.
- Chen, Allen M.; Li, Judy; Beckett, Laurel A .; Zhara, Talia; Farwell, Gregory; Lau, Derick H.; Gandour-Edwards, Regina; Vaughan, Andrew T.; Purdy, James A. (enero de 2013). "Tasas de respuesta diferencial a la irradiación entre pacientes con cáncer orofaríngeo positivo y negativo al virus del papiloma humano". The Laryngoscope . 123 (1): 152–157. doi :10.1002/lary.23570. PMID 23008061. S2CID 5106261.
- Chin, Re-I; Spencer, Christopher R.; DeWees, Todd; et al. (noviembre de 2016). "Reevaluación de la dosis de radiación posoperatoria en el tratamiento del cáncer orofaríngeo positivo al virus del papiloma humano". Cabeza y cuello . 38 (11): 1643–1649. doi :10.1002/hed.24486. PMID 27152851. S2CID 3577182.
- Cramer, John David; Ferris, Robert L.; Duvvuri, Umamaheswar (20 de mayo de 2018). "Desintensificación del tratamiento a cirugía únicamente para el cáncer orofaríngeo asociado al virus del papiloma humano en estadio I". Journal of Clinical Oncology . 36 (15 suplementos): 6003. doi :10.1200/JCO.2018.36.15_suppl.6003.
- Daly, Megan E.; Le, Quynh-Thu; Maxim, Peter G.; Loo, Billy W.; Kaplan, Michael J.; Fischbein, Nancy J.; Pinto, Harlan; Chang, Daniel T. (abril de 2010). "Radioterapia de intensidad modulada en el tratamiento del cáncer orofaríngeo: resultados clínicos y patrones de fracaso". Revista internacional de oncología radioterápica, biología y física . 76 (5): 1339–1346. doi :10.1016/j.ijrobp.2009.04.006. PMID 19540068.
- Deasy, Joseph O.; Moiseenko, Vitali; Marks, Lawrence; Chao, KS Clifford; Nam, Jiho; Eisbruch, Avraham (marzo de 2010). "Efectos de la dosis y el volumen de la radioterapia en la función de las glándulas salivales". Revista internacional de oncología radioterápica, biología y física . 76 (3): S58–S63. doi :10.1016/j.ijrobp.2009.06.090. PMC 4041494. PMID 20171519 .
- Dok, Rüveyda; Kalev, Pedro; Van Limbergen, Evert Jan; Asbagh, Layka Abbasi; Vázquez, Iria; Hauben, Esther; Sablina, Anna; Nuyts, Sandra (15 de marzo de 2014). "p16INK4a perjudica la reparación del ADN mediada por recombinación homóloga en tumores de cabeza y cuello positivos para el virus del papiloma humano". Investigación del cáncer . 74 (6): 1739-1751. doi : 10.1158/0008-5472.CAN-13-2479 . PMID 24473065.
- Feng, Felix Y.; Kim, Hyungjin M.; Lyden, Teresa H.; Haxer, Marc J.; Feng, Mary; Worden, Frank P.; Chepeha, Douglas B.; Eisbruch, Avraham (agosto de 2007). "Radioterapia de intensidad modulada para el cáncer de cabeza y cuello con el objetivo de reducir la disfagia: relaciones dosis-efecto tempranas para las estructuras de la deglución". Revista internacional de oncología radioterápica, biología y física . 68 (5): 1289–1298. doi :10.1016/j.ijrobp.2007.02.049. PMID 17560051.
- Forastiere, Arlene A.; Zhang, Qiang; Weber, Randal S.; et al. (marzo de 2013). "Resultados a largo plazo de RTOG 91-11: una comparación de tres estrategias de tratamiento no quirúrgico para preservar la laringe en pacientes con cáncer de laringe localmente avanzado". Journal of Clinical Oncology . 31 (7): 845–852. doi :10.1200/JCO.2012.43.6097. PMC 3577950 . PMID 23182993.
- Fu, Karen K.; Pajak, Thomas F.; Trotti, Andy; Jones, Christopher U.; Spencer, Sharon A.; Phillips, Theodore L.; Garden, Adam S.; Ridge, John A.; Cooper, Jay S.; Ang, K.Kian (agosto de 2000). "Estudio aleatorizado de fase III del grupo de oncología radioterapéutica (RTOG) para comparar la hiperfraccionación y dos variantes de fraccionamiento acelerado con la radioterapia de fraccionamiento estándar para carcinomas de células escamosas de cabeza y cuello: primer informe del RTOG 9003". Revista internacional de oncología radioterapéutica, biología y física . 48 (1): 7–16. doi :10.1016/S0360-3016(00)00663-5. PMID 10924966.
- Garden, Adam S.; Dong, Lei; Morrison, William H.; et al. (marzo de 2013). "Patrones de recurrencia de la enfermedad tras el tratamiento del cáncer orofaríngeo con radioterapia de intensidad modulada". Revista internacional de oncología radioterápica, biología y física . 85 (4): 941–947. doi :10.1016/j.ijrobp.2012.08.004. PMID 22975604.
- Heymach, John; Krilov, Lada; Alberg, Anthony; Baxter, Nancy; Chang, Susan Marina; Corcoran, Ryan B.; Dale, William; DeMichele, Angela; Magid Diefenbach, Catherine S.; Dreicer, Robert; Epstein, Andrew S.; Gillison, Maura L.; Graham, David L.; Jones, Joshua; Ko, Andrew H.; Lopez, Ana Maria; Maki, Robert G.; Rodriguez-Galindo, Carlos; Schilsky, Richard L.; Sznol, Mario; Westin, Shannon Neville; Burstein, Harold (abril de 2018). "Avances en cáncer clínico 2018: Informe anual sobre el progreso contra el cáncer de la Sociedad Estadounidense de Oncología Clínica". Revista de Oncología Clínica . 36 (10): 1020–1044. doi :10.1200/JCO.2017.77.0446. Número de modelo: PMID29380678.
- Kramer, Simon; Gelber, Richard D.; Snow, James B.; Marcial, Victor A.; Lowry, Louis D.; Davis, Lawrence W.; Chandler, Richard (septiembre de 1987). "Radioterapia y cirugía combinadas en el tratamiento del cáncer avanzado de cabeza y cuello: Informe final del estudio 73-03 del grupo de oncología de radioterapia". Cirugía de cabeza y cuello . 10 (1): 19–30. doi :10.1002/hed.2890100105. PMID 3449477.
- Langendijk, Johannes A.; Doornaert, Patricia; Verdonck-de Leeuw, Irma M.; Leemans, Charles R.; Aaronson, Neil K.; Slotman, Ben J. (agosto de 2008). "Impacto de la toxicidad tardía relacionada con el tratamiento en la calidad de vida de los pacientes con cáncer de cabeza y cuello tratados con radioterapia". Journal of Clinical Oncology . 26 (22): 3770–3776. doi : 10.1200/JCO.2007.14.6647 . PMID 18669465.
- Levendag, Peter C.; Teguh, David N.; Voet, Peter; et al. (octubre de 2007). "Los trastornos de disfagia en pacientes con cáncer de orofaringe se ven afectados significativamente por la dosis de radioterapia aplicada al músculo constrictor superior y medio: una relación dosis-efecto". Radioterapia y oncología . 85 (1): 64–73. doi :10.1016/j.radonc.2007.07.009. PMID 17714815.
- Li, Baoqing; Li, Dan; Lau, Derick H; Farwell, D Gregory; Luu, Quang; Rocke, David M; Newman, Kathleen; Courquin, Jean; Purdy, James A; Chen, Allen M (2009). "Análisis clínico-dosimétrico de las medidas de disfagia, incluida la dependencia de la sonda de gastrostomía, entre pacientes con cáncer de cabeza y cuello tratados definitivamente con radioterapia de intensidad modulada con quimioterapia concurrente". Oncología radioterápica . 4 (1): 52. doi : 10.1186/1748-717X-4-52 . PMC 2785826 . PMID 19909531.
- Maccomb, WS; Fletcher, GH (marzo de 1957). "Combinación planificada de cirugía y radiación en el tratamiento de cánceres primarios avanzados de cabeza y cuello". The American Journal of Roentgenology, Radio Therapy, and Nuclear Medicine . 77 (3): 397–414. PMID 13403033.
- Monroe, Marcus M.; Buchmann, Luke O.; Hunt, Jason P.; Hitchcock, Ying J.; Lloyd, Shane; Hashibe, Mia (abril de 2017). "El beneficio de la radiación adyuvante en el carcinoma escamocelular orofaríngeo T1–2 N1 tratado quirúrgicamente". Laryngoscope Investigative Otolaryngology . 2 (2): 57–62. doi :10.1002/lio2.64. PMC 5527368 . PMID 28894823.
- O'Sullivan, B; Warde, P; Grice, B; Goh, C; Payne, D; Liu, F.-F; Waldron, J; Bayley, A; Irish, J; Gullane, P; Cummings, B (octubre de 2001). "Los beneficios y las desventajas de la radioterapia ipsilateral en el carcinoma de la región amigdalina". Revista internacional de oncología radioterápica, biología y física . 51 (2): 332–343. doi :10.1016/S0360-3016(01)01613-3. PMID 11567806.
- Parsons, James T.; Mendenhall, William M.; Stringer, Scott P.; et al. (1 de junio de 2002). "Carcinoma de células escamosas de la orofaringe: cirugía, radioterapia o ambas". Cancer . 94 (11): 2967–2980. doi : 10.1002/cncr.10567 . PMID 12115386. S2CID 34438428.
- Peters, Lester J; Goepfert, Helmuth; Ang, K. Kian; et al. (abril de 1993). "Evaluación de la dosis para radioterapia posoperatoria del cáncer de cabeza y cuello: primer informe de un ensayo aleatorio prospectivo". Revista internacional de oncología radioterápica, biología y física . 26 (1): 3–11. doi :10.1016/0360-3016(93)90167-T. PMID 8482629.
- Rich, Jason T.; Milov, Simon; Lewis, James S.; Thorstad, Wade L.; Adkins, Douglas R.; Haughey, Bruce H. (septiembre de 2009). "Microcirugía láser transoral (TLM) ± terapia adyuvante para el cáncer orofaríngeo en etapa avanzada". The Laryngoscope . 119 (9): 1709–1719. doi :10.1002/lary.20552. PMC 3877921 . PMID 19572271.
- Robin, Tyler P.; Gan, Gregory N.; Tam, Moses; Westerly, David; Riaz, Nadeem; Karam, Sana D.; Lee, Nancy; Raben, David (abril de 2016). "Seguridad de la preservación de la glándula submandibular contralateral en cánceres orofaríngeos localmente avanzados: una revisión multicéntrica". Cabeza y cuello . 38 (4): 506–511. doi :10.1002/hed.23928. PMID 25482748. S2CID 2317606.
- Rosenthal, David I.; Mohamed, Abdallah SR; Garden, Adam S.; Morrison, William H.; El-Naggar, Adel K.; Kamal, Mona; Weber, Randal S.; Fuller, Clifton D.; Peters, Lester J. (agosto de 2017). "Informe final de un ensayo aleatorio prospectivo para evaluar la relación dosis-respuesta para la radioterapia posoperatoria y los grupos de riesgo patológico en pacientes con cáncer de cabeza y cuello". Revista internacional de oncología radioterápica, biología y física . 98 (5): 1002–1011. doi : 10.1016/j.ijrobp.2017.02.218. PMC 5518636. PMID 28721881.
- Sher, David J.; Adelstein, David J.; Bajaj, Gopal K.; et al. (julio de 2017). "Radioterapia para el carcinoma de células escamosas orofaríngeo: resumen ejecutivo de una guía de práctica clínica basada en evidencia de ASTRO". Oncología radioterapéutica práctica . 7 (4): 246–253. doi : 10.1016/j.prro.2017.02.002 . PMID 28428019.
- Tsai, Chiaojung Jillian; Jackson, Andrew; Setton, Jeremy; Riaz, Nadeem; McBride, Sean; Leeman, Jonathan; Kowalski, Alex; Happersett, Laura; Lee, Nancy Y. (noviembre de 2017). "Modelado de la respuesta a la dosis para la disfagia tardía en pacientes con cáncer de cabeza y cuello en la era moderna de la quimiorradiación definitiva". JCO Clinical Cancer Informatics . 1 (1): 1–7. doi :10.1200/cci.17.00070. PMC 6873915 . PMID 30657398.
- Vikram, Bhadrasain; Strong, Elliot W.; Shah, Jatin P.; Spiro, Ronald (enero de 1984). "Fallo en el sitio primario después del tratamiento multimodal en cáncer avanzado de cabeza y cuello". Cirugía de cabeza y cuello . 6 (3): 720–723. doi :10.1002/hed.2890060303. PMID 6693287.
- Tupchong, Leslie; Phil, D.; Scott, Charles B.; et al. (enero de 1991). "Estudio aleatorizado de radioterapia preoperatoria versus posoperatoria en carcinoma avanzado de cabeza y cuello: seguimiento a largo plazo del estudio RTOG 73-03". Revista internacional de oncología radioterápica, biología y física . 20 (1): 21–28. doi : 10.1016/0360-3016(91)90133-O . PMID 1993628.
- Woody, Neil M.; Koyfman, Shlomo A.; Xia, Ping; et al. (febrero de 2016). "El control regional se conserva después de la radioterapia con dosis reducida en los ganglios linfáticos afectados en el cáncer orofaríngeo positivo al VPH". Oral Oncology . 53 : 91–96. doi :10.1016/j.oraloncology.2015.11.004. PMID 26711089.
Quimioterapia y quimiorradiación
- Ang, K. Kian; Zhang, Qiang; Rosenthal, David I.; et al. (20 de septiembre de 2014). "Ensayo aleatorizado de fase III de radioterapia acelerada concurrente más cisplatino con o sin cetuximab para carcinoma de cabeza y cuello en estadio III a IV: RTOG 0522". Journal of Clinical Oncology . 32 (27): 2940–2950. doi :10.1200/JCO.2013.53.5633. PMC 4162493 . PMID 25154822.
- Bachaud, Jean-Marc; Cohen-Jonathan, Elizabeth; Alzieu, Claude; David, Jean-Marc; Serrano, Elie; Daly-Schveitzer, Nicolas (diciembre de 1996). "Radioterapia posoperatoria combinada e infusión semanal de cisplatino para carcinoma de cabeza y cuello localmente avanzado: informe final de un ensayo aleatorizado". Revista internacional de oncología radioterápica, biología y física . 36 (5): 999–1004. doi :10.1016/S0360-3016(96)00430-0. PMID 8985019.
- Bernier, Jacques; Domenge, Christian; Ozsahin, Mahmut; et al. (6 de mayo de 2004). "Irradiación posoperatoria con o sin quimioterapia concomitante para el cáncer de cabeza y cuello localmente avanzado". New England Journal of Medicine . 350 (19): 1945–1952. doi : 10.1056/NEJMoa032641 . PMID 15128894.
- Bernier, Jacques; Cooper, Jay S.; Pajak, TF; et al. (octubre de 2005). "Definición de los niveles de riesgo en cánceres de cabeza y cuello localmente avanzados: un análisis comparativo de ensayos de radioterapia posoperatoria concurrente más quimioterapia de la EORTC (#22931) y RTOG (#9501)". Cabeza y cuello . 27 (10): 843–850. doi :10.1002/hed.20279. PMID 16161069. S2CID 13746453.
- Blanchard, Pierre; Baujat, Bertrand; Holostenco, Victoria; Bourredjem, Abderrahmane; Baey, Charlotte; Bourhis, Jean; Pignon, Jean-Pierre (julio de 2011). "Metaanálisis de la quimioterapia en el cáncer de cabeza y cuello (MACH-NC): un análisis exhaustivo por localización del tumor". Radioterapia y oncología . 100 (1): 33–40. doi :10.1016/j.radonc.2011.05.036. PMID 21684027.
- Bonner, James A; Harari, Paul M; Giralt, Jordi; et al. (enero de 2010). "Radioterapia más cetuximab para el cáncer de cabeza y cuello locoregionalmente avanzado: datos de supervivencia a 5 años de un ensayo aleatorizado de fase 3 y relación entre la erupción inducida por cetuximab y la supervivencia". The Lancet Oncology . 11 (1): 21–28. doi :10.1016/S1470-2045(09)70311-0. PMID 19897418.
- Calais, Gilles; Bardet, Etienne; Señor, cristiano; Alfonsí, Marc; Bourhis, Jean; Rin, Beatrix; Tortochaux, Jacques; Hombre, Yooye Tao Kong; Auvray, Hugues; Garaud, Pascal (enero de 2004). "Radioterapia con docetaxel semanal concomitante para el carcinoma de orofaringe en estadios III/IV. Resultados del ensayo de fase II 98-02 GORTEC". Revista Internacional de Oncología Radioterápica, Biología y Física . 58 (1): 161–166. doi :10.1016/S0360-3016(03)01370-1. PMID 14697434.
- Chen, Allen M; Felix, Carol; Wang, Pin-Chieh; et al. (junio de 2017). "Radioterapia de dosis reducida para el carcinoma de células escamosas de la orofaringe asociado al virus del papiloma humano: un estudio de fase 2 de un solo brazo". The Lancet Oncology (manuscrito enviado). 18 (6): 803–811. doi :10.1016/S1470-2045(17)30246-2. PMC 6488353 . PMID 28434660.
- Chera, Bhishamjit S.; Amdur, Robert J.; Tepper, Joel; et al. (diciembre de 2015). "Ensayo de fase 2 de radioquimioterapia desintensificada para carcinoma de células escamosas orofaríngeo asociado al virus del papiloma humano de riesgo favorable". Revista internacional de oncología radioterápica, biología y física . 93 (5): 976–985. doi :10.1016/j.ijrobp.2015.08.033. PMID 26581135.
- Cmelak, Anthony J.; Li, Sigui; Goldwasser, Meredith A.; Murphy, Barbara; Cannon, Michael; Pinto, Harlan; Rosenthal, David I.; Gillison, Maura; Forastiere, Arlene A. (septiembre de 2007). "Ensayo de fase II de quimiorradiación para la preservación de órganos en carcinomas de células escamosas resecables en estadio III o IV de laringe u orofaringe: resultados del estudio E2399 del Eastern Cooperative Oncology Group". Journal of Clinical Oncology . 25 (25): 3971–3977. doi : 10.1200/JCO.2007.10.8951 . PMID 17761982.
- Cohen, EE; Karrison, TG; Kocherginsky, M; et al. (1 de septiembre de 2014). "Ensayo aleatorizado de fase III de quimioterapia de inducción en pacientes con cáncer de cabeza y cuello localmente avanzado N2 o N3". Journal of Clinical Oncology . 32 (25): 2735–43. doi :10.1200/JCO.2013.54.6309. PMC 4876357 . PMID 25049329.
- Cooper, Jay S.; Pajak, Thomas F.; Forastiere, Arlene A.; et al. (6 de mayo de 2004). "Radioterapia y quimioterapia concurrentes posoperatorias para el carcinoma de células escamosas de alto riesgo de cabeza y cuello". New England Journal of Medicine . 350 (19): 1937–1944. doi : 10.1056/NEJMoa032646 . PMID 15128893.
- Cooper, Jay S.; Zhang, Qiang; Pajak, Thomas F.; et al. (diciembre de 2012). "Seguimiento a largo plazo del ensayo RTOG 9501/Intergroup de fase III: radioterapia y quimioterapia concurrentes posoperatorias en el carcinoma de células escamosas de cabeza y cuello de alto riesgo". Revista internacional de oncología radioterápica, biología y física . 84 (5): 1198–1205. doi :10.1016/j.ijrobp.2012.05.008. PMC 3465463. PMID 22749632 .
- Diaz, Roberto; Jaboin, Jerry J.; Morales-Paliza, Manuel; et al. (junio de 2010). "Hipotiroidismo como consecuencia de la radioterapia de intensidad modulada con quimioterapia concurrente basada en taxanos para el cáncer de cabeza y cuello localmente avanzado". Revista internacional de oncología radioterápica, biología y física . 77 (2): 468–476. doi :10.1016/j.ijrobp.2009.05.018. PMID 19577867.
- Eisbruch, Avraham; Schwartz, Marco; Rasch, Coen; Vineberg, Karen; Damen, Eugene; Van As, Corina J.; Marsh, Robin; Pameijer, Frank A.; Balm, Alfons JM (diciembre de 2004). "Disfagia y aspiración después de la quimiorradioterapia para el cáncer de cabeza y cuello: ¿Qué estructuras anatómicas se ven afectadas y pueden preservarse mediante IMRT?". Revista internacional de oncología radioterápica, biología y física . 60 (5): 1425–1439. doi :10.1016/j.ijrobp.2004.05.050. PMID 15590174.
- Eriksen, JG; Lassen, P.; Overgaard, J. (2010). "¿Todos los pacientes con cáncer de cabeza y cuello se benefician de la radioterapia y el tratamiento concurrente con cetuximab?". The Lancet Oncology . 11 (4): 312–313. doi :10.1016/S1470-2045(10)70035-8. PMID 20359659.
- Givens, Daniel J.; Karnell, Lucy Hynds; Gupta, Anjali K.; Clamon, Gerald H.; Pagedar, Nitin A.; Chang, Kristi E.; Van Daele, Douglas J.; Funk, Gerry F. (21 de diciembre de 2009). "Eventos adversos asociados con la radioquimioterapia concurrente en pacientes con cáncer de cabeza y cuello". Archivos de otorrinolaringología y cirugía de cabeza y cuello . 135 (12): 1209–17. doi : 10.1001/archoto.2009.174 . PMID 20026818.
- Haddad, R; O'Neill, A; Rabinowits, G; et al. (marzo de 2013). "Quimioterapia de inducción seguida de quimiorradioterapia concurrente (quimiorradioterapia secuencial) frente a quimiorradioterapia concurrente sola en el cáncer de cabeza y cuello localmente avanzado (PARADIGM): un ensayo aleatorizado de fase 3". The Lancet Oncology . 14 (3): 257–64. doi :10.1016/S1470-2045(13)70011-1. PMID 23414589.
- Hall, SF; Irish, JC; Gregg, RW; Groome, PA; Rohland, S. (8 de enero de 2015). "Adherencia y adopción de las guías de práctica clínica: lecciones aprendidas de una guía de práctica clínica sobre quimioterapia concomitante con radioterapia en cáncer de cabeza y cuello". Oncología actual . 22 (2): e61–8. doi :10.3747/co.22.2235. PMC 4399625 . PMID 25908922.
- Hall, Stephen F; Liu, Fei-Fei; O'Sullivan, Brian; Shi, Willa; Rohland, Susan; Griffiths, Rebecca; Groome, Patti (22 de agosto de 2017). "¿La adición de quimioterapia concurrente a la radioterapia convencional mejoró la supervivencia de los pacientes con cáncer de orofaringe HPV+ve y HPV−ve? Un estudio poblacional". British Journal of Cancer . 117 (8): 1105–1112. doi :10.1038/bjc.2017.275. PMC 5674099 . PMID 28829763.
- Hunter, Klaudia U.; Schipper, Matthew; Feng, Felix Y.; Lyden, Teresa; Haxer, Mark; Murdoch-Kinch, Carol-Anne; Cornwall, Benjamin; Lee, Connie SY; Chepeha, Douglas B.; Eisbruch, Avraham (marzo de 2013). "Toxicidades que afectan la calidad de vida después de la quimioterapia-IMRT del cáncer orofaríngeo: estudio prospectivo de resultados informados por el paciente, evaluados por el observador y objetivos". Revista internacional de oncología radioterápica, biología y física . 85 (4): 935–940. doi :10.1016/j.ijrobp.2012.08.030. PMC 3556374. PMID 23040224 .
- Machtay, Mitchell; Moughan, Jennifer; Trotti, Andrew; Garden, Adam S.; Weber, Randal S.; Cooper, Jay S.; Forastiere, Arlene; Ang, K. Kian (20 de julio de 2008). "Factores asociados con toxicidad tardía grave después de la quimiorradiación concurrente para el cáncer de cabeza y cuello localmente avanzado: un análisis RTOG". Journal of Clinical Oncology . 26 (21): 3582–3589. doi :10.1200/JCO.2007.14.8841. PMC 4911537 . PMID 18559875.
- Marur, Shanthi; Li, Shuli; Cmelak, Anthony J.; et al. (10 de febrero de 2017). "E1308: Ensayo de fase II de quimioterapia de inducción seguida de radiación de dosis reducida y cetuximab semanal en pacientes con carcinoma de células escamosas resecable asociado al VPH de la orofaringe: Grupo de investigación del cáncer ECOG-ACRIN". Revista de oncología clínica . 35 (5): 490–497. doi :10.1200/JCO.2016.68.3300. PMC 5455313 . PMID 28029303.
- Nguyen-Tan, Phuc Felix; Zhang, Qiang; Ang, K. Kian; et al. (diciembre de 2014). "Ensayo aleatorizado de fase III para evaluar el fraccionamiento acelerado frente al fraccionamiento estándar en combinación con cisplatino concurrente para carcinomas de cabeza y cuello en el ensayo 0129 del Radiation Therapy Oncology Group: informe a largo plazo de eficacia y toxicidad". Journal of Clinical Oncology . 32 (34): 3858–3867. doi :10.1200/JCO.2014.55.3925. PMC 4239304 . PMID 25366680.
- Olson, Brennan; Clayburgh, Daniel R (30 de agosto de 2017). Utilidad de la terapia adyuvante para el carcinoma orofaríngeo pN1 . Presentaciones orales. Reunión anual de la Academia Estadounidense de Otorrinolaringología, Chicago, 10 al 13 de septiembre de 2017. Otorrinolaringología: cirugía de cabeza y cuello . Vol. 157, n.º 1, suplemento pp. P40–P173. doi : 10.1177/0194599817717251d . PMID 28854010.
- Owadally, Waheeda; Hurt, Chris; Timmins, Hayley; et al. (27 de agosto de 2015). "PATHOS: un ensayo de fase II/III de tratamiento adyuvante de intensidad reducida y estratificado por riesgo en pacientes sometidos a cirugía transoral para cáncer orofaríngeo positivo al virus del papiloma humano (VPH)". BMC Cancer . 15 (1): 602. doi : 10.1186/s12885-015-1598-x . PMC 4549836 . PMID 26311526.
- Pignon, Jean-Pierre; le Maître, Aurélie; Bourhis, Jean (octubre de 2007). "Metaanálisis de la quimioterapia en el cáncer de cabeza y cuello (MACH-NC): una actualización". Revista internacional de oncología radioterápica, biología y física . 69 (2): S112–S114. doi :10.1016/j.ijrobp.2007.04.088. PMID 17848275.
- Posner, señor; Lorch, JH; Goloubeva, O.; Bronceado, M.; Schumaker, LM; Sarlis, Nueva Jersey; Haddad, Rhode Island; Cullen, KJ (mayo de 2011). "Supervivencia y virus del papiloma humano en el cáncer de orofaringe en TAX 324: un análisis de subconjunto de un ensayo internacional de fase III". Anales de Oncología . 22 (5): 1071–1077. doi : 10.1093/annonc/mdr006. PMC 4351352 . PMID 21317223.
- Seiwert, T.; Melotek, JM; Foster, CC; Blair, EA; Karrison, TG; Agrawal, N.; Portugal, L.; Gooi, Z.; Stenson, KM; Brisson, RJ; Arshad, S.; Dekker, A.; Kochanny, S.; Saloura, V.; Spiotto, MT; Villaflor, VM; Haraf, DJ; Vokes, EE (abril de 2018). "OPTIMA: un ensayo de fase 2 de reducción de dosis y volumen de radioterapia estratificada según la respuesta a la quimioterapia de inducción para el cáncer orofaríngeo HPV+: eficacia, toxicidad y análisis del subtipo de HPV". Revista internacional de oncología radioterápica, biología y física . 100 (5): 1309. doi : 10.1016/j.ijrobp.2017.12.025 .
- Su, William; Liu, Jerry; Miles, Brett A.; Genden, Eric M.; Misiukiewicz, Krzysztof J.; Posner, Marshall; Gupta, Vishal; Bakst, Richard L.; Chu, Pei-Yi (8 de diciembre de 2016). "Radioterapia adyuvante sola para cánceres orofaríngeos relacionados con el VPH con características de alto riesgo". PLOS One . 11 (12): e0168061. Bibcode :2016PLoSO..1168061S. doi : 10.1371/journal.pone.0168061 . PMC 5145232 . PMID 27930732.
- Szturz, Petr; Seiwert, Tanguy Y.; Vermorken, Jan B. (10 de julio de 2017). "¿Qué tan estándar es el cetuximab de segunda línea en el cáncer de cabeza y cuello recurrente o metastásico en 2017?". Journal of Clinical Oncology . 35 (20): 2229–2231. doi :10.1200/JCO.2016.71.8072. PMID 28471725.
- Vlacich, Gregory; Spratt, Daniel E.; Diaz, Roberto; Phillips, John G.; Crass, Jostin; Li, Chung-I; Shyr, Yu; Cmelak, Anthony J. (marzo de 2014). "La dosis en el constrictor faríngeo inferior predice una dependencia prolongada de la sonda de gastrostomía con radioterapia y quimioterapia de intensidad modulada concurrentes para el cáncer de cabeza y cuello localmente avanzado". Radioterapia y oncología . 110 (3): 435–440. doi :10.1016/j.radonc.2013.12.007. PMID 24440043.
- Wirth, Lori J. (20 de abril de 2016). "Cetuximab en el carcinoma orofaríngeo positivo para el virus del papiloma humano". Journal of Clinical Oncology . 34 (12): 1289–1291. doi :10.1200/JCO.2015.65.1414. PMID 26884569.
Desintensificación
- An, Yi; Holsinger, F. Christopher; Husain, Zain A. (20 de diciembre de 2016). "Desintensificación de la terapia adyuvante en el cáncer orofaríngeo asociado al virus del papiloma humano". Cánceres de cabeza y cuello (revisión). 1 (1): 18. doi : 10.1186/s41199-016-0016-7 . PMC 6460758. PMID 31093347 .
- Arnaoutakis, Demetri; Sumer, Baran D. (10 de agosto de 2017). "Desintensificación del tratamiento para el cáncer orofaríngeo asociado al virus del papiloma humano". Anales de oncología quirúrgica . 24 (12): 3463–3465. doi : 10.1245/s10434-017-6045-6 . PMID 28799138.
- Brotherston, Drew C.; Poon, Ian; Le, Tuyen; Leung, Martin; Kiss, Alex; Ringash, Jolie; Balogh, Judith; Lee, Justin; Wright, James R. (febrero de 2013). "Preferencias de los pacientes para la reducción del tratamiento del cáncer orofaríngeo". Cabeza y cuello . 35 (2): 151–159. doi :10.1002/hed.22930. PMID 22431201. S2CID 30301638.
- Chera, Bhishamjit S.; Amdur, Robert J. (enero de 2018). "Estado actual y direcciones futuras de la desintensificación del tratamiento en el carcinoma escamocelular orofaríngeo asociado al virus del papiloma humano". Seminarios en oncología radioterápica . 28 (1): 27–34. doi :10.1016/j.semradonc.2017.08.001. PMID 29173753.
- Kelly, Jacqueline R.; Husain, Zain A.; Burtness, Barbara (noviembre de 2016). "Estrategias de desintensificación del tratamiento para el cáncer de cabeza y cuello". Revista Europea del Cáncer . 68 : 125–133. doi :10.1016/j.ejca.2016.09.006. PMC 5734050 . PMID 27755996.
- Mamá, DJ; Precio, K.; Moore, EJ; Patel, SH; Hinni, ML; Chintakuntlawar, AV; García, JJ; Graner, D.; Neben-Wittich, MA; Garcés, Y.; Hallemeier, CL; Precio, DL; Kasperbauer, JL; Jano, JR; Fomentar, NR; Foote, RL (diciembre de 2017). "Resultados de dos años para MC1273, una evaluación de fase 2 de reducción agresiva de la dosis para quimiorradiación adyuvante en el carcinoma de células escamosas de orofaringe + VPH (OPSCC)". Revista Internacional de Oncología Radioterápica, Biología y Física . 99 (5): 1320. doi :10.1016/j.ijrobp.2017.09.021.
- Masterson, L; Moualed, D; Liu, ZW; et al. (octubre de 2014). "Protocolos de tratamiento de desescalada para el carcinoma de células escamosas orofaríngeo asociado al virus del papiloma humano: una revisión sistemática y un metaanálisis de los ensayos clínicos actuales". Revista Europea del Cáncer . 50 (15): 2636–48. doi :10.1016/j.ejca.2014.07.001. PMID 25091798.
- Mirghani, H.; Amen, F.; Blanchard, P.; Moreau, F.; Guigay, J.; Hartl, DM; Lacau St Guily, J. (abril de 2015). "Reducción de la dosis del tratamiento en el carcinoma orofaríngeo positivo al VPH: ensayos en curso, cuestiones críticas y perspectivas". Revista internacional del cáncer . 136 (7): 1494–1503. doi : 10.1002/ijc.28847 . PMID 24622970. S2CID 21854274.
- Mirghani, Haitham; Blanchard, Pierre (enero de 2018). "Reducción del tratamiento para el cáncer orofaríngeo provocado por el VPH: ¿dónde nos encontramos?". Oncología radioterapéutica clínica y traslacional . 8 : 4–11. doi :10.1016/j.ctro.2017.10.005. PMC 5862680. PMID 29594236 .
- Quon, Harry; Richmon, Jeremy D. (agosto de 2012). "Estrategias de desintensificación del tratamiento para carcinomas de cabeza y cuello asociados al VPH". Clínicas otorrinolaringológicas de Norteamérica . 45 (4): 845–861. doi :10.1016/j.otc.2012.04.007. PMID 22793856.
Pronóstico
- Al-Mamgani, Abrahim; van Werkhoven, Erik; Navran, Arash; Karakullukcu, Baris; Hamming-Vrieze, Olga; Machiels, Melanie; van der Velden, Lilly-Ann; Vogel, Wouter V.; Klop, W. Martin (septiembre de 2017). "Recurrencia regional contralateral después de la irradiación unilateral electiva del cuello en el carcinoma de orofaringe: una revisión crítica basada en la literatura". Reseñas de tratamientos contra el cáncer . 59 : 102-108. doi :10.1016/j.ctrv.2017.07.004. PMID 28779635.
- Ang, KK; Harris, J.; Wheeler, R.; et al. (2010). "Virus del papiloma humano y supervivencia de pacientes con cáncer orofaríngeo". New England Journal of Medicine . 363 (1): 24–35. doi :10.1056/NEJMoa0912217. PMC 2943767 . PMID 20530316.
- Bhattasali, O.; Thompson, LD; Schumacher, A.; Iganej, S. (abril de 2018). "Factores pronósticos radiográficos nodales en el nuevo cáncer orofaríngeo en estadio I positivo para p16 de la 8.ª edición del AJCC: ¿todas las enfermedades N1 son iguales?". Revista internacional de oncología radioterápica, biología y física . 99 (2): S137. doi : 10.1016/j.ijrobp.2017.06.317 .
- Chernock, RD; El-mofty, SK; Thorstad, WL; Parvin, CA; Lewis, JS (2009). "Carcinoma de células escamosas no queratinizante relacionado con el VPH de la orofaringe: utilidad de las características microscópicas para predecir el resultado del paciente". Patología de cabeza y cuello . 3 (3): 186–194. doi :10.1007/s12105-009-0126-1. PMC 2811624 . PMID 20596971.
- Fakhry, Carole; Zhang, Qiang; Nguyen-Tân, Phuc Felix; et al. (4 de agosto de 2017). "Desarrollo y validación de nomogramas predictivos de supervivencia global y libre de progresión en pacientes con cáncer orofaríngeo". Journal of Clinical Oncology . 35 (36): 4057–4065. doi :10.1200/JCO.2016.72.0748. PMC 5736236 . PMID 28777690.
- Fischer, CA; Kampmann, M.; Zlobec, I.; Green, E.; Tornillo, L.; Lugli, A.; Wolfensberger, M.; Terracciano, LM (27 de abril de 2010). "Expresión de p16 en el cáncer orofaríngeo: su impacto en la estadificación y el pronóstico en comparación con los parámetros de estadificación clínica convencionales" (PDF) . Anales de Oncología . 21 (10): 1961–1966. doi : 10.1093/annonc/mdq210 . PMID 20423915.
- Gillison, Maura L. (20 de diciembre de 2006). "Virus del papiloma humano y pronóstico del carcinoma escamocelular orofaríngeo: implicaciones para la investigación clínica en cánceres de cabeza y cuello". Journal of Clinical Oncology (Editorial). 24 (36): 5623–5625. doi : 10.1200/JCO.2006.07.1829 . PMID 17179099.
- Gillison, Maura L.; Zhang, Qiang; Jordan, Richard; Xiao, Weihong; Westra, William H.; Trotti, Andy; Spencer, Sharon; Harris, Jonathan; Chung, Christine H.; Ang, K. Kian (10 de junio de 2012). "Fumar tabaco y mayor riesgo de muerte y progresión en pacientes con cáncer orofaríngeo p16-positivo y p16-negativo". Journal of Clinical Oncology . 30 (17): 2102–2111. doi :10.1200/JCO.2011.38.4099. PMC 3397696 . PMID 22565003.
- Hafkamp, Harriët C.; Manni, JJ; Haesevoets, A.; Voogd, AC; Schepers, M.; Bot, FJ; Hopman, AHN; Ramaekers, FCS; Speel, Ernst-Jan M. (15 de junio de 2008). "Marcas diferencias en la tasa de supervivencia entre fumadores y no fumadores con carcinomas de amígdalas asociados al VPH 16". Revista Internacional de Cáncer . 122 (12): 2656–2664. doi : 10.1002/ijc.23458 . PMID 18360824. S2CID 25320075.
- Haughey, Bruce H.; Sinha, Parul (septiembre de 2012). "Factores pronósticos y supervivencia exclusivos del cáncer orofaríngeo p16+ tratado quirúrgicamente". The Laryngoscope . 122 (S2): S13–S33. doi :10.1002/lary.23493. PMID 22926949. S2CID 31772853.
- Huang, Shao Hui; Waldron, John N.; Milosevic, Michael; et al. (15 de febrero de 2015). "Valor pronóstico de los neutrófilos, monocitos y linfocitos circulantes previos al tratamiento en el cáncer orofaríngeo estratificado por estado del virus del papiloma humano". Cáncer . 121 (4): 545–555. doi : 10.1002/cncr.29100 . PMID 25336438. S2CID 926930.
- Huang, K.; Banerjee, RN; Debenham, B.; Patel, A.; Sabiq, F.; Harold, L.; Skarsgard, DP; Lysack, J.; Ghosh, S.; Quon, HC (abril de 2018). "¿Qué pasa con los ganglios linfáticos enmarañados? Importancia de los ganglios linfáticos enmarañados en el carcinoma de células escamosas orofaríngeo relacionado con el VPH: un estudio de cohorte poblacional multiinstitucional". Revista internacional de oncología radioterápica, biología y física . 100 (5): 1328. doi : 10.1016/j.ijrobp.2017.12.059 .
- de Jong, MC; Pramana, J.; Knegjens, JL; Balm, AJM; Van Den Brekel, MWM; Hauptmann, M.; Begg, AC; Rasch, CRN (24 de marzo de 2010). "Los perfiles de expresión de genes de alto riesgo y de VPH predicen la respuesta a la quimiorradioterapia en el cáncer de cabeza y cuello, independientemente de los factores clínicos". Radioterapia y Oncología . 95 (3): 365–370. doi :10.1016/j.radonc.2010.02.001. ISSN 1879-0887. PMID 20346528.
- Kato, Masanari G.; Ellis, Mark A.; Nguyen, Shaun A.; Day, Terry A. (febrero de 2018). "Predictores de enfermedad ganglionar contralateral-bilateral en cáncer orofaríngeo: un estudio de la base de datos nacional sobre cáncer". Cabeza y cuello . 40 (2): 338–348. doi :10.1002/hed.24964. PMID 28963823. S2CID 10627950.
- Lewis, James S; Carpenter, Danielle H; Thorstad, Wade L; Zhang, Qin; Haughey, Bruce H (24 de junio de 2011). "La extensión extracapsular es un mal predictor de recurrencia de la enfermedad en el carcinoma de células escamosas orofaríngeo tratado quirúrgicamente". Patología moderna . 24 (11): 1413–1420. doi :10.1038/modpathol.2011.105. PMC 3925389 . PMID 21701534.
- Licitra, Lisa; Perrone, Federica; Bossi, Paolo; et al. (20 de diciembre de 2006). "El virus del papiloma humano de alto riesgo afecta el pronóstico en pacientes con carcinoma escamocelular orofaríngeo tratado quirúrgicamente". Journal of Clinical Oncology . 24 (36): 5630–5636. doi : 10.1200/JCO.2005.04.6136 . PMID 17179101.
- Lowy, D.; Munger, K. (2010). "Implicaciones pronósticas del VPH en el cáncer orofaríngeo". The New England Journal of Medicine (Editorial). 363 (1): 82–84. doi :10.1056/NEJMe1003607. PMID 20530315.
- Martel, María; Alemany, Laia; Taberna, Miren; Mena, Marisa; Todos, Sara; Bagué, Silvia; Castellsagué, Xavier; Quer, Miquel; León, Xavier (enero 2017). "El papel del VPH sobre el riesgo de segunda neoplasia primaria en pacientes con carcinoma de orofaringe". Oncología Bucal . 64 : 37–43. doi :10.1016/j.oraloncology.2016.11.011. PMID 28024722.
- Maxwell, JH; Kumar, B.; Feng, FY; et al. (9 de febrero de 2010). "El consumo de tabaco en pacientes con cáncer de orofaringe avanzado positivo al virus del papiloma humano se relaciona con un mayor riesgo de metástasis a distancia y recurrencia tumoral". Clinical Cancer Research . 16 (4): 1226–1235. doi :10.1158/1078-0432.CCR-09-2350. PMC 2822887 . PMID 20145161.
- Maxwell, Jessica H.; Ferris, Robert L.; Gooding, William; Cunningham, Diana; Mehta, Vikas; Kim, Seungwon; Myers, Eugene N.; Johnson, Jonas; Chiosea, Simion (septiembre de 2013). "Propagación extracapsular en carcinoma de cabeza y cuello: impacto del sitio y estado del virus del papiloma humano". Cáncer . 119 (18): 3302–3308. CiteSeerX 10.1.1.663.564 . doi :10.1002/cncr.28169. PMID 23797868. S2CID 32595866.
- Nguyen, Nam P.; Ly, Bevan Hong; Betz, Michael; Vinh-Hung, Vincent (18 de junio de 2010). "Importancia de la edad como factor pronóstico del carcinoma amigdalino". Anales de oncología quirúrgica . 17 (10): 2570–2577. doi :10.1245/s10434-010-1167-0. PMID 20559738. S2CID 8833627.
- O'Sullivan, Brian; Huang, Shao Hui; Siu, Lillian L.; et al. (10 de febrero de 2013). "Subgrupos de candidatos a desintensificación en el cáncer orofaríngeo relacionado con el virus del papiloma humano según el riesgo mínimo de metástasis a distancia". Journal of Clinical Oncology . 31 (5): 543–550. doi : 10.1200/JCO.2012.44.0164 . PMID 23295795.
- Ragin, Camille CR; Taioli, Emanuela (15 de octubre de 2007). "Supervivencia del carcinoma de células escamosas de cabeza y cuello en relación con la infección por el virus del papiloma humano: revisión y metanálisis". Revista Internacional del Cáncer . 121 (8): 1813–1820. doi : 10.1002/ijc.22851 . PMID 17546592. S2CID 23657353.
- Rischin, Danny; Young, Richard J.; Fisher, Richard; et al. (20 de septiembre de 2010). "Importancia pronóstica de p16INK4A y el virus del papiloma humano en pacientes con cáncer orofaríngeo tratados en el ensayo de fase III TROG 02.02". Journal of Clinical Oncology . 28 (27): 4142–4148. doi :10.1200/JCO.2010.29.2904. PMC 2953971 . PMID 20697079.
- Routman, David M.; Funk, Ryan K.; Tangsriwong, Kanograt; et al. (junio de 2017). "Tasas de recaída con cirugía sola en el cáncer de células escamosas de orofaringe de riesgo intermedio y alto relacionado con el virus del papiloma humano: una revisión multiinstitucional". Revista internacional de oncología radioterápica, biología y física . 99 (4): 938–946. doi :10.1016/j.ijrobp.2017.06.2453. PMID 28847412.
- Sinha, Parul; Lewis, James S.; Piccirillo, Jay F.; Kallogjeri, Dorina; Haughey, Bruce H. (15 de julio de 2012). "Propagación extracapsular y terapia adyuvante en carcinoma orofaríngeo positivo para p16 relacionado con el virus del papiloma humano". Cáncer . 118 (14): 3519–3530. doi : 10.1002/cncr.26671 . PMID 22086669. S2CID 28111538.
- Sinha, P.; Thorstad, WT; Nussenbaum, B.; Haughey, BH; Adkins, DR; Kallogjeri, D.; Lewis Jr., JS (enero de 2014). "Metástasis distante en carcinoma de células escamosas orofaríngeo positivo para p16: un análisis crítico de patrones y resultados". Oral Oncology . 50 (1): 45–51. doi :10.1016/j.oraloncology.2013.10.007. PMC 3942323 . PMID 24211084.
- Sinha, Parul; Kallogjeri, Dorina; Gay, Hiram; Thorstad, Wade L.; Lewis, James S.; Chernock, Rebecca; Nussenbaum, Brian; Haughey, Bruce H. (mayo de 2015). "Un elevado número de ganglios metastásicos, no la propagación extracapsular o la clasificación N, es un factor pronóstico relacionado con los ganglios en el cáncer de orofaringe positivo para p16 resecado transoralmente y diseccionado en el cuello". Oral Oncology . 51 (5): 514–520. doi :10.1016/j.oraloncology.2015.02.098. PMID 25771076.
- Trosman, Samuel J.; Koyfman, Shlomo A.; Ward, Matthew C.; et al. (1 de mayo de 2015). "Efecto del virus del papiloma humano en los patrones de falla metastásica distante en el carcinoma de células escamosas orofaríngeo tratado con quimiorradioterapia". JAMA Otolaryngology–Head & Neck Surgery . 141 (5): 457–62. doi : 10.1001/jamaoto.2015.136 . PMID 25742025.
- Ward, MJ; Thirdborough, SM; Mellows, T; et al. (29 de octubre de 2013). "Los linfocitos infiltrantes de tumores predicen el resultado en el cáncer orofaríngeo positivo al VPH". British Journal of Cancer . 110 (2): 489–500. doi :10.1038/bjc.2013.639. PMC 3899750 . PMID 24169344.
Epidemiología
- Anantharaman, Devasena; Muller, David C; Lagiou, Pagona; et al. (junio de 2016). "Efectos combinados del tabaquismo y el VPH16 en el cáncer orofaríngeo". Revista Internacional de Epidemiología . 45 (3): 752–761. doi :10.1093/ije/dyw069. PMC 5841602 . PMID 27197530.
- Chaturvedi, A.; Engels, E.; Anderson, W.; Gillison, M. (febrero de 2008). "Tendencias de incidencia de carcinomas de células escamosas orales relacionados y no relacionados con el virus del papiloma humano en los Estados Unidos". Journal of Clinical Oncology . 26 (4): 612–619. doi : 10.1200/JCO.2007.14.1713 . PMID 18235120.
- Chaturvedi, Anil K.; Engels, Eric A.; Pfeiffer, Ruth M.; et al. (10 de noviembre de 2011). "Virus del papiloma humano y aumento de la incidencia del cáncer orofaríngeo en los Estados Unidos". Journal of Clinical Oncology . 29 (32): 4294–4301. doi :10.1200/JCO.2011.36.4596. PMC 3221528 . PMID 21969503.
- Chaturvedi, Anil K.; Anderson, William F.; Lortet-Tieulent, Joannie; Curado, Maria Paula; Ferlay, Jacques; Franceschi, Silvia; Rosenberg, Philip S.; Bray, Freddie; Gillison, Maura L. (20 de diciembre de 2013). "Tendencias mundiales en las tasas de incidencia de cánceres de cavidad oral y orofaríngeos". Journal of Clinical Oncology . 31 (36): 4550–4559. doi :10.1200/JCO.2013.50.3870. PMC 3865341 . PMID 24248688.
- Chenevert, J; Chiosea, S (enero de 2012). "Incidencia del virus del papiloma humano en carcinomas de células escamosas orofaríngeos: ahora y hace 50 años". Patología humana . 43 (1): 17–22. doi :10.1016/j.humpath.2011.03.009. PMID 21777945.
- Cook, M.; Dawsey, S.; Freedman, N.; Inskip, P.; Wichner, S.; Quraishi, S.; Devesa, S. ; McGlynn, K. (2009). "Disparidades de género en la incidencia del cáncer por período de tiempo y edad". Epidemiología del cáncer, biomarcadores y prevención . 18 (4): 1174–1182. doi :10.1158/1055-9965.EPI-08-1118. PMC 2793271 . PMID 19293308.
- Dayyani, Farshid; Etzel, Carol J; Liu, Mei; Ho, Chung-Han; Lippman, Scott M; Tsao, Anne S (2010). "Metaanálisis del impacto del virus del papiloma humano (VPH) en el riesgo de cáncer y la supervivencia general en carcinomas de células escamosas de cabeza y cuello (HNSCC)". Oncología de cabeza y cuello . 2 (1): 15. doi : 10.1186/1758-3284-2-15 . PMC 2908081 . PMID 20587061.
- D'Souza, G.; Kreimer, A.; Viscidi, R.; Pawlita, M.; Fakhry, C.; Koch, W.; Westra, W.; Gillison, M. (mayo de 2007). "Estudio de casos y controles del virus del papiloma humano y cáncer de orofaringe". La Revista de Medicina de Nueva Inglaterra . 356 (19): 1944-1956. doi : 10.1056/NEJMoa065497 . ISSN 0028-4793. PMID 17494927. S2CID 18819678.
- de Martel, Catherine; Ferlay, Jacques; Franceschi, Silvia; Vignat, Jérôme; Bray, Freddie; Forman, David; Plummer, Martyn (junio de 2012). "Carga mundial de cánceres atribuibles a infecciones en 2008: una revisión y un análisis sintético". The Lancet Oncology . 13 (6): 607–615. doi :10.1016/S1470-2045(12)70137-7. PMID 22575588.
- de Martel, Catherine; Plummer, Martyn; Vignat, Jerome; Franceschi, Silvia (15 de agosto de 2017). "Carga mundial de cáncer atribuible al VPH por sitio, país y tipo de VPH". Revista Internacional del Cáncer . 141 (4): 664–670. doi :10.1002/ijc.30716. PMC 5520228 . PMID 28369882.
- Ernster, J.; Sciotto, C.; O'Brien, M.; Finch, J.; Robinson, L.; Willson, T.; Mathews, M. (diciembre de 2007). "Aumento de la incidencia del cáncer orofaríngeo y el papel del virus del papiloma humano oncogénico". The Laryngoscope . 117 (12): 2115–2128. doi :10.1097/MLG.0b013e31813e5fbb. ISSN 0023-852X. PMID 17891052. S2CID 38017888.
- Forman, David; de Martel, Catherine; Lacey, Charles J.; et al. (noviembre de 2012). "Carga mundial del virus del papiloma humano y enfermedades relacionadas". Vacuna . 30 : F12–F23. doi :10.1016/j.vaccine.2012.07.055. PMID 23199955. S2CID 30694437.
- Gillison, Maura L.; Chaturvedi, Anil K.; Anderson, William F.; Fakhry, Carole (10 de octubre de 2015). "Epidemiología del carcinoma de células escamosas de cabeza y cuello con virus del papiloma humano positivo". Journal of Clinical Oncology . 33 (29): 3235–3242. doi :10.1200/JCO.2015.61.6995. PMC 4979086 . PMID 26351338.
- Habbous, Steven; Chu, Karen P.; Lau, Harold; et al. (13 de agosto de 2017). "Virus del papiloma humano en cáncer orofaríngeo en Canadá: análisis de 5 centros oncológicos integrales mediante imputación múltiple". Revista de la Asociación Médica Canadiense . 189 (32): E1030–E1040. doi :10.1503/cmaj.161379. PMC 5555753 . PMID 28808115.
- Hammarstedt, L.; Lindquist, D.; Dahlstrand, H.; et al. (diciembre de 2006). "El virus del papiloma humano como factor de riesgo para el aumento de la incidencia del cáncer de amígdalas". Revista Internacional del Cáncer . 119 (11): 2620–2623. doi : 10.1002/ijc.22177 . ISSN 0020-7136. PMID 16991119. S2CID 20541360.
- Heck, Julia E; Berthiller, Julien; Vaccarella, Salvatore; et al. (febrero de 2010). "Comportamientos sexuales y riesgo de cáncer de cabeza y cuello: un análisis agrupado en el consorcio de Epidemiología Internacional del Cáncer de Cabeza y Cuello (INHANCE)". Revista Internacional de Epidemiología . 39 (1): 166–181. doi :10.1093/ije/dyp350. PMC 2817092 . PMID 20022926.
- Hemminki, K; Dong, C; Frisch, M (diciembre de 2000). "Cáncer de las amígdalas y otros cánceres del tracto aerodigestivo superior entre pacientes con cáncer de cuello uterino y sus maridos". Revista Europea de Prevención del Cáncer . 9 (6): 433–437. doi :10.1097/00008469-200012000-00010. PMID 11201683. S2CID 10517792.
- Hong, Angela M.; Grulich, Andrew E.; Jones, Deanna; Lee, C. Soon; Garland, Suzanne M.; Dobbins, Timothy A.; Clark, Jonathan R.; Harnett, Gerald B.; Milross, Christopher G.; O'Brien, Christopher J.; Rose, Barbara R. (abril de 2010). "Carcinoma de células escamosas de la orofaringe en varones australianos inducido por dianas de la vacuna contra el virus del papiloma humano". Vaccine . 28 (19): 3269–3272. doi :10.1016/j.vaccine.2010.02.098. PMID 20226244.
- Hong, Angela; Lee, C. Soon; Jones, Deanna; et al. (mayo de 2016b). "Aumento de la prevalencia del cáncer orofaríngeo relacionado con el virus del papiloma humano en Australia durante las últimas dos décadas". Head & Neck . 38 (5): 743–750. doi :10.1002/hed.23942. PMID 25521312. S2CID 1974978.
- Hwang, Tzer-Zen; Hsiao, Jenn-Ren; Tsai, Chia-Rung; Chang, Jeffrey S. (15 de julio de 2015). "Tendencias de incidencia del cáncer de cabeza y cuello relacionado con el virus del papiloma humano en Taiwán, 1995-2009". Revista Internacional del Cáncer . 137 (2): 395–408. doi : 10.1002/ijc.29330 . PMID 25395239. S2CID 20551422.
- Jemal, A.; Siegel, R.; Ward, E.; Hao, Y.; Xu, J.; Murray, T.; Thun, MJ (28 de enero de 2008). "Estadísticas de cáncer, 2008". CA: A Cancer Journal for Clinicians . 58 (2): 71–96. doi : 10.3322/CA.2007.0010 . PMID 18287387. S2CID 43737426.
- Marur, S.; D'souza, G.; Westra, WH; Forastiere, AA (2010). "Cáncer de cabeza y cuello asociado al VPH: una epidemia de cáncer relacionada con el virus". The Lancet Oncology . 11 (8): 781–789. doi :10.1016/S1470-2045(10)70017-6. PMC 5242182 . PMID 20451455.
- Näsman, A.; Atner, P.; Hammarstedt, L.; et al. (Julio de 2009). "Incidencia de carcinoma de amígdalas positivo para el virus del papiloma humano (VPH) en Estocolmo, Suecia: ¿una epidemia de carcinoma inducido por virus?". Revista Internacional de Cáncer . 125 (2): 362–366. doi : 10.1002/ijc.24339 . PMID 19330833. S2CID 36268685.
- Salem, A. (2010). "Descartando los vínculos entre el VPH y el cáncer de lengua agresivo en pacientes jóvenes". Anales de Oncología . 21 (1): 13–17. doi : 10.1093/annonc/mdp380 . PMID 19825879.
- Schwartz, SM; Daling, JR; Madeleine, MM; et al. (4 de noviembre de 1998). "Riesgo de cáncer oral en relación con la historia sexual y la evidencia de infección por el virus del papiloma humano". Revista JNCI del Instituto Nacional del Cáncer . 90 (21): 1626–1636. doi : 10.1093/jnci/90.21.1626 . PMID 9811312.
- Siegel, Rebeca; Naishadham, Deepa; Jemal, Ahmedin (enero de 2013). "Estadísticas del cáncer, 2013". CA: una revista sobre el cáncer para médicos . 63 (1): 11–30. doi : 10.3322/caac.21166 . PMID 23335087. S2CID 24926725.
- Siegel, Rebecca L.; Miller, Kimberly D.; Jemal, Ahmedin (enero de 2015). "Estadísticas de cáncer, 2015". CA: A Cancer Journal for Clinicians . 65 (1): 5–29. doi : 10.3322/caac.21254 . PMID 25559415. S2CID 10193624.
- Siegel, Rebecca L.; Miller, Kimberly D.; Jemal, Ahmedin (enero de 2017). "Estadísticas de cáncer, 2017". CA: A Cancer Journal for Clinicians . 67 (1): 7–30. doi : 10.3322/caac.21387 . PMID 28055103.
- Smith, E.; Ritchie, J.; Summersgill, K.; Klussmann, J.; Lee, J.; Wang, D.; Haugen, T.; Turek, L. (febrero de 2004). "Edad, comportamiento sexual e infección por virus del papiloma humano en cánceres de cavidad oral y orofaríngeos". Revista Internacional del Cáncer . 108 (5): 766–772. doi :10.1002/ijc.11633. ISSN 0020-7136. PMID 14696105. S2CID 25146008.
- Sturgis, E.; Cinciripini, P. (octubre de 2007). "Tendencias en la incidencia del cáncer de cabeza y cuello en relación con la prevalencia del tabaquismo: ¿una epidemia emergente de cánceres asociados al virus del papiloma humano?". Cáncer . 110 (7): 1429–1435. doi : 10.1002/cncr.22963 . ISSN 0008-543X. PMID 17724670. S2CID 20189903.
- Sturgis, EM; Ang, KK (1 de junio de 2011). "La epidemia de cáncer orofaríngeo asociado al VPH ya está aquí: ¿es hora de cambiar nuestros paradigmas de tratamiento?". Journal of the National Comprehensive Cancer Network . 9 (6): 665–73. doi :10.6004/jnccn.2011.0055. PMID 21636538.
- Tachezy, R (mayo de 2005). "VPH y otros factores de riesgo de cáncer de cavidad oral/orofaringe en la República Checa". Oral Diseases . 11 (3): 181–185. doi :10.1111/j.1601-0825.2005.01112.x. PMID 15888110.
- Tezal, Mine; Sullivan Nasca, Maureen; Stoler, Daniel L.; Melendy, Thomas; Hyland, Andrew; Smaldino, Philip J.; Rigual, Nestor R.; Loree, Thom R. (1 de abril de 2009). "Sinergia entre periodontitis crónica y virus del papiloma humano en la base de los cánceres de lengua". Archivos de otorrinolaringología y cirugía de cabeza y cuello . 135 (4): 391–6. doi : 10.1001/archoto.2009.6 . PMID 19380363.
- Tezal, M.; Sullivan, MA; Hyland, A.; et al. (10 de septiembre de 2009). "Periodontitis crónica e incidencia del carcinoma de células escamosas de cabeza y cuello". Epidemiología del cáncer, biomarcadores y prevención . 18 (9): 2406–2412. doi : 10.1158/1055-9965.EPI-09-0334 . PMID 19745222.
- Viens, Laura J.; Henley, S. Jane; Watson, Meg; Markowitz, Lauri E.; Thomas, Cheryll C.; Thompson, Trevor D.; Razzaghi, Hilda; Saraiya, Mona (8 de julio de 2016). "Cánceres asociados al virus del papiloma humano: Estados Unidos, 2008-2012". MMWR. Informe semanal de morbilidad y mortalidad . 65 (26): 661–666. doi : 10.15585/mmwr.mm6526a1 . PMID: 27387669.
Libros y actas de congresos
- Bernier , Jacques, ed. (2016). Cáncer de cabeza y cuello: tratamiento multimodal. Springer International Publishing . ISBN 978-3-319-27601-4.
- Brierley, JD; Gospodarowicz, MK; Wittekind, Ch., eds. (2017). Clasificación TNM de tumores malignos (8.ª ed.). Chichester, West Sussex, Reino Unido: Wiley-Blackwell . ISBN 978-1-4443-3241-4.
- Cardesa, Antonio; Slootweg, Pieter J.; Gale, Nina; Franchi, Alessandro, eds. (2017). Patología de la cabeza y el cuello (2ª ed.). Saltador . ISBN 978-3-662-49672-5.
- Golusiński, Wojciech; Leemans, C. René; Dietz, Andreas, eds. (2017). Infección por VPH en cáncer de cabeza y cuello. Resultados recientes en investigación sobre el cáncer. Vol. 206. Springer . ISBN 978-3-319-43580-0.
- DeVita, Vincent T. ; Lawrence, Theodore S.; Rosenberg, Steven A., eds. (2008) [1982]. Cáncer: principios y práctica de la oncología (8.ª ed.) de DeVita, Hellman y Rosenberg. Filadelfia: Lippincott Williams & Wilkins . ISBN 978-0-7817-7207-5.
- Hayat, MA, ed. (2010). Métodos de diagnóstico, tratamiento y pronóstico del cáncer: Volumen 7: Panorama general, cáncer de cabeza y cuello y cáncer de tiroides. Springer Science & Business Media . ISBN 978-90-481-3186-0.
- Kerr, David J. ; Haller, Daniel G.; van de Velde, Cornelis JH; Baumann, Michael, eds. (2016) [1995]. Oxford Textbook of Oncology (3.ª ed.). Oxford University Press . ISBN 978-0-19-965610-3.
- Myers, Jeffrey N.; Sturgis, Erich M., eds. (2013). Cáncer de cavidad oral y orofaringe, un número de Otolaryngologic Clinics, libro electrónico. Elsevier Health Sciences . ISBN 978-0-323-18632-2.
- Olshan, Andrew F., ed. (2010). Epidemiología, patogenia y prevención del cáncer de cabeza y cuello. Springer Science & Business Media . ISBN 978-1-4419-1471-2.
- Sobin, LH; Gospodarowicz, MK; Wittekind, Ch., eds. (2010). Clasificación TNM de tumores malignos (7.ª ed.). Chichester, West Sussex, Reino Unido: Wiley-Blackwell . ISBN 978-1-4443-3241-4.
- Standring, Susan , ed. (2015). Anatomía de Gray: la base anatómica de la práctica clínica (41.ª ed.). Elsevier Health Sciences . ISBN 978-0-7020-6851-5., véase también Anatomía de Gray
Capítulos, monografías, informes y tesis
- Bruni, L; Barrionuevo-Rosas, L; Albero, G; Serrano, B; Mena, M; Gómez, D; Muñoz, J; Bosch, FX; de Sanjosé, S (7 de julio de 2017). Virus del papiloma humano y enfermedades relacionadas en el mundo (PDF) . HPVIC . Consultado el 11 de agosto de 2017 ., en HPVIC (2017)
- Chaturvedi, Anil; Gillison, Maura L. (4 de marzo de 2010). Virus del papiloma humano y cáncer de cabeza y cuello. Springer. Págs. 87–116. ISBN 978-1-4419-1471-2., en Olshan (2010)
- Chung, Christine H; Dietz, Andreas; Gregoire, Vincent; et al. (2016). Cáncer de cabeza y cuello. Oxford University Press. págs. 329–364. ISBN 9780199656103., en Kerr et al (2016)
- Hammarstedt, Lalle (25 de abril de 2008), Cáncer de amígdalas: incidencia, prevalencia del VPH y supervivencia (tesis doctoral), Estocolmo: Departamento de Neurociencia Clínica, Instituto Karolinska , ISBN 978-91-7357-587-4, consultado el 3 de junio de 2017
- McHanwell, Stephen (7 de agosto de 2015). Faringe. Elsevier Health Sciences. págs. 571–585. ISBN 9780702068515., en Standring (2015)
- Helliwell, T; Woolgar, JA (1998). Estándares y conjuntos de datos mínimos para informar sobre cánceres comunes. Conjunto de datos mínimo para informes de histopatología de cabeza y cuello . Londres: The Royal College of Pathologists .
- Johnson, Newell; Chaturvedi, Anil (2016). Carga mundial de cánceres de cavidad oral y faringe (PDF) (Libro blanco de la conferencia) . Consultado el 12 de agosto de 2017 ., en GOCF (2016)
- Mehanna, H. "Actualización de los estudios de intensificación y desintensificación en el VPH". En Golusiński, Leemans y Dietz (2017), págs. 251-256. . extracto aquí
- Munck-Wikland, Eva; Hammarstedt, Lalle; Dahlstrand, Hanna (7 de abril de 2010). Papel del virus del papiloma humano en el cáncer de amígdalas. Saltador. págs. 271–283. ISBN 9789048131860., en Hayat (2010) ( extracto adicional aquí)
- Grupo de trabajo del IARC sobre la evaluación de los riesgos carcinógenos para los seres humanos (1995). "Virus del papiloma humano". Monografías del IARC sobre la evaluación de los riesgos carcinógenos para los seres humanos . 64 : 1–378. PMC 5366848. PMID 16755705 .
- Grupo de trabajo del IARC sobre la evaluación de los riesgos carcinógenos para los seres humanos (2007). «Virus del papiloma humano». Monografías del IARC sobre la evaluación de los riesgos carcinógenos para los seres humanos . 90 : 1–636. PMC 4781057. PMID 18354839 .
- Grupo de trabajo del IARC sobre la evaluación de los riesgos carcinógenos para los seres humanos (2012). "Virus del papiloma humano". Agentes biológicos . Vol. 100B. Lyon: Agencia Internacional para la Investigación sobre el Cáncer . pp. 255–314. ISBN 978-9283213192.
{{cite book}}:|journal=ignorado ( ayuda )
Sitios web
- Bath, Charlotte (25 de abril de 2017). "La desintensificación del tratamiento del cáncer orofaríngeo con VPH positivo podría reducir la toxicidad y, al mismo tiempo, mantener la función y la supervivencia". ASCO Post (Informe del Simposio multidisciplinario de cabeza y cuello de 2016). ASCO . Consultado el 3 de agosto de 2017 .
- Hunt, Jennifer L (21 de marzo de 2010). "Molecular Assessment of HPV in Patients with Head and Neck Tumors" (PDF) . Asociación de Patología Molecular . Academia Estadounidense y Canadiense de Patología . Archivado desde el original (PDF) el 16 de julio de 2011 . Consultado el 30 de mayo de 2017 .
- "Cáncer de la cavidad oral y faringe por subsitio" (PDF) . Revisión de estadísticas de cáncer de SEER 1975–2007 . Programa de Vigilancia, Epidemiología y Resultados Finales (SEER). 15 de abril de 2010 . Consultado el 3 de junio de 2017 .
- "La faringe". TeachMeAnatomy . TeachMe. 29 de abril de 2017 . Consultado el 20 de junio de 2017 .
- Dubner, Sanford (19 de junio de 2017). «Cáncer de cabeza y cuello: resección y disección del cuello: anatomía relevante». Medscape . WebMD . Consultado el 17 de julio de 2017 .
- Joshi, Arjun S; Vashishta, Rishi; George, Philip E (18 de noviembre de 2013). "Anatomía de la faringe". Medscape . WebMD . Consultado el 20 de junio de 2017 .
- "Tratamiento del cáncer orofaríngeo". Cáncer de cabeza y cuello: versión para pacientes . Institutos Nacionales de Salud: Instituto Nacional del Cáncer . Diciembre de 2016. Archivado desde el original el 11 de febrero de 2021. Consultado el 12 de junio de 2017 .
- Consejo editorial del PDQ sobre el tratamiento para adultos (28 de marzo de 2018). «Tratamiento del cáncer de orofaringe en adultos (PDQ®): versión para profesionales de la salud». Tratamiento del cáncer de orofaringe en adultos (PDQ®) . Institutos Nacionales de la Salud – Instituto Nacional del Cáncer . PMID 26389168 . Consultado el 1 de julio de 2018 .
{{cite book}}:|website=ignorado ( ayuda ) - "Tratamiento del cáncer orofaríngeo". emedicinehealth . WebMD . 1 de agosto de 2017 . Consultado el 6 de agosto de 2017 .
- ¿Es seguro el sexo oral? (Producción televisiva). Inglaterra: BBC Three . 10 de enero de 2011.
- «Centro de información sobre el VPH». Lyon : Agencia Internacional de Investigación sobre el Cáncer e Instituto Catalán de Oncología . Consultado el 11 de agosto de 2017 .
- "The Global Oral Cancer Forum 2016" (Actas de la conferencia). Fundación Henry Schein Cares. 2017. Consultado el 12 de agosto de 2017 .
- "Se ha descubierto que el cetuximab con radiación es inferior al tratamiento estándar en el cáncer orofaríngeo con VPH positivo". Comunicados de prensa . Institutos Nacionales de Salud . 14 de agosto de 2018 . Consultado el 15 de agosto de 2018 .
Pautas de tratamiento
- "Serie basada en evidencias (EBS) y guías de práctica (PG) sobre cáncer de cabeza y cuello". Guías basadas en evidencias . Cancer Care Ontario . 31 de marzo de 2017 . Consultado el 22 de mayo de 2017 .
- "El tratamiento del cáncer de cabeza y cuello en Ontario. EBS 5-3". Diciembre de 2009. Consultado el 22 de mayo de 2017 ., en CCO (2017)
- "Pruebas de rutina de VPH en carcinoma de células escamosas de cabeza y cuello. EBS 5-9". Mayo de 2013. Consultado el 22 de mayo de 2017 ., en CCO (2017)
- "Cánceres de cabeza y cuello" (PDF) . Pautas de la NCCN 2.2018 . National Comprehensive Cancer Network . 20 de junio de 2018 . Consultado el 22 de junio de 2018 .
- "Cabeza y cuello". Pautas para el manejo del cáncer . Columbia Británica: BC Cancer Agency . 2017. Archivado desde el original el 24 de agosto de 2017. Consultado el 30 de junio de 2017 .