Paramagnetismo

| Física de la materia condensada |
|---|
 |
El paramagnetismo es una forma de magnetismo por la cual algunos materiales son débilmente atraídos por un campo magnético aplicado externamente y forman campos magnéticos internos inducidos en la dirección del campo magnético aplicado. En contraste con este comportamiento, los materiales diamagnéticos son repelidos por campos magnéticos y forman campos magnéticos inducidos en la dirección opuesta a la del campo magnético aplicado. [1] Los materiales paramagnéticos incluyen la mayoría de los elementos químicos y algunos compuestos ; [2] tienen una permeabilidad magnética relativa ligeramente mayor que 1 (es decir, una pequeña susceptibilidad magnética positiva ) y, por lo tanto, son atraídos por los campos magnéticos. El momento magnético inducido por el campo aplicado es lineal en la intensidad del campo y bastante débil. Por lo general, se requiere una balanza analítica sensible para detectar el efecto y las mediciones modernas en materiales paramagnéticos a menudo se realizan con un magnetómetro SQUID .
El paramagnetismo se debe a la presencia de electrones desapareados en el material, por lo que la mayoría de los átomos con orbitales atómicos incompletamente llenos son paramagnéticos, aunque existen excepciones como el cobre. Debido a su espín , los electrones desapareados tienen un momento dipolar magnético y actúan como pequeños imanes. Un campo magnético externo hace que los espines de los electrones se alineen paralelos al campo, lo que provoca una atracción neta. Los materiales paramagnéticos incluyen aluminio , oxígeno , titanio y óxido de hierro (FeO). Por lo tanto, en química se utiliza una regla empírica simple para determinar si una partícula (átomo, ion o molécula) es paramagnética o diamagnética: [3] si todos los electrones de la partícula están apareados, entonces la sustancia hecha de esta partícula es diamagnética; si tiene electrones desapareados, entonces la sustancia es paramagnética.
A diferencia de los ferroimanes , los paraimanes no retienen ninguna magnetización en ausencia de un campo magnético aplicado externamente porque el movimiento térmico aleatoriza las orientaciones de los espines. (Algunos materiales paramagnéticos retienen el desorden de espín incluso en cero absoluto , lo que significa que son paramagnéticos en el estado fundamental , es decir, en ausencia de movimiento térmico). Por lo tanto, la magnetización total cae a cero cuando se elimina el campo aplicado. Incluso en presencia del campo solo hay una pequeña magnetización inducida porque solo una pequeña fracción de los espines estarán orientados por el campo. Esta fracción es proporcional a la intensidad del campo y esto explica la dependencia lineal. La atracción experimentada por los materiales ferromagnéticos no es lineal y mucho más fuerte, de modo que se observa fácilmente, por ejemplo, en la atracción entre un imán de refrigerador y el hierro del propio refrigerador.
Relación con los espines de los electrones
Los átomos o moléculas constituyentes de materiales paramagnéticos tienen momentos magnéticos permanentes ( dipolos ), incluso en ausencia de un campo aplicado. El momento permanente generalmente se debe al giro de los electrones desapareados en orbitales electrónicos atómicos o moleculares (ver Momento magnético ). En el paramagnetismo puro, los dipolos no interactúan entre sí y están orientados aleatoriamente en ausencia de un campo externo debido a la agitación térmica, lo que resulta en un momento magnético neto cero. Cuando se aplica un campo magnético, los dipolos tenderán a alinearse con el campo aplicado, lo que resultará en un momento magnético neto en la dirección del campo aplicado. En la descripción clásica, se puede entender que esta alineación ocurre debido a un par proporcionado en los momentos magnéticos por un campo aplicado, que intenta alinear los dipolos paralelos al campo aplicado. Sin embargo, los verdaderos orígenes de la alineación solo se pueden entender a través de las propiedades mecánico-cuánticas del espín y el momento angular .
Si hay suficiente intercambio de energía entre dipolos vecinos, estos interactuarán y pueden alinearse o antialinearse espontáneamente y formar dominios magnéticos, lo que da como resultado ferromagnetismo (imanes permanentes) o antiferromagnetismo , respectivamente. El comportamiento paramagnético también se puede observar en materiales ferromagnéticos que están por encima de su temperatura de Curie y en antiferroimanes por encima de su temperatura de Néel . A estas temperaturas, la energía térmica disponible simplemente supera la energía de interacción entre los espines.
En general, los efectos paramagnéticos son bastante pequeños: la susceptibilidad magnética es del orden de 10 −3 a 10 −5 para la mayoría de los paraimanes, pero puede ser tan alta como 10 −1 para los paraimanes sintéticos como los ferrofluidos .
Deslocalización
| Material | Susceptibilidad magnética, [10 −5 ] (Unidades del SI) |
|---|---|
| Tungsteno | 6.8 |
| Cesio | 5.1 |
| Aluminio | 2.2 |
| Litio | 1.4 |
| Magnesio | 1.2 |
| Sodio | 0,72 |
En los materiales conductores, los electrones están deslocalizados , es decir, viajan a través del sólido más o menos como electrones libres . La conductividad puede entenderse en una imagen de estructura de bandas como algo que surge del llenado incompleto de las bandas de energía. En un conductor no magnético ordinario, la banda de conducción es idéntica para los electrones de espín hacia arriba y hacia abajo. Cuando se aplica un campo magnético, la banda de conducción se divide en una banda de espín hacia arriba y otra de espín hacia abajo debido a la diferencia en la energía potencial magnética para los electrones de espín hacia arriba y hacia abajo. Dado que el nivel de Fermi debe ser idéntico para ambas bandas, esto significa que habrá un pequeño excedente del tipo de espín en la banda que se movió hacia abajo. Este efecto es una forma débil de paramagnetismo conocida como paramagnetismo de Pauli .
El efecto siempre compite con una respuesta diamagnética de signo opuesto debido a todos los electrones del núcleo de los átomos. Las formas más fuertes de magnetismo generalmente requieren electrones localizados en lugar de itinerantes. Sin embargo, en algunos casos puede resultar una estructura de bandas en la que hay dos subbandas deslocalizadas con estados de espines opuestos que tienen energías diferentes. Si una subbanda se llena preferentemente sobre la otra, se puede tener un orden ferromagnético itinerante. Esta situación generalmente solo ocurre en bandas (d) relativamente estrechas, que están poco deslocalizadas.
electrones s y p
En general, una fuerte deslocalización en un sólido debido a una gran superposición con las funciones de onda vecinas significa que habrá una gran velocidad de Fermi ; esto significa que el número de electrones en una banda es menos sensible a los cambios en la energía de esa banda, lo que implica un magnetismo débil. Esta es la razón por la que los metales de tipo s y p son típicamente paramagnéticos de Pauli o, como en el caso del oro, incluso diamagnéticos. En el último caso, la contribución diamagnética de los electrones internos de la capa cerrada simplemente gana sobre el término paramagnético débil de los electrones casi libres.
electrones d y f
Los efectos magnéticos más fuertes se observan típicamente solo cuando están involucrados los electrones d o f. En particular, estos últimos suelen estar fuertemente localizados. Además, el tamaño del momento magnético en un átomo de lantánido puede ser bastante grande, ya que puede transportar hasta 7 electrones desapareados en el caso del gadolinio (III) (de ahí su uso en MRI ). Los altos momentos magnéticos asociados con los lantánidos son una de las razones por las que los imanes superfuertes suelen basarse en elementos como el neodimio o el samario .
Localización molecular
La imagen anterior es una generalización en lo que respecta a materiales con una red extendida en lugar de una estructura molecular. La estructura molecular también puede conducir a la localización de electrones. Aunque normalmente hay razones energéticas por las que una estructura molecular resulta tal que no exhibe orbitales parcialmente llenos (es decir, espines desapareados), algunas fracciones de capa no cerrada sí ocurren en la naturaleza. El oxígeno molecular es un buen ejemplo. Incluso en el sólido congelado contiene moléculas dirradicales que resultan en un comportamiento paramagnético. Los espines desapareados residen en orbitales derivados de funciones de onda p del oxígeno, pero la superposición se limita al vecino en las moléculas de O 2 . Las distancias a otros átomos de oxígeno en la red siguen siendo demasiado grandes para conducir a la deslocalización y los momentos magnéticos siguen sin estar apareados.
Teoría
El teorema de Bohr-Van Leeuwen demuestra que no puede haber diamagnetismo ni paramagnetismo en un sistema puramente clásico. La respuesta paramagnética tiene entonces dos posibles orígenes cuánticos, ya sea a partir de los momentos magnéticos permanentes de los iones o del movimiento espacial de los electrones de conducción en el interior del material. Ambas descripciones se dan a continuación.
Ley de Curie
Para niveles bajos de magnetización, la magnetización de los paraimanes sigue lo que se conoce como ley de Curie , al menos aproximadamente. Esta ley indica que la susceptibilidad, , de los materiales paramagnéticos es inversamente proporcional a su temperatura, es decir, que los materiales se vuelven más magnéticos a temperaturas más bajas. La expresión matemática es: donde:
- es la magnetización resultante, medida en amperios /metro (A/m),
- es la susceptibilidad magnética del volumen ( adimensional ),
- es el campo magnético auxiliar (A/m),
- es la temperatura absoluta, medida en kelvin (K),
- es una constante de Curie específica del material (K).
La ley de Curie es válida en las condiciones comunes de baja magnetización ( μ B H ≲ k B T ), pero no se aplica en el régimen de campo alto/temperatura baja donde ocurre la saturación de la magnetización ( μ B H ≳ k B T ) y los dipolos magnéticos están todos alineados con el campo aplicado. Cuando los dipolos están alineados, aumentar el campo externo no aumentará la magnetización total ya que no puede haber más alineación.
Para un ion paramagnético con momentos magnéticos no interactuantes con momento angular J , la constante de Curie está relacionada con los momentos magnéticos de los iones individuales,
donde n es el número de átomos por unidad de volumen. El parámetro μ eff se interpreta como el momento magnético efectivo por ion paramagnético. Si se utiliza un tratamiento clásico con momentos magnéticos moleculares representados como dipolos magnéticos discretos, μ , surgirá una expresión de la Ley de Curie de la misma forma, con μ apareciendo en lugar de μ eff .
La Ley de Curie se puede derivar considerando una sustancia con momentos magnéticos no interactuantes con momento angular J . Si las contribuciones orbitales al momento magnético son despreciables (un caso común), entonces en lo que sigue J = S . Si aplicamos un campo magnético a lo largo de lo que elegimos llamar el eje z , los niveles de energía de cada centro paramagnético experimentarán la división Zeeman de sus niveles de energía, cada uno con un componente z etiquetado como M J (o simplemente M S para el caso magnético de solo espín). Aplicando las estadísticas semiclásicas de Boltzmann , la magnetización de dicha sustancia es
Donde es el componente z del momento magnético para cada nivel Zeeman, por lo que se denomina magnetón de Bohr y g J es el factor g de Landé , que se reduce al factor g de electrones libres, g S cuando J = S . (en este tratamiento, suponemos que los componentes x e y de la magnetización, promediados sobre todas las moléculas, se cancelan porque el campo aplicado a lo largo del eje z los deja orientados aleatoriamente). La energía de cada nivel Zeeman es . Para temperaturas superiores a unos pocos K , , y podemos aplicar la aproximación : que produce: La magnetización en masa es entonces y la susceptibilidad está dada por
Cuando las contribuciones del momento angular orbital al momento magnético son pequeñas, como ocurre para la mayoría de los radicales orgánicos o para los complejos de metales de transición octaédricos con configuraciones d 3 o d 5 de alto espín , el momento magnético efectivo toma la forma ( con factor g g e = 2,0023... ≈ 2), donde N u es el número de electrones desapareados . En otros complejos de metales de transición esto produce una estimación útil, aunque algo más burda.
Cuando la constante de Curie es nula, los efectos de segundo orden que acoplan el estado fundamental con los estados excitados también pueden conducir a una susceptibilidad paramagnética independiente de la temperatura, conocida como susceptibilidad de Van Vleck .
Paramagnetismo de Pauli
En el caso de algunos metales alcalinos y metales nobles, los electrones de conducción interactúan débilmente y se deslocalizan en el espacio formando un gas de Fermi . En el caso de estos materiales, una contribución a la respuesta magnética proviene de la interacción entre los espines de los electrones y el campo magnético, conocida como paramagnetismo de Pauli. Para un campo magnético pequeño , la energía adicional por electrón proveniente de la interacción entre el espín de un electrón y el campo magnético viene dada por:
donde es la permeabilidad al vacío , es el momento magnético del electrón , es el magnetón de Bohr , es la constante de Planck reducida y el factor g se cancela con el espín . El indica que el signo es positivo (negativo) cuando el componente de espín del electrón en la dirección de es paralelo (antiparalelo) al campo magnético.

Para temperaturas bajas con respecto a la temperatura de Fermi (alrededor de 10 4 kelvin para los metales), la densidad numérica de electrones ( ) que apuntan paralelos (antiparalelos) al campo magnético se puede escribir como:
con la densidad total de electrones libres y la densidad electrónica de estados (número de estados por energía por volumen) en la energía de Fermi .
En esta aproximación, la magnetización se da como el momento magnético de un electrón multiplicado por la diferencia de densidades:
lo que produce una susceptibilidad paramagnética positiva independiente de la temperatura:
La susceptibilidad paramagnética de Pauli es un efecto macroscópico y debe contrastarse con la susceptibilidad diamagnética de Landau , que es igual a menos un tercio de la de Pauli y también proviene de electrones deslocalizados. La susceptibilidad de Pauli proviene de la interacción del espín con el campo magnético, mientras que la susceptibilidad de Landau proviene del movimiento espacial de los electrones y es independiente del espín. En semiconductores dopados, la relación entre las susceptibilidades de Landau y Pauli cambia, ya que la masa efectiva de los portadores de carga puede diferir de la masa del electrón .
La respuesta magnética calculada para un gas de electrones no refleja la situación completa, ya que debe incluirse la susceptibilidad magnética de los iones. Además, estas fórmulas pueden fallar en sistemas confinados que difieren del volumen, como los puntos cuánticos , o en campos altos, como se demuestra en el efecto De Haas-Van Alphen .
El paramagnetismo de Pauli recibe su nombre del físico Wolfgang Pauli . Antes de la teoría de Pauli, la falta de un fuerte paramagnetismo de Curie en los metales era un problema abierto, ya que el modelo líder de Drude no podía explicar esta contribución sin el uso de la estadística cuántica . El paramagnetismo de Pauli y el diamagnetismo de Landau son esencialmente aplicaciones del modelo de espín y del modelo del electrón libre ; el primero se debe al espín intrínseco de los electrones; el segundo se debe a su movimiento orbital. [5] [6]
Ejemplos de paraimanes
Los materiales denominados "paramagnéticos" son, en la mayoría de los casos, aquellos que presentan, al menos en un rango apreciable de temperaturas, susceptibilidades magnéticas que se ajustan a las leyes de Curie o de Curie-Weiss. En principio, cualquier sistema que contenga átomos, iones o moléculas con espines desapareados puede denominarse paramagnético, pero es necesario considerar cuidadosamente las interacciones entre ellos.
Sistemas con interacciones mínimas
La definición más estricta sería: un sistema con espines desapareados que no interactúan entre sí. En este sentido más estricto, el único paramagnético puro es un gas diluido de átomos de hidrógeno monoatómicos . Cada átomo tiene un electrón desapareado que no interactúa.
Un gas de átomos de litio ya posee dos electrones apareados en el núcleo que producen una respuesta diamagnética de signo opuesto. Estrictamente hablando, el litio es, por tanto, un sistema mixto, aunque hay que admitir que el componente diamagnético es débil y a menudo se descuida. En el caso de elementos más pesados, la contribución diamagnética se vuelve más importante y, en el caso del oro metálico, domina las propiedades. El elemento hidrógeno prácticamente nunca se llama "paramagnético" porque el gas monoatómico es estable solo a temperaturas extremadamente altas; los átomos de H se combinan para formar H 2 molecular y, al hacerlo, los momentos magnéticos se pierden ( se extinguen ), debido al par de espines. Por tanto, el hidrógeno es diamagnético y lo mismo se aplica a muchos otros elementos. Aunque la configuración electrónica de los átomos individuales (e iones) de la mayoría de los elementos contiene espines no apareados, no son necesariamente paramagnéticos, porque a temperatura ambiente, el enfriamiento es más la regla que la excepción. La tendencia a la extinción es más débil en el caso de los electrones f porque los orbitales f (especialmente 4 f ) están contraídos radialmente y se superponen sólo débilmente con los orbitales de los átomos adyacentes. En consecuencia, los elementos lantánidos con orbitales 4f incompletamente llenos son paramagnéticos u ordenados magnéticamente. [7]
| Material | μeff / μB |
|---|---|
| [Cr( NH3 ) 6 ] Br3 | 3.77 |
| K3 [Cr(CN ) 6 ] | 3.87 |
| K3 [ MoCl6 ] | 3,79 |
| K4 [V(CN ) 6 ] | 3,78 |
| [Mn( NH3 ) 6 ] Cl2 | 5,92 |
| (NH 4 ) 2 [Mn(SO 4 ) 2 ]·6H 2 O | 5,92 |
| NH4 [Fe ( SO4 ) 2 ] · 12H2O | 5.89 |
Por lo tanto, los paraimanes de fase condensada solo son posibles si las interacciones de los espines que conducen a la extinción o al ordenamiento se mantienen a raya mediante el aislamiento estructural de los centros magnéticos. Hay dos clases de materiales para los que esto es válido:
- Materiales moleculares con un centro paramagnético (aislado).
- Buenos ejemplos son los complejos de coordinación de metales d o f o proteínas con dichos centros, por ejemplo, la mioglobina . En dichos materiales, la parte orgánica de la molécula actúa como una envoltura que protege los espines de sus vecinos.
- Las moléculas pequeñas pueden ser estables en forma de radicales, como el oxígeno O2 . Este tipo de sistemas son bastante raros porque tienden a ser bastante reactivos.
- Sistemas diluidos.
- La disolución de una especie paramagnética en una red diamagnética en pequeñas concentraciones, p. ej., Nd 3+ en CaCl 2 , separará los iones de neodimio a distancias suficientemente grandes como para que no interactúen. Estos sistemas son de suma importancia para lo que puede considerarse el método más sensible para estudiar sistemas paramagnéticos: EPR .
Sistemas con interacciones

Como se ha indicado anteriormente, muchos materiales que contienen elementos d o f conservan espines no apagados. Las sales de dichos elementos suelen mostrar un comportamiento paramagnético, pero a temperaturas suficientemente bajas los momentos magnéticos pueden ordenarse. No es raro llamar a dichos materiales "paraimanes" cuando se hace referencia a su comportamiento paramagnético por encima de sus puntos de Curie o Néel, en particular si dichas temperaturas son muy bajas o nunca se han medido correctamente. Incluso en el caso del hierro, no es raro decir que se convierte en un paraimán por encima de su punto de Curie relativamente alto. En ese caso, el punto de Curie se considera una transición de fase entre un ferroimán y un "paraimán". La palabra paraimán ahora simplemente se refiere a la respuesta lineal del sistema a un campo aplicado, cuya dependencia de la temperatura requiere una versión modificada de la ley de Curie, conocida como la ley de Curie-Weiss :
Esta ley modificada incluye un término θ que describe la interacción de intercambio que está presente aunque superada por el movimiento térmico. El signo de θ depende de si predominan las interacciones ferromagnéticas o antiferromagnéticas y rara vez es exactamente cero, excepto en los casos aislados y diluidos mencionados anteriormente.
Obviamente, la descripción paramagnética de Curie-Weiss anterior T N o T C es una interpretación bastante diferente de la palabra "paramagnético", ya que no implica la ausencia de interacciones, sino más bien que la estructura magnética es aleatoria en ausencia de un campo externo a estas temperaturas suficientemente altas. Incluso si θ está cerca de cero, esto no significa que no haya interacciones, solo que las ferromagnéticas alineantes y las antiferromagnéticas antialineantes se cancelan. Una complicación adicional es que las interacciones a menudo son diferentes en diferentes direcciones de la red cristalina ( anisotropía ), lo que conduce a estructuras magnéticas complicadas una vez ordenadas.
La aleatoriedad de la estructura también se aplica a muchos metales que muestran una respuesta paramagnética neta en un amplio rango de temperaturas. Sin embargo, no siguen una ley de tipo Curie en función de la temperatura; a menudo son más o menos independientes de la temperatura. Este tipo de comportamiento es de naturaleza itinerante y se lo denomina mejor paramagnetismo de Pauli, pero no es raro ver, por ejemplo, al metal aluminio , llamado "paraimán", aunque las interacciones son lo suficientemente fuertes como para otorgarle a este elemento una muy buena conductividad eléctrica.
Superparaimanes
Algunos materiales muestran un comportamiento magnético inducido que sigue una ley de tipo Curie pero con valores excepcionalmente grandes para las constantes de Curie. Estos materiales se conocen como superparaimanes . Se caracterizan por un fuerte tipo de acoplamiento ferromagnético o ferromagnético en dominios de un tamaño limitado que se comportan independientemente unos de otros. Las propiedades en masa de un sistema de este tipo se asemejan a las de un paraimán, pero a nivel microscópico están ordenadas. Los materiales muestran una temperatura de ordenación por encima de la cual el comportamiento revierte al paramagnetismo ordinario (con interacción). Los ferrofluidos son un buen ejemplo, pero el fenómeno también puede ocurrir dentro de sólidos, por ejemplo, cuando se introducen centros paramagnéticos diluidos en un medio itinerante fuerte de acoplamiento ferromagnético como cuando se sustituye Fe en TlCu2Se2 o la aleación AuFe . Dichos sistemas contienen cúmulos acoplados ferromagnéticamente que se congelan a temperaturas más bajas. También se denominan microimanes .
Véase también
Referencias
- ^ Miessler, GL y Tarr, DA (2010) Química inorgánica 3.ª ed., editorial Pearson/Prentice Hall, ISBN 0-13-035471-6 .
- ^ Paramagnetismo. Enciclopedia Británica
- ^ "Propiedades magnéticas". Chemistry LibreTexts . 2013-10-02 . Consultado el 2020-01-21 .
- ^ Nave, Carl L. "Propiedades magnéticas de los sólidos". HyperPhysics . Consultado el 9 de noviembre de 2008 .
- ^ Pauli, Z.Phys. 41, 81, 1927
- ^ Landau, Z.Phys. 64, 629, 1930
- ^ Jensen, J. y MacKintosh, AR (1991). Magnetismo de tierras raras. Oxford: Clarendon Press. Archivado desde el original el 12 de diciembre de 2010. Consultado el 12 de julio de 2009 .
- ^ Orchard, AF (2003) Magnetoquímica . Oxford University Press.
Lectura adicional
- Las Conferencias Feynman sobre Física, vol. II, cap. 35: "Paramagnetismo y resonancia magnética"
- Charles Kittel, Introducción a la física del estado sólido (Wiley: Nueva York, 1996).
- John David Jackson, Electrodinámica clásica (Wiley: Nueva York, 1999).
Enlaces externos
- "Magnetismo: modelos y mecanismos" en E. Pavarini, E. Koch y U. Schollwöck: fenómenos emergentes en materia correlacionada , Jülich, 2013, ISBN 978-3-89336-884-6
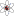

















![{\displaystyle M=n{\bar {m}}={\frac {n}{3k_{\mathrm {B} }T}}[g_{J}^{2}J(J+1)\mu _{\mathrm {B} }^{2}]H,}](https://wikimedia.org/api/rest_v1/media/math/render/svg/257d97112cc5f0ec19efdb3501671be22be79a85)






















