Apnea obstructiva del sueño
| Apnea obstructiva del sueño | |
|---|---|
| Otros nombres | Apnea obstructiva del sueño |
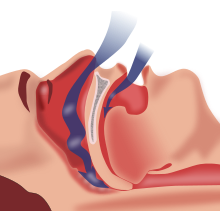 | |
| Apnea obstructiva del sueño: a medida que el tejido blando cae hacia la parte posterior de la garganta, impide el paso del aire (flechas azules) a través de la tráquea . | |
| Especialidad | Medicina del sueño |
La apnea obstructiva del sueño ( AOS ) es el trastorno respiratorio relacionado con el sueño más común y se caracteriza por episodios recurrentes de obstrucción total o parcial de las vías respiratorias superiores que conducen a una reducción o ausencia de respiración durante el sueño . Estos episodios se denominan " apneas " con cese completo o casi completo de la respiración, o " hipopneas " cuando la reducción de la respiración es parcial. En cualquier caso, puede producirse una caída de la saturación de oxígeno en sangre , una interrupción del sueño o ambas. Una alta frecuencia de apneas o hipopneas durante el sueño puede interferir con la calidad del sueño, lo que, en combinación con alteraciones en la oxigenación de la sangre, se cree que contribuye a consecuencias negativas para la salud y la calidad de vida. [1] Los términos síndrome de apnea obstructiva del sueño ( SAOS ) o síndrome de apnea-hipopnea obstructiva del sueño ( SAHOS ) pueden usarse para referirse a la AOS cuando se asocia con síntomas durante el día (p. ej., somnolencia diurna excesiva, disminución de la función cognitiva). [2] [3]
La mayoría de las personas con apnea obstructiva del sueño no son conscientes de las alteraciones de la respiración mientras duermen, incluso después de despertarse. Un compañero de cama o un miembro de la familia puede observar a una persona roncando o parecer que deja de respirar, jadea o se ahoga mientras duerme. Las personas que viven o duermen solas a menudo no son conscientes de la afección. Los síntomas pueden estar presentes durante años o incluso décadas sin ser identificados, tiempo durante el cual la persona puede acostumbrarse a la somnolencia diurna, los dolores de cabeza y la fatiga asociados con niveles significativos de alteración del sueño. La apnea obstructiva del sueño se ha asociado con la morbilidad neurocognitiva y existe un vínculo entre los ronquidos y los trastornos neurocognitivos. [4]
Clasificación
En la tercera edición de la Clasificación Internacional de Trastornos del Sueño (ICSD-3), la apnea obstructiva del sueño se clasifica entre los trastornos respiratorios relacionados con el sueño y se divide en dos categorías, a saber, AOS en adultos y AOS pediátrica. [5] La apnea obstructiva del sueño se diferencia de la apnea central del sueño (ACS), que se caracteriza por episodios de reducción o cese de la respiración atribuibles a una disminución del esfuerzo, en lugar de una obstrucción de las vías respiratorias superiores. [6] A continuación, se debe evaluar el esfuerzo respiratorio para clasificar correctamente la apnea como obstructiva dada la especificidad de la actividad diafragmática en esta afección: [7] el esfuerzo inspiratorio continúa o aumenta durante todo el episodio de ausencia de flujo de aire. [8]
Cuando las hipopneas están presentes junto con las apneas, se utiliza el término apnea-hipopnea obstructiva del sueño y cuando se asocia con somnolencia diurna y otros síntomas diurnos, se llama síndrome de apnea-hipopnea obstructiva del sueño. [9] Para ser categorizada como obstructiva, la hipopnea debe cumplir con uno o más de los siguientes síntomas: (1) ronquidos durante el evento, (2) aumento del aplanamiento del flujo oronasal, o (3) respiración paradójica toracoabdominal durante el evento. [8] Si ninguno de ellos está presente durante el evento, entonces se clasifica como hipopnea central.
Signos y síntomas
Los síntomas comunes del síndrome de OSA incluyen somnolencia diurna inexplicable, sueño intranquilo y ronquidos fuertes (con períodos de silencio seguidos de jadeos). Los síntomas menos comunes son dolores de cabeza matutinos ; insomnio ; dificultad para concentrarse; cambios de humor como irritabilidad , ansiedad y depresión ; olvidos; aumento de la frecuencia cardíaca o presión arterial ; disminución del deseo sexual; aumento de peso inexplicable; aumento de la frecuencia urinaria o nicturia ; acidez estomacal frecuente o reflujo gastroesofágico ; y sudoración nocturna intensa. [10]
Muchas personas experimentan episodios de AOS transitorios, por sólo un corto período de tiempo. Esto puede ser el resultado de una infección de las vías respiratorias superiores que causa congestión nasal, junto con hinchazón de la garganta, o amigdalitis que produce temporalmente amígdalas muy agrandadas. [11] [12] El virus de Epstein-Barr , por ejemplo, es conocido por ser capaz de aumentar drásticamente el tamaño del tejido linfoide durante la infección aguda, y la AOS es bastante común en casos agudos de mononucleosis infecciosa grave . Los episodios temporales del síndrome de AOS también pueden ocurrir en personas que están bajo la influencia de una droga (como el alcohol ) que puede relajar su tono corporal excesivamente e interferir con el despertar normal de los mecanismos del sueño. [13]
Adultos
El síntoma característico del síndrome de AOS en adultos es la somnolencia diurna excesiva . Por lo general, un adulto o adolescente con AOS grave y de larga duración se queda dormido durante períodos muy breves durante las actividades diurnas habituales si se le da la oportunidad de sentarse o descansar. Este comportamiento puede ser bastante dramático y a veces ocurre durante conversaciones con otras personas en reuniones sociales. [ cita requerida ]
La hipoxia (ausencia de aporte de oxígeno) relacionada con la AOS puede provocar cambios en las neuronas del hipocampo y de la corteza frontal derecha . Investigaciones realizadas con neuroimagen revelaron evidencia de atrofia hipocampal en personas con AOS. Encontraron que la AOS puede causar problemas en la manipulación mental de la información no verbal, en las funciones ejecutivas y en la memoria de trabajo . [ cita requerida ] Esta hipoxia cerebral repetida también se considera una causa de la enfermedad de Alzheimer . [ 14 ]
El diagnóstico de apnea obstructiva del sueño es significativamente más común entre las personas que tienen una relación de pareja, quienes se dan cuenta de su condición al ser informadas por su pareja mientras duermen, ya que las personas con apnea obstructiva del sueño a menudo no son conscientes de la condición. [ cita requerida ] Existe un estigma asociado con los ronquidos fuertes, y no se considera un rasgo femenino. En consecuencia, es menos probable que las mujeres escuchen a sus parejas decirles que roncan, o que lo admitan ante ellas mismas o ante los médicos. [ cita requerida ] Además, las máquinas CPAP (presión positiva continua en las vías respiratorias) también son percibidas negativamente por las mujeres, y es menos probable que se utilicen en toda su extensión en este grupo. [ 15 ]
Niños
Aunque esta denominada "hipersomnolencia" (somnolencia excesiva) también puede darse en niños, no es en absoluto típica de los niños pequeños con apnea del sueño. Los niños pequeños con apnea del sueño grave, por el contrario, se comportan normalmente como si estuvieran "demasiado cansados" o " hiperactivos " y suelen presentar problemas de conducta como irritabilidad y déficit de atención. [16] [17] [18]
Los adultos y los niños con AOS muy grave también difieren en su constitución corporal típica . Los adultos son generalmente pesados, con cuellos particularmente cortos y pesados. Los niños pequeños, por otro lado, generalmente no sólo son delgados sino que pueden tener " retraso de crecimiento ", en el que el crecimiento se reduce. El crecimiento deficiente se produce por dos razones: el trabajo de respirar es lo suficientemente intenso como para quemar calorías a un ritmo elevado incluso en reposo, y la nariz y la garganta están tan obstruidas que comer resulta insípido y físicamente incómodo. La AOS en los niños, a diferencia de los adultos, suele estar causada por amígdalas y adenoides obstructivas y, a veces, puede curarse con amigdalectomía y adenoidectomía . [ cita requerida ]
Este problema también puede ser causado por el exceso de peso en los niños. En este caso, los síntomas son más parecidos a los que sienten los adultos, como inquietud, agotamiento, etc. Si bien la hipertrofia adenoamigdalina sigue siendo la causa más común de AOS en niños, [19] [20] la obesidad también puede desempeñar un papel en la fisiopatología de la obstrucción de las vías respiratorias superiores durante el sueño que puede conducir a AOS, lo que hace que los niños obesos sean más propensos a desarrollar la afección. [21] El reciente aumento epidémico de la prevalencia de la obesidad ha contribuido así a cambios en la prevalencia y en las características de la AOS pediátrica, [22] siendo la gravedad de la AOS proporcional al grado de obesidad. [23] [24]
La obesidad conduce al estrechamiento de la estructura de las vías respiratorias superiores debido a la infiltración grasa y los depósitos de grasa en la región anterior del cuello y las estructuras cervicales. [19] [22] Junto con la carga de peso adicional en el sistema respiratorio , aumenta el riesgo de colapso faríngeo al tiempo que reduce el volumen intratorácico y la excursión del diafragma. [22] Además, la somnolencia diurna excesiva resultante de la fragmentación del sueño puede disminuir la actividad física y, por lo tanto, conducir a un aumento de peso (por hábitos sedentarios o aumento de la ingesta de alimentos para superar la somnolencia ). [25] La obstrucción de la estructura de las vías respiratorias superiores relacionada con la obesidad ha llevado a algunos autores a distinguir entre dos tipos de AOS en niños: [21] [22] el tipo I se asocia con una marcada hipertrofia linfadenoides sin obesidad y el tipo II se asocia primero con la obesidad y con una hiperplasia linfadenoides de las vías respiratorias superiores más leve . Los dos tipos de AOS en niños pueden dar lugar a diferentes morbilidades y consecuencias. [21] Los estudios han demostrado que la pérdida de peso en adolescentes obesos puede reducir la apnea del sueño y, por lo tanto, los síntomas de la AOS. [19] [24]
Fisiopatología
Esta sección necesita citas adicionales para su verificación . ( agosto de 2021 ) |
La transición de la vigilia al sueño (ya sea sueño REM o sueño NREM) se asocia con una reducción del tono muscular de las vías respiratorias superiores. Durante el sueño REM, el tono muscular de la garganta y el cuello, así como el de la gran mayoría de los músculos esqueléticos, están casi completamente relajados. Esto permite que la lengua y el paladar blando/orofaringe se relajen, reduciendo la permeabilidad de las vías respiratorias y potencialmente impidiendo u obstruyendo por completo el flujo de aire hacia los pulmones durante la inspiración, lo que resulta en una ventilación respiratoria reducida. Si las reducciones en la ventilación se asocian con niveles de oxígeno en sangre suficientemente bajos o con esfuerzos respiratorios suficientemente altos contra una vía respiratoria obstruida, los mecanismos neurológicos pueden desencadenar una interrupción repentina del sueño, llamada despertar neurológico. Este despertar puede hacer que una persona jadee en busca de aire y se despierte. [26] Estos despertares rara vez resultan en un despertar completo, pero pueden tener un efecto negativo significativo en la calidad restauradora del sueño. En casos significativos de AOS, una consecuencia es la privación del sueño resultante de la interrupción y recuperación repetidas de la actividad del sueño. Esta interrupción del sueño en la Etapa 3 (también llamada sueño de ondas lentas ), y en el sueño REM, puede interferir con los patrones normales de crecimiento, curación y respuesta inmune , especialmente en niños y adultos jóvenes.
La causa fundamental de la AOS es un bloqueo de las vías respiratorias superiores, generalmente detrás de la lengua y la epiglotis, por lo que las vías respiratorias, que de otro modo estarían permeables en un paciente erecto y despierto, colapsan cuando el paciente está acostado boca arriba y pierde el tono muscular al entrar en un sueño profundo.
Al comienzo del sueño, el paciente se encuentra en un sueño ligero y no hay pérdida de tono en los músculos de la garganta. El flujo de aire es laminar y silencioso. A medida que avanza el colapso de las vías respiratorias superiores, la obstrucción se hace cada vez más evidente por el inicio de una respiración ruidosa a medida que aumenta la turbulencia del aire, seguida de ronquidos gradualmente más fuertes a medida que se forma un efecto Venturi a través del conducto de aire cada vez más estrecho.
La saturación de oxígeno en la sangre del paciente disminuye gradualmente hasta que cesan los ruidos del sueño, lo que significa una obstrucción total del flujo de aire de las vías respiratorias, que puede durar varios minutos.
Finalmente, el paciente debe despertar al menos parcialmente del sueño profundo al sueño ligero, recuperando automáticamente el tono muscular general. Este cambio de sueño profundo a sueño ligero a profundo se puede registrar mediante monitores de ECT .
En el sueño ligero, el tono muscular es casi normal, las vías respiratorias se abren espontáneamente, se reanuda la respiración normal sin ruidos y aumenta la saturación de oxígeno en sangre. Finalmente, el paciente vuelve a entrar en un sueño profundo, se pierde nuevamente el tono de las vías respiratorias superiores , el paciente entra en los distintos niveles de respiración ruidosa y vuelve a producirse el bloqueo de las vías respiratorias.
El ciclo de pérdida y restauración del tono muscular que coincide con períodos de sueño profundo y ligero se repite durante todo el período de sueño del paciente.
Se cuenta el número de episodios de apnea e hipopnea durante una hora determinada y se le asigna una puntuación. Si un paciente tiene un promedio de cinco o más episodios por hora, se puede confirmar que padece AOS leve. Un promedio de 30 o más episodios por hora indica que padece AOS grave.
Modelos fisiopatológicos
Las causas de la obstrucción espontánea de las vías respiratorias superiores son motivo de intenso debate entre los profesionales clínicos. Las áreas de pensamiento se dividen principalmente en tres grupos médicos.
Algunos neumólogos y neurólogos creen que los factores de riesgo son:
- Edad avanzada, aunque la AOS se presenta en neonatos, al igual que el síndrome de Pierre Robin , y en todos los grupos de edad de las personas.
- Lesión cerebral (temporal o permanente), aunque esto no representa el 99% de los pacientes con AOS que tienen cerebros normales y vidas normales.
- Disminución del tono muscular causada por drogas o alcohol, o por trastornos neurológicos. Esto tampoco explicaría la mayoría de las personas con AOS.
- Ronquidos prolongados, que se cree que pueden inducir lesiones nerviosas locales en los tejidos blandos de la faringe . Los ronquidos pueden producir vibraciones traumáticas que pueden dar lugar a lesiones nerviosas en los músculos de las vías respiratorias superiores, lo que contribuye aún más a la apnea obstructiva del sueño. [27]
- Aumento de tejido blando alrededor de las vías respiratorias, a menudo como resultado de la obesidad, aunque no se observa en todos los pacientes con AOS.
Algunos otorrinolaringólogos creen que los factores de riesgo son características estructurales que dan lugar a una vía aérea estrecha, como amígdalas agrandadas, lengua posterior agrandada o depósitos de grasa en el cuello. Otros factores que conducen a la apnea obstructiva del sueño pueden ser la respiración nasal alterada, el paladar blando flácido o una epiglotis colapsable .
Algunos cirujanos orales y maxilofaciales creen que los factores de riesgo son una serie de formas primarias de hipoplasia mandibular , que ofrece una base anatómica primaria para el desarrollo de la apnea obstructiva del sueño a través de la glosoptosis . Algunos cirujanos maxilofaciales que ofrecen cirugía ortognática para el tratamiento de la apnea obstructiva del sueño creen que sus tratamientos ofrecen garantías superiores de curación de la apnea obstructiva del sueño.
Factores de riesgo
Obesidad
Es bien sabido que los niños, adolescentes o adultos con AOS suelen ser obesos . Las personas obesas presentan un aumento del tejido graso en el cuello que potencia la obstrucción respiratoria durante el sueño. [28]
Sin embargo, las personas de todas las edades y sexos con índices de masa corporal (IMC) normales también pueden presentar AOS, y estas personas no tienen cantidades significativas de grasa subdérmica o intracuello como se muestra en las exploraciones DEXA . Se especula que pueden tener una mayor masa muscular o, alternativamente, una tendencia a una disminución del tono muscular que potencia el colapso de las vías respiratorias durante el sueño. [ cita requerida ]
Sin embargo, la pérdida de tono muscular es de todos modos una característica clave del sueño profundo, y aunque la obesidad parece una asociación común, no es un estado invariable de la AOS.
Dormir boca arriba también se considera un factor de riesgo de apnea obstructiva del sueño. Es evidente que la gravedad y la pérdida del tono de la lengua y la garganta cuando una persona entra en un sueño profundo son factores claros y obvios que contribuyen al desarrollo de la apnea obstructiva del sueño. Pero esta explicación también se ve confundida por la presencia de obesidad en el cuello.
El uso de CPAP definitivamente expande principalmente una vía aérea superior colapsada, permitiendo la respiración nasal, y el uso positivo de CPAP probaría que el colapso de las vías aéreas es la causa de la AOS.
Las lesiones de garganta, en particular las amígdalas agrandadas, son bien reconocidas como agravantes de la AOS, y su eliminación puede proporcionar un alivio total, parcial o semipermanente de la AOS, lo que también indica que las amígdalas agrandadas pueden desempeñar un papel en la patogénesis de la AOS.
Edad
La vejez suele ir acompañada de una pérdida muscular y neurológica del tono muscular de las vías respiratorias superiores. La disminución del tono muscular también es causada temporalmente por depresores químicos; las bebidas alcohólicas y los medicamentos sedantes son los más comunes. La pérdida prematura y permanente del tono muscular en las vías respiratorias superiores puede ser precipitada por una lesión cerebral traumática , trastornos neuromusculares o una mala adherencia a los tratamientos químicos o de terapia del habla.
Tono muscular
Las personas con tono muscular disminuido y tejido blando aumentado alrededor de las vías respiratorias, y características estructurales que dan lugar a una vía respiratoria estrecha tienen un alto riesgo de OSA. Los hombres, en los que la anatomía se caracteriza por una mayor masa en el torso y el cuello, tienen un mayor riesgo de desarrollar apnea del sueño, especialmente durante la mediana edad y más tarde. Por lo general, las mujeres experimentan esta afección con menos frecuencia y en menor grado que los hombres, debido en parte a la fisiología, pero posiblemente también a los niveles diferenciales de progesterona . La prevalencia en mujeres posmenopáusicas se acerca a la de los hombres en el mismo rango de edad. Las mujeres tienen un mayor riesgo de desarrollar OSA durante el embarazo . [29]
Medicación y estilo de vida
Los factores relacionados con el estilo de vida, como el tabaquismo, también pueden aumentar las probabilidades de desarrollar AOS, ya que los irritantes químicos del humo tienden a inflamar el tejido blando de las vías respiratorias superiores y a promover la retención de líquidos, lo que puede provocar un estrechamiento de las vías respiratorias superiores. Los cigarrillos también pueden tener un impacto debido a una disminución de los niveles de nicotina en sangre, lo que altera la estabilidad del sueño. [3] Por lo tanto, los fumadores muestran un mayor riesgo de desarrollar AOS, pero el efecto de los cigarrillos en el aumento de la AOS es reversible con el cese del tabaquismo. [3] Los niños expuestos al humo del cigarrillo también pueden desarrollar AOS, ya que el tejido linfadenoides proliferará excesivamente en contacto con los irritantes. [22] Una persona también puede experimentar o exacerbar la AOS con el consumo de alcohol, sedantes o cualquier otro medicamento que aumente la somnolencia, ya que la mayoría de estos fármacos también son relajantes musculares. [30] También se ha demostrado que la rinitis alérgica y el asma están implicados en el aumento de la prevalencia de hipertrofia adenoamigdalina y AOS. [31] [32]
Genético
La AOS también parece tener un componente genético: aquellos con antecedentes familiares de la misma tienen más probabilidades de desarrollarla.
Síndromes craneofaciales
Recientemente ha cobrado gran interés la idea de que existe una tendencia general en los seres humanos a desarrollar mandíbulas inferiores cortas ( neotenia ), que es una de las principales causas de la apnea obstructiva del sueño (AOS) a través de una afección combinada denominada glosoptosis . La lengua posterior "normal" se desplaza hacia atrás debido a una lengua anterior y una mandíbula inferior más pequeñas y "anormales". De la misma manera, una mandíbula superior estrecha también contribuye a la AOS debido a su relación con el volumen de las vías respiratorias. Una mandíbula superior más estrecha da como resultado conductos nasales más estrechos y una garganta más estrecha; esta también parece ser la razón por la que tantos pacientes con AOS experimentan congestión nasal, especialmente cuando están acostados.
Los cirujanos maxilofaciales ven muchos efectos de las mandíbulas inferiores pequeñas, incluidos los dientes apiñados, las maloclusiones y la apnea obstructiva del sueño (AOS), todas las cuales son tratables mediante operaciones quirúrgicas que aumentan y normalizan el tamaño de la mandíbula. Las operaciones como BIMAX personalizadas, GenioPaully e IMDO (en la adolescencia) ofrecen una opción médica válida que reemplaza todas las formas tradicionales de tratamiento de la AOS, incluidas la CPAP , las férulas de avance mandibular , la amigdalectomía y la UPPP . Existen patrones de rasgos faciales inusuales que ocurren en síndromes reconocibles. Algunos de estos síndromes craneofaciales son genéticos, otros son de causas desconocidas. En muchos síndromes craneofaciales, los rasgos que son inusuales involucran la nariz, la boca y la mandíbula, o el tono muscular en reposo, y ponen al individuo en riesgo de sufrir el síndrome de AOS.
El síndrome de Down es uno de esos síndromes. En esta anomalía cromosómica , varias características se combinan para hacer más probable la presencia de apnea obstructiva del sueño. Las características específicas del síndrome de Down que predisponen a la apnea obstructiva del sueño incluyen un tono muscular relativamente bajo, una nasofaringe estrecha y una lengua grande. La obesidad y el agrandamiento de las amígdalas y adenoides, afecciones que se dan comúnmente en la población occidental, tienen muchas más probabilidades de ser obstructivas en una persona con estas características que sin ellas. La apnea obstructiva del sueño ocurre incluso con más frecuencia en personas con síndrome de Down que en la población general. Un poco más del 50% de todas las personas con síndrome de Down experimentan apnea obstructiva del sueño, [33] y algunos médicos recomiendan la realización de pruebas de rutina en este grupo. [34]
En otros síndromes craneofaciales, la característica anormal puede mejorar la vía aérea, pero su corrección puede poner a la persona en riesgo de sufrir apnea obstructiva del sueño después de la cirugía cuando se modifica. Los síndromes de paladar hendido son un ejemplo de ello. Durante el período neonatal, todos los humanos son respiradores nasales obligados . El paladar es tanto el techo de la boca como el suelo de la nariz. Tener un paladar abierto puede dificultar la alimentación, pero generalmente no interfiere con la respiración; de hecho, si la nariz está muy obstruida, entonces un paladar abierto puede aliviar la respiración. Hay una serie de síndromes de paladar hendido en los que el paladar abierto no es la única característica anormal; además, hay un pasaje nasal estrecho, que puede no ser obvio. En estos individuos, el cierre del paladar hendido, ya sea mediante cirugía o mediante un dispositivo bucal temporal, puede provocar la aparición de una obstrucción.
El avance esquelético en un esfuerzo por aumentar físicamente el espacio aéreo faríngeo es a menudo una opción para pacientes craneofaciales con obstrucción de las vías respiratorias superiores y mandíbulas inferiores pequeñas . Estos síndromes incluyen el síndrome de Treacher Collins y la secuencia de Pierre Robin . La cirugía de avance mandibular es una de las modificaciones necesarias para mejorar las vías respiratorias; otras pueden incluir la reducción de la lengua, la amigdalectomía o la uvulopalatoplastia modificada . [ cita requerida ]
Complicación postoperatoria
La AOS también puede ocurrir como una complicación postoperatoria grave que parece estar asociada con mayor frecuencia con la cirugía de colgajo faríngeo en comparación con otros procedimientos para el tratamiento de la insuficiencia velofaríngea (VPI). [35] En la AOS, las interrupciones recurrentes de la respiración durante el sueño se asocian con una obstrucción temporal de las vías respiratorias . Después de la cirugía de colgajo faríngeo, dependiendo del tamaño y la posición, el colgajo en sí puede tener un efecto "obturador" u obstructivo dentro de la faringe durante el sueño, bloqueando los puertos de flujo de aire y obstaculizando la respiración efectiva . [36] [37] Se han documentado casos de obstrucción grave de las vías respiratorias, y los informes de AOS postoperatoria continúan aumentando a medida que los profesionales de la salud (es decir, médicos, patólogos del lenguaje del habla ) se vuelven más educados sobre esta posible condición peligrosa. [38] Posteriormente, en la práctica clínica, las preocupaciones de la AOS han igualado o superado el interés en los resultados del habla después de la cirugía de colgajo faríngeo. [ cita requerida ]
El tratamiento quirúrgico de la insuficiencia velopalatina puede causar el síndrome de apnea obstructiva del sueño. Cuando hay insuficiencia velopalatina, el aire se filtra hacia la nasofaringe incluso cuando el paladar blando debería cerrar la nariz. Se puede realizar una prueba sencilla para esta afección colocando un pequeño espejo sobre la nariz y pidiendo al sujeto que diga "P". Este sonido p, una plosiva, se produce normalmente con la vía aérea nasal cerrada: todo el aire sale por los labios fruncidos, nada por la nariz. Si es imposible decir el sonido sin empañar el espejo nasal, hay una fuga de aire, evidencia razonable de un cierre palatino deficiente. El habla a menudo no es clara debido a la incapacidad de pronunciar ciertos sonidos. Uno de los tratamientos quirúrgicos para la insuficiencia velopalatina consiste en adaptar el tejido de la parte posterior de la garganta y usarlo para causar deliberadamente una obstrucción parcial de la abertura de la nasofaringe . Esto puede causar el síndrome de OSA en personas susceptibles, particularmente en los días posteriores a la cirugía, cuando aparece hinchazón (ver a continuación: Situación especial: anestesia y cirugía). [ cita requerida ]
Por último, los pacientes con apnea obstructiva del sueño tienen un mayor riesgo de sufrir muchas complicaciones perioperatorias cuando se presentan a una cirugía, incluso si el procedimiento planificado no es en la cabeza y el cuello. Se han publicado pautas destinadas a reducir el riesgo de complicaciones perioperatorias. [39]
Consecuencias
Existen 3 niveles de consecuencias: fisiológicas, intermedias y clínicas. [40] Las consecuencias fisiológicas incluyen hipoxia, fragmentación del sueño, desregulación del sistema nervioso autónomo o hiperoxia. [40] Las consecuencias intermedias reagrupan inflamación, vasoconstricción pulmonar, disfunción metabólica general, oxidación de proteínas y lípidos o aumento de la adiposidad. [40] Las repercusiones clínicas están compuestas por hipertensión pulmonar, accidentes, obesidad, diabetes, diferentes enfermedades cardíacas o hipertensión. [40]
En los niños
La apnea obstructiva del sueño es el trastorno respiratorio del sueño (TRS) más común y afecta hasta al 11% de los niños nacidos a término; es aún más común (3 a 6 veces más) en niños nacidos prematuramente. [41] Como TRS, la AOS en niños puede llevar a varias consecuencias adversas, también a largo plazo con consecuencias que duran hasta la edad adulta. [19] Las implicaciones de la AOS en los niños son complejas y cubren una amplia gama de consecuencias: cuando no se trata, la AOS puede llevar a una morbilidad que afecta a muchos dominios diferentes de la vida (órganos, sistemas corporales, alteración del comportamiento, depresión , disminución de la calidad de vida , etc.). [22] Por lo tanto, los síntomas nocturnos que indican la presencia de AOS (por ejemplo, ronquidos , jadeos, sueño inquieto y energía excesiva utilizada para respirar durante el sueño) se asocian con síntomas diurnos como dificultades de concentración y aprendizaje e irritabilidad, deterioro del desarrollo neurocognitivo, disminución del rendimiento escolar y dificultades de comportamiento. [19] Por ejemplo, los trastornos respiratorios del sueño como la apnea obstructiva del sueño contribuyen a un comportamiento hiperactivo que puede llevar al diagnóstico y tratamiento del trastorno por déficit de atención con hiperactividad (TDAH). Sin embargo, una vez que se trata el trastorno respiratorio del sueño, el comportamiento hiperactivo puede mejorar y se puede suspender el tratamiento. [42] La obesidad también tiene un impacto en las consecuencias de la apnea obstructiva del sueño y conduce a diferentes manifestaciones o gravedad. [22] Los estudios han demostrado que, a diferencia de los adultos, los niños con trastornos respiratorios obstructivos del sueño pueden mantener la oxigenación cerebral. Sin embargo, la afección aún tiene efectos en el cerebro y puede conducir a secuelas neurocognitivas y conductuales adversas. Es particularmente preocupante ya que esas consecuencias ocurren mientras el cerebro aún se está desarrollando. [41] El grado en que se altera y fragmenta el sueño se ha relacionado significativamente con la gravedad de las consecuencias, y esta última tiene la posibilidad de disminuir una vez que se mejora el sueño. [21] Es más la interrupción de los procesos del sueño que la cantidad total de sueño que experimenta el niño lo que genera las consecuencias adversas en el funcionamiento diurno del niño; [21] Contribuye a la hiperactividad por ejemplo. [42]
Los niños con AOS pueden experimentar déficits de aprendizaje y memoria, y se ha vinculado a una reducción del coeficiente intelectual infantil. [43] La AOS no tratada también puede provocar que los niños no alcancen su potencial de altura. [44]
Consecuencias neurocognitivas y conductuales
La fragmentación del sueño nocturno se ha relacionado con alteraciones neurocognitivas, por lo tanto, la identificación de los TRS como la AOS es crucial en los niños, ya que estas alteraciones tienen la posibilidad de ser reversibles con el tratamiento adecuado para el trastorno del sueño. [45] Las disfunciones neurocognitivas y conductuales que se presentan comúnmente en los niños con AOS incluyen las siguientes: hiperactividad, impulsividad , conductas agresivas, [22] [21] bajas habilidades sociales y de comunicación y habilidades adaptativas reducidas. [19] Los niños con AOS suelen mostrar déficits cognitivos, lo que resulta en dificultades de atención y concentración , así como un menor rendimiento académico y coeficiente intelectual . [19] [21] Los bajos rendimientos académicos se han relacionado con la AOS y se ha sugerido que son el resultado de despertares corticales y simpáticos e hipoxemia que afectan la consolidación de la memoria . [46] Un estudio con niños indios afectados por AOS ha mostrado malas calificaciones escolares, incluidas matemáticas, ciencias, lenguaje y educación física. Este estudio permitió ver el impacto general de la AOS en las habilidades de aprendizaje asociadas con el lenguaje o las habilidades numéricas y el desarrollo físico. [46] Se ha sugerido que los déficits en el rendimiento académico relacionados con la AOS podrían estar mediados por una reducción de las funciones ejecutivas o de las habilidades lingüísticas, [47] dominios que contribuyen en gran medida a las capacidades de aprendizaje y la conducta. No obstante, los déficits en el rendimiento escolar pueden mejorarse si se realiza una adenoamigdalectomía en los niños para tratar la AOS. [47] Por lo tanto, es crucial identificar la AOS en los niños con dificultades escolares; muchos casos pasan desapercibidos. [47]
Como los estudios han demostrado que las habilidades de aprendizaje y las conductas pueden mejorarse si se trata la AOS, [19] [21] los déficits neurocognitivos y conductuales son, por lo tanto, al menos parcialmente reversibles. [22] Se ha postulado que esta dimensión reversible está correlacionada negativamente con la duración de los síntomas, lo que significaría que cuanto más tiempo se deje sin tratar la AOS, menos reversibles serán las consecuencias. [21]
Consecuencias somáticas y metabólicas
De manera similar a los adultos, la AOS en niños está relacionada con un mayor riesgo de morbilidad cardiovascular , [22] [21] debido al aumento de la actividad simpática y al deterioro del control autónomo cardíaco. [41] Entre las disfunciones cardiovasculares resultantes de la AOS, podemos encontrar la hipertensión sistémica [21] y la desregulación de la presión arterial [19] [48] (presión arterial elevada o variabilidad de la presión arterial, por ejemplo [41] ). Se ha demostrado que la variabilidad de la presión arterial está correlacionada con la gravedad de los síntomas, como la frecuencia de la apnea y la hipopnea . [48] La hipertensión pulmonar también es común entre los problemas cardiovasculares resultantes de la AOS. [19] Los niños con trastornos respiratorios obstructivos del sueño también muestran una frecuencia cardíaca más rápida durante la vigilia y durante el sueño. [48]
En pacientes adultos, se ha demostrado que la AOS está asociada con la resistencia a la insulina . [49] En los niños, las consecuencias metabólicas de la AOS son complicadas de evaluar, ya que también pueden estar asociadas con la pubertad y la obesidad (si está presente). [19] Sin embargo, cuando la AOS está asociada con la obesidad, la interacción de las dos condiciones puede conducir a alteraciones metabólicas como resistencia a la insulina y lipidemia alterada , [22] enfermedad hepática , adiposidad abdominal y síndrome metabólico . La obesidad interactúa con esos efectos. [48]
Enuresis nocturna
Los niños con AOS también muestran un mayor riesgo de enuresis nocturna [19] [50] y se plantea la hipótesis de que es causada por una producción excesiva de orina , [46] [51] un rendimiento deteriorado de la vejiga y la uretra [52] o una incapacidad para suprimir la contracción nocturna de la vejiga, debido a una falta de despertar. [51] [52] El riesgo de enuresis nocturna aumenta con la gravedad de la respiración alterada por el sueño: cuanto más eventos respiratorios por hora de sueño, mayor es el riesgo de enuresis nocturna. [52] La obesidad también puede desempeñar un papel, ya que está asociada con la AOS y con la diuresis nocturna (debido a una dieta poco saludable). La interacción entre la AOS y la obesidad podría dar lugar a enuresis nocturna. [51] Considerando la alta prevalencia de enuresis nocturna entre niños con trastornos respiratorios del sueño, es importante considerar este último en el diagnóstico diferencial de la enuresis nocturna ya que el tratamiento del trastorno del sueño podría tener un efecto terapéutico favorable sobre la enuresis. [53] [50] [52] Por ejemplo, una adenoamigdalectomía realizada para reducir la AOS tiene un impacto positivo en la enuresis nocturna. [53] [46] Un estudio ha demostrado que esta cirugía tiene un 60-75% de posibilidades de resolver la enuresis nocturna por completo, y un 80-85% de posibilidades de reducir sus síntomas junto con otros síntomas de la AOS. [50]
Crecimiento retardado
La apnea obstructiva del sueño no tratada en niños también puede provocar retraso en el crecimiento . Cuando se altera el sueño en niños que todavía están creciendo, puede haber consecuencias importantes. La hormona del crecimiento humana (HGH) se secreta durante la noche, especialmente durante el sueño profundo, no REM. Si esto se altera, la secreción de la hormona del crecimiento puede verse comprometida; por lo tanto, el crecimiento puede no ocurrir normalmente y los niños pueden llegar a ser más bajos que sus compañeros. [44]
Otras consecuencias
A diferencia de los adultos, la somnolencia diurna excesiva (SDE) no es el síntoma más comúnmente reportado en niños con AOS. [45] Sin embargo, utilizando cuestionarios objetivos, es posible notar que la frecuencia de SDE en niños es más alta que lo reportado por los padres o cuidadores (40-50%). [21] Y el riesgo de SDE incluso aumenta cuando la AOS está asociada con la obesidad . [21] [22]
Debido a todas las consecuencias y síntomas que genera, la AOS en niños conlleva una disminución significativa de la calidad de vida , [21] siendo esta disminución aún mayor cuando hay obesidad. [22] Sin embargo, la calidad de vida puede mejorarse con el tratamiento de la AOS. [22] Los TRS también se han relacionado con una mayor tasa de trastornos internalizantes como la ansiedad y la depresión . [54] De hecho, los síntomas depresivos han demostrado ser mayores en niños con AOS, [54] especialmente en varones. [55] Una vez más, la gravedad de los síntomas depresivos se correlaciona positivamente con la gravedad de los TRS. [54] También interactúa con la obesidad ya que los niños obesos tienen mayor riesgo de mostrar síntomas depresivos y la obesidad puede causar AOS. [55] El vínculo también puede ir en sentido inverso con la depresión que induce la obesidad (debido a comer en exceso ) que empeora la AOS. La adenoamigdalectomía puede disminuir la intensidad de los síntomas depresivos. [55]
Otras consecuencias de un sueño alterado en niños con AOS incluyen anhedonia [56] [54] aumento de la fatiga y disminución del interés en las actividades diarias, lo que a su vez puede afectar las relaciones sociales del niño. [22]
En adultos
Si bien existen algunas similitudes entre adultos y niños, la AOS no tiene las mismas consecuencias en ambas poblaciones. [57] Ejemplos de similitudes son los ronquidos , que son la queja más común tanto en la AOS pediátrica como en la AOS en adultos [57] , la variabilidad de la presión arterial y las morbilidades cardiovasculares . [3] Una diferencia importante es la somnolencia diurna excesiva (EDS) que se informa comúnmente en la AOS en adultos, [58] mientras que no es muy común en la AOS pediátrica. [57] Sin embargo, la AOS en adultos también implica una gran variedad de consecuencias adversas y graves, [59] esta última conduce a una mayor mortalidad entre los pacientes con AOS. [60] Esas consecuencias incluso se ven empeoradas por morbilidades comunes como la obesidad . [61]
Consecuencias neurocognitivas
De manera similar a los niños, la AOS afecta las funciones cognitivas en los adultos. [57] Los metaanálisis han demostrado que los deterioros cognitivos más comunes ocurren en los dominios de la atención , la memoria verbal y visual retardada a largo plazo , [62] las habilidades visoespaciales/constructivas y las funciones ejecutivas , [63] como la flexibilidad mental . [62] El funcionamiento ejecutivo, dominado principalmente por la corteza prefrontal [64] , está significativamente deteriorado en pacientes con AOS, se cree que la región prefrontal y su conectividad se ven afectadas por los trastornos del sueño. [65]
En cuanto a los déficits de memoria, la memoria verbal se ve afectada de forma significativa, ya que los pacientes muestran dificultades para recordar la información verbal de forma inmediata y tardía. Aunque los metanálisis no han demostrado déficits en la retención de información en pacientes con AOS, esos deterioros en la memoria verbal pueden estar relacionados con problemas en la codificación de la información . [66] Este déficit en la codificación de la información también se observa en la memoria visoespacial; sin embargo, la memoria visual parece estar intacta en los pacientes con AOS. [66]
Se ha sugerido que los deterioros cognitivos son resultado de la fragmentación y la privación del sueño , así como de la somnolencia diurna excesiva asociada con ellos. [63] Más precisamente, los déficits de atención y memoria parecen ser resultado de la fragmentación del sueño, mientras que los déficits en la función cognitiva global (función ejecutiva, función psicomotora, habilidades del lenguaje) están más relacionados con la hipoxia o la hipercapnia que acompañan a los eventos obstructivos durante el sueño. [63] [67] Sin embargo, no se ha encontrado una correlación consistente entre el grado de deterioro cognitivo y la gravedad de la alteración del sueño o la hipoxia. [66] [67] Estos deterioros pueden mejorar con un tratamiento eficaz para la AOS, como la terapia de presión positiva continua en las vías respiratorias (CPAP). [63] Conducir un vehículo de motor es un ejemplo de una tarea compleja que depende de las capacidades cognitivas del conductor, como la atención, el tiempo de reacción y la vigilancia. [68] Los momentos muy breves de falta de atención llamados eventos de microsueño podrían ser un indicador de deterioro de la vigilancia diurna, aunque estos pueden no estar presentes en todos los conductores con apnea obstructiva del sueño. [69]
Consecuencias conductuales
La hiperactividad y las dificultades en la regulación emocional encontradas en pacientes pediátricos (niños) no se reportan en adultos. [57] Sin embargo, la AOS en adultos se asocia con cambios de personalidad y comportamiento automático . [58] El mayor impacto de la AOS es la somnolencia diurna excesiva (EDS), reportada en aproximadamente el 30% de los pacientes con AOS. [70] La EDS puede ser causada por la alteración de la calidad del sueño, la duración insuficiente del sueño o la fragmentación del sueño [71] y es responsable de otras complicaciones, ya que puede conducir a síntomas depresivos , [72] deterioro de la vida social y disminución de la efectividad en el trabajo. [73] [74] Los estudios han demostrado que esas consecuencias de la EDS se pueden mejorar después de un tratamiento con CPAP. [75]
Consecuencias fisiológicas y metabólicas
La AOS en adultos se asocia con un mayor riesgo de morbilidad cardiovascular, diabetes , hipertensión , enfermedad de la arteria coronaria y accidente cerebrovascular [57] [58] – La AOS podría tener un papel en la etiología de estas afecciones. Esas afecciones pueden conducir a un aumento de la mortalidad [57] [58] que un tratamiento apropiado para la AOS puede reducir. [58] La AOS a menudo se relaciona con la hipertensión, ya que induce un aumento de la actividad simpática que puede conducir a la elevación de la presión arterial. Se ha sugerido que la hipercapnia relacionada con la AOS está relacionada con este desarrollo de hipertensión. [76] El tratamiento de la AOS puede prevenir el desarrollo de la hipertensión. [77] La relación entre la AOS y el exceso de peso corporal es compleja, ya que la obesidad es más frecuente entre los pacientes con AOS, pero también puede ser un factor de riesgo para el desarrollo de la AOS [58] – representa el 58% de los casos en adultos. [78] Por lo tanto, tanto la AOS como la obesidad (cuando está presente) pueden trabajar sinérgicamente y conducir a hiperlipidemia , diabetes, resistencia a la insulina y otros síntomas del síndrome metabólico . [3] [58] El síndrome metabólico en sí mismo se asocia a menudo con la AOS: entre el 74 y el 85 % de los pacientes con AOS son diagnosticados con esta afección. La terapia con CPAP puede conducir a una mejora de algunos de los componentes cardiovasculares del síndrome metabólico [77], mientras que la pérdida de peso también se recomienda por sus efectos positivos sobre las consecuencias de la AOS y las disfunciones metabólicas. [78] Por lo tanto, una intervención que incluya ejercicio y dieta es eficaz para el tratamiento de la AOS, ya que afecta positivamente la gravedad de los síntomas de la obesidad y de la AOS. [79]
Las personas con diabetes tipo 2 a menudo son co-diagnosticadas con AOS, donde las tasas de prevalencia de diabetes tipo 2 varían entre el 15% y el 30% dentro de la población con AOS. [80] La relación entre AOS y diabetes tipo 2 podría posiblemente explicarse por el hecho de que el sueño fragmentado característico de AOS y la hipoxemia irregular conducen al metabolismo desregulado de la glucosa en la sangre. [80] En particular, muchos estudios de polisomnografía mostraron que la AOS sin tratamiento empeora el control glucémico en personas con diabetes tipo 2. [80] Sin embargo, es posible que la relación entre AOS y diabetes tipo 2 sea bidireccional ya que la disfunción nerviosa relacionada con la diabetes puede afectar el sistema respiratorio e inducir alteraciones respiratorias durante el sueño. [80]
Consecuencias psicológicas
El sueño es de gran importancia para la salud psicológica y emocional . [81] Como está muy afectado en la AOS, esta condición se asocia con trastornos del estado de ánimo [82] y varios resultados psicológicos, [81] especialmente depresión y ansiedad . [83] Por lo tanto, los trastornos psicológicos se observan comúnmente en pacientes con AOS que muestran una mayor prevalencia de malestar psicológico , principalmente debido a la calidad y estructura del sueño deterioradas y los episodios repetidos de hipoxia . [81] [84] La presencia de trastornos psicológicos también puede empeorar los trastornos del sueño, lo que implica que la psicopatología puede ser un factor o una consecuencia de la AOS. [83] Las consecuencias adversas de la AOS, como las comorbilidades cardiovasculares y los trastornos metabólicos, también juegan un papel en el desarrollo de trastornos mentales, [83] y también se ha informado que los pacientes con enfermedades crónicas tienen un mayor riesgo de experimentar depresión. [82] En pacientes con AOS con trastornos psiquiátricos, es crucial tratar la AOS, ya que puede reducir los síntomas psiquiátricos. [85]
Algunos casos de AOS son causados por obstrucción nasal , que también se ha relacionado con problemas psicológicos debido a una proporción alterada de calcio y magnesio en las células cerebrales . La obstrucción nasal puede, por lo tanto, agravar la salud psicológica de los pacientes con AOS. La cirugía nasal para estos pacientes podría disminuir la gravedad de la AOS y mejorar los síntomas psicológicos. [84]
Otras consecuencias
La AOS no tratada también conduce a una disminución de la calidad de vida, dificultades en el funcionamiento social , [58] problemas y accidentes laborales [65] y una tasa muy aumentada de accidentes de tráfico . [58] [86] [87] Estos graves resultados de la AOS están relacionados principalmente con la somnolencia diurna excesiva resultante de la fragmentación del sueño y resaltan la necesidad de proporcionar a los pacientes un tratamiento adecuado. [58] Un tratamiento eficaz mejora en gran medida esas consecuencias adversas, incluida la calidad de vida. [58]
Los pacientes con AOS también informan con frecuencia trastornos de dolor como dolor de cabeza o fibromialgia , y muestran una mayor intensidad del dolor junto con una menor tolerancia al dolor . [87]
Diagnóstico
En una revisión sistemática de la evidencia publicada, el Grupo de Trabajo de Servicios Preventivos de los Estados Unidos concluyó en 2017 que había incertidumbre sobre la precisión o la utilidad clínica de todas las posibles herramientas de detección de AOS, [88] y recomendó que la evidencia es insuficiente para evaluar el equilibrio de beneficios y daños de la detección de AOS en adultos asintomáticos. [89]
El diagnóstico del síndrome de OSA se realiza cuando el paciente presenta episodios recurrentes de colapso parcial o completo de la vía aérea superior durante el sueño que resultan en apneas o hipopneas, respectivamente. [90] Los criterios que definen una apnea o una hipopnea varían. La Academia Estadounidense de Medicina del Sueño (AASM) define una apnea como una reducción en el flujo de aire de ≥ 90% que dura al menos 10 segundos. Una hipopnea se define como una reducción en el flujo de aire de ≥ 30% que dura al menos 10 segundos y se asocia con una disminución ≥ 4% en la oxigenación del pulso, o como una reducción ≥ 30% en el flujo de aire que dura al menos 10 segundos y se asocia con una disminución ≥ 3% en la oxigenación del pulso o con un despertar. [91]
Para definir la gravedad del cuadro se utiliza el Índice de Apnea-Hipopnea (IAH) o el Índice de Alteraciones Respiratorias (IDR). Mientras que el IAH mide el número medio de apneas e hipopneas por hora de sueño, el IDR añade a esta medida los despertares relacionados con el esfuerzo respiratorio (RERA). [92] Así, el síndrome de AOS se diagnostica si el IAH es > 5 episodios por hora y produce somnolencia diurna y fatiga o cuando el IDR es ≥ 15 independientemente de los síntomas. [93] Según la Asociación Americana de Medicina del Sueño, la somnolencia diurna se clasifica como leve, moderada y grave en función de su impacto en la vida social. La somnolencia diurna se puede evaluar con la Escala de Somnolencia de Epworth (ESS), un cuestionario autoinformado sobre la propensión a quedarse dormido o dormitar durante el día. [94] Las herramientas de detección de la AOS incluyen el cuestionario STOP, el cuestionario de Berlín y el cuestionario STOP-BANG, que se ha considerado una herramienta muy poderosa para detectar la AOS. [95] [96]
Criterios
Según la Clasificación Internacional de Trastornos del Sueño , existen 4 tipos de criterios. El primero se refiere al sueño: somnolencia excesiva, sueño no reparador, fatiga o síntomas de insomnio. El segundo y tercer criterio se refieren a la respiración: despertarse conteniendo la respiración, jadeando o ahogándose; ronquidos, interrupciones de la respiración o ambos durante el sueño. El último criterio gira en torno a problemas médicos como hipertensión, enfermedad de la arteria coronaria, accidente cerebrovascular, insuficiencia cardíaca, fibrilación auricular, diabetes mellitus tipo 2, trastorno del estado de ánimo o deterioro cognitivo. Se distinguen dos niveles de gravedad, el primero se determina mediante una polisomnografía o una prueba de apnea del sueño en el hogar que demuestra 5 o más eventos respiratorios predominantemente obstructivos por hora de sueño y los niveles más altos se determinan por 15 o más eventos. Si los eventos están presentes menos de 5 veces por hora, no se diagnostica apnea obstructiva del sueño. [97]
Una variabilidad considerable de una noche a otra complica aún más el diagnóstico de la apnea obstructiva del sueño. En casos poco claros, podrían ser necesarias múltiples pruebas para lograr un diagnóstico preciso. [98]
Polisomnografía
| Clasificación | IAH (adulto) | IAH (pediatría) |
|---|---|---|
| Normal | < 5 | <1 |
| Leve | ≥5, <15 | ≥1, <5 |
| Moderado | ≥15, <30 | ≥5, <10 |
| Severo | ≥ 30 | ≥10 |
La polisomnografía de nivel 1 (PSG) nocturna en el laboratorio es la prueba de referencia para el diagnóstico. Los pacientes son monitoreados con derivaciones de EEG, oximetría de pulso , sensores de temperatura y presión para detectar el flujo de aire nasal y oral, pletismografía de impedancia respiratoria o cinturones de resistencia similares alrededor del tórax y el abdomen para detectar movimiento, una derivación de ECG y sensores de EMG para detectar la contracción muscular en el mentón, el tórax y las piernas. Una hipopnea puede basarse en uno de dos criterios. Puede ser una reducción en el flujo de aire de al menos el 30% durante más de 10 segundos asociada con al menos un 4% de desaturación de oxígeno o una reducción en el flujo de aire de al menos el 30% durante más de 10 segundos asociada con al menos un 3% de desaturación de oxígeno o un despertar del sueño en el EEG. [99]
Un "evento" puede ser una apnea, caracterizada por el cese completo del flujo de aire durante al menos 10 segundos, o una hipopnea en la que el flujo de aire disminuye en un 50 por ciento durante 10 segundos o disminuye en un 30 por ciento si hay una disminución asociada en la saturación de oxígeno o un despertar del sueño. [100] Para calificar la gravedad de la apnea del sueño, la cantidad de eventos por hora se informa como el índice de apnea-hipopnea (IAH). Para los adultos, un IAH de menos de 5 se considera normal, un IAH de [5–15) es leve, [15–30) es moderado y ≥30 eventos por hora caracterizan la apnea del sueño grave. Para los pacientes pediátricos, un IAH de menos de 1 se considera normal, un IAH de [1–5) es leve, [5–10) es moderado y ≥10 eventos por hora caracterizan la apnea del sueño grave.
Oximetría domiciliaria
En pacientes con alta probabilidad de padecer AOS, un ensayo controlado aleatorio encontró que la oximetría en el hogar (un método no invasivo para monitorear la oxigenación de la sangre) puede ser adecuada y más fácil de obtener que la polisomnografía formal. [101] Los pacientes con alta probabilidad se identificaron por una puntuación en la Escala de somnolencia de Epworth (ESS) de 10 o más y una Puntuación clínica de apnea del sueño (SACS) de 15 o más. [102] Sin embargo, la oximetría en el hogar no mide los eventos apneicos o los despertares relacionados con eventos respiratorios y, por lo tanto, no produce un valor de IAH.
Tratamiento
Se utilizan numerosas opciones de tratamiento en la apnea obstructiva del sueño. [103] Se recomienda evitar el alcohol y el tabaco, [104] así como evitar los medicamentos que relajan el sistema nervioso central (por ejemplo, sedantes y relajantes musculares). Se recomienda la pérdida de peso en personas con sobrepeso . A menudo se utilizan dispositivos de avance mandibular y presión positiva continua en las vías respiratorias (CPAP) y se ha descubierto que son igualmente eficaces. [105] [106] El entrenamiento físico, incluso sin pérdida de peso, mejora la apnea del sueño. [107] No hay pruebas suficientes para apoyar el uso generalizado de medicamentos. [105] En pacientes seleccionados, por ejemplo, con hiperplasia amigdalina, se recomienda la amigdalectomía. En pacientes en los que fracasan la CPAP y los dispositivos bucales, se recomienda el tratamiento quirúrgico con uvulopalatofaringoplastia conservadora (UPPP) como cirugía de rescate . Se han publicado estudios controlados aleatorizados sobre la eficacia de la UPPP, que muestran el efecto sobre la respiración nocturna y la somnolencia diurna excesiva, [108] y un metaanálisis sistemático. [109]
Intervención física
La intervención terapéutica más utilizada es la presión positiva en las vías respiratorias , mediante la cual un respirador bombea una corriente controlada de aire a través de una máscara que se coloca sobre la nariz, la boca o ambas. La presión adicional mantiene abiertos los músculos relajados. Existen varias variantes:
- La presión positiva continua en las vías respiratorias (CPAP) es eficaz tanto para la enfermedad moderada como para la grave. [110] Es el tratamiento más común para la apnea obstructiva del sueño. [111]
- La presión positiva variable en las vías respiratorias (VPAP, por sus siglas en inglés) (también conocida como binivel (BiPAP o BPAP)) utiliza un circuito electrónico para monitorear la respiración del paciente y proporciona dos presiones diferentes, una más alta durante la inhalación y una presión más baja durante la exhalación . Este sistema es más costoso y, a veces, se utiliza con pacientes que tienen otros problemas respiratorios coexistentes o que sienten que exhalar contra una presión mayor es incómodo o interrumpe su sueño.
- EPAP nasal , que es un dispositivo similar a un vendaje que se coloca sobre las fosas nasales y que utiliza la propia respiración de la persona para crear una presión positiva en las vías respiratorias y evitar la obstrucción de la respiración. [112]
- La presión positiva automática en las vías respiratorias, también conocida como “Auto CPAP”, incorpora sensores de presión y monitorea la respiración de la persona. [113] [114]
- Una reducción del 5% en el peso entre aquellos con AOS de moderada a severa puede disminuir los síntomas de manera similar a la CPAP. [115]
Puede resultar complicado alentar a las personas con AOS moderada a grave a utilizar dispositivos CPAP, ya que su uso suele requerir un cambio de comportamiento en los hábitos de sueño. [111] El 8 % de las personas que utilizan dispositivos CPAP dejan de utilizarlos después de la primera noche, y el 50 % de las personas con AOS moderada a grave dejan de utilizar sus dispositivos durante el primer año. [111] Se ha demostrado que las iniciativas educativas y las intervenciones de apoyo para ayudar a mejorar el cumplimiento de la terapia con CPAP mejoran el tiempo durante el cual las personas que necesitan terapia con CPAP utilizan sus dispositivos. [111]
Los dispositivos bucales o férulas suelen ser los preferidos, pero pueden no ser tan eficaces como la CPAP. [110] Este dispositivo es un protector bucal similar a los que se utilizan en los deportes para proteger los dientes. Está diseñado para mantener la mandíbula inferior ligeramente hacia abajo y hacia adelante en relación con la posición natural y relajada. Esta posición mantiene la lengua más alejada de la parte posterior de la vía aérea y puede ser suficiente para aliviar la apnea o mejorar la respiración.
A muchas personas les resulta beneficioso dormir con la parte superior del cuerpo a una altura de 30 grados [116] o más, como si estuvieran en un sillón reclinable . De esta manera, se ayuda a prevenir el colapso gravitacional de las vías respiratorias. También se recomienda dormir de lado en lugar de dormir boca arriba . [117] [118] [119]
Algunos estudios han sugerido que tocar un instrumento de viento puede reducir los ronquidos y los incidentes de apnea. [120] Esto puede ser especialmente cierto en el caso de los instrumentos de lengüeta doble . [121]
Expansión palatina rápida
En los niños, es común el tratamiento de ortodoncia para ampliar el volumen de las vías respiratorias nasales, como la expansión palatina rápida no quirúrgica .
Dado que en los adultos la sutura palatina está fusionada, no se puede realizar una expansión palatina rápida regular con expansores soportados por dientes. Recientemente se ha desarrollado la expansión palatina rápida asistida por miniimplantes (MARPE) como una opción no quirúrgica para la expansión transversal del maxilar en adultos. Este método aumenta el volumen de la cavidad nasal y la nasofaringe, lo que aumenta el flujo de aire y reduce los despertares respiratorios durante el sueño. [122] [123] Los cambios son permanentes y las complicaciones son mínimas.
Cirugía
Los tratamientos quirúrgicos para modificar la anatomía de las vías respiratorias, conocidos como cirugía del sueño , son variados y deben adaptarse a las necesidades específicas de obstrucción de las vías respiratorias de un paciente. La cirugía no se considera un tratamiento de primera línea para la apnea obstructiva del sueño en adultos. Hay ensayos clínicos prospectivos, aleatorizados y comparativos, [124] y también un metaanálisis sistemático, [109] que muestra evidencia de que la uvulopalatofaringoplastia conservadora (UPPP) con o sin amigdalectomía es efectiva en pacientes seleccionados que fracasan con el tratamiento conservador. Para aquellos con apnea obstructiva del sueño que no pueden o no quieren cumplir con el tratamiento de primera línea, la intervención quirúrgica debe adaptarse a la anatomía y fisiología específicas de cada individuo, a sus preferencias personales y a la gravedad de la enfermedad. [103] La uvulopalatofaringoplastia con o sin amigdalectomía es la cirugía más común para pacientes con apnea obstructiva del sueño. Los estudios han demostrado que el efecto del tratamiento de la amigdalectomía aumenta con el tamaño de las amígdalas. [125] Sin embargo, hay poca evidencia de ensayos clínicos aleatorizados para otros tipos de cirugía del sueño . [105]
Hay varias operaciones diferentes que se pueden realizar:
- La septoplastia es un procedimiento quirúrgico correctivo para la desviación del tabique nasal en el que se endereza el tabique nasal .
- Amigdalectomía [125] o adenoidectomía en un intento de aumentar el tamaño de las vías respiratorias.
- Extirpación o reducción de partes del paladar blando y de parte o toda la úvula , como la uvulopalatofaringoplastia (UPPP) o la uvulopalatoplastia asistida por láser ( LAUP ). Las variantes modernas de este procedimiento a veces utilizan ondas de radiofrecuencia para calentar y eliminar tejido.
- La turbinectomía es un procedimiento quirúrgico en el que se eliminan todos o algunos de los huesos cornetes para aliviar la obstrucción nasal .
- Reducción de la base de la lengua, ya sea con escisión láser o ablación por radiofrecuencia .
- Avance geniogloso , en el que una pequeña porción de la mandíbula inferior que se une a la lengua se mueve hacia adelante, para alejar la lengua de la parte posterior de la vía aérea.
- Suspensión hioidea , en la que el hueso hioides en el cuello, otro punto de unión de los músculos de la lengua, se tira hacia adelante frente a la laringe .
- Avance maxilomandibular [126]
En los obesos mórbidos, una pérdida importante de peso (como la que ocurre después de una cirugía bariátrica ) a veces puede curar la afección.
La apnea obstructiva del sueño (AOS) en niños suele deberse a amígdalas y adenoides agrandadas, ya que el tejido linfoide crece rápidamente durante la primera infancia. La extirpación quirúrgica de las amígdalas agrandadas (amigdalectomía) y de las adenoides (adenoidectomía) es el tratamiento de primera línea entre los niños con AOS. La operación es un procedimiento común, pero en los casos más extremos, los niños con AOS grave requieren precauciones especiales antes de la cirugía (ver "Cirugía y síndrome de apnea obstructiva del sueño" a continuación). En algunos países, se utiliza un procedimiento quirúrgico más leve llamado amigdalotomía para extirpar el tejido amigdalino que sobresale, un método asociado con menos dolor y menor riesgo de hemorragia posoperatoria. [127]
Neuroestimulación
Para los pacientes que no pueden utilizar un dispositivo de presión positiva continua en las vías respiratorias, la Administración de Alimentos y Medicamentos de los Estados Unidos otorgó en 2014 la aprobación previa a la comercialización de un sistema de estimulación de las vías respiratorias superiores que detecta la respiración y aplica una estimulación eléctrica leve al nervio hipogloso para aumentar el tono muscular en la parte posterior de la lengua para que no colapse sobre las vías respiratorias. El dispositivo incluye un controlador de paciente portátil que permite encenderlo antes de dormir y está alimentado por un generador de pulso implantable, similar al que se utiliza para el control del ritmo cardíaco. La aprobación de este dispositivo de neuromodulación implantable activo fue precedida por un ensayo clínico cuyos resultados se publicaron en el New England Journal of Medicine . [128] [129]
Ablación por radiofrecuencia
La ablación por radiofrecuencia (ARF), que es conceptualmente análoga en algunos aspectos a la cirugía, utiliza energía de ondas de radio de baja frecuencia (300 kHz a 1 MHz) [130] para dirigirse al tejido , lo que provoca necrosis coagulativa . La ARF logra sus efectos a una temperatura de entre 40 °C y 70 °C [131], a diferencia de otros dispositivos electroquirúrgicos que requieren de entre 400 °C y 600 °C para ser eficaces. [132]
Evaluaciones posteriores de seguridad y eficacia llevaron al reconocimiento de la RFA por parte de la Academia Estadounidense de Otorrinolaringología [133] como una opción de tratamiento de somnoplastia en situaciones seleccionadas para la AOS leve a moderada, pero la evidencia fue juzgada como insuficiente para su adopción rutinaria por parte del Colegio Estadounidense de Médicos. [105]
La ablación por radiofrecuencia tiene algunas ventajas potenciales en entornos médicos cuidadosamente seleccionados , como la intolerancia al dispositivo CPAP. Por ejemplo, cuando la adherencia se define como más de cuatro horas de uso nocturno, entre el 46 % y el 83 % de los pacientes con apnea obstructiva del sueño no cumplen con el uso del dispositivo CPAP [134] por diversas razones, incluida la incomodidad al dormir.
La ablación por radiofrecuencia se realiza generalmente en un entorno ambulatorio , utilizando anestesia local o sedación consciente , y el procedimiento en sí suele durar menos de 3 minutos. El tejido objetivo, como la lengua o el paladar, generalmente se aborda a través de la boca sin necesidad de incisiones, aunque ocasionalmente se aborda el objetivo a través del cuello utilizando imágenes asistidas. [135] Si se apunta a la lengua, esto se puede hacer desde el lado dorsal o ventral . Las complicaciones incluyen ulceración , infección , debilidad o entumecimiento de los nervios e hinchazón. Estas complicaciones ocurren en menos del 1% de los procedimientos. [130]
Medicamentos
No hay evidencia suficiente para apoyar el uso de medicamentos para tratar directamente la apnea obstructiva del sueño. [105] [136] [137] Esto incluye el uso de fluoxetina , paroxetina , acetazolamida y triptófano , entre otros. [105] [138]
Estudios recientes están tratando de investigar los cannabinoides como tratamiento para la AOS, especialmente el dronabinol, que es una forma sintética del THC (delta-9-tetrahidrocannabinol). Se sabe que el cannabis influye en el sueño, por ejemplo, puede reducir la latencia del inicio del sueño, sin embargo, los resultados no son consistentes. [139] Los estudios sobre el dronabinol han demostrado un impacto positivo en la AOS, ya que observaron una reducción del IAH (Índice de Apnea-Hipopnea) y un aumento de la somnolencia autoinformada (la somnolencia objetiva no se vio afectada). [140] Sin embargo, se necesitan más pruebas ya que muchos efectos de esas sustancias siguen siendo desconocidos, especialmente los efectos de una ingesta a largo plazo. [141] El efecto sobre la somnolencia y el aumento de peso es particularmente preocupante. [142] Debido a la incertidumbre sobre sus efectos y la falta de evidencia consistente, la Academia Estadounidense de Medicina del Sueño no aprueba el uso de cannabis medicinal para el tratamiento de la AOS. [141] [143]
Sin embargo, en dos ensayos controlados, aleatorizados, doble ciego de fase 3 que incluyeron adultos con apnea obstructiva del sueño moderada a grave y obesidad, la tirzepatida durante 52 semanas redujo sustancialmente los eventos apneico-hipopnicos , el peso corporal, la carga hipóxica, la concentración de PCRus y la presión arterial sistólica , y mejoró los resultados informados por los pacientes relacionados con el sueño, todo presumiblemente mediado por una pérdida de peso inducida del 18 al 20 % desde el inicio. [144]
Existen múltiples fármacos aprobados para tratar la somnolencia diurna excesiva asociada con la apnea obstructiva del sueño, pero no la causa subyacente. Entre ellos se incluyen el solriamfetol , el modafinilo y el armodafinilo . [145] [146] [147]
Aparatos ortopédicos funcionales / aparatos bucales
La evidencia que respalda el uso de aparatos ortopédicos funcionales/ortopedia oral en niños es insuficiente y la evidencia de su efecto es muy baja. Sin embargo, los aparatos ortopédicos funcionales/ortopedia oral pueden considerarse en casos específicos como un auxiliar en el tratamiento de niños con anomalías craneofaciales que son factores de riesgo de apnea. [148]
Pronóstico
Los accidentes cerebrovasculares y otras enfermedades cardiovasculares están relacionados con la AOS, y las personas menores de 70 años tienen un mayor riesgo de muerte prematura. [90] Las personas con apnea del sueño tienen un riesgo 30% mayor de ataque cardíaco o muerte que las que no la padecen. [149] En casos graves y prolongados, el aumento de las presiones pulmonares se transmite al lado derecho del corazón. Esto puede dar lugar a una forma grave de insuficiencia cardíaca congestiva conocida como cor pulmonale . La función diastólica del corazón también se ve afectada. [150] La presión arterial elevada (es decir, hipertensión ) puede ser una consecuencia del síndrome de AOS. [151] Cuando la hipertensión es causada por la AOS, se distingue por el hecho de que, a diferencia de la mayoría de los casos (la denominada hipertensión esencial ), las lecturas no bajan significativamente cuando el individuo está durmiendo (no dipper) o incluso aumentan (dipper invertido). [152]
Sin tratamiento, la privación del sueño y la falta de oxígeno causada por la apnea del sueño aumentan los riesgos de salud como enfermedad cardiovascular , enfermedad aórtica (por ejemplo, aneurisma aórtico ), [153] presión arterial alta , [154] [155] accidente cerebrovascular , [156] diabetes , depresión clínica , [157] aumento de peso, obesidad , [40] e incluso la muerte.
La apnea obstructiva del sueño se asocia con deterioro cognitivo, incluidos déficits en el razonamiento inductivo y deductivo, la atención, la vigilancia, el aprendizaje, las funciones ejecutivas y la memoria episódica y de trabajo. La apnea obstructiva del sueño se asocia con un mayor riesgo de desarrollar deterioro cognitivo leve y demencia, y se ha asociado con cambios neuroanatómicos (reducciones en los volúmenes del hipocampo y del volumen de materia gris de los lóbulos frontal y parietal) que, sin embargo, pueden revertirse al menos en parte con el tratamiento con CPAP. [158] [159]
Epidemiología
Hasta la década de 1990, se sabía poco sobre la frecuencia de la AOS. [160] Un metaanálisis reciente de 24 estudios epidemiológicos sobre la prevalencia de la AOS en la población general de 18 años o más reveló que para ≥ 5 eventos de apnea por hora, la prevalencia de la AOS varió del 9% al 38%, específicamente del 13% al 33% en hombres y del 6% al 19% en mujeres, mientras que en la población de 65 años o más, la prevalencia de la AOS fue tan alta como 84%, incluyendo 90% en hombres y 78% en mujeres. [161] Sin embargo, para ≥ 15 eventos de apnea por hora, la prevalencia de la AOS varió del 6% al 17%, y casi 49% en la población de mayor edad de 65 años o más. [161] Además, un IMC más alto también está vinculado a una mayor prevalencia de AOS, donde un aumento del 10% en el peso corporal condujo a un riesgo 6 veces mayor de AOS en hombres y mujeres obesos. [161]
Sin embargo, la AOS está infradiagnosticada ya que no siempre va acompañada de somnolencia diurna que puede hacer que la respiración alterada durante el sueño pase desapercibida. [82] Por lo tanto, se estima que la prevalencia de la AOS con somnolencia diurna afecta del 3% al 7% de los hombres y del 2% al 5% de las mujeres, y la enfermedad es común tanto en países desarrollados como en desarrollo. [160] La prevalencia de la AOS aumenta con la edad y se diagnostica con mayor frecuencia en personas mayores de 65 años, con estimaciones que varían del 22,1% al 83,6%. [161] La prevalencia ha aumentado drásticamente en las últimas décadas debido a la incidencia de la obesidad. [77]
Los hombres se ven más afectados por la AOS que las mujeres, pero la fenomenología difiere entre ambos sexos. [40] Los ronquidos y la apnea presenciada son más frecuentes entre los hombres, pero el insomnio, por ejemplo, es más frecuente entre las mujeres. [40] La frecuencia de la AOS aumenta con la edad en las mujeres. [40] La mortalidad es mayor en las mujeres. [40]
Algunos estudios reportan que es más frecuente entre la población hispana y afroamericana que entre la población blanca. [40]
Si se estudiara cuidadosamente en un laboratorio del sueño mediante polisomnografía ("estudio del sueño" formal), se cree que aproximadamente 1 de cada 5 adultos estadounidenses tendría al menos AOS leve. [162]
Investigación
Se está estudiando la neuroestimulación como método de tratamiento. [163] Un sistema de estimulación del nervio hipogloso implantado recibió la aprobación de la marca CE europea (Conformité Européenne) en marzo de 2012. [164] También se están estudiando ejercicios de los músculos alrededor de la boca y la garganta a través de actividades como tocar el didgeridoo . [165] [166]
Véase también
Referencias
- ^ Punjabi, Naresh M.; Caffo, Brian S.; Goodwin, James L.; Gottlieb, Daniel J.; Newman, Anne B.; O'Connor, George T.; Rapoport, David M.; Redline, Susan; Resnick, Helaine E.; Robbins, John A.; Shahar, Eyal; Unruh, Mark L.; Samet, Jonathan M. (18 de agosto de 2009). "Respiración alterada durante el sueño y mortalidad: un estudio de cohorte prospectivo". PLOS Medicine . 6 (8): e1000132. doi : 10.1371/journal.pmed.1000132 . PMC 2722083 . PMID 19688045.
- ^ Barnes L, ed. (2009). Patología quirúrgica de cabeza y cuello (3.ª ed.). Nueva York: Informa healthcare. ISBN 978-1-4200-9163-2.:226
- ^ abcde Young, Terry; Skatrud, J; Peppard, PE (28 de abril de 2004). "Factores de riesgo de apnea obstructiva del sueño en adultos". JAMA . 291 (16): 2013–2016. doi :10.1001/jama.291.16.2013. PMID 15113821. S2CID 12315855.
- ^ Berry, Richard B.; Budhiraja, Rohit; Gottlieb, Daniel J.; Gozal, David; Iber, Conrad; Kapur, Vishesh K.; Marcus, Carole L.; Mehra, Reena; Parthasarathy, Sairam; Quan, Stuart F.; Redline, Susan; Strohl, Kingman P.; Ward, Sally L. Davidson; Tangredi, Michelle M.; Academia Estadounidense de Medicina del Sueño (2012). "Reglas para la puntuación de eventos respiratorios durante el sueño: actualización del Manual de la AASM de 2007 para la puntuación del sueño y eventos asociados". Revista de medicina clínica del sueño . 08 (5): 597–619. doi : 10.5664/jcsm.2172 . PMC 3459210 . PMID 23066376.
- ^ Academia Estadounidense de Medicina del Sueño (2014). Clasificación internacional de los trastornos del sueño, 3.ª edición . Darien, IL: Academia Estadounidense de Medicina del Sueño.
- ^ Tung P, Levitzky YS, Wang R, Weng J, Quan SF, Gottlieb DJ, et al. (julio de 2017). "Apnea obstructiva y central del sueño y riesgo de fibrilación auricular incidental en una cohorte comunitaria de hombres y mujeres". Revista de la Asociación Estadounidense del Corazón . 6 (7). doi :10.1161/jaha.116.004500. PMC 5586257 . PMID 28668820.
- ^ Stoohs RA, Blum HC, Knaack L, Butsch-von-der-Heydt B, Guilleminault C (marzo de 2005). "Comparación de la presión pleural y el electromiograma diafragmático transcutáneo en el síndrome de apnea obstructiva del sueño". Sleep . 28 (3): 321–329. PMID 16173653.
- ^ ab Academia Estadounidense de Medicina del Sueño. "Pautas de práctica de la AASM". AASM . Consultado el 19 de junio de 2019 .
- ^ Mbata, GC; Chukwuka, JC (2012). "Síndrome de apnea-hipopnea obstructiva del sueño". Anales de investigación en ciencias médicas y de la salud . 2 (1): 74–77. doi : 10.4103/2141-9248.96943 . PMC 3507119 . PMID 23209996.
- ^ Caporale, Mina; Palmeri, Rosana; Corallo, Francesco; Muscará, Nunzio; Romeo, Laura; Bramanti, Alessia; Marino, Silvia; Lo Buono, Viviana (23 de mayo de 2020). "Deterioro cognitivo en el síndrome de apnea obstructiva del sueño: una revisión descriptiva". Dormir y Respirar . 25 (1): 29–40. doi :10.1007/s11325-020-02084-3. PMID 32447633. S2CID 218835830.
- ^ Ezzeddini R, Darabi M, Ghasemi B, Jabbari Moghaddam Y, Abdollahi SH, Rashtchizadeh N, Gharahdaghi A, Darabi M, Ansarin M, Shaaker M, Samadi A, Karamravan J (abril de 2012). "Actividad de la fosfolipasa-A2 circulante en la apnea obstructiva del sueño y la amigdalitis recurrente". Int J Pediatr Otorrinolaringol . 76 (4): 741–744. doi :10.1016/j.ijporl.2011.12.026. PMID 22297210.
- ^ Ezzedini R, Darabi M, Ghasemi B, Darabi M, Fayezi SH, Jabbari Moghaddam Y, Mehdizadeh A, Abdollahi SH, Gharahdaghi A (mayo de 2013). "Composición de ácidos grasos tisulares en la apnea obstructiva del sueño y la amigdalitis recurrente". Int J Pediatr Otorrinolaringol . 77 (6): 1008–1012. doi :10.1016/j.ijporl.2013.03.033. PMID 23643333.
- ^ "Apnea obstructiva del sueño". Biblioteca de conceptos médicos de Lecturio . 7 de agosto de 2020. Consultado el 21 de agosto de 2021 .
- ^ Gale, Shawn D.; Hopkins, Ramona O. (enero de 2004). "Efectos de la hipoxia en el cerebro: neuroimagen y hallazgos neuropsicológicos tras intoxicación por monóxido de carbono y apnea obstructiva del sueño". Revista de la Sociedad Internacional de Neuropsicología . 10 (1): 60–71. doi :10.1017/S1355617704101082. PMID 14751008. S2CID 23745738.
- ^ Henry, Doug; Rosenthal, Leon (febrero de 2013). "'Escuchando su respiración': la importancia del género y la información de la pareja en el diagnóstico, manejo y tratamiento de la apnea obstructiva del sueño". Ciencias Sociales y Medicina . 79 : 48–56. doi :10.1016/j.socscimed.2012.05.021. PMID 22770968.
- ^ O'Brien, Louise M.; Holbrook, Cheryl R.; Mervis, Carolyn B.; Klaus, Carrie J.; Bruner, Jennifer L.; Raffield, Troy J.; Rutherford, Jennifer; Mehl, Rochelle C.; Wang, Mei; Tuell, Andrew; Hume, Brittany C.; Gozal, David (marzo de 2003). "Características neuroconductuales y del sueño de niños de 5 a 7 años con síntomas informados por los padres de trastorno por déficit de atención e hiperactividad". Pediatría . 111 (3): 554–563. doi :10.1542/peds.111.3.554. PMID 12612236.
- ^ Schechter, Michael S. (abril de 2002). "Informe técnico: diagnóstico y tratamiento del síndrome de apnea obstructiva del sueño infantil". Pediatría . 109 (4): e69. doi :10.1542/peds.109.4.e69. PMID 11927742.
- ^ Rosen, Carol L.; Storfer-Isser, Amy; Taylor, H. Gerry; Kirchner, H. Lester; Emancipator, Judith L.; Redline, Susan (diciembre de 2004). "Aumento de la morbilidad conductual en niños en edad escolar con trastornos respiratorios del sueño". Pediatría . 114 (6): 1640–1648. doi :10.1542/peds.2004-0103. PMID 15574628. S2CID 7655711.
- ^ abcdefghijkl Dehlink E, Tan HL (febrero de 2016). "Actualización sobre la apnea obstructiva del sueño pediátrica". Journal of Thoracic Disease . 8 (2): 224–235. doi :10.3978/j.issn.2072-1439.2015.12.04. PMC 4739955 . PMID 26904263.
- ^ Jazi SM, Barati B, Kheradmand A (diciembre de 2011). "Tratamiento de la hipertrofia adenoamigdalar: un ensayo aleatorio prospectivo que compara la azitromicina con la fluticasona". Revista de investigación en ciencias médicas . 16 (12): 1590–1597. PMC 3434901 . PMID 22973368.
- ^ abcdefghijklmn Capdevila OS, Kheirandish-Gozal L, Dayyat E, Gozal D (febrero de 2008). "Apnea obstructiva del sueño pediátrica: complicaciones, tratamiento y resultados a largo plazo". Actas de la American Thoracic Society . 5 (2): 274–282. doi :10.1513/pats.200708-138MG. PMC 2645258. PMID 18250221.
- ^ abcdefghijklmno Dayyat E, Kheirandish-Gozal L, Gozal D (septiembre de 2007). "Apnea obstructiva del sueño infantil: ¿una o dos entidades patológicas distintas?". Sleep Medicine Clinics . 2 (3): 433–444. doi :10.1016/j.jsmc.2007.05.004. PMC 2084206 . PMID 18769509.
- ^ Kalra M, Inge T, Garcia V, Daniels S, Lawson L, Curti R, et al. (julio de 2005). "Apnea obstructiva del sueño en adolescentes con sobrepeso extremo sometidos a cirugía bariátrica". Investigación sobre la obesidad . 13 (7): 1175–1179. doi : 10.1038/oby.2005.139 . PMID 16076986.
- ^ ab Verhulst SL, Franckx H, Van Gaal L, De Backer W, Desager K (junio de 2009). "El efecto de la pérdida de peso en la respiración alterada durante el sueño en adolescentes obesos". Obesidad . 17 (6): 1178–1183. doi : 10.1038/oby.2008.673 . PMID 19265797. S2CID 205526401.
- ^ Bower CM, Gungor A (febrero de 2000). "Síndrome de apnea obstructiva del sueño pediátrico". Clínicas otorrinolaringológicas de Norteamérica . 33 (1): 49–75. doi :10.1016/s0030-6665(05)70207-3. PMID 10637344.
- ^ Mills, Jacqueline; Kuohung, Wendy (2019). "Impacto de los ritmos circadianos en la reproducción femenina y el éxito del tratamiento de la infertilidad". Current Opinion in Endocrinology, Diabetes & Obesity . 26 (6): 317–321. doi :10.1097/MED.0000000000000511. PMID 31644470. S2CID 204865937.
- ^ Saboisky JP, Butler JE, Gandevia SC, Eckert DJ (15 de junio de 2012). "Papel funcional de la lesión neural en la apnea obstructiva del sueño". Frontiers in Neurology . 3 : 95. doi : 10.3389/fneur.2012.00095 . PMC 3375463 . PMID 22715333.
- ^ Schwab RJ, Kim C, Bagchi S, Keenan BT, Comyn FL, Wang S, et al. (junio de 2015). "Comprensión de la base anatómica del síndrome de apnea obstructiva del sueño en adolescentes". American Journal of Respiratory and Critical Care Medicine . 191 (11): 1295–1309. doi :10.1164/rccm.201501-0169OC. PMC 4476519 . PMID 25835282.
- ^ Edwards N, Sullivan CE (2008). "Respiración alterada durante el sueño en el embarazo". Clínicas de Medicina del Sueño . 3 (6): 81–95. doi :10.1016/j.jsmc.2007.10.010. PMC 1746354 . PMID 12037233.
- ^ "Apnea del sueño: síntomas y causas". Mayo Clinic .
- ^ Lu LR, Peat JK, Sullivan CE (agosto de 2003). "Ronquidos en niños en edad preescolar: prevalencia y asociación con tos nocturna y asma". Chest . 124 (2): 587–593. doi :10.1378/chest.124.2.587. PMID 12907547.
- ^ McColley, Susanna A.; Carroll, John L.; Curtis, Shelly; Loughlin, Gerald M.; Sampson, Hugh A. (enero de 1997). "Alta prevalencia de sensibilización alérgica en niños con ronquidos habituales y apnea obstructiva del sueño". Chest . 111 (1): 170–173. doi : 10.1378/chest.111.1.170 . PMID 8996012.
- ^ de Miguel-Díez J, Villa-Asensi JR, Alvarez-Sala JL (diciembre de 2003). "Prevalencia de trastornos respiratorios durante el sueño en niños con síndrome de Down: hallazgos poligráficos en 108 niños". Sleep . 26 (8): 1006–1009. doi :10.1093/sleep/26.8.1006. PMID 14746382.
- ^ Shott SR, Amin R, Chini B, Heubi C, Hotze S, Akers R (abril de 2006). "Apnea obstructiva del sueño: ¿deberían evaluarse todos los niños con síndrome de Down?". Archivos de otorrinolaringología y cirugía de cabeza y cuello . 132 (4): 432–436. doi :10.1001/archotol.132.4.432. PMID 16618913.
- ^ Sloan, Gerald M. (marzo de 2000). "Colgajo faríngeo posterior y faringoplastia del esfínter: el estado del arte". The Cleft Palate-Craniofacial Journal . 37 (2): 112–122. doi :10.1597/1545-1569_2000_037_0112_ppfasp_2.3.co_2. PMID 10749049. S2CID 208150617.
- ^ Pugh, MB et al. (2000). Apnea. Stedman's Medical Dictionary (27.ª ed.). Recuperado el 18 de junio de 2006 de la base de datos de la biblioteca médica en línea STAT!Ref. [ página necesaria ]
- ^ Liao YF, Noordhoff MS, Huang CS, Chen PK, Chen NH, Yun C, Chuang ML (marzo de 2004). "Comparación del síndrome de apnea obstructiva del sueño en niños con paladar hendido después de una palatoplastia de Furlow o un colgajo faríngeo para la insuficiencia velofaríngea". The Cleft Palate-Craniofacial Journal . 41 (2): 152–156. doi :10.1597/02-162. PMID 14989690. S2CID 20976608.
- ^ McWilliams BJ, Peterson-Falzone SJ, Hardin-Jones MA, Karnell MP (2001). Discurso de paladar hendido (3ª ed.). San Luis: Mosby. ISBN 978-0-8151-3153-3.[ página necesaria ]
- ^ Gross JB, Bachenberg KL, Benumof JL, Caplan RA, Connis RT, Coté CJ, et al. (mayo de 2006). "Pautas de práctica para el manejo perioperatorio de pacientes con apnea obstructiva del sueño: un informe del Grupo de trabajo sobre manejo perioperatorio de pacientes con apnea obstructiva del sueño de la Sociedad Estadounidense de Anestesiólogos". Anestesiología . 104 (5): 1081–1093, cuestionario 1117–1118. doi :10.1097/00000542-200605000-00026. PMID 16645462. S2CID 14151958.
- ^ abcdefghij Foldvary-Schaefer, Nancy R.; Waters, Tina E. (agosto de 2017). "Respiración alterada durante el sueño". Continuum: aprendizaje permanente en neurología . 23 (4): 1093–1116. doi :10.1212/01.CON.0000522245.13784.f6. PMID 28777178. S2CID 20852866.
- ^ abcd Walter LM, Horne RS (2018). "Respiración obstructiva durante el sueño en niños; impacto en el cerebro en desarrollo". Pediatric Respirology and Critical Care Medicine . 2 (4): 58–64. doi : 10.4103/prcm.prcm_16_18 . S2CID 80862031.
- ^ ab Chervin RD, Archbold KH (mayo de 2001). "Hiperactividad y hallazgos polisomnográficos en niños evaluados por trastornos respiratorios del sueño". Sleep . 24 (3): 313–320. doi : 10.1093/sleep/24.3.313 . PMID 11322714.
- ^ Halbower, Ann C; Degaonkar, Mahaveer; Barker, Peter B; Earley, Christopher J; Marcus, Carole L; Smith, Philip L; Prahme, M. Cristine; Mahone, E. Mark (2006). "La apnea obstructiva del sueño infantil se asocia con déficits neuropsicológicos y lesión cerebral neuronal". PLOS Medicine . 3 (8): e301. doi : 10.1371/journal.pmed.0030301 . PMC 1551912 . PMID 16933960.
- ^ ab Nieminen P, Löppönen T, Tolonen U, Lanning P, Knip M, Löppönen H. Crecimiento y marcadores bioquímicos del crecimiento en niños con ronquidos y apnea obstructiva del sueño. Pediatría. 2002;109(4):e55. doi:10.1542/peds.109.4.e55
- ^ ab O'Brien LM, Mervis CB, Holbrook CR, Bruner JL, Smith NH, McNally N, et al. (junio de 2004). "Correlaciones neuroconductuales de la respiración alterada durante el sueño en niños". Journal of Sleep Research . 13 (2): 165–172. doi :10.1111/j.1365-2869.2004.00395.x. PMID 15175097. S2CID 25860827.
- ^ abcd Goyal A, Pakhare AP, Bhatt GC, Choudhary B, Patil R (2018). "Asociación de la apnea obstructiva del sueño pediátrica con un bajo rendimiento académico: un estudio escolar de la India". Lung India . 35 (2): 132–136. doi : 10.4103/lungindia.lungindia_218_17 . PMC 5846262 . PMID 29487248.
- ^ abc Galland B, Spruyt K, Dawes P, McDowall PS, Elder D, Schaughency E (octubre de 2015). "Trastornos respiratorios del sueño y rendimiento académico: un metaanálisis". Pediatría . 136 (4): e934–946. doi : 10.1542/peds.2015-1677 . PMID 26347434. S2CID 20590026.
- ^ abcd Amin R, Somers VK, McConnell K, Willging P, Myer C, Sherman M, et al. (enero de 2008). "Presión arterial ambulatoria de 24 horas ajustada a la actividad y remodelación cardíaca en niños con trastornos respiratorios del sueño". Hipertensión . 51 (1): 84–91. doi : 10.1161/HYPERTENSIONAHA.107.099762 . PMID 18071053. S2CID 1736152.
- ^ Ip, Mary SM; Lam, Bing; Ng, Matthew MT; Lam, Wah Kit; Tsang, Kenneth WT; Lam, Karen SL (1 de marzo de 2002). "La apnea obstructiva del sueño se asocia de forma independiente con la resistencia a la insulina". American Journal of Respiratory and Critical Care Medicine . 165 (5): 670–676. doi :10.1164/ajrccm.165.5.2103001. PMID 11874812.
- ^ abc Basha, Suzanne; Bialowas, Christie; Ende, Kevin; Szeremeta, Wasyl (2005). "Efectividad de la adenoamigdalectomía en la resolución de la enuresis nocturna secundaria a la apnea obstructiva del sueño". El laringoscopio . 115 (6): 1101–1103. doi :10.1097/01.MLG.0000163762.13870.83. PMID 15933530. S2CID 44686421.
- ^ abc Barone JG, Hanson C, DaJusta DG, Gioia K, England SJ, Schneider D (julio de 2009). "La enuresis nocturna y el sobrepeso se asocian con la apnea obstructiva del sueño". Pediatría . 124 (1): e53–59. doi :10.1542/peds.2008-2805. PMID 19564269. S2CID 7324455.
- ^ abcd Brooks, Lee J.; Topol, Howard I. (mayo de 2003). "Enuresis en niños con apnea del sueño". The Journal of Pediatrics . 142 (5): 515–518. doi :10.1067/mpd.2003.158. PMID 12756383.
- ^ ab Weissbach A, Leiberman A, Tarasiuk A, Goldbart A, Tal A (agosto de 2006). "La adenoamigdalectomía mejora la enuresis en niños con síndrome de apnea obstructiva del sueño". Revista internacional de otorrinolaringología pediátrica . 70 (8): 1351–1356. doi :10.1016/j.ijporl.2006.01.011. PMID 16504310.
- ^ abcd Carotenuto M, Esposito M, Parisi L, Gallai B, Marotta R, Pascotto A, Roccella M (2012). "Síntomas depresivos y síndrome de apnea del sueño infantil". Enfermedades neuropsiquiátricas y tratamiento . 8 : 369–373. doi : 10.2147/NDT.S35974 . PMC: 3430390. PMID: 22977304 .
- ^ abc Yilmaz E, Sedky K, Bennett DS (noviembre de 2013). "La relación entre los síntomas depresivos y la apnea obstructiva del sueño en poblaciones pediátricas: un metaanálisis". Journal of Clinical Sleep Medicine . 9 (11): 1213–1220. doi :10.5664/jcsm.3178. PMC 3805811 . PMID 24235907.
- ^ Crabtree VM, Varni JW, Gozal D (septiembre de 2004). "Calidad de vida relacionada con la salud y síntomas depresivos en niños con sospecha de trastornos respiratorios del sueño". Sleep . 27 (6): 1131–1138. doi : 10.1093/sleep/27.6.1131 . PMID 15532207.
- ^ abcdefg Alsubie HS, BaHammam AS (enero de 2017). "Apnea obstructiva del sueño: los niños no son adultos pequeños". Paediatric Respiratory Reviews . 21 : 72–79. doi :10.1016/j.prrv.2016.02.003. PMID 27262609.
- ^ abcdefghijk McNicholas WT (febrero de 2008). "Diagnóstico de la apnea obstructiva del sueño en adultos". Actas de la American Thoracic Society . 5 (2): 154–160. doi :10.1513/pats.200708-118MG. PMID 18250207.
- ^ Stranks EK, Crowe SF (marzo de 2016). "Los efectos cognitivos de la apnea obstructiva del sueño: un metaanálisis actualizado". Archivos de neuropsicología clínica . 31 (2): 186–193. doi : 10.1093/arclin/acv087 . PMID 26743325.
- ^ Robichaud-Hallé L, Beaudry M, Fortin M (septiembre de 2012). "Apnea obstructiva del sueño y multimorbilidad". Medicina pulmonar BMC . 12 (60): 60. doi : 10.1186/1471-2466-12-60 . PMC 3515504 . PMID 23006602.
- ^ Romero-Corral A, Caples SM, Lopez-Jimenez F, Somers VK (marzo de 2010). "Interacciones entre la obesidad y la apnea obstructiva del sueño: implicaciones para el tratamiento". Chest . 137 (3): 711–719. doi :10.1378/chest.09-0360. PMC 3021364 . PMID 20202954.
- ^ ab Fulda S, Schulz H (2003). "Disfunción cognitiva en los trastornos respiratorios relacionados con el sueño: un metaanálisis". Investigación del sueño en línea . 5 (1): 19–51.
- ^ abcd Bucks RS, Olaithe M, Eastwood P (enero de 2013). "Función neurocognitiva en la apnea obstructiva del sueño: una meta-revisión". Respirology . 18 (1): 61–70. doi :10.1111/j.1440-1843.2012.02255.x. PMID 22913604. S2CID 27228461.
- ^ Nejati V, Salehinejad MA, Nitsche MA (enero de 2018). "Interacción de la corteza prefrontal dorsolateral izquierda (l-DLPFC) y la corteza orbitofrontal derecha (OFC) en las funciones ejecutivas calientes y frías: evidencia de la estimulación transcraneal con corriente directa (tDCS)". Neurociencia . 369 : 109–123. doi :10.1016/j.neuroscience.2017.10.042. PMID 29113929. S2CID 207258425.
- ^ ab Beebe DW, Groesz L, Wells C, Nichols A, McGee K (mayo de 2003). "Los efectos neuropsicológicos de la apnea obstructiva del sueño: un metaanálisis de datos de casos y controles basados en normas". Sleep . 26 (3): 298–307. doi : 10.1093/sleep/26.3.298 . PMID 12749549.
- ^ abc Wallace A, Bucks RS (febrero de 2013). "Memoria y apnea obstructiva del sueño: un metaanálisis". Sleep . 36 (2): 203–220. doi :10.5665/sleep.2374. PMC 3543053 . PMID 23372268.
- ^ ab Olaithe, Michelle; Bucks, Romola S.; Hillman, David R.; Eastwood, Peter R. (abril de 2018). "Déficits cognitivos en la apnea obstructiva del sueño: perspectivas de una metarevisión y comparación con los déficits observados en la EPOC, el insomnio y la privación del sueño" (PDF) . Sleep Medicine Reviews . 38 : 39–49. doi :10.1016/j.smrv.2017.03.005. PMID 28760549.
- ^ Rizzo D (agosto de 2018). "Políticas, conductas y medidas de detección de la apnea obstructiva del sueño al conducir".
{{cite journal}}: Requiere citar revista|journal=( ayuda ) - ^ Morrone E, D'Artavilla Lupo N (2020). "El microsueño como marcador de somnolencia en pacientes con apnea obstructiva del sueño". Revista de investigación del sueño . 29 (2): e12882. doi :10.1111/jsr.12882. PMID 31180173. S2CID 182949124.
- ^ Cori JM, Jackson ML, Barnes M, Westlake J, Emerson P, Lee J, et al. (junio de 2018). "Los efectos diferenciales del trabajo por turnos regulares y la apnea obstructiva del sueño sobre la somnolencia, el estado de ánimo y la función neurocognitiva". Journal of Clinical Sleep Medicine . 14 (6): 941–951. doi :10.5664/jcsm.7156. PMC 5991942 . PMID 29852909.
- ^ Slater G, Steier J (diciembre de 2012). "Somnolencia diurna excesiva en trastornos del sueño". Journal of Thoracic Disease . 4 (6): 608–616. doi :10.3978/j.issn.2072-1439.2012.10.07. PMC 3506799 . PMID 23205286.
- ^ LaGrotte C, Fernandez-Mendoza J, Calhoun SL, Liao D, Bixler EO, Vgontzas AN (septiembre de 2016). "La asociación relativa de la apnea obstructiva del sueño, la obesidad y la somnolencia diurna excesiva con la depresión incidente: un estudio longitudinal, basado en la población". Revista Internacional de Obesidad . 40 (9): 1397–1404. doi :10.1038/ijo.2016.87. PMC 5014694 . PMID 27143032.
- ^ Mulgrew AT, Ryan CF, Fleetham JA, Cheema R, Fox N, Koehoorn M, et al. (diciembre de 2007). "El impacto de la apnea obstructiva del sueño y la somnolencia diurna en la limitación laboral". Medicina del sueño . 9 (1): 42–53. doi :10.1016/j.sleep.2007.01.009. PMID 17825611.
- ^ Guilleminault C, Brooks SN (agosto de 2001). "Somnolencia diurna excesiva: un desafío para el neurólogo en ejercicio". Brain . 124 (Pt 8): 1482–1491. doi : 10.1093/brain/124.8.1482 . PMID 11459741.
- ^ Jackson ML, McEvoy RD, Banks S, Barnes M (enero de 2018). "Deterioro neuroconductual y respuesta al tratamiento con CPAP en apneas obstructivas del sueño leves a moderadas". Journal of Clinical Sleep Medicine . 14 (1): 47–56. doi :10.5664/jcsm.6878. PMC 5734892 . PMID 29198304.
- ^ Eskandari D, Zou D, Grote L, Schneider H, Penzel T, Hedner J (junio de 2017). "Asociaciones independientes entre el bicarbonato arterial, la gravedad de la apnea y la hipertensión en la apnea obstructiva del sueño". Investigación respiratoria . 18 (1): 130. doi : 10.1186/s12931-017-0607-9 . PMC 5490198 . PMID 28659192.
- ^ abc Drager LF, Togeiro SM, Polotsky VY, Lorenzi-Filho G (agosto de 2013). "Apnea obstructiva del sueño: un riesgo cardiometabólico en la obesidad y el síndrome metabólico". Revista del Colegio Americano de Cardiología . 62 (7): 569–76. doi :10.1016/j.jacc.2013.05.045. PMC 4461232 . PMID 23770180.
- ^ ab Ashrafian H, Toma T, Rowland SP, Harling L, Tan A, Efthimiou E, et al. (julio de 2015). "¿Cirugía bariátrica o pérdida de peso no quirúrgica para la apnea obstructiva del sueño? Una revisión sistemática y comparación de metanálisis". Cirugía de la obesidad . 25 (7): 1239–1250. doi :10.1007/s11695-014-1533-2. hdl : 10044/1/54731 . PMID: 25537297. S2CID : 5284156.
- ^ Dobrosielski DA, Patil S, Schwartz AR, Bandeen-Roche K, Stewart KJ (enero de 2015). "Efectos del ejercicio y la pérdida de peso en adultos mayores con apnea obstructiva del sueño". Medicina y ciencia en deportes y ejercicio . 47 (1): 20–26. doi :10.1249/MSS.0000000000000387. PMC 4246024 . PMID 24870569.
- ^ abcd Reutrakul, Sirimon; Mokhlesi, Babak (noviembre de 2017). "Apnea obstructiva del sueño y diabetes". Chest . 152 (5): 1070–1086. doi :10.1016/j.chest.2017.05.009. PMC 5812754 . PMID 28527878.
- ^ abc Guglielmi O, Magnavita N, Garbarino S (mayo de 2018). "Calidad del sueño, apnea obstructiva del sueño y distrés psicológico en conductores de camiones: un estudio transversal". Psiquiatría social y epidemiología psiquiátrica . 53 (5): 531–536. doi :10.1007/s00127-017-1474-x. PMID 29285594. S2CID 4914966.
- ^ abc Olaithe M, Nanthakumar S, Eastwood PR, Bucks RS (2015). "Disfunción cognitiva y del estado de ánimo en la apnea obstructiva del sueño (AOS) en adultos: implicaciones para la investigación y la práctica psicológica". Problemas traslacionales en la ciencia psicológica . 1 (1): 67–78. doi :10.1037/tps0000021.
- ^ abc Garbarino S, Bardwell WA, Guglielmi O, Chiorri C, Bonanni E, Magnavita N (2018). "Asociación de ansiedad y depresión en pacientes con apnea obstructiva del sueño: una revisión sistemática y un metaanálisis". Medicina conductual del sueño . 18 (1): 35–57. doi :10.1080/15402002.2018.1545649. PMID 30453780. S2CID 53872339.
- ^ ab Xiao Y, Han D, Zang H, Wang D (junio de 2016). "La efectividad de la cirugía nasal en los síntomas psicológicos en pacientes con apnea obstructiva del sueño y obstrucción nasal". Acta Oto-Laryngologica . 136 (6): 626–632. doi :10.3109/00016489.2016.1143120. PMID 26903174. S2CID 10364903.
- ^ Gupta MA, Simpson FC (enero de 2015). "Apnea obstructiva del sueño y trastornos psiquiátricos: una revisión sistemática". Revista de medicina clínica del sueño . 11 (2): 165–175. doi :10.5664/jcsm.4466. PMC 4298774 . PMID 25406268.
- ^ Jonas DE, Amick HR, Feltner C, Weber RP, Arvanitis M, Stine A, et al. (enero de 2017). "Detección de la apnea obstructiva del sueño en adultos: informe de evidencia y revisión sistemática para el grupo de trabajo de servicios preventivos de EE. UU.", JAMA . 317 (4): 415–433. doi :10.1001/jama.2016.19635. PMID 28118460. S2CID 3656829.
- ^ ab Charokopos A, Card ME, Gunderson C, Steffens C, Bastian LA (septiembre de 2018). "La asociación de la apnea obstructiva del sueño y los resultados del dolor en adultos: una revisión sistemática". Medicina del dolor . 19 (suppl_1): S69–S75. doi : 10.1093/pm/pny140 . PMID 30203008. S2CID 52182664.
- ^ Jonas DE, Amick HR, Feltner C, Weber RP, Arvanitis M, Stine A, et al. (enero de 2017). "Detección de la apnea obstructiva del sueño en adultos: informe de evidencia y revisión sistemática para el Grupo de trabajo de servicios preventivos de EE. UU.", JAMA . 317 (4): 415–433. doi : 10.1001/jama.2016.19635 . PMID 28118460.
- ^ Bibbins-Domingo K, Grossman DC, Curry SJ, Davidson KW, Epling JW, García FA, et al. (enero de 2017). "Detección de la apnea obstructiva del sueño en adultos: declaración de recomendación del grupo de trabajo de servicios preventivos de EE. UU." JAMA . 317 (4): 407–414. doi : 10.1001/jama.2016.20325 . PMID 28118461.
- ^ ab Franklin KA, Lindberg E (agosto de 2015). "La apnea obstructiva del sueño es un trastorno común en la población: una revisión sobre la epidemiología de la apnea del sueño". Journal of Thoracic Disease . 7 (8): 1311–1322. doi :10.3978/j.issn.2072-1439.2015.06.11. PMC 4561280 . PMID 26380759.
- ^ Berry RB, Quan SF, Abrue AR, et al.; para la Academia Estadounidense de Medicina del Sueño. Manual de la AASM para la puntuación del sueño y eventos asociados: reglas, terminología y especificaciones técnicas. Versión 2.6. Darien, IL: Academia Estadounidense de Medicina del Sueño; 2020.
- ^ Kapur VK, Auckley DH, Chowdhuri S, Kuhlmann DC, Mehra R, Ramar K, Harrod CG (marzo de 2017). "Guía de práctica clínica para pruebas diagnósticas de apnea obstructiva del sueño en adultos: guía de práctica clínica de la Academia Estadounidense de Medicina del Sueño". Revista de Medicina Clínica del Sueño . 13 (3): 479–504. doi :10.5664/jcsm.6506. PMC 5337595 . PMID 28162150.
- ^ Thurnheer, R. (septiembre de 2007). "Diagnóstico del síndrome de apnea obstructiva del sueño". Minerva Pneumologica . 46 (3): 191–204. S2CID 52540419.
- ^ Crook S, Sievi NA, Bloch KE, Stradling JR, Frei A, Puhan MA, Kohler M (abril de 2019). "Diferencia mínima importante de la Escala de somnolencia de Epworth en la apnea obstructiva del sueño: estimación a partir de tres ensayos controlados aleatorizados". Thorax . 74 (4): 390–396. doi : 10.1136/thoraxjnl-2018-211959 . PMID 30100576. S2CID 51967356.
- ^ Chiu HY, Chen PY, Chuang LP, Chen NH, Tu YK, Hsieh YJ, et al. (diciembre de 2017). "Precisión diagnóstica del cuestionario de Berlín, STOP-BANG, STOP y la escala de somnolencia de Epworth en la detección de la apnea obstructiva del sueño: un metanálisis bivariado". Sleep Medicine Reviews . 36 : 57–70. doi :10.1016/j.smrv.2016.10.004. PMID 27919588.
- ^ Amra B, Javani M, Soltaninejad F, Penzel T, Fietze I, Schoebel C, Farajzadegan Z (2018). "Comparación del cuestionario de Berlín, STOP-Bang y la escala de somnolencia de Epworth para diagnosticar la apnea obstructiva del sueño en pacientes persas". Revista internacional de medicina preventiva . 9 (28): 28. doi : 10.4103/ijpvm.IJPVM_131_17 . PMC 5869953 . PMID 29619152.
- ^ Academia Estadounidense de Medicina del Sueño. Clasificación internacional de los trastornos del sueño. 3.ª ed. Darien, IL: Academia Estadounidense de Medicina del Sueño, 2014. [ página necesaria ]
- ^ Tschopp, Samuel; Wimmer, Wilhelm; Caversaccio, Marco; Borner, Urs; Tschopp, Kurt (30 de marzo de 2021). "Variabilidad de una noche a otra en la apnea obstructiva del sueño mediante tonometría arterial periférica: un caso de pruebas nocturnas múltiples". Revista de medicina clínica del sueño . 17 (9): 1751–1758. doi :10.5664/jcsm.9300. ISSN 1550-9389. PMC 8636340 . PMID 33783347. S2CID 232420123.
- ^ Jennifer M. Slowik; Jacob F. Collen (2020). "Apnea obstructiva del sueño". StatPearls . PMID 29083619. Este artículo incorpora texto disponible bajo la licencia CC BY 4.0.
- ^ "Trastornos respiratorios relacionados con el sueño en adultos: recomendaciones para la definición del síndrome y técnicas de medición en la investigación clínica. Informe de un grupo de trabajo de la Academia Estadounidense de Medicina del Sueño". Sleep . 22 (5): 667–689. Agosto de 1999. doi : 10.1093/sleep/22.5.667 . PMID 10450601.
- ^ Mulgrew AT, Fox N, Ayas NT, Ryan CF (febrero de 2007). "Diagnóstico y tratamiento inicial de la apnea obstructiva del sueño sin polisomnografía: un estudio de validación aleatorizado". Anales de Medicina Interna . 146 (3): 157–166. doi :10.7326/0003-4819-146-3-200702060-00004. PMID 17283346. S2CID 25693423.
- ^ Flemons WW, Whitelaw WA, Brant R, Remmers JE (noviembre de 1994). "Razones de verosimilitud para una regla de predicción clínica de la apnea del sueño". American Journal of Respiratory and Critical Care Medicine . 150 (5 Pt 1): 1279–1285. doi :10.1164/ajrccm.150.5.7952553. PMID 7952553.
- ^ de Friedman: Apnea del sueño y ronquidos, 1.ª ed., 2008
- ^ Azagra-Calero E, Espinar-Escalona E, Barrera-Mora JM, Llamas-Carreras JM, Solano-Reina E (noviembre de 2012). "Síndrome de apnea obstructiva del sueño (SAOS). Revisión de la literatura". Medicina Oral, Patología Oral y Cirugía Bucal . 17 (6): e925–929. doi :10.4317/medoral.17706. PMC 3505711 . PMID 22549673.
- ^ abcdef Qaseem, Amir; Holty, Jon-Erik C.; Owens, Douglas K.; Dallas, Paul; Starkey, Melissa; Shekelle, Paul; Comité de Guías Clínicas del Colegio Americano de Médicos. (1 de octubre de 2013). "Manejo de la apnea obstructiva del sueño en adultos: una guía de práctica clínica del Colegio Americano de Médicos". Anales de Medicina Interna . 159 (7): 471–483. doi : 10.7326/0003-4819-159-7-201310010-00704 . PMID 24061345. S2CID 6241714.
- ^ Bratton DJ, Gaisl T, Wons AM, Kohler M (diciembre de 2015). "Dispositivos de avance mandibular frente a CPAP y presión arterial en pacientes con apnea obstructiva del sueño: una revisión sistemática y un metanálisis". JAMA . 314 (21): 2280–2293. doi : 10.1001/jama.2015.16303 . PMID 26624827.
- ^ Iftikhar IH, Kline CE, Youngstedt SD (febrero de 2014). "Efectos del entrenamiento físico en la apnea del sueño: un metaanálisis". Pulmón . 192 (1): 175–184. doi :10.1007/s00408-013-9511-3. PMC 4216726 . PMID 24077936.
- ^ Browaldh N, Nerfeldt P, Lysdahl M, Bring J, Friberg D (septiembre de 2013). "Ensayo controlado aleatorizado SKUP3: resultados polisomnográficos después de la uvulopalatofaringoplastia en pacientes seleccionados con apnea obstructiva del sueño". Thorax . 68 (9): 846–853. doi : 10.1136/thoraxjnl-2012-202610 . PMID 23644225. S2CID 27682387.
- ^ ab Stuck, Boris A.; Ravesloot, Madeline JL; Eschenhagen, Till; de Vet, HCW; Sommer, J. Ulrich (1 de octubre de 2018). "Uvulopalatofaringoplastia con o sin amigdalectomía en el tratamiento de la apnea obstructiva del sueño en adultos: una revisión sistemática". Medicina del sueño . 50 : 152–165. doi :10.1016/j.sleep.2018.05.004. PMID 30056286. S2CID 51878426.
- ^ ab Giles TL, Lasserson TJ, Smith BH, White J, Wright J, Cates CJ (julio de 2006). Giles T (ed.). "Presión positiva continua en las vías respiratorias para la apnea obstructiva del sueño en adultos". Base de datos Cochrane de revisiones sistemáticas (3): CD001106. doi :10.1002/14651858.CD001106.pub3. PMID 16855960.
- ^ abcd Askland, Kathleen; Wright, Lauren; Wozniak, Dariusz R; Emmanuel, Talia; Caston, Jessica; Smith, Ian (7 de abril de 2020). "Intervenciones educativas, de apoyo y conductuales para mejorar el uso de máquinas de presión positiva continua en las vías respiratorias en adultos con apnea obstructiva del sueño". Base de Datos Cochrane de Revisiones Sistemáticas . 2020 (4): CD007736. doi :10.1002/14651858.CD007736.pub3. PMC 7137251. PMID 32255210.
- ^ Riaz M, Certal V, Nigam G, Abdullatif J, Zaghi S, Kushida CA, Camacho M (2015). "Dispositivos de presión positiva en las vías respiratorias nasales espiratorias (Provent) para la apnea obstructiva del sueño: una revisión sistemática y un metanálisis". Trastornos del sueño . 2015 : 734798. doi : 10.1155/2015/734798 . PMC 4699057 . PMID 26798519.
- ^ Whitelaw, William A.; Brant, Rollin F.; Flemons, W. Ward (15 de enero de 2005). "Utilidad clínica de la oximetría domiciliaria en comparación con la polisomnografía para la evaluación de la apnea del sueño". American Journal of Respiratory and Critical Care Medicine . 171 (2): 188–193. doi :10.1164/rccm.200310-1360OC. PMID 15486338.Reseña en: Caples SM (2005). "La precisión de los médicos para predecir la respuesta exitosa al tratamiento en casos de apnea obstructiva del sueño sospechada no difirió entre la monitorización domiciliaria y la polisomnografía". ACP Journal Club . 143 (1): 21. doi :10.7326/ACPJC-2005-143-1-021. PMID 15989309. S2CID 219673066.
- ^ Littner M, Hirshkowitz M, Davila D, Anderson WM, Kushida CA, Woodson BT, et al. (marzo de 2002). "Parámetros prácticos para el uso de dispositivos de presión positiva continua en las vías respiratorias con titulación automática para la titulación de presiones y el tratamiento de pacientes adultos con síndrome de apnea obstructiva del sueño. Un informe de la Academia Estadounidense de Medicina del Sueño". Sleep . 25 (2): 143–147. doi :10.1093/sleep/25.2.143. PMID 11902424.
- ^ McNicholas WT, Bonsignore MR, Lévy P, Ryan S (octubre de 2016). "Apnea obstructiva del sueño leve: relevancia clínica y enfoques para su tratamiento". The Lancet. Medicina respiratoria . 4 (10): 826–834. doi :10.1016/S2213-2600(16)30146-1. PMID 27245915.
- ^ Neill AM, Angus SM, Sajkov D, McEvoy RD (enero de 1997). "Efectos de la postura durante el sueño en la estabilidad de las vías respiratorias superiores en pacientes con apnea obstructiva del sueño". American Journal of Respiratory and Critical Care Medicine . 155 (1): 199–204. doi :10.1164/ajrccm.155.1.9001312. PMID 9001312.
- ^ Nakano H, Ikeda T, Hayashi M, Ohshima E, Onizuka A (marzo de 2003). "Efectos de la posición corporal sobre los ronquidos en roncadores apneicos y no apneicos". Sleep . 26 (2): 169–172. doi : 10.1093/sleep/26.2.169 . PMID 12683476.
- ^ Loord H, Hultcrantz E (agosto de 2007). "Posicionador: un método para prevenir la apnea del sueño". Acta Oto-Laryngologica . 127 (8): 861–868. doi :10.1080/00016480601089390. PMID 17762999. S2CID 323418.
- ^ Szollosi I, Roebuck T, Thompson B, Naughton MT (agosto de 2006). "La posición lateral para dormir reduce la gravedad de la apnea central del sueño/respiración de Cheyne-Stokes". Sleep . 29 (8): 1045–1051. doi : 10.1093/sleep/29.8.1045 . PMID 16944673.
- ^ Caba, Justin (16 de abril de 2015). "Cómo el saxofón podría solucionar su apnea del sueño". Medical Daily .
- ^ Ward, Christopher P.; York, Kaki M.; McCoy, John G. (15 de junio de 2012). "Riesgo de apnea obstructiva del sueño menor en músicos de instrumentos de viento de lengüeta doble". Journal of Clinical Sleep Medicine . 08 (3): 251–255. doi :10.5664/jcsm.1906. PMC 3365082 . PMID 22701381.
- ^ Li, Qiming; Tang, Hongyi; Liu, Xueye; Luo, Qing; Jiang, Zhe; Martin, Domingo; Guo, Jing (1 de mayo de 2020). "Comparación de las dimensiones y el volumen de las vías respiratorias superiores antes y después de la expansión maxilar rápida asistida por miniimplantes". The Angle Orthodontist . 90 (3): 432–441. doi :10.2319/080919-522.1. PMC 8032299 . PMID 32045299.
- ^ Abdullatif, Jose; Certal, Victor; Zaghi, Soroush; Song, Sungjin A.; Chang, Edward T.; Gillespie, M. Boyd; Camacho, Macario (1 de mayo de 2016). "Expansión maxilar y expansión maxilomandibular para la apnea obstructiva del sueño en adultos: una revisión sistemática y un metanálisis". Revista de cirugía craneomaxilofacial . 44 (5): 574–578. doi :10.1016/j.jcms.2016.02.001. PMID 26948172.
- ^ Browaldh, Nanna; Nerfeldt, Pia; Lysdahl, Michael; Bring, Johan; Friberg, Danielle (1 de septiembre de 2013). "Ensayo controlado aleatorizado SKUP3: resultados polisomnográficos después de la uvulopalatofaringoplastia en pacientes seleccionados con apnea obstructiva del sueño". Tórax . 68 (9): 846–853. doi : 10.1136/thoraxjnl-2012-202610 . PMID 23644225. S2CID 27682387.
- ^ ab Tschopp, Samuel; Tschopp, Kurt (2019). "Tamaño de las amígdalas y resultado de la uvulopalatofaringoplastia con amigdalectomía en la apnea obstructiva del sueño". El laringoscopio . 129 (12): E449–E454. doi :10.1002/lary.27899. ISSN 1531-4995. PMID 30848478. S2CID 73503702.
- ^ "Apnea del sueño". Centro Médico de la Universidad de Maryland. Archivado desde el original el 30 de abril de 2008.
- ^ Borgström, Anna; Nerfeldt, Pia; Friberg, Danielle (1 de abril de 2017). "Adenoamigdalotomía versus adenoamigdalectomía en la apnea obstructiva del sueño pediátrica: un ensayo clínico aleatorizado". Pediatría . 139 (4): e20163314. doi : 10.1542/peds.2016-3314 . PMID 28320866. S2CID 23443654.
- ^ "Aprobación previa a la comercialización (PMA)". Archivado desde el original el 6 de mayo de 2014. Consultado el 5 de mayo de 2014 .. "Aprobación previa a la comercialización (PMA) del sistema de estimulación de las vías respiratorias superiores Inspire II" de la FDA, Administración de Alimentos y Medicamentos de los Estados Unidos, 30 de abril de 2014.
- ^ Strollo, Patrick J.; Soose, Ryan J.; Maurer, Joachim T.; de Vries, Nico; Cornelius, Jason; Froymovich, Oleg; Hanson, Ronald D.; Padhya, Tapan A.; Steward, David L.; Gillespie, M. Boyd; Woodson, B. Tucker; Van de Heyning, Paul H.; Goetting, Mark G.; Vanderveken, Olivier M.; Feldman, Neil; Knaack, Lennart; Strohl, Kingman P. (9 de enero de 2014). "Estimulación de las vías respiratorias superiores para la apnea obstructiva del sueño". New England Journal of Medicine . 370 (2): 139–149. doi : 10.1056/NEJMoa1308659 . PMID 24401051. S2CID 13764858.
- ^ ab Farrar J, Ryan J, Oliver E, Gillespie MB (octubre de 2008). "Ablación por radiofrecuencia para el tratamiento de la apnea obstructiva del sueño: un metaanálisis". The Laryngoscope . 118 (10): 1878–1883. doi :10.1097/MLG.0b013e31817d9cc1. PMID 18806478. S2CID 9844227.
- ^ Eick OJ (julio de 2002). "Ablación por radiofrecuencia controlada por temperatura". Indian Pacing and Electrophysiology Journal . 3. 2 (3): 66–73. PMC 1564057 . PMID 17006561.
- ^ Bashetty K, Nadig G, Kapoor S (octubre de 2009). "Electrocirugía en odontología estética y restauradora: una revisión de la literatura e informes de casos". Revista de odontología conservadora . 12 (4): 139–144. doi : 10.4103/0972-0707.58332 . PMC 2879725 . PMID 20543922.
- ^ "Declaración de posición: Ablación submucosa de la base de la lengua para el SAOS". Academia Estadounidense de Otorrinolaringología-Cirugía de Cabeza y Cuello . 20 de marzo de 2014.
- ^ Weaver, TE; Grunstein, RR (15 de febrero de 2008). "Adherencia a la terapia de presión positiva continua en las vías respiratorias: el desafío para un tratamiento eficaz". Actas de la American Thoracic Society . 5 (2): 173–178. doi :10.1513/pats.200708-119MG. PMC 2645251 . PMID 18250209.
- ^ Steward, David L.; Weaver, Edward M.; Woodson, B. Tucker (17 de mayo de 2016). "Radiofrecuencia controlada por temperatura multinivel para la apnea obstructiva del sueño: seguimiento extendido". Otorrinolaringología–Cirugía de cabeza y cuello . 132 (4): 630–635. doi :10.1016/j.otohns.2004.11.013. PMID 15806059. S2CID 17909484.
- ^ Gaisl, Thomas; Haile, Sarah R.; Thiel, Sira; Osswald, Martin; Kohler, Malcolm (agosto de 2019). "Eficacia de la farmacoterapia para la apnea obstructiva del sueño en adultos: una revisión sistemática y un metanálisis en red". Reseñas de medicina del sueño . 46 : 74–86. doi :10.1016/j.smrv.2019.04.009. PMID 31075665. S2CID 149455430.
- ^ Gottlieb, Daniel J.; Punjabi, Naresh M. (14 de abril de 2020). "Diagnóstico y tratamiento de la apnea obstructiva del sueño: una revisión". JAMA . 323 (14): 1389–1400. doi :10.1001/jama.2020.3514. PMID 32286648. S2CID 215759986.
- ^ Veasey, Sigrid C. (1 de febrero de 2003). "Agonistas y antagonistas de la serotonina en la apnea obstructiva del sueño". American Journal of Respiratory Medicine . 2 (1): 21–29. doi :10.1007/BF03256636. PMID 14720019. S2CID 8288291.
- ^ Babson, Kimberly A.; Sottile, James; Morabito, Danielle (27 de marzo de 2017). "Cannabis, cannabinoides y sueño: una revisión de la literatura". Current Psychiatry Reports . 19 (4): 23. doi :10.1007/s11920-017-0775-9. PMID 28349316. S2CID 7429763.
- ^ Carley, David W.; Prasad, Bharati; Reid, Kathryn J.; Malkani, Roneil; Attarian, Hryar; Abbott, Sabra M.; Vern, Boris; Xie, Hui; Yuan, Chengbo; Zee, Phyllis C. (1 de enero de 2018). "Farmacoterapia de la apnea mediante mejora cannabimimética, ensayo clínico PACE: efectos del dronabinol en la apnea obstructiva del sueño". Dormir . 41 (1). doi : 10.1093/sleep/zsx184. PMC 5806568 . PMID 29121334.
- ^ ab Ramar, Kannan; Rosen, Ilene M.; Kirsch, Douglas B.; Chervin, Ronald D.; Carden, Kelly A.; Aurora, R. Nisha; Kristo, David A.; Malhotra, Raman K.; Martin, Jennifer L.; Olson, Eric J.; Rosen, Carol L.; Rowley, James A. (15 de abril de 2018). "Cannabis medicinal y el tratamiento de la apnea obstructiva del sueño: una declaración de posición de la Academia Estadounidense de Medicina del Sueño". Revista de Medicina Clínica del Sueño . 14 (4): 679–681. doi :10.5664/jcsm.7070. PMC 5886446 . PMID 29609727.
- ^ Kolla, Bhanu Prakash; Mansukhani, Meghna P.; Olson, Eric J.; St. Louis, Erik K.; Silber, Michael H.; Morgenthaler, Timothy I. (junio de 2018). "Cannabis medicinal para la apnea obstructiva del sueño: prematuro y potencialmente dañino". Mayo Clinic Proceedings . 93 (6): 689–692. doi :10.1016/j.mayocp.2018.04.011. PMID 29866280. S2CID 46936292.
- ^ Ramar, Kannan; Kirsch, Douglas B.; Carden, Kelly A.; Rosen, Ilene M.; Malhotra, Raman K. (15 de octubre de 2018). "Cannabis medicinal, extractos sintéticos de marihuana y apnea obstructiva del sueño". Revista de medicina clínica del sueño . 14 (10): 1815–1816. doi :10.5664/jcsm.7412. PMC 6175803 . PMID 30353829.
- ^ Malhotra, Atul; Grunstein, Ronald R.; Fietze, Ingo; Weaver, Terri E.; Redline, Susan; Azarbarzin, Ali; Sands, Scott A.; Schwab, Richard J.; Dunn, Julia P.; Chakladar, Sujatro; Bunck, Mathijs C.; Bednarik, Josef (21 de junio de 2024). "Tirzepatida para el tratamiento de la apnea obstructiva del sueño y la obesidad". New England Journal of Medicine . doi :10.1056/NEJMoa2404881. ISSN 0028-4793.
- ^ "Medicación para la apnea obstructiva del sueño (AOS): estimulantes del sistema nervioso central, inhibidores de la recaptación de dopamina y noradrenalina". emedicine.medscape.com . Consultado el 15 de agosto de 2024 .
- ^ Greenblatt, Karl; Adams, Ninos (2024), "Modafinil", StatPearls , Treasure Island (FL): StatPearls Publishing, PMID 30285371 , consultado el 15 de agosto de 2024
- ^ "Sunosi: efectos secundarios, alternativas, usos, dosis y más". www.medicalnewstoday.com . 2020-09-23 . Consultado el 2024-08-15 .
- ^ Carvalho, Fernando R; Lentini-Oliveira, Débora A; Prado, Lucila BF; Prado, Gilmar F; Carvalho, Luciane BC (4 de octubre de 2016). "Aparatos bucales y aparatos ortopédicos funcionales para la apnea obstructiva del sueño en niños". Base de datos Cochrane de revisiones sistemáticas . 10 (11): CD005520. doi : 10.1002/14651858.CD005520.pub3. PMC 6458031 . PMID 27701747.
- ^ Shah NA, Botros NA, Yaggi HK, Mohsenin V (20 de mayo de 2007). "La apnea del sueño aumenta el riesgo de ataque cardíaco o muerte en un 30%" (Comunicado de prensa). New Haven, Connecticut: American Thoracic Society. Archivado desde el original el 24 de mayo de 2009.
- ^ Sun, Yi; Yuan, Hai; Zhao, Miao-Qing; Wang, Yan; Xia, Ming; Li, Yan-Zhong (abril de 2014). "Cambios estructurales y funcionales cardíacos en pacientes ancianos con síndrome de apnea-hipopnea obstructiva del sueño". Revista de investigación médica internacional . 42 (2): 395–404. doi : 10.1177/0300060513502890 . PMID 24445697. S2CID 23011075.
- ^ Silverberg DS, Iaina A, Oksenberg A (enero de 2002). "El tratamiento de la apnea obstructiva del sueño mejora la hipertensión esencial y la calidad de vida". American Family Physician . 65 (2): 229–236. PMID 11820487.
- ^ Grigg-Damberger, Madeleine (febrero de 2006). "Por qué la polisomnografía debería formar parte de la evaluación diagnóstica del accidente cerebrovascular y del ataque isquémico transitorio". Journal of Clinical Neurophysiology . 23 (1): 21–38. doi :10.1097/01.wnp.0000201077.44102.80. PMID 16514349. S2CID 19626174.
- ^ Gaisl T, Bratton DJ, Kohler M (agosto de 2015). "El impacto de la apnea obstructiva del sueño en la aorta". The European Respiratory Journal . 46 (2): 532–544. doi : 10.1183/09031936.00029315 . PMID 26113685. S2CID 14458813.
- ^ Peppard, Paul E.; Young, Terry; Palta, Mari; Skatrud, James (11 de mayo de 2000). "Estudio prospectivo de la asociación entre los trastornos respiratorios del sueño y la hipertensión". New England Journal of Medicine . 342 (19): 1378–1384. doi : 10.1056/NEJM200005113421901 . PMID 10805822.
- ^ Lavie, P.; Herer, P; Hoffstein, V (19 de febrero de 2000). "El síndrome de apnea obstructiva del sueño como factor de riesgo de hipertensión: estudio de población". BMJ . 320 (7233): 479–482. doi :10.1136/bmj.320.7233.479. PMC 27290 . PMID 10678860.
- ^ Yaggi, H. Klar; Concato, Juan; Kernan, Walter N.; Lichtman, Judith H.; Latón, Lawrence M.; Mohsenin, Vahid (10 de noviembre de 2005). "La apnea obstructiva del sueño como factor de riesgo de accidente cerebrovascular y muerte". Revista de Medicina de Nueva Inglaterra . 353 (19): 2034-2041. doi : 10.1056/NEJMoa043104 . PMID 16282178. S2CID 23360654.
- ^ Schröder, Carmen M; O'Hara, Ruth (2005). "Depresión y apnea obstructiva del sueño (AOS)". Anales de psiquiatría general . 4 (1): 13. doi : 10.1186/1744-859X-4-13 . PMC 1181621 . PMID 15982424.
- ^ Gagnon K, Baril AA, Gagnon JF, Fortin M, Décary A, Lafond C, et al. (octubre de 2014). "Deterioro cognitivo en la apnea obstructiva del sueño". Patología-Biología . 62 (5): 233–240. doi :10.1016/j.patbio.2014.05.015. PMID 25070768.
- ^ Lal C, Strange C, Bachman D (junio de 2012). "Deterioro neurocognitivo en la apnea obstructiva del sueño". Chest . 141 (6): 1601–1610. doi :10.1378/chest.11-2214. PMID 22670023.
- ^ ab Punjabi NM (febrero de 2008). "La epidemiología de la apnea obstructiva del sueño en adultos". Actas de la American Thoracic Society . 5 (2): 136–43. doi :10.1513/pats.200709-155MG. PMC 2645248 . PMID 18250205.
- ^ abcd Senaratna CV, Perret JL, Lodge CJ, Lowe AJ, Campbell BE, Matheson MC, et al. (agosto de 2017). "Prevalencia de la apnea obstructiva del sueño en la población general: una revisión sistemática". Sleep Medicine Reviews . 34 : 70–81. doi :10.1016/j.smrv.2016.07.002. PMID 27568340.
- ^ Shamsuzzaman AS, Gersh BJ, Somers VK (octubre de 2003). "Apnea obstructiva del sueño: implicaciones para la enfermedad cardíaca y vascular". JAMA . 290 (14): 1906–14. doi : 10.1001/jama.290.14.1906 . PMID 14532320.
- ^ Kezirian EJ, Boudewyns A, Eisele DW, Schwartz AR, Smith PL, Van de Heyning PH, De Backer WA (octubre de 2010). "Estimulación eléctrica del nervio hipogloso en el tratamiento de la apnea obstructiva del sueño". Sleep Medicine Reviews . 14 (5): 299–305. doi :10.1016/j.smrv.2009.10.009. PMID 20116305.
- ^ "El sistema ImThera aura6000 para la apnea del sueño se prueba en Europa". Medgadget . 15 de marzo de 2012.
- ^ Puhan, Milo A.; Suarez, Alex; Cascio, Christian Lo; Zahn, Alfred; Heitz, Markus; Braendli, Otto (2 de febrero de 2006). "Tocar didgeridoo como tratamiento alternativo para el síndrome de apnea obstructiva del sueño: ensayo controlado aleatorizado". BMJ . 332 (7536): 266–270. doi :10.1136/bmj.38705.470590.55. PMC 1360393 . PMID 16377643.
- ^ Guimarães, Kátia C.; Dräger, Luciano F.; Genta, Pedro R.; Marcondes, Bianca F.; Lorenzi-Filho, Geraldo (15 de mayo de 2009). "Efectos de los ejercicios orofaríngeos en pacientes con síndrome de apnea obstructiva del sueño moderada". Revista Estadounidense de Medicina Respiratoria y de Cuidados Críticos . 179 (10): 962–966. doi :10.1164/rccm.200806-981OC. PMID 19234106.

