Manosa
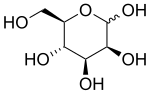 D -Manopiranosa | |
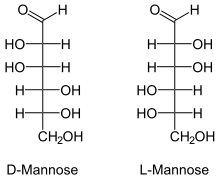 Proyecciones de Fischer | |
 | |
| Nombres | |
|---|---|
| Nombre IUPAC Manosa | |
| Nombre sistemático de la IUPAC ( 3S ,4S , 5S , 6R ) -6-(hidroximetil)oxano-2,3,4,5-tetrol | |
| Identificadores | |
| Química biológica | |
| Araña química | |
| |
| BARRIL |
|
| Malla | Manosa |
Identificador de centro de PubChem |
|
| UNIVERSIDAD | |
| Propiedades | |
| C6H12O6 | |
| Masa molar | 180,156 g·mol −1 |
| -102,90·10 −6 cm3 / mol | |
Salvo que se indique lo contrario, los datos se proporcionan para los materiales en su estado estándar (a 25 °C [77 °F], 100 kPa). | |
La manosa es un monómero de azúcar de la serie de carbohidratos de las aldohexosas . Es un epímero C-2 de la glucosa . La manosa es importante en el metabolismo humano , especialmente en la glicosilación de ciertas proteínas . Varios trastornos congénitos de la glicosilación están asociados con mutaciones en las enzimas involucradas en el metabolismo de la manosa. [1]
La manosa no es un nutriente esencial ; puede producirse en el cuerpo humano a partir de la glucosa o convertirse en glucosa. La manosa aporta de 2 a 5 kcal /g. Se excreta parcialmente en la orina .
Etimología
La raíz de la "manosa" y del " manitol " es el maná , que la Biblia describe como el alimento suministrado a los israelitas durante su viaje por la región del Sinaí . Varios árboles y arbustos pueden producir una sustancia llamada maná, como el "árbol del maná" ( Fraxinus ornus ) de cuyas secreciones se aisló originalmente el manitol. [ cita requerida ]
Estructura
La manosa se presenta comúnmente en dos anillos de diferentes tamaños: la forma piranosa (de seis miembros) y la forma furanosa (de cinco miembros). Cada cierre de anillo puede tener una configuración alfa o beta en la posición anomérica . La sustancia química experimenta rápidamente una isomerización entre estas cuatro formas. [ cita requerida ]
 α- D -Manofuranosa 0,6% | 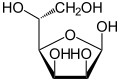 β- D -Manofuranosa 0,2% |
 α- D -Manopiranosa 63,7% | 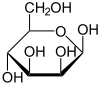 β- D -Manopiranosa 35,5% |
Metabolismo

Aunque se cree que gran parte de la manosa utilizada en la glicosilación se deriva de la glucosa, en las células de hepatoma cultivadas (células cancerosas del hígado), la mayor parte de la manosa para la biosíntesis de glicoproteínas proviene de manosa extracelular, no de glucosa. [3] Muchas de las glicoproteínas producidas en el hígado se secretan en el torrente sanguíneo, por lo que la manosa de la dieta se distribuye por todo el cuerpo. [4]
La manosa está presente en numerosos glicoconjugados , incluida la glicosilación de proteínas ligada a N. La C -manosilación también es abundante y se puede encontrar en regiones similares al colágeno. [ cita requerida ]
La digestión de muchos polisacáridos y glicoproteínas produce manosa, que es fosforilada por la hexoquinasa para generar manosa-6-fosfato . La manosa-6-fosfato se convierte en fructosa-6-fosfato , por la enzima fosfomanosa isomerasa , y luego ingresa en la vía glucolítica o se convierte en glucosa-6-fosfato por la vía gluconeogénica de los hepatocitos . [ cita requerida ]
La manosa es un monosacárido dominante en la glucosilación ligada a N , que es una modificación postraduccional de las proteínas. Se inicia mediante la transferencia en bloque de Glc 3 Man 9 GlcNAc 2 a las glucoproteínas nacientes en el retículo endoplasmático (RE) de manera cotraduccional a medida que la proteína ingresa a través del sistema de transporte. La glucosa se hidroliza en la proteína completamente plegada y las fracciones de manosa son hidrolizadas por las manosidasas residentes en el RE y el Golgi . Por lo general, las glucoproteínas humanas maduras solo contienen tres residuos de manosa enterrados bajo la modificación secuencial de GlcNAc, galactosa y ácido siálico . Esto es importante, ya que el sistema inmunológico innato en los mamíferos está preparado para reconocer los residuos de manosa expuestos. Esta actividad se debe a la prevalencia de residuos de manosa, en forma de mananos, en las superficies de las levaduras. El virus de la inmunodeficiencia humana muestra una cantidad considerable de residuos de manosa debido a la agrupación apretada de glicanos en su espícula viral . [5] [6] Estos residuos de manosa son el objetivo de anticuerpos ampliamente neutralizantes . [7]
Biotecnología
Las proteínas recombinantes producidas en levaduras pueden estar sujetas a la adición de manosa en patrones diferentes de los utilizados por las células de mamíferos. [8] Esta diferencia entre las proteínas recombinantes y las que se producen normalmente en organismos mamíferos puede influir en la eficacia de las vacunas. [ cita requerida ]
Formación
La manosa se puede formar por oxidación del manitol . [ cita requerida ]
También se puede formar a partir de glucosa en la transformación de Lobry de Bruyn–van Ekenstein . [ cita requerida ]
Usos
La manosa ( D -manosa) se utiliza como suplemento dietético para prevenir infecciones recurrentes del tracto urinario (ITU). [9] [10] En 2022 [actualizar], una revisión encontró que tomar manosa era tan eficaz como los antibióticos para prevenir las ITU, [9] mientras que otra revisión encontró que la calidad de los ensayos clínicos era demasiado baja para permitir cualquier conclusión sobre el uso de D -manosa para prevenir o tratar las ITU. [10] En 2024, un ensayo clínico aleatorizado entre 598 mujeres con ITU recurrentes reclutadas en entornos de atención primaria encontró que la proporción de las que experimentaron una ITU asistida por un médico fue del 51,0% en las que tomaron D -manosa diariamente durante 6 meses y del 55,7% en las que tomaron placebo, concluyendo que la D -manosa no debería recomendarse para prevenir futuros episodios de ITU asistida por un médico en mujeres con ITU recurrentes en atención primaria. [11]
Configuración
La manosa se diferencia de la glucosa por la inversión del centro quiral C-2 . La manosa muestra una arruga en la forma de anillo de solución. Este simple cambio conduce a la bioquímica drásticamente diferente de las dos hexosas . Este cambio también tiene el mismo efecto en las otras aldohexosas . [ cita requerida ]
Permeasa de manosa PTS

El sistema de fosfotransferasa transportadora de azúcar dependiente de PEP transporta y fosforila simultáneamente sus sustratos de azúcar. La permeasa manosa XYZ es un miembro de la familia, y las bacterias utilizan este método distintivo para la captación de azúcar, en particular hexosas exógenas en el caso de la manosa XYZ, para liberar los ésteres de fosfato en el citoplasma celular en preparación para el metabolismo, principalmente a través de la ruta de la glucólisis. [12] El complejo transportador MANXYZ también está involucrado en la infección de E. coli por el bacteriófago lambda , y las subunidades ManY y ManZ son suficientes para una infección adecuada del fago lambda. [13] MANXYZ posee cuatro dominios en tres cadenas polipeptídicas; ManX, ManY y ManZ. La subunidad ManX forma un homodímero que se localiza en el lado citoplasmático de la membrana. ManX contiene dos dominios IIA y IIB unidos por un péptido bisagra, y cada dominio contiene un sitio de fosforilación y la transferencia de fosforilo ocurre entre ambas subunidades. [14] ManX puede estar unido a la membrana o no. [13] Las subunidades ManY y ManNZ son proteínas de membrana integrales hidrofóbicas con seis y una hélice alfa transmembrana. [15] [16] [17] El grupo fosforilo de PEP se transfiere al azúcar importado a través de la enzima 1, transportador de fosfato de proteína histidina, y luego a las subunidades ManX, ManY y ManZ del complejo de transporte ManXYZ, que fosforila el azúcar hexosa entrante, creando una hexosa-6-fosfato. [ cita requerida ]
Véase también
- α-Manosidasa
- Receptor de manosa
- Suplementos nutricionales a base de oligosacáridos de manano
- Ramnosa , 6-desoxi- L -manosa
- Familia PTS de manosa-fructosa-sorbosa
Referencias
- ^ Freeze, HH; Sharma, V. (2010). "Manipulación metabólica de los trastornos de la glicosilación en humanos y modelos animales". Seminarios en biología celular y del desarrollo . 21 (6): 655–662. doi :10.1016/j.semcdb.2010.03.011. PMC 2917643 . PMID 20363348.
- ^ Witczak, Zbigniew J. (2001). "Monosacáridos. Propiedades". En Fraser-Reid, Bertram O.; Tatsuta, Kuniaki; Thiem, Joachim (eds.). Glicociencia. Química y biología química I–III . Springer. pág. 887. doi :10.1007/978-3-642-56874-9. ISBN 978-3-642-56874-9.
- ^ Alton, G.; Hasilik, M.; Niehues, R.; Panneerselvam, K.; Etchison, JR; Fana, F.; Freeze, HH (1998). "Utilización directa de manosa para la biosíntesis de glucoproteínas en mamíferos". Glycobiology . 8 (3): 285–295. doi : 10.1093/glycob/8.3.285 . PMID 9451038.
- ^ Davis, JA; Freeze, HH (2001). "Estudios del metabolismo de la manosa y efectos de la ingestión de manosa a largo plazo en el ratón". Biochimica et Biophysica Acta (BBA) - Temas generales . 1528 (2–3): 116–126. doi :10.1016/S0304-4165(01)00183-0. PMID 11687298.
- ^ Pritchard, Laura K.; Spencer, Daniel IR; Royle, Louise; Bonomelli, Camille; Seabright, Gemma E.; Behrens, Anna-Janina; Kulp, Daniel W.; Menis, Sergey; Krumm, Stefanie A. (24 de junio de 2015). "La agrupación de glicanos estabiliza el parche de manosa del VIH-1 y preserva la vulnerabilidad a los anticuerpos ampliamente neutralizantes". Nature Communications . 6 : 7479. Bibcode :2015NatCo...6.7479P. doi :10.1038/ncomms8479. PMC 4500839 . PMID 26105115.
- ^ Pritchard, Laura K.; Vasiljevic, Snezana; Ozorowski, Gabriel; Seabright, Gemma E.; Cupo, Albert; Ringe, Rajesh; Kim, Helen J.; Sanders, Rogier W.; Doores, Katie J. (16 de junio de 2015). "Las restricciones estructurales determinan la glicosilación de los trímeros de la envoltura del VIH-1". Cell Reports . 11 (10): 1604–1613. doi :10.1016/j.celrep.2015.05.017. ISSN 2211-1247. PMC 4555872 . PMID 26051934.
- ^ Crispin, Max; Doores, Katie J (1 de abril de 2015). "Dirigir los glicanos derivados del huésped a los virus con envoltura para el diseño de vacunas basadas en anticuerpos". Current Opinion in Virology . Patogénesis viral • Vacunas preventivas y terapéuticas. 11 : 63–69. doi :10.1016/j.coviro.2015.02.002. PMC 4827424 . PMID 25747313.
- ^ Vlahopoulos, S.; Gritzapis, AD; Perez, SA; Cacoullos, N.; Papamichail, M.; Baxevanis, CN (2009). "La adición de manosa por la levadura Pichia pastoris a la proteína HER-2 recombinante inhibe el reconocimiento por el anticuerpo monoclonal herceptina". Vaccine . 27 (34): 4704–4708. doi :10.1016/j.vaccine.2009.05.063. PMID 19520203.
- ^ ab Lenger, Stacy M.; Bradley, Megan S.; Thomas, Debbie A.; Bertolet, Marnie H.; Lowder, Jerry L.; Sutcliffe, Siobhan (1 de agosto de 2020). "D-manosa frente a otros agentes para la prevención recurrente de infecciones del tracto urinario en mujeres adultas: una revisión sistemática y un metanálisis". Revista estadounidense de obstetricia y ginecología . 223 (2): 265.e1–265.e13. doi :10.1016/j.ajog.2020.05.048. PMC 7395894 . PMID 32497610.
- ^ ab Cooper, Tess E; Teng, Claris; Howell, Martin; Teixeira-Pinto, Armando; Jaure, Allison; Wong, Germaine (30 de agosto de 2022). "D-manosa para la prevención y el tratamiento de las infecciones del tracto urinario". Base de Datos Cochrane de Revisiones Sistemáticas . 2022 (8): CD013608. doi :10.1002/14651858.CD013608.pub2. PMC 9427198. PMID 36041061 .
- ^ Gail Hayward; Sam Mort; Alastair D. Hay; et al. (8 de abril de 2024). "d-Manosa para la prevención de infecciones recurrentes del tracto urinario en mujeres | Un ensayo clínico aleatorizado". JAMA Intern Med . 184 (6): 619–628. doi :10.1001/jamainternmed.2024.0264. PMC 11002776 .
{{cite journal}}: Mantenimiento CS1: fecha y año ( enlace ) - ^ Postma, PW; Lengeler, JW; Jacobson, GR (1993). "Sistemas de fosfoenolpiruvato:carbohidrato fosfotransferasa de bacterias". Microbiological Reviews . 57 (3): 543–594. doi :10.1128/MMBR.57.3.543-594.1993. PMC 372926 . PMID 8246840.
- ^ ab Erni, B.; Zanolari, B. (1985). "La manosa-permeasa del sistema de fosfotransferasa bacteriana. Clonación génica y purificación del complejo enzimático IIMan/IIIMan de Escherichia coli". The Journal of Biological Chemistry . 260 (29): 15495–15503. doi : 10.1016/S0021-9258(17)36282-8 . PMID 2999119.
- ^ Erni, B.; Zanolari, B.; Graff, P.; Kocher, HP (1989). "Permeasa de manosa de Escherichia coli. Estructura del dominio y función de la subunidad fosforilante". The Journal of Biological Chemistry . 264 (31): 18733–18741. doi : 10.1016/S0021-9258(18)51529-5 . PMID 2681202.
- ^ Huber, F.; Erni, B. (1996). "Topología de membrana del transportador de manosa de Escherichia coli K12". Revista Europea de Bioquímica . 239 (3): 810–817. doi :10.1111/j.1432-1033.1996.0810u.x. PMID 8774730.
- ^ Liu, Xueli; Zeng, Jianwei; Huang, Kai; Wang, Jiawei (17 de junio de 2019). "Estructura del transportador de manosa del sistema de fosfotransferasa bacteriana". Cell Research . 29 (8): 680–682. doi :10.1038/s41422-019-0194-z. ISSN 1748-7838. PMC 6796895 . PMID 31209249.
- ^ Huang, Kai; Zeng, Jianwei; Liu, Xueli; Jiang, Tianyu; Wang, Jiawei (6 de abril de 2021). "Estructura del sistema de manosa fosfotransferasa (man-PTS) complejado con microcina E492, una bacteriocina formadora de poros". Cell Discovery . 7 (1): 20. doi :10.1038/s41421-021-00253-6. ISSN 2056-5968. PMC 8021565 . PMID 33820910.



