Licopeno
 | |
 | |
 | |
| Nombres | |
|---|---|
| Nombre IUPAC ψ,ψ-caroteno | |
| Nombre sistemático de la IUPAC (6 mi ,8 mi ,10 mi ,12 mi ,14 mi , 16 mi ,18 mi ,20 mi ,22 mi ,24 mi ,26 mi )-2,6,10,14,19,23,27,31 -Octametildotriaconta-2,6,8,10,12,14,16,18,20,22,24,26,30-tridecaeno | |
| Identificadores | |
Modelo 3D ( JSmol ) |
|
| EBICh | |
| Química biológica | |
| Araña química | |
| Tarjeta informativa de la ECHA | 100.007.227 |
| Número CE |
|
| Número E | E160d (colores) |
Identificador de centro de PubChem |
|
| UNIVERSIDAD | |
Panel de control CompTox ( EPA ) |
|
| |
| |
| Propiedades | |
| C 40 H 56 | |
| Masa molar | 536,888 g·mol −1 |
| Apariencia | sólido rojo intenso |
| Densidad | 0,889 g/ cm3 |
| Punto de fusión | 177 °C (351 °F; 450 K) [2] |
| Punto de ebullición | 660,9 °C (1221,6 °F; 934,0 K) a 760 mmHg [1] |
| insoluble | |
| Solubilidad | soluble en CS 2 , CHCl 3 , THF , éter , C 6 H 14 , aceite vegetal insoluble en CH 3 OH , C 2 H 5 OH [1] |
| Solubilidad en hexano | 1 g/L (14 °C) [1] |
| Presión de vapor | 1,33·10 −16 mmHg (25 °C) [1] |
| Peligros | |
| Seguridad y salud en el trabajo (SST/OHS): | |
Principales peligros | Combustible |
| NFPA 704 (rombo cortafuegos) | |
| punto de inflamabilidad | 350,7 °C (663,3 °F; 623,8 K) [1] |
| Página de datos complementarios | |
| Licopeno (página de datos) | |
Salvo que se indique lo contrario, los datos se proporcionan para los materiales en su estado estándar (a 25 °C [77 °F], 100 kPa). | |
El licopeno es un compuesto orgánico clasificado como tetraterpeno y caroteno . [3] El licopeno (del neolatín Lycopersicon , el nombre de un antiguo género de tomates) es un hidrocarburo carotenoide de color rojo brillante que se encuentra en los tomates y otras frutas y verduras rojas.
Aparición
Aparte de los tomates, se encuentra en las zanahorias rojas , las sandías , los pomelos y las papayas . No está presente en las fresas ni en las cerezas . [4] No tiene actividad de vitamina A. [5]
En plantas , algas y otros organismos fotosintéticos , el licopeno es un intermediario en la biosíntesis de muchos carotenoides, incluido el betacaroteno , que es responsable de la pigmentación amarilla, naranja o roja, la fotosíntesis y la fotoprotección . [5] Como todos los carotenoides, el licopeno es un tetraterpeno . [5] Es insoluble en agua. Once dobles enlaces conjugados le dan al licopeno su color rojo intenso. Debido a su fuerte color, el licopeno es útil como colorante alimentario (registrado como E160d ) y está aprobado para su uso en los EE. UU., [6] Australia y Nueva Zelanda (registrado como 160d ) [7] y la Unión Europea . [8]
Estructura y propiedades físicas
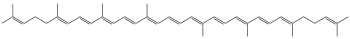
El licopeno es un tetraterpeno simétrico porque está compuesto enteramente de carbono e hidrógeno y se deriva de ocho subunidades de isopreno . [5] Los procedimientos de aislamiento del licopeno se informaron por primera vez en 1910, y la estructura de la molécula se determinó en 1931. En su forma natural, todo- trans , la molécula es larga y algo plana, limitada por su sistema de 11 enlaces dobles conjugados. La conjugación extendida es responsable de su color rojo intenso. [5]
Las plantas y las bacterias fotosintéticas producen licopeno todo- trans . [5] Cuando se expone a la luz o al calor, el licopeno puede sufrir isomerización a cualquiera de varios isómeros cis , que tienen una forma menos lineal. Estabilidades distintas de los isómeros, con la estabilidad más alta: 5-cis ≥ todo-trans ≥ 9-cis ≥ 13-cis > 15-cis > 7-cis > 11-cis: la más baja. [9] [10] En la sangre humana, varios isómeros cis constituyen más del 60% de la concentración total de licopeno, pero no se han investigado los efectos biológicos de los isómeros individuales. [11]

Los carotenoides como el licopeno se encuentran en complejos de pigmentos fotosintéticos y proteínas en plantas, bacterias fotosintéticas, hongos y algas. [5] Son responsables de los colores naranja-rojo brillantes de las frutas y verduras, realizan varias funciones en la fotosíntesis y protegen a los organismos fotosintéticos del daño excesivo de la luz. El licopeno es un intermediario clave en la biosíntesis de carotenoides, como el betacaroteno y las xantofilas . [12]
Las moléculas de licopeno dispersas se pueden encapsular en nanotubos de carbono, lo que mejora sus propiedades ópticas . [13] Se produce una transferencia de energía eficiente entre el tinte encapsulado y el nanotubo: la luz es absorbida por el tinte y se transfiere al nanotubo sin pérdida significativa. La encapsulación aumenta la estabilidad química y térmica de las moléculas de licopeno; también permite su aislamiento y caracterización individual. [14]
Biosíntesis
La biosíntesis incondicionada del licopeno en plantas eucariotas y en cianobacterias procariotas es similar, al igual que las enzimas involucradas. [5] La síntesis comienza con ácido mevalónico , que se convierte en pirofosfato de dimetilalilo . Luego, este se condensa con tres moléculas de pirofosfato de isopentenilo (un isómero del pirofosfato de dimetilalilo), para dar el pirofosfato de geranilgeranilo de 20 carbonos . Luego, dos moléculas de este producto se condensan en una configuración de cola a cola para dar el fitoeno de 40 carbonos , el primer paso comprometido en la biosíntesis de carotenoides. A través de varios pasos de desaturación, el fitoeno se convierte en licopeno. Los dos grupos isopreno terminales del licopeno se pueden ciclar para producir betacaroteno, que luego se puede transformar en una amplia variedad de xantofilas. [5]
Tinción y eliminación
El licopeno es el pigmento presente en las salsas de tomate que tiñe de color naranja los utensilios de cocina de plástico. Es insoluble en agua corriente, pero se puede disolver en disolventes orgánicos y aceites. Debido a su falta de polaridad, el licopeno presente en los preparados alimenticios manchará cualquier material suficientemente poroso , incluida la mayoría de los plásticos. Para eliminar esta mancha, los plásticos se pueden sumergir en una solución que contenga una pequeña cantidad de cloro. [15] El cloro oxida el licopeno, volviéndolo incoloro.
Dieta
Consumo por humanos
La absorción del licopeno requiere que se combine con sales biliares y grasas para formar micelas . [5] La absorción intestinal del licopeno se mejora con la presencia de grasa y con la cocción. [5] Los suplementos dietéticos de licopeno (en aceite) pueden absorberse de manera más eficiente que el licopeno de los alimentos. [5]
El licopeno no es un nutriente esencial para los humanos, pero se encuentra comúnmente en la dieta, principalmente en platos preparados a base de tomates. [4] [5] Se ha estimado que la mediana y el percentil 99 de la ingesta dietética de licopeno son 5,2 y 123 mg/d, respectivamente. [16]
Fuentes
| Fuente | mg de peso húmedo |
|---|---|
| arilo de gac | 2~6 por gramo [17] [18] |
| Tomate crudo | 4,6 por taza |
| Jugo de tomate | 22 por taza |
| Pasta de tomate | 75 por taza |
| Salsa de tomate | 2,5 por cucharada |
| Sandía | 13 por cuña |
| Pomelo rosado | 2 por media toronja |
Las frutas y verduras con alto contenido de licopeno incluyen la aceituna de otoño , el gac , los tomates, la sandía , el pomelo rosado , la guayaba rosada , la papaya , el espino amarillo , la baya de goji ( una baya pariente del tomate) y la rosa mosqueta . [5] El kétchup es una fuente dietética común de licopeno. [5] Aunque el gac ( Momordica cochinchinensis Spreng) tiene el mayor contenido de licopeno de cualquier fruta o verdura conocida (varias veces más que los tomates), [19] [20] los tomates y las salsas, jugos y kétchup a base de tomate representan más del 85% de la ingesta dietética de licopeno para la mayoría de las personas. [5] El contenido de licopeno de los tomates depende de la variedad y aumenta a medida que la fruta madura. [21]
A diferencia de otras frutas y verduras, cuyo contenido nutricional, como la vitamina C , disminuye al cocinarlas, el procesamiento de los tomates aumenta la concentración de licopeno biodisponible . [5] [22] El licopeno en la pasta de tomate es hasta cuatro veces más biodisponible que en los tomates frescos. [23] Los productos de tomate procesados, como el jugo de tomate pasteurizado, la sopa, la salsa y el kétchup, contienen una mayor concentración de licopeno biodisponible en comparación con los tomates crudos. [5] [24]
Cocinar y triturar tomates (como en el proceso de enlatado ) y servirlos en platos ricos en aceite (como salsa de espagueti o pizza ) aumenta en gran medida la asimilación del tracto digestivo al torrente sanguíneo. El licopeno es liposoluble, por lo que se dice que el aceite ayuda a la absorción. El gac tiene un alto contenido de licopeno derivado principalmente de sus cubiertas de semillas . [25] Cara cara navel y otros cítricos, como el pomelo rosado , también contienen licopeno. [4] [26] Algunos alimentos que no parecen rojos también contienen licopeno, por ejemplo, los espárragos , que contienen alrededor de 30 μg de licopeno por porción de 100 g [4] (0,3 μg/g) y el perejil y la albahaca secos , que contienen alrededor de 3,5–7,0 μg/g de licopeno. [4] Cuando se utiliza licopeno como aditivo alimentario (E160d), generalmente se obtiene de los tomates. [27]
Efectos adversos

El licopeno no es tóxico y se encuentra comúnmente en la dieta, principalmente en productos derivados del tomate. Existen casos de intolerancia o reacción alérgica al licopeno dietético, que puede causar diarrea , náuseas , dolor o calambres estomacales, gases y pérdida de apetito. [28] El licopeno puede aumentar el riesgo de sangrado cuando se toma con medicamentos anticoagulantes . [28] Debido a que el licopeno puede causar presión arterial baja, pueden ocurrir interacciones con medicamentos que afectan la presión arterial. El licopeno puede afectar el sistema inmunológico , el sistema nervioso , la sensibilidad a la luz solar o los medicamentos utilizados para dolencias estomacales. [28]
La licopenemia es una coloración anaranjada de la piel que se observa con una ingesta elevada de licopeno. [16] Se espera que la coloración desaparezca después de suspender la ingesta excesiva de licopeno. [16]
Investigación y posibles efectos sobre la salud
Una revisión de ensayos controlados aleatorios de 2020 encontró evidencia contradictoria de que el licopeno tiene un efecto sobre los factores de riesgo cardiovascular , [29] mientras que una revisión de 2017 concluyó que los productos de tomate y la suplementación con licopeno redujeron los lípidos en sangre y la presión arterial . [30]
Una revisión de 2015 encontró que el licopeno dietético estaba asociado con un riesgo reducido de cáncer de próstata , [31] mientras que un metanálisis de 2021 encontró que el licopeno dietético no afectaba el riesgo de cáncer de próstata. [32] Otras revisiones concluyeron que la investigación ha sido insuficiente para establecer si el consumo de licopeno afecta la salud humana. [33]
Situación regulatoria en Europa y Estados Unidos
En una revisión de la literatura sobre el licopeno y su beneficio potencial en la dieta, la Autoridad Europea de Seguridad Alimentaria concluyó que no había evidencia suficiente de que el licopeno tuviera efectos antioxidantes en humanos, particularmente en la piel, la función cardíaca o la protección de la visión frente a la luz ultravioleta . [34]
Aunque el licopeno de los tomates se ha probado en humanos para enfermedades cardiovasculares y cáncer de próstata, no se encontró ningún efecto sobre ninguna enfermedad. [35] La Administración de Alimentos y Medicamentos de los Estados Unidos , al rechazar las solicitudes de los fabricantes en 2005 para permitir el "etiquetado calificado" para el licopeno y la reducción de varios riesgos de cáncer, proporcionó una conclusión que sigue vigente a partir de 2015 [actualizar]:
Ningún estudio ha aportado información sobre si la ingesta de licopeno puede reducir el riesgo de padecer alguna de las formas específicas de cáncer. Con base en lo anterior, la FDA concluye que no existen pruebas creíbles que respalden una relación entre el consumo de licopeno, ya sea como ingrediente alimentario, componente de alimentos o suplemento dietético, y cualquiera de estos cánceres. [35]
En una revisión de investigaciones realizadas hasta 2024, el Instituto Nacional del Cáncer de EE. UU. concluyó que la FDA no ha aprobado el uso de licopeno como eficaz para tratar ninguna afección médica, incluidos varios tipos de cáncer. [36]
Véase también
Referencias
- ^ abcde "Licopeno". PubChem, Biblioteca Nacional de Medicina de EE. UU. 2016. Consultado el 13 de octubre de 2016 .
- ^ Haynes, William M., ed. (2011). Manual de química y física del CRC (92.ª edición). CRC Press . pág. 3.94. ISBN 978-1439855119.
- ^ Sell, Charles S. (2006). "Terpenoides". Enciclopedia Kirk-Othmer de tecnología química . doi :10.1002/0471238961.2005181602120504.a01.pub2. ISBN 0471238961.
- ^ abcde "Alimentos con mayor contenido de licopeno, Datos nutricionales, Base de datos de nutrientes del USDA, versión SR-21". nutritiondata.com . Conde Nast. 2014 . Consultado el 19 de agosto de 2014 .
- ^ abcdefghijklmnopqrs «Carotenoides: α-caroteno, β-caroteno, β-criptoxantina, licopeno, luteína y zeaxantina». Centro de Información sobre Micronutrientes, Instituto Linus Pauling, Universidad Estatal de Oregón, Corvallis, Oregón. Julio de 2016. Archivado desde el original el 21 de mayo de 2017. Consultado el 29 de mayo de 2017 .
- ^ "21 CFR 73.585. Extracto de licopeno de tomate" (PDF) . Administración de Alimentos y Medicamentos de Estados Unidos. 26 de julio de 2005.
- ^ Código de normas alimentarias de Australia y Nueva Zelanda «Norma 1.2.4 – Etiquetado de ingredientes». 8 de septiembre de 2011. Consultado el 27 de octubre de 2011 .
- ^ Agencia de Normas Alimentarias del Reino Unido: "Aditivos aprobados actualmente por la UE y sus números E" . Consultado el 27 de octubre de 2011 .
- ^ Chasse, Gregory A.; Mak, Melody L.; Deretey, Eugen; Farkas, Imre; Torday, Ladislaus L.; Papp, Julius G.; Sarma, Dittakavi SR; Agarwal, Anita; Chakravarthi, Sujatha; Agarwal, Sanjiv; Rao, A. Venket (2001). "Un estudio computacional ab initio sobre isómeros de licopeno seleccionados" (PDF) . Journal of Molecular Structure: Theochem . 571 (1–3): 27–37. doi :10.1016/S0166-1280(01)00424-9.
- ^ Chasse, Gregory A.; Chasse, Kenneth P.; Kucsman, Arpad; Torday, Ladislaus L.; Papp, Julius G. (2001). "Superficies de energía potencial conformacional de un modelo de licopeno" (PDF) . Journal of Molecular Structure: Theochem . 571 (1–3): 7–26. doi :10.1016/S0166-1280(01)00413-4.
- ^ Erdman Jr, JW (2005). "¿Cómo modifican el estado nutricional y hormonal la biodisponibilidad, la absorción y la distribución de varios isómeros del licopeno?". The Journal of Nutrition . 135 (8): 2046S–7S. doi : 10.1093/jn/135.8.2046s . PMID 16046737.
- ^ Agricultura de la NDSU. "¿De qué color es tu comida?" . Consultado el 10 de mayo de 2012 .
- ^ Yanagi, Kazuhiro; Iakoubovskii, Konstantin; Kazaoui, dijo; Minami, Nobutsugu; Maniwa, Yutaka; Miyata, Yasumitsu; Kataura, Hiromichi (2006). "Función de captación de luz del β-caroteno dentro de nanotubos de carbono" (PDF) . Física. Rev. B. 74 (15): 155420. Código bibliográfico : 2006PhRvB..74o5420Y. doi : 10.1103/PhysRevB.74.155420. Archivado desde el original (PDF) el 2 de octubre de 2020 . Consultado el 12 de febrero de 2019 .
- ^ Saito, Yuika; Yanagi, Kazuhiro; Hayazawa, Norihiko; Ishitobi, Hidekazu; Ono, Atsushi; Kataura, Hiromichi; Kawata, Satoshi (2006). "Análisis vibratorio de moléculas orgánicas encapsuladas en nanotubos de carbono mediante espectroscopia Raman mejorada con punta". Japón. J. Aplica. Física . 45 (12): 9286–9289. Código Bib : 2006JaJAP..45.9286S. doi :10.1143/JJAP.45.9286. S2CID 122152101.
- ^ Barnes, Chris (11 de octubre de 2011). "Cómo limpiar manchas de salsa de tomate de recipientes de plástico". The Huffington Post . Consultado el 29 de mayo de 2017 .
- ^ abc Trumbo PR (2005). "¿Existen efectos adversos de la exposición al licopeno?". The Journal of Nutrition . 135 (8): 2060S–1S. doi : 10.1093/jn/135.8.2060s . PMID 16046742.
Se ha observado licopenemia, caracterizada por una decoloración anaranjada de la piel, con una ingesta elevada de alimentos que contienen licopeno. Un estudio de caso informó la incidencia de licopenemia en una mujer de 61 años que había consumido ~2 L de jugo de tomate al día durante varios años (10). Aunque había evidencia de licopeno y depósitos grasos en el hígado, no hubo disfunción hepática medible. Después de 3 semanas de consumir una dieta sin jugo de tomate, la decoloración anaranjada se desvaneció.
- ^ Ishida, BK; Turner, C; Chapman, MH; McKeon, TA (28 de enero de 2004). "Composición de ácidos grasos y carotenoides de la fruta de Momordica cochinchinensis Spreng" (gac). Journal of Agricultural and Food Chemistry . 52 (2): 274–9. doi :10.1021/jf030616i. PMID 14733508.
- ^ "Informe de análisis de la Momordica cochinchinensis" (PDF) . Archivado desde el original (PDF) el 2018-04-13 . Consultado el 2018-04-13 .
- ^ Tran, XT; Parks, SE; Roach, PD; Golding, JB; Nguyen, MH (2015). "Efectos de la madurez en las propiedades fisicoquímicas de la fruta Gac (Momordica cochinchinensis Spreng.)". Ciencia y nutrición de los alimentos . 4 (2): 305–314. doi :10.1002/fsn3.291. PMC 4779482 . PMID 27004120.
- ^ Ishida BK, Turner C, Chapman MH, McKeon TA (enero de 2004). "Composición de ácidos grasos y carotenoides de la fruta de Momordica cochinchinensis Spreng". Journal of Agricultural and Food Chemistry . 52 (2): 274–9. doi :10.1021/jf030616i. PMID 14733508.
- ^ Ilahy, R; Piro, G; Tlili, I; Riahi, A; Sihem, R; Ouerghi, I; Hdider, C; Lenucci, MS (2016). "Análisis fraccionado de la composición fitoquímica y actividades antioxidantes en líneas avanzadas de mejoramiento de tomates con alto contenido de licopeno". Food Funct . 7 (1): 574–83. doi :10.1039/c5fo00553a. PMID 26462607.
- ^ Perdomo F, Cabrera Fránquiz F, Cabrera J, Serra-Majem L (2012). "Influencia del procedimiento de cocción en la biodisponibilidad del licopeno en tomate". Nutrición Hospitalaria (Madrid) . 27 (5): 1542–6. doi :10.3305/nh.2012.27.5.5908. PMID 23478703.
- ^ Kamiloglu, S.; Demirci, M.; Selen, S.; Toydemir, G.; Boyacioglu, D.; Capanoglu, E. (2014). "Procesamiento casero de tomates (Solanum lycopersicum): efectos sobre la bioaccesibilidad in vitro del licopeno total, los compuestos fenólicos, los flavonoides y la capacidad antioxidante". Revista de la ciencia de la alimentación y la agricultura . 94 (11): 2225–33. Bibcode :2014JSFA...94.2225K. doi :10.1002/jsfa.6546. PMID 24375495.
- ^ Yamaguchi, Masayoshi (2010). Carotenoides: propiedades, efectos y enfermedades . Nueva York: Nova Science Publishers. pág. 125. ISBN 9781612097138.
- ^ Aoki, H; Kieu, NT; Kuze, N; Tomisaka, K; Van Chuyen, N (2002). "Pigmentos carotenoides en la fruta GAC (Momordica cochinchinensis SPRENG)". Biociencia, biotecnología y bioquímica . 66 (11): 2479–82. doi : 10.1271/bbb.66.2479 . PMID 12506992. S2CID 2118248.
- ^ Alquezar, B; Rodrigo, MJ; Zacarías, L (2008). "Regulación de la biosíntesis de carotenoides durante la maduración del fruto en el mutante naranja de pulpa roja Cara Cara". Fitoquímica . 69 (10): 1997–2007. Bibcode :2008PChem..69.1997A. doi :10.1016/j.phytochem.2008.04.020. PMID 18538806.
- ^ Li, Lei; Liu, Zhen; Jiang, Hong; Mao, Xiangzhao (2020). "Producción biotecnológica de licopeno por microorganismos". Appl. Microbiol. Biotechnol . 104 (24): 10307–10324. doi :10.1007/s00253-020-10967-4. PMID 33097966. S2CID 225058089.
- ^ abc "Licopeno". Mayo Clinic. 2017. Archivado desde el original el 23 de septiembre de 2017. Consultado el 29 de mayo de 2017 .
- ^ Tierney, Audrey; Rumble, Chloe; Billings, Lauren; George, Elena (2020). "Efecto del licopeno dietético y suplementario sobre los factores de riesgo cardiovascular: una revisión sistemática y un metanálisis". Avances en nutrición . 11 (6): 1453–1488. doi :10.1093/advances/nmaa069. PMC 7666898 . PMID 32652029.
- ^ Cheng, Ho Ming; Koutsidis, Georgios; Logia, John K.; Ashor, Ammar; Siervo, Mario; Lara, José (2017). "Suplementación con tomate y licopeno y factores de riesgo cardiovascular: una revisión sistemática y un metanálisis" (PDF) . Aterosclerosis . 257 : 100–108. doi :10.1016/j.atherosclerosis.2017.01.009. ISSN 0021-9150. PMID 28129549. S2CID 19287598.
- ^ Chen, Ping; Zhang, Wenhao; Wang, Xiao; et al. (2015-08-21). "Licopeno y riesgo de cáncer de próstata". Medicina . 94 (33): e1260. doi :10.1097/md.0000000000001260. ISSN 0025-7974. PMC 4616444 . PMID 26287411.
- ^ Luo, Jie; Ke, Dandan; He, Qingwei (2021). "Consumo dietético de tomate y riesgo de cáncer de próstata: un metaanálisis". Frontiers in Nutrition . 8 : 625185. doi : 10.3389/fnut.2021.625185 . ISSN 2296-861X. PMC 8129008 . PMID 34017849.
- ^ Story, EN; Kopec, R. E; Schwartz, S. J; Harris, G. K (2010). "Una actualización sobre los efectos del licopeno del tomate en la salud". Revisión anual de ciencia y tecnología de los alimentos . 1 (1): 189–210. doi :10.1146/annurev.food.102308.124120. PMC 3850026 . PMID 22129335.
- ^ "Dictamen científico sobre la fundamentación de las declaraciones de propiedades saludables relacionadas con el licopeno y la protección del ADN, las proteínas y los lípidos frente al daño oxidativo (ID 1608, 1609, 1611, 1662, 1663, 1664, 1899, 1942, 2081, 2082, 2142, 2374), la protección de la piel frente al daño inducido por los rayos UV (incluido el fotooxidativo) (ID 1259, 1607, 1665, 2143, 2262, 2373), la contribución a la función cardíaca normal (ID 1610, 2372) y el mantenimiento de la visión normal (ID 1827) de conformidad con el artículo 13(1) del Reglamento (CE) n.º 1924/2006". Revista de la EFSA . 9 (4): 2031. 2011. doi : 10.2903/j.efsa.2011.2031 .
- ^ ab "Reclamos de propiedades saludables calificados: Carta sobre los tomates y el cáncer de próstata (Lycopene Health Claim Coalition) (Expediente n.º 2004Q-0201) (Actualizado el 9 de julio de 2015)". Administración de Alimentos y Medicamentos de los Estados Unidos. 8 de noviembre de 2005. Archivado desde el original el 22 de julio de 2017. Consultado el 16 de diciembre de 2019 .
- ^ "Licopeno". Instituto Nacional del Cáncer de EE. UU. 5 de abril de 2024. Consultado el 14 de septiembre de 2024 .




