Vacuna contra la gripe
 Una vacuna contra la gripe administrada a un miembro de la tripulación de la Marina de los EE. UU. | |
| Descripción de la vacuna | |
|---|---|
| Objetivo | Virus de la gripe |
| Tipo de vacuna | inactivado, atenuado, recombinante |
| Datos clínicos | |
| Nombres comerciales | Afluria, Fluarix, Fluzone, otros |
| AHFS / Drogas.com | Inactivado: Monografía Intranasal: Monografía Recombinante: Monografía |
Categoría de embarazo |
|
| Vías de administración | Intramuscular , intranasal , intradérmica |
| Código ATC | |
| Estatus legal | |
| Estatus legal | |
| Identificadores | |
| Número CAS |
|
| Araña química |
|
| BARRIL |
|
Las vacunas contra la gripe , conocidas coloquialmente como inyecciones contra la gripe [14] o la inyección contra la gripe [15] , son vacunas que protegen contra la infección por virus de la gripe . [16] [17] Se desarrollan nuevas versiones de las vacunas dos veces al año, ya que el virus de la gripe cambia rápidamente. [16] Si bien su eficacia varía de un año a otro, la mayoría proporciona una protección moderada a alta contra la gripe . [16] [18] La vacunación contra la gripe comenzó en la década de 1930, y su disponibilidad a gran escala en los Estados Unidos comenzó en 1945. [19] [20]
Tanto la Organización Mundial de la Salud como los Centros para el Control y la Prevención de Enfermedades (CDC) de Estados Unidos recomiendan la vacunación anual para casi todas las personas mayores de seis meses, especialmente aquellas con alto riesgo, [16] [21] [22] [23] y la vacuna contra la gripe está en la Lista de Medicamentos Esenciales de la Organización Mundial de la Salud . [24] El Centro Europeo para la Prevención y el Control de Enfermedades (ECDC) también recomienda la vacunación anual de los grupos de alto riesgo, [25] en particular las mujeres embarazadas, los ancianos, los niños entre seis meses y cinco años y aquellos con ciertos problemas de salud. [16] [23]
Las vacunas son generalmente seguras, incluso para las personas que tienen alergias graves al huevo . [26] Un efecto secundario común es el dolor cerca del lugar de la inyección. La fiebre se presenta en el cinco al diez por ciento de los niños vacunados, y pueden ocurrir dolores musculares temporales o sensación de cansancio. En ciertos años, la vacuna se relacionó con un aumento del síndrome de Guillain-Barré entre las personas mayores a una tasa de aproximadamente un caso por millón de dosis. [16] Las vacunas contra la gripe no se recomiendan en quienes han tenido una alergia grave a versiones anteriores de la propia vacuna. [16] [26] La vacuna viene en formas virales inactivas y debilitadas . La vacuna viva debilitada generalmente no se recomienda en mujeres embarazadas, niños menores de dos años, adultos mayores de 50 años o personas con un sistema inmunológico debilitado . [16] Dependiendo del tipo, se puede inyectar en un músculo (intramuscular) , rociar en la nariz (intranasal) o inyectar en la capa media de la piel (intradérmica). [16] La vacuna intradérmica no estuvo disponible durante las temporadas de influenza 2018-2019 y 2019-2020. [27] [28] [29]
Historia
Las vacunas se utilizan tanto en seres humanos como en animales. Se entiende por vacuna humana, a menos que se identifique específicamente que es una vacuna veterinaria, avícola o ganadera.
Orígenes y desarrollo
Durante la pandemia mundial de gripe española de 1918, "los farmacéuticos probaron todo lo que sabían, todo lo que habían oído hablar, desde el antiguo arte de sangrar a los pacientes, hasta la administración de oxígeno , pasando por el desarrollo de nuevas vacunas y sueros (principalmente contra lo que llamamos Haemophilus influenzae -un nombre derivado del hecho de que originalmente se consideró el agente etiológico- y varios tipos de neumococos). Sólo una medida terapéutica, la transfusión de sangre de pacientes recuperados a nuevas víctimas, mostró algún indicio de éxito". [30]
En 1931, Ernest William Goodpasture y sus colegas de la Universidad de Vanderbilt informaron sobre el crecimiento viral en huevos de gallina embrionados . El trabajo se extendió al crecimiento del virus de la influenza por varios trabajadores, incluidos Thomas Francis , Jonas Salk , Wilson Smith y Macfarlane Burnet , lo que condujo a las primeras vacunas experimentales contra la influenza. [31] En la década de 1940, el ejército de los EE. UU. desarrolló las primeras vacunas inactivadas aprobadas contra la influenza, que se utilizaron durante la Segunda Guerra Mundial . [32] Los huevos de gallina continuaron utilizándose para producir el virus utilizado en las vacunas contra la influenza, pero los fabricantes realizaron mejoras en la pureza del virus al desarrollar procesos mejorados para eliminar las proteínas del huevo y reducir la reactividad sistémica de la vacuna. [33] En 2012, la Administración de Alimentos y Medicamentos de los EE. UU. (FDA) aprobó las vacunas contra la influenza elaboradas mediante el cultivo del virus en cultivos celulares [34] [35] [36] y se han aprobado las vacunas contra la influenza elaboradas a partir de proteínas recombinantes [37] , y se están probando vacunas contra la influenza basadas en plantas [ ¿cuándo? ] en ensayos clínicos. [38]
Aceptación
La tecnología basada en huevos para producir la vacuna contra la gripe se creó en la década de 1950. [39] En la crisis de gripe porcina de 1976 en Estados Unidos , el presidente Gerald Ford se enfrentó a una posible pandemia de gripe porcina. El programa de vacunación se realizó a toda prisa, pero estuvo plagado de retrasos y problemas de relaciones públicas. Mientras tanto, los máximos esfuerzos militares de contención tuvieron un éxito inesperado al confinar la nueva cepa a la única base militar donde se había originado. En esa base, varios soldados enfermaron gravemente, pero solo uno murió. El programa se canceló después de que aproximadamente el 24% de la población hubiera recibido las vacunas. Se estimó que el propio programa de vacunación provocó un exceso de 25 muertes por encima de los niveles anuales normales, así como 400 hospitalizaciones adicionales, ambas por el síndrome de Guillain-Barré , lo que demuestra que la vacuna en sí no está libre de riesgos. [40] Sin embargo, al final, incluso la difamada vacuna de 1976 puede haber salvado vidas. Un estudio de 2010 encontró una respuesta inmune significativamente mejorada contra la pandemia H1N1 de 2009 en los participantes del estudio que habían recibido la vacuna contra la gripe porcina en 1976. [41] El brote de "gripe porcina" H1N1 de 2009 resultó en la rápida aprobación de las vacunas contra la influenza pandémica. [42] Pandemrix se modificó rápidamente para atacar la cepa circulante y para fines de 2010, 70 millones de personas habían recibido una dosis. [43] Ocho años después, el BMJ obtuvo acceso a los informes de farmacovigilancia de vacunas compilados por GSK (GlaxoSmithKline) durante la pandemia que, según informó el BMJ, indicaban que la muerte era 5,39 veces más probable con Pandemrix que con las otras vacunas pandémicas. [42] [43]
Vacunas tetravalentes

En marzo de 2012, la FDA aprobó una vacuna antigripal tetravalente administrada mediante pulverización nasal. [44] [45] La vacuna tetravalente Fluarix fue aprobada por la FDA en diciembre de 2012. [46]
En 2014, el Comité Asesor Nacional Canadiense sobre Inmunización (NACI) publicó una revisión de las vacunas antigripales cuadrivalentes. [47]
A partir de la temporada de influenza 2018-2019, la mayoría de las vacunas antigripales de dosis regular basadas en huevo y todas las vacunas antigripales recombinantes y cultivadas en células en los Estados Unidos son tetravalentes. [48] En la temporada de influenza 2019-2020, todas las vacunas antigripales de dosis regular y todas las vacunas antigripales recombinantes en los Estados Unidos son tetravalentes. [49]
En noviembre de 2019, la FDA aprobó la vacuna Fluzone High-Dose Quadrivalent para su uso en los Estados Unidos a partir de la temporada de influenza 2020-2021. [50] [51]
En febrero de 2020, la FDA aprobó Fluad Quadrivalent para su uso en los Estados Unidos. [52] [53] En julio de 2020, la FDA aprobó tanto Fluad como Fluad Quadrivalent para su uso en los Estados Unidos para la temporada de influenza 2020-2021. [52] [54]
El linaje B/Yamagata de la influenza B , uno de los cuatro linajes a los que se dirigen las vacunas cuadrivalentes, podría haberse extinguido en 2020/2021 debido a las medidas pandémicas de COVID-19 , [55] y no se han confirmado casos naturales desde marzo de 2020. [56] [57] En 2023, la Organización Mundial de la Salud concluyó que la protección contra el linaje Yamagata ya no era necesaria en la vacuna contra la gripe estacional, por lo que se recomienda que las futuras vacunas sean trivalentes en lugar de cuadrivalentes. [56] [57] Para la temporada de influenza del hemisferio norte 2024-2025, la FDA recomienda eliminar B/Yamagata de todas las vacunas contra la influenza. [58]
Usos médicos
La vacuna antigripal está indicada para la inmunización activa para la prevención de la enfermedad gripal causada por los subtipos A y B del virus de la influenza contenidos en la vacuna. [59] [60] [61]
Los Centros para el Control y la Prevención de Enfermedades (CDC) de Estados Unidos recomiendan la vacuna contra la gripe como la mejor manera de proteger a las personas contra la gripe y prevenir su propagación. [62] La vacuna contra la gripe también puede reducir la gravedad de la gripe si una persona contrae una cepa que la vacuna no contenía. [62] Se necesitan aproximadamente dos semanas después de la vacunación para que se formen los anticuerpos protectores . [62] [63]
Un metaanálisis de 2012 concluyó que la vacunación contra la gripe era eficaz el 67 por ciento de las veces; las poblaciones que más se beneficiaron fueron los adultos VIH positivos de entre 18 y 55 años (76 por ciento), los adultos sanos de entre 18 y 46 años (aproximadamente el 70 por ciento) y los niños sanos de entre seis y 24 meses (66 por ciento). [64] La vacuna contra la gripe también parece proteger contra el infarto de miocardio , con un beneficio del 15 al 45 por ciento. [65]
Eficacia
Los gráficos no están disponibles debido a problemas técnicos. Hay más información en Phabricator y en MediaWiki.org. |
Una vacuna se evalúa por su eficacia (el grado en que reduce el riesgo de enfermedad en condiciones controladas) y su efectividad (la reducción observada del riesgo después de que se pone en uso la vacuna). [72] En el caso de la gripe, se espera que la efectividad sea menor que la eficacia porque se mide utilizando las tasas de enfermedad similar a la gripe , que no siempre es causada por la gripe. [73] Los estudios sobre la efectividad de las vacunas contra la gripe en el mundo real son difíciles; las vacunas pueden no coincidir perfectamente, la prevalencia del virus varía ampliamente de un año a otro y la gripe a menudo se confunde con otras enfermedades similares a la gripe. [74] Sin embargo, en la mayoría de los años (16 de los 19 años anteriores a 2007), las cepas de la vacuna contra la gripe han coincidido bien con las cepas circulantes, [75] e incluso una vacuna no coincidente a menudo puede proporcionar protección cruzada. [62] El virus cambia rápidamente debido a la deriva antigénica , una ligera mutación en el virus que hace que surja una nueva cepa. [76]
La eficacia de las vacunas contra la gripe estacional varía significativamente, con una eficacia media estimada del 50-60% contra la enfermedad sintomática , [77] dependiendo de la cepa de la vacuna, la edad, la inmunidad previa y la función inmunológica, por lo que las personas vacunadas aún pueden contraer la gripe. [78] La eficacia de las vacunas contra la gripe se considera subóptima, en particular entre los ancianos, [79] pero la vacunación sigue siendo beneficiosa para reducir la tasa de mortalidad y la tasa de hospitalización debido a la gripe, así como la duración de la hospitalización. [78] [80] La vacunación de niños en edad escolar ha demostrado proporcionar protección indirecta para otros grupos de edad. Las LAIV se recomiendan para niños basándose en su eficacia superior, especialmente para niños menores de 6 años, y una mayor inmunidad contra cepas no vacunales en comparación con las vacunas inactivadas. [81] [82]
En Nueva Zelanda, entre 2012 y 2015, la efectividad de la vacuna contra el ingreso a una unidad de cuidados intensivos fue del 82 %. [83] La efectividad contra la enfermedad de influenza que requiere hospitalización en la temporada de gripe de 2019-2020 en los Estados Unidos fue del 41 % en general y del 54 % en personas de 65 años o más. [84] Una revisión encontró una efectividad del 31 % contra la muerte entre los adultos. [85] [86]
La vacunación anual repetida contra la influenza generalmente ofrece una protección consistente año tras año contra la influenza. [86] Sin embargo, hay evidencia sugestiva de que las vacunaciones repetidas pueden causar una reducción en la efectividad de la vacuna para ciertos subtipos de influenza; esto no tiene relevancia para las recomendaciones de vacunaciones anuales, pero podría influir en la política de vacunación futura. [87] [88] A partir de 2019 [actualizar], los CDC recomiendan una vacuna anual ya que la mayoría de los estudios demuestran la efectividad general de la vacunación anual contra la influenza. [86]
No hay evidencia suficiente para establecer diferencias significativas en la efectividad de los diferentes tipos de vacunas contra la influenza , [89] pero hay productos de dosis alta o adyuvados que inducen una respuesta inmune más fuerte en los ancianos. [90]
Según un estudio realizado en 2016 por profesores de la Universidad de Nueva Gales del Sur, vacunarse contra la gripe fue tan eficaz o más para prevenir un ataque cardíaco que dejar de fumar. [91]
Un estudio de los CDC de 2024 determinó que la vacuna contra la gripe de 2024 redujo el riesgo de hospitalización por gripe en un 35 % en el hemisferio sur. [92] La investigación, realizada en cinco países (Argentina, Brasil, Chile, Paraguay y Uruguay), mostró que la vacuna fue menos efectiva que la utilizada en la temporada anterior. [93]
Niños
En abril de 2002, el Comité Asesor sobre Prácticas de Inmunización (ACIP) alentó a que los niños de 6 a 23 meses de edad se vacunen anualmente contra la gripe. [94] En 2010, el ACIP recomendó la vacunación anual contra la gripe para los mayores de 6 meses. [94] Los CDC recomiendan que todos, excepto los bebés menores de seis meses, reciban la vacuna contra la gripe estacional. [21] Las campañas de vacunación suelen centrar especial atención en las personas que corren un alto riesgo de sufrir complicaciones graves si contraen la gripe, como las mujeres embarazadas, los niños menores de 59 meses, los ancianos y las personas con enfermedades crónicas o sistemas inmunitarios debilitados , así como aquellos a quienes están expuestos, como los trabajadores de la salud. [21] [95]
Como la tasa de mortalidad también es alta entre los bebés que contraen gripe, los CDC y la OMS recomiendan que los contactos domésticos y los cuidadores de los bebés se vacunen para reducir el riesgo de transmitir una infección de gripe al bebé. [95] [96]
En los niños, la vacuna parece disminuir el riesgo de gripe y posiblemente de enfermedad similar a la gripe . [97] En los niños menores de dos años, los datos son limitados. [97] Durante la temporada de gripe 2017-18, el director de los CDC indicó que el 85 por ciento de los niños que murieron "probablemente no habrán sido vacunados". [98]
En los Estados Unidos, a partir de enero de 2019 [actualizar], los CDC recomiendan que los niños de seis a 35 meses puedan recibir 0,25 mililitros o 0,5 mililitros por dosis de Fluzone Quadrivalent. [49] [99] No hay preferencia por uno u otro volumen de dosis de Fluzone Quadrivalent para ese grupo de edad. [49] Todas las personas de 36 meses de edad o más deben recibir 0,5 mililitros por dosis de Fluzone Quadrivalent. [49] A partir de octubre de 2018 [actualizar], Afluria Quadrivalent está autorizado para niños de seis meses de edad o más en los Estados Unidos. [49] [100] Los niños de seis a 35 meses de edad deben recibir 0,25 mililitros por cada dosis de Afluria Quadrivalent. [49] Todas las personas de 36 meses de edad o más deben recibir 0,5 mililitros por dosis de Afluria Quadrivalent. [49] A partir de febrero de 2018 [actualizar], Afluria Tetra está autorizada para adultos y niños de cinco años de edad o más en Canadá. [101]
En 2014, el Comité Asesor Nacional Canadiense sobre Inmunización (NACI) publicó una revisión de la vacunación contra la influenza en niños sanos de 5 a 18 años de edad [102] y en 2015 publicó una revisión del uso de Fluad pediátrico en niños de 6 a 72 meses de edad [103] . En un estudio, realizado en un centro de referencia terciario, la tasa de vacunación contra la influenza en niños fue solo del 31%. Se encontraron tasas más altas entre los pacientes pediátricos inmunodeprimidos (46%) y en pacientes con enfermedad inflamatoria intestinal (50%). [104]
Adultos
.jpg/440px-Navy_flu_shot_(50494239776).jpg)
En los adultos no vacunados, el 16% presenta síntomas similares a los de la gripe, mientras que aproximadamente el 10% de los adultos vacunados los presentan. [73] La vacunación redujo los casos confirmados de gripe de aproximadamente el 2,4% al 1,1%. [73] No se encontró ningún efecto sobre la hospitalización. [73]
En adultos trabajadores, una revisión realizada por la Colaboración Cochrane encontró que la vacunación resultó en una disminución modesta tanto de los síntomas de influenza como de los días laborales perdidos, sin afectar la transmisión o las complicaciones relacionadas con la influenza. [73] En adultos trabajadores sanos, las vacunas contra la influenza pueden brindar protección moderada contra la influenza confirmada virológicamente , aunque dicha protección se reduce considerablemente o no existe en algunas temporadas. [105]
En el caso de los trabajadores de la salud, una revisión de 2006 encontró un beneficio neto. [106] De los dieciocho estudios de esta revisión, solo dos también evaluaron la relación entre la mortalidad de los pacientes y la aceptación de la vacuna contra la gripe por parte del personal; ambos encontraron que las tasas más altas de vacunación de los trabajadores de la salud se correlacionaban con una reducción de las muertes de los pacientes. [106] Una revisión de 2014 encontró beneficios para los pacientes cuando los trabajadores de la salud fueron vacunados, como lo respalda una evidencia moderada [107] basada en parte en la reducción observada en las muertes por todas las causas en los pacientes cuyos trabajadores de la salud recibieron la vacuna en comparación con los pacientes de comparación en los que no se les ofreció la vacuna a los trabajadores. [108]
Anciano
No hay evidencia clara de un efecto en adultos mayores de 65 años. [109] Las revisiones sistemáticas que examinaron estudios controlados aleatorios y estudios de casos y controles encontraron una falta de evidencia de alta calidad. [105] [110] Las revisiones de estudios de casos y controles encontraron efectos contra la influenza, la neumonía y la muerte confirmadas por laboratorio entre los ancianos que viven en la comunidad. [111] [112]
El grupo más vulnerable a la gripe no pandémica, los ancianos, es el que menos se beneficia de la vacuna. Hay múltiples razones detrás de esta pronunciada disminución de la eficacia de la vacuna, las más comunes de las cuales son el deterioro de la función inmunológica y la fragilidad asociada con la edad avanzada. [113] En un año no pandémico, una persona en los Estados Unidos de 50 a 64 años tiene casi diez veces más probabilidades de morir de una muerte asociada a la gripe que una persona más joven, y una persona mayor de 65 años tiene más de diez veces más probabilidades de morir de una muerte asociada a la gripe que el grupo de edad de 50 a 64 años. [114]
Existe una vacuna antigripal de dosis alta específicamente formulada para proporcionar una respuesta inmunitaria más fuerte. [115] La evidencia disponible indica que vacunar a los ancianos con la vacuna de dosis alta conduce a una respuesta inmunitaria contra la gripe más fuerte que la vacuna de dosis regular. [116] [117] [118]
En noviembre de 2015, la Administración de Alimentos y Medicamentos de los Estados Unidos (FDA) aprobó una vacuna contra la gripe que contiene un adyuvante para su uso en adultos mayores de 65 años. La vacuna se comercializa como Fluad en los Estados Unidos y estuvo disponible por primera vez en la temporada de gripe 2016-2017. La vacuna contiene el adyuvante MF59C.1 [119] , que es una emulsión de aceite en agua de aceite de escualeno . Es la primera vacuna contra la gripe estacional con adyuvante comercializada en los Estados Unidos. [120] [121] [122] No está claro si existe un beneficio significativo para los ancianos por usar una vacuna contra la gripe que contenga el adyuvante MF59C.1. [123] [124] [125] Según las pautas del Comité Asesor sobre Prácticas de Inmunización , Fluad se puede usar como una alternativa a otras vacunas contra la gripe aprobadas para personas mayores de 65 años. [121]
En muchos países se recomienda vacunar a los trabajadores de la salud que trabajan con personas mayores, con el objetivo de reducir los brotes de gripe en esta población vulnerable. [126] [127] [128] Si bien no hay evidencia concluyente de ensayos clínicos aleatorios de que la vacunación de los trabajadores de la salud ayude a proteger a las personas mayores de la gripe, hay evidencia tentativa de beneficio. [129]
El uso de Fluad Quad fue aprobado en Australia en septiembre de 2019, [130] el de Fluad Quadrivalent fue aprobado en los Estados Unidos en febrero de 2020, [52] y el de Fluad Tetra fue aprobado en la Unión Europea en mayo de 2020. [131] [132]
Embarazo
Además de proteger a la madre y al niño de los efectos de una infección de gripe, la inmunización de las mujeres embarazadas tiende a aumentar sus posibilidades de tener un embarazo exitoso a término. [133]
La vacuna antigripal trivalente inactivada protege a las mujeres embarazadas infectadas por el VIH . [134]
Seguridad
Efectos secundarios
Los efectos secundarios comunes de la vacunación incluyen reacciones locales en el lugar de la inyección y síntomas similares a los de un resfriado . La fiebre, el malestar y la mialgia son menos comunes. Las vacunas contra la gripe están contraindicadas para las personas que han experimentado una reacción alérgica grave en respuesta a una vacuna contra la gripe o a cualquier componente de la vacuna. Las LAIV no se administran a niños o adolescentes con inmunodeficiencia grave o a aquellos que están usando tratamientos con salicilatos debido al riesgo de desarrollar el síndrome de Reye . [81] Las LAIV tampoco se recomiendan para niños menores de 2 años, [82] mujeres embarazadas y adultos con inmunosupresión. Las vacunas antigripales inactivadas no pueden causar gripe y se consideran seguras durante el embarazo. [81]
Si bien pueden producirse efectos secundarios de la vacuna contra la gripe, suelen ser menores e incluyen dolor, enrojecimiento e hinchazón alrededor del punto de inyección, dolor de cabeza, fiebre, náuseas o fatiga. [135] Los efectos secundarios de una vacuna en aerosol nasal pueden incluir secreción nasal, sibilancia, dolor de garganta, tos o vómitos. [136]
En algunas personas, la vacuna antigripal puede provocar efectos secundarios graves, incluida una reacción alérgica , pero esto es poco frecuente. Además, los efectos secundarios y riesgos habituales son leves y temporales en comparación con los riesgos y los efectos graves para la salud de la epidemia anual de gripe . [62]
Contrariamente a una idea errónea común , las vacunas contra la gripe no pueden provocar que las personas contraigan la enfermedad. [137] [138]
Síndrome de Guillain-Barré
Aunque se temía que el síndrome de Guillain-Barré fuera una complicación de la vacunación, los CDC afirman que la mayoría de los estudios sobre las vacunas modernas contra la gripe no han encontrado ningún vínculo con el síndrome de Guillain-Barré. [139] [140] La infección con el virus de la gripe en sí aumenta tanto el riesgo de muerte (hasta uno en diez mil) como el riesgo de desarrollar el síndrome de Guillain-Barré a un nivel mucho más alto que el nivel más alto de presunta participación en la vacuna (aproximadamente diez veces más alto según las estimaciones de 2009). [141] [142]
Aunque una revisión da una incidencia de alrededor de un caso de Guillain-Barré por cada millón de vacunaciones, [143] un estudio a gran escala en China, que abarcó cerca de cien millones de dosis de vacuna contra la gripe "porcina" H1N1 de 2009, encontró sólo once casos de síndrome de Guillain-Barré (0,1 por millón de dosis) de incidencia total en personas vacunadas, en realidad menor que la tasa normal de la enfermedad en China, y ningún otro efecto secundario notable. [142] [144]
Alergia al huevo
.jpg/440px-Ampliação_e_Modernização_da_Fábrica_de_Vacina_(40225018103).jpg)
Aunque la mayoría de las vacunas contra la gripe se producen utilizando técnicas basadas en huevos, las vacunas contra la gripe se siguen recomendando como seguras para las personas con alergia al huevo , incluso si es grave, [26] ya que no se ha demostrado un mayor riesgo de reacción alérgica a las vacunas basadas en huevo para las personas con alergia al huevo. [145] Los estudios que examinaron la seguridad de las vacunas contra la gripe en personas con alergia grave al huevo encontraron que la anafilaxia era muy rara y se producía en 1,3 casos por millón de dosis administradas. [26]
Se recomienda controlar los síntomas de la vacunación en aquellos con síntomas más graves. [146] Un estudio de casi 800 niños con alergia al huevo, incluidos más de 250 con reacciones anafilácticas previas, no tuvo reacciones alérgicas sistémicas cuando se les administró la vacuna antigripal viva atenuada . [147] [148]
Las vacunas producidas mediante otras tecnologías, en particular las vacunas recombinantes y las basadas en cultivos celulares en lugar de proteínas de huevo, comenzaron a estar disponibles a partir de 2012 en los EE. UU. [149], y más tarde en Europa [150] y Australia. [145]
Otro
Varios estudios han identificado una mayor incidencia de narcolepsia entre los receptores de la vacuna contra la influenza pandémica H1N1 con adyuvante AS03 ; [151] los esfuerzos por identificar un mecanismo para esto sugieren que la narcolepsia es autoinmune y que la vacuna contra la influenza H1N1 con adyuvante AS03 puede imitar a la hipocretina y actuar como desencadenante. [152]
Algunas vacunas inyectables contra la gripe destinadas a adultos en los Estados Unidos contienen tiomersal (también conocido como timerosal), un conservante a base de mercurio . [153] [154] A pesar de cierta controversia en los medios, [155] el Comité Asesor Mundial sobre Seguridad de las Vacunas de la Organización Mundial de la Salud ha concluido que no hay evidencia de toxicidad del tiomersal en las vacunas y no hay razón por razones de seguridad para cambiar a una administración de dosis única más costosa. [156]
No se cree que hacer ejercicio antes de recibir la vacuna contra la gripe sea perjudicial, pero tampoco hay evidencia de que tenga un efecto beneficioso. [157]
Tipos
Las vacunas contra la gripe estacional están disponibles como: [ cita requerida ]
- una inyección trivalente o cuadrivalente, que contiene la forma inactivada del virus. Generalmente se trata de una inyección intramuscular, aunque las vías subcutánea e intradérmica también pueden ser protectoras. [158]
- un aerosol nasal de vacuna antigripal viva atenuada , que contiene la forma viva pero atenuada (debilitada) del virus.
Las vacunas inyectables inducen protección basada en una respuesta inmune a los antígenos presentes en el virus inactivado, mientras que el aerosol nasal funciona estableciendo una infección a corto plazo en los conductos nasales. [159]
Reformulación anual
Cada año, el Sistema Mundial de Vigilancia y Respuesta a la Gripe de la Organización Mundial de la Salud (OMS) elige tres cepas de influenza para incluirlas en la vacunación contra la gripe estacional del año siguiente . [160] La recomendación para la vacuna trivalente comprende dos cepas de influenza A (una de A/H1N1 y otra de A/H3N2) y una cepa de influenza B (B/Victoria), que representan en conjunto las cepas que se cree que tienen más probabilidades de causar un sufrimiento humano significativo en la próxima temporada. A partir de 2012, la OMS también ha recomendado una segunda cepa de influenza B (B/Yamagata) para su uso en vacunas cuadrivalentes; esta recomendación se suspendió en 2024. [161]
- "La Red Mundial de Vigilancia de la Gripe de la OMS se creó en 1952 (en 2011 pasó a llamarse "Sistema Mundial de Vigilancia y Respuesta a la Gripe"). [162] La red comprende cuatro Centros Colaboradores de la OMS (CC de la OMS) y 112 instituciones en 83 países, que son reconocidos por la OMS como Centros Nacionales de la Gripe (NIC). Estos NIC recogen muestras en su país, realizan el aislamiento primario del virus y la caracterización antigénica preliminar. Envían las cepas recién aisladas a los CC de la OMS para un análisis antigénico y genético de alto nivel, cuyo resultado constituye la base de las recomendaciones de la OMS sobre la composición de la vacuna antigripal para el hemisferio norte y sur cada año". [163]
Las primeras recomendaciones formales de la OMS se emitieron en 1973. A partir de 1999 ha habido dos recomendaciones por año: una para el hemisferio norte y otra para el hemisferio sur. [164]
Debido al uso generalizado de intervenciones no farmacéuticas al comienzo de la pandemia de COVID-19 , el linaje de influenza B/Yamagata no ha sido aislado desde marzo de 2020 y es posible que haya sido erradicado. A partir de la temporada de influenza del hemisferio sur de 2024, la OMS y otros organismos reguladores han eliminado a B/Yamagata de las recomendaciones de vacunas contra la influenza. [161] [58] [165]
Recomendaciones
Varias organizaciones de salud pública, incluida la Organización Mundial de la Salud (OMS), recomiendan que se ofrezca de forma rutinaria la vacunación anual contra la gripe, en particular a las personas con riesgo de sufrir complicaciones a causa de la gripe y a aquellas personas que viven con personas de alto riesgo o las cuidan, entre ellas:
- personas de 50 años o más [23]
- Personas con enfermedades pulmonares crónicas, incluido el asma [23]
- Personas con enfermedades cardíacas crónicas [23]
- Personas con enfermedades hepáticas crónicas [23]
- Personas con enfermedades renales crónicas [23]
- personas a las que se les ha extirpado el bazo o cuyo bazo no funciona correctamente [ cita médica necesaria ]
- personas inmunodeprimidas [23]
- residentes de hogares de ancianos y otros centros de atención a largo plazo [23]
- trabajadores de la salud (tanto para prevenir enfermedades como para prevenir el contagio a sus pacientes) [166] [167]
- Mujeres que están o estarán embarazadas durante la temporada de gripe [23]
- Niños y adolescentes (de 6 meses a 18 años) que reciben medicamentos que contienen aspirina o salicilato y que podrían estar en riesgo de sufrir el síndrome de Reye después de una infección por el virus de la influenza [23]
- Indios americanos/nativos de Alaska [23]
- personas con obesidad extrema (índice de masa corporal ≥40 para adultos) [23]
La vacuna contra la gripe está contraindicada para menores de seis meses y para quienes tienen alergias graves y potencialmente mortales a la vacuna contra la gripe o a cualquier ingrediente de la vacuna. [21] [168] [26]
Organización Mundial de la Salud
A partir de 2016 [actualizar], la Organización Mundial de la Salud (OMS) recomienda la vacunación contra la gripe estacional para: [169] [170] [171] [172] [173]
Primera prioridad:
- Mujeres embarazadas
Segunda prioridad (sin ningún orden particular):
- Niños de 6 a 59 meses
- Anciano
- Personas con enfermedades crónicas específicas
- Trabajadores de la salud
Canadá
El Comité Asesor Nacional sobre Inmunización (NACI), el grupo que asesora a la Agencia de Salud Pública de Canadá , recomienda que se anime a todas las personas mayores de seis meses a recibir la vacuna anual contra la gripe, y que los niños entre seis y 24 meses, y sus contactos domésticos, sean considerados una alta prioridad para la vacuna contra la gripe. [174] En particular:
- Personas con alto riesgo de complicaciones o de hospitalización relacionadas con la gripe, incluidas personas con obesidad mórbida, mujeres embarazadas sanas, niños de 6 a 59 meses, ancianos, aborígenes y personas con alguna de una lista detallada de afecciones de salud crónicas.
- Personas capaces de transmitir la gripe a personas de alto riesgo, incluidos los contactos domésticos y los trabajadores de la salud.
- Personas que prestan servicios comunitarios esenciales
- Ciertos trabajadores avícolas
La vacuna antigripal viva atenuada (LAIV) no estuvo disponible en Canadá para la temporada 2019-2020. [174]
unión Europea
El Centro Europeo para la Prevención y el Control de Enfermedades (ECDC) recomienda vacunar a los ancianos como prioridad, y como prioridad secundaria a las personas con enfermedades crónicas y a los trabajadores de la salud. [175]
La estrategia de vacunación contra la gripe suele ser la de proteger a las personas vulnerables, en lugar de limitar la circulación de la gripe o eliminar la enfermedad de la gripe humana. Esto contrasta con las estrategias de alta inmunidad colectiva para otras enfermedades infecciosas como la poliomielitis y el sarampión . [176] Esto también se debe en parte a la carga financiera y logística asociada con la necesidad de una inyección anual. [177]
Reino Unido
El Servicio Nacional de Salud del Reino Unido proporciona la vacuna contra la gripe a:
- personas que tienen 65 años o más
- Personas que tienen ciertas condiciones de salud a largo plazo.
- personas que estan embarazadas
- personas que viven en una residencia de ancianos
- personas que son los principales cuidadores de una persona mayor o discapacitada, o que reciben una prestación por cuidado
- personas que viven con alguien que tiene un sistema inmunológico debilitado. [178]
Esta vacuna está disponible de forma gratuita para las personas pertenecientes a estos grupos. Las personas que no pertenecen a estos grupos y tienen entre 18 y 65 años de edad también pueden recibir una vacuna privada contra la gripe por una pequeña tarifa en farmacias y algunos consultorios privados. [179]
Estados Unidos

En los Estados Unidos se recomienda la vacunación sistemática contra la gripe para todas las personas de seis meses o más. [180] [23] [181] Se necesitan hasta dos semanas después de la vacunación para que se desarrollen suficientes anticuerpos en el cuerpo. [181] El CDC recomienda la vacunación antes de fines de octubre, [23] aunque considera que recibir una vacuna en diciembre o incluso más tarde sigue siendo beneficioso. [23] [62] [181] El ejército de los EE. UU. también requiere una vacuna contra la gripe anualmente para sus miembros del servicio activo y de reserva. [182]
Según los CDC, algunos grupos deberían evitar el virus vivo atenuado (LAIV4) (que viene en forma de aerosol nasal en los EE. UU.). [23] [183]
Dentro de su recomendación general para la vacunación general en los Estados Unidos, los CDC, que comenzaron a recomendar la vacuna contra la influenza a los trabajadores de la salud en 1981, enfatizan a los médicos la urgencia especial de la vacunación para los miembros de ciertos grupos vulnerables y sus cuidadores :
- La vacunación es especialmente importante para las personas con mayor riesgo de sufrir complicaciones graves por la gripe o para las personas que viven con personas con mayor riesgo de sufrir complicaciones graves o que las cuidan. [184] En 2009, se aprobó una nueva formulación de dosis alta de la vacuna estándar contra la gripe. [185] La Fluzone de dosis alta está destinada específicamente a personas de 65 años o más; la diferencia es que tiene cuatro veces la dosis de antígeno de la Fluzone estándar. [186] [187] [188] [189]
El gobierno de Estados Unidos exige a los hospitales que informen sobre las tasas de vacunación de sus trabajadores. Algunos estados y cientos de hospitales de Estados Unidos exigen a los trabajadores sanitarios que se vacunen o utilicen mascarillas durante la temporada de gripe. Estos requisitos a veces dan lugar a demandas sindicales basadas en argumentos limitados para la negociación colectiva , pero los defensores señalan que, en general, los tribunales han respaldado las leyes de vacunación obligatoria que afectan a la población general durante los brotes de enfermedades. [190]
La vacunación contra la gripe se considera especialmente importante para los miembros de grupos de alto riesgo que probablemente tengan complicaciones a causa de la gripe, por ejemplo, las mujeres embarazadas [23] [191] y los niños y adolescentes de seis meses a 18 años de edad que reciben medicamentos que contienen aspirina o salicilato y que podrían estar en riesgo de sufrir el síndrome de Reye después de una infección por el virus de la gripe; [23]
- Al elevar el límite de edad superior a 18 años, el objetivo es reducir tanto el tiempo que los niños y los padres pierden en visitas al pediatra y ausencias a la escuela como la necesidad de antibióticos por complicaciones [192].
- Un beneficio adicional esperado de la vacunación de los niños es una reducción en el número de casos de gripe entre los padres y otros miembros del hogar, y de la posible propagación a la comunidad en general. [192]
Los CDC indicaron que la vacuna contra la influenza viva atenuada (LAIV), también llamada vacuna en aerosol nasal, no se recomendaba para la temporada de gripe 2016-2017 en los Estados Unidos. [193]
Además, los CDC recomiendan que el personal sanitario que atiende a personas con un sistema inmunitario gravemente comprometido reciba inyecciones (TIV o QIV) en lugar de LAIV. [194]
Australia
El Gobierno australiano recomienda la vacunación contra la gripe estacional para todas las personas mayores de seis meses. Australia utiliza vacunas inactivadas . [195] Hasta 2021, la vacuna a base de huevo ha sido la única disponible (y sigue siendo la única gratuita), pero a partir de marzo de 2021 está disponible una nueva vacuna a base de células para quienes deseen pagarla, y se espera que esta se convierta en la estándar para 2026. [145] La vacuna estándar contra la gripe es gratuita para las siguientes personas: [196]
- niños de seis meses a cinco años;
- personas de 65 años o más;
- Personas aborígenes e isleñas del Estrecho de Torres de seis meses o más de edad;
- mujeres embarazadas; y
- cualquier persona mayor de seis meses de edad con afecciones médicas como asma grave, enfermedad pulmonar o enfermedad cardíaca, baja inmunidad o diabetes que puedan provocar complicaciones a causa de la gripe.
Consumo
| País | Región | % de personas mayores de 65 años |
|---|---|---|
| República de Corea | Asia | 83 |
| Australia | Oceanía | 75 |
| Reino Unido | Europa | 73 |
| Estados Unidos | Américas | 68 |
| Nueva Zelanda | Oceanía | 65 |
| Chile | Américas | 65 |
| Países Bajos | Europa | 64 |
| Canadá | Américas | 61 |
| Portugal | Europa | 61 |
| Israel | Asia | 58 |
| Irlanda | Europa | 58 |
| España | Europa | 54 |
| Italia | Europa | 53 |
| Dinamarca | Europa | 52 |
| Japón | Asia | 50 |
| Francia | Europa | 50 |
| Suecia | Europa | 49 |
| Finlandia | Europa | 48 |
| Islandia | Europa | 45 |
| Luxemburgo | Europa | 38 |
| Alemania | Europa | 35 |
| Noruega | Europa | 34 |
| Hungría | Europa | 27 |
| República Checa | Europa | 20 |
| Lituania | Europa | 13 |
| República Eslovaca | Europa | 13 |
| Eslovenia | Europa | 12 |
| Letonia | Europa | 8 |
| Pavo | Asia | 7 |
| Estonia | Europa | 5 |
Grupos de riesgo
La aceptación de la vacunación contra la gripe, tanto estacionalmente como durante las pandemias, suele ser baja. [198] Las revisiones sistemáticas de la aceptación de la vacunación contra la gripe pandémica han identificado varios factores personales que pueden influir en la aceptación, incluidos el género (mayor aceptación en hombres), la etnia (mayor en personas de minorías étnicas) y tener una enfermedad crónica. [199] [200] Las creencias en la seguridad y la eficacia de la vacuna también son importantes. [198]
Se ha comprobado que una serie de medidas son útiles para aumentar las tasas de vacunación en las personas mayores de sesenta años, entre ellas: recordatorios a los pacientes mediante folletos y cartas, recordatorios mediante postales, programas de extensión a los clientes, visitas a domicilio para recibir la vacuna, vacunaciones en grupo, vacunaciones gratuitas, pago a los médicos, recordatorios a los médicos y fomento de la competencia entre médicos. [201]
Trabajadores de la salud
A menudo se recomienda a los trabajadores de atención médica de primera línea que se vacunen contra la gripe estacional y contra cualquier gripe pandémica. Por ejemplo, en el Reino Unido se recomienda a todos los trabajadores de atención médica involucrados en la atención de pacientes que reciban la vacuna contra la gripe estacional, y también se les recomendó que se vacunen contra el virus de la gripe porcina H1N1/09 (posteriormente rebautizado como A(H1N1)pdm09 [nota 1] [202] ) durante la pandemia de 2009. Sin embargo, la aceptación suele ser baja. [167] Durante la pandemia de 2009, se observó una baja aceptación por parte de los trabajadores de atención médica en países como el Reino Unido, [167] Italia, [203] Grecia, [204] y Hong Kong. [205]
En una encuesta realizada en 2010 a trabajadores de la salud de Estados Unidos, el 63,5% informó que había recibido la vacuna contra la gripe durante la temporada 2010-2011, un aumento con respecto al 61,9% informado en la temporada anterior. Los profesionales de la salud de Estados Unidos con contacto directo con pacientes tuvieron una mayor aceptación de la vacunación, como los médicos y dentistas (84,2%) y los enfermeros profesionales (82,6%). [206] [207] [208]
La principal razón para vacunar a los trabajadores de la salud es evitar que el personal transmita la gripe a sus pacientes y reducir el ausentismo del personal en un momento de alta demanda de servicios, pero las razones que los trabajadores de la salud indican para sus decisiones de aceptar o rechazar la vacunación pueden estar más a menudo relacionadas con los beneficios personales percibidos. [167]
En los hospitales públicos de Victoria (Australia), las tasas de vacunación del personal sanitario en 2005 oscilaron entre el 34% para el personal no clínico y el 42% para el personal de laboratorio. Una de las razones para rechazar las vacunas fue la preocupación por las reacciones adversas; en un estudio, el 31% de los médicos residentes de un hospital universitario creían erróneamente que las vacunas australianas podían causar gripe. [209]
Fabricación
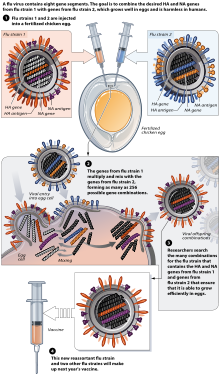
Se sigue investigando la idea de una vacuna antigripal "universal" que no requeriría una adaptación a una cepa en particular, sino que sería eficaz contra una amplia variedad de virus de la gripe. [210] Hasta noviembre de 2007 no se había anunciado ninguna vacuna candidata, [211] pero a partir de 2021 [actualizar], hay varias vacunas candidatas universales, en desarrollo preclínico y en ensayos clínicos. [212] [213] [214] [215]
En un informe de 2007, la capacidad mundial de aproximadamente 826 millones de dosis de vacunas contra la gripe estacional (inactivadas y vivas) era el doble de la producción de 413 millones de dosis. En un escenario agresivo de producción de vacunas contra la gripe pandémica para 2013, sólo se podrían producir 2.800 millones de dosis en un plazo de seis meses. Si todos los países de ingresos altos y medios altos buscaran vacunas para toda su población en una pandemia, se necesitarían casi 2.000 millones de dosis. Si China también persiguiera este objetivo, se necesitarían más de 3.000 millones de dosis para atender a esas poblaciones. [216] Se está investigando y desarrollando vacunas para identificar nuevos enfoques de vacunas que puedan producir cantidades mucho mayores de vacunas a un precio que sea asequible para la población mundial. [ cita requerida ]
A base de huevo
La mayoría de las vacunas contra la gripe se cultivan en huevos de gallina fertilizados por los fabricantes de vacunas. [217] [211] En el hemisferio norte, el proceso de fabricación comienza después del anuncio (normalmente en febrero) de las cepas recomendadas por la OMS para la temporada de gripe de invierno. [217] [218] Se seleccionan tres cepas de gripe (que representan una cepa H1N1, una H3N2 y una B) y se inoculan huevos de gallina por separado. Estas cosechas monovalentes se combinan luego para elaborar la vacuna trivalente. [219]
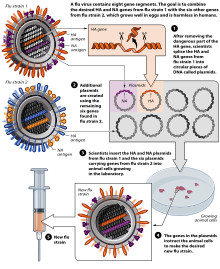
A partir de noviembre de 2007 [actualizar], tanto la inyección convencional como el aerosol nasal se fabrican utilizando huevos de gallina. La Unión Europea también aprobó Optaflu , una vacuna producida por Novartis utilizando cubas de células animales. Se espera que esta técnica sea más escalable y evite problemas con los huevos, como reacciones alérgicas e incompatibilidad con cepas que afectan a las aves como las gallinas. [211]
Las vacunas contra la gripe se producen en huevos libres de patógenos que tienen once o doce días de vida. [220] La parte superior del huevo se desinfecta frotándola con alcohol y luego se examina el huevo con una ovoscopia para identificar un área no venosa en la cavidad alantoidea donde se hace un pequeño orificio que sirve como liberador de presión. [221] Se hace un segundo orificio en la parte superior del huevo, donde se inyecta el virus de la gripe en la cavidad alantoidea, más allá de la membrana corioalantoidea. Luego, los dos orificios se sellan con parafina derretida y los huevos inoculados se incuban durante 48 horas a 37 grados Celsius. [220] Durante el tiempo de incubación, el virus se replica y los virus recién replicados se liberan en el líquido alantoideo [222]
Después de un período de incubación de 48 horas, se rompe la parte superior del huevo y se extraen los diez mililitros de líquido alantoideo, de los cuales se pueden obtener unos quince microgramos de la vacuna antigripal. En este punto, los virus se han debilitado o eliminado y el antígeno viral se purifica y se coloca dentro de viales, jeringas o atomizadores nasales. [222] Se necesitan hasta 3 huevos para producir una dosis de una vacuna trivalente, y se estima que cada año se producen 600 millones de huevos para la producción de la vacuna antigripal. [223]
Otros métodos de fabricación
Los métodos de generación de vacunas que evitan la necesidad de huevos incluyen la construcción de partículas similares al virus de la influenza (VLP). Las VLP se parecen a los virus, pero no hay necesidad de inactivación, ya que no incluyen elementos codificantes virales, sino que simplemente presentan antígenos de manera similar a un virión. Algunos métodos de producción de VLP incluyen cultivos de células de insecto Spodoptera frugiperda Sf9 y producción de vacunas a base de plantas (por ejemplo, producción en Nicotiana benthamiana ). Hay evidencia de que algunas VLP provocan anticuerpos que reconocen un panel más amplio de aislados virales antigénicamente distintos en comparación con otras vacunas en el ensayo de inhibición de la hemaglutinación (HIA). [224]
En 2011 se realizaron ensayos clínicos con una vacuna de ADN basada en genes, utilizada para preparar el sistema inmunológico después de reforzarlo con una vacuna H5N1 inactivada. [225] [226] [227]
En noviembre de 2012, Novartis recibió la aprobación de la FDA para la primera vacuna de cultivo celular. [149] [35] [228] [229] En 2013, la vacuna recombinante contra la influenza, Flublok, fue aprobada para su uso en los Estados Unidos. [37] [230] [231] [232]
El 17 de septiembre de 2020, el Comité de Medicamentos de Uso Humano (CHMP) de la Agencia Europea de Medicamentos (EMA) adoptó una opinión positiva, recomendando la concesión de una autorización de comercialización para Supemtek, una vacuna antigripal tetravalente (recombinante, preparada en cultivo celular). [233] El solicitante de este medicamento es Sanofi Pasteur. [233] Supemtek fue aprobado para uso médico en la Unión Europea en noviembre de 2020. [150] [234]
En marzo de 2021, Australia autorizó su primera vacuna basada en células, basada en una "línea celular eterna" de riñón de perro . Debido a la forma en que se produce, produce una vacuna más compatible (con las cepas de la gripe). [145]
Países fabricantes de vacunas
Según la OMS , a partir de 2019 [actualizar], los países donde se produce la vacuna contra la influenza incluyen: [235]
- Australia
- Brasil
- Canadá
- Porcelana
- Francia
- Alemania
- Hungría
- India
- Irán
- Japón
- México
- Países Bajos
- Nicaragua
- Federación Rusa
- Corea del Sur
- Reino Unido
- Estados Unidos
- Vietnam
Además, Kazajstán, Serbia y Tailandia contaban con instalaciones en las últimas etapas de establecimiento de la producción. [235]
Rentabilidad
La relación coste-efectividad de la vacunación contra la gripe estacional se ha evaluado ampliamente para diferentes grupos y en diferentes entornos. [236] En los ancianos (mayores de 65 años), la mayoría de los estudios publicados han encontrado que la vacunación ahorra costos, y los ahorros de costos asociados con la vacunación contra la gripe (por ejemplo, visitas de atención médica evitadas) superan el costo de la vacunación. [237] En los adultos mayores (de 50 a 64 años), varios estudios publicados han encontrado que la vacunación contra la gripe probablemente sea rentable, sin embargo, a menudo se encontró que los resultados de estos estudios dependían de los supuestos clave utilizados en las evaluaciones económicas. [238] La incertidumbre en los modelos de coste-efectividad de la gripe se puede explicar parcialmente por las complejidades involucradas en la estimación de la carga de la enfermedad, [239] así como por la variabilidad estacional en las cepas circulantes y la compatibilidad de la vacuna. [240] [241] En adultos sanos que trabajan (de 18 a 49 años), una revisión de 2012 encontró que la vacunación en general no ahorraba costos, y que la idoneidad para la financiación dependía de la voluntad de pagar para obtener los beneficios de salud asociados. [242] En los niños, la mayoría de los estudios han encontrado que la vacunación contra la gripe era rentable, sin embargo, muchos de los estudios incluyeron ganancias de productividad (indirectas), a las que es posible que no se les dé el mismo peso en todos los entornos. [243] Varios estudios han intentado predecir la relación costo-efectividad de las intervenciones (incluida la vacunación prepandémica) para ayudar a proteger contra una futura pandemia, sin embargo, la estimación de la relación costo-efectividad se ha complicado por la incertidumbre en cuanto a la gravedad de una posible pandemia futura y la eficacia de las medidas contra ella. [244]
Investigación
La investigación sobre la gripe incluye la virología molecular , la evolución molecular , la patogénesis , las respuestas inmunitarias del huésped , la genómica y la epidemiología . Estas ayudan a desarrollar contramedidas contra la gripe, como vacunas , terapias y herramientas de diagnóstico. Las contramedidas mejoradas contra la gripe requieren una investigación básica sobre cómo los virus entran en las células, se replican, mutan, evolucionan en nuevas cepas e inducen una respuesta inmunitaria. El Proyecto de secuenciación del genoma de la gripe está creando una biblioteca de secuencias de la gripe [245] que ayudará a los investigadores a comprender qué hace que una cepa sea más letal que otra, qué determinantes genéticos afectan más a la inmunogenicidad y cómo evoluciona el virus con el tiempo.
Un enfoque diferente utiliza el contenido de Internet para estimar el impacto de una campaña de vacunación contra la gripe. Más específicamente, los investigadores han utilizado datos de Twitter y del motor de búsqueda Bing de Microsoft , y han propuesto un marco estadístico que, después de una serie de operaciones, relaciona esta información con las estimaciones del porcentaje de reducción de la enfermedad similar a la gripe en las zonas donde se han realizado las vacunaciones. El método se ha utilizado para cuantificar el impacto de dos programas de vacunación contra la gripe en Inglaterra (2013/14 y 2014/15), en los que se administró a niños en edad escolar una vacuna viva atenuada contra la gripe (LAIV). Cabe destacar que las estimaciones del impacto coincidieron con las estimaciones de Public Health England basadas en los puntos finales de vigilancia sindrómica tradicionales. [246] [247]
Respuesta rápida a la gripe pandémica
El rápido desarrollo, producción y distribución de vacunas contra la gripe pandémica podría salvar potencialmente millones de vidas durante una pandemia de gripe. Debido al breve lapso de tiempo entre la identificación de una cepa pandémica y la necesidad de vacunación, los investigadores están buscando nuevas tecnologías para la producción de vacunas que podrían proporcionar un mejor acceso "en tiempo real" y ser producidas de manera más asequible, aumentando así el acceso para las personas que viven en países de ingresos bajos y moderados, donde es probable que se origine una pandemia de gripe, como la tecnología de virus vivos atenuados (basados en huevos o células ) y las tecnologías recombinantes (proteínas y partículas similares a virus). [248] A julio de 2009 [actualizar], se habían completado o estaban en curso más de setenta ensayos clínicos conocidos para vacunas contra la gripe pandémica. [249] En septiembre de 2009, la FDA aprobó cuatro vacunas contra el virus de la gripe H1N1 de 2009 (la cepa pandémica de 2009), y esperaba que los lotes iniciales de vacunas estuvieran disponibles dentro del mes siguiente. [250]
En enero de 2020, la Administración de Alimentos y Medicamentos de los Estados Unidos (FDA) aprobó Audenz como vacuna contra el virus de la gripe H5N1. [251] Audenz es una vacuna indicada para la inmunización activa para la prevención de enfermedades causadas por el subtipo H5N1 del virus de la influenza A contenido en la vacuna. Audenz está aprobada para su uso en personas de seis meses de edad o más con mayor riesgo de exposición al subtipo H5N1 del virus de la influenza A contenido en la vacuna. [252]
La vacuna contra la influenza zoonótica Seqirus está autorizada para su uso en la Unión Europea. [253] Es una vacuna H5N8 que está destinada a proporcionar inmunidad adquirida contra los virus de influenza A del subtipo H5. [253]
Vacunas universales contra la gripe
Una vacuna universal contra la gripe que no tuviera que diseñarse y fabricarse para cada temporada de gripe en cada hemisferio estabilizaría el suministro, evitaría errores en la predicción de las variantes de la temporada y protegería contra el escape de las cepas circulantes por mutación. [210] Una vacuna de este tipo ha sido objeto de investigación durante décadas. [254]
Un enfoque consiste en utilizar anticuerpos ampliamente neutralizantes que, a diferencia de las vacunas estacionales anuales utilizadas durante las primeras décadas del siglo XXI que provocan que el cuerpo genere una respuesta inmunitaria, proporcionen en cambio un componente de la propia respuesta inmunitaria. Los primeros anticuerpos neutralizantes se identificaron en 1993, mediante experimentación. [255] Se descubrió que los anticuerpos neutralizantes de la gripe se unían al tallo de la proteína hemaglutinina . Se identificaron anticuerpos que podían unirse a la cabeza de esas proteínas. El canal de protones M2 altamente conservado se propuso como un objetivo potencial para los anticuerpos ampliamente neutralizantes. [254] [256]
Los desafíos para los investigadores son identificar anticuerpos individuales que puedan neutralizar muchos subtipos del virus, de modo que puedan ser útiles en cualquier estación, y que se dirijan a dominios conservados que sean resistentes a la deriva antigénica . [254]
Otro enfoque es tomar los dominios conservados identificados a partir de estos proyectos y administrar grupos de estos antígenos para provocar una respuesta inmune; se están desarrollando varios enfoques con diferentes antígenos, presentados de diferentes maneras (como proteínas de fusión , montadas en partículas similares a virus , en virus no patógenos, como ADN y otros). [256] [257] [258]
También se han realizado esfuerzos para desarrollar vacunas universales que activen específicamente una respuesta de células T , basándose en datos clínicos que muestran que las personas con una respuesta temprana y fuerte de células T tienen mejores resultados cuando se infectan con influenza y porque las células T responden a epítopos conservados. El desafío para los desarrolladores es que estos epítopos se encuentran en dominios proteínicos internos que son solo levemente inmunogénicos. [256]
Al igual que el resto del campo de las vacunas, las personas que trabajan en vacunas universales han experimentado con adyuvantes de vacunas para mejorar la capacidad de sus vacunas para crear una respuesta inmune suficientemente potente y duradera. [256] [259]
Vacuna oral contra la gripe
En 2019, una vacuna oral contra la gripe se encontraba en fase de investigación clínica . [260] La vacuna oral candidata se basa en un vector de adenovirus tipo 5 modificado para eliminar los genes necesarios para la replicación, con un gen añadido que expresa una pequeña molécula de horquilla de ARN bicatenario como adyuvante . [261] En 2020, un ensayo en humanos de fase II de la forma de píldora de la vacuna mostró que era bien tolerada y proporcionaba una inmunidad similar a una vacuna inyectable autorizada . [262]
COVID-19
Se pueden administrar de forma segura una vacuna contra la influenza y una vacuna contra la COVID-19 al mismo tiempo. [63] [263] Las investigaciones preliminares indican que la vacunación contra la influenza no previene la COVID-19 , pero puede reducir la incidencia y la gravedad de la infección por COVID-19. [264]
Crítica
Tom Jefferson , que ha dirigido las revisiones de las vacunas contra la gripe en el marco de la Colaboración Cochrane , ha calificado de "basura" la evidencia clínica relativa a las vacunas contra la gripe y, por lo tanto, ha declarado que son ineficaces; ha pedido ensayos clínicos aleatorios controlados con placebo , que la mayoría de los expertos en el campo consideran poco éticos . Sus opiniones sobre la eficacia de las vacunas contra la gripe son rechazadas por instituciones médicas, como los CDC y los Institutos Nacionales de Salud , y por figuras clave en el campo como Anthony Fauci . [265]
Michael Osterholm , quien dirigió la revisión de 2012 del Centro para la Investigación y Política de Enfermedades Infecciosas sobre las vacunas contra la gripe, recomendó vacunarse pero criticó su promoción, diciendo: "Hemos promocionado y sobrevalorado esta vacuna ... no protege como se promociona. Es todo un trabajo de ventas: es todo relaciones públicas". [266]
Uso veterinario
La vacunación veterinaria contra la gripe tiene como objetivo alcanzar los cuatro objetivos siguientes: [267]
- Protección contra enfermedades clínicas
- Protección contra la infección por virus virulentos
- Protección contra la excreción del virus
- Diferenciación serológica de animales infectados de vacunados (principio DIVA).
Caballos
Los caballos con gripe equina pueden tener fiebre, tos seca, goteo nasal, depresión y renuencia a comer o beber durante varios días, pero por lo general se recuperan en dos o tres semanas. "Los programas de vacunación generalmente requieren un ciclo primario de dos dosis, con un intervalo de 3 a 6 semanas, seguido de dosis de refuerzo con un intervalo de 6 a 12 meses. Se reconoce generalmente que en muchos casos estos programas pueden no mantener niveles protectores de anticuerpos y se recomienda una administración más frecuente en situaciones de alto riesgo". [268]
En los espectáculos del Reino Unido es un requisito habitual que los caballos estén vacunados contra la gripe equina y que se presente una tarjeta de vacunación; la Federación Internacional de Deportes Ecuestres (FEI) exige la vacunación cada seis meses. [269] [270]
Aves de corral
Es posible vacunar a las aves de corral contra cepas específicas de influenza aviar altamente patógena. La vacunación debe combinarse con otras medidas de control, como la vigilancia de la infección, la detección temprana y la bioseguridad. [271] [272]
Cerdos
Las vacunas contra la gripe porcina se utilizan ampliamente en la cría de cerdos en Europa y América del Norte. La mayoría de las vacunas contra la gripe porcina incluyen una cepa H1N1 y una H3N2 .
La gripe porcina ha sido reconocida como un problema importante desde su brote en 1976. La evolución del virus ha dado lugar a respuestas inconsistentes a las vacunas tradicionales. Las vacunas comerciales estándar contra la gripe porcina son eficaces para controlar el problema cuando las cepas del virus coinciden lo suficiente como para tener una protección cruzada significativa. En los casos más difíciles se elaboran y utilizan vacunas personalizadas (autógenas) a partir de los virus específicos aislados. [ 273] El fabricante de vacunas Novartis afirma que la cepa H3N2 (identificada por primera vez en 1998) ha provocado importantes pérdidas a los criadores de cerdos. Las oleadas de abortos son un signo común y las cerdas dejan de comer durante unos días y presentan fiebre alta. La tasa de mortalidad puede llegar al quince por ciento. [274]
Perros
En 2004, se descubrió que el virus de la influenza A subtipo H3N8 causaba la influenza canina . Debido a la falta de exposición previa a este virus, los perros no tienen inmunidad natural a este virus. Sin embargo, en 2004 se descubrió una vacuna. [275]
Notas
- ^ (H1N1)pdm09 es una nomenclatura más nueva para el virus pandémico H1N1 de 2009, no una cepa diferente.
Referencias
- ^ ab "AusPAR: Hemaglutinina recombinante de influenza". Therapeutic Goods Administration (TGA) . 23 de agosto de 2021. Archivado desde el original el 11 de septiembre de 2021. Consultado el 10 de septiembre de 2021 .
- ^ ab "AusPAR: vacuna antigripal tetravalente inactivada (virión fraccionado) hemaglutinina del virus de la influenza". Therapeutic Goods Administration (TGA) . 2 de diciembre de 2020. Archivado desde el original el 11 de septiembre de 2021. Consultado el 10 de septiembre de 2021 .
- ^ "Actualizaciones de la base de datos de prescripción de medicamentos durante el embarazo". Therapeutic Goods Administration (TGA) . 21 de diciembre de 2022. Archivado desde el original el 3 de abril de 2022. Consultado el 2 de enero de 2023 .
- ^ "Medicamentos de prescripción: registro de nuevas entidades químicas en Australia, 2017". Therapeutic Goods Administration (TGA) . 21 de junio de 2022. Archivado desde el original el 10 de abril de 2023. Consultado el 9 de abril de 2023 .
- ^ "Medicamentos de prescripción: registro de nuevas entidades químicas en Australia, 2016". Therapeutic Goods Administration (TGA) . 21 de junio de 2022. Archivado desde el original el 10 de abril de 2023. Consultado el 10 de abril de 2023 .
- ^ https://www.tga.gov.au/resources/auspar/auspar-flucelvax-quad-0 [ URL básica ]
- ^ "Base resumida de la decisión (SBD) para Supemtek". Health Canada . 23 de octubre de 2014. Archivado desde el original el 30 de mayo de 2022. Consultado el 29 de mayo de 2022 .
- ^ "Resumen de la decisión regulatoria - Flucelvax Quad". Health Canada . 23 de octubre de 2014. Archivado desde el original el 7 de junio de 2022. Consultado el 7 de junio de 2022 .
- ^ "Resumen de la decisión regulatoria - Flucelvax Quad". Health Canada . 23 de octubre de 2014. Archivado desde el original el 7 de junio de 2022. Consultado el 7 de junio de 2022 .
- ^ "Resumen de la decisión reglamentaria - Influvac Tetra". Health Canada . 23 de octubre de 2014. Archivado desde el original el 7 de junio de 2022. Consultado el 7 de junio de 2022 .
- ^ "Resumen de la decisión regulatoria para Panenza (cepa de hemaglutinina A (H1N1))". Portal de medicamentos y productos sanitarios . 27 de octubre de 2023 . Consultado el 2 de abril de 2024 .
- ^ "Supemtek EPAR". Agencia Europea de Medicamentos . 25 de noviembre de 2020. Consultado el 27 de junio de 2024 .
- ^ "Fluad Tetra". Agencia Europea de Medicamentos (EMA) . 20 de mayo de 2020. Consultado el 10 de agosto de 2024 .
- ^ "Datos clave sobre la vacuna contra la gripe estacional". Gripe (influenza) . 30 de septiembre de 2024.
- ^ "La vacuna contra la gripe durante el embarazo". nhs.uk . 3 de diciembre de 2020.
- ^ abcdefghi Organización Mundial de la Salud (noviembre de 2012). "Vacunas contra la gripe. Documento de posición de la OMS". Weekly Epidemiological Record . 87 (47): 461–76. hdl : 10665/241993 . PMID 23210147.
- ^ Organización Mundial de la Salud (mayo de 2022). «Vacunas contra la gripe: documento de posición de la OMS – mayo de 2022». Weekly Epidemiological Record . 97 (19): 185–208. hdl : 10665/354265 .
- ^ Manzoli L, Ioannidis JP , Flacco ME, De Vito C, Villari P (julio de 2012). "Eficacia y daños de las vacunas contra la gripe estacional y pandémica en niños, adultos y ancianos: una revisión crítica y un nuevo análisis de 15 metanálisis". Vacunas e inmunoterapias humanas . 8 (7): 851–62. doi :10.4161/hv.19917. PMC 3495721. PMID 22777099 .
- ^ Compañeros RW (2009). Vacunas para la influenza pandémica. Dordrecht: Springer. pag. 49.ISBN 978-3-540-92165-3Archivado del original el 3 de agosto de 2020 . Consultado el 9 de septiembre de 2017 .
- ^ Análisis de vacunas: estrategias, principios y control. Springer. 2014. pág. 61. ISBN 978-3-662-45024-6Archivado del original el 3 de agosto de 2020 . Consultado el 9 de septiembre de 2017 .
- ^ abcd "Quién debería y quién NO debería vacunarse contra la gripe". Centros para el Control y la Prevención de Enfermedades (CDC) de EE. UU . . 11 de octubre de 2019. Archivado desde el original el 2 de diciembre de 2019 . Consultado el 2 de diciembre de 2019 .
 Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público .
Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público . - ^ Serie Bases inmunológicas de la inmunización: módulo 23: vacunas contra la gripe . Organización Mundial de la Salud (OMS). Octubre de 2017. hdl : 10665/259211 . ISBN 978-92-4-151305-0.
- ^ abcdefghijklmnopqrs Grohskopf LA, Alyanak E, Ferdinands JM, Broder KR, Blanton LH, Talbot HK, et al. (agosto de 2021). "Prevención y control de la influenza estacional con vacunas: recomendaciones del Comité Asesor sobre Prácticas de Inmunización, Estados Unidos, temporada de influenza 2021-22" (PDF) . MMWR Recomm Rep . 70 (5): 1–28. doi : 10.15585/mmwr.rr7005a1 . PMC 8407757 . PMID 34448800. Archivado (PDF) del original el 27 de agosto de 2021 . Consultado el 29 de agosto de 2021 .
 Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público .
Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público . - ^ Organización Mundial de la Salud (2023). Selección y uso de medicamentos esenciales 2023: anexo web A: Lista modelo de medicamentos esenciales de la Organización Mundial de la Salud: 23.ª lista (2023) . Ginebra: Organización Mundial de la Salud. hdl : 10665/371090 . OMS/MHP/HPS/EML/2023.02.
- ^ "Aplicación de la Recomendación del Consejo sobre la vacunación contra la gripe estacional (2009/1019/UE)" (PDF) . Centro Europeo para la Prevención y el Control de las Enfermedades . Enero de 2014. Archivado (PDF) del original el 10 de abril de 2020 . Consultado el 10 de abril de 2020 .
- Resumen para legos en: "Implementación de la Recomendación del Consejo sobre la vacunación contra la gripe estacional". Centro Europeo para la Prevención y el Control de Enfermedades . 9 de enero de 2014.
- ^ abcde «Vacuna contra la gripe y personas alérgicas al huevo». Centros para el Control y la Prevención de Enfermedades (CDC) de EE. UU. 25 de noviembre de 2019. Archivado desde el original el 2 de diciembre de 2019. Consultado el 2 de diciembre de 2019 .
 Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público .
Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público . - ^ "Vacunación intradérmica contra la influenza (gripe)". Centros para el Control y la Prevención de Enfermedades (CDC) de EE. UU . . 31 de octubre de 2018. Archivado desde el original el 14 de octubre de 2019 . Consultado el 14 de octubre de 2019 .
 Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público .
Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público . - ^ "Vacunas contra la influenza – Estados Unidos, temporada de influenza 2019-20". Centros para el Control y la Prevención de Enfermedades (CDC) de EE. UU . . 22 de agosto de 2019. Archivado desde el original el 14 de octubre de 2019 . Consultado el 14 de octubre de 2019 .
 Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público .
Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público . - ^ "Vacuna contra el virus de la influenza inactivada". The American Society of Health-System Pharmacists. 19 de noviembre de 2018. Archivado desde el original el 14 de octubre de 2019. Consultado el 13 de octubre de 2019 .
- ^ Instituto de Medicina (2005). Knobler SL, Mack A, Mahmoud A, Lemon SM (eds.). La amenaza de la gripe pandémica: ¿estamos preparados? Resumen del taller . The National Academies Press. pág. 62. doi :10.17226/11150. ISBN 978-0-309-09504-4. Número de identificación personal 20669448.
- ^ Plotkin, SL y Plotkin, SA "Una breve historia de la vacunación". En: Vaccines , Stanley A. Plotkin, Walter A. Orenstein, Paul A. Offit, eds. Elsevier Health Sciences, 2008, págs. 6-7.
- ^ Artenstein, AW "Influenza" en: Vacunas: una biografía , Andrew W. Artenstein, ed. págs. 191-205.
- ^ Hampson AW (junio de 2008). "Vacunas contra la gripe pandémica. Historia de nuestras vacunas actuales, sus limitaciones y los requisitos para hacer frente a una amenaza pandémica". Anales de la Academia de Medicina, Singapur . 37 (6): 510–17. doi : 10.47102/annals-acadmedsg.V37N6p510 . PMID: 18618064. S2CID : 17102174.
- ^ Milián E, Kamen AA (2015). "Tecnologías actuales y emergentes de fabricación de cultivos celulares para vacunas contra la gripe". Biomed Res Int . 2015 : 504831. doi : 10.1155/2015/504831 . PMC 4359798. PMID 25815321 .
- ^ ab "La FDA aprueba la primera vacuna contra la gripe estacional fabricada con tecnología de cultivo celular" (Comunicado de prensa). Administración de Alimentos y Medicamentos de Estados Unidos (FDA). Archivado desde el original el 2 de enero de 2013.
 Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público .
Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público . - ^ "Vacunas antigripales basadas en células". Centros para el Control y la Prevención de Enfermedades de Estados Unidos (CDC). 11 de octubre de 2019. Archivado desde el original el 2 de diciembre de 2019. Consultado el 2 de diciembre de 2019 .
 Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público .
Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público . - ^ ab "La FDA aprueba una nueva vacuna contra la gripe estacional elaborada con tecnología novedosa" (Comunicado de prensa). Administración de Alimentos y Medicamentos de Estados Unidos (FDA). 16 de enero de 2013. Archivado desde el original el 18 de mayo de 2013.
 Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público .
Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público . - ^ Landry N, Ward BJ, Trépanier S, Montomoli E, Dargis M, Lapini G, et al. (diciembre de 2010). "Desarrollo preclínico y clínico de una vacuna de partículas similares a virus de origen vegetal contra la influenza aviar H5N1". PLOS ONE . 5 (12): e15559. Bibcode :2010PLoSO...515559L. doi : 10.1371/journal.pone.0015559 . PMC 3008737 . PMID 21203523.
- ^ Osterholm MT (mayo de 2005). "Preparación para la próxima pandemia". The New England Journal of Medicine . 352 (18): 1839–42. CiteSeerX 10.1.1.608.6200 . doi :10.1056/NEJMp058068. PMID 15872196. S2CID 45893174.
- ^ "Epidemias de gripe porcina". 9 de octubre de 1999. Archivado desde el original el 9 de octubre de 1999.
- ^ McCullers JA, Van De Velde LA, Allison KJ, Branum KC, Webby RJ, Flynn PM (junio de 2010). "Los receptores de la vacuna contra la "gripe porcina" de 1976 han mejorado las respuestas de neutralización al nuevo virus de la influenza H1N1 de 2009". Clinical Infectious Diseases . 50 (11): 1487–92. doi :10.1086/652441. PMC 2946351 . PMID 20415539.
- ^ ab Doshi P (20 de septiembre de 2018). "Vacuna Pandemrix: ¿por qué no se informó al público sobre las señales de advertencia tempranas?". BMJ . 362 : k3948. doi :10.1136/bmj.k3948. ISSN 0959-8138. S2CID 52308748.
- ^ ab Doshi P (20 de septiembre de 2018). "Vacuna Pandemrix: ¿por qué no se informó al público sobre las señales de advertencia tempranas?". BMJ . 362 : Infografía. doi :10.1136/bmj.k3948. S2CID 52308748.
- ^ "La primera vacuna cuadrivalente contra la gripe estacional obtiene la aprobación de la FDA". 2 de marzo de 2012. Archivado desde el original el 4 de marzo de 2012.
- ^ "La FDA aprueba la primera vacuna tetravalente para prevenir la gripe estacional" (Comunicado de prensa). Administración de Alimentos y Medicamentos de Estados Unidos (FDA). Archivado desde el original el 21 de diciembre de 2012.
 Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público .
Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público . - ^ "Carta de aprobación del 14 de diciembre de 2012: Fluarix Quadrivalent". Administración de Alimentos y Medicamentos de los Estados Unidos (FDA). Archivado desde el original el 2 de enero de 2013.
 Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público .
Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público . - ^ Comité Asesor Nacional sobre Inmunización (NACI) (julio de 2014). Revisión de la literatura sobre las vacunas tetravalentes contra la influenza (PDF) . Ottawa: Agencia de Salud Pública de Canadá. ISBN 978-1-100-24682-6Cat.: HP40-117/2014E-PDF Pub.: 140118. Archivado (PDF) desde el original el 1 de agosto de 2020 . Consultado el 11 de enero de 2020 .
- ^ "Lo que debe saber sobre la temporada de influenza 2018-2019". Centros para el Control y la Prevención de Enfermedades (CDC) . 10 de enero de 2019. Archivado desde el original el 6 de agosto de 2020. Consultado el 5 de febrero de 2020 .
 Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público .
Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público . - ^ abcdefg «Preguntas frecuentes sobre la influenza (gripe): temporada 2019-2020». Centros para el Control y la Prevención de Enfermedades (CDC) de EE. UU . . 5 de noviembre de 2019. Archivado desde el original el 1 de diciembre de 2019 . Consultado el 30 de noviembre de 2019 .
 Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público .
Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público . - ^ "Fluzone High-Dose Quadrivalent". Administración de Alimentos y Medicamentos de Estados Unidos (FDA). 4 de noviembre de 2019. STN: BL 103914. Archivado desde el original el 12 de enero de 2020. Consultado el 5 de febrero de 2020 .
 Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público .
Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público . - ^ "La FDA aprueba la vacuna Fluzone de dosis alta cuadrivalente (contra la influenza) para adultos de 65 años o más". Sanofi (Nota de prensa). 4 de noviembre de 2019. Archivado desde el original el 1 de agosto de 2020. Consultado el 5 de febrero de 2020 .
- ^ abc "Fluad Quadrivalent". Administración de Alimentos y Medicamentos de Estados Unidos (FDA). 2 de julio de 2020. STN: 125510. Archivado desde el original el 11 de agosto de 2020. Consultado el 25 de agosto de 2020 .
 Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público .
Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público . - ^ "Seqirus recibe la aprobación de la FDA para Fluad Quadrivalent para adultos de 65 años o más". Seqirus (Comunicado de prensa). 24 de febrero de 2020. Archivado desde el original el 26 de agosto de 2020 . Consultado el 25 de agosto de 2020 .
- ^ "Seqirus comienza a enviar vacunas contra la influenza 2020/21 al mercado estadounidense". Seqirus (Comunicado de prensa). 30 de julio de 2020. Archivado desde el original el 26 de agosto de 2020 . Consultado el 25 de agosto de 2020 .
- ^ Koutsakos M, Wheatley AK, Laurie K, Kent SJ, Rockman S (diciembre de 2021). "¿Extinción del linaje de la influenza durante la pandemia de COVID-19?". Nature Reviews. Microbiología . 19 (12): 741–742. doi :10.1038/s41579-021-00642-4. PMC 8477979 . PMID 34584246.
- ^ ab Organización Mundial de la Salud (29 de septiembre de 2023). «Preguntas y respuestas: Composición recomendada de las vacunas contra el virus de la influenza para su uso en la temporada de influenza 2024 del hemisferio sur y desarrollo de virus candidatos para vacunas en preparación para pandemias» (PDF) . Archivado (PDF) del original el 10 de octubre de 2023. Consultado el 26 de octubre de 2023 .
- ^ ab Schnirring L (29 de septiembre de 2023). «Los asesores de la OMS recomiendan volver a las vacunas antigripales trivalentes». CIDRAP . Archivado desde el original el 18 de diciembre de 2023 . Consultado el 26 de octubre de 2023 .
- ^ ab "Uso de vacunas antigripales trivalentes para la temporada de gripe 2024-2025 en EE. UU." Administración de Alimentos y Medicamentos de EE. UU. (FDA) . 5 de marzo de 2024. Archivado desde el original el 7 de marzo de 2024. Consultado el 7 de marzo de 2024 .
 Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público .
Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público . - ^ "Flucelvax (antígeno del virus de la influenza a/georgia/12/2022 cvr-167 (h1n1) (derivado de células mdck, inactivado con propiolactona), antígeno del virus de la influenza a/sydney/1304/2022 (h3n2) (derivado de células mdck, inactivado con propiolactona), inyección, suspensión del antígeno del virus de la influenza b/singapore/wuh4618/2021, derivado de células mdck, inactivado con propiolactona; Flucelvax (antígeno del virus de la influenza a/georgia/12/2022 crv-167 (h1n1) (derivado de células mdck, inactivado con propiolactona), antígeno del virus de la influenza a/sydney/1304/2022 (h3n2) (derivado de células mdck, inactivado con propiolactona), virus de la influenza b b/singapore/wuh4618/2021 antígeno- derivado de células mdck, inyección inactivada con propiolactona, suspensión". DailyMed . 1 de julio de 2024 . Consultado el 31 de agosto de 2024 .
- ^ "Fluad (virus de la influenza a/victoria/4897/2022 antígeno ivr-238 (h1n1) (inactivado con formaldehído), virus de la influenza a/tailandia/8/2022 antígeno ivr-237 (h3n2) (inactivado con formaldehído), virus de la influenza b/austria/1359417/2021 antígeno bvr-26-inyección, suspensión inactivada con formaldehído". DailyMed . 1 de julio de 2024 . Consultado el 31 de agosto de 2024 .
- ^ "Fluzone High-Dose Quadrivalent Northern Hemisphere (antígeno del virus de la influenza A a/victoria/4897/2022 ivr-238 (h1n1) (inactivado con formaldehído), antígeno del virus de la influenza A a/california/122/2022 san-022 (h3n2) (inactivado con formaldehído), antígeno del virus de la influenza B b/phuket/3073/2013 (inactivado con formaldehído) y antígeno del virus de la influenza B b/michigan/01/2021 - inyección, suspensión inactivada con formaldehído". DailyMed . 30 de julio de 2024 . Consultado el 31 de agosto de 2024 .
- ^ abcdef «Datos clave sobre la vacuna contra la gripe estacional». Centros para el Control y la Prevención de Enfermedades (CDC) de EE. UU. 2 de diciembre de 2019. Archivado desde el original el 2 de diciembre de 2019. Consultado el 2 de diciembre de 2019 .
 Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público .
Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público . - ^ ab «Vacuna contra la gripe». Servicio Nacional de Salud del Reino Unido. 13 de mayo de 2022. Archivado desde el original el 26 de octubre de 2021. Consultado el 13 de agosto de 2022 .
- ^ Osterholm MT, Kelley NS, Sommer A, Belongia EA (enero de 2012). "Eficacia y efectividad de las vacunas contra la gripe: una revisión sistemática y un metanálisis". The Lancet. Enfermedades infecciosas . 12 (1): 36–44. doi :10.1016/s1473-3099(11)70295-x. PMID 22032844.
- ^ MacIntyre CR, Mahimbo A, Moa AM, Barnes M (diciembre de 2016). "Vacuna antigripal como intervención coronaria para la prevención del infarto de miocardio". Heart . 102 (24): 1953–1956. doi :10.1136/heartjnl-2016-309983. PMC 5256393 . PMID 27686519.
- ^ "Estimaciones de la eficacia de las vacunas en temporadas pasadas". Centros para el Control y la Prevención de Enfermedades (CDC) de EE. UU . . 29 de enero de 2020. Archivado desde el original el 12 de febrero de 2020 . Consultado el 4 de marzo de 2019 .
 Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público .
Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público . - ^ Centros para el Control y la Prevención de Enfermedades (CDC) (13 de agosto de 2004). "Evaluación de la eficacia de la vacuna contra la influenza 2003-04 entre niños y adultos--Colorado, 2003". MMWR. Informe semanal de morbilidad y mortalidad . 53 (31). Centros para el Control y la Prevención de Enfermedades: 707–710. ISSN 1545-861X. PMID 15306754. Archivado desde el original el 27 de abril de 2022. Consultado el 27 de abril de 2022 .En la mesa.
- ^ Centros para el Control y la Prevención de Enfermedades (CDC) (16 de enero de 2004). "Evaluación preliminar de la eficacia de la vacuna antigripal inactivada 2003-04 - Colorado, diciembre de 2003". MMWR. Informe semanal de morbilidad y mortalidad . 53 (1). Centros para el Control y la Prevención de Enfermedades: 8–11. ISSN 1545-861X. PMID 14724559. Archivado desde el original el 29 de mayo de 2022. Consultado el 25 de abril de 2022 .
- ^ "Informes de vigilancia semanales anteriores". Centros para el Control y la Prevención de Enfermedades . 29 de abril de 2022. Archivado desde el original el 22 de abril de 2022. Consultado el 25 de abril de 2022 .
- ^ Chung JR (11 de marzo de 2022). "Estimaciones provisionales de la eficacia de la vacuna contra la influenza estacional 2021-22: Estados Unidos, febrero de 2022". MMWR. Informe semanal de morbilidad y mortalidad . 71 (10): 365–370. doi :10.15585/mmwr.mm7110a1. ISSN 0149-2195. PMC 8911998. PMID 35271561. Archivado desde el original el 16 de mayo de 2022. Consultado el 25 de mayo de 2022 .
- ^ Dreisbach EN (3 de junio de 2021). "Los CDC no pueden estimar la efectividad de la vacuna contra la gripe después de una temporada históricamente leve". Healio. Archivado desde el original el 8 de octubre de 2021. Consultado el 18 de abril de 2022 .
- ^ Fedson DS (1998). "Medición de la protección: eficacia frente a efectividad". Avances en la estandarización biológica . 95 : 195–201. PMID 9855432.
- ^ abcde Demicheli V, Jefferson T, Ferroni E, Rivetti A, Di Pietrantonj C (febrero de 2018). "Vacunas para prevenir la influenza en adultos sanos". Base de Datos Cochrane de Revisiones Sistemáticas . 2020 (2): CD001269. doi : 10.1002/14651858.CD001269.pub6 . PMC 6491184. PMID 29388196 .
- ^ Jefferson T (octubre de 2006). "Vacunación contra la gripe: políticas versus evidencia". BMJ . 333 (7574): 912–15. doi :10.1136/bmj.38995.531701.80. PMC 1626345 . PMID 17068038.
- ^ "Temporada de influenza (gripe) 2007-2008". Centros para el Control y la Prevención de Enfermedades (CDC) de Estados Unidos. 26 de junio de 2008. Archivado desde el original el 6 de marzo de 2008.
 Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público .
Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público . - ^ Carrat F, Flahault A (septiembre de 2007). "Vacuna contra la gripe: el desafío de la deriva antigénica". Vaccine . 25 (39–40): 6852–6862. doi :10.1016/j.vaccine.2007.07.027. PMID 17719149.
- ^ Sautto GA, Kirchenbaum GA, Ross TM (19 de enero de 2018). "Hacia una vacuna universal contra la gripe: diferentes enfoques para un objetivo". Virology Journal . 15 (1): 17. doi : 10.1186/s12985-017-0918-y . PMC 5785881 . PMID 29370862.
- ^ ab Chow EJ, Doyle JD, Uyeki TM (12 de junio de 2019). "Enfermedad crítica relacionada con el virus de la influenza: prevención, diagnóstico, tratamiento". Cuidados críticos . 23 (1): 214. doi : 10.1186/s13054-019-2491-9 . PMC 6563376 . PMID 31189475.
- ^ Krammer F, Smith GJ, Fouchier RA, Peiris M, Kedzierska K, Doherty PC, et al. (28 de junio de 2018). "Influenza". Nature Reviews Disease Primers . 4 (1): 3. doi :10.1038/s41572-018-0002-y. PMC 7097467 . PMID 29955068.
- ^ Dabestani NM, Leidner AJ, Seiber EE, Kim H, Graitcer SB, Foppa IM, et al. (septiembre de 2019). "Una revisión de la relación coste-efectividad de la vacunación contra la influenza en adultos y otros servicios preventivos". Medicina preventiva . 126 : 105734. doi :10.1016/j.ypmed.2019.05.022. PMC 6778688. PMID 31152830 .
- ^ abc Ghebrehewet S, MacPherson P, Ho A (7 de diciembre de 2016). "Influenza". El BMJ . 355 : i6258. doi :10.1136/bmj.i6258. PMC 5141587 . PMID 27927672.
- ^ ab Principi N, Esposito S (4 de marzo de 2018). "Protección de los niños contra la gripe: problemas emergentes". Vacunas e inmunoterapias humanas . 14 (3): 750–757. doi :10.1080/21645515.2017.1279772. PMC 5861800. PMID 28129049 .
- ^ Thompson MG, Pierse N, Huang QS, Prasad N, Duque J, Newbern EC, et al. (18 de septiembre de 2018). "Eficacia de la vacuna contra la gripe para prevenir las admisiones a cuidados intensivos asociadas a la gripe y atenuar la enfermedad grave entre los adultos de Nueva Zelanda 2012-2015". Vacuna . 36 (39): 5916–5925. doi :10.1016/j.vaccine.2018.07.028. ISSN 0264-410X. PMID 30077480. S2CID 51922011. Archivado desde el original el 27 de mayo de 2022 . Consultado el 23 de abril de 2022 .
- ^ Tenforde MW, Talbot HK, Trabue CH, Gaglani M, McNeal TS, Monto AS, et al. (30 de diciembre de 2020). "Efectividad de la vacuna contra la influenza contra la hospitalización en los Estados Unidos, 2019-2020". The Journal of Infectious Diseases . 224 (5): 813–820. doi :10.1093/infdis/jiaa800. ISSN 0022-1899. PMC 8408767 . PMID 33378531. Archivado desde el original el 23 de abril de 2022 . Consultado el 23 de abril de 2022 .
- ^ Ferdinands JM, Thompson MG, Blanton L, Spencer S, Grant L, Fry AM (23 de junio de 2021). "¿La vacunación contra la influenza atenúa la gravedad de las infecciones intercurrentes? Una revisión narrativa y recomendaciones para futuras investigaciones". Vacuna . 39 (28): 3678–3695. doi :10.1016/j.vaccine.2021.05.011. ISSN 0264-410X. PMID 34090700. S2CID 235361401. Archivado desde el original el 23 de abril de 2022 . Consultado el 23 de abril de 2022 .
- ^ abc "Efectividad de las vacunas: ¿Qué tan bien funcionan las vacunas contra la gripe?". Centros para el Control y la Prevención de Enfermedades (CDC) de EE. UU . . 12 de octubre de 2018. Archivado desde el original el 25 de octubre de 2019 . Consultado el 24 de octubre de 2019 .
 Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público .
Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público . - ^ Ramsay LC, Buchan SA, Stirling RG, Cowling BJ, Feng S, Kwong JC, et al. (enero de 2019). "El impacto de la vacunación repetida en la efectividad de la vacuna contra la influenza: una revisión sistemática y un metanálisis". BMC Med . 17 (1): 9. doi : 10.1186/s12916-018-1239-8 . PMC 6327561 . PMID 30626399.
- ^ Belongia EA, Skowronski DM, McLean HQ, Chambers C, Sundaram ME, De Serres G (julio de 2017). "Vacunación anual repetida contra la influenza y efectividad de la vacuna: revisión de la evidencia". Expert Rev Vaccines . 16 (7): 723–36. doi : 10.1080/14760584.2017.1334554 . PMID 28562111.
- ^ Gemmill I, Young K (7 de junio de 2018). "Resumen de la revisión de la literatura del NACI sobre la eficacia comparativa de las vacunas antigripales inactivadas con virus subunitarios y fraccionados en adultos mayores". Informe de enfermedades transmisibles de Canadá . 44 (6): 129–133. doi :10.14745/ccdr.v44i06a02. ISSN 1481-8531. PMC 6449119 . PMID 31015805. Archivado desde el original el 17 de mayo de 2020 . Consultado el 2 de junio de 2020 .
- ^ "La gripe y las personas de 65 años o más". Centros para el Control y la Prevención de Enfermedades . 26 de agosto de 2021. Archivado desde el original el 22 de abril de 2022. Consultado el 21 de abril de 2022 .
- ^ MacIntyre CR, Mahimbo A, Moa AM, Barnes M (diciembre de 2016). "Vacuna antigripal como intervención coronaria para la prevención del infarto de miocardio". Heart . 102 (24): 1953–1956. doi :10.1136/heartjnl-2016-309983. PMC 5256393 . PMID 27686519.
- ^ Zeno EE (2024). "Estimaciones provisionales de la eficacia de las vacunas contra la influenza en el hemisferio sur de 2024 para prevenir la hospitalización asociada a la influenza: Red REVELAC-i, cinco países sudamericanos, marzo-julio de 2024". MMWR. Informe semanal de morbilidad y mortalidad . 73 . doi :10.15585/mmwr.mm7339a1. ISSN 0149-2195.
- ^ Benadjaoud Y. "La vacuna contra la gripe redujo el riesgo de hospitalización en el hemisferio sur en un 35%: CDC". ABC News . Consultado el 4 de octubre de 2024 .
- ^ ab "Cronología histórica de la influenza | Influenza pandémica (gripe) | CDC". 11 de marzo de 2020. Archivado desde el original el 30 de enero de 2022. Consultado el 27 de enero de 2022 .
- ^ ab «Influenza (estacional)». Organización Mundial de la Salud (OMS) . 6 de noviembre de 2018. Archivado desde el original el 25 de octubre de 2019. Consultado el 24 de octubre de 2019 .
- ^ "Estudio de muertes relacionadas con la gripe en niños muestra que los niños sanos corren riesgo". Centros para el Control y la Prevención de Enfermedades (CDC) de EE. UU . . 12 de febrero de 2018. Archivado desde el original el 2 de diciembre de 2019 . Consultado el 2 de diciembre de 2019 .
 Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público .
Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público . - ^ ab Jefferson T, Rivetti A, Di Pietrantonj C, Demicheli V (febrero de 2018). "Vacunas para prevenir la influenza en niños sanos". Base de Datos Cochrane de Revisiones Sistemáticas . 2018 (2): CD004879. doi : 10.1002/14651858.CD004879.pub5 . PMC 6491174. PMID 29388195.
- ^ Steenhuysen J (22 de enero de 2018). "El director de los CDC de EE. UU. insta a vacunarse contra la gripe a medida que aumentan las muertes pediátricas". Reuters. Archivado desde el original el 6 de mayo de 2021. Consultado el 26 de enero de 2018 .
- ^ "Fluzone High-Dose Quadrivalent". Administración de Alimentos y Medicamentos de Estados Unidos (FDA). 14 de noviembre de 2019. Archivado desde el original el 1 de diciembre de 2019. Consultado el 30 de noviembre de 2019 .
 Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público .
Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público . - ^ "Afluria Quadrivalent". Administración de Alimentos y Medicamentos de Estados Unidos (FDA). 8 de noviembre de 2019. Archivado desde el original el 1 de diciembre de 2019. Consultado el 30 de noviembre de 2019 .
 Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público .
Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público . - ^ Comité Asesor Nacional sobre Inmunización (NACI) (noviembre de 2018). «Declaración complementaria – Afluria Tetra – Declaración del Comité Asesor (ACS)». Agencia de Salud Pública de Canadá . Ottawa. Cat.: HP37-25E-PDF Pub.: 180566. Archivado desde el original el 12 de enero de 2020. Consultado el 11 de enero de 2020 .
- ^ Revisión de la literatura sobre la vacunación contra la gripe en jóvenes sanos de 5 a 18 años (PDF) (Informe). Ottawa: Agencia de Salud Pública de Canadá. Julio de 2014. ISBN 978-1-100-24681-9Cat.: HP40-116/2014E-PDF Pub.: 140116. Archivado (PDF) desde el original el 1 de agosto de 2020 . Consultado el 12 de enero de 2020 .
- ^ Revisión de la literatura sobre el uso de la vacuna antigripal pediátrica en niños de 6 a 72 meses de edad (PDF) (Informe). Ottawa: Agencia de Salud Pública de Canadá. 2015. Archivado (PDF) del original el 17 de mayo de 2020 . Consultado el 11 de enero de 2020 .
- ^ Peleg N, Zevit N, Shamir R, Chodick G, Levy I (enero de 2015). "Tasas de vacunación contra la gripe estacional y motivos de no vacunación en niños con trastornos gastrointestinales". Vacuna . 33 (1): 182–186. doi :10.1016/j.vaccine.2014.10.086. PMID 25444802.
- ^ ab Osterholm MT, Kelley NS, Sommer A, Belongia EA (enero de 2012). "Eficacia y efectividad de las vacunas contra la gripe: una revisión sistemática y un metanálisis". The Lancet. Enfermedades infecciosas . 12 (1): 36–44. doi :10.1016/S1473-3099(11)70295-X. PMID 22032844.
- ^ ab Burls A, Jordan R, Barton P, Olowokure B, Wake B, Albon E, et al. (mayo de 2006). "Vacunar a los trabajadores sanitarios contra la gripe para proteger a los más vulnerables: ¿es un buen uso de los recursos sanitarios? Una revisión sistemática de la evidencia y una evaluación económica". Vaccine . 24 (19): 4212–21. doi :10.1016/j.vaccine.2005.12.043. PMID 16546308.
- ^ Ahmed F, Lindley MC, Allred N, Weinbaum CM, Grohskopf L (enero de 2014). "Efecto de la vacunación antigripal del personal sanitario sobre la morbilidad y la mortalidad entre los pacientes: revisión sistemática y clasificación de la evidencia". Clinical Infectious Diseases . 58 (1): 50–57. doi : 10.1093/cid/cit580 . PMID 24046301.
- ^ Griffin MR (enero de 2014). "Vacunación antigripal de los trabajadores sanitarios: preparación para la acción". Clinical Infectious Diseases . 58 (1): 58–60. doi : 10.1093/cid/cit590 . PMID 24046312.
- ^ Simonsen L, Viboud C, Taylor RJ, Miller MA, Jackson L (octubre de 2009). "Beneficios de la vacunación contra la gripe y la mortalidad: nuevos conocimientos, nuevas oportunidades". Vacuna . 27 (45): 6300–04. doi :10.1016/j.vaccine.2009.07.008. PMID 19840664.
- ^ Demicheli V, Jefferson T, Di Pietrantonj C, Ferroni E, Thorning S, Thomas RE, et al. (febrero de 2018). "Vacunas para prevenir la influenza en los ancianos". Base de Datos Cochrane de Revisiones Sistemáticas . 2 (11): CD004876. doi : 10.1002/14651858.CD004876.pub4 . PMC 6491101 . PMID 29388197.
- ^ Darvishian M, Bijlsma MJ, Hak E, van den Heuvel ER (diciembre de 2014). "Efectividad de la vacuna contra la gripe estacional en ancianos que viven en la comunidad: un metaanálisis de estudios de casos y controles con diseño de prueba negativa". The Lancet. Enfermedades infecciosas . 14 (12): 1228–39. doi :10.1016/S1473-3099(14)70960-0. PMID 25455990.
- ^ Nichol KL, Nordin JD, Nelson DB, Mullooly JP, Hak E (octubre de 2007). "Eficacia de la vacuna antigripal en ancianos que viven en la comunidad". The New England Journal of Medicine . 357 (14): 1373–81. doi : 10.1056/NEJMoa070844 . PMID 17914038. S2CID 14850833.
- ^ Simonsen L, Taylor RJ, Viboud C, Miller MA, Jackson LA (octubre de 2007). "Beneficios de la vacunación contra la gripe en la mortalidad de las personas mayores: una controversia en curso". The Lancet. Enfermedades infecciosas . 7 (10): 658–66. doi :10.1016/S1473-3099(07)70236-0. PMID 17897608.
- ^ Thompson WW, Shay DK, Weintraub E, Brammer L, Cox N, Anderson LJ, et al. (enero de 2003). "Mortalidad asociada con la influenza y el virus respiratorio sincitial en los Estados Unidos". JAMA . 289 (2): 179–86. doi : 10.1001/jama.289.2.179 . PMID 12517228. S2CID 5018362.
- ^ "Vacuna antigripal de dosis alta para personas mayores « Science-Based Medicine ». Sciencebasedmedicine.org. 19 de octubre de 2010. Archivado desde el original el 8 de mayo de 2013. Consultado el 17 de octubre de 2013 .
- ^ "Vacuna contra la influenza estacional de dosis alta Fluzone". Centros para el Control y la Prevención de Enfermedades (CDC) de EE. UU. 6 de septiembre de 2019. Archivado desde el original el 2 de diciembre de 2019 . Consultado el 2 de diciembre de 2019 .
- ^ DiazGranados CA, Dunning AJ, Kimmel M, Kirby D, Treanor J, Collins A, et al. (agosto de 2014). "Eficacia de la vacuna contra la influenza de dosis alta versus dosis estándar en adultos mayores". The New England Journal of Medicine . 371 (7): 635–45. doi : 10.1056/NEJMoa1315727 . PMID 25119609. S2CID 205096393.
- ^ Wells C, Grobelna A (8 de enero de 2019). "Vacuna antigripal de dosis alta para adultos: una revisión de la eficacia clínica, la relación coste-eficacia y las directrices" (PDF) . Informe de respuesta rápida . Ottawa: Agencia Canadiense de Medicamentos y Tecnologías en Salud (CADTH). ISSN 1922-8147. PMID 31141324. Archivado (PDF) del original el 1 de agosto de 2020. Consultado el 15 de agosto de 2022 .
- ^ Mascagni P, Vicenzi E, Kajaste-Rudnitski A, Pellicciotta G, Monti A, Cervi C, et al. (2012). "Evaluación de la eficacia y seguridad de la vacuna contra la influenza pandémica A/H1N1/2009 en un grupo de trabajadores de la salud". La Medicina del Trabajo . 103 (3): 220–29. PMID 22838300.
- ^ "La FDA aprueba la primera vacuna contra la influenza estacional que contiene un adyuvante" (Nota de prensa). Administración de Alimentos y Medicamentos de Estados Unidos (FDA). 24 de noviembre de 2015. Archivado desde el original el 22 de julio de 2017 . Consultado el 20 de agosto de 2017 .
 Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público .
Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público . - ^ ab "Vacuna antigripal con adyuvante". Centros para el Control y la Prevención de Enfermedades (CDC) de EE. UU . . 4 de septiembre de 2019. Archivado desde el original el 2 de diciembre de 2019 . Consultado el 2 de diciembre de 2019 .
 Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público .
Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público . - ^ "Fluad". Administración de Alimentos y Medicamentos de Estados Unidos (FDA). 8 de noviembre de 2019. STN 125510. Archivado desde el original el 2 de diciembre de 2019. Consultado el 2 de diciembre de 2019 .
 Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público .
Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público . - ^ "Vacuna antigripal con adyuvante de escualeno: nueva preparación. No es mejor que los productos disponibles". Prescrire International . 13 (74): 206–08. Diciembre de 2004. PMID 15599987.
- ^ Camilloni B, Basileo M, Valente S, Nunzi E, Iorio AM (2015). "Inmunogenicidad de vacunas antigripales mejoradas administradas intradérmicamente y adyuvadas con MF59 en sujetos mayores de 60 años: una revisión de la literatura". Vacunas humanas e inmunoterapias . 11 (3): 553–63. doi :10.1080/21645515.2015.1011562. PMC 4514405 . PMID 25714138.
- Resumen para legos en: "Actualización de la revisión bibliográfica sobre la eficacia y efectividad de las vacunas antigripales trivalentes inactivadas de dosis alta (Fluzone de dosis alta) y con adyuvante MF59 (Fluad) en adultos de 65 años de edad y mayores". Agencia de Salud Pública de Canadá . 1 de mayo de 2018.
- ^ Van Damme P, Arnou R, Kafeja F, Fiquet A, Richard P, Thomas S, et al. (mayo de 2010). "Evaluación de la no inferioridad de la vacuna intradérmica frente a la vacuna antigripal estacional con adyuvante utilizando dos técnicas serológicas: un estudio comparativo aleatorizado". BMC Infectious Diseases . 10 : 134. doi : 10.1186/1471-2334-10-134 . PMC 2895601 . PMID 20504306.
- ^ Haverkate M, D'Ancona F, Giambi C, Johansen K, Lopalco PL, Cozza V, et al. (Colectivo de puntos de contacto de los guardianes del proyecto VENICE) (mayo de 2012). "Vacunación obligatoria y recomendada en la UE, Islandia y Noruega: resultados de la encuesta VENICE 2010 sobre las formas de implementar los programas nacionales de vacunación". Euro Surveillance . 17 (22). doi : 10.2807/ese.17.22.20183-en . PMID 22687916.
- ^ Field RI (noviembre de 2009). "Vacunación obligatoria de los trabajadores de la salud: ¿qué derechos deberían tener prioridad?". P & T . 34 (11): 615–18. PMC 2810172 . PMID 20140133.
- ^ Kassianos G (2015). "Disposición de los trabajadores sanitarios europeos a vacunarse contra la gripe estacional: situación actual y sugerencias para mejorar". Drugs in Context . 4 : 212268. doi :10.7573/dic.212268. PMC 4316812 . PMID 25657810.
- ^ Thomas RE, Jefferson T, Lasserson TJ (junio de 2016). "Vacunación contra la influenza para trabajadores de la salud que atienden a personas de 60 años o más que viven en instituciones de cuidados a largo plazo". Base de datos Cochrane de revisiones sistemáticas . 2016 (6): CD005187. doi : 10.1002/14651858.CD005187.pub5 . PMC 8504984. PMID 27251461 .
- ^ "Resumen de la decisión sobre medicamentos de venta con receta de Fluad Quad Australian". Administración de Productos Terapéuticos (TGA) . 13 de diciembre de 2019. Archivado desde el original el 8 de marzo de 2020. Consultado el 24 de agosto de 2020 .
- ^ "Fluad Tetra EPAR". Agencia Europea de Medicamentos (EMA) . 24 de marzo de 2020. Archivado desde el original el 1 de agosto de 2020. Consultado el 29 de mayo de 2020 .
- ^ "Información del producto Fluad Tetra". Registro de medicamentos de la Unión . Archivado desde el original el 5 de marzo de 2023. Consultado el 3 de marzo de 2023 .
- ^ Fell DB, Sprague AE, Liu N, Yasseen AS, Wen SW, Smith G, et al. (junio de 2012). "Vacunación contra la influenza H1N1 durante el embarazo y resultados fetales y neonatales". American Journal of Public Health (manuscrito enviado). 102 (6): e33–40. doi :10.2105/AJPH.2011.300606. PMC 3483960. PMID 22515877 .
- ^ Madhi SA, Cutland CL, Kuwanda L, Weinberg A, Hugo A, Jones S, et al. (septiembre de 2014). "Vacunación antigripal de mujeres embarazadas y protección de sus bebés". The New England Journal of Medicine . 371 (10): 918–31. doi :10.1056/NEJMoa1401480. hdl : 2263/42412 . PMID 25184864.
- ^ "Vacuna contra la gripe". CDC . 2020. Archivado desde el original el 2 de diciembre de 2019 . Consultado el 24 de septiembre de 2020 .
- ^ "Conceptos erróneos sobre las vacunas contra la gripe". CDC . 2020. Archivado desde el original el 10 de agosto de 2020 . Consultado el 24 de septiembre de 2020 .
- ^ McNeil Jr DG (1 de octubre de 2018). «Más de 80.000 estadounidenses murieron de gripe el invierno pasado, la cifra más alta en años». The New York Times . Archivado desde el original el 1 de octubre de 2018. Consultado el 24 de junio de 2024 .
- ^ "5 mitos sobre la vacuna antigripal". Organización Mundial de la Salud . Archivado desde el original el 14 de febrero de 2024. Consultado el 24 de junio de 2024 .
- ^ Haber P, Sejvar J, Mikaeloff Y, DeStefano F (2009). "Vacunas y síndrome de Guillain-Barré". Drug Safety . 32 (4): 309–23. doi :10.2165/00002018-200932040-00005. PMID 19388722. S2CID 33670594.
- ^ "Texto reorganizado". JAMA Otolaryngology–Head & Neck Surgery . 141 (5): 428. Mayo de 2015. doi :10.1001/jamaoto.2015.0540. PMID 25996397. S2CID 26612829.
- ^ Stowe J, Andrews N, Wise L, Miller E (febrero de 2009). "Investigación de la asociación temporal del síndrome de Guillain-Barré con la vacuna antigripal y la enfermedad similar a la gripe utilizando la base de datos de investigación de medicina general del Reino Unido". American Journal of Epidemiology . 169 (3): 382–88. doi : 10.1093/aje/kwn310 . PMID 19033158.
- ^ ab Sivadon-Tardy V, Orlikowski D, Porcher R, Sharshar T, Durand MC, Enouf V, et al. (enero de 2009). "Síndrome de Guillain-Barré e infección por el virus de la gripe". Clinical Infectious Diseases . 48 (1): 48–56. doi : 10.1086/594124 . PMID 19025491.
- ^ Vellozzi C, Burwen DR, Dobardzic A, Ball R, Walton K, Haber P (marzo de 2009). "Seguridad de las vacunas antigripales inactivadas trivalentes en adultos: antecedentes para el control de la seguridad de las vacunas antigripales pandémicas". Vaccine . 27 (15): 2114–20. doi :10.1016/j.vaccine.2009.01.125. PMID 19356614. Archivado desde el original el 1 de agosto de 2020 . Consultado el 21 de mayo de 2020 .
- ^ Reinberg S (2 de febrero de 2011). "Estudio revela que la vacuna contra la gripe H1N1 del año pasado fue segura". US News & World Report . Archivado desde el original el 25 de abril de 2013.
- ^ abcd Roberts L (27 de marzo de 2021). "Las primeras vacunas antigripales basadas en células de Australia que se lanzarán esta temporada de gripe". ABC News . Archivado desde el original el 27 de abril de 2021 . Consultado el 28 de abril de 2021 .
- ^ Comité Asesor Nacional sobre Inmunización (NACI) (agosto de 2012). "Declaración sobre la vacuna contra la gripe estacional para 2012-2013" (PDF) . Informe sobre enfermedades transmisibles de Canadá . 38 . Ottawa. Archivado desde el original (PDF) el 17 de enero de 2013 . Consultado el 18 de julio de 2013 .
- ^ Turner PJ, Southern J, Andrews NJ, Miller E, Erlewyn-Lajeunesse M (diciembre de 2015). "Seguridad de la vacuna antigripal viva atenuada en jóvenes con alergia al huevo: estudio de cohorte prospectivo multicéntrico". BMJ . 351 : h6291. doi :10.1136/bmj.h6291. PMC 4673102 . PMID 26645895.
- ^ Greenhawt M (diciembre de 2015). "Vacuna antigripal viva atenuada para niños con alergia al huevo". BMJ . 351 : h6656. doi :10.1136/bmj.h6656. PMID 26657778. S2CID 37037904.
- ^ ab "Novartis recibe la aprobación de la FDA para Flucelvax, la primera vacuna de cultivo celular en EE. UU. que ayuda a proteger contra la gripe estacional" (Nota de prensa). Novartis. 20 de noviembre de 2012. Archivado desde el original el 28 de noviembre de 2012.
- ^ ab "Supemtek EPAR". Agencia Europea de Medicamentos (EMA) . 15 de septiembre de 2020. Archivado desde el original el 10 de enero de 2021. Consultado el 27 de noviembre de 2020 .
- ^ Informe técnico: Narcolepsia asociada a la vacunación contra la gripe pandémica (PDF) . Estocolmo, Suecia: Centro Europeo para la Prevención y el Control de Enfermedades (ECDC). 2012. ISBN 978-92-9193-388-4. Archivado desde el original (PDF) el 31 de diciembre de 2013 . Consultado el 30 de diciembre de 2013 .
- ^ Yong E (2013). "La narcolepsia se confirma como enfermedad autoinmune". Nature . doi :10.1038/nature.2013.14413. S2CID 74850662.
- ^ "El timerosal en la vacuna contra la gripe". Centros para el Control y la Prevención de Enfermedades de EE. UU . . 16 de octubre de 2015. Archivado desde el original el 2 de diciembre de 2019 . Consultado el 2 de diciembre de 2019 .
 Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público .
Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público . - ^ "Thimerosal en las vacunas Thimerosal – Preocupaciones – Seguridad de las vacunas". Centros para el Control y la Prevención de Enfermedades de EE. UU . . 27 de octubre de 2015. Archivado desde el original el 2 de noviembre de 2019 . Consultado el 2 de diciembre de 2019 .
 Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público .
Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público . - ^ Offit PA (septiembre de 2007). "Thimerosal y vacunas: una advertencia". The New England Journal of Medicine . 357 (13): 1278–79. doi : 10.1056/NEJMp078187 . PMID 17898096. S2CID 36318722.
- ^ Comité Asesor Mundial sobre Seguridad de las Vacunas (14 de julio de 2006). «Tiomersal y vacunas». Organización Mundial de la Salud (OMS). Archivado desde el original el 6 de noviembre de 2009. Consultado el 20 de noviembre de 2007 .
- ^ Grande AJ, Reid H, Thomas EE, Nunan D, Foster C (agosto de 2016). "Ejercicio previo a la vacunación antigripal para limitar la incidencia de la gripe y sus complicaciones relacionadas en adultos". Base de datos Cochrane de revisiones sistemáticas . 2016 (8): CD011857. doi :10.1002/14651858.CD011857.pub2. PMC 8504432. PMID 27545762 .
- ^ Plotkin SA, Orenstein WA (1988). Vacunas . Filadelfia: WB Saunders Company. pag. 424.ISBN 978-0-7216-1946-0. Recuperado el 7 de septiembre de 2020 .
- ^ Monografía del producto: Flumist (PDF) , Astrazeneca Canada Inc., 20 de junio de 2014, archivado (PDF) del original el 30 de septiembre de 2020 , consultado el 5 de septiembre de 2020
- ^ "Sistema mundial de vigilancia y respuesta a la gripe (GISRS)". Organización Mundial de la Salud. Archivado desde el original el 3 de octubre de 2011. Consultado el 22 de octubre de 2019 .
- ^ ab Schnirring L (29 de septiembre de 2023). «Los asesores de la OMS recomiendan volver a las vacunas antigripales trivalentes». Centro de Investigación y Políticas sobre Enfermedades Infecciosas . Archivado desde el original el 18 de diciembre de 2023. Consultado el 23 de enero de 2024 .
- ^ "En el punto de mira: la gripe". Organización Mundial de la Salud. Archivado desde el original el 18 de octubre de 2019. Consultado el 22 de octubre de 2019 .
- ^ "Vigilancia mundial de la gripe". OMS . Archivado desde el original el 30 de abril de 2003.
- ^ Organización Mundial de la Salud (2000). Informe de la OMS sobre la vigilancia mundial de las enfermedades infecciosas propensas a epidemias: gripe . Organización Mundial de la Salud (OMS). hdl : 10665/66485 . WHO/CDS/CSR/ISR/2000/1.
- ^ "Recomendaciones de la UE para la composición de la vacuna contra la gripe estacional 2024/2025". Agencia Europea de Medicamentos (EMA) . 26 de marzo de 2024. Archivado desde el original el 28 de marzo de 2024. Consultado el 28 de marzo de 2024 .
- ^ To KW, Lai A, Lee KC, Koh D, Lee SS (octubre de 2016). "Aumento de la cobertura de vacunación antigripal en trabajadores sanitarios: revisión de desafíos y soluciones". The Journal of Hospital Infection . 94 (2): 133–42. doi :10.1016/j.jhin.2016.07.003. PMID 27546456.
- ^ abcd Rubin GJ, Potts HW, Michie S (marzo de 2011). "Probable aceptación de las vacunas contra la gripe porcina y estacional entre los trabajadores sanitarios. Un análisis transversal de los datos de una encuesta telefónica en el Reino Unido". Vaccine . 29 (13): 2421–28. doi :10.1016/j.vaccine.2011.01.035. PMID 21277402.
- ^ "Vacuna contra la gripe estacional". Centros para el Control y la Prevención de Enfermedades (CDC) de EE. UU . . 9 de diciembre de 2019. Archivado desde el original el 2 de diciembre de 2019 . Consultado el 12 de enero de 2020 .
 Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público .
Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público . - ^ "Uso de vacunas". Organización Mundial de la Salud (OMS). Archivado desde el original el 15 de diciembre de 2012. Consultado el 15 de enero de 2017 .
- ^ "Hoja informativa sobre la gripe estacional". Organización Mundial de la Salud (OMS). Noviembre de 2016. Archivado desde el original el 30 de noviembre de 2014. Consultado el 15 de enero de 2017 .
- ^ "Influenza (estacional)". OMS . 6 de noviembre de 2018. Archivado desde el original el 14 de octubre de 2019. Consultado el 14 de octubre de 2019 .
- ^ "Métodos para evaluar la cobertura de vacunación antigripal en grupos destinatarios (2016)". OMS/Europa . 19 de marzo de 2018. Archivado desde el original el 14 de octubre de 2019. Consultado el 14 de octubre de 2019 .
- ^ "Recomendaciones sobre la vacunación antigripal durante la temporada de invierno 2019-2020". OMS/Europa . 24 de septiembre de 2019. Archivado desde el original el 14 de octubre de 2019. Consultado el 14 de octubre de 2019 .
- ^ ab Capítulo sobre la influenza y declaración sobre la vacuna contra la influenza estacional para 2019-2020 de la Guía canadiense de inmunización (PDF) (informe). Agencia de Salud Pública de Canadá. Mayo de 2019. Cat.: HP37-25E-PDF; Pub.: 180883. Archivado (PDF) del original el 16 de julio de 2020 . Consultado el 2 de junio de 2020 .
- ^ "Grupos de riesgo de gripe grave". Centro Europeo para la Prevención y el Control de Enfermedades (ECDC) . 20 de octubre de 2017. Archivado desde el original el 22 de octubre de 2019. Consultado el 22 de octubre de 2019 .
- ^ "ECDC Reviews – New WHO recommendationes on seasonal influenza ..." Centro Europeo para la Prevención y el Control de Enfermedades (ECDC) . Archivado desde el original el 10 de mayo de 2017. Consultado el 25 de diciembre de 2016 .
- ^ "Orientaciones del ECDC: grupos de riesgo prioritarios para la vacunación contra la gripe" (PDF) . Centro Europeo para la Prevención y el Control de Enfermedades (ECDC). pp. 7–8. Archivado desde el original (PDF) el 25 de diciembre de 2016. Consultado el 25 de diciembre de 2016 .
- ^ "Vacuna contra la gripe". nhs.uk . 6 de marzo de 2024.
- ^ "Vacunas privadas contra la gripe | Reservar una cita en la farmacia | Acceso para pacientes" www.patientaccess.com .
- ^ Grohskopf LA, Ferdinands JM, Blanton LH, Broder KR, Loehr J (agosto de 2024). "Prevención y control de la influenza estacional con vacunas: recomendaciones del Comité Asesor sobre Prácticas de Inmunización — Estados Unidos, temporada de influenza 2024-25" (PDF) . MMWR. Recomendaciones e informes . 73 (5): 1–25. doi : 10.15585/mmwr.rr7305a1 . PMID 39197095.
- ^ abc "Los niños y la gripe". Centros para el Control y la Prevención de Enfermedades (CDC) de EE. UU. 23 de octubre de 2019. Archivado desde el original el 11 de noviembre de 2019.
 Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público .
Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público . - ^ Rahman K (21 de octubre de 2021). «Lista completa de vacunas obligatorias por parte del ejército estadounidense». Newsweek . Archivado desde el original el 19 de diciembre de 2023.
- ^ "Vacuna viva atenuada contra la influenza [LAIV] (vacuna contra la influenza en aerosol nasal)". Centros para el Control y la Prevención de Enfermedades (CDC) de EE. UU . . 16 de septiembre de 2019. Archivado desde el original el 14 de octubre de 2019 . Consultado el 14 de octubre de 2019 .
 Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público .
Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público . - ^ "Vacunación contra la influenza: un resumen para médicos y profesionales de la salud: influenza estacional". Centros para el Control y la Prevención de Enfermedades (CDC) de EE. UU. 6 de septiembre de 2018. Archivado desde el original el 24 de febrero de 2008.
 Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público .
Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público . - ^ "Fluzone, Fluzone High-Dose y Fluzone Intradermal". Administración de Alimentos y Medicamentos de Estados Unidos (FDA). 11 de julio de 2017. Archivado desde el original el 22 de julio de 2017. Consultado el 1 de junio de 2020 .
- ^ Couch RB, Winokur P, Brady R, Belshe R, Chen WH, Cate TR, et al. (noviembre de 2007). "Seguridad e inmunogenicidad de una vacuna antigripal trivalente de dosis alta entre sujetos de edad avanzada". Vaccine . 25 (44): 7656–63. doi :10.1016/j.vaccine.2007.08.042. PMC 2243220 . PMID 17913310.
- ^ Lee JK, Lam GK, Shin T, Kim J, Krishnan A, Greenberg DP, et al. (mayo de 2018). "Eficacia y efectividad de la vacunación contra la influenza en dosis alta versus dosis estándar para adultos mayores: una revisión sistemática y metanálisis". Expert Rev Vaccines . 17 (5): 435–443. doi :10.1080/14760584.2018.1471989. PMID 29715054. S2CID 21688517.
- ^ Robertson CA, DiazGranados CA, Decker MD, Chit A, Mercer M, Greenberg DP (diciembre de 2016). "Vacuna antigripal de dosis alta Fluzone". Expert Rev Vaccines . 15 (12): 1495–1505. doi : 10.1080/14760584.2016.1254044 . PMID 27813430.
- ^ Actualización de la revisión de la literatura sobre la eficacia y efectividad de las vacunas antigripales trivalentes inactivadas de dosis alta (Fluzone High-Dose) y con adyuvante MF59 (Fluad) en adultos de 65 años de edad y mayores (PDF) (Informe). Ottawa: Agencia de Salud Pública de Canadá. Mayo de 2018. HP40-210/2018E-PDF. Archivado (PDF) del original el 21 de julio de 2020 . Consultado el 1 de junio de 2020 .
- ^ Tanner L (13 de enero de 2013). "Los hospitales toman medidas drásticas contra los trabajadores que se niegan a recibir la vacuna contra la gripe". NBC News. Archivado desde el original el 3 de diciembre de 2013. Consultado el 24 de julio de 2014 .
- ^ Centros para el Control y la Prevención de Enfermedades (CDC) (diciembre de 2010). "Cobertura de vacunación contra la influenza estacional y la influenza H1N1 2009 entre mujeres embarazadas: 10 estados, temporada de influenza 2009-10" (PDF) . Informe semanal de morbilidad y mortalidad (MMWR) . 59 (47): 1541–45. PMID 21124293. Archivado (PDF) desde el original el 25 de junio de 2017.
 Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público .
Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público . - ^ ab Altman LK (28 de febrero de 2008). "Panel recomienda vacunas contra la gripe para niños de hasta 18 años". The New York Times . Archivado desde el original el 22 de enero de 2015.
- ^ "ACIP vota en contra del uso de LAIV para la temporada de gripe 2016-2017" (Comunicado de prensa). Centros para el Control y la Prevención de Enfermedades (CDC) de EE. UU. 22 de junio de 2016. Archivado desde el original el 25 de noviembre de 2016 . Consultado el 26 de noviembre de 2016 .
 Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público .
Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público . - ^ "Calendarios de vacunación". Centros para el Control y la Prevención de Enfermedades (CDC) de Estados Unidos. Archivado desde el original el 5 de noviembre de 2014. Consultado el 4 de noviembre de 2014 .
 Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público .
Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público . - ^ "Preguntas frecuentes sobre la vacuna contra la gripe". Healthdirect, Departamento de Salud, Gobierno de Australia. 1 de abril de 2019. Archivado desde el original el 29 de mayo de 2019. Consultado el 29 de mayo de 2019 .
- ^ "Hoja informativa sobre la gripe". Healthdirect, Departamento de Salud, Gobierno de Australia. 1 de abril de 2019. Archivado desde el original el 29 de mayo de 2019. Consultado el 29 de mayo de 2019 .
- ^ "Uso de servicios sanitarios – Tasas de vacunación contra la gripe – Datos de la OCDE". theOECD . Archivado desde el original el 8 de agosto de 2020 . Consultado el 24 de abril de 2020 .
- ^ ab Han YK, Michie S, Potts HW, Rubin GJ (marzo de 2016). "Predictores de la aceptación de la vacuna contra la influenza durante la pandemia de influenza A H1N1v (gripe porcina) de 2009/10: resultados de cinco encuestas nacionales en el Reino Unido". Medicina preventiva . 84 : 57–61. doi :10.1016/j.ypmed.2015.12.018. PMC 4766366 . PMID 26757401.
- ^ Bish A, Yardley L, Nicoll A, Michie S (septiembre de 2011). "Factores asociados con la aceptación de la vacunación contra la gripe pandémica: una revisión sistemática". Vaccine . 29 (38): 6472–84. doi :10.1016/j.vaccine.2011.06.107. PMID 21756960.
- ^ Brien S, Kwong JC, Buckeridge DL (febrero de 2012). "Los determinantes de la vacunación contra la gripe pandémica A/H1N1 de 2009: una revisión sistemática". Vacuna . 30 (7): 1255–64. doi :10.1016/j.vaccine.2011.12.089. PMID 22214889.
- ^ Thomas RE, Lorenzetti DL (mayo de 2018). "Intervenciones para aumentar las tasas de vacunación contra la influenza en personas de 60 años o más en la comunidad". Base de datos Cochrane de revisiones sistemáticas . 5 (5): CD005188. doi : 10.1002/14651858.CD005188.pub4 . PMC 6494593. PMID 29845606 .
- ^ Centros para el Control y la Prevención de Enfermedades (CDC) (octubre de 2009). "Actualización sobre las vacunas monovalentes contra la influenza A (H1N1) 2009" (PDF) . Informe semanal de morbilidad y mortalidad (MMWR) . 58 (39): 1100–01. PMID 19816398. Archivado (PDF) desde el original el 29 de junio de 2011.
 Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público .
Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público . - ^ La Torre G, Di Thiene D, Cadeddu C, Ricciardi W, Boccia A (diciembre de 2009). "Comportamientos respecto de las medidas preventivas contra la gripe pandémica H1N1 entre los trabajadores sanitarios italianos, octubre de 2009". Vigilancia del euro . 14 (49). PMID 20003908.
- ^ Amodio E, Anastasi G, Marsala MG, Torregrossa MV, Romano N, Firenze A (febrero de 2011). "Vacunación contra la gripe pandémica A (H1N1) de 2009 entre los trabajadores sanitarios del principal hospital universitario de Sicilia (Italia)". Vaccine . 29 (7): 1408–12. doi :10.1016/j.vaccine.2010.12.041. PMID 21199700.
- ^ Chor JS, Ngai KL, Goggins WB, Wong MC, Wong SY, Lee N, et al. (agosto de 2009). "Disposición de los trabajadores sanitarios de Hong Kong a aceptar la vacunación antigripal prepandémica en diferentes niveles de alerta de la OMS: dos encuestas por cuestionario". BMJ . 339 : b3391. doi :10.1136/bmj.b3391. PMC 2731837 . PMID 19706937.
- ^ Schnirring L (18 de agosto de 2011). «Los CDC actualizan las recomendaciones de vacunación contra la gripe». Centro de Investigación y Políticas sobre Enfermedades Infecciosas (CIDRAP) . Archivado desde el original el 25 de octubre de 2019. Consultado el 24 de octubre de 2019 .
- ^ Centros para el Control y la Prevención de Enfermedades (CDC) (agosto de 2011). "Cobertura de vacunación contra la influenza entre el personal de atención médica – Estados Unidos, temporada de influenza 2010-11" (PDF) . Informe semanal de morbilidad y mortalidad (MMWR) . 60 (32): 1073–77. PMID 21849963. Archivado (PDF) desde el original el 25 de mayo de 2017.
 Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público .
Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público . - ^ Centros para el Control y la Prevención de Enfermedades (CDC) (septiembre de 2012). «Cobertura de vacunación contra la influenza entre el personal de atención médica: temporada de influenza 2011-12, Estados Unidos» (PDF) . Informe semanal de morbilidad y mortalidad (MMWR) . 61 : 753–57. PMID 23013720. Archivado (PDF) del original el 24 de junio de 2017.
 Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público .
Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público . - ^ Bull AL, Bennett N, Pitcher HC, Russo PL, Richards MJ (febrero de 2007). "Cobertura de la vacuna antigripal entre los trabajadores sanitarios de los hospitales públicos de Victoria". The Medical Journal of Australia . 186 (4): 185–86. doi :10.5694/j.1326-5377.2007.tb00858.x. PMID 17309419. S2CID 25091208.
- ^ ab Abbasi J (noviembre de 2019). "La búsqueda de una vacuna universal contra la gripe se intensifica". JAMA . 322 (20): 1942–1944. doi :10.1001/jama.2019.16816. PMID 31693060. S2CID 207903441.
- ^ abc Greenfieldboyce N (8 de noviembre de 2007). Nuevas y antiguas formas de elaborar vacunas contra la gripe (transmisión radial). NPR . Archivado desde el original el 24 de octubre de 2019. Consultado el 23 de octubre de 2019 .
- ^ Nachbagauer R, Krammer F (abril de 2017). "Vacunas universales contra el virus de la influenza y anticuerpos terapéuticos". Microbiología clínica e infecciones . 23 (4): 222–228. doi :10.1016/j.cmi.2017.02.009. PMC 5389886 . PMID 28216325.
- ^ Balfour H (2 de junio de 2021). "Comienza el primer ensayo universal de la vacuna contra la gripe en humanos". European Pharmaceutical Review . Archivado desde el original el 29 de marzo de 2022. Consultado el 6 de febrero de 2022.
El ensayo de fase I (NCT04896086) evaluará la seguridad e inmunogenicidad de la vacuna experimental, FluMos-v1.
- ^ Bernstein DI, Guptill J, Naficy A, Nachbagauer R, Berlanda-Scorza F, Feser J, et al. (enero de 2020). "Inmunogenicidad de candidatos a vacunas universales contra el virus de la influenza basados en hemaglutinina quimérica: resultados provisionales de un ensayo clínico de fase 1 aleatorizado y controlado con placebo". The Lancet. Enfermedades infecciosas . 20 (1): 80–91. doi : 10.1016/S1473-3099(19)30393-7 . PMC 6928577 . PMID 31630990.
- ^ Nachbagauer R, Feser J, Naficy A, Bernstein DI, Guptill J, Walter EB, et al. (enero de 2021). "Un enfoque de vacuna universal contra el virus de la influenza basado en hemaglutinina quimérica induce una inmunidad amplia y duradera en un ensayo de fase I aleatorizado y controlado con placebo". Nature Medicine . 27 (1): 106–114. doi : 10.1038/s41591-020-1118-7 . PMID 33288923.
- ^ "Estrategias de acceso amplio a la vacuna contra la gripe a nivel mundial". Path . Octubre de 2007. Archivado desde el original el 14 de octubre de 2019 . Consultado el 16 de septiembre de 2009 .
- ^ ab "cómo se hace" (PDF) . Archivado desde el original (PDF) el 5 de julio de 2010.
- ^ "Virus y reactivos de la vacuna contra la gripe". Organización Mundial de la Salud (OMS). Archivado desde el original el 27 de mayo de 2013.
- ^ "Recomendaciones para la producción y control de la vacuna antigripal (inactivada)" (PDF) . Organización Mundial de la Salud (OMS). Archivado (PDF) desde el original el 28 de octubre de 2013. Consultado el 27 de mayo de 2013 .
- ^ ab Racaniello V (diciembre de 2009). "Crecimiento del virus de la gripe en huevos". Blog de Virología. Archivado desde el original el 25 de diciembre de 2014.
- ^ Izzat F (abril de 2012). "Cultivo viral en embriones de pollo". Youtube. Archivado desde el original el 26 de mayo de 2015.
- ^ ab "Cómo se elaboran las vacunas contra la influenza (gripe)". Centros para el Control y la Prevención de Enfermedades (CDC) de EE. UU. 26 de noviembre de 2019. Archivado desde el original el 2 de diciembre de 2019 . Consultado el 2 de diciembre de 2019 .
 Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público .
Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público . - ^ Seemann G, Kock M (2008). «Huevos fértiles: un producto valioso para la producción de vacunas». Lohmann Breeders . Archivado desde el original el 23 de noviembre de 2023. Consultado el 19 de octubre de 2023 .
- ^ Bright RA, Carter DM, Daniluk S, Toapanta FR, Ahmad A, Gavrilov V, et al. (mayo de 2007). "Las partículas similares al virus de la gripe provocan respuestas inmunitarias más amplias que el virus de la gripe inactivado con el virión completo o la hemaglutinina recombinante". Vaccine . 25 (19): 3871–78. doi :10.1016/j.vaccine.2007.01.106. PMID 17337102.
- ^ "La preparación con vacuna de ADN hace que la vacuna contra la gripe aviar funcione mejor (NIH News)". 3 de octubre de 2011. Archivado desde el original el 27 de septiembre de 2012.
- ^ Número de ensayo clínico NCT00776711 para la "Vacuna para la prevención de la gripe aviar" en ClinicalTrials.gov
- ^ Número de ensayo clínico NCT01086657 para "Estudio de fase I, aleatorizado y abierto en adultos sanos sobre la seguridad e inmunogenicidad de los intervalos de inmunización primaria y de refuerzo con la vacuna monovalente contra la influenza subunitaria viral (H5N1), A/Indonesia/05/2005 (Sanofi Pasteur, Inc), administrada sola o después de la vacuna de plásmido de ADN recombinante (H5), VRC-AVIDNA036-00-VP (VRC, NIAID)" en ClinicalTrials.gov
- ^ Centro de evaluación e investigación de productos biológicos. "Productos aprobados – Carta de aprobación del 20 de noviembre de 2012 – Flucelvax". Administración de Alimentos y Medicamentos de los Estados Unidos (FDA). Archivado desde el original el 3 de diciembre de 2012.
 Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público .
Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público . - ^ "Seqirus recibe la aprobación de la FDA para la vacuna Flucelvax Quadrivalent (contra la influenza) para personas de cuatro años de edad y mayores" (Comunicado de prensa). Seqirus . 23 de mayo de 2016. Archivado desde el original el 16 de enero de 2017 . Consultado el 15 de enero de 2017 .
- ^ Roos R (14 de octubre de 2019). «La FDA aprueba la primera vacuna contra la gripe cultivada en células de insectos». Centro de Investigación y Políticas sobre Enfermedades Infecciosas (CIDRAP) . Archivado desde el original el 14 de octubre de 2019. Consultado el 14 de octubre de 2019 .
- ^ "Flublok". Administración de Alimentos y Medicamentos de Estados Unidos (FDA). 26 de febrero de 2018. STN 125285. Archivado desde el original el 14 de octubre de 2019. Consultado el 14 de octubre de 2019 .
 Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público .
Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público . - ^ "Flublok Quadrivalent". Administración de Alimentos y Medicamentos de Estados Unidos (FDA). 2 de agosto de 2019. STN 125285. Archivado desde el original el 14 de octubre de 2019. Consultado el 14 de octubre de 2019 .
 Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público .
Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público . - ^ ab «Supemtek: pendiente de decisión de la CE». Agencia Europea de Medicamentos (EMA) . 17 de septiembre de 2020. Archivado desde el original el 23 de septiembre de 2020. Consultado el 21 de septiembre de 2020 .El texto se ha copiado de esta fuente, cuyos derechos de autor pertenecen a la Agencia Europea de Medicamentos. Se autoriza la reproducción siempre que se cite la fuente.
- ^ "Información del producto Supemtek". Registro de medicamentos de la Unión . Archivado desde el original el 5 de marzo de 2023. Consultado el 3 de marzo de 2023 .
- ^ ab Sparrow E, Wood JG, Chadwick C, Newall AT, Torvaldsen S, Moen A, et al. (enero de 2021). "Capacidad de producción mundial de vacunas contra la influenza estacional y pandémica en 2019". Vacuna . 39 (3): 512–520. doi :10.1016/j.vaccine.2020.12.018. PMC 7814984 . PMID 33341308.
- ^ Jit M, Newall AT, Beutels P (abril de 2013). "Cuestiones clave para estimar el impacto y la relación coste-eficacia de las estrategias de vacunación contra la gripe estacional". Vacunas humanas e inmunoterapias . 9 (4): 834–40. doi :10.4161/hv.23637. PMC 3903903 . PMID 23357859.
- ^ Postma MJ, Baltussen RP, Palache AM, Wilschut JC (abril de 2006). "Más evidencia de la favorable relación coste-efectividad de la vacunación antigripal en ancianos". Expert Review of Pharmacoeconomics & Outcomes Research . 6 (2): 215–27. doi :10.1586/14737167.6.2.215. PMID 20528557. S2CID 12765724.
- ^ Newall AT, Kelly H, Harsley S, Scuffham PA (2009). "Rentabilidad de la vacunación contra la gripe en adultos mayores: una revisión crítica de las evaluaciones económicas para el grupo de edad de 50 a 64 años". PharmacoEconomics . 27 (6): 439–50. doi : 10.2165/00019053-200927060-00001 . PMID 19640008. S2CID 20855671.
- ^ Newall AT, Viboud C, Wood JG (junio de 2010). "Mortalidad atribuible a la gripe en australianos mayores de 50 años: una comparación de diferentes enfoques de modelado". Epidemiología e infección . 138 (6): 836–42. doi : 10.1017/S095026880999118X . PMID 19941685. S2CID 29939376.
- ^ Newall AT, Dehollain JP, Creighton P, Beutels P, Wood JG (agosto de 2013). "Comprensión de la relación coste-efectividad de la vacunación contra la gripe en niños: opciones metodológicas y variabilidad estacional". PharmacoEconomics . 31 (8): 693–702. doi : 10.1007/s40273-013-0060-7 . PMID 23645539. S2CID 8616720.
- ^ Newall AT, Scuffham PA (diciembre de 2011). "Incertidumbre y variabilidad en los modelos de coste-efectividad de la gripe". Revista Australiana y Neozelandesa de Salud Pública . 35 (6): 576, respuesta del autor 576–77. doi :10.1111/j.1753-6405.2011.00788.x. PMID 22151168. S2CID 22402257.
- ^ Gatwood J, Meltzer MI, Messonnier M, Ortega-Sanchez IR, Balkrishnan R, Prosser LA (enero de 2012). "Vacunación contra la influenza estacional de adultos sanos en edad laboral: una revisión de evaluaciones económicas". Drugs . 72 (1): 35–48. doi :10.2165/11597310-000000000-00000. PMID 22191794. S2CID 46305863.
- ^ Newall AT, Jit M, Beutels P (agosto de 2012). "Evaluaciones económicas de la vacunación contra la gripe infantil: una revisión crítica". PharmacoEconomics . 30 (8): 647–60. doi : 10.2165/11599130-000000000-00000 . PMID 22788257. S2CID 38289883.
- ^ Newall AT, Wood JG, Oudin N, MacIntyre CR (febrero de 2010). "Relación coste-eficacia de las estrategias de mitigación de la gripe pandémica basadas en fármacos". Enfermedades infecciosas emergentes . 16 (2): 224–30. doi :10.3201/eid1602.090571. PMC 2957998 . PMID 20113551.
- ^ "Proyecto de secuenciación del genoma de la gripe: descripción general". Institutos Nacionales de Salud – Instituto Nacional de Alergias y Enfermedades Infecciosas. Archivado desde el original el 27 de junio de 2011. Consultado el 27 de mayo de 2013 .
- ^ Lampos V, Yom-Tov E, Pebody R, Cox IJ (2015). "Evaluación del impacto de una intervención sanitaria a través de contenido de Internet generado por el usuario" (PDF) . Minería de datos y descubrimiento de conocimiento . 29 (5): 1434–57. doi : 10.1007/s10618-015-0427-9 . S2CID 215415165. Archivado desde el original el 28 de agosto de 2021 . Consultado el 15 de agosto de 2022 .
- ^ Wagner M, Lampos V, Yom-Tov E, Pebody R, Cox IJ (diciembre de 2017). "Estimación del impacto poblacional de un nuevo programa de vacunación pediátrica contra la influenza en Inglaterra mediante el uso de contenido de redes sociales". Revista de investigación médica en Internet . 19 (12): e416. doi : 10.2196/jmir.8184 . PMC 6257312 . PMID 29269339.
- ^ "Infecciones respiratorias agudas (actualización septiembre de 2009)". Organización Mundial de la Salud (OMS). Septiembre de 2009. Archivado desde el original el 29 de septiembre de 2009 . Consultado el 16 de septiembre de 2009 .
- ^ "Tablas sobre los ensayos clínicos de prototipos de vacunas contra la gripe pandémica". Organización Mundial de la Salud (OMS). Julio de 2009. Archivado desde el original el 6 de marzo de 2009. Consultado el 21 de septiembre de 2009 .
- ^ "La FDA aprueba vacunas contra el virus de la influenza H1N1 de 2009" (Comunicado de prensa). 15 de septiembre de 2009. Archivado desde el original el 15 de octubre de 2009 . Consultado el 15 de octubre de 2009 .
 Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público .
Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público . - ^ Keown A (4 de febrero de 2020). «La FDA aprueba Audenz de Seqirus como vacuna contra una posible pandemia de gripe». BioSpace . Archivado desde el original el 5 de febrero de 2020. Consultado el 5 de febrero de 2020 .
- ^ "Audenz". Administración de Alimentos y Medicamentos de Estados Unidos (FDA). 31 de enero de 2020. STN: 125692. Archivado desde el original el 6 de agosto de 2020. Consultado el 5 de febrero de 2020 .
 Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público .
Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público . - ^ ab "Vacuna contra la gripe zoonótica Seqirus EPAR". Agencia Europea de Medicamentos (EMA) . 9 de octubre de 2023. Consultado el 26 de septiembre de 2024 .
- ^ abc Cho A, Wrammert J (abril de 2016). "Implicaciones de los anticuerpos ampliamente neutralizantes en el desarrollo de una vacuna universal contra la gripe". Current Opinion in Virology . 17 : 110–115. doi :10.1016/j.coviro.2016.03.002. PMC 4940123 . PMID 27031684.
- ^ Okuno Y, Isegawa Y, Sasao F, Ueda S (mayo de 1993). "Un epítopo neutralizante común conservado entre las hemaglutininas de las cepas H1 y H2 del virus de la influenza A". Revista de Virología . 67 (5): 2552–2558. doi :10.1128/JVI.67.5.2552-2558.1993. PMC 237575 . PMID 7682624.
- ^ abcd Soema PC, Kompier R, Amorij JP, Kersten GF (agosto de 2015). "Vacunas antigripales actuales y de próxima generación: estrategias de formulación y producción". Revista Europea de Farmacia y Biofarmacia . 94 : 251–263. doi : 10.1016/j.ejpb.2015.05.023 . hdl : 1887/43765 . PMID 26047796.
- ^ Deng L, Cho KJ, Fiers W, Saelens X (febrero de 2015). "Vacunas universales contra la influenza A basadas en M2e". Vacunas . 3 (1): 105–36. doi : 10.3390/vaccines3010105 . PMC 4494237 . PMID 26344949.
- ^ Gottlieb T, Ben-Yedidia T (noviembre de 2014). "Enfoques basados en epítopos para una vacuna universal contra la influenza". Journal of Autoimmunity . 54 : 15–20. doi :10.1016/j.jaut.2014.07.005. PMID 25172355.
- ^ Toussi DN, Massari P (abril de 2014). "Efecto adyuvante inmunológico de ligandos de receptores tipo Toll definidos molecularmente". Vacunas . 2 (2): 323–53. doi : 10.3390/vaccines2020323 . PMC 4494261 . PMID 26344622.
- ^ Sederstrom J (19 de julio de 2019). "Investigadores exploran la vacuna oral contra la gripe y las opciones de tratamiento". Drug Topics. Archivado desde el original el 8 de junio de 2020. Consultado el 27 de enero de 2020 .
- ^ Jasty M, Bragdon CR, Schutzer S, Rubash H, Haire T, Harris WH (diciembre de 1989). "Crecimiento óseo en prótesis totales de cadera caninas recubiertas porosas. Cuantificación mediante microscopía electrónica de barrido retrodispersada y análisis de imágenes". Scanning Microscopy . 3 (4): 1051–6, discusión 1056–57. doi :10.1016/s1473-3099(15)00252-2. PMID 2633331.
- ^ Liebowitz D, Gottlieb K, Kolhatkar NS, Garg SJ, Asher JM, Nazareno J, et al. (abril de 2020). "Eficacia, inmunogenicidad y seguridad de una vacuna oral contra la influenza: un estudio de desafío en humanos de fase 2 controlado con placebo y controlado con principio activo". The Lancet. Enfermedades infecciosas . 20 (4). Elsevier: 435–444. doi :10.1016/S1473-3099(19)30584-5. PMID 31978354. S2CID 210892802.
- ^ Triggle N (8 de octubre de 2021). "La vacuna contra la gripe es vital este invierno junto con la vacuna contra la COVID". BBC News . Archivado desde el original el 14 de noviembre de 2021. Consultado el 13 de agosto de 2022 .
- ^ Callaway E (16 de mayo de 2022). "La vacuna contra la gripe podría reducir el riesgo de COVID". Nature . 605 (7911): 602. Bibcode :2022Natur.605..602C. doi : 10.1038/d41586-022-01315-9 . PMID 35581411. S2CID 248859545.
- ^ Brownlee S (1 de noviembre de 2009). "¿Importa la vacuna?". The Atlantic . Archivado desde el original el 9 de diciembre de 2014. Consultado el 8 de diciembre de 2014 .
- ^ Rabin RC (5 de noviembre de 2012). "Reevaluación de las vacunas contra la gripe a medida que se acerca la temporada". The New York Times . Archivado desde el original el 10 de noviembre de 2016. Consultado el 30 de diciembre de 2016 .
"Hemos promocionado y promocionado excesivamente esta vacuna", dijo Michael T. Osterholm, director del Centro de Investigación y Política de Enfermedades Infecciosas, así como de su Centro de Excelencia para la Investigación y Vigilancia de la Gripe. "No protege como se promociona. Es todo un trabajo de ventas: todo es relaciones públicas".
- ^ Informe sobre la gripe (libro en línea) Archivado el 10 de mayo de 2016 en Wayback Machine capítulo Gripe aviar por Timm C. Harder y Ortrud Werner
- ^ equiflunet_vaccines Archivado el 10 de enero de 2006 en Wayback Machine.
- ^ "Federación Ecuestre y de Carreras de los EAU". 22 de marzo de 2005. Archivado desde el original el 22 de marzo de 2005.
- ^ "Directrices de la FEI" (PDF) . Archivado (PDF) del original el 26 de octubre de 2007.
- ^ «Vacunación de las aves de corral contra la gripe aviar altamente patógena: vacunas disponibles y estrategias de vacunación». efsa.europa.eu . 10 de octubre de 2023 . Consultado el 9 de mayo de 2024 .
- ^ "Elaboración de un virus candidato a vacuna (CVV) para un virus de influenza aviar de alta patogenicidad (HPAI)". Centros para el Control y la Prevención de Enfermedades (CDC) de EE. UU . . 3 de junio de 2024 . Consultado el 15 de junio de 2024 .
- ^ "El virus de la gripe porcina se vuelve endémico". 15 de septiembre de 2007. Archivado desde el original el 29 de abril de 2009.
- ^ "Vacunas personalizadas: porcinas". Archivado desde el original el 30 de abril de 2009.
- ^ Karaca K, Dubovi EJ, Siger L, Robles A, Audonnet JC, Jiansheng Y, et al. (febrero de 2007). "Evaluación de la capacidad de las vacunas contra el virus de la influenza equina con vectores de viruela del canario para inducir respuestas inmunitarias humorales contra los virus de la influenza canina en perros". American Journal of Veterinary Research . 68 (2): 208–12. doi :10.2460/ajvr.68.2.208. PMID 17269888.
Lectura adicional
- Serie Bases inmunológicas de la inmunización: módulo 23: vacunas contra la gripe . Organización Mundial de la Salud (OMS). Octubre de 2017. hdl : 10665/259211 . ISBN 978-92-4-151305-0.
- Ramsay M, ed. (21 de enero de 2021). «Capítulo 19: Influenza». Inmunización contra enfermedades infecciosas. Public Health England. Archivado desde el original el 12 de noviembre de 2019. Consultado el 24 de octubre de 2019 .
- Hall E, Wodi AP, Hamborsky J, Morelli V, Schillie S, eds. (2021). "Capítulo 12: Influenza". Epidemiología y prevención de enfermedades prevenibles mediante vacunación (14.ª ed.). Washington DC: Centros para el Control y la Prevención de Enfermedades (CDC) de EE. UU. Archivado desde el original el 30 de diciembre de 2016. Consultado el 24 de octubre de 2019 .
- Budd A, Blanton L, Grohskopf L, Campbell A, Dugan V, Wentworth DE, et al. (29 de marzo de 2019). "Capítulo 6: Influenza". En Roush SW, Baldy LM, Hall MA (eds.). Manual para la vigilancia de enfermedades prevenibles mediante vacunación. Atlanta GA: Centros para el Control y la Prevención de Enfermedades (CDC) de EE. UU. Archivado desde el original el 1 de agosto de 2020. Consultado el 24 de octubre de 2019 .
- Comité Asesor Nacional sobre Inmunización (mayo de 2020). «Capítulo sobre la influenza y declaración sobre la vacuna contra la influenza estacional para 2020-2021 de la Guía canadiense de inmunización» (PDF) . Agencia de Salud Pública de Canadá . Cat.: HP37-25F-PDF; Pub.: 200003. Archivado (PDF) del original el 3 de agosto de 2020. Consultado el 2 de junio de 2020 .
- Resumen para legos en: Young K, Gemmill I, Harrison R, et al. (Comité Asesor Nacional sobre Inmunización) (7 de mayo de 2020). "Resumen de la Declaración del Comité Asesor Nacional sobre Inmunización sobre la Vacunación contra la Gripe Estacional para 2020-2021". Informe sobre enfermedades transmisibles de Canadá . Vol. 46, núm. 5.
- Comité Asesor Nacional sobre Inmunización (NACI) (mayo de 2018). Revisión de la literatura del NACI sobre la eficacia comparativa y la inmunogenicidad de las vacunas antigripales inactivadas con virus de subunidades y de virus fraccionados en adultos de 65 años de edad y mayores (PDF) . Gobierno de Canadá. ISBN 978-0-660-26438-7Cat.: HP40-213/2018E-PDF; Pub.: 180039. Archivado (PDF) desde el original el 18 de julio de 2020 . Consultado el 12 de enero de 2020 .
- Resumen para legos en: Gemmill I, Young K, et al. (Comité Asesor Nacional sobre Inmunización) (7 de junio de 2018). "Resumen de la revisión bibliográfica del NACI sobre la eficacia comparativa de las vacunas antigripales inactivadas con virus de subunidades y de virus fraccionados en adultos mayores". Informe sobre enfermedades transmisibles de Canadá . Vol. 44, núm. 6.
- Rajaram S, Wojcik R, Moore C, Ortiz de Lejarazu R, de Lusignan S, Montomoli E, et al. (agosto de 2020). "El impacto del virus de influenza candidato y la fabricación a partir de huevos en la efectividad de la vacuna: revisión de la literatura y consenso de expertos". Vaccine . 38 (38): 6047–6056. doi : 10.1016/j.vaccine.2020.06.021 . PMID 32600916.
Enlaces externos
- Declaración informativa sobre la vacuna antigripal inactivada, Centros para el Control y la Prevención de Enfermedades (CDC) de EE. UU.
- Declaración informativa sobre la vacuna antigripal intranasal viva, Centros para el Control y la Prevención de Enfermedades (CDC) de EE. UU.
- Vacunación contra la influenza estacional y enfermedades prevenibles, Centros para el Control y la Prevención de Enfermedades (CDC) de EE. UU.
- Conceptos erróneos sobre la gripe estacional y las vacunas contra la gripe, Centros para el Control y la Prevención de Enfermedades (CDC) de EE. UU.
- Vacunas contra la gripe en los encabezados de temas médicos (MeSH) de la Biblioteca Nacional de Medicina de EE. UU.


