Ciclosporina
 | |
 | |
| Datos clínicos | |
|---|---|
| Pronunciación | / ˌ s aɪ k l ə ˈ s p ɔːr ɪ n / [1] |
| Nombres comerciales | Neoral, Sandimmune, Restasis, Gengraf, otros |
| Otros nombres | ciclosporina, ciclosporina A, [2] ciclosporina A, ciclosporina A (CsA), ciclosporina ( USAN US ) |
| AHFS / Drogas.com | Monografía |
| MedlinePlus | a601207 |
| Datos de licencia |
|
Categoría de embarazo |
|
| Vías de administración | Oral , intravenosa (IV), gotas para los ojos |
| Clase de droga | Inhibidor de la calcineurina |
| Código ATC | |
| Estatus legal | |
| Estatus legal |
|
| Datos farmacocinéticos | |
| Biodisponibilidad | variable |
| Metabolismo | CYP3A4 del hígado |
| Vida media de eliminación | variable (aproximadamente 24 horas) |
| Excreción | Conducto biliar |
| Identificadores | |
| |
| Número CAS | |
| Identificador de centro de PubChem |
|
| Unión Internacional para la Investigación y el Desarrollo (IUPHAR)/BPS |
|
| Banco de medicamentos | |
| Araña química | |
| UNIVERSIDAD |
|
| BARRIL | |
| EBICh |
|
| Química biológica | |
| Ligando PDB |
|
| Panel de control CompTox ( EPA ) |
|
| Tarjeta informativa de la ECHA | 100.119.569 |
| Datos químicos y físicos | |
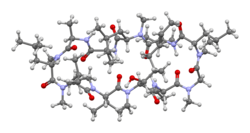
| Fórmula | C62H111N11O12 |
| Masa molar | 1 202,635 g · mol −1 |
| Modelo 3D ( JSmol ) |
|
| |
| |
 norte norte Y (¿que es esto?) (verificar) Y (¿que es esto?) (verificar) | |
La ciclosporina , también escrita ciclosporina y ciclosporina , es un inhibidor de la calcineurina , utilizado como medicamento inmunosupresor . Se toma por vía oral o intravenosa para la artritis reumatoide , la psoriasis , la enfermedad de Crohn , el síndrome nefrótico , el eczema y en los trasplantes de órganos para prevenir el rechazo . [14] [15] También se utiliza como gotas para los ojos para la queratoconjuntivitis seca (ojos secos). [16]
Los efectos secundarios comunes incluyen presión arterial alta, dolor de cabeza, problemas renales , aumento del crecimiento del cabello y vómitos. [15] Otros efectos secundarios graves incluyen un mayor riesgo de infección, problemas hepáticos y un mayor riesgo de linfoma . [15] Se deben controlar los niveles sanguíneos del medicamento para disminuir el riesgo de efectos secundarios. [15] El uso durante el embarazo puede provocar un parto prematuro ; sin embargo, la ciclosporina no parece causar defectos de nacimiento . [17]
Se cree que la ciclosporina actúa disminuyendo la función de los linfocitos . [15] Lo hace formando un complejo con la ciclofilina para bloquear la actividad de la fosfatasa de la calcineurina , que a su vez disminuye la producción de citocinas inflamatorias por parte de los linfocitos T. [18]
La ciclosporina se aisló en 1971 del hongo Tolypocladium inflatum y entró en uso médico en 1983. [19] Está en la Lista de Medicamentos Esenciales de la Organización Mundial de la Salud . [20] [21] En 2021, fue el medicamento número 175 más recetado en los Estados Unidos, con más de 2 millones de recetas. [22] [23] Está disponible como medicamento genérico . [24]
Usos médicos
La ciclosporina está indicada para tratar y prevenir la enfermedad de injerto contra huésped en el trasplante de médula ósea y para prevenir el rechazo de trasplantes de riñón , corazón e hígado . [8] [7] También está aprobada en los EE. UU. para el tratamiento de la artritis reumatoide y la psoriasis , la queratitis numular persistente después de la queratoconjuntivitis adenoviral , [25] [7] y como gotas para los ojos para tratar los ojos secos causados por el síndrome de Sjögren y la disfunción de las glándulas de Meibomio . [9]
Además de estas indicaciones, la ciclosporina también se utiliza en la dermatitis atópica grave , [26] Se ha utilizado en la artritis reumatoide grave y enfermedades relacionadas. [27]
La ciclosporina también se ha utilizado en personas con colitis ulcerosa aguda grave y urticaria que no responden al tratamiento con esteroides . [28]
Efectos secundarios
Los efectos secundarios de la ciclosporina pueden incluir agrandamiento de las encías , aumento del crecimiento del cabello, convulsiones , úlceras pépticas , pancreatitis , fiebre , vómitos , diarrea , confusión , aumento del colesterol , dificultad para respirar , entumecimiento y hormigueo (particularmente en los labios), picazón , presión arterial alta , retención de potasio (que posiblemente lleve a hipercalemia ), disfunción renal y hepática , [29] sensación de ardor en las puntas de los dedos y una mayor vulnerabilidad a infecciones fúngicas y virales oportunistas . La ciclosporina causa hipertensión al inducir vasoconstricción en los riñones y aumentar la reabsorción de sodio. El aumento de la presión arterial puede causar eventos cardiovasculares; por lo tanto, se recomienda que se utilice la dosis efectiva más baja para las personas que requieren un tratamiento a largo plazo. [30]
El uso de ciclosporina después de un trasplante de riñón se asocia con un aumento de los niveles de ácido úrico en la sangre y, en algunos casos, gota . [31]
La ciclosporina está catalogada como carcinógeno del Grupo 1 por la IARC (es decir, hay evidencia suficiente de carcinogenicidad en humanos), [32] provocando específicamente cáncer de piel de células escamosas y linfoma no Hodgkin . [33]
Farmacología
Mecanismo de acción
El principal efecto de la ciclosporina es reducir la actividad de las células T ; lo hace inhibiendo la calcineurina en la vía de la calcineurina-fosfatasa y evitando que se abra el poro de transición de permeabilidad mitocondrial. La ciclosporina se une a la proteína citosólica ciclofilina (inmunofilina) de los linfocitos , especialmente de las células T. Este complejo ciclosporina-ciclofilina inhibe la calcineurina , que normalmente es responsable de activar la transcripción de la interleucina 2. En las células T, la activación del receptor de células T normalmente aumenta el calcio intracelular, que actúa a través de la calmodulina para activar la calcineurina. Luego, la calcineurina desfosforila el factor de transcripción NF-AT (factor nuclear de células T activadas), que se mueve al núcleo de la célula T y aumenta la transcripción de genes para IL-2 y citocinas relacionadas. [18] La ciclosporina, al prevenir la desfosforilación de NF-AT, conduce a una reducción de la función de las células T efectoras ; [34] [35] [36] [37] no afecta la actividad citostática . [ cita médica necesaria ]
La ciclosporina también se une a la proteína ciclofilina D que constituye parte del poro de transición de permeabilidad mitocondrial (MPTP), [35] [38] impidiendo así la apertura del MPTP. El MPTP se encuentra en la membrana mitocondrial de las células del músculo cardíaco. La apertura del MPTP significa un cambio repentino en la permeabilidad de la membrana mitocondrial interna, permitiendo que los protones y otros iones y solutos de un tamaño de hasta ~1,5 kDa pasen a través de la membrana interna. Este cambio de permeabilidad se considera una catástrofe celular, [39] [40] que conduce a la muerte celular. Sin embargo, las breves aperturas del poro de transición de permeabilidad mitocondrial desempeñan un papel fisiológico esencial en el mantenimiento de la homeostasis mitocondrial saludable. [41]
La ciclosporina puede inducir una remisión de la proteinuria causada por enfermedades como la enfermedad de masa muscular y la glomerulonefritis esclerosante focal y segmentaria. [42] La ciclosporina bloquea la desfosforilación mediada por calcineurina de la sinaptopodina, un regulador de las GTPasas Rho en los podocitos, preservando así la interacción sinaptopodina-14-3-3 beta dependiente de la fosforilación. La preservación de esta interacción, a su vez, protege a la sinaptopodina de la degradación mediada por la catepsina L. En conjunto, el efecto antiproteinúrico de la ciclosporina resulta, al menos en parte, del mantenimiento de la abundancia de la proteína sinaptopodina en los podocitos, que, a su vez, es suficiente para mantener la integridad de la barrera de filtración glomerular y proteger contra la proteinuria. [43]
Farmacocinética
La ciclosporina es un péptido cíclico de 11 aminoácidos ; contiene un solo aminoácido D , que rara vez se encuentra en la naturaleza. A diferencia de la mayoría de los péptidos, la ciclosporina no se sintetiza en los ribosomas. [44]
La ciclosporina se metaboliza en gran medida en humanos y animales después de su ingestión. Los metabolitos, que incluyen ciclosporina B, C, D, E, H y L, [45] tienen menos del 10% de la actividad inmunosupresora de la ciclosporina y están asociados con una mayor toxicidad renal. [46]
Biosíntesis
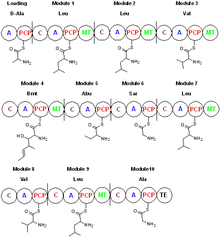
La ciclosporina es sintetizada por una sintetasa de péptidos no ribosómico , la ciclosporina sintetasa. [47] La enzima contiene un dominio de adenilación , un dominio de tiolación , un dominio de condensación y un dominio de N-metiltransferasa . El dominio de adenilación es responsable del reconocimiento y activación del sustrato, mientras que el dominio de tiolación une covalentemente los aminoácidos adenilados a la fosfopanteteína y el dominio de condensación alarga la cadena peptídica. Los sustratos de la ciclosporina sintetasa incluyen L- valina , L- leucina , L- alanina , glicina , ácido 2-aminobutírico , 4-metil treonina y D-alanina , que es el aminoácido inicial en el proceso biosintético. [48] Con el dominio de adenilación, la ciclosporina sintetasa genera los aminoácidos acil-adenilados, luego une covalentemente el aminoácido a la fosfopanteteína a través de un enlace tioéster . Algunos de los sustratos de aminoácidos se N-metilan por la S-adenosil metionina . El paso de ciclización libera la ciclosporina de la enzima . [49] Los aminoácidos como D-Ala y butenil-metil-L-treonina (Bmt) indican que la ciclosporina sintetasa requiere la acción de otras enzimas. La racemización de L-Ala a D-Ala por la alanina racemasa depende del fosfato de piridoxal . La formación de butenil-metil-L-treonina la realiza una policétido sintasa Bmt que utiliza acetato/malonato como material de partida. [50]
Grupo de genes
Tolypocladium inflatum , la especie que se utiliza actualmente para la producción masiva de ciclosporina, tiene los genes biosintéticos organizados en un grupo de 12 genes. De estos 12 genes, SimA ( Q09164 ) es la ciclosporina sintetasa, SimB ( CAA02484.1 ) es la alanina racemasa y SimG (similar a ATQ39432.1 ) es la policétido sintasa. [51] Estos genes están asociados con un retrotransposón activo. [52] Aunque estas secuencias están mal anotadas en GenBank y otras bases de datos, se pueden encontrar secuencias 90% similares para Beauveria felina (o Amphichorda ~ ) productora de ciclosporina . [53] SimB tiene dos parálogos en el mismo organismo con funciones diferentes pero superpuestas gracias a su baja especificidad. [54]
Historia
En 1970, empleados de Sandoz (ahora Novartis ) en Basilea , Suiza , aislaron nuevas cepas de hongos a partir de muestras de suelo tomadas en Noruega y Wisconsin (Estados Unidos) . Ambas cepas producían una familia de productos naturales llamados ciclosporinas. Se aislaron dos componentes relacionados que tenían actividad antifúngica a partir de extractos de estos hongos. La cepa noruega, Tolypocladium inflatum Gams , se utilizó más tarde para la fermentación a gran escala de ciclosporina. [55]
El efecto inmunosupresor del producto natural ciclosporina fue descubierto el 31 de enero de 1972 [56] en una prueba de detección de la supresión inmunitaria diseñada e implementada por Hartmann F. Stähelin en Sandoz. [57] [55] La estructura química de la ciclosporina se determinó en 1976, también en Sandoz. [58] [59] El éxito del fármaco candidato ciclosporina en la prevención del rechazo de órganos fue demostrado en trasplantes de riñón por RY Calne y colegas en la Universidad de Cambridge, [60] y en trasplantes de hígado realizados por Thomas Starzl en el Hospital Infantil de Pittsburgh . El primer paciente, el 9 de marzo de 1980, fue una mujer de 28 años. [61] En los Estados Unidos, la Administración de Alimentos y Medicamentos (FDA) aprobó la ciclosporina para uso clínico en 1983. [62] [63] [64] [65]
Las memorias de Thomas Starzl de 1992 explican, a través de los ojos de un cirujano de trasplantes, que la ciclosporina fue un fármaco que marcó una época en el alotrasplante de órganos sólidos. [66] Amplió enormemente la aplicabilidad clínica de dicho trasplante al avanzar sustancialmente el componente farmacoterapéutico antirrechazo. [66] En pocas palabras, los mayores límites para aplicar dicho trasplante de manera más amplia no eran el costo ni la habilidad quirúrgica (por formidables que sean), sino más bien el problema del rechazo del aloinjerto y la escasez de órganos de donantes. La ciclosporina fue un avance importante contra la parte del desafío relacionada con el rechazo. [66]
Sociedad y cultura
Estatus legal
En julio de 2024, el Comité de Medicamentos de Uso Humano (CHMP) de la Agencia Europea de Medicamentos adoptó un dictamen positivo, recomendando la concesión de una autorización de comercialización para el medicamento Vevizye, destinado al tratamiento de la enfermedad del ojo seco. [12] El solicitante de este medicamento es Novaliq GmbH. [12] Vevizye fue autorizado para uso médico en la Unión Europea en septiembre de 2024. [12]
Nombres
Los científicos de habla alemana que primero lo aislaron llamaron ciclosporina al producto natural [55] y ciclosporina cuando se tradujo al inglés. Según las pautas de denominación común internacional (DCI) para medicamentos, [67] la y se reemplazó por i para que la DCI del medicamento se escriba ciclosporina. [ cita requerida ]
La ciclosporina es el DCI y el nombre aprobado británico (BAN), mientras que la ciclosporina es el nombre adoptado en los Estados Unidos (USAN) y la ciclosporina es un antiguo BAN. [68]
Formularios disponibles
La ciclosporina presenta una solubilidad muy baja en agua y, como consecuencia, se han desarrollado formas de suspensión y emulsión del medicamento para administración oral e inyección. La ciclosporina fue comercializada originalmente por Sandoz (ahora Novartis ), bajo la marca Sandimmune, que está disponible como cápsulas de gelatina blanda, una solución oral y una formulación para administración intravenosa. Todas estas son composiciones no acuosas. [8] Una microemulsión más nueva , [69] formulación administrada por vía oral, Neoral, [7] está disponible como una solución y como cápsulas de gelatina blanda. Las composiciones de Neoral están diseñadas para formar microemulsiones en contacto con el agua. [70] [71]
Las preparaciones genéricas de ciclosporina se han comercializado bajo varias marcas comerciales, entre ellas Cicloral (de Sandoz/Hexal), Gengraf (de Abbott ) y Deximune (de Dexcel Pharma). Desde 2002, una emulsión tópica de ciclosporina para tratar la inflamación causada por la queratoconjuntivitis seca (síndrome del ojo seco) se ha comercializado bajo la marca Restasis. [9] Ikervis es una formulación similar con una concentración del 0,1%. [72] Las formulaciones de ciclosporina inhalada están en desarrollo clínico e incluyen una solución en propilenglicol y dispersiones de liposomas . [73] [74]
Investigación
Neuroprotección
La ciclosporina se encuentra en un estudio clínico de fase II/III (adaptativo) en Europa para determinar su capacidad para mejorar el daño celular neuronal y la lesión por reperfusión (fase III) en la lesión cerebral traumática. Este estudio multicéntrico está siendo organizado por NeuroVive Pharma y el Consorcio Europeo de Lesiones Cerebrales utilizando la formulación de ciclosporina de NeuroVive llamada Neurostat (también conocida por su nombre comercial cardioprotector de Ciclomulsión). Esta formulación utiliza una base de emulsión lipídica en lugar de cremophor y etanol. [75] NeuroSTAT se comparó con Sandimmune en un estudio de fase I y se encontró que era bioequivalente. En este estudio, NeuroSTAT no exhibió las reacciones anafilácticas y de hipersensibilidad encontradas en los productos basados en cremophor y etanol. [76]
La ciclosporina se ha investigado como un posible agente neuroprotector en condiciones como la lesión cerebral traumática , y se ha demostrado en experimentos con animales que reduce el daño cerebral asociado con la lesión. [77] La ciclosporina bloquea la formación del poro de transición de permeabilidad mitocondrial , que se ha descubierto que causa gran parte del daño asociado con la lesión en la cabeza y las enfermedades neurodegenerativas . Las propiedades neuroprotectoras de la ciclosporina se descubrieron por primera vez a principios de la década de 1990 cuando dos investigadores (Eskil Elmér y Hiroyuki Uchino) estaban realizando experimentos en trasplante de células. Un hallazgo imprevisto fue que la ciclosporina A era fuertemente neuroprotectora cuando cruzaba la barrera hematoencefálica. [78] Este mismo proceso de destrucción mitocondrial a través de la apertura del poro MPT está implicado en hacer que las lesiones cerebrales traumáticas sean mucho peores. [79]
Enfermedad cardíaca
La ciclosporina se ha utilizado experimentalmente para tratar la hipertrofia cardíaca [35] [80] (un aumento del volumen celular).
La apertura inadecuada del poro de transición de permeabilidad mitocondrial (MPTP) se manifiesta en la isquemia [35] (restricción del flujo sanguíneo al tejido) y la lesión por reperfusión [35] (daño que ocurre después de la isquemia cuando el flujo sanguíneo regresa al tejido), después del infarto de miocardio [36] (ataque cardíaco) y cuando ocurren mutaciones en la ADN polimerasa mitocondrial. [35] El corazón intenta compensar el estado de enfermedad aumentando el Ca intracelular.2+
para aumentar las tasas de ciclos de contractilidad. [38] Niveles constitutivamente altos de Ca mitocondrial2+
provocar una apertura inadecuada del MPTP que conduce a una disminución del rango de función cardíaca, lo que lleva a una hipertrofia cardíaca como un intento de compensar el problema. [38] [36]
Se ha demostrado que la ciclosporina A disminuye la hipertrofia cardíaca al afectar a los miocitos cardíacos de muchas maneras. La ciclosporina A se une a la ciclofilina D para bloquear la apertura del MPTP y, por lo tanto, disminuye la liberación de la proteína citocromo C, que puede causar muerte celular programada. [35] [38] [81] CypD es una proteína dentro del MPTP que actúa como una puerta; la unión de la ciclosporina A disminuye la cantidad de apertura inapropiada del MPTP, lo que disminuye el calcio intramitocondrial .2+
. [38] Disminución del calcio intramitocondrial2+
permite la reversión de la hipertrofia cardíaca causada en la respuesta cardíaca original. [38] La disminución de la liberación de citocromo C provocó una disminución de la muerte celular durante lesiones y enfermedades. [35] La ciclosporina A también inhibe la vía de la calcineurina de la fosfatasa (14). [35] [36] [82] Se ha demostrado que la inhibición de esta vía disminuye la hipertrofia miocárdica. [36] [80] [82]
Uso veterinario
El medicamento está aprobado en los Estados Unidos para el tratamiento de la dermatitis atópica en perros. [83] A diferencia de la forma humana del medicamento, las dosis más bajas utilizadas en perros significan que el fármaco actúa como un inmunomodulador y tiene menos efectos secundarios que en los humanos. Los beneficios de usar este producto incluyen la menor necesidad de terapias concurrentes para controlar la afección. Está disponible como ungüento oftálmico para perros llamado Optimmune , fabricado por Intervet , que es parte de Merck . También se usa para tratar la adenitis sebácea (respuesta inmunitaria contra las glándulas sebáceas ), el pénfigo foliáceo (enfermedad cutánea ampollosa autoinmune), la enfermedad inflamatoria intestinal , la furunculosis anal (enfermedad inflamatoria anal) y la miastenia gravis (una enfermedad neuromuscular). [83] [84]
Referencias
- ^ "ciclosporina". Dictionary.com Unabridged . Random House . nd Archivado desde el original el 18 de noviembre de 2010 . Consultado el 13 de julio de 2011 .
- ^ Laupacis A, Keown PA, Ulan RA, McKenzie N, Stiller CR (mayo de 1982). "Ciclosporina A: un potente inmunosupresor". Revista de la Asociación Médica Canadiense . 126 (9): 1041–6. PMC 1863293 . PMID 7074504.
- ^ "Lista de todos los medicamentos con advertencias de recuadro negro obtenida por la FDA (use los enlaces Descargar resultados completos y Ver consulta)". nctr-crs.fda.gov . FDA . Consultado el 22 de octubre de 2023 .
- ^ "Resumen de la decisión regulatoria para Restasis Multidosis". Registro de Medicamentos y Productos Sanitarios . 23 de octubre de 2014. Archivado desde el original el 7 de junio de 2022. Consultado el 7 de junio de 2022 .
- ^ "Resumen de la decisión regulatoria para Verkazia". Registro de Medicamentos y Productos Sanitarios . 23 de octubre de 2014. Archivado desde el original el 7 de junio de 2022. Consultado el 7 de junio de 2022 .
- ^ "Aspectos destacados de los productos sanitarios en 2021: Anexos de productos aprobados en 2021". Health Canada . 3 de agosto de 2022 . Consultado el 25 de marzo de 2024 .
- ^ abcd "Cápsula de Neoral-ciclosporina, solución de Neoral-ciclosporina rellena de líquido". DailyMed . Archivado desde el original el 5 de julio de 2013 . Consultado el 3 de febrero de 2022 .
- ^ abc "Sandimmune- cápsula de ciclosporina, relleno de líquido Sandimmune- inyección de ciclosporina Sandimmune- solución de ciclosporina". DailyMed . Archivado desde el original el 21 de abril de 2014 . Consultado el 3 de febrero de 2022 .
- ^ abc "Restasis-emulsión de ciclosporina". DailyMed . Archivado desde el original el 30 de marzo de 2014 . Consultado el 3 de febrero de 2022 .
- ^ "Vevye - solución oftálmica de ciclosporina en gotas". DailyMed . 26 de mayo de 2023. Archivado desde el original el 29 de agosto de 2023 . Consultado el 29 de agosto de 2023 .
- ^ "Ikervis". Agencia Europea de Medicamentos . 17 de septiembre de 2018. Archivado desde el original el 13 de agosto de 2022. Consultado el 27 de febrero de 2023 .
- ^ abcd «Vevizye EPAR». Agencia Europea de Medicamentos . 25 de julio de 2024. Consultado el 27 de julio de 2024 .El texto se ha copiado de esta fuente, cuyos derechos de autor pertenecen a la Agencia Europea de Medicamentos. Se autoriza la reproducción siempre que se cite la fuente.
- ^ "Vevizye PI". Registro de medicamentos de la Unión . 23 de septiembre de 2024. Consultado el 27 de septiembre de 2024 .
- ^ Organización Mundial de la Salud (2009). Stuart MC, Kouimtzi M, Hill SR (eds.). Formulario Modelo de la OMS 2008. Organización Mundial de la Salud. pág. 221. hdl : 10665/44053 . ISBN. 9789241547659.
- ^ abcde «Ciclosporina». Sociedad Estadounidense de Farmacéuticos de Sistemas de Salud. Archivado desde el original el 17 de octubre de 2016. Consultado el 8 de diciembre de 2016 .
- ^ "Efecto de ciclosporina". Sociedad Estadounidense de Farmacéuticos de Sistemas de Salud. Archivado desde el original el 13 de enero de 2016. Consultado el 8 de diciembre de 2016 .
- ^ "Uso de ciclosporina durante el embarazo". Drugs.com . Archivado desde el original el 14 de septiembre de 2017. Consultado el 20 de diciembre de 2016 .
- ^ ab Matsuda S, Koyasu S (mayo de 2000). "Mecanismos de acción de la ciclosporina" (PDF) . Inmunofarmacología . 47 (2–3): 119–25. doi :10.1016/S0162-3109(00)00192-2. PMID 10878286. Archivado desde el original (PDF) el 11 de agosto de 2017 . Consultado el 4 de marzo de 2018 .
- ^ Watts R, Clunie G, Hall F, Marshall T (2009). Reumatología. Oxford University Press. pág. 558. ISBN 978-0-19-922999-4Archivado desde el original el 5 de noviembre de 2017.
- ^ Organización Mundial de la Salud (2019). Lista modelo de medicamentos esenciales de la Organización Mundial de la Salud: 21.ª lista , 2019. Ginebra: Organización Mundial de la Salud. hdl : 10665/325771 . OMS/MVP/EMP/IAU/2019.06. Licencia: CC BY-NC-SA 3.0 IGO.
- ^ Organización Mundial de la Salud (2021). Lista modelo de medicamentos esenciales de la Organización Mundial de la Salud: 22.ª lista (2021) . Ginebra: Organización Mundial de la Salud. hdl : 10665/345533 . OMS/MHP/HPS/EML/2021.02.
- ^ "Los 300 mejores de 2021". ClinCalc . Archivado desde el original el 15 de enero de 2024 . Consultado el 14 de enero de 2024 .
- ^ "Ciclosporina - Estadísticas de uso de fármacos". ClinCalc . Consultado el 14 de enero de 2024 .
- ^ "La FDA aprueba el primer genérico de Restasis". Administración de Alimentos y Medicamentos de Estados Unidos (FDA) (Nota de prensa). 2 de febrero de 2022. Archivado desde el original el 2 de febrero de 2022 . Consultado el 3 de febrero de 2022 .
- ^ Reinhard T (2000). "Lokales ciclosporina A bei Nummuli nach queratoconjuntivitis epidémica Eine Pilotstudie - Springer". El oftalmólogo . 97 (11): 764–768. doi :10.1007/s003470070025. PMID 11130165. S2CID 399211.
- ^ Paolino A, Alexander H, Broderick C, Flohr C (mayo de 2023). "Tratamientos sistémicos no biológicos para la dermatitis atópica: estado actual de la técnica y direcciones futuras". Alergia clínica y experimental . 53 (5): 495–510. doi : 10.1111/cea.14301 . PMID 36949024.
- ^ Dijkmans BA, van Rijthoven AW, Goei Thè HS, Boers M, Cats A (agosto de 1992). "Ciclosporina en la artritis reumatoide". Seminarios sobre artritis y reumatismo . 22 (1): 30–36. doi :10.1016/0049-0172(92)90046-g. PMID 1411580.
- ^ Lichtiger S, Present DH, Kornbluth A, Gelernt I, Bauer J, Galler G, et al. (junio de 1994). "Ciclosporina en la colitis ulcerosa grave refractaria a la terapia con esteroides". The New England Journal of Medicine . 330 (26): 1841–5. doi : 10.1056/NEJM199406303302601 . PMID 8196726.
- ^ Naesens M, Kuypers DR, Sarwal M (febrero de 2009). «Nefrotoxicidad por inhibidores de calcineurina» (PDF) . Revista clínica de la Sociedad Americana de Nefrología . 4 (2): 481–508. doi : 10.2215/CJN.04800908 . PMID 19218475. Archivado (PDF) del original el 20 de julio de 2018. Consultado el 20 de abril de 2018 .
- ^ Robert N, Wong GW, Wright JM (enero de 2010). "Efecto de la ciclosporina en la presión arterial". Base de datos Cochrane de revisiones sistemáticas (1): CD007893. doi :10.1002/14651858.CD007893.pub2. PMID 20091657.
- ^ Figg WD (febrero de 1990). "Hiperuricemia y gota inducidas por ciclosporina". The New England Journal of Medicine . 322 (5): 334–336. doi : 10.1056/NEJM199002013220514 . PMID 2296276.
- ^ Agentes clasificados por las monografías del IARC, volúmenes 1–110 Archivado el 25 de octubre de 2011 en Wayback Machine.
- ^ Grupo de trabajo del IARC sobre la evaluación del riesgo carcinogénico para los seres humanos (2012). Ciclosporina. Agencia Internacional para la Investigación sobre el Cáncer. Archivado desde el original el 28 de agosto de 2021. Consultado el 23 de febrero de 2018 .
- ^ Ganong WF (2005). "27". Revista de fisiología médica (22.ª edición). Nueva York: McGraw-Hill Medical. pág. 530. ISBN 978-0-07-144040-0.
- ^ abcdefghi Mott JL, Zhang D, Freeman JC, Mikolajczak P, Chang SW, Zassenhaus HP (julio de 2004). "La ciclosporina A previene la enfermedad cardíaca debida a mutaciones aleatorias del ADN mitocondrial". Biochemical and Biophysical Research Communications . 319 (4): 1210–5. doi :10.1016/j.bbrc.2004.05.104. PMID 15194495.
- ^ abcde Youn TJ, Piao H, Kwon JS, Choi SY, Kim HS, Park DG, et al. (diciembre de 2002). "Efectos de la inhibición de la vía de señalización dependiente de calcineurina por ciclosporina A en la remodelación cardíaca temprana y tardía después de un infarto de miocardio". Revista Europea de Insuficiencia Cardíaca . 4 (6): 713–8. doi : 10.1016/S1388-9842(02)00120-4 . PMID 12453541. S2CID 9181082.
- ^ Handschumacher RE, Harding MW, Rice J, Drugge RJ, Speicher DW (noviembre de 1984). "Ciclofilina: una proteína de unión citosólica específica para la ciclosporina A". Science . 226 (4674): 544–7. Bibcode :1984Sci...226..544H. doi :10.1126/science.6238408. PMID 6238408.
- ^ abcdef Elrod JW, Wong R, Mishra S, Vagnozzi RJ, Sakthievel B, Goonasekera SA, et al. (octubre de 2010). "La ciclofilina D controla el intercambio de Ca(2+) dependiente de los poros mitocondriales, la flexibilidad metabólica y la propensión a la insuficiencia cardíaca en ratones". Journal of Clinical Investigation . 120 (10): 3680–7. doi :10.1172/JCI43171. PMC 2947235 . PMID 20890047.
- ^ Briston T, Selwood DL, Szabadkai G, Duchen MR (enero de 2019). "Transición de la permeabilidad mitocondrial: una lesión molecular con múltiples dianas farmacológicas" (PDF) . Tendencias en ciencias farmacológicas . 40 (1): 50–70. doi :10.1016/j.tips.2018.11.004. PMID 30527591. S2CID 54470812. Archivado (PDF) del original el 21 de enero de 2022 . Consultado el 2 de agosto de 2021 .
- ^ Morciano G, Giorgi C, Bonora M, Punzetti S, Pavasini R, Wieckowski MR, et al. (enero de 2015). "Identidad molecular del poro de transición de la permeabilidad mitocondrial y su papel en la lesión por isquemia-reperfusión". Journal of Molecular and Cellular Cardiology . 78 : 142–53. doi :10.1016/j.yjmcc.2014.08.015. hdl : 11392/2149014 . PMID 25172387.
- ^ Zorov DB, Juhaszova M, Sollott SJ (julio de 2014). "Especies reactivas de oxígeno mitocondriales (ROS) y liberación de ROS inducida por ROS". Physiological Reviews . 94 (3): 909–50. doi :10.1152/physrev.00026.2013. PMC 4101632 . PMID 24987008.
- ^ Meyrier A (2005). "Tratamiento de la glomeruloesclerosis focal y segmentaria". Opinión de expertos sobre farmacoterapia . 6 (9): 1539–1549. doi :10.1517/14656566.6.9.1539. PMID 16086641. S2CID 35867347.
- ^ Faul C, Donnelly M, Merscher-Gomez S, Chang YH, Franz S, Delfgaauw J, et al. (2008). "El citoesqueleto de actina de los podocitos renales es un objetivo directo del efecto antiproteinúrico de la ciclosporina A". Nature Medicine . 14 (9): 931–938. doi :10.1038/nm.1857. PMC 4109287 . PMID 18724379.
- ^ Borel JF (junio de 2002). "Historia del descubrimiento de la ciclosporina y de su desarrollo farmacológico temprano". Wiener Klinische Wochenschrift . 114 (12): 433–7. PMID 12422576.
Algunas fuentes enumeran el hongo bajo un nombre de especie alternativo, Hypocladium inflatum gams, como Pritchard y Sneader en 2005:
* Pritchard DI (mayo de 2005). "Obtención de una sucesión química para la ciclosporina a partir de parásitos y patógenos humanos". Drug Discovery Today . 10 (10): 688–91. doi :10.1016/S1359-6446(05)03395-7. PMID 15896681.
* Sneader W (23 de junio de 2005). "Ciclosporina". Descubrimiento de fármacos: una historia . John Wiley & Sons. págs. 298-299. ISBN 978-0-471-89979-2.
Sin embargo, el nombre, "Beauveria nivea", también aparece en varios otros artículos, incluyendo uno publicado en línea en 2001 por Harriet Upton titulado "Origen de los fármacos en uso actual: la historia de la ciclosporina Archivado el 8 de marzo de 2005 en Wayback Machine " (consultado el 19 de junio de 2005). Mark Plotkin afirma en su libro Medicine Quest , Penguin Books 2001, páginas 46-47, que en 1996 la investigadora en micología Kathie Hodge descubrió que, de hecho, se trata de una especie de Cordyceps . - ^ Wang CP, Hartman NR, Venkataramanan R, Jardine I, Lin FT, Knapp JE, et al. (1989). "Aislamiento de 10 metabolitos de ciclosporina de la bilis humana". Metabolismo y disposición de fármacos . 17 (3): 292–6. PMC 3154783 . PMID 2568911.
- ^ Copeland KR, Yatscoff RW, McKenna RM (febrero de 1990). "Actividad inmunosupresora de los metabolitos de ciclosporina comparada y caracterizada por espectroscopia de masas y resonancia magnética nuclear". Química clínica . 36 (2): 225–9. doi : 10.1093/clinchem/36.2.225 . PMID 2137384.
- ^ Lawen A (octubre de 2015). "Biosíntesis de ciclosporinas y otros inhibidores naturales de peptidil prolil cis / trans isomerasa". Biochimica et Biophysica Acta (BBA) - Temas generales . 1850 (10): 2111–20. doi :10.1016/j.bbagen.2014.12.009. PMID 25497210.
- ^ Dittmann J, Wenger RM, Kleinkauf H, Lawen A (enero de 1994). "Mecanismo de la biosíntesis de la ciclosporina A. Evidencia de síntesis a través de un único precursor undecapéptido lineal". Journal of Biological Chemistry . 269 (4): 2841–6. doi : 10.1016/S0021-9258(17)42019-9 . PMID 8300618.
- ^ Hoppert M, Gentzsch C, Schörgendorfer K (octubre de 2001). "Estructura y localización de la ciclosporina sintetasa, la enzima clave de la biosíntesis de ciclosporina en Tolypocladium inflatum" (PDF) . Archivos de Microbiología . 176 (4): 285–93. Bibcode :2001ArMic.176..285H. doi :10.1007/s002030100324. PMID 11685373. S2CID 33075098.[ enlace muerto permanente ]
- ^ Dewick, P. (2001) Productos naturales medicinales. John Wiley & Sons, Ltd. 2.ª ed.
- ^ Yang X, Feng P, Yin Y, Bushley K, Spatafora JW, Wang C (octubre de 2018). "Tolypocladium inflatum beneficia la adaptación de los hongos al medio ambiente". mBio . 9 (5). doi :10.1128/mBio.01211-18. PMC 6168864 . PMID 30279281.
- ^ Bushley KE, Raja R, Jaiswal P, Cumbie JS, Nonogaki M, Boyd AE, et al. (junio de 2013). "El genoma de Tolypocladium inflatum: evolución, organización y expresión del grupo de genes biosintéticos de la ciclosporina". PLOS Genetics . 9 (6): e1003496. doi : 10.1371/journal.pgen.1003496 . PMC 3688495 . PMID 23818858.
- ^ Xu L, Li Y, Biggins JB, Bowman BR, Verdine GL, Gloer JB, et al. (marzo de 2018). "Identificación de ciclosporina C de Amphichorda felina utilizando un ensayo de sensibilidad diferencial a la temperatura de Cryptococcus neoformans". Applied Microbiology and Biotechnology . 102 (5): 2337–2350. doi :10.1007/s00253-018-8792-0. PMC 5942556 . PMID 29396588.
- ^ di Salvo ML, Florio R, Paiardini A, Vivoli M, D'Aguanno S, Contestabile R (enero de 2013). "Alanina racemasa de Tolypocladium inflatum: una enzima clave dependiente de PLP en la biosíntesis de ciclosporina y un modelo de promiscuidad catalítica". Archivos de bioquímica y biofísica . 529 (2): 55–65. doi :10.1016/j.abb.2012.11.011. PMID 23219598.
- ^ abc Borel JF, Kis ZL, Beveridge T (1995). "La historia del descubrimiento y desarrollo de la ciclosporina (Sandimmune)". En Merluzzi VJ, Adams J (eds.). La búsqueda de fármacos antiinflamatorios: historias clínicas desde el concepto hasta la práctica clínica . Boston: Birkhäuser. págs. 27–63. ISBN 978-1-4615-9846-6Archivado desde el original el 5 de noviembre de 2017.
- ^ Cheng M (2013). "Hartmann Stahelin (1925-2011) y la controvertida historia de la ciclosporina A". Trasplante Clínico . 27 (3): 326–329. doi :10.1111/ctr.12072. PMID 23331048. S2CID 39502677.
- ^ Borel JF, Feurer C, Gubler HU, Stähelin H (julio de 1976). "Efectos biológicos de la ciclosporina A: un nuevo agente antilinfocítico". Agentes y acciones . 6 (4): 468–75. doi :10.1007/bf01973261. PMID 8969. S2CID 2862779.
- ^ Rüegger A, Kuhn M, Lichti H, Loosli HR, Huguenin R, Quiquerez C, et al. (1976). "[Ciclosporina A, un metabolito peptídico de Trichoderma polysporum (Link ex Pers.) Rifai, con una notable actividad inmunosupresora]" [Ciclosporina A, un metabolito peptídico de Trichoderma polysporum (Link ex Pers.) Rifai, con una notable actividad inmunosupresora]. Helvetica Chimica Acta (en alemán). 59 (4): 1075–92. doi :10.1002/hlca.19760590412. PMID 950308.
- ^ Heusler K, Pletscher A (junio de 2001). "La controvertida historia temprana de la ciclosporina". Swiss Medical Weekly . 131 (21–22): 299–302. doi : 10.4414/smw.2001.09702 . PMID 11584691. S2CID 24662504.
- ^ Calne RY, White DJ, Thiru S, Evans DB, McMaster P, Dunn DC, et al. (1978). "Ciclosporina A en pacientes que reciben aloinjertos renales de donantes cadavéricos". The Lancet . 2 (8104–5): 1323–7. doi :10.1016/S0140-6736(78)91970-0. PMID 82836. S2CID 10731038.
- ^ Starzl TE, Klintmalm GB, Porter KA, Iwatsuki S, Schröter GP (julio de 1981). "Trasplante hepático con uso de ciclosporina a y prednisona". The New England Journal of Medicine . 305 (5): 266–9. doi :10.1056/NEJM198107303050507. PMC 2772056 . PMID 7017414.
- ^ Kolata G (septiembre de 1983). "La FDA acelera la aprobación de la ciclosporina". Science . 221 (4617): 1273. Bibcode :1983Sci...221.1273K. doi :10.1126/science.221.4617.1273-a. PMID 17776314.
El 2 de septiembre (1983), la Administración de Alimentos y Medicamentos aprobó la ciclosporina, un nuevo fármaco que suprime el sistema inmunológico.
- ^ Gottesman J (20 de marzo de 1988). «Milestones in Cardiac Care». Los Angeles Times . Archivado desde el original el 26 de febrero de 2017.
- ^ "Primer trasplante cardíaco pediátrico exitoso [9 de junio de 1984]". Centro Médico de la Universidad de Columbia, Departamento de Cirugía, Programa de Trasplante Cardíaco. Archivado desde el original el 1 de marzo de 2017.
[La ciclosporina] obtuvo la aprobación de la FDA a fines de 1983, ...
- ^ "Medicamentos@FDA: Productos farmacéuticos aprobados por la FDA [Haga clic en "Fecha(s) de aprobación e historial]". Administración de Alimentos y Medicamentos de los Estados Unidos. Archivado desde el original el 1 de marzo de 2017.
Nombre(s) del medicamento: Sandimmune (ciclosporina), Compañía: Novartis, Fecha de acción: 14/11/1983, Tipo de acción: Aprobación, Clasificación de presentación: Tipo 1 - Nueva entidad molecular, Prioridad de revisión: Prioridad
- ^ abc Starzl TE (1992). The Puzzle People: Memorias de un cirujano de trasplantes. University of Pittsburgh Press. doi :10.2307/j.ctt9qh63b. ISBN 978-0-8229-3714-2.
- ^ "Directrices para el uso de denominaciones comunes internacionales (DCI) para sustancias farmacéuticas". Organización Mundial de la Salud. 1997.
Para facilitar la traducción y la pronunciación de las DCI, se debe utilizar "f" en lugar de "ph", "t" en lugar de "th", "e" en lugar de "ae" u "oe", e "i" en lugar de "y"; se debe evitar el uso de las letras "h" y "k".
[ enlace muerto ] - ^ "La historia de la ciclosporina". www.davidmoore.org.uk . Enero de 2013. Archivado desde el original el 22 de octubre de 2022 . Consultado el 24 de octubre de 2022 .
- ^ Gibaud S, Attivi D (agosto de 2012). "Microemulsiones para administración oral y sus aplicaciones terapéuticas". Opinión de expertos sobre administración de fármacos . 9 (8): 937–51. doi :10.1517/17425247.2012.694865. PMID 22663249. S2CID 28468973. Archivado desde el original el 5 de marzo de 2018. Consultado el 4 de marzo de 2018 .
- ^ Min DI (marzo de 1996). "Neoral: una ciclosporina en microemulsión". Journal of Transplant Coordination . 6 (1): 5–8. doi :10.7182/prtr.1.6.1.f04016025hh795up (inactivo el 7 de septiembre de 2024). PMID 9157923.
{{cite journal}}: CS1 maint: DOI inactivo a partir de septiembre de 2024 ( enlace ) - ^ "Neoral" (PDF) . Panel de datos de la FDA . Administración de Alimentos y Medicamentos (FDA); Novartis . Septiembre de 2009. Archivado (PDF) del original el 20 de octubre de 2022 . Consultado el 24 de octubre de 2022 .
- ^ "Ikervis". Santen. Archivado desde el original el 3 de julio de 2018. Consultado el 3 de julio de 2018 .
- ^ Número de ensayo clínico NCT01287078 para "Solución para inhalación de ciclosporina (CIS) en receptores de trasplantes de pulmón y de trasplantes de células madre hematopoyéticas para el tratamiento de la bronquiolitis obliterante" en ClinicalTrials.gov .
- ^ Trammer B, Amann A, Haltner-Ukomadu E, Tillmanns S, Keller M, Högger P (noviembre de 2008). "Permeabilidad comparativa y cinética de difusión de liposomas de ciclosporina A y solución de propilenglicol desde tejido pulmonar humano a sangre humana ex vivo". Revista Europea de Farmacia y Biofarmacia . 70 (3): 758–64. doi :10.1016/j.ejpb.2008.07.001. PMID 18656538.
- ^ Administrador. "Hem - NeuroVive Pharmaceutical AB". neurovive.com . Archivado desde el original el 6 de enero de 2014.
- ^ Ehinger KH, Hansson MJ, Sjövall F, Elmér E (enero de 2013). "Evaluación de la bioequivalencia y la tolerabilidad de una nueva emulsión lipídica de ciclosporina intravenosa en comparación con la ciclosporina de marca en Cremophor EL" (PDF) . Clinical Drug Investigation . 33 (1): 25–34. doi :10.1007/s40261-012-0029-x. PMC 3586182 . PMID 23179472. Archivado (PDF) del original el 26 de octubre de 2018 . Consultado el 26 de octubre de 2018 .
- ^ Sullivan PG, Thompson M, Scheff SW (febrero de 2000). "La infusión continua de ciclosporina A después de una lesión mejora significativamente el daño cortical después de una lesión cerebral traumática". Neurología experimental . 161 (2): 631–7. doi :10.1006/exnr.1999.7282. PMID 10686082. S2CID 25190221.
- ^ Uchino H, Elmér E, Uchino K, Lindvall O, Siesjö BK (diciembre de 1995). "La ciclosporina A mejora drásticamente el daño del hipocampo CA1 después de una isquemia transitoria del prosencéfalo en la rata". Acta Physiologica Scandinavica . 155 (4): 469–71. doi :10.1111/j.1748-1716.1995.tb09999.x. PMID 8719269.
- ^ Sullivan PG, Sebastian AH, Hall ED (febrero de 2011). "Análisis de la ventana terapéutica de los efectos neuroprotectores de la ciclosporina A después de una lesión cerebral traumática". Journal of Neurotrauma . 28 (2): 311–8. doi :10.1089/neu.2010.1646. PMC 3037811 . PMID 21142667.
- ^ ab Mende U, Kagen A, Cohen A, Aramburu J, Schoen FJ, Neer EJ (noviembre de 1998). "La expresión cardíaca transitoria de Galphaq constitutivamente activo conduce a hipertrofia y miocardiopatía dilatada por vías dependientes e independientes de la calcineurina". Actas de la Academia Nacional de Ciencias de los Estados Unidos de América . 95 (23): 13893–8. Bibcode :1998PNAS...9513893M. doi : 10.1073/pnas.95.23.13893 . PMC 24952 . PMID 9811897.
- ^ Wilkinson ST, Johnson DB, Tardif HL, Tome ME, Briehl MM (marzo de 2010). "El aumento del citocromo c se correlaciona con una supervivencia deficiente en el linfoma agresivo". Oncology Letters . 1 (2): 227–230. doi :10.3892/ol_00000040. PMC 2927837 . PMID 20798784.
- ^ ab Lim HW, De Windt LJ, Mante J, Kimball TR, Witt SA, Sussman MA, et al. (abril de 2000). "Reversión de la hipertrofia cardíaca en modelos de enfermedades transgénicas mediante inhibición de la calcineurina". Journal of Molecular and Cellular Cardiology . 32 (4): 697–709. doi :10.1006/jmcc.2000.1113. PMID 10756124. S2CID 10904494.
- ^ ab Archer TM, Boothe DM, Langston VC, Fellman CL, Lunsford KV, Mackin AJ (2014). "Tratamiento oral con ciclosporina en perros: una revisión de la literatura". Revista de Medicina Interna Veterinaria . 28 (1): 1–20. doi :10.1111/jvim.12265. PMC 4895546 . PMID 24341787.
- ^ Palmeiro BS (enero de 2013). "Ciclosporina en dermatología veterinaria". Clínicas veterinarias de Norteamérica: Práctica en animales pequeños . 43 (1): 153–71. doi :10.1016/j.cvsm.2012.09.007. PMID 23182330.
Enlaces externos
- Ciclosporina en los encabezados de materias médicas (MeSH) de la Biblioteca Nacional de Medicina de EE. UU.
