Cefuroxima
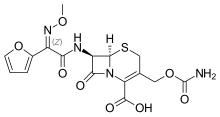 | |
 | |
| Datos clínicos | |
|---|---|
| Nombres comerciales | Zinacef, otros |
| AHFS / Drogas.com | Monografía |
| MedlinePlus | a601206 |
| Datos de licencia |
|
| Vías de administración | Intramuscular , intravenosa , por vía oral |
| Clase de droga | Cefalosporina de segunda generación |
| Código ATC | |
| Estatus legal | |
| Estatus legal |
|
| Datos farmacocinéticos | |
| Biodisponibilidad | 37% en ayunas, hasta 52% si se toma después de las comidas |
| Vida media de eliminación | 80 minutos |
| Excreción | Orina 66–100% sin cambios |
| Identificadores | |
| |
| Número CAS | |
| Identificador de centro de PubChem |
|
| Banco de medicamentos | |
| Araña química | |
| UNIVERSIDAD |
|
| BARRIL | |
| Química biológica | |
| Panel de control CompTox ( EPA ) |
|
| Tarjeta informativa de la ECHA | 100.054.127 |
| Datos químicos y físicos | |
| Fórmula | C16H16N4O8S |
| Masa molar | 424,38 g·mol −1 |
| Modelo 3D ( JSmol ) |
|
| |
| (verificar) | |
La cefuroxima , que se vende bajo la marca Zinacef , entre otras, es un antibiótico de cefalosporina de segunda generación [3] que se utiliza para tratar y prevenir una serie de infecciones bacterianas . [4] Estas incluyen neumonía , meningitis , otitis media , sepsis , infecciones del tracto urinario y enfermedad de Lyme . [5] Se utiliza por vía oral o mediante inyección en una vena o músculo . [5]
Los efectos secundarios comunes incluyen náuseas, diarrea, reacciones alérgicas y dolor en el lugar de la inyección. [5] Los efectos secundarios graves pueden incluir infección por Clostridioides difficile , anafilaxia y síndrome de Stevens-Johnson . [5] Se cree que su uso durante el embarazo y la lactancia es seguro. [6] Es una cefalosporina de segunda generación y actúa interfiriendo en la capacidad de una bacteria para formar una pared celular , lo que provoca su muerte. [5]
La cefuroxima fue patentada en 1971 y aprobada para uso médico en 1977. [7] Está en la Lista de Medicamentos Esenciales de la Organización Mundial de la Salud . [8] En 2020, fue el medicamento número 325 más recetado en los Estados Unidos, con más de 800 mil recetas. [9]
Usos médicos
La cefuroxima es activa contra muchas bacterias, incluidas cepas susceptibles de estafilococos y estreptococos , así como una variedad de organismos gramnegativos. [10] Al igual que con las otras cefalosporinas, es susceptible a la beta-lactamasa , aunque como variedad de segunda generación, lo es menos. Por lo tanto, puede tener mayor actividad contra Haemophilus influenzae , Neisseria gonorrhoeae y la enfermedad de Lyme . A diferencia de otras cefalosporinas de segunda generación, la cefuroxima puede atravesar la barrera hematoencefálica . [11]
Una revisión sistemática encontró evidencia de alta calidad de que inyectar cefuroxima en el ojo después de la cirugía de cataratas reducirá la probabilidad de desarrollar endoftalmitis después de la cirugía. [12]
Efectos secundarios
La cefuroxima es generalmente bien tolerada y sus efectos secundarios suelen ser transitorios. Si se ingiere después de las comidas, este antibiótico se absorbe mejor y es menos probable que cause sus efectos secundarios más comunes ( diarrea , náuseas, vómitos, dolores de cabeza/ migrañas , mareos y dolor abdominal) en comparación con la mayoría de los antibióticos de su clase. [ cita médica requerida ]
Aunque existe un riesgo ampliamente establecido de alergia cruzada de alrededor del 10% entre las cefalosporinas y la penicilina , una evaluación realizada en 2006 no ha demostrado un mayor riesgo de reacción alérgica cruzada para la cefuroxima y varias otras cefalosporinas de segunda generación o posteriores. [13]
Compuestos relacionados
La cefuroxima axetilo es un profármaco de éster acetoxietilo de la cefuroxima que es eficaz cuando se toma por vía oral. [14] Es una cefalosporina de segunda generación . [15]
Nombres comerciales
En EE. UU. se comercializa como Zinacef por Covis Pharmaceuticals desde que la compañía adquirió los derechos estadounidenses del producto de GSK . [16] GSK había seguido comercializando una suspensión oral pediátrica como Ceftin; sin embargo, esta presentación se suspendió a partir del 24 de junio de 2017. [17]
En Bangladesh, está disponible como Sefur por Opsonin Pharma, Kilbac por Incepta, Axim por Aristopharma, Rofurox por Radiant, Xorimax por Sandoz y Uroxime por EURO Pharma Ltd. En la India, está disponible como Ceftum y Cefuall por Allencia Biosciences en forma de comprimidos y Supacef en forma de inyección por GSK. [18] En Polonia, está disponible como Zamur por Mepha , subsidiaria de Teva Pharmaceutical Industries . [19] En Australia, la primera forma "genérica" de cefuroxima axetilo, Pharmacor Cefuroxime (comprimidos) de Pharmacor Pty Ltd, fue registrada el 27 de marzo de 2017 por la Administración de Productos Terapéuticos . [20] La cefuroxima axetilo se vende en forma de comprimidos en Turquía bajo las marcas Aksef [21] y Cefaks. [22] La cefuroxima axetilo también está disponible (en dos concentraciones) como gránulos para suspensión oral de Aspen Pharmacare Australia Pty Ltd bajo la marca Zinnat cefuroxime. [23]
Referencias
- ^ "Lista de todos los medicamentos con advertencias de recuadro negro obtenida por la FDA (use los enlaces Descargar resultados completos y Ver consulta)". nctr-crs.fda.gov . FDA . Consultado el 22 de octubre de 2023 .
- ^ "Actualizaciones de seguridad de la marca en la monografía de productos". Health Canada . 7 de julio de 2016 . Consultado el 13 de julio de 2024 .
- ^ Katzung B (2018). Farmacología básica y clínica . McGraw Hill. pág. 803.
- ^ Formulario nacional británico: BNF 76 (76.ª edición). Pharmaceutical Press. 2018. pág. 518. ISBN 9780857113382.
- ^ abcde "Monografía de cefuroxima sódica para profesionales". Drugs.com . Sociedad Estadounidense de Farmacéuticos del Sistema de Salud . Consultado el 22 de marzo de 2019 .
- ^ "Uso de cefuroxima durante el embarazo". Drugs.com . Consultado el 3 de marzo de 2019 .
- ^ Fischer J, Ganellin CR (2006). Descubrimiento de fármacos basado en análogos. John Wiley & Sons. pág. 493. ISBN 9783527607495.
- ^ Organización Mundial de la Salud (2019). Lista modelo de medicamentos esenciales de la Organización Mundial de la Salud: 21.ª lista , 2019. Ginebra: Organización Mundial de la Salud. hdl : 10665/325771 . OMS/MVP/EMP/IAU/2019.06. Licencia: CC BY-NC-SA 3.0 IGO.
- ^ "Cefuroxima: estadísticas de uso de medicamentos". ClinCalc . Consultado el 7 de octubre de 2022 .
- ^ "Apéndice 5: descripción general de los antibióticos". Manual de medicamentos de la UCI de Wellington . Consultado el 7 de abril de 2023 .
- ^ Root RK, Waldvogel F, Corey L, Stamm WE (1999). Enfermedades infecciosas clínicas: un enfoque práctico. Oxford University Press. pág. 259. ISBN 9780195081039.
- ^ Gower EW, Lindsley K, Tulenko SE, Nanji AA, Leyngold I, McDonnell PJ (febrero de 2017). "Antibióticos perioperatorios para la prevención de la endoftalmitis aguda después de la cirugía de cataratas". Base de datos Cochrane de revisiones sistemáticas . 2017 (2): CD006364. doi :10.1002/14651858.CD006364.pub3. PMC 5375161. PMID 28192644 .
- ^ Pichichero ME (febrero de 2006). "Las cefalosporinas se pueden prescribir de forma segura a los pacientes alérgicos a la penicilina" (PDF) . The Journal of Family Practice . 55 (2): 106–112. PMID 16451776. Archivado desde el original (PDF) el 24 de febrero de 2012.
- ^ Sneader W (23 de junio de 2005). Descubrimiento de fármacos: historia. John Wiley & Sons. ISBN 9780471899792.
- ^ Glatt AE (15 de marzo de 1986). "Cefalosporinas de segunda generación". Hospital Practice (Office Ed.) . 21 (3): 158A–158B, 158E, 158H–158L. doi :10.1080/21548331.1986.11704945. ISSN 8750-2836. PMID 3081544.
- ^ "Covis Pharma adquirirá los derechos estadounidenses de GlaxoSmithKline para Fortaz®, Zinacef®, Lanoxin®, Parnate® y Zantac® inyectable". Covis-pharma-sarl (Nota de prensa) . Consultado el 6 de agosto de 2012 .
- ^ "Escasez de medicamentos por parte de la FDA". Administración de Alimentos y Medicamentos (FDA). 20 de marzo de 2018.
- ^ "GlaxoSmithKline Pharmaceuticals Limited – Medicamentos de venta con receta – Antiinfecciosos". Gsk-india.com. 26 de marzo de 2013. Archivado desde el original el 22 de marzo de 2016. Consultado el 12 de marzo de 2012 .
- ^ "Charakterystyka produktu lecznicznego" (PDF) . Urząd Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych. 12 de noviembre de 2015.
- ^ "Medicamentos de prescripción: registro de nuevos medicamentos genéricos y medicamentos biosimilares, 2017". TGA . Administración de Productos Terapéuticos. 26 de marzo de 2018 . Consultado el 30 de julio de 2018 .
- ^ "Aksef 500 mg 20 comprimidos". Nobel İlaç Sanayii ve Ticaret A.Ş. Consultado el 26 de abril de 2023 .
- ^ "Productos antiinfecciosos y antiparasitarios de uso sistémico". DEVA Holding . Consultado el 3 de mayo de 2023 .
- ^ "ARTG ID 81301". TGA . Administración de Productos Terapéuticos. Archivado desde el original el 28 de agosto de 2021 . Consultado el 30 de julio de 2018 .

