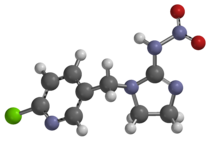
Imidacloprid
 | |
 | |
| Nombres | |
|---|---|
| Nombre IUPAC N- {1-[(6-cloro-3-piridil)metil]-4,5-dihidroimidazol-2-il}nitramida | |
| Identificadores | |
Modelo 3D ( JSmol ) |
|
| EBICh | |
| Química biológica | |
| Araña química | |
| Banco de medicamentos | |
| Tarjeta informativa de la ECHA | 100.102.643 |
| BARRIL | |
Identificador de centro de PubChem |
|
| UNIVERSIDAD | |
Panel de control CompTox ( EPA ) |
|
| |
| |
| Propiedades | |
| C9H10ClN5O2 | |
| Masa molar | 255.661 |
| Apariencia | Cristales incoloros |
| Punto de fusión | 136,4 a 143,8 °C (277,5 a 290,8 °F; 409,5 a 416,9 K) |
| 0,51 g/L (20 °C) | |
| Farmacología | |
| QP53AX17 ( OMS ) | |
| Estatus legal |
|
Salvo que se indique lo contrario, los datos se proporcionan para los materiales en su estado estándar (a 25 °C [77 °F], 100 kPa). | |
El imidacloprid es un insecticida sistémico que pertenece a una clase de sustancias químicas llamadas neonicotinoides que actúan sobre el sistema nervioso central de los insectos. La sustancia química actúa interfiriendo en la transmisión de estímulos en el sistema nervioso de los insectos. En concreto, provoca un bloqueo de la vía neuronal nicotinérgica . Al bloquear los receptores nicotínicos de acetilcolina , el imidacloprid impide que la acetilcolina transmita impulsos entre los nervios, lo que provoca la parálisis y la muerte del insecto. Es eficaz por contacto y por acción estomacal. [1] Dado que el imidacloprid se une mucho más fuertemente a los receptores neuronales de los insectos que a los de los mamíferos, este insecticida es más tóxico para los insectos que para los mamíferos. [3]
Desde 1999 [4] hasta al menos 2018 [actualizar], [5] [6] el imidacloprid fue el insecticida más utilizado en el mundo. Aunque ya no tiene patente, el principal fabricante de este producto químico es Bayer CropScience (parte de Bayer AG ). Se vende con muchos nombres para muchos usos; se puede aplicar por inyección en el suelo, inyección en los árboles , aplicación en la piel de la planta, aplicación foliar al voleo o aplicación terrestre como una formulación granular o líquida, o como un tratamiento de semillas recubierto de pesticida . [7] [3] [8] El imidacloprid se usa ampliamente para el control de plagas en la agricultura. Otros usos incluyen la aplicación a cimientos para prevenir daños por termitas, el control de plagas en jardines y césped, el tratamiento de mascotas domésticas para controlar pulgas, [3] la protección de árboles contra insectos perforadores, [9] y en el tratamiento conservante de algunos tipos de productos de madera. [10]
Una revisión de 2018 realizada por la Autoridad Europea de Seguridad Alimentaria (AESA) concluyó que la mayoría de los usos de pesticidas neonicotinoides como el imidacloprid representan un riesgo para las abejas silvestres y las abejas melíferas. [11] [12] En 2022, la Agencia de Protección Ambiental de los Estados Unidos (EPA) concluyó que es probable que el imidacloprid afecte negativamente al 79 por ciento de las especies amenazadas o en peligro de extinción incluidas en la lista federal y al 83 por ciento de los hábitats críticos. [13] El pesticida ha estado prohibido para todo uso al aire libre en toda la Unión Europea desde 2018, pero tiene una aprobación parcial en los Estados Unidos y algunos otros países. Todavía sigue siendo de uso generalizado en otras partes importantes del mundo. [14] [15]
Usar
El imidacloprid es uno de los insecticidas más utilizados en el mundo. [4] [5] [6] Sus principales usos incluyen:
- Tratamiento de semillas: el imidacloprid es un insecticida para el tratamiento de semillas muy popular en el mundo [8]
- Agricultura – Control de pulgones , escarabajos de la caña , trips , [16] chinches apestosas , langostas y una variedad de otros insectos que dañan los cultivos.
- Arboricultura – Control del barrenador esmeralda del fresno , del pulgón lanígero de la cicuta [ 17] y de otros insectos que atacan a los árboles (incluidos la cicuta , el arce , el roble y el abedul ) [9]
- Protección del hogar: control de termitas , [3] [16] hormigas carpinteras , cucarachas e insectos amantes de la humedad.
- Animales domésticos – Control de pulgas (aplicado en la nuca) [3]
- Césped: control de larvas de escarabajo japonés (p. ej., larvas de gusanos)
- Jardinería – Control de pulgones y otras plagas
Cuando se usa en plantas, el imidacloprid, que es sistémico, es absorbido lentamente por las raíces de las plantas y se traslada lentamente hacia la planta a través del tejido del xilema .
Aplicación a los árboles
Cuando se utiliza en árboles, puede tardar entre 30 y 60 días en alcanzar la copa (según el tamaño y la altura) y penetrar en las hojas en cantidades lo suficientemente altas como para ser eficaz. El imidacloprid se puede encontrar en el tronco, las ramas, las ramitas, las hojas, los folíolos y las semillas. Muchos árboles son polinizados por el viento. Pero otros, como los árboles frutales, el tilo, la catalpa y los árboles de acacia negra, son polinizados por las abejas y el viento y es probable que el imidacloprid se encuentre en las flores en pequeñas cantidades. Se deben utilizar dosis más altas para controlar los insectos perforadores que otros tipos. [9]
Uso en Estados Unidos

El Servicio Geológico de Estados Unidos ha mapeado el uso anual estimado del compuesto en la agricultura estadounidense y muestra una tendencia creciente desde su introducción en 1994 hasta 2014, cuando alcanzó 2.000.000 libras (910.000 kg). [18] Sin embargo, el uso entre 2015 y 2019 disminuyó debido a las preocupaciones sobre el efecto de los químicos neonicotinoides en los insectos polinizadores. [19] En mayo de 2019, la Agencia de Protección Ambiental revocó la aprobación de varios productos que contenían imidacloprid como parte de un acuerdo legal, aunque algunas formulaciones continúan estando disponibles. [20] [21]
Historia
El 21 de enero de 1986, Nihon Tokushu Noyaku Seizo KK de Tokio, Japón, presentó una patente y la concedió el 3 de mayo de 1988 para imidacloprid en los Estados Unidos (Patente de EE. UU. N.º 4.742.060). [22]
El 25 de marzo de 1992, Miles, Inc. (posteriormente Bayer CropScience) solicitó el registro del imidacloprid para césped y plantas ornamentales en los Estados Unidos. El 10 de marzo de 1994, la Agencia de Protección Ambiental de los Estados Unidos aprobó el registro del imidacloprid. [23]
El 26 de enero de 2005, el Registro Federal señaló el establecimiento de las «(Tolerancias de plaguicidas para) Exenciones de emergencia» para el imidacloprid. Se concedió su uso a Hawái para el uso de este plaguicida en plátanos y a los estados de Minnesota, Nebraska y Dakota del Norte para el uso de este plaguicida en girasoles . [24]
Inscripciones
El imidacloprid se vende bajo varias marcas comerciales, entre ellas Confidor (Bayer CropScience India), [25] Marathon (OHP, EE. UU.). [26] [27]
Bioquímica
El imidacloprid es un insecticida sistémico que pertenece a la clase de insecticidas neonicotinoides cloronicotinilados . Actúa interfiriendo en la transmisión de los impulsos nerviosos en los insectos al unirse de forma irreversible a los receptores nicotínicos de acetilcolina específicos de los insectos . [28]
Como pesticida sistémico, el imidacloprid se traslada o se mueve fácilmente en el xilema de las plantas desde el suelo hacia las hojas, frutos, polen y néctar de una planta. El imidacloprid también exhibe un excelente movimiento translaminar en las plantas y puede penetrar la cutícula de las hojas y moverse fácilmente hacia el tejido foliar. [29]
Dado que el imidacloprid es eficaz en niveles muy bajos (nanogramos y picogramos), se puede aplicar en concentraciones mucho más bajas (por ejemplo, 0,05–0,125 lb/acre o 55–140 g/ha) que otros insecticidas. La disponibilidad del imidacloprid y su paquete de toxicidad favorable en comparación con otros insecticidas en el mercado en la década de 1990 permitió a la EPA reemplazar insecticidas más tóxicos, incluidos los inhibidores de la acetilcolinesterasa, los compuestos organofosforados y los metilcarbamatos. [30] [31]
Toxicología
Según estudios de laboratorio realizados en ratas, la Organización Mundial de la Salud y la Agencia de Protección Ambiental de los Estados Unidos (EPA) han clasificado al imidacloprid como "moderadamente tóxico" en una base oral aguda para mamíferos y de baja toxicidad en una base dérmica (clase II o III, que requiere una etiqueta de "Advertencia" o "Precaución"). La EPA de los Estados Unidos lo clasifica como un carcinógeno "poco probable" y como débilmente mutagénico (grupo E). No figura en la lista de toxicidad reproductiva o del desarrollo , pero sí en la Orden de detección de nivel 1 de la EPA para sustancias químicas que se deben analizar en el marco del Programa de detección de disruptores endocrinos (EDSP). [23] [32] Las tolerancias para los residuos de imidacloprid en los alimentos varían de 0,02 mg/kg en huevos a 3,0 mg/kg en lúpulo . [1]
Mamíferos
El imidacloprid y su metabolito nitrosoimina (WAK 3839) se han estudiado en profundidad en ratas, ratones y perros.
En los perros, la LD 50 es de 450 mg/kg de peso corporal (es decir, en cualquier muestra de perros de tamaño mediano que pesen 13 kilogramos (29 lb), la mitad de ellos morirían después de consumir 5.850 mg de imidacloprid, o aproximadamente 1 ⁄ 5 de onza). La LD 50 por inhalación aguda en ratas no se alcanzó en las mayores concentraciones alcanzables, 69 miligramos por metro cúbico de aire como aerosol y 5.323 mg de ia/m 3 de aire como polvo.
En los mamíferos, los efectos primarios tras la exposición oral aguda a dosis altas de imidacloprid son mortalidad, efectos colinérgicos transitorios (mareos, apatía, efectos locomotrices, dificultad para respirar) y retraso transitorio del crecimiento. La exposición a dosis altas puede estar asociada con cambios degenerativos en los testículos, el timo, la médula ósea y el páncreas. También se han observado efectos cardiovasculares y hematológicos a dosis más altas.
Los efectos principales de la exposición prolongada a dosis bajas de imidacloprid se producen en el hígado, la tiroides y el peso corporal (reducción). Las exposiciones orales a dosis bajas o medias se han asociado con toxicidad reproductiva, retraso del desarrollo y déficits neuroconductuales en ratas y conejos. El imidacloprid no es carcinógeno en animales de laboratorio ni mutagénico en ensayos de laboratorio estándar. [33]
No es irritante para los ojos ni la piel de conejos y cobayas . [1]
En los seres humanos se esperan efectos similares. Los efectos primarios tras la ingestión oral aguda incluyen emesis , diaforesis , somnolencia y desorientación . [3]
Abejas
El imidacloprid es extremadamente tóxico para las abejas: su LD50 oscila entre 5 y 70 nanogramos por abeja. [34] Las colonias de abejas varían en su capacidad para metabolizar toxinas, lo que explica este amplio rango. El imidacloprid es más tóxico para las abejas que el organofosforado dimetoato (LD50 oral de 152 ng/abeja) o el piretroide cipermetrina (LD50 oral de 160 ng/abeja). [34] La toxicidad del imidacloprid para las abejas difiere de la de la mayoría de los insecticidas en que es más tóxico por vía oral que por contacto. La LD50 aguda por contacto es de 0,024 μg de ingrediente activo por abeja. [ 35]
En estudios de laboratorio, se ha demostrado que los niveles subletales de imidacloprid afectan la navegación, el comportamiento de búsqueda de alimento, el comportamiento de alimentación y el rendimiento del aprendizaje olfativo en las abejas melíferas ( Apis mellifera ). [34] [36] [37] [ 38] [39] [40] [41] [42] En general, sin embargo, a pesar del hecho de que muchos estudios de laboratorio han demostrado el potencial de toxicidad de los neonicotinoides, la mayoría de los estudios de campo han encontrado solo efectos limitados o nulos en las abejas melíferas. [43]
En los abejorros, la exposición a 10 ppb de imidacloprid reduce el comportamiento natural de búsqueda de alimento, aumenta la mortalidad de las obreras y conduce a un menor desarrollo de la cría. [44] [45] El mecanismo probable es que la vía del mevalonato se regula sustancialmente a la baja por la exposición crónica al imidacloprid, lo que puede ayudar a explicar el deterioro de las funciones cognitivas por este imidacloprid. [46]
Pájaros
Se considera que el imidacloprid es extremadamente tóxico para las aves y causa toxicidad reproductiva aviar. [28]
En la codorniz bobwhite ( Colinus virginianus ), se determinó que el imidacloprid era moderadamente tóxico con una LD50 de 14 días de 152 mg ai/kg. Fue ligeramente tóxico en un estudio dietético de 5 días con una LC50 oral aguda de 1420 mg ai/kg de dieta, una NOAEC de < 69 mg ai/kg de dieta y una LOAEC = 69 mg ai/kg de dieta. Las aves expuestas exhibieron ataxia, caída de alas, opistótonos, inmovilidad, hiperactividad, buches e intestinos llenos de líquido e hígados descoloridos. En un estudio de toxicidad reproductiva con codorniz bobwhite, la NOAEC = 120 mg ai/kg de dieta y la LOAEC = 240 mg ai/kg de dieta. Se observó adelgazamiento de la cáscara del huevo y disminución del peso adulto con una dieta de 240 mg ai/kg. [23] [28]
El imidacloprid es altamente tóxico para cuatro especies de aves: codorniz japonesa, gorrión doméstico, canario y paloma. La LD50 oral aguda para la codorniz japonesa ( Coturnix coturnix ) es de 31 mg ia/kg de peso corporal con un NOAEL = 3,1 mg ia/kg. La LD50 oral aguda para el gorrión doméstico ( Passer domesticus ) es de 41 mg ia/kg de peso corporal con un NOAEL = 3 mg ia/kg y un NOAEL = 6 mg ia/kg. Las LD50 para la paloma ( Columba livia ) y el canario ( Serinus canaria ) son de 25–50 mg ia/kg. Los patos silvestres son más resistentes a los efectos del imidacloprid con una CL50 dietética de 5 días de > 4797 ppm. La NOAEC para el peso corporal y el consumo de alimento es de 69 mg ia/kg de dieta. Los estudios reproductivos con patos silvestres mostraron un adelgazamiento de la cáscara del huevo con una dieta de 240 mg de ia/kg. [23] [28]
Según la Autoridad Europea de Seguridad Alimentaria, el imidacloprid supone un riesgo agudo potencial tanto para las aves herbívoras como para las insectívoras . [31] El riesgo crónico no ha sido bien establecido. [28]
Un estudio observacional de 2014 realizado en los Países Bajos correlacionó las disminuciones de algunas poblaciones de aves con residuos ambientales de imidacloprid, aunque no llegó a concluir que la asociación fuera causal. [47]
Vida acuática
El imidacloprid es altamente tóxico de forma aguda para los invertebrados acuáticos , con valores de CE 50 de 0,037 a 0,115 ppm. También es altamente tóxico para los invertebrados acuáticos de forma crónica (efectos sobre el crecimiento y el movimiento): NOAEC / LOAEC = 1,8/3,6 ppm en dáfnidos ; NOAEC = 0,001 en mosquitos Chironomus y NOAEC/LOAEC = 0,00006/0,0013 ppm en camarones mísidos .
Su toxicidad para los peces es relativamente baja; [1] sin embargo, la EPA ha solicitado una revisión de los efectos secundarios en los peces con cadenas alimentarias que incluyen invertebrados acuáticos sensibles. [16] Una investigación publicada en 2018 demostró la acumulación de imidacloprid en la sangre de la trucha arcoíris, contradiciendo las afirmaciones de Bayer de que la persistencia (bioacumulación) no ocurre con el imidacloprid. [48] [49]
La vida vegetal
Se ha demostrado que el imidacloprid desactiva algunos genes que algunas variedades de arroz utilizan para producir sustancias químicas defensivas. Si bien el imidacloprid se utiliza para controlar la chicharrita marrón y otras plagas del arroz, hay evidencia de que el imidacloprid en realidad aumenta la susceptibilidad de la planta de arroz a la infestación y los ataques de la chicharrita. [50] Se ha demostrado que el imidacloprid aumenta la tasa de fotosíntesis en el algodón de las tierras altas a temperaturas superiores a los 36 grados Celsius (97 grados Fahrenheit). [51]
Destino ambiental
Las principales vías de disipación del imidacloprid en el medio ambiente son la fotólisis acuosa (vida media = 1–4 horas) y la absorción por las plantas. Los principales fotometabolitos incluyen desnitroimidazol, olefina, urea y cinco metabolitos menores. El producto final de la fotodegradación es el ácido 6-cloronicotínico (6-CNA) y, en última instancia, el dióxido de carbono. Dado que el imidacloprid tiene una presión de vapor baja , normalmente no se volatiliza fácilmente. [28]
Aunque el imidacloprid se descompone rápidamente en agua en presencia de luz, permanece persistente en agua en ausencia de luz. Tiene una solubilidad en agua de 0,61 g/L, que es relativamente alta. [52] En la oscuridad, a un pH entre 5 y 7, se descompone muy lentamente, y a un pH de 9, la vida media es de aproximadamente 1 año. En el suelo en condiciones aeróbicas, el imidacloprid es persistente con una vida media del orden de 1 a 3 años. En la superficie del suelo, la vida media es de 39 días. [53] Los principales metabolitos del suelo incluyen nitrosimina de imidacloprid, desnitro de imidacloprid y urea de imidacloprid, que finalmente se degradan a ácido 6-cloronicotínico, CO 2 y residuos unidos. [16] [28] Recientemente se ha demostrado que el ácido 6-cloronicotínico se mineraliza a través de una vía de ácido nicotínico (vitamina B 3 ) en una bacteria del suelo. [54]
En el suelo, el imidacloprid se une fuertemente a la materia orgánica. Cuando no se expone a la luz, el imidacloprid se descompone lentamente en el agua y, por lo tanto, tiene el potencial de persistir en las aguas subterráneas durante períodos prolongados. Sin embargo, en un estudio de las aguas subterráneas en áreas de los Estados Unidos que habían sido tratadas con imidacloprid para el barrenador esmeralda del fresno , por lo general no se detectó imidacloprid. Cuando se detectó, estaba presente en niveles muy bajos, principalmente en concentraciones inferiores a 1 parte por mil millones (ppb) con un máximo de 7 ppb, que están por debajo de los niveles de preocupación para la salud humana. Las detecciones se han producido generalmente en áreas con suelos porosos rocosos o arenosos con poca materia orgánica, donde el riesgo de lixiviación es alto y/o donde el nivel freático estaba cerca de la superficie. [55]
Debido a su alta solubilidad en agua (0,5-0,6 g/L) y persistencia, tanto la Agencia de Protección Ambiental de Estados Unidos como la Agencia Reguladora de Manejo de Plagas de Canadá consideran que el imidacloprid tiene un alto potencial de escurrirse hacia las aguas superficiales y de filtrarse hacia las aguas subterráneas, por lo que advierten de no aplicarlo en áreas donde los suelos son permeables, en particular donde el nivel freático es poco profundo. [16] [28]
Según las normas establecidas por el Ministerio de Medio Ambiente de Canadá, si se utiliza correctamente (a las dosis recomendadas, sin riego y cuando no se prevén fuertes lluvias), el imidacloprid no se filtra típicamente en las capas más profundas del suelo a pesar de su alta solubilidad en agua (Rouchaud et al. 1994; Tomlin 2000; Krohn y Hellpointner 2002). [28] En una serie de ensayos de campo realizados por Rouchaud et al. (1994, 1996), en los que se aplicó imidacloprid a parcelas de remolacha azucarera, se demostró de forma consistente que no se produjo una filtración detectable de imidacloprid en la capa de suelo de 10 a 20 cm. Se aplicó imidacloprid a un campo de maíz en Minnesota y no se encontraron residuos de imidacloprid en los segmentos de la columna de muestra por debajo del segmento de profundidad de 0 a 15,2 cm (Rice et al. 1991, como se revisó en Mulye 1995). [16] [28]
Sin embargo, un estudio de monitoreo del agua de 2012 realizado por el estado de California, mediante la recolección de escorrentía agrícola durante las temporadas de crecimiento de 2010 y 2011, encontró imidacloprid en el 89% de las muestras, con niveles que oscilaban entre 0,1 y 3,2 μg/L. El 19% de las muestras excedían el umbral de la EPA para toxicidad crónica para invertebrados acuáticos de 1,05 μg/L. Los autores también señalan que las directrices canadienses y europeas son mucho más bajas (0,23 μg/L y 0,067 μg/L, respectivamente) y se excedieron en el 73% y el 88% de las muestras, respectivamente. Los autores concluyeron que "el imidacloprid comúnmente se desplaza fuera del sitio y contamina las aguas superficiales en concentraciones que podrían dañar a los invertebrados acuáticos". [56]
Regulación
unión Europea
A mediados y finales de los años 1990, los apicultores franceses informaron de una pérdida significativa de abejas, que atribuyeron al uso de imidacloprid. [ cita requerida ] En 1999, el Ministro de Agricultura francés suspendió el uso de imidacloprid en las semillas de girasol y designó un equipo de científicos expertos para examinar el impacto del imidacloprid en las abejas. En 2003, este grupo emitió un informe que concluyó que el imidacloprid planteaba un riesgo significativo para las abejas. [57] En 2004, el Ministro de Agricultura francés suspendió el uso de imidacloprid como tratamiento de semillas de girasol y maíz. Ciertos tratamientos de semillas con imidacloprid también se prohibieron temporalmente en Italia, tras estudios de seguimiento preliminares que identificaron correlaciones entre las pérdidas de abejas y el uso de pesticidas neonicotinoides. [58]
En enero de 2013, un informe de la Autoridad Europea de Seguridad Alimentaria (AESA) concluyó que los neonicotinoides planteaban un riesgo inaceptablemente alto para las abejas: "Se identificó un alto riesgo agudo para las abejas melíferas por exposición a través de la deriva de polvo para usos de tratamiento de semillas en maíz, colza y cereales. También se identificó un alto riesgo agudo por exposición a través de residuos en el néctar y/o polen". [31] La AESA también identificó una serie de lagunas en la evidencia científica y no pudo finalizar las evaluaciones de riesgo para algunos usos autorizados en la Unión Europea (UE). Después del informe, los estados miembros de la UE votaron para restringir el uso de los tres neonicotinoides principales, incluido el imidacloprid, para el tratamiento de semillas, aplicación al suelo (gránulos) y tratamiento foliar en cultivos atractivos para las abejas. [59]
En febrero de 2018, la Autoridad Europea de Seguridad Alimentaria publicó un nuevo informe en el que concluía que los neonicotinoides representaban un grave peligro para las abejas . [31] En abril de 2018, los estados miembros de la UE decidieron prohibir los neonicotinoides para todos los usos al aire libre. [60]
Estados Unidos
El 1 de julio de 2022, la Mancomunidad de Massachusetts en los Estados Unidos prohibió las ventas comerciales de imidacloprid y otros neonicotinoides ( acetamiprid , clotianidina , dinotefurano , tiacloprid y tiametoxam ) al público en general para todos los usos al aire libre. [61] Los distribuidores autorizados podrán vender solo a personas autorizadas y certificadas para el uso de pesticidas. Los estados de Maryland, Connecticut y Vermont también restringen el uso de pesticidas neonicotinoides. [62]
Véase también
Referencias
- ^ abcde "Perfiles de información sobre plaguicidas: Imidacloprid Breaz". Red de toxicología de extensión . Consultado el 7 de abril de 2012 .
- ^ "Aspectos destacados de los productos sanitarios en 2021: Anexos de productos aprobados en 2021". Health Canada . 3 de agosto de 2022 . Consultado el 25 de marzo de 2024 .
- ^ abcdef Gervais y otros 2010.
- ^ ab Yamamoto, Izuru (1999). "De la nicotina a los nicotinoides: 1962 a 1997". En Yamamoto, Izuru; Casida, John (eds.). Insecticidas nicotinoides y el receptor nicotínico de acetilcolina . Tokio: Springer-Verlag. págs. 3–27.
- ^ ab Casida, John E. (7 de enero de 2018). "Neonicotinoides y otros moduladores competitivos del receptor nicotínico de insectos: progreso y perspectivas". Revisión anual de entomología . 63 (1). Revisiones anuales : 125–144. doi :10.1146/annurev-ento-020117-043042. ISSN 0066-4170. PMID 29324040.
- ^ ab Ihara, Makoto; Matsuda, Kazuhiko (2018). "Neonicotinoides: mecanismos moleculares de acción, conocimientos sobre la resistencia y el impacto en los polinizadores". Current Opinion in Insect Science . 30 . Elsevier : 86–92. doi :10.1016/j.cois.2018.09.009. ISSN 2214-5745. PMID 30553491. S2CID 58767188.
- ^ "Imidacloprid: evaluación de riesgos ecológicos y para la salud humana. Informe final" (PDF) . Servicio Forestal del USDA. 2005. Archivado desde el original (PDF) el 13 de mayo de 2021. Consultado el 23 de julio de 2021 .
- ^ ab "Bayer seedgrowth". Bayer SeedGrowth . Archivado desde el original el 17 de enero de 2021. Consultado el 11 de abril de 2021 .
- ^ abc Herms DA, McCullough DG, Smitley DR, Sadof C, Williamson RC, Nixon PL (2009). "Opciones de insecticidas para proteger a los fresnos del barrenador esmeralda del fresno" (PDF) . Boletín del Centro de Manejo Integrado de Plagas del Norte Central. Archivado desde el original (PDF) el 26 de enero de 2016. Consultado el 7 de abril de 2012 .
- ^ Informe del Servicio de Evaluación del Consejo Internacional de Códigos ESR-1851, de agosto de 2011. Archivado el 12 de diciembre de 2018 en Wayback Machine.
- ^ "Neonicotinoides: riesgos para las abejas confirmados | EFSA". www.efsa.europa.eu . 2018-02-28 . Consultado el 2023-06-23 .
- ^ "Conclusión sobre la revisión por pares de la evaluación de riesgos de los plaguicidas para las abejas en relación con la sustancia activa clotianidina". EFSA Journal . 11 : 3066. 2013. doi :10.2903/j.efsa.2013.3066.
- ^ US EPA, OCSPP (16 de junio de 2022). "La EPA finaliza las evaluaciones biológicas que evalúan los efectos potenciales de tres pesticidas neonicotinoides en especies en peligro de extinción". www.epa.gov . Consultado el 23 de junio de 2023 .
- ^ Carrington, Damian (27 de abril de 2018). «La UE acuerda la prohibición total de los pesticidas que dañan a las abejas». The Guardian . ISSN 0261-3077 . Consultado el 23 de junio de 2023 .
- ^ Milman, Oliver (8 de marzo de 2022). "Temores por las abejas mientras Estados Unidos se dispone a ampliar el uso de pesticidas tóxicos que paralizan a los insectos". The Guardian . ISSN 0261-3077 . Consultado el 23 de junio de 2023 .
- ^ abcdef Federoff, NE; Vaughan, Allen; Barrett, MR (13 de noviembre de 2008). "Formulación del problema de la División de destino y efectos ambientales para la revisión del registro de imidacloprid". US EPA . Consultado el 18 de abril de 2012 .
- ^ Preston, Richard (2007). "Una muerte en el bosque". The New Yorker .
- ^ ab Servicio Geológico de Estados Unidos (12 de octubre de 2021). «Uso anual estimado de pesticidas agrícolas para imidacloprid, 2019» . Consultado el 24 de enero de 2022 .
- ^ "Acciones de la EPA para proteger a los polinizadores". US EPA . 3 de septiembre de 2013 . Consultado el 24 de enero de 2022 .
- ^ Allington A (21 de mayo de 2019). "La EPA frena el uso de 12 pesticidas que dañan a las abejas". Bloomberg . Consultado el 24 de enero de 2022 .
- ^ Bayer (abril de 2021). «Insecticidas neonicotinoides» (PDF) . Consultado el 24 de enero de 2022 .
- ^ Patente de EE. UU. N.º 4.742.060 Archivado el 20 de septiembre de 2018 en Wayback Machine - uspto.gov
- ^ abcd «Índice de imidacloprid (código PC 129099) – Pesticidas». US EPA . 27 de julio de 2011 . Consultado el 24 de julio de 2021 .
- ^ Imidacloprid; Tolerancias de pesticidas para exenciones de emergencia Registro Federal: 26 de enero de 2005 (volumen 70, número 16), páginas 3634-3642- epa.gov
- ^ "Insecticida Confidor". Bayer CropScience India . Archivado desde el original el 19 de abril de 2021. Consultado el 11 de abril de 2021 .
- ^ US EPA ( United States Environmental Protection Agency ) (2015-04-21). "Enmienda de la etiqueta: revisiones menores de la etiqueta Nombre del producto: Insecticida granulado para invernaderos y viveros Marathon al 1 % Número de registro de la EPA: 59807-15 Fecha de solicitud: 17 de marzo de 2015 Número de decisión: 502678" (PDF) . Archivado desde el original (PDF) el 2021-04-11.
- ^ OHP. "MARATHON 1% Granular" (PDF) . Archivado desde el original (PDF) el 16 de mayo de 2018.
- ^ abcdefghij Consejo Canadiense de Ministros de Medio Ambiente (2007). Directrices canadienses sobre calidad del agua: imidacloprid: documento de apoyo científico (PDF) . Winnipeg, Manitoba: Consejo Canadiense de Ministros de Medio Ambiente. ISBN 978-1-896997-71-1Archivado desde el original (PDF) el 19 de marzo de 2013. Consultado el 13 de febrero de 2012 .
- ^ Destino ambiental del imidacloprid Archivado el 16 de marzo de 2012 en Wayback Machine Departamento de Regulación de Pesticidas de California 2006
- ^ "Imidacloprid: Documento de caracterización de riesgos: exposición a través de la dieta y el agua potable" (PDF) . Agencia de Protección Ambiental de California. 9 de febrero de 2006 . Consultado el 7 de abril de 2012 .
- ^ abcd "Conclusión sobre la revisión por pares de la evaluación de riesgos de los plaguicidas para las abejas en relación con la sustancia activa clotianidina". EFSA Journal . 11 : 3066. 2013. doi :10.2903/j.efsa.2013.3066.
- ^ Programa de detección de disruptores endocrinos: Anuncio de emisión de orden de detección de nivel 1. Aviso del Registro Federal, 21 de octubre de 2009. Vol. 74, N.º 202, págs. 54422-54428
- ^ USDA, Forest Service, Forest Health Protection (28 de diciembre de 2005). Imidacloprid – Human Health and Ecological Risk Assessment – Final Report "HUMAN HEALTH RISK ASSESSMENT / Overview. 3-1". Servicio Forestal de los Estados Unidos . Consultado el 30 de julio de 2013. [ enlace roto ]
- ^ abc Suchail, Séverine; Guez, David; Belzunces, Luc P. (noviembre de 2001). "Discrepancia entre la toxicidad aguda y crónica inducida por imidacloprid y sus metabolitos en Apis mellifera ". Toxicología y química ambiental . 20 (11): 2482–2486. doi :10.1002/etc.5620201113. PMID 11699773. S2CID 22209995.
- ^ Suchail, Séverine; Guez, David; Belzunces, Luc P. (julio de 2000). "Características de la toxicidad del imidacloprid en dos subespecies de Apis mellifera" (PDF) . Toxicología y química ambiental . 19 (7): 1901–1905. doi :10.1002/etc.5620190726. S2CID 84822758.
- ^ Armengaud, C.; Lambin, M.; Gauthier, M. (2002), "Efectos del imidacloprid en los procesos neuronales de la memoria", en Devillers, J; Pham-Delegue, MH (eds.), Abejas melíferas: estimación del impacto ambiental de los productos químicos , Nueva York: Taylor & Francis, págs. 85-100, ISBN 9780415275187
- ^ Decourtye, A; Lacassie, E; Pham-Delegue, MH (2003). "El rendimiento de aprendizaje de las abejas ( Apis mellifera L ) se ve afectado de forma diferente por el imidacloprid según la estación". Pest Manag. Sci . 59 (3): 269–278. doi :10.1002/ps.631. PMID 12639043.
- ^ Decourtye, A.; Armengaud, C.; Devillers, RM; Cluzeau, S. (2004). "El imidacloprid afecta la memoria y el metabolismo cerebral en la abeja melífera ( Apis mellifera L )". Pesticide Biochem Phys . 78 (2): 83–92. doi :10.1016/j.pestbp.2003.10.001.
- ^ Guez, D.; Suchail, S.; Gauthier, M.; Maleszka, R.; Belzunces, L. (2001). "Efectos contrastantes del imidacloprid en la habituación en abejas de 7 y 8 días de edad ( Apis mellifera )". Neurobiología del aprendizaje y la memoria . 76 (2): 183–191. doi :10.1006/nlme.2000.3995. PMID 11502148. S2CID 17822619.
- ^ Pham-Delegue, MH; Cluzeau, S. (1999), "Effets des produits phytosanitaires sur l'abeille; incidencia du traitement des semences de tournesol par Gaucho sur les disparitions de butineuses", Rapport final de synthese au Ministere de l'Agriculture et de la Peche
- ^ Lambin, M.; Armengaud, C.; Ramond, S.; Gauthier, M. (2001). "Facilitación inducida por imidacloprid de la habituación al reflejo de extensión de la probóscide en la abeja melífera". Archivos de bioquímica y fisiología de insectos . 48 (3): 129–134. doi :10.1002/arch.1065. PMID 11673842.
- ^ Williamson, SM; Wright, GA (2013). "La exposición a múltiples pesticidas colinérgicos afecta el aprendizaje y la memoria olfativa en las abejas" (PDF) . Journal of Experimental Biology . 216 (10): 1799–1807. doi : 10.1242/jeb.083931. ISSN 0022-0949. PMC 3641805. PMID 23393272.
- ^ "Neonicotinoides". Pollinator Network @ Cornell . Consultado el 10 de mayo de 2019 .
- ^ Gill RJ; Ramos-Rodriguez O.; Raine NE (2012). "La exposición combinada a pesticidas afecta gravemente los rasgos a nivel individual y de colonia en las abejas". Nature . 491 (7422): 105–108. Bibcode :2012Natur.491..105G. doi :10.1038/nature11585. PMC 3495159 . PMID 23086150.
- ^ Bryden, John; Gill, Richard J.; Mitton, Robert AA; Raine, Nigel E.; Jansen, Vincent AA (2013). "El estrés subletal crónico provoca el fracaso de las colonias de abejas". Ecology Letters . 16 (12): 1463–1469. doi :10.1111/ele.12188. PMC 4299506 . PMID 24112478.
- ^ Erban T.; Sopko B.; Talacko P.; Harant K.; Kadlikova K.; Halesova T.; Riddellova K.; Pekas A. (2019). "La exposición crónica de los abejorros al neonicotinoide imidacloprid suprime toda la vía del mevalonato y la síntesis de ácidos grasos". J Proteomics . 196 : 69–80. doi :10.1016/j.jprot.2018.12.022. PMID 30583045. S2CID 58641344.
- ^ Hallmann CA, Foppen RP, van Turnhout CA, de Kroon H, Jongejans E (julio de 2014). "La disminución de las aves insectívoras está asociada a altas concentraciones de neonicotinoides". Nature . 511 (7509): 341–3. Bibcode :2014Natur.511..341H. doi :10.1038/nature13531. hdl : 2066/130120 . PMID 25030173. S2CID 4464169.
- ^ Frew JA, Brown JT, Fitzsimmons PN, Hoffman AD, Sadilek M, Grue CE, Nichols, JW (febrero de 2018). "Toxicocinética del insecticida neonicotinoide imidacloprid en la trucha arcoíris (Oncorhynchus mykiss)". Comp Biochem Physiol C . 205 : 34–42. doi :10.1016/j.cbpc.2018.01.002. PMC 5847319 . PMID 29378254.
- ^ "Análisis de riesgo-beneficio del imidacloprid de Bayer". greenstarsproject.org . 21 de marzo de 2021 . Consultado el 14 de diciembre de 2021 .
- ^ Cheng Y, Shi ZP, Jiang LB, Ge LQ, Wu JC, Jahn GC (marzo de 2012). "Posible conexión entre los cambios inducidos por imidacloprid en los perfiles de transcripción de genes del arroz y la susceptibilidad al insecto marrón Nilaparvatalugens Stål (Hemiptera: Delphacidae)". Pestic Biochem Physiol . 102–531 (3): 213–219. doi :10.1016/j.pestbp.2012.01.003. PMC 3334832 . PMID 22544984.
- ^ Gonias, Evangelos D.; Oosterhuis, Derrick M.; Bibi, Androniki C. (2007). "Respuesta fisiológica del algodón al insecticida imidacloprid bajo estrés por altas temperaturas". Journal of Plant Growth Regulation . 27 (1): 77–82. doi :10.1007/s00344-007-9033-4. ISSN 0721-7595. S2CID 20930112.
- ^ Flores-Céspedes, Francisco; Figueredo-Flores, Cristina Isabel; Daza-Fernández, Isabel; Vidal Peña, Fernando; Villafranca-Sánchez, Matilde; Fernández-Pérez, Manuel (18 de enero de 2012). "Preparación y caracterización de matrices de imidacloprid lignina-polietilenglicol recubiertas con etilcelulosa". Revista de Química Agrícola y Alimentaria . 60 (4): 1042-1051. doi :10.1021/jf2037483. PMID 22224401.
- ^ Matthew Fossen (2006). «Environmental Fate of Imidacloprid» (PDF) . Archivado desde el original (PDF) el 16 de marzo de 2012. Consultado el 16 de abril de 2016 .
- ^ Shettigar M, Pearce S, Pandey R, Khan F, Dorrian SJ, Balotra S, Russell RJ, Oakeshott JG, Pandey G (2012). "Clonación de una nueva clorohidrolasa de ácido 6-cloronicotínico a partir de la cepa SG-6C de Bradyrhizobiaceae mineralizante de ácido 6-cloronicotínico recientemente aislada". PLOS ONE . 7 (11): e51162. Bibcode :2012PLoSO...751162S. doi : 10.1371/journal.pone.0051162 . PMC 3511419 . PMID 23226482.
- ^ Hahn, Jeffrey; Herms, Daniel A.; McCullough, Deborah G. (febrero de 2011). "Preguntas frecuentes sobre los posibles efectos secundarios de los insecticidas sistémicos utilizados para controlar el barrenador esmeralda del fresno" Archivado el 1 de agosto de 2012 en Wayback Machine . Extensión de la Universidad de Michigan, Universidad Estatal de Michigan, Extensión de la Universidad Estatal de Ohio.
- ^ Starner, Keith; Goh, Kean S. (2012). "Detecciones de imidacloprid en aguas superficiales de tres regiones agrícolas de California, EE. UU., 2010-2011". Boletín de contaminación ambiental y toxicología . 88 (3): 316–321. doi :10.1007/s00128-011-0515-5. PMID 22228315. S2CID 18454777.
- ^ Comité Scientifique et Technique (18 de septiembre de 2003). "Imidaclopride utilisé en enrobage de semences (Gaucho) et problems des abeilles: Rapport final" [Imidacloprid utilizado para recubrir semillas (Gaucho) y trastornos de las abejas: informe final] (PDF) (en francés). Archivado desde el original (PDF) el 16 de marzo de 2012 . Consultado el 18 de abril de 2012 .
- ^ "Trastorno de colapso de colonias: prohibiciones europeas de pesticidas neonicotinoides – Pesticidas – EPA de EE. UU.". epa.gov . 23 de junio de 2010. Archivado desde el original el 4 de septiembre de 2011 . Consultado el 24 de julio de 2021 .
- ^ McDonald-Gibson, Charlotte (29 de abril de 2013). «'Victoria para las abejas' cuando la Unión Europea prohíbe los pesticidas neonicotinoides a los que se culpa de destruir la población de abejas». The Independent . Archivado desde el original el 1 de mayo de 2013. Consultado el 1 de mayo de 2013 .
- ^ "La UE prohibirá por completo los insecticidas neonicotinoides para proteger a las abejas". Reuters . 27 de abril de 2018 . Consultado el 29 de abril de 2018 .
- ^ "PREGUNTAS FRECUENTES, Cambio de registro de pesticidas que contienen neonicotinoides".
- ^ "Los reguladores de Massachusetts restringirán el uso por parte de los consumidores de pesticidas neonicotinoides tóxicos para las abejas".
Enlaces externos
- Gervais, JA; Luukinen, B.; Buhl, K.; Stone, D. (2010). "Ficha técnica de imidacloprid". Centro Nacional de Información sobre Pesticidas . Consultado el 23 de julio de 2021 .
- "CHO – Hoja informativa sobre el insecticida Merit que mata larvas y que contiene imidacloprid". flora.org . 21 de junio de 2012. Archivado desde el original el 21 de junio de 2012 . Consultado el 24 de julio de 2021 .
- "Imidacloprid – Bayer". Resumen de expertos . 9 de octubre de 2006. Archivado desde el original el 9 de octubre de 2006 . Consultado el 24 de julio de 2021 .
{{cite web}}: CS1 maint: URL no apta ( enlace ) - Imidacloprid en la base de datos de propiedades de pesticidas (PPDB)



