Melatonina
 | |
 | |
| Nombres | |
|---|---|
| Nombre IUPAC N-[2-(5-metoxi-1H-indol-3-il)etil]acetamida | |
| Otros nombres 5-Metoxi-N-acetiltriptamina; N-Acetil-5-metoxitriptamina; NSC-113928 | |
| Identificadores | |
| |
Modelo 3D ( JSmol ) |
|
| EBICh |
|
| Química biológica |
|
| Araña química |
|
| Banco de medicamentos |
|
| Tarjeta informativa de la ECHA | 100.000.725 |
| Número CE |
|
| BARRIL |
|
| Malla | Melatonina |
Identificador de centro de PubChem |
|
| UNIVERSIDAD |
|
Panel de control CompTox ( EPA ) |
|
| |
| |
| Propiedades | |
| C13H16N2O2 | |
| Masa molar | 232,281 g/mol |
| Punto de fusión | 117 |
Salvo que se indique lo contrario, los datos se proporcionan para los materiales en su estado estándar (a 25 °C [77 °F], 100 kPa). | |
La melatonina , una indolamina , es un compuesto natural producido por varios organismos , entre ellos bacterias y eucariotas . [1] Su descubrimiento en 1958 por Aaron B. Lerner y sus colegas se debió al aislamiento de una sustancia de la glándula pineal de las vacas que podía inducir el aclaramiento de la piel en las ranas comunes . Este compuesto fue identificado posteriormente como una hormona secretada en el cerebro durante la noche, que desempeña un papel crucial en la regulación del ciclo sueño-vigilia , también conocido como ritmo circadiano, en los vertebrados . [2] [3]
En los vertebrados, las funciones de la melatonina se extienden a la sincronización de los ciclos sueño-vigilia, abarcando el tiempo sueño-vigilia y la regulación de la presión arterial , así como el control de la ritmicidad estacional ( ciclo circanual ), que incluye la reproducción, el engorde, la muda y la hibernación. [4] Sus efectos están mediados por la activación de los receptores de melatonina y su papel como antioxidante . [5] [6] [7] En plantas y bacterias, la melatonina sirve principalmente como un mecanismo de defensa contra el estrés oxidativo , lo que indica su importancia evolutiva. [8] Las mitocondrias , orgánulos clave dentro de las células, son los principales productores de melatonina antioxidante, [9] lo que subraya los "orígenes antiguos" de la molécula y su papel fundamental en la protección de las primeras células de las especies reactivas de oxígeno . [10] [11]
Además de sus funciones endógenas como hormona y antioxidante, la melatonina también se administra de forma exógena como suplemento dietético y medicamento . Se utiliza en el tratamiento de trastornos del sueño , incluidos el insomnio y diversos trastornos del ritmo circadiano del sueño .
Actividad biológica
En los seres humanos, la melatonina actúa principalmente como un potente agonista completo de dos tipos de receptores de melatonina : el receptor de melatonina 1 , con afinidad de unión picomolar , y el receptor de melatonina 2 , con afinidad de unión nanomolar. Ambos receptores son parte de la familia de receptores acoplados a proteína G (GPCR), específicamente los GPCR de la subunidad alfa de G i/o , [12] [13] aunque el receptor de melatonina 1 también exhibe acoplamiento con la subunidad alfa de G q . [12]
Además, la melatonina funciona como un antioxidante de alta capacidad , o eliminador de radicales libres, dentro de las mitocondrias , desempeñando un doble papel en la lucha contra el estrés oxidativo celular . En primer lugar, neutraliza directamente los radicales libres , y en segundo lugar, promueve la expresión génica de enzimas antioxidantes esenciales, como la superóxido dismutasa , la glutatión peroxidasa , la glutatión reductasa y la catalasa . Este aumento en la expresión de enzimas antioxidantes está mediado por vías de transducción de señales activadas por la unión de la melatonina a sus receptores. A través de estos mecanismos, la melatonina protege a la célula contra el estrés oxidativo de dos maneras, y desempeña otras funciones en la salud humana además de regular el ciclo sueño-vigilia. [14] [12] [15] [16] [17] [18]
Funciones biológicas
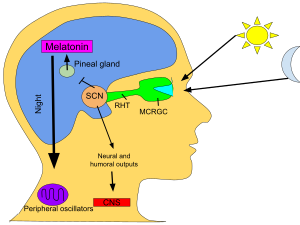
Ritmo circadiano
En los mamíferos, la melatonina es fundamental para la regulación de los ciclos de sueño-vigilia, o ritmos circadianos. [19] El establecimiento de niveles regulares de melatonina en los bebés humanos ocurre alrededor del tercer mes después del nacimiento, con concentraciones máximas observadas entre la medianoche y las 8:00 am. [ 20 ] Se ha documentado que la producción de melatonina disminuye a medida que una persona envejece. [21] Además, se observa un cambio en el momento de la secreción de melatonina durante la adolescencia, lo que resulta en tiempos de sueño y vigilia retrasados, lo que aumenta su riesgo de trastorno de la fase de sueño retrasado durante este período. [22]
Las propiedades antioxidantes de la melatonina se reconocieron por primera vez en 1993. [23] Los estudios in vitro revelan que la melatonina neutraliza directamente varias especies reactivas de oxígeno , incluyendo hidroxilo (OH•), superóxido (O2−•), y especies reactivas de nitrógeno como el óxido nítrico (NO•). [24] [25] En las plantas, la melatonina trabaja sinérgicamente con otros antioxidantes, mejorando la eficacia general de cada antioxidante. [25] Se ha descubierto que este compuesto es dos veces más eficaz que la vitamina E , un conocido antioxidante lipofílico potente , para combatir el estrés oxidativo. [26] La promoción de la expresión de enzimas antioxidantes, como la superóxido dismutasa, la glutatión peroxidasa, la glutatión reductasa y la catalasa, está mediada por vías de transducción de señales activadas por el receptor de melatonina. [12] [14]
La concentración de melatonina en la matriz mitocondrial es significativamente mayor que la que se encuentra en el plasma sanguíneo , [15] [16] [17] lo que enfatiza su papel no solo en la eliminación directa de radicales libres sino también en la modulación de la expresión de enzimas antioxidantes y el mantenimiento de la integridad mitocondrial. Este papel multifacético muestra la importancia fisiológica de la melatonina como antioxidante mitocondrial, una noción apoyada por numerosos académicos. [14] [15] [16] [17] [18]
Además, la interacción de la melatonina con especies reactivas de oxígeno y nitrógeno da como resultado la formación de metabolitos capaces de reducir los radicales libres. [12] [18] Estos metabolitos, incluidos la 3-hidroximelatonina cíclica , la N1-acetil-N2-formil-5-metoxiquinuramina (AFMK) y la N1-acetil-5-metoxiquinuramina (AMK), contribuyen a los efectos antioxidantes más amplios de la melatonina a través de otras reacciones redox con radicales libres. [12] [18]
Sistema inmunitario
Se reconoce la interacción de la melatonina con el sistema inmunológico , pero los detalles de estas interacciones siguen estando inadecuadamente definidos. [27] [28] [ necesita actualización ] Un efecto antiinflamatorio parece ser el más significativo. [ cita requerida ] La eficacia de la melatonina en el tratamiento de enfermedades ha sido objeto de ensayos limitados, y la mayoría de los datos disponibles derivan de estudios preliminares a pequeña escala. Se postula que cualquier impacto inmunológico beneficioso es atribuible a la acción de la melatonina sobre los receptores de alta afinidad (MT1 y MT2), que están presentes en las células inmunocompetentes. Las investigaciones preclínicas sugieren que la melatonina puede aumentar la producción de citocinas y promover la expansión de las células T , [29] mitigando potencialmente así las inmunodeficiencias adquiridas . [30]
Regulación del peso
Se cree que el potencial de la melatonina para regular el aumento de peso implica su efecto inhibidor sobre la leptina , una hormona que sirve como indicador a largo plazo del estado energético del cuerpo. [31] [32] La leptina es importante para regular el equilibrio energético y el peso corporal al indicar saciedad y reducir la ingesta de alimentos. La melatonina, al modular las acciones de la leptina fuera de las horas de vigilia, puede contribuir a la restauración de la sensibilidad a la leptina durante el día, contrarrestando así la resistencia a la leptina .
Bioquímica
Biosíntesis

La biosíntesis de melatonina en animales implica una secuencia de reacciones enzimáticas que comienzan con el L -triptófano , que puede sintetizarse a través de la vía del shikimato a partir del corismato , que se encuentra en las plantas, u obtenerse a partir del catabolismo proteico . El paso inicial en la vía de biosíntesis de melatonina es la hidroxilación del anillo indólico del L -triptófano por la enzima triptófano hidroxilasa , lo que da como resultado la formación de 5-hidroxitriptófano (5-HTP). Posteriormente, el 5-HTP sufre una descarboxilación , facilitada por el fosfato de piridoxal y la enzima 5-hidroxitriptófano descarboxilasa , lo que produce serotonina . [33]
La serotonina, un neurotransmisor esencial , se convierte además en N -acetilserotonina por la acción de la serotonina N -acetiltransferasa , utilizando acetil-CoA . [34] El paso final en la vía implica la metilación del grupo hidroxilo de la N -acetilserotonina por la hidroxiindol O -metiltransferasa , con S -adenosil metionina como donante de metilo , para producir melatonina. [34]
En bacterias , protistos , hongos y plantas, la síntesis de melatonina también involucra al triptófano como intermediario, pero se origina indirectamente a partir de la vía del shikimato. La vía comienza con D -eritrosa 4-fosfato y fosfoenolpiruvato , y en las células fotosintéticas , involucra además dióxido de carbono . Si bien las reacciones biosintéticas posteriores comparten similitudes con las de los animales, existen ligeras variaciones en las enzimas involucradas en las etapas finales. [35] [36]
La hipótesis de que la síntesis de melatonina ocurre dentro de las mitocondrias y los cloroplastos sugiere una importancia evolutiva y funcional de la melatonina en el metabolismo energético celular y los mecanismos de defensa contra el estrés oxidativo, lo que refleja los orígenes antiguos de la molécula y sus funciones multifacéticas en diferentes dominios de la vida . [37]
Mecanismo

El mecanismo de biosíntesis de la melatonina se inicia con la hidroxilación del L -triptófano, un proceso que requiere que el cofactor tetrahidrobiopterina (THB) reaccione con el oxígeno y el hierro del sitio activo de la triptófano hidroxilasa. Aunque no se comprende por completo el mecanismo completo, se han propuesto dos mecanismos principales:
El primer mecanismo implica una transferencia lenta de un electrón del THB al oxígeno molecular (O 2 ), produciendo potencialmente un superóxido ( O−2). Este superóxido podría luego recombinarse con el radical THB para formar 4a-peroxipterina. La 4a-peroxipterina puede reaccionar con el hierro del sitio activo (II) para crear un intermedio hierro-peroxipterina o transferir directamente un átomo de oxígeno al hierro, facilitando la hidroxilación del L -triptófano.
Alternativamente, el segundo mecanismo propone que el oxígeno interactúa primero con el hierro (II) del sitio activo, formando superóxido de hierro (III). Esta molécula podría reaccionar luego con THB para formar un intermediario de hierro-peroxipterina.
Tras la formación de óxido de hierro (IV) a partir del intermediario hierro-peroxipterina, este óxido ataca selectivamente un doble enlace para producir un carbocatión en la posición C5 del anillo indólico. Un desplazamiento 1,2 posterior del hidrógeno y la pérdida de uno de los dos átomos de hidrógeno en C5 restaurarían la aromaticidad , produciendo 5-hidroxi- L -triptófano. [38]
La descarboxilación del 5-hidroxi- L -triptófano para producir 5-hidroxitriptamina es facilitada por una enzima descarboxilasa con fosfato de piridoxal (PLP) como cofactor. [39] El PLP forma una imina con el derivado del aminoácido, lo que facilita la ruptura del enlace carbono-carbono y la liberación de dióxido de carbono. La protonación de la amina derivada del triptófano restaura la aromaticidad del anillo de piridina , lo que conduce a la producción de 5-hidroxitriptamina y PLP. [40]
Se ha planteado la hipótesis de que la serotonina N -acetiltransferasa, con el residuo de histidina His122, desprotona la amina primaria de la 5-hidroxitriptamina. Esta desprotonación permite que el par solitario de la amina ataque al acetil-CoA, formando un intermediario tetraédrico . El tiol de la coenzima A actúa entonces como un grupo saliente cuando es atacado por una base general, produciendo N -acetilserotonina. [41]
El paso final en la biosíntesis de la melatonina implica la metilación de la N -acetilserotonina en la posición hidroxilo por SAM, lo que resulta en la producción de S -adenosil homocisteína (SAH) y melatonina. [40] [42]
Regulación
En los vertebrados, la secreción de melatonina se regula a través de la activación del receptor beta-1 adrenérgico por la hormona noradrenalina . [43] La noradrenalina aumenta la concentración de AMPc intracelular a través de los receptores beta-adrenérgicos , que a su vez activa la proteína quinasa A dependiente de AMPc (PKA). Luego, la PKA fosforila la arilalquilamina N -acetiltransferasa (AANAT), la penúltima enzima en la vía de síntesis de melatonina. Cuando se expone a la luz del día, la estimulación noradrenérgica cesa, lo que lleva a la degradación inmediata de la proteína por proteólisis proteasomal . [44] La producción de melatonina se reanuda por la noche, una fase conocida como el inicio de la melatonina en luz tenue .
La luz azul, especialmente en el rango de 460 a 480 nm , inhibe la biosíntesis de melatonina [45] , siendo el grado de supresión directamente proporcional a la intensidad y duración de la exposición a la luz. Históricamente, los seres humanos en climas templados experimentaron una exposición limitada a la luz azul del día durante los meses de invierno, recibiendo principalmente luz de fuentes que emitían luz predominantemente amarilla, como los incendios [46] Las bombillas incandescentes utilizadas ampliamente a lo largo del siglo XX emitían niveles relativamente bajos de luz azul [47] Se ha descubierto que la luz que contiene solo longitudes de onda superiores a 530 nm no suprime la melatonina en condiciones de luz brillante [48] El uso de anteojos que bloquean la luz azul en las horas previas a la hora de acostarse puede mitigar la supresión de melatonina [49] Además, se recomienda el uso de anteojos que bloqueen la luz azul durante las últimas horas antes de acostarse para las personas que necesitan adaptarse a una hora de acostarse más temprana, ya que la melatonina facilita el inicio del sueño [50] .
Metabolismo
La melatonina se metaboliza con una vida media de eliminación que varía de 20 a 50 minutos. [51] [2] [52] La vía metabólica primaria transforma la melatonina en 6-hidroximelatonina , que luego se conjuga con sulfato y se excreta en la orina como un producto de desecho. [53] Se metaboliza principalmente por la enzima hepática CYP1A2 y en menor medida por CYP1A1 , CYP2C19 y CYP1B1 . [53]
Medición
Tanto para fines de investigación como clínicos, los niveles de melatonina en humanos se pueden determinar mediante análisis de saliva o plasma sanguíneo. [54]
Uso como medicamento y suplemento.
La melatonina se utiliza tanto como medicamento recetado como suplemento dietético de venta libre para el tratamiento de los trastornos del sueño , incluido el insomnio y varios trastornos del sueño del ritmo circadiano , como el trastorno de la fase de sueño retrasada , el trastorno del desfase horario y el trastorno del sueño por trabajo a turnos . [55] Además de la melatonina, en medicina se utilizan una variedad de agonistas sintéticos del receptor de melatonina , a saber, ramelteón , tasimelteón y agomelatina . [56] [57]
Un estudio publicado por el Journal of the American Medical Association (JAMA) en abril de 2023 encontró que un 12% de las 30 preparaciones de productos de melatonina analizadas tenían cantidades de melatonina dentro del ±10% de las cantidades especificadas en sus etiquetas. Se encontró que algunos suplementos contenían hasta un 347% del contenido declarado de melatonina. En Europa, la melatonina está clasificada como un ingrediente farmacéutico activo , lo que destaca la supervisión regulatoria de su uso y distribución. Por el contrario, a partir de 2022 [actualizar], Estados Unidos estaba considerando la inclusión de la melatonina en las prácticas de preparación de compuestos farmacéuticos . Un estudio anterior de 2022 concluyó que el consumo de productos de melatonina no regulados puede exponer a las personas, incluidos los niños, a cantidades de melatonina que van desde 40 a 130 veces más altas que los niveles recomendados cuando los productos se usan "según las indicaciones". [58]
Historia
Descubrimiento
El descubrimiento de la melatonina está vinculado al estudio de los cambios de color de la piel en algunos anfibios y reptiles, un fenómeno observado inicialmente a través de la administración de extractos de la glándula pineal. [59] [60] En 1917, Carey Pratt McCord y Floyd P. Allen descubrieron que la alimentación con extractos de las glándulas pineales de las vacas hacía que la piel de los renacuajos se aclarara al contraer los melanóforos epidérmicos oscuros . [61] [62]
La hormona melatonina fue aislada en 1958 por Aaron B. Lerner , profesor de dermatología , y su equipo de la Universidad de Yale . Motivados por la posibilidad de que una sustancia de la glándula pineal pudiera ser beneficiosa en el tratamiento de enfermedades de la piel , extrajeron e identificaron la melatonina a partir de extractos de glándula pineal bovina. [63] Investigaciones posteriores a mediados de la década de 1970 realizadas por Lynch y otros demostraron que la producción de melatonina sigue un ritmo circadiano en las glándulas pineales humanas. [64]
La primera patente para el uso terapéutico de la melatonina como ayuda para dormir en dosis bajas fue otorgada a Richard Wurtman en el Instituto Tecnológico de Massachusetts en 1995. [65]
Etimología
La etimología de la melatonina se deriva de sus propiedades aclarantes de la piel. Como se detalla en su publicación en el Journal of the American Chemical Society , [66] Lerner y sus colegas propusieron el nombre melatonina, derivado de las palabras griegas melas , que significa 'negro' u 'oscuro', y tonos , que significa 'trabajo', [67] 'color' [68] o 'suprimir'. [69] Esta convención de nomenclatura sigue la de la serotonina , otro agente que afecta el color de la piel, descubierto en 1948 como modulador del tono vascular , que influyó en su nombre basado en su efecto vasoconstrictor sérico. [70] Por lo tanto, la melatonina recibió el nombre acertado para reflejar su papel en la prevención del oscurecimiento de la piel, destacando la intersección de la bioquímica y la lingüística en el descubrimiento científico. [66]
Aparición
Animales y humanos
En los vertebrados, la melatonina se produce en la oscuridad, por lo tanto, generalmente por la noche, por la glándula pineal , una pequeña glándula endocrina [71] ubicada en el centro del cerebro pero fuera de la barrera hematoencefálica . La información de luz/oscuridad llega a los núcleos supraquiasmáticos desde las células ganglionares fotosensibles de la retina de los ojos [72] [73] en lugar de la señal de melatonina (como se postuló alguna vez). Conocida como "la hormona de la oscuridad", la aparición de melatonina al anochecer promueve la actividad en los animales nocturnos (activos de noche) y el sueño en los diurnos , incluidos los humanos. [74]
En los seres humanos, se producen aproximadamente 30 μg de melatonina al día y el 80 % de la cantidad total se produce durante la noche. La concentración plasmática máxima de melatonina durante la noche es de 80 a 120 pg/ml y las concentraciones durante el día están entre 10 y 20 pg/ml. [75] [76]
Muchos animales y humanos utilizan la variación en la duración de la producción de melatonina cada día como un reloj estacional. [77] En animales, incluidos los humanos, [78] el perfil de la síntesis y secreción de melatonina se ve afectado por la duración variable de la noche en verano en comparación con el invierno. El cambio en la duración de la secreción sirve así como una señal biológica para la organización de funciones estacionales dependientes de la duración del día ( fotoperiódicas ), como la reproducción, el comportamiento, el crecimiento del pelaje y la coloración del camuflaje en animales estacionales. [78] En los reproductores estacionales que no tienen largos períodos de gestación y que se aparean durante las horas de luz del día más largas, la señal de melatonina controla la variación estacional en su fisiología sexual, y la melatonina exógena puede inducir efectos fisiológicos similares en animales, incluidos los pájaros miná [79] y los hámsteres. [80] La melatonina puede suprimir la libido al inhibir la secreción de la hormona luteinizante y la hormona estimulante del folículo de la glándula pituitaria anterior , especialmente en mamíferos que tienen una temporada de reproducción cuando las horas de luz del día son largas. La melatonina inhibe la reproducción de las hembras de día largo , mientras que estimula la reproducción de las hembras de día corto . En las ovejas, la administración de melatonina también ha demostrado tener un efecto antioxidante e inmunomodulador en las crías estresadas prenatalmente, ayudándolas a sobrevivir los primeros días cruciales de sus vidas. [81]
Durante la noche, la melatonina regula la leptina , reduciendo sus niveles.
Los cetáceos han perdido todos los genes que sintetizan la melatonina, así como los que codifican para sus receptores. [82] Se cree que esto está relacionado con su patrón de sueño unihemisférico (un hemisferio cerebral a la vez). Se han encontrado tendencias similares en los sirenios . [82]
Plantas
Hasta su identificación en plantas en 1987, durante décadas se creyó que la melatonina era principalmente una neurohormona animal. Cuando se identificó la melatonina en extractos de café en la década de 1970, se creyó que era un subproducto del proceso de extracción. Sin embargo, posteriormente se ha encontrado melatonina en todas las plantas que se han investigado. Está presente en todas las diferentes partes de las plantas, incluidas las hojas, los tallos, las raíces, los frutos y las semillas, en proporciones variables. [8] [83] Las concentraciones de melatonina difieren no solo entre especies de plantas, sino también entre variedades de la misma especie dependiendo de las condiciones agronómicas de crecimiento, variando desde picogramos hasta varios microgramos por gramo. [36] [84] Se han medido concentraciones notablemente altas de melatonina en bebidas populares como el café, el té, el vino y la cerveza, y en cultivos como el maíz, el arroz, el trigo, la cebada y la avena. [8] En algunos alimentos y bebidas comunes, incluidos el café [8] y las nueces, [85] se ha estimado o medido que la concentración de melatonina es suficientemente alta como para elevar el nivel de melatonina en sangre por encima de los valores basales diurnos.
Aunque no se ha establecido claramente el papel de la melatonina como hormona vegetal, su participación en procesos como el crecimiento y la fotosíntesis está bien establecida. Solo se ha demostrado evidencia limitada de ritmos circadianos endógenos en los niveles de melatonina en algunas especies de plantas y no se han descrito receptores unidos a la membrana análogos a los conocidos en animales. Más bien, la melatonina desempeña funciones importantes en las plantas como regulador del crecimiento, así como protector del estrés ambiental. Se sintetiza en las plantas cuando están expuestas tanto a estreses biológicos, por ejemplo, infección por hongos, como a estreses no biológicos como temperaturas extremas, toxinas, aumento de la salinidad del suelo , sequía, etc. [36] [86] [87]
El estrés oxidativo inducido por herbicidas se ha mitigado experimentalmente in vivo en un arroz transgénico con alto contenido de melatonina . [88] [89] [90] Estudios realizados en lechuga cultivada en condiciones de suelo salino han demostrado que la aplicación de melatonina mitiga significativamente los efectos nocivos de la salinidad. La aplicación foliar aumenta el número de hojas, su superficie, aumenta el peso fresco y el contenido de clorofila a y clorofila b, y el contenido de carotenoides en comparación con plantas no tratadas con melatonina. [90]
La resistencia a enfermedades fúngicas es otra función. La melatonina añadida aumenta la resistencia en Malus prunifolia contra Diplocarpon mali . [89] [91] También actúa como un inhibidor del crecimiento de patógenos fúngicos, incluidos Alternaria , Botrytis y Fusarium spp. Disminuye la velocidad de infección. Como tratamiento de semillas , protege a Lupinus albus de los hongos. Ralentiza drásticamente la infección de Arabidopsis thaliana por Pseudomonas syringae en tomate DC3000 y la infección de Nicotiana benthamiana . [91]
Hongos
Se ha observado que la melatonina reduce la tolerancia al estrés en Phytophthora infestans en sistemas planta-patógeno. [92] La compañía farmacéutica danesa Novo Nordisk ha utilizado levadura genéticamente modificada ( Saccharomyces cerevisiae ) para producir melatonina. [93]
Bacteria
La melatonina es producida por las α-proteobacterias y las cianobacterias fotosintéticas. No hay informes de su presencia en arqueas, lo que indica que la melatonina se originó en bacterias [11], probablemente para proteger a las primeras células de los efectos dañinos del oxígeno en la atmósfera de la Tierra primitiva. [10]
Novo Nordisk ha utilizado Escherichia coli genéticamente modificada para producir melatonina. [94] [95]
Arqueas
En 2022, el descubrimiento de la serotonina N-acetiltransferasa (SNAT) , la penúltima enzima limitante de la velocidad en la vía biosintética de la melatonina , en la arqueona Thermoplasma volcanium [96] coloca firmemente la biosíntesis de melatonina en los tres dominios principales de la vida, remontándose a unos 4 mil millones de años atrás. [97]
Productos alimenticios
Se ha informado de la presencia natural de melatonina en alimentos como las cerezas ácidas (entre 0,17 y 13,46 ng/g), [98] los plátanos, las ciruelas, las uvas, el arroz, los cereales, las hierbas, [99] el aceite de oliva, el vino [100] y la cerveza. [101] El consumo de leche y cerezas ácidas puede mejorar la calidad del sueño. [102] Cuando las aves ingieren alimentos vegetales ricos en melatonina, como el arroz, la melatonina se une a los receptores de melatonina en sus cerebros. [103] Cuando los seres humanos consumen alimentos ricos en melatonina, como el plátano, la piña y la naranja, los niveles de melatonina en sangre aumentan significativamente. [104]
Referencias
- ^ Amaral FG, Cipolla-Neto J (2018). "Una breve revisión sobre la melatonina, una hormona pineal". Archivos de Endocrinología y Metabolismo . 62 (4): 472–479. doi :10.20945/2359-3997000000066. PMC 10118741 . PMID 30304113. S2CID 52954755.
- ^ ab Auld F, Maschauer EL, Morrison I, Skene DJ, Riha RL (agosto de 2017). "Evidencia de la eficacia de la melatonina en el tratamiento de los trastornos primarios del sueño en adultos" (PDF) . Sleep Medicine Reviews . 34 : 10–22. doi :10.1016/j.smrv.2016.06.005. hdl : 20.500.11820/0e890bda-4b1d-4786-a907-a03b1580fd07 . PMID 28648359.
- ^ Faraone SV (2014). TDAH: intervenciones no farmacológicas, un número de Child and Adolescent Psychiatric Clinics of North America, libro electrónico. Elsevier Health Sciences. pág. 888. ISBN 978-0-323-32602-5.
- ^ Altun A, Ugur-Altun B (mayo de 2007). "Melatonina: utilización terapéutica y clínica". Revista internacional de práctica clínica . 61 (5): 835–45. doi : 10.1111/j.1742-1241.2006.01191.x . PMID 17298593. S2CID 18050554.
- ^ Boutin JA, Audinot V, Ferry G, Delagrange P (agosto de 2005). "Herramientas moleculares para estudiar las vías y acciones de la melatonina". Tendencias en ciencias farmacológicas . 26 (8): 412–9. doi :10.1016/j.tips.2005.06.006. PMID 15992934.
- ^ Hardeland R (julio de 2005). "Protección antioxidante por melatonina: multiplicidad de mecanismos desde la desintoxicación radical hasta la evitación radical". Endocrine . 27 (2): 119–30. doi :10.1385/ENDO:27:2:119. PMID 16217125. S2CID 46984486.
- ^ Reiter RJ, Acuña-Castroviejo D, Tan DX, Burkhardt S (junio de 2001). "Daño molecular mediado por radicales libres. Mecanismos de las acciones protectoras de la melatonina en el sistema nervioso central". Anales de la Academia de Ciencias de Nueva York . 939 (1): 200–15. Bibcode :2001NYASA.939..200R. doi :10.1111/j.1749-6632.2001.tb03627.x. PMID 11462772. S2CID 20404509.
- ^ abcd Tan DX, Hardeland R, Manchester LC, Korkmaz A, Ma S, Rosales-Corral S, Reiter RJ (enero de 2012). "Roles funcionales de la melatonina en plantas y perspectivas en la ciencia nutricional y agrícola". Journal of Experimental Botany . 63 (2): 577–97. doi : 10.1093/jxb/err256 . PMID 22016420.
- ^ Reiter RJ, Tan DX, Rosales-Corral S, Galano A, Zhou XJ, Xu B (2018). "Mitocondrias: orgánulos centrales para las acciones antioxidantes y antienvejecimiento de la melatonina". Moléculas . 23 (2): 509. doi : 10.3390/molecules23020509 . PMC 6017324 . PMID 29495303.
- ^ ab Manchester LC, Coto-Montes A, Boga JA, Andersen LP, Zhou Z, Galano A, Vriend J, Tan DX, Reiter RJ (2015). "Melatonina: una molécula antigua que hace que el oxígeno sea metabólicamente tolerable". Journal of Pineal Research . 59 (4): 403–419. doi : 10.1111/jpi.12267 . PMID 26272235. S2CID 24373303.
- ^ ab Zhao D, Yu Y, Shen Y, Liu Q, Zhao Z, Sharma R, Reiter RJ (2019). "Síntesis y función de la melatonina: historia evolutiva en animales y plantas". Frontiers in Endocrinology . 10 : 249. doi : 10.3389/fendo.2019.00249 . PMC 6481276 . PMID 31057485.
- ^ abcdef Jockers R, Delagrange P, Dubocovich ML, Markus RP, Renault N, Tosini G, et al. (Septiembre de 2016). "Actualización sobre receptores de melatonina: IUPHAR Review 20". Revista británica de farmacología . 173 (18): 2702–25. doi :10.1111/bph.13536. PMC 4995287 . PMID 27314810.
Por lo tanto, una molécula de melatonina y sus metabolitos asociados podrían eliminar una gran cantidad de especies reactivas y, por lo tanto, se cree que la capacidad antioxidante general de la melatonina es mayor que la de otros antioxidantes conocidos, como la vitamina C y la vitamina E, en condiciones in vitro o in vivo (Gitto et al., 2001; Sharma y Haldar, 2006; Ortiz et al., 2013).
- ^ "Receptores de melatonina | Receptores acoplados a proteína G | Guía de farmacología de la IUPHAR/BPS". www.guidetopharmacology.org . Consultado el 7 de abril de 2017 .
- ^ abc Sharafati-Chaleshtori R, Shirzad H, Rafieian-Kopaei M, Soltani A (2017). "Melatonina y enfermedades mitocondriales humanas". Revista de investigación en ciencias médicas . 22 : 2. doi : 10.4103/1735-1995.199092 . PMC 5361446 . PMID 28400824.
- ^ abc Reiter RJ, Rosales-Corral S, Tan DX, Jou MJ, Galano A, Xu B (noviembre de 2017). "La melatonina como antioxidante dirigido a las mitocondrias: una de las mejores ideas de la evolución". Ciencias de la vida celular y molecular . 74 (21): 3863–3881. doi :10.1007/s00018-017-2609-7. PMC 11107735 . PMID 28864909. S2CID 23820389.
La melatonina se dirige específicamente a las mitocondrias, donde parece funcionar como un antioxidante de ápice ... La medición de la distribución subcelular de la melatonina ha demostrado que la concentración de este indol en las mitocondrias supera en gran medida la de la sangre.
- ^ abc Reiter RJ, Mayo JC, Tan DX, Sainz RM, Alatorre-Jimenez M, Qin L (octubre de 2016). "La melatonina como antioxidante: promete poco pero cumple mucho". Journal of Pineal Research . 61 (3): 253–78. doi : 10.1111/jpi.12360 . PMID 27500468. S2CID 35435683.
Existe evidencia creíble que sugiere que la melatonina debería clasificarse como un antioxidante dirigido a las mitocondrias.
- ^ abc Manchester LC, Coto-Montes A, Boga JA, Andersen LP, Zhou Z, Galano A, et al. (noviembre de 2015). "Melatonina: una molécula antigua que hace que el oxígeno sea metabólicamente tolerable". Journal of Pineal Research . 59 (4): 403–19. doi : 10.1111/jpi.12267 . PMID 26272235. S2CID 24373303.
Aunque originalmente se pensaba que se producía y secretaba exclusivamente en la glándula pineal de los vertebrados [53], ahora se sabe que el indol está presente en muchos, quizás todos, los órganos de los vertebrados [54] y en los órganos de todas las plantas que se han investigado [48, 55, 56]. El hecho de que la melatonina no se limita únicamente a la glándula pineal también lo destacan los informes de que está presente en invertebrados [57–59], que carecen de glándula pineal y algunos de los cuales constan de una sola célula.
- ^ abcd Mayo JC, Sainz RM, González-Menéndez P, Hevia D, Cernuda-Cernuda R (noviembre de 2017). "Transporte de melatonina a las mitocondrias". Ciencias de la vida celulares y moleculares . 74 (21): 3927–3940. doi :10.1007/s00018-017-2616-8. PMC 11107582 . PMID 28828619. S2CID 10920415.
- ^ Emet M, Ozcan H, Ozel L, Yayla M, Halici Z, Hacimuftuoglu A (junio de 2016). "Una revisión de la melatonina, sus receptores y fármacos". The Eurasian Journal of Medicine . 48 (2): 135–41. doi :10.5152/eurasianjmed.2015.0267. PMC 4970552 . PMID 27551178.
- ^ Ardura J, Gutierrez R, Andres J, Agapito T (2003). "Aparición y evolución del ritmo circadiano de la melatonina en niños". Investigación hormonal . 59 (2): 66–72. doi :10.1159/000068571 (inactivo el 8 de octubre de 2024). PMID 12589109. S2CID 41937922.
{{cite journal}}: CS1 maint: DOI inactivo a partir de octubre de 2024 ( enlace ) - ^ Sack RL, Lewy AJ, Erb DL, Vollmer WM, Singer CM (1986). "La producción humana de melatonina disminuye con la edad". Journal of Pineal Research . 3 (4): 379–88. doi :10.1111/j.1600-079X.1986.tb00760.x. PMID 3783419. S2CID 33664568.
- ^ Hagenauer MH, Perryman JI, Lee TM, Carskadon MA (junio de 2009). "Cambios en la regulación homeostática y circadiana del sueño en la adolescencia". Neurociencia del desarrollo . 31 (4): 276–84. doi :10.1159/000216538. PMC 2820578 . PMID 19546564.
- ^ Tan DX, Chen LD, Poeggeler B, L Manchester C, Reiter RJ (1993). "Melatonina: un potente eliminador de radicales hidroxilo endógeno". Endocr. J. 1 : 57–60.
- ^ Poeggeler B, Saarela S, Reiter RJ, Tan DX, Chen LD, Manchester LC, Barlow-Walden LR (noviembre de 1994). "Melatonina: un potente eliminador de radicales endógenos y donador de electrones: nuevos aspectos de la química de oxidación de este indol a los que se accedió in vitro". Anales de la Academia de Ciencias de Nueva York . 738 (1): 419–20. Bibcode :1994NYASA.738..419P. doi :10.1111/j.1749-6632.1994.tb21831.x. PMID 7832450. S2CID 36383425.
- ^ ab Arnao MB, Hernández-Ruiz J (mayo de 2006). "La función fisiológica de la melatonina en plantas". Plant Signaling & Behavior . 1 (3): 89–95. Bibcode :2006PlSiB...1...89A. doi :10.4161/psb.1.3.2640. PMC 2635004 . PMID 19521488.
- ^ Pieri C, Marra M, Moroni F, Recchioni R, Marcheselli F (1994). "Melatonina: un eliminador de radicales peroxilo más eficaz que la vitamina E". Ciencias de la vida . 55 (15): PL271-6. doi :10.1016/0024-3205(94)00666-0. PMID 7934611.
- ^ Carrillo-Vico A, Guerrero JM, Lardone PJ, Reiter RJ (julio de 2005). "Una revisión de las múltiples acciones de la melatonina sobre el sistema inmunológico". Endocrine . 27 (2): 189–200. doi :10.1385/ENDO:27:2:189. PMID 16217132. S2CID 21133107.
- ^ Arushanian EB, Beĭer EV (2002). "[Propiedades inmunotrópicas de la melatonina pineal]". Eksperimental'naia i Klinicheskaia Farmakologiia (en ruso). 65 (5): 73–80. PMID 12596522.
- ^ Carrillo-Vico A, Reiter RJ, Lardone PJ, Herrera JL, Fernández-Montesinos R, Guerrero JM, Pozo D (mayo de 2006). "El papel modulador de la melatonina sobre la capacidad de respuesta inmune". Opinión actual sobre medicamentos en investigación . 7 (5): 423–31. PMID 16729718.
- ^ Maestroni GJ (marzo de 2001). "El potencial inmunoterapéutico de la melatonina". Opinión de expertos sobre fármacos en investigación . 10 (3): 467–76. doi :10.1517/13543784.10.3.467. PMID 11227046. S2CID 6822594.
- ^ Suriagandhi V, Nachiappan V (enero de 2022). "Efectos protectores de la melatonina contra la obesidad inducida por la resistencia a la leptina". Investigación sobre el cerebro conductual . 417 : 113598. doi :10.1016/j.bbr.2021.113598. PMID 34563600. S2CID 237603177.
- ^ Kelesidis T, Kelesidis I, Chou S, Mantzoros CS (enero de 2010). "Revisión narrativa: el papel de la leptina en la fisiología humana: aplicaciones clínicas emergentes". Anales de Medicina Interna . 152 (2): 93–100. doi :10.7326/0003-4819-152-2-201001190-00008. PMC 2829242 . PMID 20083828.
- ^ "Biosíntesis de serotonina y melatonina MetaCyc".
- ^ ab Tordjman S, Chokron S, Delorme R, Charrier A, Bellissant E, Jaafari N, Fougerou C (abril de 2017). "Melatonina: farmacología, funciones y beneficios terapéuticos". Neurofarmacología actual . 15 (3): 434–443. doi :10.2174/1570159X14666161228122115. PMC 5405617. PMID 28503116 .
- ^ Bochkov DV, Sysolyatin SV, Kalashnikov AI, Surmacheva IA (enero de 2012). "Ácido shikímico: revisión de sus técnicas analíticas, de aislamiento y de purificación a partir de fuentes vegetales y microbianas". Journal of Chemical Biology . 5 (1): 5–17. doi :10.1007/s12154-011-0064-8. PMC 3251648 . PMID 22826715.
- ^ abc Hardeland R (febrero de 2015). "Melatonina en plantas y otros fotótrofos: avances y lagunas en relación con la diversidad de funciones". Journal of Experimental Botany . 66 (3): 627–46. doi :10.1093/jxb/eru386. PMID 25240067.
- ^ Tan DX, Manchester LC, Liu X, Rosales-Corral SA, Acuna-Castroviejo D, Reiter RJ (marzo de 2013). "Mitocondrias y cloroplastos como sitios originales de síntesis de melatonina: una hipótesis relacionada con la función primaria y evolución de la melatonina en eucariotas". Journal of Pineal Research . 54 (2): 127–38. doi : 10.1111/jpi.12026 . PMID 23137057. S2CID 206140413.
- ^ Roberts KM, Fitzpatrick PF (abril de 2013). "Mecanismos de la triptófano y la tirosina hidroxilasa". IUBMB Life . 65 (4): 350–7. doi :10.1002/iub.1144. PMC 4270200 . PMID 23441081.
- ^ Sumi-Ichinose C, Ichinose H, Takahashi E, Hori T, Nagatsu T (marzo de 1992). "Clonación molecular del ADN genómico y asignación cromosómica del gen de la descarboxilasa de L-aminoácidos aromáticos humanos, la enzima para la biosíntesis de catecolaminas y serotonina". Bioquímica . 31 (8): 2229–38. doi :10.1021/bi00123a004. PMID 1540578.
- ^ ab Dewick PM (2002). Productos naturales medicinales. Un enfoque biosintético (2.ª ed.). Wiley. ISBN 978-0-471-49640-3.
- ^ Hickman AB, Klein DC, Dyda F (enero de 1999). "Biosíntesis de melatonina: la estructura de la serotonina N-acetiltransferasa a una resolución de 2,5 A sugiere un mecanismo catalítico". Molecular Cell . 3 (1): 23–32. doi : 10.1016/S1097-2765(00)80171-9 . PMID 10024876.
- ^ Donohue SJ, Roseboom PH, Illnerova H, Weller JL, Klein DC (octubre de 1993). "Hidroxiindol-O-metiltransferasa humana: presencia del fragmento LINE-1 en un clon de ADNc y ARNm pineal". ADN y biología celular . 12 (8): 715–27. doi :10.1089/dna.1993.12.715. PMID 8397829.
- ^ Nesbitt AD, Leschziner GD, Peatfield RC (septiembre de 2014). "Cefalea, fármacos y sueño". Cefalea (revisión). 34 (10): 756–66. doi :10.1177/0333102414542662. PMID 25053748. S2CID 33548757.
- ^ Schomerus C, Korf HW (diciembre de 2005). "Mecanismos que regulan la síntesis de melatonina en el órgano pineal de los mamíferos". Anales de la Academia de Ciencias de Nueva York . 1057 (1): 372–83. Bibcode :2005NYASA1057..372S. doi :10.1196/annals.1356.028. PMID 16399907. S2CID 20517556.
- ^ Brainard GC, Hanifin JP, Greeson JM, Byrne B, Glickman G, Gerner E, Rollag MD (agosto de 2001). "Espectro de acción para la regulación de la melatonina en humanos: evidencia de un nuevo fotorreceptor circadiano". The Journal of Neuroscience . 21 (16): 6405–12. doi :10.1523/JNEUROSCI.21-16-06405.2001. PMC 6763155 . PMID 11487664.
- ^ Holzman DC (enero de 2010). "¿Qué hay en un color? El efecto único de la luz azul en la salud humana". Environmental Health Perspectives . 118 (1): A22-7. doi :10.1289/ehp.118-a22. PMC 2831986 . PMID 20061218.
- ^ "Noticias recientes – Programa de gráficos por computadora". www.graphics.cornell.edu .
- ^ Kayumov L, Casper RF, Hawa RJ, Perelman B, Chung SA, Sokalsky S, Shapiro CM (mayo de 2005). "El bloqueo de la luz de baja longitud de onda previene la supresión nocturna de melatonina sin efectos adversos en el rendimiento durante el trabajo por turnos simulado". The Journal of Clinical Endocrinology and Metabolism . 90 (5): 2755–61. doi : 10.1210/jc.2004-2062 . PMID 15713707.
- ^ "Un estudio de la Universidad de Houston muestra que las gafas con filtro de luz azul por la noche aumentan la melatonina en un 58 %". designeroptics.com . 25 de agosto de 2021 . Consultado el 26 de agosto de 2021 .
- ^ Burkhart K, Phelps JR (diciembre de 2009). "Lentes de color ámbar para bloquear la luz azul y mejorar el sueño: un ensayo aleatorizado". Chronobiology International . 26 (8): 1602–12. doi :10.3109/07420520903523719. PMID 20030543. S2CID 145296760.
- ^ "Melatonina". www.drugbank.ca . Consultado el 29 de enero de 2019 .
- ^ Hardeland R, Poeggeler B, Srinivasan V, Trakht I, Pandi-Perumal SR, Cardinali DP (2008). "Fármacos melatoninérgicos en la práctica clínica". Investigación científica . 58 (1): 1–10. doi :10.1055/s-0031-1296459. PMID 18368944. S2CID 38857779.
- ^ ab Ma X, Idle JR, Krausz KW, Gonzalez FJ (abril de 2005). "Metabolismo de la melatonina por los citocromos humanos P450". Metabolismo y disposición de fármacos . 33 (4): 489–494. doi :10.1124/dmd.104.002410. PMID 15616152. S2CID 14555783. Consultado el 25 de enero de 2023 .
- ^ Kennaway DJ (agosto de 2019). "Una revisión crítica de los ensayos de melatonina: pasado y presente". Revista de investigación pineal . 67 (1): e12572. doi : 10.1111/jpi.12572 . PMID 30919486.
- ^ Riha RL (noviembre de 2018). "El uso y mal uso de melatonina exógena en el tratamiento de los trastornos del sueño". Curr Opin Pulm Med . 24 (6): 543–548. doi :10.1097/MCP.0000000000000522. PMID 30148726. S2CID 52096729.
- ^ Williams WP, McLin DE, Dressman MA, Neubauer DN (septiembre de 2016). "Revisión comparativa de agonistas de melatonina aprobados para el tratamiento de los trastornos del ritmo circadiano sueño-vigilia". Farmacoterapia . 36 (9): 1028–41. doi :10.1002/phar.1822. PMC 5108473 . PMID 27500861.
- ^ Atkin T, Comai S, Gobbi G (abril de 2018). "Medicamentos para el insomnio más allá de las benzodiazepinas: farmacología, aplicaciones clínicas y descubrimiento". Pharmacol Rev . 70 (2): 197–245. doi : 10.1124/pr.117.014381 . PMID 29487083. S2CID 3578916.
- ^ Cohen PA, Avula B, Wang Y, Katragunta K, Khan I. (abril de 2023) "Cantidad de melatonina y CBD en gomitas de melatonina vendidas en EE. UU." JAMA . 329 (16): 1401–1402. doi :10.1001/jama.2023.2296. PMID 37097362
- ^ Filadelfi AM, Castrucci AM (mayo de 1996). "Aspectos comparativos del sistema pineal/melatonina de vertebrados poiquilotermos". Journal of Pineal Research . 20 (4): 175–86. doi :10.1111/j.1600-079X.1996.tb00256.x. PMID 8836950. S2CID 41959214.
- ^ Sugden D, Davidson K, Hough KA, Teh MT (octubre de 2004). "Melatonina, receptores de melatonina y melanóforos: una historia conmovedora". Pigment Cell Research . 17 (5): 454–60. doi : 10.1111/j.1600-0749.2004.00185.x . PMID 15357831.
- ^ Coates PM, Blackman MR, Cragg GM, Levine M, Moss J, White JD (2005). Enciclopedia de suplementos dietéticos. Nueva York, NY: Marcel Dekker. pp. 457–66. ISBN 978-0-8247-5504-1.
- ^ McCord CP, Allen FP (enero de 1917). "Evidencias que asocian la función de la glándula pineal con alteraciones de la pigmentación". J Exp Zool . 23 (1): 206–24. Bibcode :1917JEZ....23..207M. doi :10.1002/jez.1400230108.
- ^ Lerner AB, Case JD, Takahashi Y (julio de 1960). "Aislamiento de melatonina y ácido 5-metoxiindol-3-acético de glándulas pineales bovinas". The Journal of Biological Chemistry . 235 (7): 1992–7. doi : 10.1016/S0021-9258(18)69351-2 . PMID 14415935.
- ^ Lynch HJ, Wurtman RJ, Moskowitz MA, Archer MC, Ho MH (enero de 1975). "Ritmo diario de la melatonina urinaria humana". Science . 187 (4172): 169–71. Bibcode :1975Sci...187..169L. doi :10.1126/science.1167425. PMID 1167425.
- ^ Patente estadounidense 5449683, Wurtman RJ, "Métodos para inducir el sueño utilizando melatonina", expedida el 12 de septiembre de 1995, asignada al Instituto Tecnológico de Massachusetts
- ^ ab Lerner AB, Case JD, Takahashi Y, Lee TH, Mori W (1958). "Aislamiento de melatonina, el factor de la glándula pineal que aclara los melanocitos". Journal of the American Chemical Society . 80 (10): 2587. doi :10.1021/ja01543a060. ISSN 0002-7863.
- ^ Goeser S, Ruble J, Chandler L (1997). "Melatonina: perspectivas históricas y clínicas". Revista de atención farmacéutica en el control del dolor y los síntomas . 5 (1): 37–49. doi :10.1300/J088v05n01_04.
- ^ Beyer CE, Steketee JD, Saphier D (1998). "Propiedades antioxidantes de la melatonina: un misterio emergente". Farmacología bioquímica . 56 (10): 1265–1272. doi :10.1016/s0006-2952(98)00180-4. ISSN 0006-2952. PMID 9825724.
- ^ Liebmann PM, Wölfler A, Felsner P, Hofer D, Schauenstein K (1997). "La melatonina y el sistema inmunológico". Archivos Internacionales de Alergia e Inmunología . 112 (3): 203–211. doi :10.1159/000237455. ISSN 1018-2438. PMID 9066504.
- ^ Rapport MM, Green AA, Page IH (diciembre de 1948). "Serotonina, vasoconstrictor sérico; aislamiento y caracterización". The Journal of Biological Chemistry . 176 (3): 1243–1251. doi : 10.1016/S0021-9258(18)57137-4 . PMID 18100415.
- ^ Reiter RJ (mayo de 1991). "Melatonina pineal: biología celular de su síntesis y de sus interacciones fisiológicas". Endocrine Reviews . 12 (2): 151–80. doi :10.1210/edrv-12-2-151. PMID 1649044. S2CID 3219721.
- ^ Richardson GS (2005). "El sistema circadiano humano en el sueño normal y desordenado". The Journal of Clinical Psychiatry . 66 (Supl. 9): 3–9, cuestionario 42–3. PMID 16336035.
- ^ Perreau-Lenz S, Pévet P, Buijs RM, Kalsbeek A (enero de 2004). "El reloj biológico: el guardaespaldas de la homeostasis temporal". Cronobiología Internacional . 21 (1): 1–25. doi :10.1081/CBI-120027984. PMID 15129821. S2CID 42725506.
- ^ Foster RG (junio de 2020). "Sueño, ritmos circadianos y salud". Interface Focus . 10 (3): 20190098. doi :10.1098/rsfs.2019.0098. PMC 7202392 . PMID 32382406.
- ^ Karasek M, Winczyk K (2006). "Melatonina en humanos". Revista de Fisiología y Farmacología . 57 Suppl 5: 19–39. ISSN 1899-1505. PMID 17218758.
- ^ Kolli AR, Kuczaj AK, Calvino-Martin F, Hoeng J (2024). "La farmacocinética simulada de la cafeína y la melatonina inhaladas de productos existentes indica la falta de consideraciones dosimétricas". Toxicología alimentaria y química . 187 : 114601. doi : 10.1016/j.fct.2024.114601 . ISSN 0278-6915. PMID 38493979.
- ^ Lincoln GA, Andersson H, Loudon A (octubre de 2003). "Los genes del reloj en las células del calendario como base del cronometraje anual en mamíferos: una hipótesis unificadora". The Journal of Endocrinology . 179 (1): 1–13. doi : 10.1677/joe.0.1790001 . PMID 14529560.
- ^ ab Arendt J, Skene DJ (febrero de 2005). "La melatonina como cronobiótico". Sleep Medicine Reviews . 9 (1): 25–39. doi :10.1016/j.smrv.2004.05.002. PMID 15649736.
La melatonina exógena tiene efectos agudos de inducción de somnolencia y reducción de la temperatura durante el "día biológico" y, cuando se administra en el momento adecuado (es más eficaz alrededor del anochecer y el amanecer), cambiará la fase del reloj circadiano humano (sueño, melatonina endógena, temperatura corporal central, cortisol) a momentos más tempranos (avance del cambio de fase) o más tardíos (retraso del cambio de fase).
- ^ Chaturvedi CM (1984). "Efecto de la melatonina sobre las glándulas suprarrenales y las gónadas del Mynah común Acridtheres tristis". Revista Australiana de Zoología . 32 (6): 803–09. doi :10.1071/ZO9840803.
- ^ Chen HJ (julio de 1981). "Regresión testicular espontánea e inducida por melatonina en hámsteres dorados machos: aumento de la sensibilidad del macho viejo a la inhibición de la melatonina". Neuroendocrinología . 33 (1): 43–6. doi :10.1159/000123198. PMID 7254478.
- ^ Bouroutzika E, Ciliberti MG, Caroprese M, Theodosiadou E, Papadopoulos S, Makri S, Skaperda ZV, Kotsadam G, Michailidis ML, Valiakos G, Chadio S, Kouretas D, Valasi I (5 de noviembre de 2021). "Asociación de la administración de melatonina en ovejas preñadas con el crecimiento, el estado redox y la inmunidad de sus crías". Animales . 11 (11): 3161. doi : 10.3390/ani11113161 . ISSN 2076-2615. PMC 8614450 . PMID 34827893.
- ^ ab Huelsmann M, Hecker N, Springer MS, Gatesy J, Sharma V, Hiller M (septiembre de 2019). "Los genes perdidos durante la transición de la tierra al agua en los cetáceos resaltan los cambios genómicos asociados con las adaptaciones acuáticas". Science Advances . 5 (9): eaaw6671. Bibcode :2019SciA....5.6671H. doi :10.1126/sciadv.aaw6671. PMC 6760925 . PMID 31579821.
- ^ Paredes SD, Korkmaz A, Manchester LC, Tan DX, Reiter RJ (1 de enero de 2009). "Fitomelatonina: una revisión". Revista de botánica experimental . 60 (1): 57–69. doi : 10.1093/jxb/ern284 . PMID 19033551. S2CID 15738948.
- ^ Bonnefont-Rousselot D, Collin F (noviembre de 2010). "Melatonina: acción como antioxidante y posibles aplicaciones en enfermedades humanas y envejecimiento". Toxicología . 278 (1): 55–67. Bibcode :2010Toxgy.278...55B. doi :10.1016/j.tox.2010.04.008. PMID 20417677.
- ^ Reiter RJ, Manchester LC, Tan DX (septiembre de 2005). "Melatonina en nueces: influencia en los niveles de melatonina y la capacidad antioxidante total de la sangre". Nutrition . 21 (9): 920–4. doi :10.1016/j.nut.2005.02.005. PMID 15979282.
- ^ Reiter RJ, Tan DX, Zhou Z, Cruz MH, Fuentes-Broto L, Galano A (abril de 2015). "Fitomelatonina: ayuda a las plantas a sobrevivir y prosperar". Moléculas . 20 (4): 7396–437. doi : 10.3390/molecules20047396 . PMC 6272735 . PMID 25911967.
- ^ Arnao MB, Hernández-Ruiz J (septiembre de 2015). "Funciones de la melatonina en plantas: una revisión". Journal of Pineal Research . 59 (2): 133–50. doi : 10.1111/jpi.12253 . PMID 26094813.
- ^ Park S, Lee DE, Jang H, Byeon Y, Kim YS, Back K (abril de 2013). "Las plantas de arroz transgénico ricas en melatonina exhiben resistencia al estrés oxidativo inducido por herbicidas". Journal of Pineal Research . 54 (3). Wiley : 258–63. doi :10.1111/j.1600-079x.2012.01029.x. PMID 22856683. S2CID 6291664.
- ^ ab Arnao MB, Hernández-Ruiz J (diciembre de 2014). "Melatonina: ¿regulador y/o bioestimulador del crecimiento vegetal durante el estrés?". Tendencias en la ciencia de las plantas . 19 (12). Elsevier : 789–97. Bibcode :2014TPS....19..789A. doi :10.1016/j.tplants.2014.07.006. PMID 25156541. S2CID 38637203.
- ^ ab EL-Bauome HA, Doklega SM, Saleh SA, Mohamed AS, Suliman AA, Abd El-Hady MA (febrero de 2024). "Efectos de la melatonina sobre el crecimiento de las plantas de lechuga, enzimas antioxidantes y pigmentos fotosintéticos en condiciones de estrés por salinidad". Folia horticulturae . 36 (1). Sociedad Polaca de Ciencias Hortícolas: 1–17. doi : 10.2478/fhort-2024-0001 . S2CID 19887642.
- ^ ab Arnao MB, Hernández-Ruiz J (septiembre de 2015). "Funciones de la melatonina en plantas: una revisión". Revista de investigación pineal . 59 (2). Wiley : 133–50. doi : 10.1111/jpi.12253 . PMID 26094813. S2CID 19887642.
- ^ Socaciu AI, Ionuţ R, Socaciu MA, Ungur AP, Bârsan M, Chiorean A, et al. (diciembre de 2020). "La melatonina, un regulador metabólico ubicuo: funciones, mecanismos y efectos sobre la alteración circadiana y las enfermedades degenerativas". Reseñas de trastornos endocrinos y metabólicos . 21 (4): 465–478. doi :10.1007/s11154-020-09570-9. PMID 32691289. S2CID 220657247.
- ^ Germann SM, Baallal Jacobsen SA, Schneider K, Harrison SJ, Jensen NB, Chen X, Stahlhut SG, Borodina I, et al. (2016). "Producción microbiana basada en glucosa de la hormona melatonina en la levadura Saccharomyces cerevisiae". Revista de biotecnología . 11 (5): 717–724. doi :10.1002/biot.201500143. PMC 5066760 . PMID 26710256.
- ^ Luo H, Schneider K, Christensen U, Lei Y, Herrgard M, Palsson BØ (2020). "Síntesis microbiana de la hormona humana melatonina a escala de gramos". ACS Synthetic Biology . 9 (6): 1240–1245. doi :10.1021/acssynbio.0c00065. ISSN 2161-5063. PMID 32501000. S2CID 219331624.
- ^ Arnao MB, Giraldo-Acosta M, Castejón-Castillejo A, Losada-Lorán M, Sánchez-Herrerías P, El Mihyaoui A, Cano A, Hernández-Ruiz J (2023). "Melatonina de microorganismos, algas y plantas como posibles alternativas a la melatonina sintética". Metabolitos . 13 (1): 72. doi : 10.3390/metabo13010072 . PMC 9862825 . PMID 36676997.
- ^ Lee K, Choi GH, Back K (21 de marzo de 2022). "Caracterización funcional de la serotonina N-acetiltransferasa en Archaeon Thermoplasma volcanium". Antioxidantes . 11 (3): 596. doi : 10.3390/antiox11030596 . ISSN 2076-3921. PMC 8945778 . PMID 35326246.
- ^ Hoshino Y, Villanueva L (10 de marzo de 2023). "Cuatro mil millones de años de evolución del terpenoma microbiano". FEMS Microbiology Reviews . 47 (2): fuad008. doi :10.1093/femsre/fuad008. ISSN 1574-6976. PMID 36941124.
- ^ Burkhardt S, Tan DX, Manchester LC, Hardeland R, Reiter RJ (octubre de 2001). "Detección y cuantificación del antioxidante melatonina en cerezas ácidas Montmorency y Balaton (Prunus cerasus)". Journal of Agricultural and Food Chemistry . 49 (10): 4898–902. doi :10.1021/jf010321. PMID 11600041.
- ^ González-Flores D, Velardo B, Garrido M, González-Gómez D, Lozano M, Ayuso MC, Barriga C, Paredes SD, Rodríguez AB (2011). "La ingestión de ciruelas japonesas (Prunus salicina Lindl. cv. Crimson Globe) aumenta los niveles urinarios de 6-sulfatoximelatonina y de capacidad antioxidante total en humanos jóvenes, de mediana edad y ancianos: Caracterización nutricional y funcional de su contenido". Revista de Investigación en Alimentación y Nutrición . 50 (4): 229–36.
- ^ Lamont KT, Somers S, Lacerda L, Opie LH, Lecour S (mayo de 2011). "¿El vino tinto está a un sorbo SEGURO de la cardioprotección? Mecanismos implicados en la cardioprotección inducida por resveratrol y melatonina". Journal of Pineal Research . 50 (4): 374–80. doi :10.1111/j.1600-079X.2010.00853.x. PMID 21342247. S2CID 8034935.
- ^ Salehi B (5 de julio de 2019). "Melatonina en plantas medicinales y alimenticias" (PDF) . Cells . 681 . Archivado desde el original (PDF) el 29 de noviembre de 2021 . Consultado el 2 de julio de 2021 .
- ^ Pereira N, Naufel MF, Ribeiro EB, Tufik S, Hachul H (enero de 2020). "Influencia de las fuentes dietéticas de melatonina en la calidad del sueño: una revisión". Revista de ciencia de los alimentos . 85 (1). Wiley: 5–13. doi : 10.1111/1750-3841.14952 . PMID 31856339.
- ^ Hattori A, Migitaka H, Iigo M, Itoh M, Yamamoto K, Ohtani-Kaneko R, et al. (marzo de 1995). "Identificación de melatonina en plantas y sus efectos sobre los niveles plasmáticos de melatonina y la unión a los receptores de melatonina en vertebrados". Bioquímica y Biología Molecular Internacional . 35 (3): 627–34. PMID 7773197.
- ^ Sae-Teaw M, Johns J, Johns NP, Subongkot S (agosto de 2013). "Niveles séricos de melatonina y capacidades antioxidantes después del consumo de piña, naranja o plátano por voluntarios varones sanos". Journal of Pineal Research . 55 (1): 58–64. doi : 10.1111/jpi.12025 . PMID 23137025. S2CID 979886.
Enlaces externos
- "Melatonina". Chemwatch.

