Gas CS
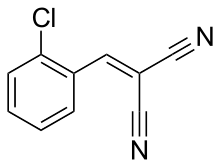
El compuesto 2-clorobenzalmalononitrilo (también llamado o -clorobencilideno malononitrilo ; fórmula química: C 10 H 5 ClN 2 ), un cianocarbono , es el componente definitorio del agente lacrimógeno comúnmente conocido como gas CS , un gas lacrimógeno que se utiliza como agente de control de disturbios y cuyo uso está prohibido en la guerra debido al Protocolo de Ginebra de 1925 .
 | |
 | |
| Nombres | |
|---|---|
| Nombre IUPAC preferido [(2-Clorofenil)metilideno]propanodinitrilo | |
| Otros nombres 2-(2-Clorobencilideno)malononitrilo 2-Clorobenzalmalononitrilo o -Clorobencilideno malononitrilo Gas lacrimógeno | |
| Identificadores | |
Modelo 3D ( JSmol ) |
|
| Química biológica |
|
| Araña química | |
| Tarjeta informativa de la ECHA | 100.018.435 |
| Número CE |
|
| |
Identificador de centro de PubChem |
|
| Número RTECS |
|
| UNIVERSIDAD |
|
| Número de la ONU | 2810, 3276, 2811 |
Panel de control CompTox ( EPA ) |
|
| |
| |
| Propiedades | |
| C10H5ClN2 [ 1 ] | |
| Masa molar | 188,6 g/mol [2] |
| Apariencia | Polvo cristalino blanco. Gas incoloro al quemarse. |
| Olor | Parecido a la pimienta [3] |
| Densidad | 1,04 g/ cm3 |
| Punto de fusión | 93 °C (199 °F; 366 K) |
| Punto de ebullición | 310 °C (590 °F; 583 K) [4] |
| Insoluble | |
| Presión de vapor | 3,4×10 −5 mmHg a 20 °C |
| Peligros | |
| Etiquetado SGA : | |
     | |
| Peligro | |
| H302 , H314 , H330 , H335 , H372 , H410 | |
| P260 , P261 , P264 , P270 , P271 , P273 , P280 , P284 , P301+P312 , P301+P330+P331 , P303+P361+P353 , P304+P340 , P305+P351+P338 , P310 , P312 , P314 , P320 , P321 , P330 , P363 , P391 , P403+P233 , P405 , P501 | |
| NFPA 704 (rombo cortafuegos) | |
| Dosis o concentración letal (LD, LC): | |
LC Lo ( valor más bajo publicado ) |
|
| NIOSH (límites de exposición a la salud en EE. UU.): | |
PEL (Permisible) | TWA 0,05 ppm (0,4 mg/m3 ) [ 3] |
REL (recomendado) | C 0,05 ppm (0,4 mg/m 3 ) [piel] [3] |
IDLH (Peligro inmediato) | 2 mg/m3 [ 3] |
| Compuestos relacionados | |
Compuestos relacionados | SDB 5-cloro-2-quinolincarbonitrilo |
Salvo que se indique lo contrario, los datos se proporcionan para los materiales en su estado estándar (a 25 °C [77 °F], 100 kPa). | |
La exposición provoca una sensación de ardor y lagrimeo en los ojos hasta el punto de que el sujeto no puede mantener los ojos abiertos, y una irritación ardiente de las membranas mucosas de la nariz, la boca y la garganta, lo que resulta en tos profusa, secreción de moco nasal, desorientación y dificultad para respirar, incapacitando parcialmente al sujeto. El gas CS es un aerosol de un disolvente volátil (una sustancia que disuelve otras sustancias activas y que se evapora fácilmente) y 2-clorobenzalmalononitrilo, que es un compuesto sólido a temperatura ambiente. El gas CS se acepta generalmente como no letal .
Historia
El gas CS fue sintetizado por primera vez por dos estadounidenses, Ben Corson y Roger Stoughton, [6] en el Middlebury College de Vermont en 1928, y el nombre de la sustancia química se deriva de las primeras letras de los apellidos de los científicos. [7] [8]
El CS fue desarrollado y probado en secreto en Porton Down, Wiltshire , Reino Unido, en los años 1950 y 1960. El CS se utilizó primero en animales y, posteriormente, en voluntarios del ejército británico . El CS tiene menos efecto en los animales porque tienen conductos lacrimales diferentes y, en el caso de los mamíferos no humanos, su pelaje inhibe la libre entrada del gas. [9]
En 2002, la Oficina de Seguridad Internacional y No Proliferación del Departamento de Estado de Estados Unidos, dirigida por Colin Powell, hizo una distinción clara entre "agentes antidisturbios", como el gas CS, y "armas químicas letales". La Oficina citó el apoyo a esta postura por parte del Reino Unido y Japón. [10]
Producción
El CS se sintetiza mediante la reacción de 2-clorobenzaldehído y malononitrilo a través de la condensación de Knoevenagel :

- ClC 6 H 4 CHO + H 2 C (CN) 2 → ClC 6 H 4 CHC (CN) 2 + H 2 O
La reacción se cataliza con una base débil como la piperidina o la piridina . El método de producción no ha cambiado desde que Corson y Stoughton descubrieron la sustancia. [11] Se han sugerido otras bases, métodos sin disolventes y la promoción con microondas para mejorar la producción de la sustancia. [12]
Las propiedades fisiológicas ya habían sido descubiertas por los primeros químicos que sintetizaron el compuesto en 1928: "Propiedades fisiológicas. Algunos de estos dinitrilos tienen el efecto de estornudar y producir gases lacrimógenos. Son inofensivos cuando están húmedos, pero su manipulación en polvo seco es desastrosa". [11]
Utilizar como aerosol
Como el 2-clorobenzalmalononitrilo es un sólido a temperatura ambiente, no un gas , se han utilizado diversas técnicas para hacer que este sólido se pueda utilizar como aerosol :
- Derretido y rociado en forma fundida.
- Disuelto en disolvente orgánico.
- Polvo seco CS2 (CS2 es una forma micropulverizada y siliconizada de CS) .
- CS a partir de granadas térmicas por generación de gases calientes. [2]
En el asedio de Waco , en Estados Unidos, se disolvió CS en el disolvente orgánico diclorometano (también conocido como cloruro de metileno). La solución se dispersó como aerosol mediante una fuerza explosiva y, cuando el diclorometano altamente volátil se evaporó, los cristales de CS precipitaron y formaron una fina dispersión en el aire. [2]
Efectos



Se han producido muchos tipos de gases lacrimógenos y otros agentes de control de disturbios con efectos que van desde un leve lagrimeo de los ojos hasta vómitos inmediatos y postración . CN y CS son los más utilizados y conocidos, pero se han desarrollado alrededor de 15 tipos diferentes de gases lacrimógenos en todo el mundo, por ejemplo, adamsita o bromoacetona , CNB y CNC. CS se ha convertido en el más popular debido a su fuerte efecto. El efecto del CS en una persona dependerá de si está envasado como una solución o se usa como un aerosol . El tamaño de las gotas de la solución y el tamaño de las partículas de CS después de la evaporación son factores que determinan su efecto en el cuerpo humano. [13]
El producto químico reacciona con la humedad de la piel y los ojos, provocando una sensación de ardor y el cierre inmediato, forzado e incontrolable de los ojos. Los efectos suelen incluir lágrimas que brotan de los ojos, tos profusa, secreción nasal excepcional llena de mucosidad, ardor en los ojos, párpados, nariz y garganta, desorientación, mareos y dificultad para respirar. También quema la piel sudorosa o quemada por el sol. En dosis muy concentradas, también puede inducir tos y vómitos intensos. La mayoría de los efectos inmediatos desaparecen en unas pocas horas (como la secreción nasal excepcional y la tos profusa), aunque los síntomas respiratorios, gastrointestinales y orales pueden persistir durante meses. [14] [15] La exposición excesiva puede causar quemaduras químicas que resultan en cicatrices permanentes. [16]
Los adultos expuestos a gases lacrimógenos durante las protestas de 2020 en Portland, Oregón, EE. UU., también informaron cambios menstruales (899; 54,5 % de las 1650 mujeres encuestadas). La exposición a gases lacrimógenos está asociada con el uso evitable de atención médica. [17]
Efectos secundarios
Las personas u objetos contaminados con gas CS pueden causar exposición secundaria a otras personas, incluidos los profesionales sanitarios y la policía . Además, la exposición repetida puede causar sensibilización . [18]
Toxicidad
El canal iónico TRPA1 (Transient Receptor Potential-Ankyrin 1) expresado en los nociceptores (especialmente el trigémino ) se ha implicado como el sitio de acción del gas CS en modelos de roedores. [19] [20]
Aunque se describe como un arma no letal para el control de multitudes, los estudios han puesto en duda esta clasificación. El CS puede causar daño pulmonar grave y también puede dañar significativamente el corazón y el hígado. [21]
El 28 de septiembre de 2000, el Prof. Dr. Uwe Heinrich publicó un estudio encargado por John C. Danforth , de la Oficina del Asesor Especial de los Estados Unidos , para investigar el uso de CS por parte del FBI en el complejo de Mount Carmel de la Rama Davidiana . Dijo que no se habían reportado muertes humanas, pero concluyó que la letalidad del CS utilizado habría sido determinada principalmente por dos factores: si se utilizaron máscaras de gas y si los ocupantes quedaron atrapados en una habitación. Sugiere que si no se utilizaron máscaras de gas y los ocupantes quedaron atrapados, entonces, "existe una clara posibilidad de que este tipo de exposición al CS pueda contribuir significativamente a efectos letales o incluso causarlos". [2]
El gas CS puede tener un efecto clastogénico (cambio cromosómico anormal) en las células de los mamíferos, pero ningún estudio lo ha vinculado con abortos espontáneos o muertes fetales. [21] En Egipto, se informó que el gas CS fue la causa de la muerte de varios manifestantes en la calle Mohamed Mahmoud cerca de la plaza Tahrir durante las protestas de noviembre de 2011. El solvente en el que se disuelve el CS, metil isobutil cetona (MIBK), está clasificado como nocivo por inhalación; irritante para los ojos y el sistema respiratorio; y la exposición repetida puede causar sequedad o agrietamiento de la piel. [22]
Véase también
- Lista de partes en la Convención sobre Armas Químicas
- Lista de usos del gas CS por país
- Gas CR
- Gas CN
- Spray de pimienta
- Convención sobre armas químicas
- Granadas de mano
Referencias
- ^ Williams KE. "Datos detallados sobre el agente lacrimógeno O-clorobencilideno malononitrilo (CS)" (PDF) . Centro de Promoción de la Salud y Medicina Preventiva del Ejército de los Estados Unidos . Archivado desde el original (PDF) el 26 de septiembre de 2007.
- ^ abcd Heinrich U (septiembre de 2000). "Posibles efectos letales del gas lacrimógeno CS en los Davidianos durante la redada del FBI en el complejo de Mount Carmel cerca de Waco, Texas" (PDF) . Archivado (PDF) del original el 25 de diciembre de 2014. Consultado el 23 de septiembre de 2007 .
- ^ abcd Guía de bolsillo del NIOSH sobre peligros químicos. "#0122". Instituto Nacional de Seguridad y Salud Ocupacional (NIOSH).
- ^ Hoenig, Steven L. (2006). Compendio de agentes de guerra química. Springer. pág. 138. ISBN 978-0-387-34626-7.
- ^ "o-Clorobencilideno malononitrilo". Concentraciones inmediatamente peligrosas para la vida o la salud (IDLH) . Instituto Nacional de Seguridad y Salud Ocupacional (NIOSH).
- ^ Corson BB, Stoughton RW (1928). "Reacciones de dinitrilos alfa y beta insaturados". Revista de la Sociedad Química Americana . 50 (10): 2825–2837. doi :10.1021/ja01397a037.
- ^ "CS" . Oxford English Dictionary (edición en línea). Oxford University Press . (Se requiere suscripción o membresía a una institución participante).
- ^ "CS, compuesto químico Archivado el 19 de diciembre de 2005 en Wayback Machine . ". columbia.thefreedictionary.com Archivado el 29 de julio de 2005 en Wayback Machine . Consultado el 23 de septiembre de 2007.
- ^ "Ortoclorobencilidenomalononitrilo ClC6H4CHCCN(CN)2 Archivado el 28 de noviembre de 2006 en Wayback Machine . Zarc International. Recuperado el 23 de septiembre de 2007.
- ^ "Protocolo para la prohibición del empleo en la guerra de gases asfixiantes, tóxicos o similares y de medios bacteriológicos de guerra (Protocolo de Ginebra)". Departamento de Estado de los Estados Unidos. 25 de septiembre de 2002. Consultado el 24 de agosto de 2013 .
- ^ ab Corson BB, Stoughton RW (1928). "Reacciones de dinitrilos alfa, beta-insaturados". J Am Chem Soc . 50 (10): 2825–2837. doi :10.1021/ja01397a037.
- ^ Pande A, Ganesan K, Jain AK, Gupta PK, Malhotr RC (2005). "Nuevo proceso ecológico para la síntesis de 2-clorobencilidenomalononitrilo y análogos de ITS utilizando agua como disolvente". Org Proc Res Develop . 9 (2): 133–136. doi :10.1021/op0498262.
- ^ "Contención más segura: informe de la conferencia celebrada en abril de 2002 en Church House, Westminster". Autoridad de Quejas contra la Policía. Recuperado el 23 de septiembre de 2007.
- ^ Karagama YG, Newton JR, Newbegin CJ (abril de 2003). "Efectos físicos a corto y largo plazo de la exposición al CS en aerosol". Revista de la Royal Society of Medicine . 96 (4): 172–4. doi :10.1177/014107680309600404. PMC 539444 . PMID 12668703.
- ^ Torgrimson-Ojerio BN, Mularski KS, Peyton MR, Keast EM, Hassan A, Ivlev I (abril de 2021). "Problemas de salud y utilización de la atención médica entre adultos que informaron haber estado expuestos a gases lacrimógenos durante las protestas de 2020 en Portland (Oregón): una encuesta transversal". BMC Public Health . 21 (1): 803. doi : 10.1186/s12889-021-10859-w . PMC 8074355 . PMID 33902512.
- ^ "El hombre que usó el aerosol CS quedó marcado de por vida" Archivado el 5 de marzo de 2016 en Wayback Machine . BBC News . 2 de febrero de 2006. Recuperado el 23 de septiembre de 2007.
- ^ Torgrimson-Ojerio BN, Mularski KS, Peyton MR, Keast EM, Hassan A, Ivlev I (abril de 2021). "Problemas de salud y utilización de la atención médica entre adultos que informaron haber estado expuestos a gases lacrimógenos durante las protestas de 2020 en Portland (Oregón): una encuesta transversal". BMC Public Health . 21 (1): 803. doi : 10.1186/s12889-021-10859-w . PMC 8074355 . PMID 33902512.
- ^ Carron PN, Yersin B (junio de 2009). "Gestión de los efectos de la exposición al gas lacrimógeno". BMJ . 338 : b2283. doi :10.1136/bmj.b2283. PMID 19542106. S2CID 7870564.
- ^ Bessac BF, Sivula M, von Hehn CA, Caceres AI, Escalera J, Jordt SE (abril de 2009). "Los antagonistas transitorios de la anquirina 1 bloquean los efectos nocivos de los isocianatos industriales tóxicos y los gases lacrimógenos". FASEB Journal . 23 (4): 1102–14. doi : 10.1096/fj.08-117812 . PMC 2660642 . PMID 19036859.
- ^ Brône B, Peeters PJ, Marrannes R, Mercken M, Nuydens R, Meert T, Gijsen HJ (septiembre de 2008). "Los gases lacrimógenos CN, CR y CS son activadores potentes del receptor TRPA1 humano". Toxicología y farmacología aplicada . 231 (2): 150–6. doi :10.1016/j.taap.2008.04.005. PMID 18501939.
- ^ ab Hu H, Fine J, Epstein P, Kelsey K, Reynolds P, Walker B (agosto de 1989). "Gas lacrimógeno: ¿agente acosador o arma química tóxica?". JAMA . 262 (5): 660–3. doi :10.1001/jama.1989.03430050076030. PMID 2501523.
- ^ "MSDS para 99% 4-Metil-2-pentanona (MIBK)" (PDF) . Alfa Aesar. Archivado desde el original (PDF) el 16 de agosto de 2018 . Consultado el 7 de enero de 2013 .
Enlaces externos
- Salem H, Gutting B, Kluchinsky T, Boardman C, Tuorinsky S, Hout J (2008). Aspectos médicos de la guerra química, Capítulo 13 Agentes de control de disturbios, Instituto Médico del Ejército de los Estados Unidos, Instituto Borden, págs. 441–484 (2008).
- Carron PN, Yersin B (junio de 2009). "Gestión de los efectos de la exposición al gas lacrimógeno". BMJ . 338 (7710): b2283. doi :10.1136/bmj.b2283. PMID 19542106. S2CID 7870564.
- Hout J, Hook G, LaPuma P, White D (2010). "Identificación de compuestos formados durante la dispersión térmica a baja temperatura de o-clorobencilideno malononitrilo encapsulado (agente de control de disturbios CS)" Journal of Occupational and Environmental Hygiene, junio de 2010
- Cromatografía de gases NIST
- CDC – Guía de bolsillo de NIOSH sobre peligros químicos: o-clorobencilideno malononitrilo
- Recomendaciones 69 y 70 del informe Patten relativas al equipamiento para el orden público Documento preparado por el grupo directivo dirigido por la Oficina de Irlanda del Norte – abril de 2001
- Declaración de los Comités de Toxicidad, Mutagenicidad y Carcinogenicidad de las Sustancias Químicas en Alimentos, Productos de Consumo y Medio Ambiente sobre el Malononitrilo de 2-clorobencilideno (CS) y el CS en aerosol, septiembre de 1999. (pdf)
- Revista de Combate No Letal, enero de 2003. Una bomba de gas lacrimógeno nociva es más poderosa en la paz que en la guerra.
- "Tecnologías de control de multitudes: una evaluación de las opciones tecnológicas de control de multitudes para la Unión Europea" – Fundación Omega (pdf)
- Información de eMedicine sobre irritantes: Cs, Cn, Cnc, Ca, Cr, Cnb, PS




