Aciclovir
 | |
 | |
| Datos clínicos | |
|---|---|
| Pronunciación | / eɪ ˈ s aɪ k l oʊ v ɪər / |
| Nombres comerciales | Zovirax, otros [1] |
| Otros nombres | Acicloguanosina, aciclovir ( BAN UK ), aciclovir ( USAN US ) |
| AHFS / Drogas.com |
|
| MedlinePlus | a681045 |
| Datos de licencia |
|
Categoría de embarazo |
|
| Vías de administración | Intravenoso , por vía oral , tópico , ungüento para los ojos. |
| Código ATC | |
| Estatus legal | |
| Estatus legal | |
| Datos farmacocinéticos | |
| Biodisponibilidad | 15–20% (por vía oral) [3] |
| Unión de proteínas | 9–33% [3] |
| Metabolismo | Hígado |
| Vida media de eliminación | 2–4 horas |
| Excreción | Riñón (62–90% como fármaco inalterado) |
| Identificadores | |
| |
| Número CAS | |
| Identificador de centro de PubChem |
|
| Identificador de seguridad de PubChem |
|
| Unión Internacional para la Investigación y el Desarrollo (IUPHAR)/BPS |
|
| Banco de medicamentos | |
| Araña química | |
| UNIVERSIDAD |
|
| BARRIL | |
| EBICh | |
| Química biológica | |
| Ligando PDB |
|
| Panel de control CompTox ( EPA ) |
|
| Tarjeta informativa de la ECHA | 100.056.059 |
| Datos químicos y físicos | |
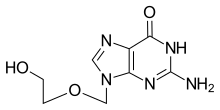
| Fórmula | C8H11N5O3 |
| Masa molar | 225,208 g·mol −1 |
| Modelo 3D ( JSmol ) |
|
| Punto de fusión | 256,5 °C (493,7 °F) |
| |
| (verificar) | |
El aciclovir , también conocido como aciclovir , [4] es un medicamento antiviral . [5] Se utiliza principalmente para el tratamiento de infecciones por el virus del herpes simple , varicela y herpes zóster . [6] Otros usos incluyen la prevención de infecciones por citomegalovirus después del trasplante y complicaciones graves de la infección por el virus de Epstein-Barr . [6] [7] Se puede tomar por vía oral, aplicar como crema o inyectar . [6]
Los efectos secundarios comunes incluyen náuseas y diarrea. [6] Los efectos secundarios potencialmente graves incluyen problemas renales y plaquetas bajas . [6] Se recomienda mayor cuidado en aquellos con función hepática o renal deficiente. [6] En general, se considera seguro para su uso en el embarazo sin que se hayan observado daños. [6] [8] Parece ser seguro durante la lactancia . [9] [10] El aciclovir es un análogo de nucleósido que imita a la guanosina . [6] Funciona disminuyendo la producción del ADN del virus . [6]
El aciclovir fue patentado en 1974 por Burroughs Wellcome y aprobado para uso médico en 1981. [11] Está en la Lista de Medicamentos Esenciales de la Organización Mundial de la Salud . [12] Está disponible como medicamento genérico y se comercializa bajo muchas marcas en todo el mundo. [1] En 2022, fue el 134.º medicamento más recetado en los Estados Unidos, con más de 4 millones de recetas. [13] [14]
Uso médico

El aciclovir se utiliza para el tratamiento de las infecciones por el virus del herpes simple (VHS) y el virus varicela zóster , incluidos: [3] [15] [16]
- Herpes simple genital (tratamiento y prevención )
- Herpes simple neonatal
- Herpes labial ( herpes labial )
- Herpes
- Varicela aguda en pacientes inmunodeprimidos
- Encefalitis por herpes simple
- Infecciones mucocutáneas agudas por VHS en pacientes inmunodeprimidos
- Herpes ocular y blefaritis por herpes simple (una forma crónica (a largo plazo) de infección ocular por herpes)
- Prevención de los virus del herpes en personas inmunodeprimidas (como personas sometidas a quimioterapia contra el cáncer) [17]
Su eficacia en el tratamiento de las infecciones por el virus de Epstein-Barr es menos clara. [6] No se ha encontrado que sea útil para la mononucleosis infecciosa debida al virus de Epstein-Barr. [18] El valaciclovir y el aciclovir actúan inhibiendo la replicación del ADN viral, pero hasta 2016 había poca evidencia de que sean efectivos contra el virus de Epstein-Barr, son caros, corren el riesgo de causar resistencia a los agentes antivirales y (en el 1% al 10% de los casos) pueden causar efectos secundarios desagradables . [19]
El aciclovir tomado por vía oral no parece disminuir el riesgo de dolor después del herpes zóster. [20] En aquellos con herpes en el ojo, el aciclovir puede ser más eficaz y seguro que la idoxuridina . [21] No está claro si las gotas oftálmicas de aciclovir son más eficaces que las gotas oftálmicas de brivudina . [21]
El aciclovir intravenoso es eficaz para tratar afecciones médicas graves causadas por diferentes especies de la familia del virus del herpes, incluidas infecciones localizadas graves del virus del herpes, herpes genital grave, varicela y encefalitis por virus del herpes . También es eficaz en infecciones sistémicas o traumáticas por herpes, eczema herpético y meningitis por virus del herpes . Las revisiones de investigaciones que datan de la década de 1980 muestran que hay algún efecto en la reducción del número y la duración de las lesiones si se aplica aciclovir en una etapa temprana de un brote. [22] La investigación muestra la efectividad del aciclovir tópico tanto en las etapas tempranas como tardías del brote, además de mejorar metodológicamente y en términos de certeza estadística de estudios previos. [23] Los ensayos con aciclovir muestran que este agente no tiene ningún papel en la prevención de la transmisión del VIH , pero puede ayudar a retardar la progresión de la enfermedad por VIH en personas que no toman terapia antirretroviral (TAR) . Este hallazgo resalta la importancia de probar estrategias simples y económicas que no sean TAR, como aciclovir y cotrimoxazol , en personas con VIH. [24]
Embarazo
Los CDC y otros han declarado que durante los episodios graves recurrentes o primeros episodios de herpes genital, se puede utilizar aciclovir. [25] Para las infecciones graves por HSV (especialmente HSV diseminado), también se puede utilizar aciclovir IV. [26]
Los estudios en ratones, conejos y ratas (con dosis más de 10 veces el equivalente a la utilizada en humanos) administradas durante la organogénesis no han podido demostrar defectos de nacimiento. [27] Los estudios en ratas a las que se les administró el equivalente a 63 veces las concentraciones estándar en estado estacionario del fármaco en humanos [Nota 1] el día 10 de gestación mostraron anomalías en la cabeza y la cola. [27]
Los CDC recomiendan el aciclovir para el tratamiento de la varicela durante el embarazo, especialmente durante el segundo y tercer trimestre. [28]
El aciclovir se excreta en la leche materna, por lo que se recomienda precaución en mujeres que amamantan. Se ha demostrado en estudios de prueba limitados que el lactante está expuesto a aproximadamente 0,3 mg/kg/día tras la administración oral de aciclovir a la madre. Si las madres lactantes tienen lesiones herpéticas cerca o sobre el pecho, se debe evitar la lactancia. [29] [30]
Efectos adversos
Terapia sistémica
Las reacciones adversas frecuentes (≥1% de los pacientes) asociadas con la terapia sistémica con aciclovir (oral o IV) incluyen náuseas, vómitos, diarrea, encefalopatía (solo con uso IV), reacciones en el lugar de la inyección (solo con uso IV) y dolor de cabeza. En dosis altas, se han reportado alucinaciones . Los efectos adversos poco frecuentes (0,1–1% de los pacientes) incluyen agitación, vértigo , confusión, mareos, edema , artralgia , dolor de garganta, estreñimiento, dolor abdominal, pérdida de cabello, erupción cutánea y debilidad. Los efectos adversos raros (<0,1% de los pacientes) incluyen coma, convulsiones, neutropenia , leucopenia , cristaluria , anorexia , fatiga, hepatitis , síndrome de Stevens-Johnson , necrólisis epidérmica tóxica , púrpura trombocitopénica trombótica , anafilaxia , [15] y síndrome de Cotard .
El aciclovir intravenoso puede causar nefrotoxicidad reversible en hasta un 5% a 10% de los pacientes debido a la precipitación de cristales de aciclovir en el riñón. La nefropatía por cristales de aciclovir es más común cuando se administra aciclovir en infusión rápida y en pacientes con deshidratación e insuficiencia renal preexistente. Una hidratación adecuada, una velocidad de infusión más lenta y una dosificación basada en la función renal pueden reducir este riesgo. [31] [32] [33]
Se ha demostrado que el metabolito del aciclovir, 9-carboximetoximetilguanina (9-CMMG), desempeña un papel en los eventos adversos neurológicos, particularmente en personas mayores y en aquellas con función renal reducida. [34] [35] [36]
Terapia tópica
La crema tópica de aciclovir se asocia comúnmente (≥1 % de los pacientes) con: piel seca o descamada o sensaciones transitorias de escozor/quemazón. Los efectos adversos poco frecuentes incluyen eritema o picazón. [15] Cuando se aplica en el ojo, el aciclovir se asocia comúnmente (≥1 % de los pacientes) con escozor leve transitorio. Con poca frecuencia (0,1–1 % de los pacientes), el aciclovir oftálmico se asocia con queratitis puntiforme superficial o reacciones alérgicas. [15]
Interacciones farmacológicas
Ketoconazol : Los estudios de replicación in vitro han demostrado una actividad antiviral sinérgica y dependiente de la dosis contra el VHS-1 y el VHS-2 cuando se administra con aciclovir. Sin embargo, este efecto no se ha establecido clínicamente y es necesario realizar más estudios para evaluar el verdadero potencial de esta sinergia. [37]
Probenecid : Se han observado informes de un aumento de la vida media del aciclovir, así como una disminución de la excreción urinaria y del aclaramiento renal en estudios en los que se administra probenecid simultáneamente con aciclovir. [29]
Interferón : tiene efectos sinérgicos cuando se administra con aciclovir y se debe tener precaución al administrar aciclovir a pacientes que reciben interferón intravenoso. [38]
Zidovudina : aunque se administra a menudo con aciclovir en pacientes con VIH, se ha informado de neurotoxicidad en al menos un paciente que presentó somnolencia extrema y letargo 30 a 60 días después de recibir aciclovir IV; los síntomas se resolvieron cuando se suspendió el aciclovir. [39]
Detección en fluidos biológicos
El aciclovir se puede cuantificar en plasma o suero para controlar la acumulación del fármaco en pacientes con disfunción renal o para confirmar un diagnóstico de intoxicación en víctimas de sobredosis aguda. [40]
Mecanismo de acción


El aciclovir es convertido por la timidina quinasa viral en monofosfato de aciclovir, que luego es convertido por las quinasas de la célula huésped en trifosfato de aciclovir (ACV-TP, también conocido como aciclo- GTP ). [27] El ACV-TP es un inhibidor muy potente de la replicación del ADN viral . El ACV-TP inhibe e inactiva competitivamente la ADN polimerasa viral . [41] Su forma monofosfato también se incorpora al ADN viral, lo que resulta en la terminación de la cadena . [27] [42] [43]
Resistencia
La resistencia al aciclovir es poco frecuente en personas con sistemas inmunitarios sanos, pero es más frecuente (hasta un 10 %) en personas con inmunodeficiencias que reciben profilaxis antiviral crónica (receptores de trasplantes, personas con síndrome de inmunodeficiencia adquirida debido a infección por VIH). Los mecanismos de resistencia en el VHS incluyen deficiencia de la timidina quinasa viral y mutaciones de la timidina quinasa viral o de la ADN polimerasa, que alteran la sensibilidad al sustrato. [44] [45]
Microbiología

El aciclovir es activo contra la mayoría de las especies de la familia de los herpesvirus . En orden descendente de actividad: [46] [47]
- Virus del herpes simple tipo I (HSV-1)
- Virus del herpes simple tipo II (HSV-2)
- Virus de la varicela zóster
- Virus de Epstein-Barr
- Citomegalovirus humano : menor actividad
Farmacocinética
El aciclovir es poco soluble en agua y tiene una biodisponibilidad oral baja (15-30%), por lo que la administración intravenosa es necesaria si se requieren altas concentraciones. Cuando se administra por vía oral, la concentración plasmática máxima se produce después de 1-2 horas. Según el Sistema de Clasificación Biofarmacéutica, el aciclovir es un fármaco de clase III, es decir, soluble con baja permeabilidad intestinal. [48] El aciclovir tiene una alta tasa de distribución; se informa que la unión a proteínas varía del 9 al 33%. [49] La vida media de eliminación (t 1/2 ) del aciclovir depende del grupo de edad; los neonatos tienen a la mitad de 4 horas, los niños de 1 a 12 años tienen a la mitad de 2 a 3 horas, mientras que los adultos tienen a la mitad de 3 horas. [3]
Química
Los detalles de la síntesis del aciclovir fueron publicados por primera vez por científicos de la Universidad de Buffalo . [50]
En el primer paso mostrado, se alquiló 2,6-dicloro purina con 1-benzoiloxi-2-clorometoxietano. El grupo cloro en la posición 6 del anillo heterocíclico es más reactivo que el cloro en la posición 2, por lo que puede reemplazarse selectivamente por un grupo amino , que luego se convirtió en una amida utilizando ácido nitroso . Finalmente, el cloro restante se reemplazó por el grupo amino de aciclovir utilizando amoníaco en metanol. [51] Se han revisado esta síntesis y otros métodos para preparar el compuesto. [52]
Historia
El aciclovir fue visto como el comienzo de una nueva era en la terapia antiviral, ya que es extremadamente selectivo y tiene baja citotoxicidad . [5] Desde su descubrimiento a mediados de la década de 1970, se ha utilizado como un fármaco eficaz para el tratamiento de infecciones causadas por la mayoría de las especies conocidas de la familia del herpesvirus, incluidos los virus del herpes simple y la varicela zóster. Los nucleósidos aislados de una esponja del Caribe , Cryptotethya crypta , fueron la base para la síntesis de aciclovir. [53] [54] [55] Fue codescubierto por Howard Schaeffer después de su trabajo con Robert Vince , S. Bittner y S. Gurwara en el análogo de adenosina acicloadenosina que mostró una prometedora actividad antiviral. [50] Más tarde, Schaeffer se unió a Burroughs Wellcome y continuó el desarrollo de aciclovir con la farmacóloga Gertrude B. Elion . [56] En 1979 se emitió una patente estadounidense sobre aciclovir que incluía a Schaeffer como inventor. [57] Más tarde, Vince inventó el abacavir , un fármaco inhibidor no selectivo de la transcriptasa inversa para pacientes con VIH. [58] Elion recibió el Premio Nobel de Medicina en 1988 , en parte por el desarrollo del aciclovir. [59]
El valaciclovir , una forma de profármaco relacionada , comenzó a utilizarse con fines médicos en 1995. Se convierte en aciclovir en el cuerpo después de su absorción. [60]
En 2009, el aciclovir en combinación con crema de hidrocortisona, comercializado como Xerese, fue aprobado en los Estados Unidos para el tratamiento temprano del herpes labial recurrente (herpes labial) para reducir la probabilidad de herpes labial ulcerativo y acortar el tiempo de curación de la lesión en adultos y niños (de seis años de edad y mayores). [61] [62]
Sociedad y cultura
Nombres
Originalmente se comercializó como Zovirax; las patentes expiraron en la década de 1990 y desde entonces es genérico y se comercializa bajo muchas marcas en todo el mundo. [1]
Notas
- ^ Sujeto a las mismas condiciones que antes
Referencias
- ^ abc "Aciclovir". Drugs.com . Archivado desde el original el 23 de septiembre de 2015. Consultado el 6 de septiembre de 2015 .
- ^ "Salud de la piel". Health Canada . 9 de mayo de 2018. Consultado el 13 de abril de 2024 .
- ^ abcd "Dosis, indicaciones, interacciones, efectos adversos y más de Zovirax (aciclovir)". Referencia de Medscape . WebMD. Archivado desde el original el 19 de febrero de 2014. Consultado el 5 de febrero de 2014 .
- ^ Kevin ES. "El Aciclovir" (en alemán). Kevin . Consultado el 25 de mayo de 2017 .
- ^ ab de Clercq E, Field HJ (5 de octubre de 2005). "Profármacos antivirales: el desarrollo de estrategias de profármacos exitosas para la quimioterapia antiviral". British Journal of Pharmacology . Vol. 147, núm. 1. Wiley-Blackwell (publicado en enero de 2006). págs. 1–11. doi :10.1038/sj.bjp.0706446. PMC 1615839 . PMID 16284630.
- ^ abcdefghij "Aciclovir". Sociedad Estadounidense de Farmacéuticos de Sistemas de Salud. Archivado desde el original el 5 de enero de 2015. Consultado el 1 de enero de 2015 .
- ^ Rafailidis PI, Mavros MN, Kapaskelis A, Falagas ME (noviembre de 2010). "Tratamiento antiviral para infecciones graves por VEB en pacientes aparentemente inmunocompetentes". Journal of Clinical Virology . 49 (3): 151–157. doi :10.1016/j.jcv.2010.07.008. PMID 20739216.
- ^ "Base de datos de prescripción de medicamentos durante el embarazo". Gobierno de Australia . 3 de marzo de 2014. Archivado desde el original el 8 de abril de 2014. Consultado el 22 de abril de 2014 .
- ^ Hamilton R (2015). Farmacopea de bolsillo Tarascon 2015, edición de lujo para bata de laboratorio . Jones & Bartlett Learning. pág. 59. ISBN 9781284057560.
- ^ "Uso de aciclovir durante la lactancia". 10 de marzo de 2015. Archivado desde el original el 5 de marzo de 2016. Consultado el 8 de marzo de 2016. Incluso con las dosis maternas más altas ,
la dosis de aciclovir en la leche es solo alrededor del 1% de una dosis infantil típica y no se esperaría que causara ningún efecto adverso en los bebés amamantados.
- ^ Fischer J, Ganellin CR (2006). Descubrimiento de fármacos basado en análogos. John Wiley & Sons. pág. 504. ISBN 9783527607495.
- ^ Organización Mundial de la Salud (2023). Selección y uso de medicamentos esenciales 2023: anexo web A: Lista modelo de medicamentos esenciales de la Organización Mundial de la Salud: 23.ª lista (2023) . Ginebra: Organización Mundial de la Salud. hdl : 10665/371090 . OMS/MHP/HPS/EML/2023.02.
- ^ "Los 300 mejores de 2022". ClinCalc . Archivado desde el original el 30 de agosto de 2024 . Consultado el 30 de agosto de 2024 .
- ^ "Estadísticas de uso del fármaco aciclovir, Estados Unidos, 2013-2022". ClinCalc . Consultado el 30 de agosto de 2024 .
- ^ abcd Rossi, S, ed. (2013). Manual de medicamentos australianos (edición de 2013). Adelaida: The Australian Medicines Handbook Unit Trust. ISBN 978-0-9805790-9-3.
- ^ Comité Conjunto de Formularios (2013). Formulario Nacional Británico (BNF) (65.ª ed.). Londres: Pharmaceutical Press. ISBN 978-0-85711-084-8.
- ^ Elad S, Zadik Y, Hewson I, Hovan A, Correa ME, Logan R, et al. (agosto de 2010). "Una revisión sistemática de las infecciones virales asociadas con afectación oral en pacientes con cáncer: un enfoque en Herpesviridea". Atención de apoyo en el cáncer . 18 (8): 993–1006. doi :10.1007/s00520-010-0900-3. PMID 20544224. S2CID 2969472.
- ^ Gershburg E, Pagano JS (agosto de 2005). "Infecciones por el virus de Epstein-Barr: perspectivas de tratamiento". The Journal of Antimicrobial Chemotherapy . 56 (2): 277–281. CiteSeerX 10.1.1.320.6721 . doi :10.1093/jac/dki240. PMID 16006448.
- ^ De Paor M, O'Brien K, Fahey T, Smith SM (diciembre de 2016). "Agentes antivirales para la mononucleosis infecciosa (fiebre glandular)". Base de Datos Cochrane de Revisiones Sistemáticas . 2016 (12): CD011487. doi :10.1002/14651858.CD011487.pub2. PMC 6463965. PMID 27933614 .
- ^ Chen N, Li Q, Yang J, Zhou M, Zhou D, He L (febrero de 2014). "Tratamiento antiviral para prevenir la neuralgia posherpética". Base de datos Cochrane de revisiones sistemáticas . 2014 (2): CD006866. doi :10.1002/14651858.CD006866.pub3. PMC 10583132. PMID 24500927 .
- ^ ab Wilhelmus KR (enero de 2015). "Tratamiento antiviral y otras intervenciones terapéuticas para la queratitis epitelial causada por el virus del herpes simple". Base de datos Cochrane de revisiones sistemáticas . 1 (1): CD002898. doi :10.1002/14651858.CD002898.pub5. PMC 4443501. PMID 25879115.
- ^ Worrall G (enero de 1996). "Aciclovir en el herpes labial recurrente". BMJ . 312 (7022): 6. doi :10.1136/bmj.312.7022.6. PMC 2349724 . PMID 8555890. Archivado desde el original el 15 de mayo de 2007. – Editorial
- ^ Spruance SL, Nett R, Marbury T, Wolff R, Johnson J, Spaulding T (julio de 2002). "Crema de aciclovir para el tratamiento del herpes simple labial: resultados de dos ensayos clínicos aleatorizados, doble ciego, controlados con vehículo y multicéntricos". Agentes antimicrobianos y quimioterapia . 46 (7): 2238–2243. doi :10.1128/aac.46.7.2238-2243.2002. PMC 127288. PMID 12069980 .
- ^ Mascolinli M, Kort R (junio de 2010). "5.ª Conferencia de la Sociedad Internacional del SIDA sobre patogénesis, tratamiento y prevención del VIH: resumen de las principales investigaciones e implicaciones para las políticas y la práctica: prevención biomédica". Revista de la Sociedad Internacional del SIDA . 13 (Supl 1): S4. doi : 10.1186/1758-2652-13-S1-S4 . PMC 2880255 . PMID 20519025.
- ^ "Medicamentos para infecciones virales no relacionadas con el VIH". Pautas de tratamiento de Medical Letter . 3 (32): 23–32. Abril de 2005. PMID 15767977.
- ^ Kaplan JE, Benson C, Holmes KK, Brooks JT, Pau A, Masur H (abril de 2009). "Directrices para la prevención y el tratamiento de infecciones oportunistas en adultos y adolescentes infectados por el VIH: recomendaciones de los CDC, los Institutos Nacionales de Salud y la Asociación de Medicina del VIH de la Sociedad de Enfermedades Infecciosas de Estados Unidos". MMWR. Recomendaciones e informes . 58 (RR-4): 1–207, cuestionario CE1–4. PMID 19357635.
- ^ abcd "NOMBRE DEL PRODUCTO DE LA INFORMACIÓN SOBRE EL MEDICAMENTO OZVIR TABLETAS" (PDF) . TGA eBusiness Services . Ranbaxy Australia Pty Ltd. 26 de agosto de 2011. Archivado desde el original el 20 de agosto de 2016 . Consultado el 6 de febrero de 2014 .
- ^ Centros para el Control y la Prevención de Enfermedades (enero de 2006). Epidemiología y prevención de enfermedades prevenibles mediante vacunación (novena edición). Fundación de Salud Pública. págs. 171–192.
- ^ ab "Etiqueta de aciclovir" (PDF) . GSK . FDA. 2005. Archivado desde el original (PDF) el 8 de septiembre de 2017.
- ^ Gartner LM, Morton J, Lawrence RA, Naylor AJ, O'Hare D, Schanler RJ, et al. (febrero de 2005). "Lactancia materna y uso de leche materna". Pediatría . 115 (2): 496–506. doi : 10.1542/peds.2004-2491 . PMID 15687461. S2CID 5791615.
- ^ Razonable RR (octubre de 2011). «Medicamentos antivirales para virus distintos del virus de inmunodeficiencia humana». Mayo Clinic Proceedings . 86 (10): 1009–1026. doi :10.4065/mcp.2011.0309. PMC 3184032 . PMID 21964179.
- ^ Brigden D, Rosling AE, Woods NC (julio de 1982). "Función renal después de la inyección intravenosa de aciclovir". The American Journal of Medicine . 73 (1A): 182–185. doi :10.1016/0002-9343(82)90087-0. PMID 6285711.
- ^ Sawyer MH, Webb DE, Balow JE, Straus SE (junio de 1988). "Insuficiencia renal inducida por aciclovir. Curso clínico e histología". The American Journal of Medicine . 84 (6): 1067–1071. doi :10.1016/0002-9343(88)90313-0. PMID 3376977.
- ^ Helldén A, Odar-Cederlöf I, Diener P, Barkholt L, Medin C, Svensson JO, et al. (junio de 2003). "Concentraciones séricas elevadas del principal metabolito del aciclovir, la 9-carboximetoximetilguanina, en pacientes con insuficiencia renal y efectos secundarios neuropsiquiátricos relacionados con el aciclovir: un estudio observacional". Nefrología, diálisis y trasplante . 18 (6): 1135–1141. doi : 10.1093/ndt/gfg119 . PMID 12748346.
- ^ Berry L, Venkatesan P (diciembre de 2014). "Neurotoxicidad inducida por aciclovir: utilidad de los niveles de CMMG en el LCR y el suero en el diagnóstico". Journal of Clinical Virology . 61 (4): 608–610. doi :10.1016/j.jcv.2014.09.001. PMID 25440915.
- ^ Chowdhury MA, Derar N, Hasan S, Hinch B, Ratnam S, Assaly R (2016). "Neurotoxicidad inducida por aciclovir: informe de un caso y revisión de la literatura". American Journal of Therapeutics . 23 (3): e941–e943. doi :10.1097/MJT.0000000000000093. PMID 24942005. S2CID 32983100.
- ^ Pottage JC, Kessler HA, Goodrich JM, Chase R, Benson CA, Kapell K, et al. (agosto de 1986). "Actividad in vitro del ketoconazol contra el virus del herpes simple". Agentes antimicrobianos y quimioterapia . 30 (2): 215–219. doi : 10.1128 /aac.30.2.215. PMC 180521. PMID 3021048.
- ^ GlaxoSmithKline. Información de prescripción de Zovirax® (aciclovir sódico) inyectable. Research Triangle Park, NC; noviembre de 2003
- ^ Bach MC (febrero de 1987). "Posible interacción farmacológica durante la terapia con azidotimidina y aciclovir para el SIDA". The New England Journal of Medicine . 316 (9): 547. doi :10.1056/NEJM198702263160912. PMID 3468354.
- ^ Baselt RC (2008). Disposición de fármacos y sustancias químicas tóxicas en el hombre (8.ª ed.). Foster City, CA: Biomedical Publications. pp. 29–31. ISBN 9780962652370.
- ^ "Cápsulas de VALTREX (clorhidrato de valaciclovir) -GSKSource". gsksource.com . Consultado el 2 de agosto de 2019 .
- ^ "Acyclovir (acyclovir) Capsule Acyclovir (acyclovir) Tablet [Genpharm Inc.]". DailyMed . Genpharm Inc. Noviembre de 2006. Archivado desde el original el 21 de febrero de 2014 . Consultado el 5 de febrero de 2014 .
- ^ "Comprimidos de aciclovir BP 400 mg - Resumen de las características del producto (RCP)". Compendio electrónico de medicamentos . Actavis UK Ltd. 20 de agosto de 2012. Archivado desde el original el 22 de febrero de 2014. Consultado el 5 de febrero de 2014 .
- ^ Sweetman, S, ed. (7 de agosto de 2013). "Aciclovir". Martindale: The Complete Drug Reference . Londres, Reino Unido: Pharmaceutical Press . Consultado el 6 de febrero de 2014 .
- ^ Piret J, Boivin G (febrero de 2011). "Resistencia de los virus del herpes simple a los análogos de nucleósidos: mecanismos, prevalencia y tratamiento". Agentes antimicrobianos y quimioterapia . 55 (2): 459–472. doi :10.1128/AAC.00615-10. PMC 3028810. PMID 21078929 .
- ^ O'Brien JJ, Campoli-Richards DM (marzo de 1989). "Aciclovir. Una revisión actualizada de su actividad antiviral, propiedades farmacocinéticas y eficacia terapéutica". Drugs . 37 (3): 233–309. doi : 10.2165/00003495-198937030-00002 . PMID 2653790. S2CID 240858022.
- ^ Wagstaff AJ, Faulds D, Goa KL (enero de 1994). "Aciclovir. Una reevaluación de su actividad antiviral, propiedades farmacocinéticas y eficacia terapéutica". Drugs . 47 (1): 153–205. doi : 10.2165/00003495-199447010-00009 . PMID 7510619.
- ^ Karmoker JR, Hasan I, Ahmed N, Saifuddin M, Reza MS (2019). "Desarrollo y optimización de microesferas mucoadhesivas cargadas con aciclovir mediante diseño Box-Behnken". Revista de Ciencias Farmacéuticas de la Universidad de Dhaka . 18 (1): 1–12. doi : 10.3329/dujps.v18i1.41421 .
- ^ "Comprimidos de aciclovir BP 400 mg - Resumen de las características del producto (RCP) - (emc)". www.medicines.org.uk .
- ^ ab Schaeffer HJ, Gurwara S, Vince R, Bittner S (abril de 1971). "Nuevo sustrato de la adenosina desaminasa". Journal of Medicinal Chemistry . 14 (4): 367–369. doi :10.1021/jm00286a024. PMID 5553754.
- ^ Patente estadounidense 4199574, Schaeffer HJ, "Métodos y composiciones para tratar infecciones virales y nucleósidos acíclicos de guanina", publicada el 22 de abril de 1980, asignada a Burroughs Wellcome.
- ^ Vardanyan R, Hruby V (2016). "34: Medicamentos antivirales". Síntesis de los medicamentos más vendidos . Academic Press. págs. 706–708. doi : 10.1016/B978-0-12-411492-0.00034-1 . ISBN . 9780124114920.S2CID 75449475 .
- ^ Garrison T (1999). Oceanografía: una invitación a la ciencia marina, 3.ª ed . Belmont, CA: Wadsworth Publishing Company. pág. 471.
- ^ Sepčić K (2000). "Compuestos bioactivos de alquilpiridinio de esponjas marinas". Toxin Reviews . 19 (2): 139–160. doi :10.1081/TXR-100100318. S2CID 84041855.
- ^ Laport MS, Santos OC, Muricy G (enero de 2009). "Esponjas marinas: fuentes potenciales de nuevos fármacos antimicrobianos". Current Pharmaceutical Biotechnology . 10 (1): 86–105. doi :10.2174/138920109787048625. PMID 19149592.
- ^ Elion GB, Furman PA, Fyfe JA, de Miranda P, Beauchamp L, Schaeffer HJ (diciembre de 1977). "Selectividad de la acción de un agente antiherpético, 9-(2-hidroxietoximetil)guanina". Actas de la Academia Nacional de Ciencias de los Estados Unidos de América . 74 (12): 5716–5720. Bibcode :1977PNAS...74.5716E. doi : 10.1073/pnas.74.12.5716 . PMC 431864 . PMID 202961.
- ^ US 4146715, Schaeffer HJ, "2-Amido-9-(2-aciloxietoximetil)hipoxantinas", expedida el 27 de marzo de 1979, asignada a Burrough Wellcome Co.
- ^ Vince R (2008). "Una breve historia del desarrollo de Ziagen". Chemtracts . 21 : 127–134.
- ^ "El Premio Nobel - Gertrude B. Elion".
- ^ "Monografía de clorhidrato de valaciclovir para profesionales". Drugs.com . Sociedad Estadounidense de Farmacéuticos del Sistema de Salud . Consultado el 17 de marzo de 2019 .
- ^ "Paquete de aprobación de medicamentos: Aciclovir e hidrocortisona NDA n.º 022436". Administración de Alimentos y Medicamentos de Estados Unidos (FDA) . 13 de diciembre de 2019. Archivado desde el original el 13 de diciembre de 2019. Consultado el 13 de diciembre de 2019 .
 Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público .
Este artículo incorpora texto de esta fuente, que se encuentra en el dominio público . - ^ "Xerese - crema de aciclovir e hidrocortisona". DailyMed . 12 de diciembre de 2019. Archivado desde el original el 13 de diciembre de 2019 . Consultado el 12 de diciembre de 2019 .
Lectura adicional
- Hazra S, Konrad M, Lavie A (agosto de 2010). "El anillo de azúcar del nucleósido es necesario para el posicionamiento productivo del sustrato en el sitio activo de la desoxicitidina quinasa humana (dCK): implicaciones para el desarrollo de análogos de guanina acíclicas activados por dCK". Journal of Medicinal Chemistry . 53 (15): 5792–5800. doi :10.1021/jm1005379. PMC 2936711 . PMID 20684612.
- Harvey SC (1990). "Absorción, acción y disposición de fármacos". En Remington JP, Gennaro AR (eds.). Remington's Pharmaceutical Sciences (18.ª ed.). Easton, Pensilvania: Mack Pub. Co. págs. 697–702. ISBN 978-0-912734-04-0.
- Huovinen P, Valtonen V (1994). Neuvonen PJ (ed.). Kliininen Farmakologia (en finlandés). Helsinki: Kandidaattikustannus Oy. ISBN 951-8951-09-8.
- Périgaud C, Gosselin G, Imbach JL (1992). "Análogos de nucleósidos como agentes quimioterapéuticos: una revisión". Nucleósidos y nucleótidos . 11 (2–4): 903–945. doi :10.1080/07328319208021748.
- Rang HP, Dale MM, Ritter JM (2003). Farmacología (5.ª ed.). Pearson Professional Ltd. ISBN 0-443-07145-4.




