Inhibidor de la recaptación de serotonina y noradrenalina
| Inhibidor de la recaptación de serotonina y noradrenalina | |
|---|---|
| Clase de droga | |
 Duloxetina , un ejemplo de un IRSN. | |
| Identificadores de clase | |
| Sinónimos | Inhibidor selectivo de la recaptación de serotonina y noradrenalina; SNaRI |
| Usar | Depresión ; Ansiedad ; Dolor ; Obesidad ; Síntomas de la menopausia |
| Objetivo biológico | Transportador de serotonina ; Transportador de noradrenalina |
| Enlaces externos | |
| Malla | D000068760 |
| Estatus legal | |
| En Wikidata | |
Los inhibidores de la recaptación de serotonina y noradrenalina ( IRSN ) son una clase de medicamentos antidepresivos que se utilizan para tratar el trastorno depresivo mayor (TDM), los trastornos de ansiedad , la fobia social, el dolor neuropático crónico , el síndrome de fibromialgia (SFM) y los síntomas de la menopausia . Los usos no aprobados incluyen tratamientos para el trastorno por déficit de atención con hiperactividad (TDAH), el trastorno obsesivo-compulsivo (TOC) y la prevención de la migraña . [1] Los IRSN son inhibidores de la recaptación de monoamina ; específicamente, inhiben la recaptación de serotonina y noradrenalina . Se cree que estos neurotransmisores desempeñan un papel importante en la regulación del estado de ánimo. Los IRSN se pueden contrastar con los inhibidores selectivos de la recaptación de serotonina (ISRS) y los inhibidores de la recaptación de noradrenalina (IRN), que actúan sobre neurotransmisores individuales. [2]
El transportador de serotonina humano (SERT) y el transportador de noradrenalina (NAT) son proteínas de transporte de membrana que son responsables de la recaptación de serotonina y noradrenalina desde la hendidura sináptica hacia la terminal nerviosa presináptica. La inhibición dual de la recaptación de serotonina y noradrenalina puede ofrecer ventajas sobre otros fármacos antidepresivos al tratar una gama más amplia de síntomas. [3] Pueden ser especialmente útiles en el dolor crónico o neuropático concomitante . [4]
Los ISRN, junto con los ISRS y los INR, son antidepresivos de segunda generación . Desde su introducción a fines de la década de 1980, los antidepresivos de segunda generación han reemplazado en gran medida a los antidepresivos de primera generación, como los antidepresivos tricíclicos (ATC) y los inhibidores de la monoaminooxidasa (IMAO), como los medicamentos de elección para el tratamiento del TDM debido a su mejor tolerabilidad y perfil de seguridad. [5]
Medicamentos

Hay ocho IRSN aprobados por la FDA en los Estados Unidos, siendo la venlafaxina el primer fármaco desarrollado en 1993 y el levomilnacipran el último en desarrollarse en 2013. Los fármacos varían según sus otros usos médicos, estructura química, efectos adversos y eficacia. [6]
| Medicamento | Nombre de marca | Indicaciones de la FDA | Año de aprobación | Estructura química | Notas |
|---|---|---|---|---|---|
| Desvenlafaxina [7] | Pristiq Khedezla (ER) |
| 2007 |  | El metabolito activo de la venlafaxina. Se cree que actúa de manera similar, aunque algunas evidencias sugieren tasas de respuesta más bajas en comparación con la venlafaxina y la duloxetina. Fue introducido por Wyeth en mayo de 2008 y fue entonces el tercer IRSN aprobado. [8] |
| Duloxetina [9] | Cymbalta Irenka |
| 2004 |  | Aprobado para el tratamiento de la depresión y el dolor neuropático en agosto de 2004. La duloxetina está contraindicada en pacientes con consumo excesivo de alcohol o enfermedad hepática crónica, ya que la duloxetina puede aumentar los niveles de ciertas enzimas hepáticas que pueden provocar hepatitis aguda u otras enfermedades en ciertos pacientes en riesgo. El riesgo de daño hepático parece ser sólo para pacientes que ya están en riesgo, a diferencia del antidepresivo nefazodona , que, aunque poco común, puede causar espontáneamente insuficiencia hepática en pacientes sanos. [13] La duloxetina también está aprobada para el trastorno depresivo mayor (TDM), el trastorno de ansiedad generalizada (TAG), la neuropatía diabética, el dolor musculoesquelético crónico, incluido el dolor crónico de osteoartritis y el dolor lumbar crónico . [11] La duloxetina también sufre metabolismo hepático y se ha demostrado que causa inhibición de la enzima hepática citocromo P450 CYP 2D6 . [14] Se debe tener precaución al tomar Duloxetina con otros medicamentos que se metabolizan por CYP 2D6 ya que esto puede precipitar una posible interacción fármaco-fármaco. [14] |
| Levomilnacipran | Fetzima |
| 2013 | 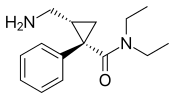 | El isómero levógiro del milnaciprán. En desarrollo para el tratamiento de la depresión en Estados Unidos y Canadá, fue aprobado por la FDA para el tratamiento del trastorno depresivo mayor en julio de 2013. |
| Milnaciprán | Impulsor Ixel Savella |
| 1996 |  | Se ha demostrado que es significativamente eficaz en el tratamiento de la depresión y la fibromialgia. [15] La Administración de Alimentos y Medicamentos (FDA) aprobó el milnaciprán para el tratamiento de la fibromialgia en los Estados Unidos en enero de 2009, sin embargo, no está aprobado para la depresión en ese país. [ cita requerida ] El milnaciprán ha estado disponible comercialmente en Europa y Asia durante varios años. [ cita requerida ] Se introdujo por primera vez en Francia en 1996. [ cita requerida ] |
| Sibutramina | Meridiana |
| 1997 |  | Un inhibidor selectivo de la recaptación de serotonina y norepinefrina (IRSN) que, en lugar de desarrollarse para el tratamiento de la depresión, se comercializó ampliamente como un supresor del apetito con fines de pérdida de peso . La sibutramina fue el primer fármaco para el tratamiento de la obesidad que se aprobó en 30 años. [17] Se ha asociado con un aumento de eventos cardiovasculares y accidentes cerebrovasculares y se retiró del mercado en varios países y regiones, incluido Estados Unidos, en 2010. [18] |
| Tramadol | Ultram |
| 1977 | 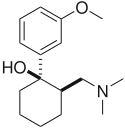 | Es un opioide débil y un inhibidor selectivo de la recaptación de serotonina y noradrenalina (IRSN). Fue aprobado por la FDA en 1995, aunque se comercializa en Alemania desde 1977. El fármaco se utiliza para tratar el dolor agudo y crónico. Ha demostrado ser eficaz en el tratamiento de la fibromialgia, aunque no está aprobado específicamente para este fin. El fármaco también se está investigando como antidepresivo y para el tratamiento del dolor neuropático. Su estructura química es similar a la de la venlafaxina. Debido a que es un opioide, existe riesgo de abuso y adicción, pero tiene menos potencial de abuso, depresión respiratoria y estreñimiento en comparación con otros opioides (hidrocodona, oxicodona, etc.). [19] |
| Venlafaxina | Effexor |
| 1994 |  | El primer inhibidor selectivo de la recaptación de serotonina y noradrenérgico (ISRN) y el más utilizado. Fue introducido por Wyeth en 1994. Los efectos de recaptación de venlafaxina dependen de la dosis. En dosis bajas (<150 mg/día), actúa sólo sobre la transmisión serotoninérgica. En dosis moderadas (>150 mg/día), actúa sobre los sistemas serotoninérgico y noradrenérgico, mientras que en dosis altas (>300 mg/día), también afecta la neurotransmisión dopaminérgica. [22] En dosis pequeñas, la venlafaxina también ha demostrado ser eficaz en el tratamiento de los síntomas vasomotores (sofocos y sudores nocturnos) de la menopausia. [21] |
Historia
En 1952, se descubrió que la iproniazida , un agente antimicobacteriano , tenía propiedades psicoactivas mientras se investigaba como un posible tratamiento para la tuberculosis . Los investigadores notaron que los pacientes que recibían iproniazida se volvían más alegres, más optimistas y más activos físicamente. Poco después de su desarrollo, se demostró que la iproniazida y las sustancias relacionadas ralentizaban la descomposición enzimática de la serotonina, la dopamina y la noradrenalina mediante la inhibición de la enzima monoaminooxidasa . Por esta razón, esta clase de medicamentos se conoció como inhibidores de la monoaminooxidasa o IMAO. Durante este tiempo, también se investigó el desarrollo de agentes antidepresivos distintivamente diferentes. La imipramina se convirtió en el primer antidepresivo tricíclico (ATC) clínicamente útil . Se descubrió que la imipramina afectaba a numerosos sistemas de neurotransmisores y bloqueaba la recaptación de noradrenalina y serotonina de la sinapsis , aumentando así los niveles de estos neurotransmisores. El uso de IMAO y ATC proporcionó avances importantes en el tratamiento de la depresión , pero su uso estuvo limitado por efectos secundarios desagradables y problemas importantes de seguridad y toxicidad . [23]
Durante los años 1960 y 1970, la hipótesis de las catecolaminas en la emoción y su relación con la depresión fue de amplio interés y la disminución de los niveles de ciertos neurotransmisores, como la noradrenalina, la serotonina y la dopamina, podría desempeñar un papel en la patogénesis de la depresión. Esto condujo al desarrollo de la fluoxetina , el primer ISRS. El perfil mejorado de seguridad y tolerabilidad de los ISRS en pacientes con TDM, en comparación con los ATC y los IMAO, representó otro avance importante en el tratamiento de la depresión. [23]
Desde finales de los años 1980, los ISRS han dominado el mercado de los antidepresivos. Hoy en día, hay un mayor interés en los antidepresivos con mecanismos de acción más amplios que pueden ofrecer mejoras en la eficacia y la tolerabilidad. En 1993, se introdujo en el mercado estadounidense un nuevo fármaco llamado venlafaxina , un inhibidor de la recaptación de serotonina y noradrenalina. [20] La venlafaxina fue el primer compuesto descrito en una nueva clase de sustancias antidepresivas llamadas feniletilaminas . Estas sustancias no están relacionadas con los ATC ni con otros ISRS. La venlafaxina bloquea la recaptación neuronal de serotonina, noradrenalina y, en menor medida, dopamina en el sistema nervioso central . A diferencia de varios otros antidepresivos, la venlafaxina puede inducir un inicio rápido de acción debido principalmente a una inhibición posterior de la recaptación de noradrenalina. [24] Véase la cronología en la figura 1.

Mecanismo de acción
Las monoaminas están relacionadas con la fisiopatología de la depresión. Los síntomas pueden aparecer porque las concentraciones de neurotransmisores, como la noradrenalina y la serotonina, son insuficientes, lo que provoca cambios posteriores. [10] [25] Los medicamentos para la depresión afectan la transmisión de serotonina, noradrenalina y dopamina. [10] Los antidepresivos más antiguos y menos selectivos, como los ATC y los IMAO, inhiben la recaptación o el metabolismo de la noradrenalina y la serotonina en el cerebro, lo que da lugar a concentraciones más altas de neurotransmisores. [25] Los antidepresivos que tienen mecanismos de acción duales inhiben la recaptación tanto de serotonina como de noradrenalina y, en algunos casos, inhiben con un efecto débil la recaptación de dopamina. [10] Los antidepresivos afectan a receptores neuronales variables como los canales colinérgicos muscarínicos, α 1 y α 2 -adrenérgicos, H 1 -histaminérgicos y de sodio en el músculo cardíaco , lo que lleva a una disminución de la conducción cardíaca y cardiotoxicidad asociada particularmente con los ATC, y en menor medida con los ISRS. [26] La selectividad de los agentes antidepresivos se basa en los neurotransmisores que se cree que influyen en los síntomas de la depresión. [27] Los medicamentos que bloquean selectivamente la recaptación de serotonina y norepinefrina tratan eficazmente la depresión y son mejor tolerados que los ATC. Los ATC tienen efectos integrales en varios receptores de neurotransmisores, lo que conduce a la falta de tolerabilidad y un mayor riesgo de toxicidad. [2]
Antidepresivos tricíclicos

Los ATC fueron los primeros medicamentos que tenían un mecanismo de acción dual. El mecanismo de acción de los antidepresivos tricíclicos de aminas secundarias se entiende solo en parte. Los ATC tienen efectos de inhibición dual sobre los transportadores de recaptación de noradrenalina y los transportadores de recaptación de serotonina. Se obtienen mayores concentraciones de noradrenalina y serotonina inhibiendo ambas proteínas transportadoras. Los ATC tienen una afinidad sustancialmente mayor por las proteínas de recaptación de noradrenalina que los ISRS. Esto se debe a la formación de metabolitos de ATC de aminas secundarias. [28] [29]
Además, los ATC interactúan con los receptores adrenérgicos . Esta interacción parece ser fundamental para aumentar la disponibilidad de noradrenalina en las hendiduras sinápticas o cerca de ellas. Las acciones de los antidepresivos tricíclicos similares a la imipramina tienen adaptaciones secundarias complejas a sus acciones iniciales y sostenidas como inhibidores del transporte de noradrenalina y bloqueo variable del transporte de serotonina.
La noradrenalina interactúa con los subtipos de receptores adrenérgicos postsinápticos α y β y con los autorreceptores presinápticos α 2. Los receptores α 2 incluyen autorreceptores presinápticos que limitan la actividad neurofisiológica de las neuronas noradrenérgicas en el sistema nervioso central . La formación de noradrenalina es reducida por los autorreceptores a través de la enzima limitante de la velocidad tirosina hidroxilasa , un efecto mediado por la disminución de la fosforilación mediada por AMP cíclico -activación de la enzima . [29] Los receptores α 2 también causan una disminución de la expresión intracelular de AMP cíclico que resulta en la relajación del músculo liso o una disminución de la secreción. [30]
Los ATC activan un mecanismo de retroalimentación negativa a través de sus efectos sobre los receptores presinápticos. Una explicación probable de los efectos sobre la disminución de la liberación de neurotransmisores es que, a medida que los receptores se activan, se produce una inhibición de la liberación de neurotransmisores (incluida la supresión de las corrientes de Ca2 + dependientes del voltaje y la activación de las corrientes de K + operadas por el receptor acoplado a la proteína G ). La exposición repetida a agentes con este tipo de mecanismo conduce a la inhibición de la liberación de neurotransmisores, pero la administración repetida de ATC finalmente conduce a una disminución de las respuestas de los receptores α2 . La desensibilización de estas respuestas puede deberse a una mayor exposición a la noradrenalina endógena o a la ocupación prolongada de los mecanismos de transporte de noradrenalina (a través de un efecto alostérico). La adaptación permite que la síntesis y secreción presináptica de noradrenalina vuelva a, o incluso supere, los niveles normales de noradrenalina en las hendiduras sinápticas. En general, la inhibición de la recaptación de noradrenalina inducida por los ATC conduce a una disminución de las tasas de activación neuronal (mediada a través de los autorreceptores α 2 ), de la actividad metabólica y de la liberación de neurotransmisores. [29]
Los ATC no bloquean el transporte de dopamina directamente, pero podrían facilitar los efectos dopaminérgicos indirectamente al inhibir el transporte de dopamina a las terminales noradrenérgicas de la corteza cerebral . [29] Debido a que afectan a tantos receptores diferentes, los ATC tienen efectos adversos, poca tolerabilidad y un mayor riesgo de toxicidad. [2]
Inhibidores selectivos de la recaptación de serotonina
Los inhibidores selectivos de la recaptación de serotonina (ISRS) inhiben selectivamente la recaptación de serotonina y son un grupo ampliamente utilizado de antidepresivos. [31] Con una mayor selectividad del receptor en comparación con los ATC, se evitan efectos no deseados como la mala tolerabilidad. [29] La serotonina se sintetiza a partir de un aminoácido llamado L -triptófano . El sistema de transporte activo regula la captación de triptófano a través de la barrera hematoencefálica . Las vías serotoninérgicas se clasifican en dos vías principales en el cerebro: las proyecciones ascendentes desde el rafe medial y dorsal y las proyecciones descendentes desde el rafe caudal hacia la médula espinal .
Inhibidores selectivos de la recaptación de noradrenalina
Las neuronas noradrenérgicas se encuentran en dos regiones principales del cerebro: el locus coeruleus y el tegmental lateral . Con la administración de IRSN, se induce la actividad neuronal en la región del locus coeruleus debido al aumento de la concentración de noradrenalina en la hendidura sináptica. Esto da como resultado la activación de los receptores adrenérgicos α2 [25] , como se mencionó anteriormente.
Los ensayos han demostrado que los IRSN tienen una tendencia insignificante hacia los receptores mACh , α 1 y α 2 adrenérgicos o H 1 . [27]
Inhibidores duales de la recaptación de serotonina y noradrenalina
Los agentes con doble inhibición de la recaptación de serotonina y noradrenalina (IRSN) a veces se denominan inhibidores no tricíclicos de la recaptación de serotonina y noradrenalina. Los estudios clínicos sugieren que los compuestos que aumentan la concentración en la hendidura sináptica tanto de noradrenalina como de serotonina son más exitosos que los agentes de acción única en el tratamiento de la depresión, pero los datos no son concluyentes sobre si los IRSN son una opción de tratamiento más eficaz que los ISRS para la depresión. [32] [33] [34]
Los IRSN no tricíclicos tienen varias diferencias importantes que se basan en la farmacocinética, el metabolismo a metabolitos activos, la inhibición de las isoformas del CYP , el efecto de las interacciones fármaco-fármaco y la vida media de los IRSN no tricíclicos. [28] [35]
La combinación de mecanismos de acción en un único agente activo es un avance importante en psicofarmacología . [35]
Relación estructura-actividad
Andamiaje de ariloxipropanamina
Varios inhibidores de la recaptación contienen un andamiaje de ariloxipropanamina. Este motivo estructural tiene potencial para la unión de alta afinidad a los transportes de aminas biógenas. [35] Los fármacos que contienen un andamiaje de ariloxipropanamina tienen un perfil de selectividad para los transportadores de noradrenalina y serotonina que depende del patrón de sustitución del anillo ariloxi. Los NRI selectivos contienen un sustituyente en la posición 2' del anillo ariloxi, pero los ISRS contienen un sustituyente en la posición 4' del anillo ariloxi. La atomoxetina, la nisoxetina y la reboxetina tienen un grupo de sustitución en la posición 2' y son NRI selectivos, mientras que los compuestos que tienen un grupo de sustitución en la posición 4' (como la fluoxetina y la paroxetina ) son ISRS. La duloxetina contiene un grupo fenilo fusionado en las posiciones 2' y 3', por lo tanto, tiene efectos inhibidores selectivos duales de la recaptación de noradrenalina y serotonina y tiene potencias similares para ambos transportadores. [36] La naturaleza del sustituyente aromático también tiene una influencia significativa en la actividad y selectividad de los compuestos como inhibidores de los transportadores de serotonina o noradrenalina. [35]

Andamiaje de cicloalcanol-etilamina
La venlafaxina y la desvenlafaxina contienen un andamiaje de cicloalcanol etilamina. Aumentar la naturaleza atractora de electrones del anillo aromático proporciona un efecto inhibidor más potente de la captación de norepinefrina y mejora la selectividad de la norepinefrina sobre el transportador de serotonina. [36] Se probaron los efectos de los sustituyentes cloro, metoxi y trifluorometilo en el anillo aromático del andamiaje de cicloalcanol etilamina. Los resultados mostraron que el análogo m -trifluorometilo con mayor capacidad atractora de electrones exhibió el efecto inhibidor más potente de la norepinefrina y la mayor selectividad sobre la captación de serotonina. [36] WY-46824 , un derivado que contiene piperazina, ha mostrado inhibición de la recaptación de norepinefrina y dopamina . Una síntesis y pruebas posteriores identificaron WAY-256805, un potente inhibidor de la recaptación de noradrenalina que mostró una excelente selectividad y fue eficaz en modelos animales de depresión, dolor y disfunción termorreguladora. [37]

Milnaciprán

El milnaciprán es estructuralmente diferente de otros SNRI. [28] La relación estructura-actividad de los derivados del milnaciprán a nivel de transportador todavía no está muy clara y se basa en la eficacia in vivo que se informó en 1987. La N -metilación del milnaciprán en el grupo sustituyente R 4 y R 5 reduce la actividad de la noradrenalina y la serotonina. [38] Las investigaciones sobre diferentes amidas secundarias en los grupos de sustitución R 6 y R 7 mostraron que los electrones π juegan un papel importante en la interacción entre transportadores y ligandos. Un grupo fenilo en el sustituyente R 6 mostró efecto sobre los transportadores de noradrenalina. Los grupos sustituyentes en R 6 y R 7 con doble enlace alílico mostraron un efecto mejorado significativo sobre los transportadores de noradrenalina y serotonina. [38] Los estudios muestran que al introducir un grupo 2-metilo en el sustituyente R 3 , la potencia en los transportadores de noradrenalina y serotonina se elimina casi por completo. Los grupos metilo en los grupos sustituyentes R 1 y R 2 también eliminan la potencia de los transportadores de noradrenalina y serotonina. Los investigadores descubrieron que reemplazar uno de los grupos etilo del milnaciprán con una fracción alílica aumenta la potencia de la noradrenalina. [39] El farmacóforo de los derivados del milnaciprán aún no está del todo claro. [38]
La conformación del milnaciprán es una parte importante de su farmacóforo. Cambiar su estereoquímica afecta la concentración de noradrenalina y serotonina. El milnaciprán se comercializa como una mezcla racémica . Los efectos del milnaciprán residen en el isómero (1 S ,2 R ) y la sustitución del grupo fenilo en el isómero (1 S ,2 R ) tiene un impacto negativo en la concentración de noradrenalina. [39] El milnaciprán tiene un peso molecular bajo y una lipofilicidad baja . Debido a estas propiedades, el milnaciprán exhibe una farmacocinética casi ideal en humanos, como alta biodisponibilidad , baja variabilidad intersujeto, interacción limitada con enzimas hepáticas , distribución tisular moderada y una vida media de eliminación razonablemente larga. Se cree que la falta de interacciones fármaco-fármaco del milnaciprán a través de las enzimas del citocromo P450 es una característica atractiva porque muchos de los fármacos del sistema nervioso central son altamente lipofílicos y se eliminan principalmente por enzimas hepáticas. [39]
Desarrollo futuro de la relación estructura-actividad
La aplicación de un andamiaje de ariloxipropanamina ha generado una serie de IMAO potentes. [40] Antes del desarrollo de la duloxetina, la exploración de las relaciones entre la estructura y la actividad de la ariloxipropanamina dio como resultado la identificación de la fluoxetina y la atomoxetina. El mismo motivo se puede encontrar en la reboxetina, donde está restringida en un sistema de anillo de morfolina . Se han realizado algunos estudios en los que el oxígeno de la reboxetina se reemplaza por azufre para dar ariltiometilmorfolina. Algunos de los derivados de ariltiometilmorfolina mantienen niveles potentes de inhibición de la recaptación de serotonina y norepinefrina. La inhibición dual de la recaptación de serotonina y norepinefrina reside en diferentes enantiómeros para el andamiaje de ariltiometilmorfolina. [41] También se han derivado posibles fármacos candidatos con actividad inhibidora dual de la recaptación de serotonina y norepinefrina a partir de plantillas de piperazina, 3-amino-pirrolidina y bencilamina. [42]
Ensayos clínicos
Depresión
Varios estudios han demostrado que los fármacos antidepresivos que combinan actividad serotoninérgica y noradrenérgica son generalmente más eficaces que los ISRS, que actúan sobre la recaptación de serotonina por sí mismos. Los fármacos antidepresivos serotoninérgicos-noradrenérgicos pueden tener una modesta ventaja de eficacia en comparación con los ISRS en el tratamiento del trastorno depresivo mayor (TDM), [43] pero son ligeramente peor tolerados. [44] Se necesitan más investigaciones para examinar las posibles diferencias de eficacia en subpoblaciones específicas de TDM o para síntomas específicos de TDM, entre estas clases de fármacos antidepresivos.
Analgésico
Los datos de los ensayos clínicos han indicado que los IRSN podrían tener propiedades analgésicas. Aunque la percepción y transmisión de los estímulos del dolor en el sistema nervioso central no se han dilucidado por completo, hay datos extensos que respaldan el papel de la serotonina y la noradrenalina en la modulación del dolor. Los hallazgos de los ensayos clínicos en humanos han demostrado que estos antidepresivos pueden ayudar a reducir el dolor y el deterioro funcional en las afecciones de dolor central y neuropático. Esta propiedad de los IRSN podría usarse para reducir las dosis de otros medicamentos analgésicos y disminuir la frecuencia de problemas de seguridad, eficacia limitada y tolerabilidad. [45] Los datos de la investigación clínica han demostrado en pacientes con TAG que el IRSN duloxetina es significativamente más eficaz que el placebo para reducir los síntomas relacionados con el dolor del TAG, después del tratamiento a corto y largo plazo. Sin embargo, los hallazgos sugirieron que dichos síntomas de dolor físico reaparecen en situaciones de recaída, lo que indica la necesidad de un tratamiento continuo en pacientes con TAG y síntomas físicos dolorosos concurrentes. [46]
Indicaciones
Los IRSN se han probado para el tratamiento de las siguientes afecciones:
- Trastorno depresivo mayor (TDM)
- Trastorno de estrés postraumático (TEPT)
- Trastorno de ansiedad generalizada (TAG)
- Trastorno de ansiedad social (TAS)
- Trastorno obsesivo compulsivo [47]
- Trastorno de pánico
- Dolor neuropático
- Fibromialgia
- Dolor musculoesquelético crónico
Farmacología
Vía de administración
セロトニン・ノルアドレナリン,サインバルタ,デュロキセチン,再取り込み阻害薬DSCF7713.jpg/440px-2024-03-16_Duloxetine(SNRI)セロトニン・ノルアドレナリン,サインバルタ,デュロキセチン,再取り込み阻害薬DSCF7713.jpg)
Los inhibidores de la recaptación de serotonina y noradrenalina se administran por vía oral, generalmente en forma de cápsulas o comprimidos. Se recomienda tomar los inhibidores de la recaptación de serotonina y noradrenalina por la mañana con el desayuno, lo que no afecta los niveles del fármaco, pero puede ayudar con ciertos efectos secundarios. [48] La noradrenalina tiene efectos activadores en el cuerpo y, por lo tanto, puede causar insomnio en algunos pacientes si se toma antes de acostarse. [49] Los inhibidores de la recaptación de serotonina y noradrenalina también pueden causar náuseas, que suelen ser leves y desaparecen en unas pocas semanas de tratamiento, pero tomar el medicamento con alimentos puede ayudar a aliviarlas. [50]
Modo de acción
Se pensaba que la afección para la que se indican principalmente los IRSN, el trastorno depresivo mayor, era causada principalmente por la disminución de los niveles de serotonina y noradrenalina en la hendidura sináptica, lo que causa una señalización errática. Sin embargo, esta teoría ha sido refutada. [51] Con base en la hipótesis de la monoamina de la depresión, que afirma que la disminución de las concentraciones de neurotransmisores monoamínicos conduce a síntomas depresivos, se determinaron las siguientes relaciones: "La noradrenalina puede estar relacionada con el estado de alerta y la energía, así como con la ansiedad, la atención y el interés por la vida; [la falta de] serotonina con la ansiedad, las obsesiones y las compulsiones; y la dopamina con la atención, la motivación, el placer y la recompensa, así como con el interés por la vida". [52] Los IRSN funcionan inhibiendo la recaptación de los neurotransmisores serotonina y noradrenalina. Esto da como resultado un aumento de las concentraciones extracelulares de serotonina y noradrenalina y, en consecuencia, un aumento de la neurotransmisión . La mayoría de los inhibidores de la recaptación de serotonina y noradrenalina, entre ellos la venlafaxina, la desvenlafaxina y la duloxetina, son varias veces más selectivos para la serotonina que para la noradrenalina, mientras que el milnaciprán es tres veces más selectivo para la noradrenalina que para la serotonina. Se cree que la elevación de los niveles de noradrenalina es necesaria para que un antidepresivo sea eficaz contra el dolor neuropático , una propiedad compartida con los antidepresivos tricíclicos (ATC) más antiguos, pero no con los ISRS. [53]
Estudios recientes han demostrado que la depresión puede estar relacionada con una mayor respuesta inflamatoria [54] , por lo que se han realizado intentos de encontrar un mecanismo adicional para los IRSN. Los estudios han demostrado que los IRSN, así como los ISRS, tienen una acción antiinflamatoria significativa sobre la microglía [55], además de su efecto sobre los niveles de serotonina y noradrenalina. Como tal, es posible que exista un mecanismo adicional de estos fármacos que actúe en combinación con el mecanismo previamente entendido. La implicación detrás de estos hallazgos sugiere el uso de los IRSN como posibles antiinflamatorios después de una lesión cerebral o cualquier otra enfermedad en la que la inflamación del cerebro sea un problema. Sin embargo, independientemente del mecanismo, la eficacia de estos fármacos en el tratamiento de las enfermedades para las que han sido indicados ha sido probada, tanto clínicamente como en la práctica. [ ¿ síntesis incorrecta? ]
Farmacodinamia
La mayoría de los IRSN funcionan junto con metabolitos primarios y secundarios para inhibir la recaptación de serotonina, norepinefrina y cantidades marginales de dopamina. Por ejemplo, la venlafaxina funciona junto con su metabolito primario O -desmetilvenlafaxina para inhibir fuertemente la recaptación de serotonina y norepinefrina en el cerebro. La evidencia también sugiere que la dopamina y la norepinefrina se comportan de manera cotransportativa, debido a la inactivación de la dopamina por la recaptación de norepinefrina en la corteza frontal , un área del cerebro que carece en gran medida de transportadores de dopamina. Este efecto de los IRSN da como resultado un aumento de la neurotransmisión de dopamina, además de los aumentos en la actividad de serotonina y norepinefrina. [56] Además, debido a que los IRSN son extremadamente selectivos, no tienen efectos mensurables en otros receptores no deseados, en contraste con la inhibición de la monoaminooxidasa . [57] Las pruebas farmacéuticas han determinado que el uso tanto de IRSN como de ISRS también puede generar una acción antiinflamatoria significativa sobre la microglía . [55] [16] [58] [59] [11] [60]
Perfiles de actividad
| Compuesto | Sertificacion | NETO | ~Relación ( 5-HT : NE ) | ||
|---|---|---|---|---|---|
| Yo | IC50 | Yo | IC50 | ||
| Venlafaxina | 7.8 | 145 | 1.920 | 1420 | 9.8:1 |
| Desvenlafaxina | 40.2 | 47.3 | 558.4 | 531.3 | 11.2:1 |
| Duloxetina | 0,07 | 3.7 | 1.17 | 20 | 5.4:1 |
| Atomoxetina | 87 [62] | 5.4 [62] | 0,06:1 (= 1:16) | ||
| Milnaciprán | 8.44 | 151 | 22 | 68 | 0,45:1 (= 1:2,2) |
| Levomilnacipran | 11.2 | 19.0 | 92.2 | 10.5 | 0,55:1 (= 1:1,8) |
| Todos los valores de Ki y IC 50 están expresados en nM . La relación 5 -HT / NE se basa en los valores de IC 50 para SERT y NET . [61] | |||||
Farmacocinética
La vida media de la venlafaxina es de aproximadamente 5 horas, y con una dosis diaria, la concentración en estado estacionario se alcanza después de aproximadamente 3 días, aunque su metabolito activo, la desvenlafaxina, dura más. [59] La vida media de la desvenlafaxina es de aproximadamente 11 horas, y las concentraciones en estado estacionario se alcanzan después de 4 a 5 días. [58] La vida media de la duloxetina es de aproximadamente 12 horas (rango: 8-17 horas), y el estado estacionario se alcanza después de aproximadamente 3 días. [11] El milnaciprán tiene una vida media de aproximadamente 6 a 8 horas, y los niveles en estado estacionario se alcanzan dentro de las 36 a 48 horas. [60]
Contraindicaciones
Los IRSN están contraindicados en pacientes que toman IMAO en las últimas dos semanas debido al mayor riesgo de síndrome serotoninérgico , que puede ser potencialmente mortal. [64] Otros fármacos y sustancias que deben evitarse debido al mayor riesgo de síndrome serotoninérgico cuando se combinan con un IRSN incluyen: otros antidepresivos , anticonvulsivos , analgésicos , agentes antieméticos , medicamentos contra la migraña , azul de metileno , linezolida , litio , hierba de San Juan , éxtasis y LSD . [64] Los signos y síntomas del síndrome serotoninérgico incluyen: hipertermia, rigidez, mioclono , inestabilidad autonómica con signos vitales fluctuantes y cambios en el estado mental que incluyen agitación extrema que progresa al delirio y coma. [11]
Debido a los efectos del aumento de los niveles de noradrenalina y, por lo tanto, de la mayor actividad noradrenérgica , la hipertensión preexistente debe controlarse antes del tratamiento con IRSN y la presión arterial debe controlarse periódicamente durante el tratamiento. [65] La duloxetina también se ha asociado con casos de insuficiencia hepática y no debe prescribirse a pacientes con consumo crónico de alcohol o enfermedad hepática. Los estudios han encontrado que la duloxetina puede aumentar las pruebas de función hepática tres veces por encima de su límite superior normal. [66] Los pacientes con enfermedad de la arteria coronaria deben tener precaución con el uso de IRSN. [67] Además, debido a las acciones de algunos IRSN sobre la obesidad, a los pacientes con trastornos alimentarios importantes como la anorexia nerviosa o la bulimia no se les deben prescribir IRSN. [16] La duloxetina y el milnaciprán también están contraindicados en pacientes con glaucoma de ángulo estrecho no controlado, ya que se ha demostrado que aumentan la incidencia de midriasis . [11] [60]
Efectos secundarios
Debido a que los inhibidores selectivos de la recaptación de serotonina y noradrenalina actúan de manera similar para elevar los niveles de serotonina, comparten muchos efectos secundarios, aunque en distintos grados. Los efectos secundarios más comunes incluyen náuseas/vómitos, sudoración, pérdida de apetito, mareos, dolor de cabeza, aumento de los pensamientos suicidas y disfunción sexual. [68] La elevación de los niveles de noradrenalina a veces puede causar ansiedad, pulso levemente elevado y presión arterial elevada. Sin embargo, los antidepresivos selectivos de noradrenalina, como la reboxetina y la desipramina, han tratado con éxito los trastornos de ansiedad. [69] Las personas con riesgo de hipertensión y enfermedad cardíaca deben controlar su presión arterial. [16] [58] [59] [11] [60]
Disfunción sexual
Los IRSN, de manera similar a los ISRS, pueden causar varios tipos de disfunción sexual, como disfunción eréctil, disminución de la libido, anhedonia sexual y anorgasmia . [11] [59] [70] Los dos efectos secundarios sexuales comunes son la disminución del interés en el sexo (libido) y la dificultad para alcanzar el clímax ( anorgasmia ), que suelen ser algo más leves con los IRSN en comparación con los ISRS. [71] Para controlar la disfunción sexual, los estudios han demostrado que cambiar o aumentar con bupropión o agregar un inhibidor de la PDE5 ha disminuido los síntomas de disfunción sexual. [72] Los estudios han demostrado que los inhibidores de la PDE5, como sildenafil (Viagra), tadalafil (Cialis), vardenafil (Levitra) y avanafil (Stendra), a veces han sido útiles para disminuir la disfunción sexual, incluida la disfunción eréctil, aunque se ha demostrado que son más efectivos en hombres que en mujeres. [72]
Síndrome de serotonina
Un efecto secundario grave, pero poco frecuente, de los ISRS es el síndrome serotoninérgico, que se produce por un exceso de serotonina en el organismo. El síndrome serotoninérgico puede ser causado por tomar múltiples fármacos serotoninérgicos, como los ISRS o los ISRS. Otros fármacos que contribuyen al síndrome serotoninérgico incluyen inhibidores de la MAO, linezolid, tedizolid, azul de metileno, procarbazina, anfetaminas, clomipramina y más. [73] Los primeros síntomas del síndrome serotoninérgico pueden incluir náuseas, vómitos, diarrea, sudoración, agitación, confusión, rigidez muscular, pupilas dilatadas, hipertermia, rigidez y piel de gallina. Los síntomas más graves incluyen fiebre, convulsiones, ritmo cardíaco irregular, delirio y coma. [74] [75] [11] Si aparecen signos o síntomas, suspenda inmediatamente el tratamiento con agentes serotoninérgicos. [74] Se recomienda eliminar de 4 a 5 semividas del agente serotoninérgico antes de usar un inhibidor de la MAO. [76]
Sangría
Algunos estudios sugieren que existen riesgos de sangrado gastrointestinal superior, especialmente venlafaxina, debido al deterioro de la agregación plaquetaria y al agotamiento de los niveles de serotonina plaquetaria. [77] [78] De manera similar a los ISRS, los IRSN pueden interactuar con anticoagulantes , como la warfarina . Hay más evidencia de que los ISRS tienen un mayor riesgo de sangrado que los IRSN. [77] Los estudios han sugerido precaución al usar IRSN o ISRS con dosis altas de medicamentos antiinflamatorios no esteroideos (AINE) , como ibuprofeno o naproxeno debido a un mayor riesgo de sangrado gastrointestinal superior. [34]
Problemas visuales

De manera similar a otros antidepresivos, se ha descubierto que los medicamentos IRSN causan síndrome de nieve visual , una afección caracterizada por estática visual, palinopsia (imagen residual negativa), nictalopía (visión deficiente por la noche) y fotofobia (presentación más brillante de luces o colores resaltados). La evidencia muestra que el 8,9% de los que tomaron IRSN experimentaron nieve visual, el 10,5% experimentaron palinopsia, el 15,3% experimentaron fotofobia y el 17,7% experimentaron nictolopía como resultado de la ingesta de prescripción de IRSN. También se ha informado que la amitriptilina y el citalopram empeoran o causan síntomas de VSS. [79]
Precauciones
Cómo iniciar un régimen de IRSN
Debido a los cambios extremos en la actividad noradrenérgica producidos por la inhibición de la recaptación de noradrenalina y serotonina, a los pacientes que recién comienzan un régimen con IRSN se les administran dosis más bajas que la dosis final esperada para permitir que el cuerpo se aclimate a los efectos del fármaco. A medida que el paciente continúa con dosis bajas sin efectos secundarios, la dosis se aumenta gradualmente hasta que el paciente nota una mejoría de los síntomas sin efectos secundarios perjudiciales. [80]
Síndrome de discontinuación
Al igual que con los ISRS, la interrupción abrupta de un IRSN suele provocar abstinencia o " síndrome de discontinuación ", que puede incluir estados de ansiedad y otros síntomas. Por lo tanto, se recomienda que los usuarios que deseen interrumpir un IRSN reduzcan gradualmente la dosis bajo la supervisión de un profesional. Se ha informado que el síndrome de discontinuación es notablemente peor con venlafaxina en comparación con otros IRSN. Por lo tanto, como el tramadol está relacionado con la venlafaxina, se aplican las mismas condiciones. [81] Esto probablemente se deba a la vida media relativamente corta de la venlafaxina y, por lo tanto, a su rápida eliminación tras la interrupción. En algunos casos, puede recomendarse cambiar de venlafaxina a fluoxetina, un ISRS de acción prolongada, y luego reducir gradualmente la dosis de fluoxetina, para reducir los síntomas de discontinuación. [82] [83] Los signos y síntomas de abstinencia por la interrupción abrupta de un IRSN incluyen mareos, ansiedad, insomnio, náuseas, sudoración y síntomas similares a los de la gripe, como letargo y malestar. [83]
Sobredosis
Causas
La sobredosis de inhibidores selectivos de la recaptación de serotonina y noradrenalina puede ser causada por combinaciones de fármacos o por cantidades excesivas del propio fármaco. La venlafaxina es ligeramente más tóxica en caso de sobredosis que la duloxetina o los inhibidores selectivos de la recaptación de serotonina. [16] [58] [59] [11] [60] [84]
Síntomas
Los síntomas de sobredosis de IRSN, ya sea por una interacción farmacológica mixta o por el fármaco solo, varían en intensidad e incidencia según la cantidad de medicamento ingerido y la sensibilidad de la persona al tratamiento con IRSN. Los posibles síntomas pueden incluir: [11]
- Somnolencia
- Coma
- Síndrome serotoninérgico
- Convulsiones
- Síncope
- Taquicardia
- Hipotensión
- Hipertensión
- Hipertermia
- Vómitos
Gestión
La sobredosis suele tratarse sintomáticamente, especialmente en el caso del síndrome serotoninérgico, que requiere tratamiento con ciproheptadina y control de la temperatura en función de la progresión de la toxicidad de la serotonina. [85] A menudo se controla a los pacientes para comprobar sus signos vitales y limpiar las vías respiratorias para garantizar que reciben niveles adecuados de oxígeno. Otra opción es utilizar carbón activado en el tracto gastrointestinal para absorber el exceso de neurotransmisores. [11]
Comparación con los ISRS
Debido a que los IRSN se desarrollaron más recientemente que los ISRS, hay relativamente pocos de ellos. Sin embargo, los IRSN se encuentran entre los antidepresivos más utilizados en la actualidad. En 2009, Cymbalta y Effexor fueron los medicamentos de marca 11.º y 12.º más recetados en los Estados Unidos, respectivamente. Esto se traduce en el segundo y tercer antidepresivo más común, detrás de Lexapro ( escitalopram ), un ISRS. [86] En algunos estudios, los IRSN demostraron una eficacia antidepresiva ligeramente superior a la de los ISRS (tasas de respuesta del 63,6 % frente al 59,3 %). [43] Sin embargo, en un estudio, el escitalopram tuvo un perfil de eficacia superior a la venlafaxina. [87]
Poblaciones especiales
Embarazo
La FDA no ha aprobado ningún antidepresivo durante el embarazo. [88] El uso de antidepresivos durante el embarazo puede provocar anomalías en el feto que afecten el desarrollo funcional del cerebro y el comportamiento. [88] Los estudios han demostrado correlaciones entre las mujeres embarazadas tratadas con IRSN y el riesgo de trastornos hipertensivos, [89] preeclampsia, [90] aborto espontáneo, [91] convulsiones en niños, [92] y muchos otros efectos adversos.
Pediatría
Se ha demostrado que los ISRS y los IRSN son eficaces en el tratamiento del trastorno depresivo mayor y la ansiedad en poblaciones pediátricas. [93] Sin embargo, las diferencias en el metabolismo, la función renal y el porcentaje total de agua corporal y grasa corporal pueden influir en la farmacocinética de los medicamentos en los jóvenes en comparación con los adultos. [94] Además, existe un riesgo de mayor suicidio en las poblaciones pediátricas para el tratamiento del trastorno depresivo mayor, especialmente con venlafaxina. [93] La fluoxetina y el escitalopram son los únicos antidepresivos aprobados para el trastorno depresivo mayor en niños y adolescentes. [94] Una revisión de la literatura realizada por Castagna, et. al de 2023 muestra indicios de eficacia en el tratamiento del trastorno de ansiedad generalizada pediátrico. Actualmente, la duloxetina, un IRSN, es el único medicamento aprobado por la FDA para el TAG pediátrico, a pesar de que los ISRS suelen ser el tratamiento de primera línea. [94] [95] Se sugiere que estos medicamentos se combinen con psicoterapia para maximizar la eficacia. [96] [94]
Geriatría
La mayoría de los antidepresivos, incluidos los IRSN, son seguros y eficaces en la población geriátrica. La población geriátrica tiene un mayor riesgo de sufrir efectos adversos relacionados con la interacción farmacológica, ya que es más probable que experimente polifarmacia. [97] Las decisiones a menudo se basan en condiciones comórbidas, interacciones farmacológicas y tolerancia del paciente. Debido a las diferencias en la composición corporal y el metabolismo, las dosis iniciales suelen ser la mitad de la dosis recomendada para adultos más jóvenes. [98] Los estudios muestran que estos factores también aumentan el riesgo de efectos adversos de la población geriátrica cuando se trata con IRSN pero no con ISRS. [99] [100]
Investigación
Una revisión sistemática que analizó la eficacia de los antidepresivos para aliviar el dolor concluyó que solo 11 de 42 comparaciones mostraron evidencia de eficacia. Siete de las once comparaciones pertenecen a la clase de fármacos IRSN. [101]
Véase también
- Lista de antidepresivos
- Agente liberador de serotonina (SRA)
- Inhibidor selectivo de la recaptación de serotonina (ISRS)
- Inhibidor de la recaptación de serotonina, noradrenalina y dopamina (SNDRI)
Referencias
- ^ Profesional médico de Cleveland Clinic (5 de marzo de 2023). «IRSN». Cleveland Clinic . Consultado el 9 de enero de 2024 .
- ^ abc Stahl SM, Grady MM, Moret C, Briley M (septiembre de 2005). "IRSN: su farmacología, eficacia clínica y tolerabilidad en comparación con otras clases de antidepresivos". Espectros del SNC . 10 (9): 732–747. doi :10.1017/S1092852900019726. PMID 16142213.
- ^ Cashman JR, Ghirmai S (octubre de 2009). "Inhibición de la recaptación de serotonina y noradrenalina e inhibición de la fosfodiesterasa por inhibidores multiobjetivo como agentes potenciales para la depresión". Química bioorgánica y medicinal . 17 (19): 6890–6897. doi :10.1016/j.bmc.2009.08.025. PMID 19740668.
- ^ Wright ME, Rizzolo D (marzo de 2017). "Una actualización sobre el manejo y tratamiento farmacológico del dolor neuropático". JAAPA . 30 (3): 13–17. doi :10.1097/01.JAA.0000512228.23432.f7. PMID 28151738. S2CID 205396280.
- ^ Spina E, Santoro V, D'Arrigo C (julio de 2008). "Interacciones farmacocinéticas clínicamente relevantes con antidepresivos de segunda generación: una actualización". Clinical Therapeutics . 30 (7): 1206–1227. doi :10.1016/S0149-2918(08)80047-1. PMID 18691982.
- ^ Hillhouse TM, Porter JH (febrero de 2015). "Una breve historia del desarrollo de los fármacos antidepresivos: desde las monoaminas hasta el glutamato". Experimental and Clinical Psychopharmacology . 23 (1): 1–21. doi :10.1037/a0038550. PMC 4428540 . PMID 25643025.
- ^ ab Deecher DC, Beyer CE, Johnston G, Bray J, Shah S, Abou-Gharbia M, et al. (agosto de 2006). "Succinato de desvenlafaxina: un nuevo inhibidor de la recaptación de serotonina y noradrenalina". Revista de farmacología y terapéutica experimental . 318 (2): 657–665. doi :10.1124/jpet.106.103382. PMID 16675639. S2CID 15063064.
- ^ ab Perry R, Cassagnol M (junio de 2009). "Desvenlafaxina: un nuevo inhibidor de la recaptación de serotonina y noradrenalina para el tratamiento de adultos con trastorno depresivo mayor". Clinical Therapeutics . 31 (1): 1374–1404. doi :10.1016/j.clinthera.2009.07.012. PMID 19698900.
- ^ Iyengar S, Webster AA, Hemrick-Luecke SK, Xu JY, Simmons RM (noviembre de 2004). "Eficacia de la duloxetina, un inhibidor potente y equilibrado de la recaptación de serotonina y noradrenalina en modelos de dolor persistente en ratas". The Journal of Pharmacology and Experimental Therapeutics . 311 (2): 576–584. doi :10.1124/jpet.104.070656. PMID 15254142. S2CID 18022449.
- ^ abcd Hunziker ME, Suehs BT, Bettinger TL, Crismon ML (agosto de 2005). "Clorhidrato de duloxetina: un nuevo medicamento de doble acción para el tratamiento del trastorno depresivo mayor". Terapéutica clínica . 27 (8): 1126–1143. doi :10.1016/j.clinthera.2005.08.010. PMID 16199241.
- ^ abcdefghijkl "Cápsula de clorhidrato de duloxetina Cymbalta, liberación retardada". DailyMed . 20 de septiembre de 2021 . Consultado el 12 de febrero de 2023 .
- ^ "Yentreve (clorhidrato de duloxetina) cápsulas gastrorresistentes duras. Resumen de las características del producto" (PDF) . Agencia Europea de Medicamentos. Archivado desde el original (PDF) el 26 de junio de 2016 . Consultado el 29 de agosto de 2016 .
- ^ "Comprimido de clorhidrato de nefazodona". DailyMed . 16 de noviembre de 2021 . Consultado el 12 de febrero de 2023 .
- ^ ab Frampton JE, Plosker GL (2007). "Duloxetina: una revisión de su uso en el tratamiento del trastorno depresivo mayor". Fármacos para el sistema nervioso central . 21 (7): 581–609. doi :10.2165/00023210-200721070-00004. PMID 17579500. S2CID 22242897.
- ^ ab Morishita S, Arita S (febrero de 2003). "El uso clínico de milnacipran para la depresión". Psiquiatría europea . 18 (1): 34–35. doi :10.1016/S0924-9338(02)00003-2. PMID 12648895. S2CID 5978467.
- ^ abcde "Meridia (clorhidrato de sibutramina monohidrato) Cápsulas C-IV. Información completa de prescripción (etiqueta archivada)". Abbott Laboratories, North Chicago, IL 60064, EE. UU . Consultado el 2 de septiembre de 2016 .
- ^ Luque CA, Rey JA (abril de 2002). "El descubrimiento y el estado de la sibutramina como fármaco antiobesidad". Revista Europea de Farmacología . 440 (2–3): 119–128. doi :10.1016/S0014-2999(02)01423-1. PMID 12007530.
- ^ Rockoff JD, Dooren JC (8 de octubre de 2010). "Abbott retira de los estantes de Estados Unidos el fármaco dietético Meridia". The Wall Street Journal . Archivado desde el original el 11 de octubre de 2010. Consultado el 8 de octubre de 2010 .
- ^ Keating GM (2006). "Cápsulas de liberación sostenida de tramadol". Drugs . 66 (2): 223–230. doi :10.2165/00003495-200666020-00006. PMID 16451094. S2CID 22620947.
- ^ ab Gutiérrez MA, Stimmel GL, Aiso JY (agosto de 2003). "Venlafaxina: una actualización de 2003". Terapéutica Clínica . 25 (8): 2138–2154. doi :10.1016/s0149-2918(03)80210-2. PMID 14512125.
- ^ ab Joffe H, Guthrie KA, LaCroix AZ, Reed SD, Ensrud KE, Manson JE, et al. (julio de 2014). "Estradiol en dosis bajas y el inhibidor de la recaptación de serotonina y noradrenalina venlafaxina para los síntomas vasomotores: un ensayo clínico aleatorizado". JAMA Internal Medicine . 174 (7): 1058–1066. doi :10.1001/jamainternmed.2014.1891. PMC 4179877 . PMID 24861828.
- ^ Redrobe JP, Bourin M, Colombel MC, Baker GB (julio de 1998). "Propiedades noradrenérgicas y serotoninérgicas dependientes de la dosis de venlafaxina en modelos animales indicativas de actividad antidepresiva". Psicofarmacología . 138 (1): 1–8. doi :10.1007/s002130050638. PMID 9694520. S2CID 35064471.
- ^ ab Lieberman JA (2003). "Historia del uso de antidepresivos en atención primaria" (PDF) . Primary Care Companion J Clin Psychiatry . 5 (S7): 6–10. Archivado desde el original (PDF) el 2014-06-11 . Consultado el 2014-03-05 .
- ^ Ruelas EG, Diaz-Martinez A, Ruiz RM, Estudio TV, Grupo C (1997). "Una evaluación abierta de la aceptabilidad, eficacia y tolerancia de la venlafaxina en entornos de atención habitual". Investigación terapéutica actual . 58 (9): 609–630. doi :10.1016/S0011-393X(97)80088-4.
- ^ abc Grandoso L, Pineda J, Ugedo L (mayo de 2004). "Estudio comparativo de los efectos de la desipramina y la reboxetina sobre las neuronas del locus coeruleus en cortes cerebrales de rata". Neurofarmacología . 46 (6): 815–823. doi :10.1016/j.neuropharm.2003.11.033. PMID 15033341. S2CID 13228862.
- ^ Pacher P, Kecskemeti V (2004). "Efectos secundarios cardiovasculares de los nuevos antidepresivos y antipsicóticos: ¿nuevos fármacos, viejas preocupaciones?". Current Pharmaceutical Design . 10 (20): 2463–2475. doi :10.2174/1381612043383872. PMC 2493295 . PMID 15320756.
- ^ ab Brunello N, Mendlewicz J, Kasper S, Leonard B, Montgomery S, Nelson J, et al. (octubre de 2002). "El papel de la noradrenalina y la inhibición selectiva de la recaptación de noradrenalina en la depresión". Neuropsicofarmacología europea . 12 (5): 461–475. doi :10.1016/s0924-977x(02)00057-3. PMID 12208564. S2CID 7989883.
- ^ abc Lemke TL, Williams DA, Roche VF, Zito SW (2008). Principios de química medicinal de Foye (6.ª ed.). EE. UU.: Lippincott Williams & Wilkins. págs. 547–67, 581–582.
- ^ abcde Brunton LL, Lazo JS, Parker KL, eds. (2006). Goodman & Gilman's: The Pharmacological Basis of Therapeutics (11.ª ed.). Nueva York: McGraw-Hill.
- ^ Silverthorn DU, ed. (2007). Fisiología humana (4.ª ed.). San Francisco: Pearson. págs. 383–384.
- ^ Nutt DJ, Forshall S, Bell C, Rich A, Sandford J, Nash J, et al. (julio de 1999). "Mecanismos de acción de los inhibidores selectivos de la recaptación de serotonina en el tratamiento de trastornos psiquiátricos". Neuropsicofarmacología europea . 9 (Supl. 3): S81–S86. doi :10.1016/S0924-977X(99)00030-9. PMID 10523062. S2CID 23634771.
- ^ Santarsieri D, Schwartz TL (2015). "Eficacia de los antidepresivos y carga de efectos secundarios: una guía rápida para médicos". Drugs in Context . 4 : 212290. doi :10.7573/dic.212290. PMC 4630974 . PMID 26576188.
- ^ Clevenger SS, Malhotra D, Dang J, Vanle B, IsHak WW (enero de 2018). "El papel de los inhibidores selectivos de la recaptación de serotonina en la prevención de la recaída del trastorno depresivo mayor". Avances terapéuticos en psicofarmacología . 8 (1): 49–58. doi :10.1177/2045125317737264. PMC 5761909 . PMID 29344343.
- ^ ab Zeind C, Carvalho MG (2018). Terapéutica aplicada: el uso clínico de los fármacos, 11.ª edición . Wolters Kluwer. pp. 1813–1833. ISBN 9781496318299.
- ^ abcd Boot J, Cases M, Clark BP, Findlay J, Gallagher PT, Hayhurst L, et al. (febrero de 2005). "Descubrimiento y relaciones estructura-actividad de nuevos inhibidores selectivos de la recaptación de noradrenalina y de serotonina/noradrenalina duales". Bioorganic & Medicinal Chemistry Letters . 15 (3): 699–703. doi :10.1016/j.bmcl.2004.11.025. PMID 15664840.
- ^ abc Mahaney PE, Vu AT, McComas CC, Zhang P, Nogle LM, Watts WL, et al. (diciembre de 2006). "Síntesis y actividad de una nueva clase de inhibidores de la recaptación de serotonina y noradrenalina de doble acción: 3-(1H-indol-1-il)-3-arilpropan-1-aminas". Química bioorgánica y medicinal . 14 (24): 8455–8466. doi :10.1016/j.bmc.2006.08.039. PMID 16973367.
- ^ Mahaney PE, Gavrin LK, Trybulski EJ, Stack GP, Vu TA, Cohn ST, et al. (julio de 2008). "Relaciones estructura-actividad del andamiaje de cicloalcanol etilamina: descubrimiento de inhibidores selectivos de la recaptación de noradrenalina". Journal of Medicinal Chemistry . 51 (13): 4038–4049. doi :10.1021/jm8002262. PMID 18557608.
- ^ abc Chen C, Dyck B, Fleck BA, Foster AC, Grey J, Jovic F, et al. (febrero de 2008). "Estudios sobre la SAR y el farmacóforo de los derivados de milnacipran como inhibidores del transportador de monoamina". Bioorganic & Medicinal Chemistry Letters . 18 (4): 1346–1349. doi :10.1016/j.bmcl.2008.01.011. PMID 18207394.
- ^ abc Tamiya J, Dyck B, Zhang M, Phan K, Fleck BA, Aparicio A, et al. (junio de 2008). "Identificación de análogos de 1S,2R-milnacipran como potentes inhibidores del transportador de noradrenalina y serotonina". Bioorganic & Medicinal Chemistry Letters . 18 (11): 3328–3332. doi :10.1016/j.bmcl.2008.04.025. PMID 18445525.
- ^ Vu AT, Cohn ST, Terefenko EA, Moore WJ, Zhang P, Mahaney PE, et al. (mayo de 2009). "3-(Arylamino)-3-fenilpropan-2-olaminas como una nueva serie de inhibidores duales de la recaptación de serotonina y noradrenalina". Bioorganic & Medicinal Chemistry Letters . 19 (9): 2464–2467. doi :10.1016/j.bmcl.2009.03.054. PMID 19329313.
- ^ Boot JR, Brace G, Delatour CL, Dezutter N, Fairhurst J, Findlay J, et al. (noviembre de 2004). "Benzotieniloxifenilpropanaminas, nuevos inhibidores duales de la recaptación de serotonina y noradrenalina". Bioorganic & Medicinal Chemistry Letters . 14 (21): 5395–5399. doi :10.1016/j.bmcl.2004.08.005. PMID 15454233.
- ^ Fish PV, Deur C, Gan X, Greene K, Hoople D, Mackenny M, et al. (abril de 2008). "Diseño y síntesis de derivados de morfolina. SAR para inhibición dual de la recaptación de serotonina y noradrenalina". Bioorganic & Medicinal Chemistry Letters . 18 (8): 2562–2566. doi :10.1016/j.bmcl.2008.03.050. PMID 18387300.
- ^ ab Papakostas GI, Thase ME, Fava M, Nelson JC, Shelton RC (diciembre de 2007). "¿Son los fármacos antidepresivos que combinan mecanismos de acción serotoninérgicos y noradrenérgicos más eficaces que los inhibidores selectivos de la recaptación de serotonina en el tratamiento del trastorno depresivo mayor? Un metaanálisis de estudios de agentes más nuevos". Biological Psychiatry . 62 (11): 1217–1227. doi :10.1016/j.biopsych.2007.03.027. PMID 17588546. S2CID 45621773.
- ^ Nemeroff CB, Thase ME (2007). "Una comparación doble ciego, controlada con placebo del tratamiento con venlafaxina y fluoxetina en pacientes ambulatorios deprimidos". Journal of Psychiatric Research . 41 (3–4): 351–359. doi :10.1016/j.jpsychires.2005.07.009. PMID 16165158.
- ^ Marks DM, Shah MJ, Patkar AA, Masand PS, Park GY, Pae CU (diciembre de 2009). "Inhibidores de la recaptación de serotonina y noradrenalina para el control del dolor: premisa y promesa". Neurofarmacología actual . 7 (4): 331–336. doi :10.2174/157015909790031201. PMC 2811866 . PMID 20514212.
- ^ Beesdo K, Hartford J, Russell J, Spann M, Ball S, Wittchen HU (diciembre de 2009). "El efecto a corto y largo plazo de la duloxetina sobre los síntomas físicos dolorosos en pacientes con trastorno de ansiedad generalizada: resultados de tres ensayos clínicos". Journal of Anxiety Disorders . 23 (8): 1064–1071. doi :10.1016/j.janxdis.2009.07.008. PMID 19643572.
- ^ Sansone RA, Sansone LA (junio de 2011). "¿Alternativas farmacológicas de los IRSN para el tratamiento del trastorno obsesivo compulsivo?". Innovaciones en neurociencia clínica . 8 (6): 10–14. PMC 3140892. PMID 21779536 .
- ^ Troy SM, Parker VP, Hicks DR, Pollack GM, Chiang ST (octubre de 1997). "Farmacocinética y efecto de los alimentos sobre la biodisponibilidad de la venlafaxina administrada por vía oral". Journal of Clinical Pharmacology . 37 (10): 954–961. doi :10.1002/j.1552-4604.1997.tb04270.x. PMID 9505987. S2CID 33518952.
- ^ Wichniak A, Wierzbicka A, Walęcka M, Jernajczyk W (agosto de 2017). "Efectos de los antidepresivos sobre el sueño". Informes de psiquiatría actuales . 19 (9): 63. doi :10.1007/s11920-017-0816-4. PMC 5548844 . PMID 28791566.
- ^ "Útil para el dolor crónico además de la depresión". Mayo Clinic . Consultado el 24 de octubre de 2019 .
- ^ Moncrieff J, Cooper RE, Stockmann T, Amendola S, Hengartner MP, Horowitz MA (agosto de 2023). "La teoría de la serotonina de la depresión: una revisión sistemática general de la evidencia". Psiquiatría molecular . 28 (8): 3243–3256. doi : 10.1038/s41380-022-01661-0 . PMC 10618090 . PMID 35854107. S2CID 250646781.
- ^ Nutt DJ (2008). "Relación de los neurotransmisores con los síntomas del trastorno depresivo mayor". The Journal of Clinical Psychiatry . 69 : 4–7. PMID 18494537.
- ^ Sindrup SH, Otto M, Finnerup NB, Jensen TS (junio de 2005). "Antidepresivos en el tratamiento del dolor neuropático". Farmacología básica y clínica y toxicología . 96 (6): 399–409. doi : 10.1111/j.1742-7843.2005.pto_96696601.x . PMID 15910402.
- ^ Shelton RC, Miller AH (2011). "Inflamación en la depresión: ¿es la adiposidad una causa?". Diálogos en neurociencia clínica . 13 (1): 41–53. doi :10.31887/DCNS.2011.13.1/rshelton. PMC 3181969. PMID 21485745 .
- ^ ab Tynan RJ, Weidenhofer J, Hinwood M, Cairns MJ, Day TA, Walker FR (marzo de 2012). "Un examen comparativo de los efectos antiinflamatorios de los antidepresivos ISRS y IRSN en la microglia estimulada por LPS". Cerebro, comportamiento e inmunidad . 26 (3): 469–479. doi :10.1016/j.bbi.2011.12.011. PMID 22251606. S2CID 39281923.
- ^ "Cambridge University Press - Anuncio de servicio".
- ^ Lambert O, Bourin M (noviembre de 2002). "IRSN: mecanismo de acción y características clínicas". Expert Review of Neurotherapeutics . 2 (6): 849–858. doi :10.1586/14737175.2.6.849. PMID 19810918. S2CID 37792842.
- ^ abcd "Pristiq Extended-Release- comprimido de succinato de desvenlafaxina, liberación prolongada". DailyMed . 25 de marzo de 2022 . Consultado el 12 de febrero de 2023 .
- ^ abcde «Effexor XR: cápsula de clorhidrato de venlafaxina de liberación prolongada». DailyMed . 29 de agosto de 2022 . Consultado el 12 de febrero de 2023 .
- ^ abcde "Comprimido recubierto con película de Savella-clorhidrato de milnaciprán Kit de Savella-clorhidrato de milnaciprán". DailyMed . 23 de diciembre de 2022 . Consultado el 12 de febrero de 2023 .
- ^ ab Raouf M, Glogowski AJ, Bettinger JJ, Fudin J (agosto de 2017). "Inhibidores de la recaptación de serotonina-norepinefrina y la influencia de la afinidad de unión (Ki) en la analgesia". Revista de farmacia clínica y terapéutica . 42 (4): 513–517. doi : 10.1111/jcpt.12534 . PMID 28503727.
- ^ abc Upadhyaya HP, Desaiah D, Schuh KJ, Bymaster FP, Kallman MJ, Clarke DO, et al. (marzo de 2013). "Una revisión de la evaluación del potencial de abuso de atomoxetina: un medicamento no estimulante para el trastorno por déficit de atención e hiperactividad". Psicofarmacología . 226 (2). Springer Nature: 189–200. doi :10.1007/s00213-013-2986-z. PMC 3579642 . PMID 23397050.
- ^ Roth BL , Driscol J (diciembre de 2012). "PDSP Ki Database". Programa de detección de drogas psicoactivas (PDSP) . Universidad de Carolina del Norte en Chapel Hill y el Instituto Nacional de Salud Mental de los Estados Unidos . Consultado el 7 de julio de 2018 .
- ^ ab Boyer EW, Shannon M (marzo de 2005). "El síndrome de la serotonina". The New England Journal of Medicine . 352 (11): 1112–1120. doi :10.1056/NEJMra041867. PMID 15784664. S2CID 37959124.
- ^ Zhong Z, Wang L, Wen X, Liu Y, Fan Y, Liu Z (noviembre de 2017). "Un metaanálisis de los efectos de los inhibidores selectivos de la recaptación de serotonina sobre la presión arterial en el tratamiento de la depresión: resultados de ensayos controlados con placebo e inhibidores de la recaptación de serotonina y noradrenalina". Enfermedades neuropsiquiátricas y tratamiento . 13 : 2781–2796. doi : 10.2147/NDT.S141832 . PMC 5683798. PMID 29158677 .
- ^ McIntyre RS et al. El perfil de seguridad hepática de la duloxetina: una revisión. Expert Opin Drug Metab Toxicol . 2008;4(3):281–285.
- ^ Mladěnka P, Applová L, Patočka J, Costa VM, Remiao F, Pourová J, et al. (julio de 2018). "Revisión exhaustiva de la toxicidad cardiovascular de fármacos y agentes relacionados". Medicinal Research Reviews . 38 (4): 1332–1403. doi :10.1002/med.21476. PMC 6033155 . PMID 29315692.
- ^ "Antidepresivos IRSN". poison.org . Consultado el 21 de octubre de 2019 .
- ^ Versiani M, Cassano G, Perugi G, Benedetti A, Mastalli L, Nardi A, et al. (enero de 2002). "Reboxetina, un inhibidor selectivo de la recaptación de noradrenalina, es un tratamiento eficaz y bien tolerado para el trastorno de pánico". The Journal of Clinical Psychiatry . 63 (1): 31–37. doi :10.4088/jcp.v63n0107. PMID 11838623.
- ^ Olivier JD, Olivier B (1 de septiembre de 2019). "Antidepresivos y disfunciones sexuales: una perspectiva traslacional". Current Sexual Health Reports . 11 (3): 156–166. doi : 10.1007/s11930-019-00205-y .
- ^ Clayton AH, Montejo AL (2006). "Trastorno depresivo mayor, antidepresivos y disfunción sexual". The Journal of Clinical Psychiatry . 67 (Supl. 6): 33–37. PMID 16848675.
- ^ ab Jing E, Straw-Wilson K (julio de 2016). "Disfunción sexual en los inhibidores selectivos de la recaptación de serotonina (ISRS) y posibles soluciones: una revisión narrativa de la literatura". The Mental Health Clinician . 6 (4): 191–196. doi :10.9740/mhc.2016.07.191. PMC 6007725 . PMID 29955469.
- ^ "Síndrome serotoninérgico: prevención, reconocimiento y tratamiento". www.mdedge.com . Consultado el 21 de noviembre de 2019 .
- ^ ab Frank C (julio de 2008). "Reconocimiento y tratamiento del síndrome serotoninérgico". Canadian Family Physician . 54 (7): 988–992. PMC 2464814 . PMID 18625822.
- ^ "Antidepresivos IRSN". poison.org . Consultado el 23 de octubre de 2019 .
- ^ Tint A, Haddad PM, Anderson IM (mayo de 2008). "El efecto de la tasa de reducción gradual de la dosis de antidepresivos en la incidencia de síntomas de interrupción: un estudio aleatorizado". Journal of Psychopharmacology . 22 (3): 330–332. doi :10.1177/0269881107081550. PMID 18515448. S2CID 145217439.
- ^ ab Cochran KA, Cavallari LH, Shapiro NL, Bishop JR (agosto de 2011). "Incidencia de sangrado con el uso concomitante de antidepresivos y warfarina". Monitoreo terapéutico de fármacos . 33 (4): 433–438. doi :10.1097/FTD.0b013e318224996e. PMC 3212440. PMID 21743381 .
- ^ Cheng YL, Hu HY, Lin XH, Luo JC, Peng YL, Hou MC, et al. (noviembre de 2015). "El uso de ISRS, pero no de IRSN, aumentó el sangrado gastrointestinal superior e inferior: un estudio de cohorte poblacional a nivel nacional en Taiwán". Medicina . 94 (46): e2022. doi :10.1097/MD.0000000000002022. PMC 4652818 . PMID 26579809.
- ^ Curr Neurol, Neurosci Rep. (2022). "Nieve visual: actualizaciones en patología". Informes actuales de neurología y neurociencia . 22 (3). Institutos Nacionales de Salud: 209–217. doi :10.1007/s11910-022-01182-x. PMC 8889058. PMID 35235167 .
- ^ "Duloxetina: información sobre el medicamento". UpToDate . Consultado el 28 de junio de 2012 .
- ^ Perahia DG, Pritchett YL, Kajdasz DK, Bauer M, Jain R, Russell JM, et al. (enero de 2008). "Una comparación aleatorizada y doble ciego de duloxetina y venlafaxina en el tratamiento de pacientes con trastorno depresivo mayor". Journal of Psychiatric Research . 42 (1): 22–34. doi :10.1016/j.jpsychires.2007.01.008. PMID 17445831.
- ^ Wilson E, Lader M (diciembre de 2015). "Una revisión del manejo de los síntomas de discontinuación de antidepresivos". Avances terapéuticos en psicofarmacología . 5 (6): 357–368. doi :10.1177/2045125315612334. PMC 4722507 . PMID 26834969.
- ^ ab Fava GA, Benasi G, Lucente M, Offidani E, Cosci F, Guidi J (2018). "Síntomas de abstinencia tras la interrupción del inhibidor de la recaptación de serotonina y noradrenalina: revisión sistemática" (PDF) . Psicoterapia y psicosomática . 87 (4): 195–203. doi : 10.1159/000491524 . PMID 30016772.
- ^ Taylor D, Lenox-Smith A, Bradley A (junio de 2013). "Una revisión de la idoneidad de la duloxetina y la venlafaxina para su uso en pacientes con depresión en atención primaria, con especial atención a la seguridad cardiovascular, el suicidio y la mortalidad por sobredosis de antidepresivos". Avances terapéuticos en psicofarmacología . 3 (3): 151–161. doi :10.1177/2045125312472890. PMC 3805457 . PMID 24167687.
- ^ Simon LV, Hashmi MF, Keenaghan M (2019). "Síndrome serotoninérgico". EstadísticasPerlas . Publicación de StatPearls. PMID 29493999 . Consultado el 21 de noviembre de 2019 .
- ^ "Los 200 principales medicamentos de marca de 2009 por prescripciones totales" (PDF) . SDI/Verispan, VONA, año completo 2009 . www.drugtopics.com. Archivado desde el original (PDF) el 14 de julio de 2011 . Consultado el 6 de abril de 2011 .
- ^ Llorca PM, Fernandez JL (abril de 2007). "Escitalopram en el tratamiento del trastorno depresivo mayor: eficacia clínica, tolerabilidad y coste-efectividad frente a la formulación de liberación prolongada de venlafaxina". Revista Internacional de Práctica Clínica . 61 (4): 702–710. doi : 10.1111/j.1742-1241.2007.01335.x . PMID 17394446.
- ^ ab Dubovicky M, Belovicova K, Csatlosova K, Bogi E (septiembre de 2017). "Riesgos del uso de antidepresivos ISRS/IRSN durante el embarazo y la lactancia". Toxicología interdisciplinaria . 10 (1): 30–34. doi :10.1515/intox-2017-0004. PMC 6096863 . PMID 30123033.
- ^ Benevent J, Araujo M, Karki S, Delarue-Hurault C, Waser J, Lacroix I, et al. (julio de 2023). "Riesgo de trastornos hipertensivos del embarazo en mujeres tratadas con inhibidores de la recaptación de serotonina y noradrenalina: un estudio comparativo utilizando la base de datos EFEMERIS". The Journal of Clinical Psychiatry . 84 (4): 47872. doi :10.4088/JCP.22m14734. PMID 37437238.
- ^ Tran YH, Huynh HK, Faas MM, de Vos S, Groen H (febrero de 2022). "Uso de antidepresivos durante el embarazo y desarrollo de la preeclampsia: un enfoque en las clases de acción y los transportadores/receptores específicos a los que se dirigen los antidepresivos". Revista de investigación psiquiátrica . 146 : 92–101. doi :10.1016/j.jpsychires.2021.12.038. PMID 34959164.
- ^ Smith S, Martin F, Rai D, Forbes H (enero de 2024). "Asociación entre el uso de antidepresivos durante el embarazo y el aborto espontáneo: una revisión sistemática y un metanálisis". BMJ Open . 14 (1): e074600. doi :10.1136/bmjopen-2023-074600. PMC 10824002 . PMID 38272551.
- ^ Wiggs KK, Sujan AC, Rickert ME, Quinn PD, Larsson H, Lichtenstein P, et al. (junio de 2022). "Uso materno de antidepresivos serotoninérgicos durante el embarazo y riesgo de convulsiones en niños". Neurología . 98 (23): e2329–e2336. doi :10.1212/WNL.0000000000200516. PMC 9202527 . PMID 35545445.
- ^ ab Strawn JR, Mills JA, Sauley BA, Welge JA (abril de 2018). "El impacto de la dosis y la clase de antidepresivos en la respuesta al tratamiento en los trastornos de ansiedad pediátricos: un metaanálisis". Revista de la Academia Estadounidense de Psiquiatría Infantil y Adolescente . 57 (4): 235–244.e2. doi :10.1016/j.jaac.2018.01.015. PMC 5877120. PMID 29588049 .
- ^ abcd Strawn JR, Vaughn S, Ramsey LB (abril de 2022). "Psicofarmacología pediátrica para trastornos depresivos y de ansiedad". Focus . 20 (2): 184–190. doi :10.1176/appi.focus.20210036. PMC 10153505 . PMID 37153132.
- ^ Strawn JR, Prakash A, Zhang Q, Pangallo BA, Stroud CE, Cai N, et al. (abril de 2015). "Un estudio aleatorizado y controlado con placebo de duloxetina para el tratamiento de niños y adolescentes con trastorno de ansiedad generalizada". Revista de la Academia Estadounidense de Psiquiatría Infantil y Adolescente . 54 (4): 283–293. doi :10.1016/j.jaac.2015.01.008. PMID 25791145.
- ^ Castagna PJ, Farahdel E, Potenza MN, Crowley MJ (mayo de 2023). "El estado actual de la técnica en farmacoterapia para el trastorno de ansiedad generalizada pediátrica". Opinión de expertos sobre farmacoterapia . 24 (7): 835–847. doi :10.1080/14656566.2023.2199921. PMC 10197951. PMID 37074259 .
- ^ Brender R, Mulsant BH, Blumberger DM (octubre de 2021). "Actualización de la farmacoterapia antidepresiva en la depresión en la vejez". Opinión de expertos sobre farmacoterapia . 22 (14): 1909–1917. doi :10.1080/14656566.2021.1921736. PMID 33910422.
- ^ Mulsant BH, Blumberger DM, Ismail Z, Rabheru K, Rapoport MJ (agosto de 2014). "Un enfoque sistemático de la farmacoterapia para la depresión mayor geriátrica". Clinics in Geriatric Medicine . 30 (3): 517–534. doi :10.1016/j.cger.2014.05.002. PMC 4122285 . PMID 25037293.
- ^ Simon G (octubre de 2019). "Revisión: en adultos mayores con depresión mayor aguda, los IRSN, pero no los ISRS, aumentan los eventos adversos en comparación con el placebo". Annals of Internal Medicine . 171 (8): JC39. doi :10.7326/acpj201910150-039. PMID 31610552.
- ^ "Más eventos adversos con los IRSN que con placebo en pacientes mayores". Actualización en psicofarmacología de la Universidad de Brown . 30 (10): 7–8. Octubre de 2019. doi :10.1002/pu.30488. ISSN 1068-5308.
- ^ Ferreira GE, Abdel-Shaheed C, Underwood M, Finnerup NB, Day RO, McLachlan A, et al. (febrero de 2023). "Eficacia, seguridad y tolerabilidad de los antidepresivos para el dolor en adultos: descripción general de las revisiones sistemáticas". BMJ . 380 : e072415. doi :10.1136/bmj-2022-072415. PMC 9887507 . PMID 36725015.
