Promegstone
 | |
| Datos clínicos | |
|---|---|
| Nombres comerciales | Piedra de surgencia |
| Otros nombres | PMG; R-5020; RU-5020; 17α,21-Dimetil-δ 9 -19-norprogesterona; 17α,21-Dimetil-19-norpregna-4,9-dieno-3,20-diona |
| Vías de administración | Por la boca [1] |
| Clase de droga | Progestágeno ; Progestina |
| Código ATC |
|
| Datos farmacocinéticos | |
| Unión de proteínas | A la albúmina [1] |
| Metabolismo | Hígado ( hidroxilación ) [1] [3] |
| Metabolitos | • Trimegestona |
| Vida media de eliminación | Promegestona: ? Trimegesta: 13,8–15,6 horas [1] [2] |
| Identificadores | |
| |
| Número CAS |
|
| Identificador de centro de PubChem |
|
| Araña química |
|
| UNIVERSIDAD |
|
| BARRIL |
|
| EBICh |
|
| Química biológica |
|
| Panel de control CompTox ( EPA ) |
|
| Tarjeta informativa de la ECHA | 100.207.681 |
| Datos químicos y físicos | |
| Fórmula | C22H30O2 |
| Masa molar | 326,480 g·mol −1 |
| Modelo 3D ( JSmol ) |
|
| |
| |
Promegestone , vendido bajo la marca Surgestone , es un medicamento progestágeno que se utiliza en la terapia hormonal menopáusica y en el tratamiento de trastornos ginecológicos . [4] [1] [5] [6] Se toma por vía oral . [1]
Los efectos secundarios de la promegestona incluyen irregularidades menstruales , entre otros. [7] La promegestona es una progestina, o un progestágeno sintético , y por lo tanto es un agonista del receptor de progesterona , el objetivo biológico de los progestágenos como la progesterona . [1] Tiene una actividad antiandrogénica , glucocorticoide y antimineralocorticoide débil y ninguna otra actividad hormonal importante. [1] [8] [2] El medicamento es en gran medida un profármaco de la trimegestona . [7] [1]
La promegestona se describió por primera vez en 1973 y se introdujo para uso médico en Francia en 1983. [9] [10] [11] Solo se ha comercializado en unos pocos países, incluidos Francia, Portugal , Túnez y Argentina . [6] [12] Además de su uso como medicamento, la promegestona se ha utilizado ampliamente en la investigación científica como radioligando del receptor de progesterona. [4] [13]
Usos médicos
La promegestona se utiliza en la terapia hormonal menopáusica y en el tratamiento de afecciones ginecológicas causadas por insuficiencia lútea , incluidos los trastornos premenopáusicos , la dismenorrea y otros trastornos menstruales , y el síndrome premenstrual . [1] [5] También se ha utilizado para tratar trastornos benignos de las mamas, como la mastalgia (dolor de mamas). [14] Los comprimidos de promegestona tienen un efecto anticonceptivo y se utilizan como una forma de control de la natalidad a base de progestágeno solo , aunque no está específicamente autorizado como tal. [15]
Efectos secundarios
Los efectos secundarios de la promegestona incluyen irregularidades menstruales , entre otros. [7] No tiene efectos secundarios androgénicos . [4] [5]
Farmacología
Farmacodinamia

La promegestona es un progestágeno o un agonista del receptor de progesterona . [1] [3] Tiene alrededor del 200% de la afinidad de la progesterona por el PR. [1] [3] La dosis de transformación endometrial de promegestona es de 10 mg por ciclo y su dosis inhibidora de la ovulación es de 0,5 mg/día. [1] [3] La promegestona tiene una actividad glucocorticoide débil además de su actividad progestágena. [1] [3] Por el contrario, no tiene actividad androgénica , estrogénica , mineralocorticoide u otra actividad hormonal . [1] [3] [5] Parece poseer actividad antiandrogénica . [13] Su principal metabolito, la trimegestona, tiene una actividad antimineralocorticoide y antiandrogénica débil . [8] [2] Además, se ha descubierto que la promegestona posee cierta actividad neurosteroide al actuar como un antagonista no competitivo del receptor nicotínico de acetilcolina , de manera similar a la progesterona. [16]
Farmacocinética
Después de la administración oral , los niveles séricos máximos de promegestona se alcanzan después de 1 a 2 horas. [1] [3] El medicamento se une principalmente a la albúmina ; no se une a la globulina transportadora de hormonas sexuales y se une solo débilmente a la globulina transportadora de corticosteroides . [1] [3] [17] El metabolismo de la promegestona es principalmente a través de la hidroxilación en la posición C21 y en otras posiciones. [1] [3] La progesterona se hidroxila de manera similar en la posición C21, en 11-desoxicorticosterona (21-hidroxiprogesterona). [18] Sin embargo, el doble enlace C9(10) de la promegestona limita en gran medida la reducción del anillo A que sufre la progesterona, lo que da como resultado que la 21-hidroxilación sea la principal vía metabólica de la promegestona. [18] El medicamento se metaboliza estereoselectivamente en trimegestona , el metabolito 21( S )-hidroxi , que es el compuesto principal que se encuentra en el plasma ; circula en niveles aproximadamente el doble de los de la propia promegestona. [7] Además, la trimegestona tiene una afinidad más de tres veces mayor por el PR que la promegestona. [1] Como tal, la promegestona es en gran medida un profármaco de la trimegestona. [7] [19] Un segundo metabolito, la 21( R )-hidroxipromegestona, circula en concentraciones mucho más bajas ( AUCNiveles del área bajo la curva de información sobre herramientasrelación para los isómeros ( S )- y ( R )- de aproximadamente 21). [7] La vida media de eliminación de la trimegestona es de 13,8 a 15,6 horas. [1] [2] La promegestona, la trimegestona y la 21( R )-hidroxipromegestona no se excretan en la orina , mientras que el 3% de una dosis se recupera como el conjugado glucurónido y/o sulfato de la trimegestona y el 1% de una dosis se recupera como el conjugado glucurónido y/o sulfato de la 21( R )-hidroxipromegestona. [7]
Química
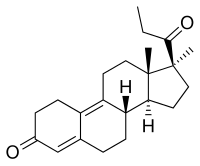
La promegestona, también conocida como 17α,21-dimetil-δ 9 -19-norprogesterona o como 17α,21-dimetil-19-norpregna-4,9-dieno-3,20-diona, es un esteroide norpregnano sintético y un derivado de la progesterona . [9] [12] [11] [1] Es específicamente un derivado combinado de 17α-metilprogesterona y 19-norprogesterona , o de 17α-metil-19-norprogesterona . [9] [11] [1] Los derivados relacionados de 17α-metil-19-norprogesterona incluyen demegestona y trimegestona . [9] [12] [1]
Historia
La promegestona se describió por primera vez en la literatura en 1973 y se introdujo para uso médico en Francia en 1983. [9] [10] [11] [5] Fue desarrollada por Roussel Uclaf en Francia. [5]
Sociedad y cultura
Nombres genéricos
Promegestona es el nombre genérico del medicamento y su DCITooltip Nombre común internacional, mientras que promégestone es su DCFInformación sobre herramientas Denominación Comuna Francesa. [6] [9] [12] También se le conoce por su nombre de código de desarrollo R-5020 o RU-5020 . [6] [9] [12]
Nombres de marca
Promegestone se comercializa exclusivamente bajo la marca Surgestone. [6] [12]
Disponibilidad
La promegestona se comercializa o se ha comercializado en Francia , Portugal , Túnez y Argentina . [6] [12]
Referencias
- ^ abcdefghijklmnopqrstu vw Kuhl H (agosto de 2005). "Farmacología de los estrógenos y progestágenos: influencia de diferentes vías de administración" (PDF) . Climaterio . 8 (Supl. 1): 3–63. doi :10.1080/13697130500148875. PMID 16112947. S2CID 24616324.
- ^ abcd Sitruk-Ware R, Bossemeyer R, Bouchard P (junio de 2007). "Propiedades preclínicas y clínicas de la trimegestona: una progestina potente y selectiva". Endocrinología ginecológica . 23 (6): 310–319. doi :10.1080/09513590701267727. PMID 17616854. S2CID 39422122.
- ^ abcdefghi Kuhl H (2011). «Farmacología de los progestágenos» (PDF) . Journal für Reproduktionsmedizin und Endokrinologie-Revista de medicina reproductiva y endocrinología . 8 (Número especial 1): 157–176.
- ^ abc Raynaud JP, Ojasoo T (1983). "[Promegestona, una nueva progestina]". Journal de Gynécologie, Obstétrique et Biologie de la Reproduction (en francés). 12 (7): 697–710. PMID 6366037.
- ^ abcdef Allen RC (11 de septiembre de 1984). "To Market – 1983". En Baily DM (ed.). Informes anuales en química medicinal . Vol. 19. Academic Press. págs. 323–. ISBN 978-0-08-058363-1.
- ^ abcdef "Lista de progestinas".
- ^ abcdefg Tulunay FC, Orme M (6 de diciembre de 2012). Colaboración europea: hacia el desarrollo de fármacos y la farmacoterapia racional: Actas del sexto congreso de la Asociación Europea de Farmacología Clínica y Terapéutica, Estambul, 24-28 de junio de 2003. Springer Science & Business Media. pp. 107-11. ISBN 978-3-642-55454-4.
Investigación de la farmacocinética y el metabolismo de la promegestona en voluntarias sanas tras la administración oral única de 1 mg de promegestona I Gualano V., 1Geneteau A., I Chassard D., I Fordham P., 2Schatz B. I Aster-Cephac, 3/5, Rue Eugene Millon, 75015 París, Francia 2Laboratoire Aventis, 46 Quai De La Rapee, F-75601 París Cedex 12, Francia. Se administró una dosis oral única de 1 mg de promegestona (Surgestonee, 2x0,5 mg) a 12 mujeres premenopáusicas sanas. Los objetivos fueron determinar las concentraciones de promegestona y sus metabolitos y sus parámetros farmacocinéticos. Se realizó un seguimiento de las muestras de sangre y orina hasta 96 horas después de la dosis. Para evitar cualquier interferencia con las hormonas naturales, la promegestona se administró entre el día 7 y 10 del ciclo menstrual. La seguridad clínica y la tolerabilidad fueron buenas. La mayoría de los eventos adversos menores observados se estimaron posiblemente relacionados con el fármaco del estudio (trastornos menstruales) porque clásicamente se relacionaban con la terapia con progestinas. Además, no se observaron modificaciones biológicas clínicamente relevantes. Hubo un metabolismo estereoselectivo de la promegestona a favor de la 21S hidroxi-promegestona, el principal compuesto circulante en plasma (cociente AUC 5/R de aproximadamente 21). Los niveles de 21S hidroxi-promegestona son aproximadamente dos veces mayores que los de la promegestona inalterada. Los niveles plasmáticos del segundo metabolito, es decir, 21R hidroxi-promegestona, son muy inferiores a los de la promegestona y la 21S hidroxi-promegestona. La promegestona, la 215 hidroxi- y la 21R hidroxi-promegestona no se excretan en la orina. Aproximadamente el 3% de la dosis se recuperó en la orina como sulfo y/o glucuroconjugado 21S hidroxi-promegestona y aproximadamente el 1% de la dosis como sulfo y/o glucuroconjugado 21R hidroxi-promegestona.
- ^ ab Winneker RC, Bitran D, Zhang Z (noviembre de 2003). "La biología preclínica de una nueva progestina potente y selectiva: trimegestona". Esteroides . 68 (10–13): 915–920. doi :10.1016/s0039-128x(03)00142-9. PMID 14667983. S2CID 24893971.
- ^ abcdefg Elks J (14 de noviembre de 2014). Diccionario de fármacos: datos químicos: datos químicos, estructuras y bibliografías. Springer. pp. 1026–. ISBN 978-1-4757-2085-3.
- ^ ab Philibert D, Raynaud JP (julio de 1973). "Unión de progesterona en el útero inmaduro de ratón y rata". Esteroides . 22 (1): 89–98. doi :10.1016/0039-128x(73)90073-1. PMID 4353432.
- ^ abcd William Andrew Publishing (22 de octubre de 2013). Pharmaceutical Manufacturing Encyclopedia, 3.ª edición. Elsevier. págs. 2935–36. ISBN 978-0-8155-1856-3.
- ^ abcdefg Index Nominum 2000: Directorio internacional de medicamentos. Taylor y Francisco. Enero de 2000. págs. 883–. ISBN 978-3-88763-075-1.
- ^ ab Raynaud JP, Ojasoo T, Vaché V (1981). "Trazadores estables y específicos". Procesos reproductivos y anticoncepción . Endocrinología bioquímica. Springer. págs. 163-179. doi :10.1007/978-1-4684-3824-6_7. ISBN 978-1-4684-3826-0.
- ^ Uzan S, Denis C, Pomi V, Varin C (febrero de 1992). "Ensayo doble ciego de promegestona (R 5020) y linestrenol en el tratamiento de la enfermedad benigna de la mama". Revista Europea de Obstetricia, Ginecología y Biología Reproductiva . 43 (3): 219–227. doi : 10.1016/0028-2243(92)90177-z . PMID 1563574.
- ^ Gourdy P, Bachelot A, Catteau-Jonard S, Chabbert-Buffet N, Christin-Maître S, Conard J, et al. (noviembre de 2012). "Anticoncepción hormonal en mujeres con riesgo de trastornos vasculares y metabólicos: directrices de la Sociedad Francesa de Endocrinología". Annales d'Endocrinologie . 73 (5): 469–487. doi :10.1016/j.ando.2012.09.001. PMID 23078975.
- ^ Blanton MP, Xie Y, Dangott LJ, Cohen JB (febrero de 1999). "El esteroide promegestona es un antagonista no competitivo del receptor nicotínico de acetilcolina Torpedo que interactúa con la interfaz lípido-proteína". Farmacología molecular . 55 (2): 269–278. doi :10.1124/mol.55.2.269. PMID 9927618. S2CID 491327.
- ^ Chan DW, Slaunwhite WR (mayo de 1977). "La unión de una progestina sintética, R5020, a la transcortina y la albúmina sérica". Revista de endocrinología clínica y metabolismo . 44 (5): 983–985. doi :10.1210/jcem-44-5-983. PMID 858781.
- ^ ab Litwack G (2 de diciembre de 2012). Acciones bioquímicas de las hormonas. Elsevier. pp. 314–. ISBN 978-0-323-15344-7.
- ^ Carp HJ (9 de abril de 2015). Progestágenos en obstetricia y ginecología. Springer. pp. 34–. ISBN 978-3-319-14385-9.
Lectura adicional
- Raynaud JP, Ojasoo T (1983). "[Promegestona, una nueva progestina]". Journal de Gynécologie, Obstétrique et Biologie de la Reproduction (en francés). 12 (7): 697–710. PMID 6366037.
- Brun G, Dargent D, Pontonnier G, Petrescou L (mayo de 1984). "[Uso clínico de promegestona, un agente progestacional con alta especificidad por los receptores]". Revue Française de Gynécologie et d'Obstétrique (en francés). 79 (5): 423–426. PMID 6396815.