Receptor de manosa
| Receptor de manosa de macrófagos | |
|---|---|
| Identificadores | |
| Símbolo | vacuna triple vírica |
| Membranoma | 56 |
| receptor de manosa, tipo C 1 | |||||||
|---|---|---|---|---|---|---|---|
| Identificadores | |||||||
| Símbolo | MRC1 | ||||||
| Símbolos alternativos | CD206 | ||||||
| Gen NCBI | 4360 | ||||||
| HGNC | 7228 | ||||||
| OMI | 153618 | ||||||
| Secuencia de referencia | Número de modelo_002438 | ||||||
| Protección unificada | P22897 | ||||||
| Otros datos | |||||||
| Lugar | Cap. 10 pág. 13 | ||||||
| |||||||
| receptor de manosa, tipo C 2 | |||||||
|---|---|---|---|---|---|---|---|
| Identificadores | |||||||
| Símbolo | MRC2 | ||||||
| Símbolos alternativos | CD280 | ||||||
| Gen NCBI | 9902 | ||||||
| HGNC | 16875 | ||||||
| Secuencia de referencia | NM_006039 | ||||||
| Protección unificada | Q9UBG0 | ||||||
| Otros datos | |||||||
| Lugar | Crónica 17 q23 | ||||||
| |||||||
El receptor de manosa ( Cluster of Differentiation 206, CD206 ) es una lectina de tipo C presente principalmente en la superficie de los macrófagos , células dendríticas inmaduras y células endoteliales sinusoidales del hígado, pero también se expresa en la superficie de las células de la piel como los fibroblastos dérmicos humanos y los queratinocitos . [1] [2] Es el primer miembro de una familia de receptores endocíticos que incluye Endo180 (CD280) , PLA2R de tipo M y DEC-205 (CD205) . [3]
El receptor reconoce residuos terminales de manosa , N -acetilglucosamina y fucosa en los glicanos unidos a las proteínas [4] que se encuentran en la superficie de algunos microorganismos , y desempeña un papel tanto en el sistema inmunitario innato como en el adaptativo . Otras funciones incluyen la eliminación de las glicoproteínas de la circulación, incluidas las hormonas glicoproteicas sulfatadas y las glicoproteínas liberadas en respuesta a eventos patológicos . [5] El receptor de manosa se recicla continuamente entre la membrana plasmática y los compartimentos endosómicos de una manera dependiente de la clatrina . [6]
Estructura
Organización del dominio

El receptor de manosa es una proteína transmembrana de tipo I , con un extremo N-terminal extracelular y un extremo C-terminal intracelular . Primero se sintetiza como un precursor inactivo, pero se escinde proteolíticamente a su forma activa en el aparato de Golgi . [8] En general, la porción extracelular del receptor está compuesta por 8 dominios de reconocimiento de carbohidratos de tipo C consecutivos (CRD) más cercanos a la membrana plasmática, seguidos de un solo dominio de repetición de fibronectina tipo II y un dominio rico en cisteína N-terminal . La cola citoplasmática no es capaz de transducir señales de forma aislada, ya que carece de los motivos de señalización adecuados. [9]
Dominio rico en cisteína N-terminal
El dominio rico en cisteína N-terminal es homólogo a la cadena B de ricina y se une a fracciones de azúcar sulfatadas, con una afinidad particularmente alta por los residuos de N -acetilgalactosamina y galactosa sulfatados en las posiciones 3 y 4 de sus anillos de piranosa . [10]
Otros ligandos incluyen los sulfatos de condroitina A y B, así como las estructuras sulfatadas Lewis x y Lewis a . [6] El receptor de manosa es el único miembro de la familia en el que este dominio es funcional. [5]
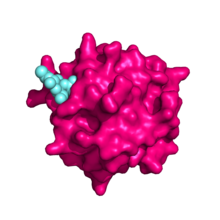
Dominio de repetición de fibronectina tipo II
El dominio de repetición de tipo II de la fibronectina se conserva entre todos los miembros de la familia del receptor de manosa. Los colágenos I-IV se unen a esta región con alta afinidad, mientras que el colágeno V se une solo débilmente. A través de este dominio, el receptor de manosa internaliza el colágeno en los macrófagos y las células sinusoidales del hígado , independientemente de la actividad de lectina del receptor. [9] Junto con el dominio rico en cisteína N-terminal, este dominio es el más conservado entre ratones y humanos (92%). [8]
Dominios de reconocimiento de carbohidratos de tipo C (CRD)
Los 8 CRD en tándem de la región extracelular del receptor de manosa comparten solo un 30% de homología entre sí. Cada uno de ellos contiene al menos algunos de los residuos de aminoácidos necesarios para la unión del Ca2 + y del ligando, algo común en los CRD funcionales de tipo C. Solo los CRD 4 y 5 contienen todos los residuos necesarios para la unión del azúcar, lo que forma un núcleo de unión al ligando resistente a las proteasas . El ligando más común son los residuos terminales de manosa, pero también se unen la N -acetilglucosamina y la fucosa. [8]
La principal interacción entre el CRD-4 y su ligando de azúcar es a través de la ligación directa al Ca 2+ conservado en el sitio de unión del azúcar, de manera similar al mecanismo de unión de la lectina de unión a manano (MBL). Sin embargo, una cuarta parte de la energía libre de la unión del azúcar está asociada con las interacciones de apilamiento hidrofóbico formadas entre una cara del anillo de azúcar y la cadena lateral de un residuo de tirosina conservado en el sitio de unión, lo que no se observa en la MBL. A pesar de las similitudes en la unión de manosa entre el receptor de manosa y la MBL, estas diferencias sugieren que la unión de manosa por parte del receptor de manosa evolucionó de forma independiente a la de otras lectinas de tipo C. [11]
Individualmente, los CRD se unen a la manosa con una afinidad débil. Se cree que la unión de alta afinidad es resultado de la agrupación de múltiples CRD. Esta agrupación permite la unión de ligandos ramificados y multivalentes , como los oligosacáridos N-ligados con alto contenido de manosa . [12]
Conformación
Se ha sugerido que el receptor de manosa puede existir en al menos dos conformaciones estructurales diferentes . Los CRD de tipo C están separados por regiones de enlace de 10 a 20 aminoácidos que contienen varios residuos de prolina , cuya cadena lateral cíclica es bastante rígida y favorece una conformación en la que el dominio rico en cisteína N-terminal se extiende lo más lejos posible de la membrana plasmática. [13]
Alternativamente, las interacciones entre CRD vecinos pueden mantenerlos muy cerca uno del otro y hacer que la región extracelular del receptor se doble, poniendo el dominio rico en cisteína del extremo N en estrecho contacto con los CRD. Esto posicionaría a los CRD 4 y 5 más lejos de la membrana para maximizar su interacción con ligandos potenciales. La resistencia a la proteólisis mostrada por los CRD 4 y 5 sugiere que se producen interacciones físicas entre los dos dominios, lo que respalda la existencia de esta conformación en forma de U. [13]
Se cree que las transiciones entre estas dos conformaciones ocurren de manera dependiente del pH, lo que regula la selectividad y liberación del ligando durante la endocitosis. Se cree que el pH más bajo y más ácido de los endosomas tempranos es responsable de la liberación del ligando. [13]
Procesamiento proteolítico
Una forma funcional y soluble del receptor de manosa se produce tras la escisión proteolítica de la forma unida a la membrana por metaloproteasas que se encuentran en el entorno extracelular. [14] [15]
La proteína soluble consiste en toda la región extracelular del receptor y puede estar involucrada en el transporte de proteínas manosiladas fuera de los sitios de inflamación . [9] Se ha demostrado que el desprendimiento del receptor de manosa de los macrófagos se mejora con el reconocimiento de patógenos fúngicos como Candida albicans y Aspergillus fumigatus , lo que sugiere que la forma soluble puede desempeñar un papel en el reconocimiento de patógenos fúngicos. De esta manera, el equilibrio entre el receptor de manosa soluble y unido a la membrana podría afectar la orientación de los patógenos fúngicos durante el curso de la infección. [16]
Glicosilación
El receptor de manosa está muy glicosilado y sus sitios de glicosilación ligados a N están altamente conservados entre ratones y humanos, lo que indica un papel importante para esta modificación postraduccional . La presencia de residuos de ácido siálico en los glicanos ligados a N del receptor de manosa es importante por su papel en la unión tanto de las glicoproteínas sulfatadas como de las manosiladas. La sialilación regula la multimerización del receptor, que se sabe que influye en la unión a las glicoproteínas sulfatadas. También se sabe que los residuos terminales de ácido siálico son necesarios para la unión a los glicanos manosilados. La ausencia de ácido siálico reduce la capacidad de los receptores para unirse e internalizar los glicanos manosilados, pero no afecta su localización en la membrana plasmática ni su actividad endocítica. [9] [17]
Función
Fagocitosis de patógenos
Varios microorganismos patógenos, incluidos C. albicans , [15] [18] Pneumocystis carinii [19] [20] y Leishmania donovani [21] [22] muestran glicanos en sus superficies con residuos de manosa terminales que son reconocidos por los CRD de tipo C del receptor de manosa, actuando así como un marcador de no propio. Tras el reconocimiento, el receptor internaliza el patógeno unido y lo transporta a los lisosomas para su degradación a través de la vía fagocítica . De esta manera, el receptor de manosa actúa como un receptor de reconocimiento de patrones . La presencia de un motivo de secuencia diaromática FENTLY (Phe-Glu-Asn-Thr-Leu-Tyr) en la cola citoplasmática del receptor es vital para su internalización mediada por clatrina. [6] Esto está respaldado por la evidencia de que las células Cos-1 transfectadas con el receptor de manosa que carece de su cola C-terminal son incapaces de endocitar C. albicans y P. carinii . [6]
Sorprendentemente, los ratones knock out para el receptor de manosa no muestran una mayor susceptibilidad a la infección, lo que sugiere que el receptor no es esencial para la fagocitosis. Sin embargo, no se puede rechazar su participación ya que otros mecanismos pueden compensarla. Por ejemplo, la infección de ratones knock out con P. carinii resultó en un mayor reclutamiento de macrófagos al sitio de la infección. Además, otros receptores presentes en la superficie de las células fagocíticas, como DC-SIGN , SIGNR1 y Endo180, exhiben una capacidad de unión de ligando similar a la del receptor de manosa y, por lo tanto, es probable que en su ausencia, estas proteínas puedan compensar e inducir la fagocitosis. [6]
También se cree que la capacidad del receptor de manosa para ayudar a la internalización de patógenos facilita la infección por Mycobacterium tuberculosis y Mycobacterium leprae . Estas bacterias residen y se multiplican en los macrófagos, impidiendo la formación del fagolisosoma para evitar la degradación. Por lo tanto, al mediar su entrada en el macrófago, el bloqueo del receptor de manosa ayuda a estos patógenos a infectar y crecer en su célula diana. [6] [23]
Endocitosis mediada por clatrina
Las regiones CRD del receptor de manosa en las células endoteliales sinusoidales del hígado eliminan una cantidad de material de desecho que va desde macromoléculas solubles hasta partículas de gran tamaño. [24] Estos incluyen enzimas lisosomales, [25] cadenas α de colágeno, [26] propéptidos C-terminales de procolágenos de tipo I, [27] y activador tisular del plasminógeno. [28] Los estudios de unión indican que cada célula endotelial sinusoidal del hígado expresa un grupo superficial de 20.000-25.000 receptores de manosa. El receptor de manosa en la célula endotelial sinusoidal del hígado es un receptor de reciclaje rápido, con una Ke (constante de velocidad endocítica) de 4,12 min-1, que corresponde a una vida media de 10 s para el grupo superficial de complejos receptor-ligando. [29]
A diferencia de los macrófagos que utilizan los receptores de manosa para la fagocitosis de partículas >200 nm, el receptor de manosa en las células endoteliales sinusoidales del hígado media la endocitosis mediada por clatrina de macromoléculas y nanopartículas <200 nm. [24]
Presentación de antígenos
El receptor de manosa también puede desempeñar un papel en la captación y presentación de antígenos por células dendríticas inmaduras en el sistema inmunológico adaptativo. Al unirse al receptor, los antígenos manosilados se internalizan y se transportan a compartimentos endocíticos dentro de la célula para cargarse en moléculas del complejo mayor de histocompatibilidad (MHC) u otras moléculas de presentación de antígenos relacionadas. Un ejemplo indirecto de esto es el procesamiento del antígeno glicolípido lipoarabinomanano , derivado de Mycobacteria . El lipoarabinomanano (LAM) se presenta a las células T en complejo con CD1b, pero también es capaz de unirse al receptor de manosa. Dado que la presencia de manano , un ligando alternativo, inhibe la proliferación de células T dependiente de LAM, se sugiere que el receptor se une a LAM extracelular, lo internaliza y luego lo transporta a vesículas endocíticas para ser cargado en CD1b. [8]
Las células dendríticas maduras y los macrófagos utilizan el receptor de manosa para la presentación de antígenos de una manera diferente. El receptor soluble escindido se une a los antígenos circulantes y los dirige a las células efectoras en los órganos linfoides a través de su dominio rico en cisteína, activando así el sistema inmunitario adaptativo. [8]
Señalización intracelular
La cola citoplasmática del receptor de manosa no contiene ningún motivo de señalización, pero el receptor ha demostrado ser esencial para la producción de citocinas proinflamatorias y antiinflamatorias , lo que indica un papel más pasivo del receptor en la fagocitosis de patógenos. [6] [8] Esto sugiere que el receptor de manosa es asistido por otros receptores de la superficie celular para desencadenar una cascada de señalización. Por ejemplo, se ha demostrado que las células HEK 293 cotransfectadas con el receptor de manosa humano y el ADNc del receptor tipo Toll 2 humano pueden secretar IL-8 en respuesta a la infección por P. carinii , mientras que las transfectadas con cualquiera de los receptores solo no lo hicieron. [30] Es posible que los dos receptores formen un complejo en la superficie celular que facilite la transducción de señales tras el desafío patógeno.
Resolución de la inflamación
Otra función clave del receptor de manosa es regular los niveles de moléculas liberadas en la circulación durante la respuesta inflamatoria. En respuesta a eventos patológicos, se liberan glicoproteínas que incluyen hidrolasas lisosomales , activador tisular del plasminógeno y mieloperoxidasa de neutrófilos para ayudar a combatir cualquier microorganismo invasor. Una vez que la amenaza ha disminuido, estas glicoproteínas pueden ser dañinas para los tejidos del huésped, por lo que sus niveles en la circulación deben controlarse estrictamente. [6]
Los oligosacáridos ricos en manosa presentes en la superficie de estas glicoproteínas actúan para marcar su naturaleza transitoria, ya que finalmente son reconocidos por el receptor de manosa y eliminados de la circulación. Los ratones deficientes en el receptor de manosa son menos capaces de eliminar estas proteínas y muestran mayores concentraciones de varias hidrolasas lisosomales en la sangre. [5]
En consonancia con esta función, el receptor de manosa se expresa en niveles bajos durante la inflamación y en niveles altos durante la resolución de la inflamación, para garantizar que los agentes inflamatorios se eliminen de la circulación solo en el momento apropiado. [5]
Aclaramiento de hormonas glicoproteicas
El dominio rico en cisteína N-terminal del receptor de manosa juega un papel importante en el reconocimiento de las hormonas glicoproteicas sulfatadas y su eliminación de la circulación. [8]
Las hormonas glicoproteicas como la lutropina , que desencadena la liberación del óvulo durante la ovulación , deben estimular sus receptores en pulsos para evitar la desensibilización del receptor . Los glicanos en su superficie están cubiertos con N -acetilgalactosamina sulfatada (GalNAc), lo que los convierte en ligandos para el dominio de homología de ricina rico en cisteína del receptor de manosa. Esta etiqueta asegura un ciclo de liberación, estimulación y eliminación de la circulación. [7]
Los ratones knock-out que carecen de la enzima necesaria para añadir la estructura de protección GalNAc sulfatada muestran vidas medias más largas para la lutropina, lo que da como resultado una mayor activación del receptor y la producción de estrógeno . Los ratones knock-out hembra alcanzan la madurez sexual más rápido que sus contrapartes de tipo salvaje, tienen un ciclo estral más largo y producen más camadas. Por lo tanto, la etiqueta GalNAc sulfatada es muy importante para regular las concentraciones séricas de ciertas hormonas glicoproteicas. [7]
Tipos
Los humanos expresan dos tipos de receptores de manosa, cada uno codificado por su propio gen:
| Gene | Proteína | Nombres alternativos |
|---|---|---|
| MRC1 | Receptor de manosa 1 de macrófagos | Receptor de manosa tipo C 1, miembro D de la familia 13 del dominio de lectina tipo C (CLEC13D), CD206, MMR |
| MRC2 | Receptor de manosa 2 de macrófagos | Receptor de manosa tipo C 2, proteína asociada al receptor del activador del plasminógeno tipo uroquinasa, CD280 |
Aplicaciones en salud y enfermedad
Las propiedades de internalización selectiva del receptor de manosa indican una serie de posibles aplicaciones en la salud y la enfermedad. Al manipular la glicosilación de proteínas bioactivas importantes hasta un estado altamente manosilado, sus niveles séricos podrían regularse estrictamente y podrían dirigirse específicamente a las células que expresan el receptor de manosa. También existe el potencial de utilizar el receptor de manosa como objetivo para mejorar la activación de los macrófagos y la presentación de antígenos. [5] [8] [31]
MRC2/ Endo180 [32] interactúa con Basigin /CD147 a través de su cuarto dominio de lectina de tipo C para formar un complejo supresor de transición epitelial-mesenquimal molecular que, si se interrumpe, da como resultado la inducción de un comportamiento invasivo de las células epiteliales de próstata asociado con una mala supervivencia del cáncer de próstata . [33] El aumento de la rigidez de la membrana basal debido a su glicación también puede desencadenar una invasión dependiente de Endo180 de las células epiteliales de próstata y este mecanismo biomecánico está asociado con una mala supervivencia del cáncer de próstata . [34] Se ha sugerido que la estabilización del complejo supresor de transición epitelial-mesenquimal Endo180-CD147 y la orientación de la forma no complejada de Endo180 en células invasivas podrían tener un beneficio terapéutico en la prevención de la progresión del cáncer y la metástasis . [35]
Referencias
- ^ Szolnoky G, Bata-Csörgö Z, Kenderessy AS, Kiss M, Pivarcsi A, Novák Z, Nagy Newman K, Michel G, Ruzicka T, Maródi L, Dobozy A, Kemény L (agosto de 2001). "Un receptor de unión a manosa se expresa en los queratinocitos humanos y media en la destrucción de Candida albicans". Revista de Dermatología de Investigación . 117 (2): 205-13. doi : 10.1046/j.1523-1747.2001.14071.x . PMID 11511295.
- ^ Sheikh H, Yarwood H, Ashworth A, Isacke CM (marzo de 2000). "Endo180, una glicoproteína de reciclaje endocítico relacionada con el receptor de manosa de macrófagos, se expresa en fibroblastos, células endoteliales y macrófagos y funciona como un receptor de lectina". Journal of Cell Science . 113 (6): 1021–32. doi :10.1242/jcs.113.6.1021. PMID 10683150.
- ^ East L, Isacke CM (2002). "La familia de receptores de manosa". Biochimica et Biophysica Acta (BBA) - Temas generales . 1572 (2–3): 364–86. doi :10.1016/S0304-4165(02)00319-7. PMID 12223280.
- ^ Schlesinger PH, Doebber TW, Mandell BF, White R, DeSchryver C, Rodman JS, Miller MJ, Stahl P (1978). "Aclaramiento plasmático de glicoproteínas con manosa terminal y N-acetilglucosamina por células hepáticas no parenquimatosas. Estudios con beta-glucuronidasa, N-acetil-β-D-glucosaminidasa, ribonucleasa B y agalacto-orosomucoide". Revista bioquímica . 176 (1): 103–9. doi :10.1042/bj1760103. PMC 1186209 . PMID 728098.
- ^ abcde Lee SJ, Evers S, Roeder D, Parlow AF, Risteli J, Risteli L, Lee YC, Feizi T, Langen H, Nussenzweig MC (2002). "Regulación mediada por el receptor de manosa de la homeostasis de las glicoproteínas séricas". Ciencia . 295 (5561): 1898–901. Código Bib : 2002 Ciencia... 295.1898L. doi : 10.1126/ciencia.1069540. PMID 11884756. S2CID 31432874.
- ^ abcdefgh Gazi U, Martinez-Pomares L (2009). "Influencia del receptor de manosa en la respuesta inmune del huésped". Inmunobiología . 214 (7): 554–61. doi :10.1016/j.imbio.2008.11.004. PMID 19162368.
- ^ abc Taylor M, Drickamer K (2011). Introducción a la glicobiología . Oxford University Press. ISBN 978-0-19-956911-3.
- ^ abcdefgh Stahl PD, Ezekowitz RA (1998). "El receptor de manosa es un receptor de reconocimiento de patrones que participa en la defensa del huésped". Current Opinion in Immunology . 10 (1): 50–5. doi :10.1016/S0952-7915(98)80031-9. PMID 9523111.
- ^ abcd Martinez-Pomares L (2012). "El receptor de manosa". Revista de Biología Leucocitaria . 92 (6): 1177–86. doi : 10.1189/jlb.0512231 . PMID 22966131. S2CID 27512588.
- ^ Fiete DJ, Beranek MC, Baenziger JU (marzo de 1998). "Un dominio rico en cisteína del receptor "manosa" media la unión de GalNAc-4-SO4". Actas de la Academia Nacional de Ciencias de los Estados Unidos de América . 95 (5): 2089–93. Bibcode :1998PNAS...95.2089F. doi : 10.1073/pnas.95.5.2089 . PMC 19259 . PMID 9482843.
- ^ Mullin NP, Hitchen PG, Taylor ME (1997). "Mecanismo de unión de Ca2+ y monosacáridos a un dominio de reconocimiento de carbohidratos de tipo C del receptor de manosa de macrófagos". Journal of Biological Chemistry . 272 (9): 5668–81. doi : 10.1074/jbc.272.9.5668 . PMID 9038177.
- ^ Weis WI, Drickamer K (1996). "Base estructural del reconocimiento de carbohidratos por lectina". Revisión anual de bioquímica . 65 : 441–73. doi :10.1146/annurev.bi.65.070196.002301. PMID 8811186.
- ^ abc Llorca O (2008). "Conformaciones extendidas y dobladas de la familia de receptores de manosa". Ciencias de la vida celular y molecular . 65 (9): 1302–10. doi :10.1007/s00018-007-7497-9. PMC 11131820 . PMID 18193159. S2CID 5038725.
- ^ Jordens R, Thompson A, Amons R, Koning F (1999). "Las células dendríticas humanas liberan una forma funcional y soluble del receptor de manosa". Inmunología internacional . 11 (11): 1775–80. doi :10.1093/intimm/11.11.1775. PMID 10545481.
- ^ ab Martínez-Pomares L, Mahoney JA, Káposzta R, Linehan SA, Stahl PD, Gordon S (1998). "Una forma soluble funcional del receptor de manosa murino es producida por macrófagos in vitro y está presente en suero de ratón". Journal of Biological Chemistry . 273 (36): 23376–80. doi : 10.1074/jbc.273.36.23376 . hdl : 2437/116851 . PMID 9722572.
- ^ Gazi U, Rosas M, Singh S, Heinsbroek S, Haq I, Johnson S, Brown GD, Williams DL, Taylor PR, Martinez-Pomares L (2011). "El reconocimiento fúngico mejora la liberación del receptor de manosa a través de la interacción con dectin-1". Journal of Biological Chemistry . 286 (10): 7822–9. doi : 10.1074/jbc.M110.185025 . PMC 3048669 . PMID 21205820.
- ^ Su Y, Bakker T, Harris J, Tsang C, Brown GD, Wormald MR, Gordon S, Dwek RA, Rudd PM, Martinez-Pomares L (2005). "La glicosilación influye en las actividades de lectina del receptor de manosa de los macrófagos". Journal of Biological Chemistry . 280 (38): 32811–20. doi : 10.1074/jbc.M503457200 . PMID 15983039.
- ^ Maródi L, Korchak HM, Johnston RB (1991). "Mecanismos de defensa del huésped contra especies de Candida. I. Fagocitosis por monocitos y macrófagos derivados de monocitos". Journal of Immunology . 146 (8): 2783–9. doi : 10.4049/jimmunol.146.8.2783 . PMID 1901885.
- ^ Ezekowitz RA, Williams DJ, Koziel H, Armstrong MY, Warner A, Richards FF, Rose RM (1991). "Captación de Pneumocystis carinii mediada por el receptor de manosa de los macrófagos". Nature . 351 (6322): 155–8. Bibcode :1991Natur.351..155E. doi :10.1038/351155a0. PMID 1903183. S2CID 1763804.
- ^ O'Riordan DM, Standing JE, Limper AH (1995). "La glicoproteína A de Pneumocystis carinii se une a los receptores de manosa de los macrófagos". Infección e inmunidad . 63 (3): 779–84. doi :10.1128/IAI.63.3.779-784.1995. PMC 173070 . PMID 7868247.
- ^ Chakraborty R, Chakraborty P, Basu MK (1998). "Receptor de fucosilo manosil de macrófagos: su papel en la invasión de promastigotes virulentos y avirulentos de L. donovani ". Bioscience Reports . 18 (3): 129–42. doi :10.1023/A:1020192512001. PMID 9798785. S2CID 4903749.
- ^ Chakraborty P, Ghosh D, Basu MK (2001). "La modulación del receptor de manosa de los macrófagos afecta la captación de promastigotes virulentos y avirulentos de Leishmania donovani ". Journal of Parasitology . 87 (5): 1023–7. doi :10.1645/0022-3395(2001)087[1023:MOMMRA]2.0.CO;2. PMID 11695359. S2CID 26732461.
- ^ Kang PB, Azad AK, Torrelles JB, Kaufman TM, Beharka A, Tibesar E, DesJardin LE, Schlesinger LS (2005). "El receptor de manosa de macrófagos humanos dirige la biogénesis del fagosoma mediada por lipoarabinomanano de Mycobacterium tuberculosis". Journal of Experimental Medicine . 202 (7): 987–99. doi :10.1084/jem.20051239. PMC 2213176 . PMID 16203868.
- ^ ab Sørensen KK, Simon-Santamaria J, McCuskey RS, Smedsrød B (20 de septiembre de 2015). "Células endoteliales sinusoidales del hígado". Fisiología integral . 5 (4): 1751–74. doi : 10.1002/cphy.c140078 . PMID 26426467.
- ^ Elvevold K, Simon-Santamaria J, Hasvold H, McCourt P, Smedsrød B, Sørensen KK (diciembre de 2008). "Las células endoteliales sinusoidales del hígado dependen del reclutamiento de enzimas lisosomales mediado por el receptor de manosa para una capacidad de degradación normal". Hepatología . 48 (6): 2007–15. doi :10.1002/hep.22527. PMID 19026003. S2CID 29069000.
- ^ Malovic I, Sørensen KK, Elvevold KH, Nedredal GI, Paulsen S, Erofeev AV, Smedsrød BH, McCourt PA (junio de 2007). "El receptor de manosa en las células endoteliales sinusoidales del hígado murino es el principal receptor de eliminación de colágeno desnaturalizado". Hepatología . 45 (6): 1454–61. doi : 10.1002/hep.21639 . PMID 17518370. S2CID 26022255.
- ^ Smedsrød B, Melkko J, Risteli L, Risteli J (15 de octubre de 1990). "El propéptido C-terminal circulante del procolágeno tipo I se elimina principalmente a través del receptor de manosa en las células endoteliales del hígado". The Biochemical Journal . 271 (2): 345–50. doi :10.1042/bj2710345. PMC 1149560 . PMID 2241919.
- ^ Smedsrød B, Einarsson M, Pertoft H (16 de junio de 1988). "El activador tisular del plasminógeno es endocitado por los receptores de manosa y galactosa de las células del hígado de rata". Trombosis y hemostasia . 59 (3): 480–4. doi : 10.1055/s-0038-1647519 . PMID 2847350.
- ^ Magnusson S, Berg T (1 de febrero de 1989). "Endocitosis extremadamente rápida mediada por el receptor de manosa de células de hígado de rata endotelial sinusoidal". The Biochemical Journal . 257 (3): 651–6. doi :10.1042/bj2570651. PMC 1135637 . PMID 2930475.
- ^ Tachado SD, Zhang J, Zhu J, Patel N, Cushion M, Koziel H (2007). "La liberación de IL-8 mediada por Pneumocystis por los macrófagos requiere la coexpresión de receptores de manosa y TLR2". Journal of Leukocyte Biology . 81 (1): 205–11. doi :10.1189/jlb.1005580. PMID 17020928. S2CID 15056895.
- ^ Chang CF, Wan J, Li Q, Renfroe SC, Heller NM, Wang J (julio de 2017). "La microglia y los macrófagos con activación alternativa sesgada promueven la resolución del hematoma en la hemorragia intracerebral experimental". Neurobiología de la enfermedad . 103 : 54–69. doi :10.1016/j.nbd.2017.03.016. PMC 5540140 . PMID 28365213.
- ^ "WikiGenes: MRC2 - receptor de manosa C, tipo 2 Homo sapiens".
- ^ Rodriguez-Teja M, Gronau JH, Minamidate A, Darby S, Gaughan L, Robson C, et al. (marzo de 2015). "Resultado de supervivencia y supresión de la EMT mediada por una interacción de dominio de lectina de Endo180 y CD147". Investigación molecular sobre el cáncer . 13 (3): 538–47. doi : 10.1158/1541-7786.MCR-14-0344-T . PMID 25381222.
- ^ Rodriguez-Teja M, Gronau JH, Breit C, Zhang YZ, Minamidate A, Caley MP, et al. (marzo de 2015). "La membrana basal modificada por AGE coopera con Endo180 para promover la invasividad de las células epiteliales y disminuir la supervivencia del cáncer de próstata" (PDF) . The Journal of Pathology . 235 (4): 581–92. doi :10.1002/path.4485. PMID 25408555. S2CID 40735796.
- ^ Sturge J (marzo de 2016). "Endo180 a la vanguardia del tratamiento del cáncer de hueso y más allá". The Journal of Pathology . 238 (4): 485–8. doi :10.1002/path.4673. PMC 4819699 . PMID 26576691.
Enlaces externos
- Receptor de manosa+ en los encabezados de temas médicos (MeSH) de la Biblioteca Nacional de Medicina de EE. UU.
- Receptor de manosa de macrófagos