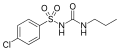
Sulfonilurea

Las sulfonilureas o sulfonilureas son una clase de compuestos orgánicos utilizados en medicina y agricultura . El grupo funcional consiste en un grupo sulfonilo (-S(=O) 2 ) con su átomo de azufre unido a un átomo de nitrógeno de un grupo ureileno (N,N-deshidrourea, un derivado deshidrogenado de la urea ). Las cadenas laterales R1 y R2 distinguen varias sulfonilureas. Las sulfonilureas son el herbicida más utilizado. [1]
Usos agrícolas
Muchas sulfonilureas también se utilizan como herbicidas , porque pueden interferir con la biosíntesis de ciertos aminoácidos en las plantas . [2]
Como herbicidas, las sulfonilureas funcionan interfiriendo con la biosíntesis de los aminoácidos valina, isoleucina y leucina, específicamente a través de la inhibición de la acetolactato sintasa . Los compuestos de esta clase incluyen amidosulfurón, azimsulfurón, bensulfurón-metilo, clorimurón-etilo, clorsulfurón , etametsulfurón-metilo, cinosulfurón, etoxisulfurón, flazasulfurón , flupirsulfurón-metil-sodio, imazosulfurón, metsulfurón-metilo , nicosulfurón, [3] oxasulfurón, primisulfurón-metilo, prosulfurón, pirazosulfurón-etilo, rimsulfurón, sulfometurón-metilo , sulfosulfurón, tifensulfurón-metilo, triasulfurón, tribenurón-metilo y triflusulfurón-metilo. [4] Son herbicidas de amplio espectro que matan las malas hierbas o plagas de las plantas inhibiendo la enzima acetolactato sintasa . En la década de 1960, se aplicaba típicamente más de 1 kg/ha (0,89 lb/acre) de producto químico para la protección de cultivos, mientras que los sulfonilureatos permiten tan solo un 1% de esa cantidad de material para lograr el mismo efecto. [5] [6]
Usos médicos
Tratamiento de la diabetes tipo 2
Se utilizan ampliamente como fármacos antidiabéticos en el tratamiento de la diabetes mellitus tipo 2. Actúan aumentando la secreción de insulina de las células beta del páncreas . [7]
Las sulfonilureas son ineficaces cuando hay una deficiencia absoluta de producción de insulina, como en la diabetes tipo 1 o después de una pancreatectomía. [8]
Las sulfonilureas se pueden utilizar para tratar algunos tipos de diabetes neonatal . Históricamente, a las personas con hiperglucemia y niveles bajos de insulina en sangre se les diagnosticaba diabetes tipo 1 de manera predeterminada, pero se ha descubierto que los pacientes que reciben este diagnóstico antes de los 6 meses de edad suelen ser candidatos para recibir sulfonilureas en lugar de insulina durante toda la vida. [9]
Una revisión sistemática Cochrane de 2011 evaluó los efectos sobre el tratamiento de la diabetes autoinmune latente en adultos (LADA) y encontró que las sulfonilureas no mejoraron el control metabólico de la glucosa a los 3 y 12 meses, incluso empeorando los niveles de HbA1c en algunos casos, en comparación con la insulina. [10] La misma revisión no encontró mejoría del péptido C en ayunas después del tratamiento con sulfonilurea. [10] Aún así, es importante destacar que los estudios disponibles para ser incluidos en esta revisión presentaron fallas considerables en calidad y diseño. [10]
Si bien las sulfonilureas anteriores se asociaron con peores resultados, los agentes más nuevos no parecen aumentar el riesgo de muerte, ataques cardíacos o accidentes cerebrovasculares. [11] Esto se ve reforzado por una revisión sistemática Cochrane de 2020 que no encontró suficiente evidencia de reducción de la mortalidad por todas las causas, eventos adversos graves, mortalidad cardiovascular, infarto de miocardio no fatal, accidente cerebrovascular no fatal o enfermedad renal terminal al comparar la monoterapia con metformina con sulfonilureas. [12] Esta misma revisión tampoco encontró una mejora en la calidad de vida relacionada con la salud. [12]
En individuos con intolerancia a la glucosa , una revisión sistemática de 2019 solo encontró un ensayo adecuado que comparaba los efectos de la sulfonilurea con metformina en la reducción o el retraso del riesgo de desarrollar diabetes tipo 2, sin embargo, este ensayo no informó resultados relevantes para el paciente. [13] Otra revisión sistemática completada en el mismo año sugirió que hay evidencia limitada de si el uso combinado de metformina con sulfonilurea en comparación con la combinación de metformina más otra intervención para reducir la glucosa, proporciona beneficios o daños en la mortalidad, eventos adversos graves y complicaciones macrovasculares y microvasculares . [14] La terapia combinada de metformina y sulfonilurea pareció conducir a un mayor riesgo de hipoglucemia . [14]
Inhibidores de la interleucina-1 β
Las sulfonilureas también se utilizan experimentalmente para inhibir la liberación de interleucina 1 beta del inflamasoma NALP3 (o NLRP3) . [15] [16]
Efectos secundarios
Las sulfonilureas (a diferencia de la metformina , las tiazolidinedionas , la pramlintida y otros tratamientos más nuevos) pueden inducir hipoglucemia como resultado de excesos en la producción y liberación de insulina. La hipoglucemia parece ocurrir con mayor frecuencia con las sulfonilureas que con otros tratamientos. [17] Esto suele ocurrir si la dosis es demasiado alta y el paciente está en ayunas. Algunas personas intentan cambiar los hábitos alimentarios para evitarlo, sin embargo, puede ser contraproducente.
Al igual que la insulina , las sulfonilureas pueden inducir aumento de peso, principalmente como resultado de su efecto de aumentar los niveles de insulina y, por lo tanto, el uso de glucosa y otros combustibles metabólicos. Otros efectos secundarios son: malestar gastrointestinal, dolor de cabeza y reacciones de hipersensibilidad .
La seguridad de la terapia con sulfonilureas durante el embarazo no está establecida. Se ha informado de hipoglucemia prolongada (de 4 a 10 días) en niños nacidos de madres que tomaban sulfonilureas en el momento del parto. [18] El deterioro de la función hepática o renal aumenta el riesgo de hipoglucemia y son contraindicaciones. Dado que tampoco se pueden utilizar otros fármacos antidiabéticos en estas circunstancias, generalmente se recomienda la terapia con insulina durante el embarazo y en caso de insuficiencia hepática y renal , aunque algunos de los agentes más nuevos ofrecen opciones potencialmente mejores.
Una revisión Cochrane de 2011 encontró evidencia de que el tratamiento de LADA con sulfonilureas conduce a una dependencia de insulina más temprana en aproximadamente el 30% de los casos. [10]
Una revisión Cochrane de 2014 encontró evidencia tentativa de que las personas tratadas con sulfonilureas tienen menos eventos cardiovasculares no fatales que aquellas tratadas con metformina (RR 0,7) pero un mayor riesgo de hipoglucemia grave (RR 5,6). No hubo suficientes datos disponibles para determinar el riesgo de mortalidad o de mortalidad cardiovascular. [19] Una revisión anterior realizada por el mismo grupo encontró un aumento estadísticamente significativo en el riesgo de muerte cardiovascular para las sulfonilureas de primera generación en relación con el placebo (RR 2,6), pero no hubo suficientes datos para determinar el riesgo relativo de las sulfonilureas de primera generación en relación con la insulina (RR 1,4). Asimismo, no fue posible determinar el riesgo relativo de mortalidad de las sulfonilureas de segunda generación en relación con la metformina (RR 1,0), la insulina (RR 1,0) o el placebo. [20] La FDA exige que las sulfonilureas lleven una advertencia en la etiqueta sobre el aumento del riesgo de muerte cardiovascular. [18]
Una revisión sistemática Cochrane de 2020 que comparó la monoterapia con metformina con sulfonilureas no encontró evidencia suficiente de reducción de la mortalidad por todas las causas, eventos adversos graves, mortalidad cardiovascular, infarto de miocardio no fatal, accidente cerebrovascular no fatal o enfermedad renal terminal . [12]
Las sulfonilureas de segunda generación tienen una mayor potencia en peso, en comparación con las sulfonilureas de primera generación. [21] De manera similar, los estudios ACCORD (Acción para el Control del Riesgo Cardiovascular en la Diabetes) [22] y VADT (Ensayo de Diabetes de Asuntos de Veteranos) [23] no mostraron una reducción en el ataque cardíaco o la muerte en pacientes asignados a un control estricto de la glucosa con varios medicamentos.
Interacciones
Los fármacos que potencian o prolongan los efectos de las sulfonilureas y por tanto aumentan el riesgo de hipoglucemia incluyen el ácido acetilsalicílico y derivados, el alopurinol , las sulfonamidas y los fibratos . Los fármacos que empeoran la tolerancia a la glucosa , contraviniendo los efectos de los antidiabéticos, incluyen los corticosteroides , la isoniazida , los anticonceptivos orales y otros estrógenos , los simpaticomiméticos y las hormonas tiroideas . Las sulfonilureas tienden a interactuar con una amplia variedad de otros fármacos, pero estas interacciones, así como su importancia clínica, varían de una sustancia a otra. [24] [25]
Estructura
Las sulfonilureas contienen una estructura central de S -arilsulfonilurea con un sustituyente p en el anillo de fenilo ( R 1 ) y varios grupos que terminan el grupo terminal N ′ de la urea ( R 2 ). Químicamente, esta funcionalidad se puede instalar fácilmente haciendo reaccionar arilsulfonamidas (R 1 —C 6 H 4 —SO 2 NH 2 ) con isocianatos (R 2 —NCO).
- Clorpropamida (1.ª generación)
- Tolazamida (1.ª generación)
- Gliclazida (2da generación)
- Glimepirida (2da generación)
Clasificación
Las sulfonilureas se dividen en tres clases según la eficacia terapéutica de su acción antidiabética:
- Medicamentos de primera generación:
Entre ellos se incluyen acetohexamida , carbutamida , clorpropamida , gliciclamida (tolciclamida), metahexamida , tolazamida y tolbutamida .
- Medicamentos de segunda generación:
Incluyen glibenclamida (gliburida), glibornurida , gliclazida , glipizida , gliquidona , glisoxepida y glicopiramida .
- Medicamentos de tercera generación:
Entre ellos se encuentra la glimepirida , aunque a veces se considera un fármaco de segunda generación. [26] [27]
Mecanismo de acción

Las sulfonilureas se unen a los canales de K + (K ATP ) sensibles al ATP en la membrana celular de las células beta pancreáticas y los cierran , lo que despolariza la célula al impedir la salida del potasio. Esta despolarización abre los canales de Ca 2+ dependientes del voltaje . El aumento del calcio intracelular conduce a una mayor fusión de los gránulos de insulina con la membrana celular y, por lo tanto, a una mayor secreción de insulina madura. [28]
Existe cierta evidencia de que las sulfonilureas también sensibilizan a las células β a la glucosa, que limitan la producción de glucosa en el hígado , que disminuyen la lipólisis (descomposición y liberación de ácidos grasos por el tejido adiposo ) y disminuyen la depuración de insulina por el hígado. [29]
El canal K ATP es un complejo octamérico del canal de iones de potasio rectificador interno K ir 6.x y el receptor de sulfonilurea SUR que se asocian con una estequiometría de 4:4. [28]
Además, se ha demostrado que las sulfonilureas interactúan con el factor de intercambio de nucleótidos Epac2 . [30] [31] Los ratones que carecían de este factor mostraron un efecto reductor de glucosa disminuido tras el tratamiento con sulfonilurea.
Historia
Las sulfonilureas fueron descubiertas en 1942 por el químico Marcel Janbon y sus colaboradores en Francia, [32] quienes estudiaban antibióticos de sulfonamida y descubrieron que el compuesto sulfonilurea inducía hipoglucemia en animales. [33]
La investigación y el desarrollo ( investigación traslacional y desarrollo de aplicaciones comerciales) de sulfonilureas como productos farmacéuticos (como agentes diagnósticos y terapéuticos en prediabetes y diabetes) ocurrieron en las décadas de 1950 y 1960, como se explora en Tolbutamida § Historia .
La investigación y el desarrollo (investigación translacional y desarrollo de aplicaciones comerciales) de sulfonilureas como herbicidas se llevaron a cabo en los años 1970 y 1980, como se explora, por ejemplo, en un volumen de la Sloan Technology Series centrado en los aspectos sociotecnológicos de la agricultura (Canine 1995); [34] la Estación Experimental DuPont lideró este desarrollo. [34]
Referencias
- ^ Costello, Ryan A.; Nicolas, Samar; Shivkumar, Abhijit (2024), "Sulfonilureas", StatPearls , Treasure Island (FL): StatPearls Publishing, PMID 30020597 , consultado el 1 de agosto de 2024
- ^ Duggleby RG, McCourt JA, Guddat LW (marzo de 2008). "Estructura y mecanismo de inhibición de la acetohidroxiácido sintasa de las plantas". Fisiología y bioquímica de las plantas . 46 (3): 309–324. Bibcode :2008PlPB...46..309D. doi :10.1016/j.plaphy.2007.12.004. PMID 18234503.
- ^ "Nicosulfurón". EXTOXNET . Consultado el 9 de mayo de 2013 .
- ^ Arnold P. Appleby, Franz Müller, Serge Carpy "Control de malezas" en Ullmann's Encyclopedia of Industrial Chemistry 2002, Wiley-VCH, Weinheim. doi :10.1002/14356007.a28_165
- ^ "Pesticidas en la agricultura y el medio ambiente: Impactos en la salud humana" (PDF) . aesacademy.org .
- ^ Lamberth C, Jeanmart S, Luksch T, Plant A (agosto de 2013). "Desafíos y tendencias actuales en el descubrimiento de agroquímicos". Science . 341 (6147): 742–6. Bibcode :2013Sci...341..742L. doi :10.1126/science.1237227. PMID 23950530. S2CID 206548681.
- ^ Seino S (agosto de 2012). "Señalización celular en la secreción de insulina: los objetivos moleculares de ATP, AMPc y sulfonilurea". Diabetologia . 55 (8): 2096–2108. doi :10.1007/s00125-012-2562-9. PMID 22555472. S2CID 7146975.
- ^ "Sulfonilureas", LiverTox: Información clínica y de investigación sobre la lesión hepática inducida por fármacos , Bethesda (MD): Instituto Nacional de Diabetes y Enfermedades Digestivas y Renales, 2012, PMID 31643682 , consultado el 1 de agosto de 2024
- ^ Greeley SA, Tucker SE, Naylor RN, Bell GI, Philipson LH (agosto de 2010). "Diabetes mellitus neonatal: un modelo para la medicina personalizada". Tendencias en endocrinología y metabolismo . 21 (8): 464–472. doi :10.1016/j.tem.2010.03.004. PMC 2914172. PMID 20434356 .
- ^ abcd Brophy S, Davies H, Mannan S, Brunt H, Williams R (septiembre de 2011). "Intervenciones para la diabetes autoinmune latente (LADA) en adultos". Base de datos Cochrane de revisiones sistemáticas . 2011 (9): CD006165. doi :10.1002/14651858.cd006165.pub3. PMC 6486159. PMID 21901702 .
- ^ Rados DV, Pinto LC, Remonti LR, Leitão CB, Gross JL (junio de 2016). "Corrección: la asociación entre el uso de sulfonilureas y la mortalidad por todas las causas y cardiovascular: un metaanálisis con análisis secuencial de ensayos clínicos aleatorizados". PLOS Medicine . 13 (6): e1002091. doi : 10.1371/journal.pmed.1002091 . PMC 4920361 . PMID 27340828.
- ^ abc Gnesin F, Thuesen AC, Kähler LK, Madsbad S, Hemmingsen B, et al. (Grupo Cochrane de Trastornos Metabólicos y Endocrinos) (junio de 2020). "Monoterapia con metformina para adultos con diabetes mellitus tipo 2". Base de Datos Cochrane de Revisiones Sistemáticas . 2020 (6): CD012906. doi : 10.1002 /14651858.CD012906.pub2. PMC 7386876. PMID 32501595.
- ^ Madsen KS, Chi Y, Metzendorf MI, Richter B, Hemmingsen B, et al. (Grupo Cochrane de Trastornos Metabólicos y Endocrinos) (diciembre de 2019). "Metformina para la prevención o el retraso de la diabetes mellitus tipo 2 y sus complicaciones asociadas en personas con mayor riesgo de desarrollar diabetes mellitus tipo 2". Base de Datos Cochrane de Revisiones Sistemáticas . 2019 (12): CD008558. doi :10.1002/14651858.CD008558.pub2. PMC 6889926. PMID 31794067 .
- ^ ab Madsen KS, Kähler P, Kähler LK, Madsbad S, Gnesin F, Metzendorf MI, et al. (abril de 2019). Grupo Cochrane de Trastornos Metabólicos y Endocrinos (ed.). "Terapia combinada con metformina y sulfonilurea de segunda o tercera generación para adultos con diabetes mellitus tipo 2". Base de Datos Cochrane de Revisiones Sistemáticas . 4 ( 4): CD012368. doi :10.1002/14651858.CD012368.pub2. PMC 6472662. PMID 30998259.
- ^ Kulkarni, Amol A.; Sajith, Ayyiliath M.; Duarte, Trevor T.; Tena, Anahis; Spencer, Charles T.; Bowen, J. Phillip (2020). "Diseño, síntesis y selección de inhibidores del inflamasoma NLRP3 derivados de sulfonilurea". Medicinal Chemistry Research . 29 (1): 126–135. doi :10.1007/s00044-019-02466-7. ISSN 1054-2523. PMC 7223447 . PMID 32435125.
- ^ Coll RC, Robertson AA, Chae JJ, Higgins SC, Muñoz-Planillo R, Inserra MC, et al. (marzo de 2015). "Un inhibidor de moléculas pequeñas del inflamasoma NLRP3 para el tratamiento de enfermedades inflamatorias". Nature Medicine . 21 (3): 248–255. doi :10.1038/nm.3806. PMC 4392179 . PMID 25686105.
- ^ Shyangdan DS, Royle P, Clar C, Sharma P, Waugh N, Snaith A (octubre de 2011). "Análogos de péptidos similares al glucagón para la diabetes mellitus tipo 2". Base de datos Cochrane de revisiones sistemáticas . 2011 (10): CD006423. doi :10.1002/14651858.cd006423.pub2. PMC 6486297. PMID 21975753 .
- ^ ab "Tabletas de Diaßeta (gliburida) USP" (PDF) . Sanofi-Aventis US LLC . Administración de Alimentos y Medicamentos de los Estados Unidos. 2009.
- ^ Hemmingsen B, Schroll JB, Wetterslev J, Gluud C, Vaag A, Sonne DP, et al. (julio de 2014). "Monoterapia con sulfonilureas versus metformina en pacientes con diabetes tipo 2: una revisión sistemática Cochrane y un metanálisis de ensayos clínicos aleatorizados y análisis secuencial de ensayos". CMAJ Open . 2 (3): E162–E175. doi :10.9778/cmajo.20130073. PMC 4185978 . PMID 25295236.
- ^ Hemmingsen B, Schroll JB, Lund SS, Wetterslev J, Gluud C, Vaag A, et al. (abril de 2013). Hemmingsen B (ed.). "Monoterapia con sulfonilurea para pacientes con diabetes mellitus tipo 2". Base de Datos Cochrane de Revisiones Sistemáticas . 4 (4): CD009008. doi :10.1002/14651858.CD009008.pub2. PMID 23633364. (Retractado, ver doi :10.1002/14651858.CD009008.pub3, PMID 26222249, Retraction Watch )
- ^ "Sulfonilureas, segunda generación", LiverTox: información clínica y de investigación sobre la lesión hepática inducida por fármacos , Bethesda (MD): Instituto Nacional de Diabetes y Enfermedades Digestivas y Renales, 2012, PMID 31643463 , consultado el 16 de agosto de 2024
- ^ Gerstein HC, Miller ME, Byington RP, Goff DC, Bigger JT, Buse JB, et al. (junio de 2008). "Efectos de la reducción intensiva de la glucosa en la diabetes tipo 2". The New England Journal of Medicine . 358 (24): 2545–2559. doi :10.1056/NEJMoa0802743. PMC 4551392 . PMID 18539917.
- ^ Duckworth W, Abraira C, Moritz T, Reda D, Emanuele N, Reaven PD, et al. (enero de 2009). "Control de glucosa y complicaciones vasculares en veteranos con diabetes tipo 2". The New England Journal of Medicine . 360 (2): 129–139. doi : 10.1056/NEJMoa0808431 . PMID 19092145. S2CID 16608858.
- ^ Haberfeld H, ed. (2009). Austria-Codex (en alemán) (edición 2009/2010). Viena: Österreichischer Apothekerverlag. ISBN 978-3-85200-196-8.
- ^ Dinnendahl V, Fricke U, eds. (2010). Perfil Arzneistoff (en alemán). vol. 4 (23 ed.). Eschborn, Alemania: Govi Pharmazeutischer Verlag. ISBN 978-3-7741-9846-3.
- ^ Triplitt CL, Reasner CA (2011). "Capítulo 83: diabetes mellitus". En DiPiro JT, Talbert RL, Yee GC, Matzke GR, Wells BG, Posey LM (eds.). Farmacoterapia: un enfoque fisiopatológico (8.ª ed.). Nueva York, NY: McGraw-Hill. pág. 1274. ISBN 978-0-07-170354-3.
- ^ Davidson J (2000). Diabetes mellitus clínica: un enfoque orientado a los problemas. Stuttgart: Thieme. p. 422. ISBN 978-0-86577-840-5.
- ^ ab Proks P, Reimann F, Green N, Gribble F, Ashcroft F (diciembre de 2002). "Estimulación de la secreción de insulina por sulfonilureas". Diabetes . 51 (Supl 3): S368–S376. doi : 10.2337/diabetes.51.2007.S368 . PMID 12475777.
- ^ Yu, Ming; Feng, Xiao-Yu; Yao, Shuai; Wang, Chang; Yang, Ping (16 de septiembre de 2022). "Ciertos fármacos de sulfonilurea aumentan los ácidos grasos libres séricos en pacientes diabéticos: una revisión sistemática y un metanálisis". Revista mundial de casos clínicos . 10 (26): 9524–9535. doi : 10.12998/wjcc.v10.i26.9524 . ISSN 2307-8960. PMC 9477688 . PMID 36159441.
- ^ Zhang CL, Katoh M, Shibasaki T, Minami K, Sunaga Y, Takahashi H, et al. (Julio de 2009). "El sensor cAMP Epac2 es un objetivo directo de las sulfonilureas antidiabéticas". Ciencia . 325 (5940): 607–610. Código Bib : 2009 Ciencia... 325..607Z. doi : 10.1126/ciencia.1172256. PMID 19644119. S2CID 8923842.
- ^ Takahashi T, Shibasaki T, Takahashi H, Sugawara K, Ono A, Inoue N, et al. (octubre de 2013). "Las sulfonilureas antidiabéticas y el AMPc activan cooperativamente Epac2A". Science Signaling . 6 (298): ra94. doi :10.1126/scisignal.2004581. hdl : 20.500.14094/D1005987 . PMID 24150255. S2CID 27711862.
- ^ Janbon M, Chaptal J, Vedel A, Schaap J (1942). "Accidentes hipoglucémicos graves por un sulfamidotiodiazol (le VK 57 ou 2254 RP)". Montpellier Med . 441 : 21–22.
- ^ Patlak M (diciembre de 2002). "Nuevas armas para combatir una enfermedad antigua: el tratamiento de la diabetes". FASEB Journal . 16 (14): 1853. doi : 10.1096/fj.02-0974bkt . PMID 12468446. S2CID 35412249.
- ^ ab Canine C (1995). "Guerra contra las malas hierbas". Dream Reaper: La historia de un inventor anticuado en el mundo de alta tecnología y alto riesgo de la agricultura moderna . Sloan Technology Series. págs. 189-213. ISBN 9780517472378.