Podocito
| Podocito | |
|---|---|
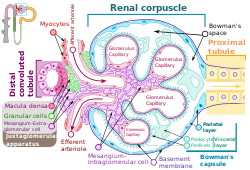 Los podocitos que se muestran en verde recubren la cápsula de Bowman en el corpúsculo renal y envuelven los capilares como parte importante del proceso de filtración en los riñones. | |
| Detalles | |
| Precursor | Mesodermo intermedio |
| Ubicación | Cápsula renal de Bowman |
| Identificadores | |
| latín | podocitos |
| Malla | D050199 |
| FMA | 70967 |
| Términos anatómicos de microanatomía [editar en Wikidata] | |
Los podocitos son células de la cápsula de Bowman en los riñones que envuelven los capilares del glomérulo . Los podocitos forman el revestimiento epitelial de la cápsula de Bowman, la tercera capa a través de la cual se produce la filtración de la sangre. [1] La cápsula de Bowman filtra la sangre , reteniendo moléculas grandes como las proteínas, mientras que las moléculas más pequeñas como el agua , las sales y los azúcares se filtran como el primer paso en la formación de la orina . Aunque varias vísceras tienen capas epiteliales , el nombre de células epiteliales viscerales generalmente se refiere específicamente a los podocitos, que son células epiteliales especializadas que residen en la capa visceral de la cápsula.
Los podocitos tienen largos procesos primarios llamados trabéculas que forman procesos secundarios conocidos como pedicelos o procesos del pie (por lo que las células se denominan podo- + -cito ). [2] Los pedicelos envuelven los capilares y dejan ranuras entre ellos. La sangre se filtra a través de estas ranuras, cada una conocida como ranura de filtración , diafragma de ranura o poro de ranura . [3] Se requieren varias proteínas para que los pedicelos envuelvan los capilares y funcionen. Cuando los bebés nacen con ciertos defectos en estas proteínas, como la nefrina y el CD2AP , sus riñones no pueden funcionar. Las personas tienen variaciones en estas proteínas, y algunas variaciones pueden predisponerlas a insuficiencia renal más adelante en la vida. La nefrina es una proteína similar a una cremallera que forma el diafragma de ranura, con espacios entre los dientes de la cremallera lo suficientemente grandes para permitir el paso del azúcar y el agua, pero demasiado pequeños para permitir el paso de las proteínas. Los defectos de la nefrina son responsables de la insuficiencia renal congénita. CD2AP regula el citoesqueleto del podocito y estabiliza el diafragma de hendidura. [4] [5]
Estructura

Un podocito tiene una estructura compleja. Su cuerpo celular tiene procesos principales o primarios que se extienden y forman procesos secundarios como los pedicelos o procesos del pie del podocito . [6] Los procesos primarios están sostenidos por microtúbulos y filamentos intermedios . Los pedicelos tienen un citoesqueleto basado en actina. [6] Los podocitos se encuentran recubriendo las cápsulas de Bowman en las nefronas del riñón. Los pedicelos o procesos del pie envuelven los capilares glomerulares para formar las hendiduras de filtración. [7] Los pedicelos aumentan la superficie de las células, lo que permite una ultrafiltración eficiente . [8]

Los podocitos secretan y mantienen la membrana basal . [3]
Hay numerosas vesículas recubiertas y fosas recubiertas a lo largo del dominio basolateral de los podocitos, lo que indica una alta tasa de tráfico vesicular .
Los podocitos poseen un retículo endoplasmático bien desarrollado y un gran aparato de Golgi , indicativo de una alta capacidad de síntesis de proteínas y modificaciones postraduccionales .
También existe evidencia creciente de una gran cantidad de cuerpos multivesiculares y otros componentes lisosomales observados en estas células, lo que indica una alta actividad endocítica .
Necesidades energéticas
Los podocitos requieren una cantidad significativa de energía para preservar la integridad estructural de sus procesos pediátricos, dado el estrés mecánico sustancial que soportan durante el proceso de filtración glomerular. [9]
Los cambios dinámicos en la presión capilar glomerular ejercen fuerzas de tracción y estiramiento sobre los procesos pediocíticos y pueden provocar tensión mecánica en su citoesqueleto . Al mismo tiempo, el movimiento del ultrafiltrado glomerular genera una tensión de corte en el flujo de fluido, que ejerce una fuerza tangencial sobre la superficie de estos procesos pediocíticos. [10]
Para preservar la intrincada arquitectura de su proceso podal, los podocitos requieren un gasto sustancial de ATP para mantener su estructura y organización citoesquelética, contrarrestar la elevada presión capilar glomerular y estabilizar la pared capilar. [10]
Función

A. Células endoteliales del glomérulo; 1. poro (fenestra).
B. Membrana basal glomerular: 1. lámina rara interna 2. lámina densa 3. lámina rara externa
C. Podocitos: 1. proteína enzimática y estructural 2. hendidura de filtración 3. diafragma
Los podocitos tienen procesos primarios llamados trabéculas, que envuelven los capilares glomerulares . [2] Las trabéculas a su vez tienen procesos secundarios llamados pedicelos o procesos del pie. [2] Los pedicelos se entrelazan, dando lugar así a espacios delgados llamados hendiduras de filtración. [3] Las hendiduras están cubiertas por diafragmas de hendidura que se componen de una serie de proteínas de la superficie celular, entre ellas nefrina , podocalixina y P-cadherina , que restringen el paso de macromoléculas grandes como la albúmina sérica y la gammaglobulina y garantizan que permanezcan en el torrente sanguíneo. [11] Las proteínas necesarias para el correcto funcionamiento del diafragma de hendidura incluyen nefrina , [12] NEPH1 , NEPH2 , [13] podocina , CD2AP . [14] y FAT1 . [15]

Las moléculas pequeñas como el agua , la glucosa y las sales iónicas pueden pasar a través de las rendijas de filtración y formar un ultrafiltrado en el líquido tubular , que luego es procesado por la nefrona para producir orina .
Los podocitos también participan en la regulación de la tasa de filtración glomerular (TFG). Cuando los podocitos se contraen, provocan el cierre de las rendijas de filtración. Esto disminuye la TFG al reducir la superficie disponible para la filtración.
Importancia clínica

La pérdida de los procesos podales de los podocitos (es decir, borramiento de los podocitos) es un sello distintivo de la enfermedad de cambios mínimos , por lo que a veces se la ha denominado enfermedad de los procesos podales. [17]
La interrupción de las ranuras de filtración o la destrucción de los podocitos pueden provocar una proteinuria masiva , en la que se pierden grandes cantidades de proteínas de la sangre.
Un ejemplo de ello es la nefrosis de tipo finlandés , una enfermedad congénita que se caracteriza por una proteinuria neonatal que conduce a una insuficiencia renal terminal . Se ha descubierto que esta enfermedad está causada por una mutación en el gen de la nefrina .
En 2002, el profesor Moin Saleem de la Universidad de Bristol creó la primera línea celular de podocitos humanos inmortalizados condicionalmente. [18] [ se necesita más explicación ] Esto significó que los podocitos podían cultivarse y estudiarse en el laboratorio. Desde entonces se han hecho muchos descubrimientos. El síndrome nefrótico ocurre cuando hay una ruptura de la barrera de filtración glomerular. Los podocitos forman una capa de la barrera de filtración. Las mutaciones genéticas pueden causar disfunción de los podocitos que conduce a una incapacidad de la barrera de filtración para restringir la pérdida de proteínas urinarias. Actualmente se sabe que 53 genes desempeñan un papel en el síndrome nefrótico genético. [19] En el síndrome nefrótico idiopático, no se conoce ninguna mutación genética. Se cree que es causado por un factor de permeabilidad circulante hasta ahora desconocido. [20] Evidencias recientes sugieren que el factor podría ser liberado por las células T o las células B, [21] [22] Las líneas celulares de podocito pueden ser tratadas con plasma de pacientes con síndrome nefrótico para entender las respuestas específicas del podocito al factor circulante. Hay evidencia creciente de que el factor circulante podría estar enviando señales al podocito a través del receptor PAR-1 . [23] [ se necesita más explicación ]
Se ha propuesto la presencia de podocitos en la orina como un marcador diagnóstico temprano de la preeclampsia . [24]
Véase también
- Lista de tipos de células humanas derivadas de las capas germinales
- Lista de los distintos tipos de células del cuerpo humano adulto
Referencias
- ^ "Podocito" en el Diccionario médico de Dorland
- ^ abc Ovalle WK, Nahirney PC (28 de febrero de 2013). Netter's Essential Histology E-Book. Elsevier Health Sciences. ISBN 978-1-4557-0307-4. Recuperado el 2 de junio de 2020 .
- ^ abc Lote CJ (2012). "Filtración glomerular". Principios de fisiología renal (5.ª ed.). Nueva York: Springer Science+Business Media. pág. 34. doi :10.1007/978-1-4614-3785-7_3. ISBN 978-1-4614-3784-0.
- ^ Wickelgren I (octubre de 1999). "Se encuentran los primeros componentes para un nuevo filtro renal". Science . 286 (5438): 225–226. doi :10.1126/science.286.5438.225. PMID 10577188. S2CID 43237744.
- ^ Löwik MM, Groenen PJ, Levtchenko EN, Monnens LA, van den Heuvel LP (noviembre de 2009). "Análisis genético molecular de los genes de los podocitos en la glomeruloesclerosis focal y segmentaria: una revisión". Revista Europea de Pediatría . 168 (11): 1291–1304. doi :10.1007/s00431-009-1017-x. PMC 2745545 . PMID 19562370.
- ^ ab Reiser J, Altintas MM (2016). "Podocitos". F1000Res . 5 : 114. doi : 10.12688/f1000research.7255.1 . PMC 4755401 . PMID 26918173.
- ^ Imagen de histología: 22401lba de Vaughan, Deborah (2002). Un sistema de aprendizaje en histología: CD-ROM y guía . Oxford University Press . ISBN 978-0195151732.
- ^ Nosek TM. "Epitelio; tipos de células". Fundamentos de fisiología humana . Archivado desde el original el 24 de marzo de 2016.
- ^ Baek, J; Lee, YH; Jeong, HY; Lee, SY (septiembre de 2023). "Control de calidad mitocondrial y su papel emergente en la patogénesis de la enfermedad renal diabética". Investigación renal y práctica clínica . 42 (5): 546–560. doi :10.23876/j.krcp.22.233. PMC 10565453. PMID 37448292 .
- ^ ab Blaine, J; Dylewski, J (16 de julio de 2020). "Regulación del citoesqueleto de actina en podocitos". Cells . 9 (7). doi : 10.3390/cells9071700 . PMID 32708597.
- ^ Jarad G, Miner JH (mayo de 2009). "Actualización sobre la barrera de filtración glomerular". Current Opinion in Nephrology and Hypertension . 18 (3): 226–232. doi :10.1097/mnh.0b013e3283296044. PMC 2895306 . PMID 19374010.
- ^ Wartiovaara J, Ofverstedt LG, Khoshnoodi J, Zhang J, Mäkelä E, Sandin S, et al. (noviembre de 2004). "Las hebras de nefrina contribuyen a un andamiaje de diafragma de hendidura porosa como se revela mediante tomografía electrónica". The Journal of Clinical Investigation . 114 (10): 1475–1483. doi :10.1172/JCI22562. PMC 525744 . PMID 15545998.
- ^ Neumann-Haefelin E, Kramer-Zucker A, Slanchev K, Hartleben B, Noutsou F, Martin K, et al. (junio de 2010). "Un enfoque de organismo modelo: definición del papel de las proteínas Neph como reguladores de la morfogénesis neuronal y renal". Human Molecular Genetics . 19 (12): 2347–2359. doi :10.1093/hmg/ddq108. PMID 20233749.
- ^ Fukasawa H, Bornheimer S, Kudlicka K, Farquhar MG (julio de 2009). "Los diafragmas de hendidura contienen proteínas de unión estrecha". Revista de la Sociedad Americana de Nefrología . 20 (7): 1491–1503. doi :10.1681/ASN.2008101117. PMC 2709684 . PMID 19478094.
- ^ Ciani L, Patel A, Allen ND, ffrench-Constant C (mayo de 2003). "Los ratones que carecen de la protocadherina gigante mFAT1 presentan anomalías en la unión de la hendidura renal y un fenotipo de ciclopía y anoftalmia parcialmente penetrante". Biología molecular y celular . 23 (10): 3575–3582. doi :10.1128/mcb.23.10.3575-3582.2003. PMC 164754 . PMID 12724416.
- ^ Cutrim ÉMM, Neves PDMM, Campos MAG, Wanderley DC, Teixeira-Júnior AAL, Muniz MPR; et al. (2022). "Glomerulopatía colapsante: una revisión del consorcio brasileño en colapso". Front Med (Lausana) . 9 : 846173. doi : 10.3389/fmed.2022.846173 . PMC 8927620 . PMID 35308512.
{{cite journal}}: CS1 maint: varios nombres: lista de autores ( enlace )
- Licencia CC-BY 4.0 - ^ Vivarelli M, Massella L, Ruggiero B, Emma F (febrero de 2017). "Enfermedad de cambios mínimos". Revista clínica de la Sociedad Estadounidense de Nefrología . 12 (2): 332–345. doi :10.2215/CJN.05000516. PMC 5293332 . PMID 27940460.
- ^ Saleem, Moin A.; O'Hare, Michael J.; Reiser, Jochen; Coward, Richard J.; Inward, Carol D.; Farren, Timothy; Xing, Chang Ying; Ni, Lan; Mathieson, Peter W.; Mundel, Peter (marzo de 2002). "Una línea celular de podocitos humanos condicionalmente inmortalizada que demuestra la expresión de nefrina y podocina". Revista de la Sociedad Americana de Nefrología . 13 (3): 630–638. doi : 10.1681/ASN.V133630 . ISSN 1046-6673. PMID 11856766.
- ^ Bierzynska, Agnieszka; McCarthy, Hugh J.; Soderquest, Katrina; Sen, Ethan S.; Colby, Elizabeth; Ding, Wen Y.; Nabhan, Marwa M.; Kerecuk, Larissa; Hegde, Shivram; Hughes, David; Marks, Stephen; Feather, Sally; Jones, Caroline; Webb, Nicholas JA; Ognjanovic, Milos (abril de 2017). "El perfil genómico y clínico de una cohorte nacional de síndrome nefrótico aboga por un enfoque de medicina de precisión para el manejo de la enfermedad". Kidney International . 91 (4): 937–947. doi :10.1016/j.kint.2016.10.013. hdl : 1983/c730c0d6-5527-435a-8c27-a99fd990a0e8 . Revista de Biología Molecular y Genética .
- ^ Maas, Rutger J.; Deegens, Jeroen K.; Wetzels, Jack F. (2014). "Factores de permeabilidad en el síndrome nefrótico idiopático: perspectivas históricas y lecciones para el futuro". Nefrología Diálisis Trasplante . 29 (12). academic.oup.com: 2207–2216. doi : 10.1093/ndt/gfu355 . PMID 25416821 . Consultado el 26 de abril de 2023 .
- ^ Hackl, Inés; Zed, Seif El Din Abo; Diefenhardt, Paul; Binz-Lotter, Julia; Ehren, Rasmus; Weber, Lutz Thorsten (18 de noviembre de 2021). "El papel del sistema inmunológico en el síndrome nefrótico idiopático". Pediatría Molecular y Celular . 8 (1): 18. doi : 10.1186/s40348-021-00128-6 . ISSN 2194-7791. PMC 8600105 . PMID 34792685.
- ^ May, Carl J.; Welsh, Gavin I.; Chesor, Musleeha; Lait, Phillipa J.; Schewitz-Bowers, Lauren P.; Lee, Richard WJ; Saleem, Moin A. (1 de octubre de 2019). "Las células Th17 humanas producen un mediador soluble que aumenta la motilidad de los podocitos a través de vías de señalización que imitan la activación de PAR-1". Revista estadounidense de fisiología. Fisiología renal . 317 (4): F913–F921. doi :10.1152/ajprenal.00093.2019. ISSN 1522-1466. PMC 6843047. PMID 31339775 .
- ^ May, Carl J.; Chesor, Musleeha; Hunter, Sarah E.; Hayes, Bryony; Barr, Rachel; Roberts, Tim; Barrington, Fern A.; Farmer, Louise; Ni, Lan; Jackson, Maisie; Snethen, Heidi; Tavakolidakhrabadi, Nadia; Goldstone, Max; Gilbert, Rodney; Beesley, Matt (marzo de 2023). "La estimulación del receptor 1 activado por la proteasa de podocito en ratones produce glomeruloesclerosis focal y segmentaria que refleja los eventos de señalización de la enfermedad humana". Kidney International . 104 (2): 265–278. doi : 10.1016/j.kint.2023.02.031 . ISSN 0085-2538. PMC 7616342 . PMID 36940798. S2CID 257639270.
- ^ Konieczny A, Ryba M, Wartacz J, Czyżewska-Buczyńska A, Hruby Z, Witkiewicz W (2013). "Podocitos en orina, ¿un nuevo biomarcador de preeclampsia?" (PDF) . Avances en Medicina Clínica y Experimental . 22 (2): 145-149. PMID 23709369.
Enlaces externos
- Fotografía de anatomía: Urinario/mamífero/vasc1/vasc1 - Organología comparada en la Universidad de California, Davis - "Mamífero, vasculatura renal (EM, alta)"
- Imagen de histología: 22401loa – Sistema de aprendizaje de histología de la Universidad de Boston - "Ultraestructura de la célula: podocitos y capilares glomerulares"
- Asignatura de Histología UIUC 1400
- podocyte.ca [ enlace muerto permanente ] en el Instituto de Investigación Samuel Lunenfeld
- Imagen de histología: 22402loa – Sistema de aprendizaje de histología en la Universidad de Boston
- Imagen de histología: 22403loa – Sistema de aprendizaje de histología en la Universidad de Boston