Infección por el virus del papiloma humano
| Infección por el virus del papiloma humano | |
|---|---|
| Otros nombres | Virus del papiloma humano |
 | |
| La principal proteína de la cápside L1 del VPH 11 | |
| Especialidad | Enfermedades infecciosas , ginecología , oncología. |
| Síntomas | Ninguna, verrugas [1] [2] |
| Complicaciones | Cáncer de cuello uterino , vulva , vagina , pene , ano , boca, amígdalas o garganta [1] [2] [3] |
| Causas | El virus del papiloma humano se transmite por contacto directo [4] [5] |
| Factores de riesgo | Contacto sexual |
| Prevención | Vacunas contra el VPH , condones [4] [6] |
| Frecuencia | La mayoría de las personas se infectan en algún momento [4] |
La infección por el virus del papiloma humano ( infección por VPH ) es causada por un virus de ADN de la familia Papillomaviridae . [5] Muchas infecciones por VPH no causan síntomas y el 90% se resuelven espontáneamente en dos años. [1] En algunos casos, una infección por VPH persiste y da lugar a verrugas o lesiones precancerosas . [2] Estas lesiones, dependiendo del sitio afectado, aumentan el riesgo de cáncer de cuello uterino , vulva , vagina , pene , ano , boca, amígdalas o garganta . [1] [2] [3] Casi todo el cáncer de cuello uterino se debe al VPH, y dos cepas, VPH16 y VPH18 , representan el 70% de todos los casos. [1] [7] El VPH16 es responsable de casi el 90% de los cánceres orofaríngeos positivos para VPH . [3] Entre el 60% y el 90% de los otros cánceres enumerados anteriormente también están relacionados con el VPH. [7] El HPV6 y el HPV11 son causas comunes de verrugas genitales y papilomatosis laríngea . [1]
Una infección por VPH es causada por el virus del papiloma humano , un virus de ADN de la familia del virus del papiloma. [8] Se han descrito más de 200 tipos. [9] Una persona puede infectarse con más de un tipo de VPH, [10] y solo se sabe que la enfermedad afecta a los humanos. [5] [11] Más de 40 tipos pueden transmitirse a través del contacto sexual e infectar el ano y los genitales . [4] Los factores de riesgo para la infección persistente por tipos de transmisión sexual incluyen la primera relación sexual a una edad temprana , múltiples parejas sexuales, tabaquismo y función inmunológica deficiente . [1] Estos tipos generalmente se transmiten por contacto directo sostenido de piel con piel, siendo el sexo vaginal y anal los métodos más comunes. [4] La infección por VPH también puede transmitirse de una madre a su bebé durante el embarazo . [10] No hay evidencia de que el VPH pueda transmitirse a través de elementos comunes como los asientos del inodoro, [12] pero los tipos que causan verrugas pueden propagarse a través de superficies como los pisos. [13] El VPH no se elimina con los desinfectantes y desinfectantes de manos comunes, lo que aumenta la posibilidad de que el virus se transfiera a través de agentes infecciosos no vivos llamados fómites . [14]
Las vacunas contra el VPH pueden prevenir los tipos más comunes de infección. [4] Para que sean más eficaces, la inoculación debe realizarse antes del inicio de la actividad sexual y, por lo tanto, se recomiendan entre los 9 y los 13 años de edad. [1] La detección del cáncer de cuello uterino , como la prueba de Papanicolaou ("prueba de Papanicolaou"), o el examen del cuello uterino después de aplicar ácido acético , puede detectar tanto el cáncer en etapa temprana como las células anormales que pueden convertirse en cáncer. [1] La detección permite un tratamiento temprano que produce mejores resultados. [1] La detección ha reducido tanto el número de casos como el número de muertes por cáncer de cuello uterino. [15] Las verrugas genitales se pueden eliminar mediante congelación . [5]
Casi todas las personas sexualmente activas se infectan por el VPH en algún momento de sus vidas. [4] El VPH es la infección de transmisión sexual (ITS) más común a nivel mundial. [5] Los VPH de alto riesgo causan alrededor del 5% de todos los cánceres en todo el mundo y alrededor de 37.300 casos de cáncer en los Estados Unidos cada año. [9] El cáncer de cuello uterino es uno de los cánceres más comunes en todo el mundo, causando un estimado de 604.000 casos nuevos y 342.000 muertes en 2020. [1] Aproximadamente el 90% de estos nuevos casos y muertes por cáncer de cuello uterino ocurrieron en países de ingresos bajos y medios . [1] Aproximadamente el 1% de los adultos sexualmente activos tienen verrugas genitales. [10] Se han descrito casos de verrugas en la piel desde la época de la antigua Grecia , pero no fue hasta 1907 que se determinó que eran causadas por un virus. [16]
Tipos de VPH
El VPH es un grupo de más de 200 virus relacionados, que se designan con un número para cada tipo de virus. [9] Algunos tipos de VPH, como el VPH5, pueden generar infecciones que persisten durante toda la vida del individuo sin manifestar nunca ningún síntoma clínico. Los tipos de VPH 1 y 2 pueden causar verrugas comunes en algunos individuos infectados. [17] Los tipos de VPH 6 y 11 pueden causar verrugas genitales y papilomatosis laríngea . [1]
Muchos tipos de VPH son cancerígenos . [18] Aproximadamente doce tipos de VPH (incluidos los tipos 16, 18, 31 y 45) se denominan tipos de "alto riesgo" porque la infección persistente se ha relacionado con el cáncer de orofaringe , [3] laringe , [3] vulva , vagina , cuello uterino , pene y ano . [9] [19] [20] Todos estos cánceres implican una infección de transmisión sexual del VPH al tejido epitelial estratificado . [1] [2] El tipo 16 del VPH es la cepa con más probabilidades de causar cáncer y está presente en aproximadamente el 47% de todos los cánceres de cuello uterino, [21] [22] y en muchos cánceres vaginales y vulvares, [23] cánceres de pene, cánceres anales y cánceres de cabeza y cuello.
La siguiente tabla enumera los síntomas comunes de la infección por VPH y los tipos de VPH asociados.
| Enfermedad | Tipo de VPH |
|---|---|
| Verrugas comunes | 2, 7, 22 |
| Verrugas plantares | 1, 2, 4, 63 |
| Verrugas planas | 3, 10, 28 |
| Verrugas anogenitales | 6, 11, 42, 44 y otros [24] |
| Displasia anal (lesiones) | 16, 18, 31, 53, 58 [25] |
| Cánceres genitales |
|
| Epidermodisplasia verruciforme | Más de 15 tipos |
| Hiperplasia epitelial focal (boca) | 13, 32 |
| Papilomas en la boca | 6, 7, 11, 16, 32 |
| Cáncer orofaríngeo | 16 [3] |
| Quiste verrugoso | 60 |
| Papilomatosis laríngea | 6, 11 |
Las vacunas contra el VPH disponibles protegen contra dos, cuatro o nueve tipos de VPH. [27] Hay seis vacunas profilácticas contra el VPH autorizadas para su uso: las vacunas bivalentes Cervarix , Cecolin y Walrinvax ; las vacunas cuadrivalentes Cervavax y Gardasil ; y la vacuna nonavalente Gardasil 9. [ 27] Todas las vacunas contra el VPH protegen al menos contra los tipos 16 y 18 de VPH, que causan el mayor riesgo de cáncer de cuello uterino. Las vacunas cuadrivalentes también protegen contra los tipos 6 y 11 de VPH. La vacuna nonavalente Gardasil 9 brinda protección contra esos cuatro tipos (6, 11, 16 y 18), junto con otros cinco tipos de VPH de alto riesgo responsables del 20% de los cánceres de cuello uterino (tipos 31, 33, 45, 52 y 58). [27]
Signos y síntomas
Verrugas

.jpg/440px-Sample_HPV-6_Histology_Report_for_Throat_Warts_(Papiloma).jpg)
La infección de la piel (infección " cutánea ") por VPH está muy extendida. [28] Las infecciones de la piel por VPH pueden causar crecimientos cutáneos no cancerosos llamados verrugas . Las verrugas son causadas por un crecimiento rápido de células en la capa externa de la piel. [29] Si bien se han descrito casos de verrugas desde la época de la antigua Grecia, su causa viral no se conoció hasta 1907. [16]
Las verrugas cutáneas son más comunes en la infancia y suelen aparecer y desaparecer espontáneamente en el transcurso de semanas o meses. Las verrugas cutáneas recurrentes son comunes. [30] Se cree que todos los VPH son capaces de establecer infecciones "latentes" a largo plazo en pequeñas cantidades de células madre presentes en la piel. Aunque estas infecciones latentes pueden no erradicarse nunca por completo, se cree que el control inmunológico bloquea la aparición de síntomas como las verrugas. El control inmunológico es específico del tipo de VPH, lo que significa que una persona puede volverse resistente a un tipo de VPH y permanecer susceptible a otros tipos. [ cita requerida ]
Los tipos de verrugas incluyen:
- Las verrugas comunes se encuentran generalmente en las manos y los pies, pero también pueden aparecer en otras zonas, como los codos o las rodillas. Las verrugas comunes tienen una superficie característica similar a la de una coliflor y suelen estar ligeramente elevadas por encima de la piel circundante. Los tipos cutáneos de VPH pueden causar verrugas genitales, pero no están asociados con el desarrollo de cáncer. [ cita requerida ]
- Las verrugas plantares se encuentran en las plantas de los pies, crecen hacia adentro y generalmente causan dolor al caminar.
- Las verrugas subungueales o periungueales se forman debajo de la uña (subungueales), alrededor de la uña o en la cutícula (periungueales). Son más difíciles de tratar que las verrugas en otras localizaciones. [31]
- Las verrugas planas se encuentran con mayor frecuencia en los brazos, la cara o la frente. Al igual que las verrugas comunes, las verrugas planas se presentan con mayor frecuencia en niños y adolescentes. En personas con una función inmunológica normal, las verrugas planas no están asociadas con el desarrollo de cáncer. [32]
Las verrugas comunes, planas y plantares tienen muchas menos probabilidades de propagarse de persona a persona.
Verrugas genitales
La infección por VPH de la piel en la zona genital es la infección de transmisión sexual más común en todo el mundo. [33] Estas infecciones están asociadas con verrugas genitales o anales (conocidas médicamente como condilomas acuminados o verrugas venéreas), y estas verrugas son el signo más fácilmente reconocible de la infección genital por VPH. [ cita requerida ]
Las cepas de VPH que pueden causar verrugas genitales suelen ser diferentes de las que causan verrugas en otras partes del cuerpo, como las manos o los pies, o incluso la parte interna de los muslos. Una amplia variedad de tipos de VPH pueden causar verrugas genitales, pero los tipos 6 y 11 juntos representan alrededor del 90% de todos los casos. [34] [35] Sin embargo, en total más de 40 tipos de VPH se transmiten a través del contacto sexual y pueden infectar la piel del ano y los genitales. [4] Estas infecciones pueden causar verrugas genitales, aunque también pueden permanecer asintomáticas. [ cita requerida ]
La gran mayoría de las infecciones genitales por VPH nunca causan síntomas evidentes y el sistema inmunológico las elimina en cuestión de meses. Además, las personas pueden transmitir el virus a otras incluso si no presentan síntomas evidentes de infección. La mayoría de las personas contraen infecciones genitales por VPH en algún momento de sus vidas, y aproximadamente el 10% de las mujeres están infectadas en la actualidad. [33] Un gran aumento en la incidencia de la infección genital por VPH ocurre a la edad en que las personas comienzan a tener actividad sexual. Al igual que con los VPH cutáneos, se cree que la inmunidad al VPH genital es específica para una cepa específica de VPH. [ cita requerida ]
Papilomatosis laríngea
Además de las verrugas genitales, la infección por los tipos 6 y 11 del VPH puede causar una enfermedad poco frecuente conocida como papilomatosis laríngea recurrente , en la que se forman verrugas en la laringe [36] u otras zonas del tracto respiratorio. [37] [38] Estas verrugas pueden reaparecer con frecuencia, pueden interferir con la respiración y, en casos extremadamente raros, pueden progresar a cáncer. Por estas razones, puede ser aconsejable repetir la cirugía para eliminar las verrugas. [37] [39]
Cáncer
Estadísticas de casos
El cáncer de cuello uterino es uno de los cánceres más comunes en todo el mundo, causando aproximadamente 604.000 casos nuevos y 342.000 muertes en 2020. [1] Alrededor del 90% de estos casos nuevos y muertes por cáncer de cuello uterino ocurrieron en países de ingresos bajos y medios , donde las pruebas de detección y el tratamiento de los cambios tempranos en las células del cuello uterino no están fácilmente disponibles. [1]
En Estados Unidos, cada año se producen alrededor de 37.300 casos de cáncer debido al VPH. [9]
| Área de cáncer | Número medio anual de casos | VPH atribuible (estimado) | Atribuible al VPH 16/18 (estimado) |
|---|---|---|---|
| Cuello uterino | 11.771 | 10.700 | 7.800 |
| Orofaringe (hombres) | 12.638 | 9.100 | 8.000 |
| Orofaringe (mujeres) | 3.100 | 2.000 | 1.600 |
| Vulva | 3.554 | 2.400 | 1.700 |
| Ano (mujeres) | 3.260 | 3.000 | 2.600 |
| Ano (hombres) | 1.750 | 1.600 | 1.400 |
| Pene | 1.168 | 700 | 600 |
| Vagina | 802 | 600 | 400 |
| Recto (mujeres) | 513 | 500 | 400 |
| Recto (hombres) | 237 | 200 | 200 |
| Total | 38.793 | 30.700 | 24.600 |
Desarrollo del cáncer
En algunas personas infectadas, el sistema inmunológico puede dejar de controlar el VPH. La infección persistente con tipos de VPH de alto riesgo, como los tipos 16, 18, 31 y 45, puede favorecer el desarrollo de cáncer. [41] Los cofactores como el humo del cigarrillo también pueden aumentar el riesgo de cánceres relacionados con el VPH. [42] [43]
Se cree que el VPH causa cáncer al integrar su genoma en el ADN nuclear . Algunos de los primeros genes expresados por el VPH, como E6 y E7, actúan como oncogenes que promueven el crecimiento tumoral y la transformación maligna . [16] La integración del genoma del VPH también puede causar carcinogénesis al promover la inestabilidad genómica asociada con alteraciones en el número de copias del ADN. [44]
E6 produce una proteína (también llamada E6) que se une simultáneamente a dos proteínas de la célula huésped llamadas p53 y proteína asociada a E6 ( E6-AP ). E6AP es una ligasa de ubiquitina E3 , una enzima cuyo propósito es marcar proteínas con una modificación postraduccional llamada ubiquitina. Al unir ambas proteínas, E6 induce a E6AP a unir una cadena de moléculas de ubiquitina a p53, marcando así a p53 para la degradación proteosomal . [45] [46] Normalmente, p53 actúa para prevenir el crecimiento celular y promueve la muerte celular en presencia de daño en el ADN. p53 también regula positivamente la proteína p21, que bloquea la formación del complejo ciclina D/Cdk4 , previniendo así la fosforilación de la proteína del retinoblastoma (RB) y, a su vez, deteniendo la progresión del ciclo celular al prevenir la activación de E2F . En resumen, p53 es una proteína supresora de tumores que detiene el ciclo celular y previene el crecimiento y la supervivencia celular cuando se produce daño al ADN. [47] Por lo tanto, la degradación de p53, inducida por E6, promueve la división celular descontrolada, el crecimiento celular y la supervivencia celular, todas características del cáncer. [48]
Es importante señalar que, si bien la interacción entre E6, E6AP y p53 fue la primera en caracterizarse, existen muchas otras proteínas en la célula huésped que interactúan con E6 y ayudan a la inducción del cáncer. [49]
Carcinoma de células escamosas de la piel
Los estudios también han demostrado una relación entre una amplia gama de tipos de VPH y el carcinoma de células escamosas de la piel . En tales casos, los estudios in vitro sugieren que la proteína E6 del virus VPH puede inhibir la apoptosis inducida por la luz ultravioleta . [50]
Cáncer de cuello uterino

Casi todos los casos de cáncer de cuello uterino están asociados con la infección por VPH, con dos tipos, VPH16 y VPH18, presentes en el 70% de los casos. [1] [7] [21] [51] [52] [53] En 2012, la Agencia Internacional para la Investigación sobre el Cáncer consideró que doce tipos de VPH eran cancerígenos para el cáncer de cuello uterino : 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58 y 59. [54] Un estudio encontró que el 74% de los carcinomas de células escamosas y el 78% de los adenocarcinomas dieron positivo para los tipos de VPH 16 o 18. [55] La infección persistente por VPH aumenta el riesgo de desarrollar carcinoma de cuello uterino. Las personas que tienen una mayor incidencia de estos tipos de infección son las mujeres con VIH/SIDA, que tienen un riesgo 22 veces mayor de cáncer de cuello uterino. [56] [57]
Los tipos de VPH cancerígenos en el cáncer de cuello uterino pertenecen al género alfapapilomavirus y pueden agruparse en clados de VPH . [58] Los dos clados principales de VPH cancerígenos, alfapapilomavirus-9 (A9) y alfapapilomavirus-7 (A7), contienen HPV16 y HPV18 , respectivamente. [59] Se ha demostrado que estos dos clados de VPH tienen diferentes efectos sobre las características moleculares del tumor y el pronóstico del paciente, y el clado A7 se asocia con vías más agresivas y un pronóstico inferior. [60]
En 2020, se produjeron alrededor de 604.000 casos nuevos y 342.000 muertes por cáncer de cuello uterino en todo el mundo. Alrededor del 90% de estos casos se produjeron en el mundo en desarrollo . [1]
La mayoría de las infecciones por VPH del cuello uterino son eliminadas rápidamente por el sistema inmunológico y no progresan a cáncer de cuello uterino (ver más abajo la subsección Eliminación en Virología). Debido a que el proceso de transformación de células cervicales normales en cancerosas es lento, el cáncer se presenta en personas que han estado infectadas con VPH durante mucho tiempo, generalmente más de una década o más (infección persistente). [37] [61] Además, tanto la infección por VPH como el cáncer de cuello uterino impulsan modificaciones metabólicas que pueden estar correlacionadas con la regulación aberrante de enzimas relacionadas con las vías metabólicas. [62]
Las variantes no europeas (NE) del VPH16 son significativamente más cancerígenas que las variantes europeas (E) del VPH16. [63]
Cáncer de ano
El riesgo de cáncer anal es entre 17 y 31 veces mayor entre las personas VIH positivas que fueron coinfectadas con VPH de alto riesgo, y 80 veces mayor, especialmente entre los hombres VIH positivos que tienen relaciones sexuales con hombres. [64]
La prueba de Papanicolaou anal para detectar el cáncer anal podría beneficiar a algunas subpoblaciones de hombres o mujeres que tienen sexo anal. [65] Sin embargo, no existe consenso sobre si dicha prueba es beneficiosa o quién debería hacerse una prueba de Papanicolaou anal. [66] [67]
Cáncer de pene
El VPH está asociado con aproximadamente el 50% de los cánceres de pene . En los Estados Unidos, el cáncer de pene representa aproximadamente el 0,5% de todos los casos de cáncer en hombres. El VPH16 es el tipo más comúnmente asociado detectado. El riesgo de cáncer de pene aumenta de 2 a 3 veces para las personas que están infectadas con VIH y VPH. [64]
Cánceres de cabeza y cuello
La infección oral con tipos de VPH de alto riesgo cancerígeno (más comúnmente VPH 16) [40] se asocia con un número creciente de cánceres de cabeza y cuello . [68] [52] [69] [70] Esta asociación es independiente del consumo de tabaco y alcohol . [70] [71] [72]
El porcentaje local varía ampliamente, desde el 70% en los Estados Unidos [73] hasta el 4% en Brasil. [74] Tener sexo anal u oral con una pareja infectada con VPH puede aumentar el riesgo de desarrollar estos tipos de cáncer. [69]
En Estados Unidos, el número de nuevos casos de cáncer de cabeza y cuello asociados al VPH diagnosticados ha superado el de casos de cáncer de cuello uterino. [68] La tasa de estos cánceres ha aumentado de un estimado de 0,8 casos por cada 100.000 personas en 1988 [75] a 4,5 por cada 100.000 en 2012 [40] y, a partir de 2021, la tasa ha seguido aumentando. [76] Los investigadores explican estos datos recientes por un aumento del sexo oral. Este tipo de cáncer es más común en hombres que en mujeres. [77]
Se ha informado del perfil mutacional del cáncer de cabeza y cuello HPV-positivo y HPV-negativo, lo que demuestra además que son enfermedades fundamentalmente distintas. [78]
Cáncer de pulmón
Algunas evidencias vinculan el VPH con tumores benignos y malignos del tracto respiratorio superior. La Agencia Internacional para la Investigación sobre el Cáncer ha descubierto que las personas con cáncer de pulmón tenían significativamente más probabilidades de tener varias formas de alto riesgo de anticuerpos contra el VPH en comparación con las que no tenían cáncer de pulmón. [79] Los investigadores que buscaban el VPH entre 1.633 pacientes con cáncer de pulmón y 2.729 personas sin la enfermedad pulmonar descubrieron que las personas con cáncer de pulmón tenían más tipos de VPH que los pacientes sin cáncer, y entre los pacientes con cáncer de pulmón, las probabilidades de tener ocho tipos graves de VPH aumentaron significativamente. [80] Además, la expresión de proteínas estructurales del VPH mediante inmunohistoquímica y estudios in vitro sugieren la presencia del VPH en el cáncer bronquial y sus lesiones precursoras. [81] Otro estudio detectó el VPH en el condensado del aliento exhalado (EBC), el cepillado bronquial y el tejido pulmonar neoplásico de los casos, y encontró la presencia de una infección por VPH en el 16,4% de los sujetos afectados por cáncer de pulmón de células no pequeñas, pero en ninguno de los controles. [82] Las frecuencias promedio reportadas de VPH en cánceres de pulmón fueron 17% y 15% en Europa y las Américas, respectivamente, y el número medio de VPH en muestras de cáncer de pulmón asiático fue 35,7%, con una heterogeneidad considerable entre ciertos países y regiones. [83]
Cáncer de piel
En casos muy raros, el VPH puede causar epidermodisplasia verruciforme (EV) en personas con un sistema inmunológico debilitado . El virus, sin control por parte del sistema inmunológico, provoca la sobreproducción de queratina por parte de las células de la piel , lo que da lugar a lesiones parecidas a verrugas o cuernos cutáneos que, en última instancia, pueden transformarse en cáncer de piel , pero no se comprende bien su desarrollo. [84] [85] Los tipos específicos de VPH que se asocian con EV son HPV5, HPV8 y HPV14. [85]
Causa
Transmisión
El VPH de transmisión sexual se divide en dos categorías: de bajo riesgo y de alto riesgo. Los VPH de bajo riesgo causan verrugas en los genitales o alrededor de ellos. Los tipos 6 y 11 causan el 90% de todas las verrugas genitales y la papilomatosis respiratoria recurrente que causa tumores benignos en las vías respiratorias. Los VPH de alto riesgo causan cáncer y consisten en unos doce tipos identificados. [9] Los tipos 16 y 18 son responsables de causar la mayoría de los cánceres causados por el VPH. Estos VPH de alto riesgo causan el 5% de los cánceres en el mundo. En los Estados Unidos, los VPH de alto riesgo causan el 3% de todos los casos de cáncer en mujeres y el 2% en hombres. [86]
Los factores de riesgo de infecciones genitales persistentes por VPH, que aumentan el riesgo de desarrollar cáncer, incluyen la primera relación sexual a una edad temprana, tener múltiples parejas, fumar y la inmunosupresión. [1] El VPH genital se transmite por contacto directo sostenido de piel con piel, siendo el sexo vaginal, anal y oral los métodos más comunes. [4] [19] Ocasionalmente, puede transmitirse por sexo manual o de una madre a su bebé durante el embarazo . [87] [88] El VPH es difícil de eliminar mediante técnicas estándar de desinfección hospitalaria y puede transmitirse en un entorno de atención médica en equipo ginecológico reutilizable, como transductores de ultrasonido vaginal. El período de transmisibilidad aún se desconoce, pero probablemente sea al menos mientras persistan las lesiones visibles del VPH. El VPH todavía puede transmitirse incluso después de que las lesiones se hayan tratado y ya no sean visibles o presentes. [89]
Perinatal
Aunque los tipos genitales de VPH pueden transmitirse de madre a hijo durante el parto, la aparición de enfermedades genitales relacionadas con el VPH en recién nacidos es poco frecuente. Sin embargo, la falta de aparición no descarta la infección latente asintomática, ya que el virus ha demostrado ser capaz de ocultarse durante décadas. La transmisión perinatal de los tipos 6 y 11 de VPH puede dar lugar al desarrollo de papilomatosis respiratoria recurrente de inicio juvenil (JORRP). La JORRP es muy poco frecuente, con tasas de alrededor de 2 casos por cada 100.000 niños en los Estados Unidos. [37] Aunque las tasas de JORRP son sustancialmente más altas si una mujer presenta verrugas genitales en el momento de dar a luz, el riesgo de JORRP en tales casos sigue siendo inferior al 1%. [ cita requerida ]
Infecciones genitales
Las infecciones genitales por VPH se transmiten principalmente por contacto con los genitales, el ano o la boca de una pareja sexual infectada. [90]
De los 120 virus del papiloma humano conocidos, 51 especies y tres subtipos infectan la mucosa genital. [91] Quince se clasifican como tipos de alto riesgo (16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59, 68, 73 y 82), tres como de alto riesgo probable (26, 53 y 66) y doce como de bajo riesgo (6, 11, 40, 42, 43, 44, 54, 61, 70, 72, 81 y 89). [18]
Los condones no protegen completamente contra el virus porque las áreas alrededor de los genitales, incluida la zona interna del muslo, no están cubiertas, lo que expone estas áreas a la piel de la persona infectada. [92]
Manos
Los estudios han demostrado que la transmisión del VPH se produce entre las manos y los genitales de la misma persona y sus parejas sexuales. Hernández realizó pruebas en los genitales y la mano dominante de cada persona en 25 parejas heterosexuales cada dos meses durante un promedio de siete meses. Encontró dos parejas en las que los genitales del hombre infectaron la mano de la mujer con VPH de alto riesgo, dos en las que la mano de ella infectó los genitales del hombre, una en la que los genitales de ella infectaron la mano del hombre, dos en las que el hombre infectó su propia mano y dos en las que la mujer infectó su propia mano. [93] [94] Las manos no fueron la principal fuente de transmisión en estas 25 parejas, pero fueron significativas. [ cita requerida ]
Partridge informa que las yemas de los dedos de los hombres dieron positivo para VPH de alto riesgo en más de la mitad de la tasa (26 % cada dos años) que sus genitales (48 %). [95] Winer informa que el 14 % de las muestras de yemas de los dedos de mujeres sexualmente activas dieron positivo. [96]
El contacto no sexual con las manos parece tener poco o ningún papel en la transmisión del VPH. Winer encontró que las catorce muestras de las yemas de los dedos de mujeres vírgenes eran negativas al comienzo de su estudio de las yemas de los dedos. [96] En un informe independiente sobre la infección genital por VPH, el 1% de las mujeres vírgenes (1 de 76) que no habían tenido contacto sexual dieron positivo en la prueba del VPH, mientras que el 10% de las mujeres vírgenes que informaron haber tenido contacto sexual sin penetración dieron positivo (7 de 72). [97]
Objetos compartidos
El intercambio de objetos posiblemente contaminados, por ejemplo, cuchillas de afeitar, [89] puede transmitir el VPH. [98] [99] [100] Aunque es posible, la transmisión por vías distintas a las relaciones sexuales es menos común para la infección genital femenina por VPH. [90] El contacto de los dedos con los genitales es una forma posible de transmisión, pero es poco probable que sea una fuente significativa. [96] [101]
Sangre
Aunque tradicionalmente se ha asumido que el VPH no es transmisible a través de la sangre, ya que se piensa que solo infecta los tejidos cutáneos y mucosos, estudios recientes han puesto en duda esta noción. Históricamente, el ADN del VPH se ha detectado en la sangre de pacientes con cáncer de cuello uterino. [102] En 2005, un grupo informó que, en muestras de sangre congeladas de 57 pacientes pediátricos sexualmente ingenuos que tenían infección por VIH vertical o adquirida por transfusión , 8 (14,0%) de estas muestras también dieron positivo para VPH-16. [103] Esto parece indicar que puede ser posible que el VPH se transmita a través de una transfusión de sangre . Sin embargo, como la transmisión no sexual del VPH por otros medios no es poco común, esto no se pudo probar definitivamente. En 2009, un grupo analizó muestras de sangre de la Cruz Roja Australiana de 180 donantes masculinos sanos para el VPH, y posteriormente encontró ADN de una o más cepas del virus en 15 (8,3%) de las muestras. [104] Sin embargo, es importante señalar que detectar la presencia de ADN del VPH en la sangre no es lo mismo que detectar el virus en sí en la sangre, y aún se desconoce si el virus puede o no residir en la sangre de las personas infectadas. Por lo tanto, queda por determinar si el VPH puede o no transmitirse a través de la sangre. [102] Esto es preocupante, ya que actualmente no se examinan las donaciones de sangre para detectar el VPH, y al menos algunas organizaciones como la Cruz Roja Americana y otras sociedades de la Cruz Roja no parecen prohibir actualmente que las personas con VPH donen sangre. [105]
Cirugía
Se ha documentado la transmisión hospitalaria del VPH, especialmente al personal quirúrgico. Los cirujanos, incluidos los urólogos y/o cualquier persona en la sala, están expuestos a la infección por VPH por inhalación de partículas virales nocivas durante la electrocauterización o la ablación láser de un condiloma (verruga). [106] Se ha informado de un caso de un cirujano láser que desarrolló una papilomatosis laríngea extensa después de realizar una ablación láser a pacientes con condilomas anogenitales. [106]
Virología

La infección por VPH se limita a las células basales del epitelio estratificado , el único tejido en el que se replican. [108] El virus no puede unirse al tejido vivo; en cambio, infecta los tejidos epiteliales a través de microabrasiones u otros traumatismos epiteliales que exponen segmentos de la membrana basal . [108] El proceso infeccioso es lento y tarda entre 12 y 24 horas en iniciarse la transcripción. Se cree que los anticuerpos implicados desempeñan un papel neutralizante importante mientras los viriones aún residen en la membrana basal y las superficies celulares. [108]
Se cree que las lesiones por VPH surgen de la proliferación de queratinocitos basales infectados . La infección ocurre típicamente cuando las células basales en el huésped se exponen al virus infeccioso a través de una barrera epitelial alterada, como ocurriría durante las relaciones sexuales o después de abrasiones menores de la piel. No se ha demostrado que las infecciones por VPH sean citolíticas ; más bien, las partículas virales se liberan como resultado de la degeneración de las células descamativas . El VPH puede sobrevivir durante muchos meses y a bajas temperaturas sin un huésped; por lo tanto, una persona con verrugas plantares puede propagar el virus al caminar descalza. [35]
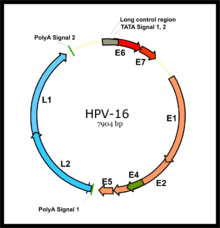
El VPH es un pequeño virus de ADN circular de doble cadena con un genoma de aproximadamente 8000 pares de bases. [19] [109] El ciclo de vida del VPH sigue estrictamente el programa de diferenciación del queratinocito huésped. Se cree que el virión del VPH infecta los tejidos epiteliales a través de microabrasiones, por lo que el virión se asocia con receptores putativos como las integrinas alfa , las lamininas y la anexina A2 [110] lo que lleva a la entrada de los viriones en las células epiteliales basales a través de endocitosis mediada por clatrina y /o endocitosis mediada por caveolina dependiendo del tipo de VPH. [111] En este punto, el genoma viral es transportado al núcleo por mecanismos desconocidos y se establece en un número de copias de 10-200 genomas virales por célula. Luego se produce una sofisticada cascada transcripcional a medida que el queratinocito huésped comienza a dividirse y se diferencia cada vez más en las capas superiores del epitelio. [ cita requerida ]
Evolución
La filogenia de las distintas cepas del VPH refleja en general los patrones de migración del Homo sapiens y sugiere que el VPH puede haberse diversificado junto con la población humana. Los estudios sugieren que el VPH evolucionó a lo largo de cinco ramas principales que reflejan la etnia de los huéspedes humanos y se diversificó junto con la población humana. [112]
Los investigadores identificaron inicialmente dos variantes principales de HPV16, europea (HPV16-E) y no europea (HPV16-NE). [113] Análisis más recientes basados en miles de genomas de HPV16 muestran que de hecho existen dos clados principales, que se subdividen en cuatro linajes (designados AD) e incluso se subdividen en 16 sublinajes (A1–4, B1–4, C1–4 y D1–4). [114] [115] Los sublinajes A1-A3 constituyen la variante europea, A4 la variante asiática, B1-B4 la variante africana tipo I, C1–C4 la variante africana tipo II, D1 la variante norteamericana, D2 la variante asiático americana tipo I, D3 la variante asiático americana tipo II. [114] Los diversos linajes y sublinajes tienen diferente capacidad oncogénica, donde en general, se considera que los linajes no europeos aumentan el riesgo de cáncer. [116] Aunque el HPV16 es un virus de ADN, existen signos de recombinación entre los diferentes linajes. [115] [117] Con base en un análisis de más de 3600 genomas, entre el 0,3 y el 1,2% de ellos podrían ser recombinantes. [115] Por lo tanto, idealmente, la genotipificación (para la evaluación del riesgo de cáncer) del HPV16 no debería basarse solo en ciertos genes, sino en todos los genes de todo el genoma. [115]
Una herramienta bioinformática llamada HPV16-Genotyper realiza i) genotipificación del linaje HPV16, ii) detecta posibles eventos de recombinación, iii) identifica, dentro de las secuencias enviadas, mutaciones/SNP que se ha informado (en la literatura) que aumentan el riesgo de cáncer. [115]
Proteínas E6/E7

Las dos oncoproteínas primarias de los tipos de VPH de alto riesgo son E6 y E7. La designación "E" indica que estas dos proteínas son proteínas tempranas (expresadas temprano en el ciclo de vida del VPH), mientras que la designación "L" indica que son proteínas tardías (expresión tardía). [52] El genoma del VPH está compuesto por seis marcos de lectura abiertos (ORF) tempranos (E1, E2, E4, E5, E6 y E7) , dos ORF tardíos (L1 y L2) y una región de control larga (LCR) no codificante. [119] Después de que la célula huésped se infecta, el promotor temprano viral se activa y se transcribe un ARN primario policistrónico que contiene los seis ORF tempranos. Este ARN policistrónico luego experimenta un empalme de ARN activo para generar múltiples isoformas de ARNm . [120] Uno de los ARN de isoforma empalmados, E6*I, sirve como ARNm E7 para traducir la proteína E7. [121] Sin embargo, la transcripción temprana viral está sujeta a la regulación de E2 viral y los niveles altos de E2 reprimen la transcripción. Los genomas del VPH se integran en el genoma del huésped mediante la interrupción del marco de lectura abierto de E2, lo que evita la represión de E2 en E6 y E7. Por lo tanto, la integración del genoma viral en el genoma del ADN del huésped aumenta la expresión de E6 y E7 para promover la proliferación celular y la posibilidad de malignidad. El grado en el que se expresan E6 y E7 se correlaciona con el tipo de lesión cervical que puede desarrollarse en última instancia. [109]
- Papel en el cáncer
A veces, los genomas del papilomavirus se encuentran integrados en el genoma del huésped, y esto es especialmente notable en los HPV oncogénicos. [122] Las proteínas E6/E7 inactivan dos proteínas supresoras de tumores, p53 (inactivada por E6) y pRb (inactivada por E7). [123] Se cree que los oncogenes virales E6 y E7 [124] modifican el ciclo celular para retener el queratinocito huésped diferenciador en un estado que es favorable para la amplificación de la replicación del genoma viral y la consiguiente expresión tardía del gen. E6 en asociación con la proteína asociada a E6 del huésped, que tiene actividad de ubiquitina ligasa, actúa para ubiquitinar p53, lo que lleva a su degradación proteosomal. E7 (en HPV oncogénicos) actúa como la proteína transformadora primaria. E7 compite por la unión de la proteína del retinoblastoma (pRb), liberando el factor de transcripción E2F para transactivar sus objetivos, impulsando así el ciclo celular hacia adelante. Todos los VPH pueden inducir una proliferación transitoria, pero solo las cepas 16 y 18 pueden inmortalizar líneas celulares in vitro . También se ha demostrado que los VPH 16 y 18 no pueden inmortalizar células primarias de rata por sí solos; es necesario que haya una activación del oncogén ras . En las capas superiores del epitelio del huésped, los genes tardíos L1 y L2 se transcriben/traducen y sirven como proteínas estructurales que encapsidan los genomas virales amplificados. Una vez que el genoma está encapsidado, la cápside parece experimentar un evento de ensamblaje/maduración dependiente de redox, que está ligado a un gradiente redox natural que abarca las capas de tejido epitelial suprabasal y cornificada. Este evento de ensamblaje/maduración estabiliza los viriones y aumenta su infectividad específica. [125] Luego, los viriones pueden desprenderse en las escamas muertas del epitelio del huésped y el ciclo de vida viral continúa. [126] Un estudio de 2010 descubrió que E6 y E7 están involucrados en la acumulación nuclear de beta-catenina y la activación de la señalización de Wnt en cánceres inducidos por VPH. [127]
Periodo de latencia
Una vez que un virión del VPH invade una célula, se produce una infección activa y el virus puede transmitirse. Pueden transcurrir varios meses o años antes de que se desarrollen lesiones intraepiteliales escamosas (SIL) y puedan detectarse clínicamente. El tiempo transcurrido entre la infección activa y la enfermedad clínicamente detectable puede dificultar que los epidemiólogos establezcan cuál de las parejas fue la fuente de infección. [106]
Autorización
La mayoría de las infecciones por VPH se curan en la mayoría de las personas sin necesidad de medidas médicas ni consecuencias. La tabla proporciona datos sobre los tipos de alto riesgo (es decir, los tipos que se encuentran en los cánceres). [ cita requerida ]
| Meses después de la prueba positiva inicial | 8 meses | 12 meses | 18 meses |
|---|---|---|---|
| % de hombres que dieron negativo | 70% | 80% | 100% |
La eliminación de una infección no siempre genera inmunidad si existe una fuente de infección nueva o continua. El estudio de Hernández de 2005-6 sobre 25 parejas informa que "varios casos indicaron una aparente reinfección [de la pareja] después de la eliminación del virus". [93]
Diagnóstico

Se han identificado más de 200 tipos de VPH, que se designan mediante números. [9] [8] [123] Se pueden dividir en tipos de "bajo riesgo" y "alto riesgo". Los tipos de bajo riesgo causan verrugas y los tipos de alto riesgo pueden causar lesiones o cáncer. [130] [131]
Pruebas cervicales
Las directrices de la Sociedad Estadounidense del Cáncer recomiendan diferentes estrategias de detección del cáncer de cuello uterino en función de la edad de la mujer, los antecedentes de detección, los factores de riesgo y la elección de las pruebas. [132] Debido a la relación entre el VPH y el cáncer de cuello uterino, la ACS actualmente recomienda la detección temprana del cáncer de cuello uterino en adultos asintomáticos de riesgo promedio principalmente con citología cervical mediante frotis de Papanicolaou, independientemente del estado de vacunación contra el VPH. Las mujeres de 30 a 65 años deben realizarse preferiblemente la prueba del VPH y la prueba de Papanicolaou cada 5 años. En otros grupos de edad, una prueba de Papanicolaou sola puede ser suficiente a menos que se les haya diagnosticado células escamosas atípicas de significado incierto (ASC-US). [133] Se recomienda la realización de pruebas conjuntas con una prueba de Papanicolaou y una prueba del VPH porque disminuye la tasa de falsos negativos. Según el Instituto Nacional del Cáncer, "la prueba más común detecta el ADN de varios tipos de VPH de alto riesgo, pero no puede identificar los tipos que están presentes. Otra prueba es específica para el ADN de los tipos de VPH 16 y 18, los dos tipos que causan la mayoría de los cánceres asociados al VPH. Una tercera prueba puede detectar el ADN de varios tipos de VPH de alto riesgo y puede indicar si está presente el VPH-16 o el VPH-18. Una cuarta prueba detecta el ARN de los tipos de VPH de alto riesgo más comunes. Estas pruebas pueden detectar infecciones por VPH antes de que las anomalías celulares sean evidentes. [ cita requerida ]
"En teoría, las pruebas de ADN y ARN del VPH podrían utilizarse para identificar infecciones por VPH en células extraídas de cualquier parte del cuerpo. Sin embargo, la FDA las ha aprobado sólo para dos indicaciones: para realizar pruebas de seguimiento a mujeres que parecen tener resultados anormales en la prueba de Papanicolaou y para la detección del cáncer de cuello uterino en combinación con una prueba de Papanicolaou en mujeres mayores de 30 años" . [134]
Prueba de boca
Las directrices para la detección del cáncer orofaríngeo del Grupo de Trabajo de Servicios Preventivos y la Asociación Dental Americana en los EE. UU. sugieren un examen visual convencional, pero debido a que algunas partes de la orofaringe son difíciles de ver, este cáncer a menudo solo se detecta en etapas más avanzadas. [64]
El diagnóstico del cáncer orofaríngeo se realiza mediante una biopsia de células o tejidos exfoliados. La National Comprehensive Cancer Network y el College of American Pathologists recomiendan realizar pruebas de detección del VPH en el cáncer orofaríngeo. [64] Sin embargo, aunque se recomienda realizar pruebas, no existe un tipo específico de prueba que se utilice para detectar el VPH en tumores orales que actualmente recomiende la FDA en los Estados Unidos. Debido a que el tipo 16 del VPH es el tipo más común que se encuentra en el cáncer orofaríngeo, la inmunohistoquímica p16 es una opción de prueba que se utiliza para determinar la presencia del VPH, [135] lo que puede ayudar a determinar el curso del tratamiento ya que los tumores que son negativos para p16 tienen mejores resultados. Otra opción que ha surgido como una opción confiable es la hibridación in situ (ISH) del ADN del VPH, que permite la visualización del VPH. [64]
Poniendo a prueba a los hombres
No hay una amplia gama de pruebas disponibles a pesar de que el VPH es común; la mayoría de los estudios sobre el VPH utilizaron herramientas y análisis personalizados que no están disponibles para el público en general. [136] [ necesita actualización ] Los médicos a menudo dependen de la vacuna entre los jóvenes y de las altas tasas de desaparición (ver la subsección de desaparición en Virología) para crear un bajo riesgo de enfermedad y mortalidad, y tratar los cánceres cuando aparecen. Otros creen que reducir la infección por VPH en más hombres y mujeres, incluso cuando no presenta síntomas, es importante (inmunidad de grupo) para prevenir más cánceres en lugar de simplemente tratarlos. [137] [138] [ necesita actualización ] Cuando se utilizan pruebas, los resultados negativos de las pruebas muestran seguridad frente a la transmisión, y los resultados positivos de las pruebas muestran dónde se necesita protección (condones, guantes) para prevenir la transmisión hasta que la infección desaparezca. [139]
Se han realizado estudios para detectar y detectar el VPH en hombres, incluidos los tipos de alto riesgo (es decir, los tipos que se encuentran en los cánceres), en los dedos, la boca, la saliva, el ano, la uretra, la orina, el semen, la sangre, el escroto y el pene. [136]
El kit Qiagen/Digene mencionado anteriormente se utilizó con éxito fuera de etiqueta para realizar pruebas en el pene, el escroto y el ano [140] de hombres que mantenían relaciones a largo plazo con mujeres que dieron positivo para el VPH de alto riesgo. Se descubrió que el 60 % de estos hombres eran portadores del virus, principalmente en el pene. [140] [ necesita actualización ] Se han realizado estudios similares en mujeres utilizando citocepillos (un cepillo endocervical para tomar muestras del cuello uterino en las mujeres) y análisis personalizados. [141] [142] [ necesita actualización ]
En un estudio, los investigadores tomaron muestras de la uretra, el escroto y el pene de los sujetos. [141] [142] [ necesita actualización ] Las muestras tomadas de la uretra agregaron menos del 1% a la tasa de VPH. Estudios como este llevaron a Giuliano a recomendar tomar muestras del glande, el cuerpo y el pliegue entre ellos, junto con el escroto, ya que tomar muestras de la uretra o el ano agregó muy poco al diagnóstico. [95] Dunne recomienda tomar muestras del glande, el cuerpo, su pliegue y el prepucio. [136]
En un estudio se pidió a los sujetos que no se lavaran los genitales durante 12 horas antes de la toma de la muestra, incluida la uretra, el escroto y el pene. [141] Otros estudios no mencionan el lavado, una laguna particular en los estudios sobre las manos. [ cita requerida ]
En un estudio pequeño se utilizaron cepillos citológicos húmedos en lugar de mojar la piel. [142] Se encontró que una mayor proporción de hombres eran positivos al VPH cuando se frotaba la piel con un papel de lija de grano 600 antes de frotarla con el cepillo, en lugar de frotarla sin preparación. No está claro si el papel de lija recogía los viriones o simplemente los aflojaba para que el hisopo los recogiera. [ cita requerida ]
Los estudios han demostrado que la autotoma de muestra (con papel de lija y hisopos de Dacron) es tan eficaz como la realizada por un médico y, a veces, más, ya que las pacientes estaban más dispuestas que un médico a raspar vigorosamente. [143] [ necesita actualización ] [144] Las mujeres tuvieron un éxito similar en la autotoma de muestra utilizando tampones, hisopos, cepillos citológicos y lavado. [145] [ necesita actualización ]
En varios estudios se utilizaron citocepillos para tomar muestras de las yemas de los dedos y debajo de las uñas, sin mojar el área ni el cepillo. [96] [101] [146] [ necesita actualización ]
Otros estudios analizaron orina, semen y sangre y encontraron cantidades variables de VPH, [136] pero aún no existe una prueba disponible públicamente para estos casos.
Otras pruebas
Aunque es posible realizar pruebas de ADN del VPH en otros tipos de infecciones, [136] no existen pruebas aprobadas por la FDA para la detección general en los Estados Unidos [147] ni pruebas aprobadas por el gobierno canadiense, [148] ya que las pruebas no son concluyentes y se consideran médicamente innecesarias. [149]
Las verrugas genitales son el único signo visible del VPH genital de bajo riesgo y se pueden identificar con una inspección visual. Sin embargo, estos crecimientos visibles son el resultado de tipos de VPH no cancerígenos. El ácido acético al cinco por ciento (vinagre) se utiliza para identificar tanto las verrugas como las lesiones de neoplasia intraepitelial escamosa (SIL) con un éxito limitado [ cita requerida ] al hacer que el tejido anormal parezca blanco, pero la mayoría de los médicos han encontrado que esta técnica es útil solo en áreas húmedas, como el tracto genital femenino. [ cita requerida ] En este momento, las pruebas de VPH para hombres se utilizan solo en investigación. [ cita requerida ]
Se han realizado investigaciones sobre la detección del VPH mediante la presencia de anticuerpos. El enfoque consiste en buscar una respuesta inmunitaria en la sangre, que contendría anticuerpos contra el VPH si el paciente es positivo. [150] [151] [152] [153] No se ha demostrado la fiabilidad de dichas pruebas, ya que hasta agosto de 2018 no había ningún producto aprobado por la FDA; [154] las pruebas en sangre serían una prueba menos invasiva para fines de detección.
Prevención
Las vacunas contra el VPH pueden prevenir los tipos más comunes de infección. [4] Para que sean eficaces, deben utilizarse antes de que se produzca la infección y, por lo tanto, se recomiendan entre los nueve y los trece años. Las pruebas de detección del cáncer de cuello uterino , como la prueba de Papanicolaou (pap) o la observación del cuello uterino después de utilizar ácido acético , pueden detectar el cáncer en etapa temprana o células anormales que pueden convertirse en cáncer. Esto permite un tratamiento temprano que produce mejores resultados. [1] Las pruebas de detección han reducido tanto el número como las muertes por cáncer de cuello uterino en el mundo desarrollado. [15] Las verrugas se pueden eliminar mediante congelación . [5]
Vacunas
Existen tres vacunas disponibles para prevenir la infección por algunos tipos de VPH: Gardasil , Gardasil 9 y Cervarix ; las tres protegen contra la infección inicial con los tipos de VPH 16 y 18, que causan la mayoría de los casos de cáncer asociados al VPH. Gardasil también protege contra los tipos de VPH 6 y 11, que causan el 90% de las verrugas genitales. Gardasil es una vacuna tetravalente recombinante, mientras que Cervarix es bivalente y se prepara a partir de partículas similares a virus (VLP) de la proteína de la cápside L1 . Gardasil 9 es nonavalente y tiene el potencial de prevenir alrededor del 90% de los cánceres de cuello uterino, vulvar, vaginal y anal. Puede proteger contra los tipos de VPH 6, 11, 16, 18, 31, 33, 45, 52 y 58; los últimos cinco causan hasta el 20% de los cánceres de cuello uterino que no estaban cubiertos anteriormente. [155]
Las vacunas aportan pocos beneficios a las mujeres que ya están infectadas con los tipos 16 y 18 del VPH. [156] Por este motivo, la vacuna se recomienda principalmente para aquellas mujeres que aún no han estado expuestas al VPH durante las relaciones sexuales. El documento de posición de la Organización Mundial de la Salud sobre la vacunación contra el VPH describe claramente las estrategias adecuadas y rentables para utilizar la vacuna contra el VPH en los programas del sector público. [157]
Hay evidencia de alta certeza de que las vacunas contra el VPH protegen contra lesiones precancerosas de cuello uterino en mujeres jóvenes, en particular aquellas vacunadas entre los 15 y los 26 años. [158] Las vacunas contra el VPH no aumentan el riesgo de eventos adversos graves. [158] Se necesita un seguimiento más prolongado para monitorear el impacto de las vacunas contra el VPH en el cáncer de cuello uterino. [158]
Los CDC recomiendan que las vacunas se administren en dos dosis con un intervalo de al menos 6 meses para las personas de 11 a 12 años, y en tres dosis para las mayores de 13 años. [159] En la mayoría de los países, están financiadas solo para uso femenino, pero están aprobadas para uso masculino en muchos países y financiadas para adolescentes varones en Australia. La vacuna no tiene ningún efecto terapéutico sobre las infecciones por VPH existentes o las lesiones cervicales. [160] En 2010, el 49% de las adolescentes en los EE. UU. recibieron la vacuna contra el VPH. [ cita requerida ]
A raíz de estudios que sugerían que la vacuna es más eficaz en niñas más jóvenes [161] que en adolescentes mayores, el Reino Unido, Suiza, México, los Países Bajos y Quebec comenzaron a ofrecer la vacuna en un esquema de dos dosis para niñas menores de 15 años en 2014. [ cita requerida ]
Las recomendaciones sobre la detección del cáncer de cuello uterino no han cambiado para las mujeres que reciben la vacuna contra el VPH. Sigue siendo una recomendación que las mujeres continúen realizándose pruebas de detección del cáncer de cuello uterino, como la prueba de Papanicolaou, incluso después de recibir la vacuna, ya que no previene todos los tipos de cáncer de cuello uterino. [160] [162]
Tanto los hombres como las mujeres son portadores del VPH. [163] La vacuna Gardasil también protege a los hombres contra el cáncer anal y las verrugas genitales. [164]
Se ha observado la duración de la eficacia de ambas vacunas desde que se desarrollaron por primera vez y se espera que sea duradera. [165]
En diciembre de 2014, la FDA aprobó una vacuna basada en Gardasil de nueve valencias, Gardasil 9, para proteger contra la infección con las cuatro cepas de VPH cubiertas por la primera generación de Gardasil, así como otras cinco cepas responsables del 20% de los cánceres de cuello uterino (VPH-31, VPH-33, VPH-45, VPH-52 y VPH-58). [166]
Condones
Los Centros para el Control y la Prevención de Enfermedades afirman que " el uso del condón masculino puede reducir el riesgo de infección genital por el virus del papiloma humano (VPH)", pero proporciona un menor grado de protección en comparación con otras infecciones de transmisión sexual "porque el VPH también puede transmitirse por exposición a áreas (por ejemplo, piel infectada o superficies mucosas) que no están cubiertas o protegidas por el condón". [167]
Desinfección
El virus es inusualmente resistente y es inmune a la mayoría de los desinfectantes comunes. Es el primer virus que se ha demostrado que es resistente a la inactivación por glutaraldehído , que se encuentra entre los desinfectantes fuertes más comunes utilizados en los hospitales. [168] El blanqueador de hipoclorito de sodio diluido es eficaz, [168] pero no se puede utilizar en algunos tipos de equipos reutilizables, como los transductores de ultrasonido. [87] Como resultado de estas dificultades, existe una creciente preocupación sobre la posibilidad de transmitir el virus en el equipo de atención médica, en particular el equipo ginecológico reutilizable que no se puede esterilizar en autoclave . [169] [170] Para este tipo de equipo, algunas autoridades sanitarias fomentan el uso de desinfección UV [171] o un "desinfectante de alto nivel [blanqueador] a base de oxidantes sin hipoclorito con afirmaciones en la etiqueta para virus sin envoltura", [172] como una solución fuerte de peróxido de hidrógeno [173] [171] o toallitas de dióxido de cloro . [171] Se espera que estos métodos de desinfección sean relativamente eficaces contra el VPH. [ cita requerida ]
Gestión
Actualmente no existe un tratamiento específico para la infección por VPH. [174] [175] [176] Sin embargo, el sistema inmunológico suele eliminar la infección viral a niveles indetectables. [177] Según los Centros para el Control y la Prevención de Enfermedades , el sistema inmunológico del cuerpo elimina el VPH de forma natural en un plazo de dos años en el 90 % de los casos (consulte la subsección Eliminación en Virología para obtener más detalles). [174] Sin embargo, los expertos no se ponen de acuerdo sobre si el virus se elimina o se reduce a niveles indetectables, y es difícil saber cuándo es contagioso. [178] [ necesita actualización ]
En muchos centros de salud se recomienda y practica el seguimiento. [179] A veces, el seguimiento no es exitoso porque una parte de los pacientes tratados no regresan para ser evaluados. Además de los métodos habituales de llamadas telefónicas y correo postal, los mensajes de texto y el correo electrónico pueden mejorar la cantidad de personas que regresan para recibir atención. [180] A partir de 2015, no está claro cuál es el mejor método de seguimiento después del tratamiento de la neoplasia intraepitelial cervical . [181]
Epidemiología
A nivel mundial, el 12% de las mujeres son positivas para el ADN del VPH, con tasas que varían según la edad y el país. [182] Las tasas más altas de VPH se dan en mujeres más jóvenes, con una tasa del 24% en mujeres menores de 25 años. [183] Las tasas disminuyen en los grupos de mayor edad en Europa y las Américas, pero menos en África y Asia. Las tasas son más altas en África subsahariana (24%) y Europa del Este (21%) y más bajas en América del Norte (5%) y Asia Occidental (2%). [182]
Los tipos más comunes de VPH en todo el mundo son el VPH16 (3,2%), el VPH18 (1,4%), el VPH52 (0,9%), el VPH31 (0,8%) y el VPH58 (0,7%). Los tipos de VPH de alto riesgo también se distribuyen de manera desigual: el VPH16 tiene una tasa de alrededor del 13% en África y del 30% en Asia occidental y central. [183]
Al igual que muchas enfermedades, el VPH afecta desproporcionadamente a los países de bajos ingresos y pobres en recursos. Las tasas más altas de VPH en África subsahariana, por ejemplo, pueden estar relacionadas con la alta exposición al virus de inmunodeficiencia humana (VIH) en la región. Otros factores que influyen en la propagación mundial de la enfermedad son los comportamientos sexuales, incluida la edad de inicio de las relaciones sexuales, el número de parejas sexuales y la facilidad de acceso a los métodos anticonceptivos de barrera, todos los cuales varían a nivel mundial. [182] [184]
Estados Unidos
| Edad (años) | Prevalencia (%) |
|---|---|
| 14 a 19 | 24,5% |
| 20 a 24 | 44,8% |
| 25 a 29 | 27,4% |
| 30 a 39 | 27,5% |
| 40 a 49 | 25,2% |
| 50 a 59 | 19,6% |
| 14 a 59 | 26,8% |
Se estima que el VPH es la infección de transmisión sexual más común en los Estados Unidos. [185] La mayoría de los hombres y mujeres sexualmente activos probablemente adquirirán la infección genital por VPH en algún momento de sus vidas. [21] La Asociación Estadounidense de Salud Social estima que alrededor del 75 al 80% de los estadounidenses sexualmente activos se infectarán con VPH en algún momento de su vida. [186] [187] A la edad de 50 años, más del 80% de las mujeres estadounidenses habrán contraído al menos una cepa de VPH genital. [185] [188] Se estimó que, en el año 2000, hubo aproximadamente 6,2 millones de nuevas infecciones por VPH entre los estadounidenses de 15 a 44 años; de estas, aproximadamente el 74% se produjo en personas de entre 15 y 24 años. [189] De las ITS estudiadas, el VPH genital fue la más comúnmente adquirida. [189] En los Estados Unidos, se estima que el 10% de la población tiene una infección activa por VPH, el 4% tiene una infección que ha causado anomalías citológicas y un 1% adicional tiene una infección que causa verrugas genitales. [190]
Las estimaciones de prevalencia del VPH varían entre el 14% y más del 90%. [191] Una razón para la diferencia es que algunos estudios informan sobre mujeres que actualmente tienen una infección detectable, mientras que otros estudios informan sobre mujeres que alguna vez tuvieron una infección detectable. [192] [193] Otra causa de discrepancia es la diferencia en las cepas que se analizaron. [ cita requerida ]
Un estudio reveló que, durante el período 2003-2004, en un momento dado , el 26,8% de las mujeres de 14 a 59 años estaban infectadas con al menos un tipo de VPH. Esta cifra es superior a las estimaciones anteriores: el 15,2% estaban infectadas con uno o más de los tipos de alto riesgo que pueden causar cáncer. [185] [194]
La prevalencia de los tipos de alto y bajo riesgo es aproximadamente similar a lo largo del tiempo. [185]
El virus del papiloma humano no está incluido entre las enfermedades que normalmente se deben notificar a los CDC a partir de 2011. [195] [196]
Irlanda
En promedio, se diagnosticaron 538 casos de cánceres asociados al VPH por año en Irlanda durante el período de 2010 a 2014. [197] El cáncer de cuello uterino fue el cáncer asociado al VPH más frecuente con un promedio de 292 casos por año (74% del total femenino y 54% del total general de cánceres asociados al VPH). [197] Un estudio de 996 muestras de citología cervical en una población femenina urbana irlandesa, examinada de manera oportunista, encontró una prevalencia general del VPH del 19,8%, el VPH 16 en el 20% y el VPH 18 en el 12% fueron los tipos de alto riesgo detectados más comunes. En Europa, los tipos 16 y 18 son responsables de más del 70% de los cánceres de cuello uterino. [198] Las tasas generales de cánceres invasivos asociados al VPH pueden estar aumentando. Entre 1994 y 2014, hubo un aumento del 2% en la tasa de cánceres invasivos asociados al VPH por año para ambos sexos en Irlanda. [197]
Como se sabe que el VPH está asociado con las verrugas anogenitales, estas deben notificarse al Centro de Vigilancia de Protección de la Salud (HPSC). Las verrugas genitales son la segunda ETS más común en Irlanda. [199] En 2017 se notificaron 1281 casos de verrugas anogenitales, lo que representó una disminución con respecto a la cifra de 2016 de 1593. [200] La tasa específica por edad más alta, tanto para hombres como para mujeres, se registró en el rango de edad de 25 a 29 años; el 53 % de los casos se dieron en hombres. [200]
Sri Lanka
En Sri Lanka, la prevalencia del VPH es del 15,5% independientemente de sus anomalías citológicas. [201]
Mongolia interior
En la Región Autónoma de Mongolia Interior, la prevalencia general del VPH es del 14,5%, pero muestra una disparidad étnica sustancial; la prevalencia en las mujeres mongolas (14,9%) es mucho mayor que la de las participantes Han (4,3%). [202] La urbanización, el número de parejas sexuales y el historial de PAP aparecen como factores de riesgo para la infección por VPH en las mujeres Han, pero no en las mujeres mongolas. Por lo tanto, la región es un ejemplo importante de que la epidemiología del VPH está más relacionada con factores culturales y étnicos y no con la geografía en sí. [ cita requerida ]
Historia
En 1972, Stefania Jabłońska propuso en Polonia la asociación de los virus del papiloma humano con el cáncer de piel en la epidermodisplasia verruciforme . En 1976, Harald zur Hausen publicó la hipótesis de que el virus del papiloma humano desempeña un papel importante en la causa del cáncer de cuello uterino . En 1978, Jabłońska y Gerard Orth en el Instituto Pasteur descubrieron el VPH-5 en el cáncer de piel . [203] En 1983 y 1984, zur Hausen y sus colaboradores identificaron el VPH16 y el VPH18 en el cáncer de cuello uterino. [204]
La línea celular HeLa contiene ADN adicional en su genoma que se originó a partir del VPH tipo 18. [205]
Investigación
La cohorte Ludwig-McGill HPV es uno de los estudios longitudinales más grandes del mundo sobre la historia natural de la infección por el virus del papiloma humano (VPH) y el riesgo de cáncer de cuello uterino . Fue establecida en 1993 por Ludwig Cancer Research y la Universidad McGill en Montreal, Canadá. [206]
Referencias
- ^ abcdefghijklmnopqrst «Virus del papiloma humano (VPH) y cáncer de cuello uterino - OMS». Organización Mundial de la Salud . 22 de febrero de 2022. Archivado desde el original el 22 de abril de 2023.
- ^ abcde Ljubojevic S, Skerlev M (2014). "Enfermedades asociadas al VPH". Clinics in Dermatology . 32 (2): 227–34. doi :10.1016/j.clindermatol.2013.08.007. PMID 24559558.
- ^ abcdef Anjum, Fatima; Zohaib, Jamal (4 de diciembre de 2020). "Carcinoma de células escamosas orofaríngeo". Definiciones (edición actualizada). Treasure Island (FL): StatPearls Publishing. doi :10.32388/G6TG1L. PMID 33085415. S2CID 229252540. Bookshelf ID: NBK563268 . Consultado el 6 de febrero de 2021 a través de NCBI .
- ^ abcdefghij "¿Qué es el VPH?". Centros para el Control y la Prevención de Enfermedades . 28 de diciembre de 2015. Archivado desde el original el 7 de agosto de 2016. Consultado el 10 de agosto de 2016 .
- ^ abcdef Milner DA (2015). Patología diagnóstica: enfermedades infecciosas. Elsevier Health Sciences. pág. 40. ISBN 978-0-323-40037-4Archivado desde el original el 11 de septiembre de 2017.
- ^ "Hoja informativa para el personal de salud pública | Eficacia del preservativo | CDC". Centros para el Control y la Prevención de Enfermedades . 25 de marzo de 2013. Archivado desde el original el 27 de mayo de 2017. Consultado el 1 de mayo de 2017 .
- ^ abc «El vínculo entre el VPH y el cáncer». Centros para el Control y la Prevención de Enfermedades . 30 de septiembre de 2015. Archivado desde el original el 9 de noviembre de 2015. Consultado el 11 de agosto de 2016 .
- ^ ab Bzhalava D, Guan P, Franceschi S, Dillner J, Clifford G (octubre de 2013). "Una revisión sistemática de la prevalencia de los tipos de virus del papiloma humano mucosos y cutáneos". Virology . 445 (1–2): 224–31. doi : 10.1016/j.virol.2013.07.015 . PMID 23928291.
- ^ abcdefgh «El VPH y el cáncer - Instituto Nacional del Cáncer». Instituto Nacional del Cáncer . 18 de octubre de 2023 . Consultado el 18 de enero de 2024 .
- ^ abc «Preguntas y respuestas sobre el virus del papiloma humano (VPH)». Centros para el Control y la Prevención de Enfermedades . 28 de diciembre de 2015. Archivado desde el original el 11 de agosto de 2016. Consultado el 11 de agosto de 2016 .
- ^ "Libro rosa (virus del papiloma humano)" (PDF) . Centros para el Control y la Prevención de Enfermedades . Archivado (PDF) del original el 21 de marzo de 2017 . Consultado el 18 de abril de 2017 .
- ^ "Cinco cosas que quizás no sepas sobre el virus del papiloma humano". Centros para el Control y la Prevención de Enfermedades . 20 de enero de 2016. Consultado el 22 de mayo de 2020 .
- ^ "Virus del papiloma humano (VPH)" (PDF) . WRHA . 18 de noviembre de 2019 . Consultado el 26 de marzo de 2019 .
- ^ Meyers J, Ryndock E, Conway MJ, Meyers C, Robison R (junio de 2014). "Susceptibilidad del virus del papiloma humano de alto riesgo tipo 16 a los desinfectantes clínicos". J Antimicrob Chemother . 69 (6): 1546–50. doi :10.1093/jac/dku006. PMC 4019329 . PMID 24500190.
- ^ ab Sawaya GF, Kulasingam S, Denberg TD, Qaseem A (junio de 2015). "Examen de detección del cáncer de cuello uterino en mujeres con riesgo promedio: recomendaciones de mejores prácticas del Comité de pautas clínicas del Colegio Estadounidense de Médicos". Anales de Medicina Interna . 162 (12): 851–9. doi : 10.7326/M14-2426 . PMID 25928075. S2CID 25957804.
- ^ abc Tyring S, Moore AY, Lupi O (2016). Manifestaciones mucocutáneas de enfermedades virales: una guía ilustrada para el diagnóstico y el tratamiento (2.ª ed.). CRC Press. pág. 207. ISBN 978-1-4200-7313-3.
- ^ M Al Aboud A, Nigam PK (2022). "Verruga (plantar, verruga vulgar, verrugas)". Stat Pearls. PMID 28613701. Consultado el 4 de diciembre de 2019 .
- ^ ab Muñoz N, Bosch FX, de Sanjosé S, Herrero R, Castellsagué X, Shah KV, et al. (Grupo de estudio multicéntrico sobre cáncer de cuello uterino de la Agencia Internacional para la Investigación del Cáncer) (febrero de 2003). "Clasificación epidemiológica de los tipos de virus del papiloma humano asociados con el cáncer de cuello uterino". The New England Journal of Medicine . 348 (6): 518–27. doi :10.1056/NEJMoa021641. hdl : 2445/122831 . PMID 12571259. S2CID 1451343.
- ^ abc Pahud BA, Ault KA (diciembre de 2015). "El impacto ampliado de la vacuna contra el virus del papiloma humano". Clínicas de enfermedades infecciosas de Norteamérica (revisión). 29 (4): 715–24. doi :10.1016/j.idc.2015.07.007. PMID 26610422.
- ^ Nowińska K, Ciesielska U, Podhorska-Okołów M, Dzięgiel P (2017). "El papel del virus del papiloma humano en la transformación oncogénica y su contribución a la etiología de las lesiones precancerosas y el cáncer de laringe: una revisión". Avances en medicina clínica y experimental . 26 (3): 539–547. doi : 10.17219/acem/67461 . PMID 28791831.
- ^ abc Baseman JG, Koutsky LA (marzo de 2005). "La epidemiología de las infecciones por el virus del papiloma humano". Journal of Clinical Virology . 32 (Suppl 1): S16-24. doi :10.1016/j.jcv.2004.12.008. PMID 15753008.
En general, estos estudios basados en el ADN, combinados con mediciones de anticuerpos específicos de tipo contra antígenos de la cápside del VPH, han demostrado que la mayoría (>50%) de las mujeres sexualmente activas han sido infectadas por uno o más tipos genitales del VPH en algún momento [S17].
- ^ Noel J, Lespagnard L, Fayt I, Verhest A, Dargent J (enero de 2001). "Evidencia de infección por virus del papiloma humano pero ausencia de virus de Epstein-Barr en carcinoma de cuello uterino similar al linfoepitelioma: informe de dos casos y revisión de la literatura". Patología humana . 32 (1): 135–8. doi :10.1053/hupa.2001.20901. PMID 11172309.
- ^ "Neoplasia intraepitelial vulvar: signos y síntomas variados: lo que necesita saber". www.advanceweb.com. Archivado desde el original el 16 de julio de 2012. Consultado el 5 de agosto de 2009 .
- ^ abc Kumar V, Abbas AK, Fausto N, Mitchell R (2007). "Capítulo 19 El sistema genital femenino y la mama". Robbins Basic Pathology (8.ª ed.). Filadelfia: Saunders. ISBN 978-1-4160-2973-1.
- ^ Palefsky JM, Holly EA, Ralston ML, Jay N (febrero de 1998). "Prevalencia y factores de riesgo de la infección por el virus del papiloma humano del canal anal en hombres homosexuales VIH-positivos y VIH-negativos". The Journal of Infectious Diseases . 177 (2): 361–7. doi : 10.1086/514194 . PMID 9466522.
- ^ Muñoz N, Castellsagué X, de González AB, Gissmann L (agosto de 2006). "Capítulo 1: VPH en la etiología del cáncer humano". Vaccine . 24 Suppl 3 (3): S3/1–10. doi :10.1016/j.vaccine.2006.05.115. PMID 16949995.
- ^ abc Organización Mundial de la Salud (diciembre de 2022). «Vacunas contra el virus del papiloma humano: documento de posición de la OMS (actualización de 2022)». Weekly Epidemiological Record . 97 (50): 645–672. hdl : 10665/365351 .
- ^ Antonsson A, Forslund O, Ekberg H, Sterner G, Hansson BG (diciembre de 2000). "La ubicuidad y la impresionante diversidad genómica de los virus del papiloma de la piel humana sugieren una naturaleza comensálica de estos virus". Revista de Virología . 74 (24): 11636–41. doi :10.1128/JVI.74.24.11636-11641.2000. PMC 112445 . PMID 11090162.
- ^ Mayo Clinic.com, Verrugas comunes, http://www.mayoclinic.com/print/common-warts/DS00370/ Archivado el 17 de octubre de 2011 en Wayback Machine.
- ^ Al Aboud, Ahmad M.; Nigam, Pramod K. (11 de agosto de 2020). "Verruga". StatPearls. Treasure Island (Florida): StatPearls Publishing. PMID 28613701.
- ^ Lountzis NI, Rahman O (julio de 2008). "Imágenes en medicina clínica. Verrugas digitales". The New England Journal of Medicine . 359 (2): 177. doi :10.1056/NEJMicm071912. PMID 18614785.
- ^ MedlinePlus, Verrugas, https://www.nlm.nih.gov/medlineplus/warts.html#cat42 Archivado el 5 de junio de 2016 en Wayback Machine (referencia general con enlaces). Consulte también
- ^ ab Informe mundial sobre el cáncer 2014. Organización Mundial de la Salud. 2014. pp. Capítulo 5.12. ISBN 978-92-832-0429-9.
- ^ Greer CE, Wheeler CM, Ladner MB, Beutner K, Coyne MY, Liang H, et al. (agosto de 1995). "Distribución de tipos de virus del papiloma humano (VPH) y respuesta serológica a partículas similares al virus del VPH tipo 6 en pacientes con verrugas genitales". Journal of Clinical Microbiology . 33 (8): 2058–63. doi :10.1128/jcm.33.8.2058-2063.1995. PMC 228335 . PMID 7559948.
- ^ ab "Virus del papiloma humano". Medscape . 16 de octubre de 2018. Archivado desde el original el 29 de noviembre de 2016.
- ^ "Fotografías de papilomas de laringe — Voice Medicine, Nueva York". Voicemedicine.com. Archivado desde el original el 12 de junio de 2010. Consultado el 29 de agosto de 2010 .
- ^ abcd Sinal SH, Woods CR (octubre de 2005). "Infecciones por virus del papiloma humano de los tractos genital y respiratorio en niños pequeños". Seminarios sobre enfermedades infecciosas pediátricas . 16 (4): 306–16. doi :10.1053/j.spid.2005.06.010. PMID 16210110.
- ^ Wu R, Sun S, Steinberg BM (2003). "Requisito de activación de STAT3 para la diferenciación del epitelio escamoso estratificado de la mucosa". Molecular Medicine . 9 (3–4): 77–84. doi :10.2119/2003-00001.Wu. PMC 1430729 . PMID 12865943.
- ^ Moore CE, Wiatrak BJ, McClatchey KD, Koopmann CF, Thomas GR, Bradford CR, Carey TE (mayo de 1999). "Tipos de virus del papiloma humano de alto riesgo y carcinoma de células escamosas en pacientes con papilomas respiratorios". Otorrinolaringología–Cirugía de cabeza y cuello . 120 (5): 698–705. doi :10.1053/hn.1999.v120.a91773. PMID 10229596. S2CID 6560398.
- ^ abc Viens LJ, Henley SJ, Watson M, Markowitz LE, Thomas CC, Thompson TD, et al. (julio de 2016). "Cánceres asociados al virus del papiloma humano: Estados Unidos, 2008-2012". MMWR. Informe semanal de morbilidad y mortalidad . 65 (26): 661–6. doi : 10.15585/mmwr.mm6526a1 . PMID 27387669.
- ^ Schiffman M, Castle PE (noviembre de 2005). "La promesa de la prevención mundial del cáncer de cuello uterino". The New England Journal of Medicine . 353 (20): 2101–4. doi : 10.1056/NEJMp058171 . PMID 16291978.
- ^ Alam S, Conway MJ, Chen HS, Meyers C (enero de 2008). "El carcinógeno del humo del cigarrillo benzo[a]pireno mejora la síntesis del virus del papiloma humano". Journal of Virology . 82 (2): 1053–8. doi :10.1128/JVI.01813-07. PMC 2224590 . PMID 17989183.
- ^ Lu B, Hagensee ME, Lee JH, Wu Y, Stockwell HG, Nielson CM, et al. (febrero de 2010). "Factores epidemiológicos asociados con la seropositividad a las partículas similares al virus del papiloma humano tipo 16 y 18 y riesgo de infección posterior en hombres". Epidemiología del cáncer, biomarcadores y prevención . 19 (2): 511–6. doi : 10.1158/1055-9965.EPI-09-0790 . PMID 20086109. S2CID 22440577.
- ^ Parfenov M, Pedamallu CS, Gehlenborg N, Freeman SS, Danilova L, Bristow CA, et al. (octubre de 2014). "Caracterización de las interacciones entre el VPH y el genoma del huésped en cánceres primarios de cabeza y cuello". Actas de la Academia Nacional de Ciencias de los Estados Unidos de América . 111 (43): 15544–9. Bibcode :2014PNAS..11115544P. doi : 10.1073/pnas.1416074111 . PMC 4217452 . PMID 25313082.
- ^ Scheffner, Martin; Huibregtse, Jon M.; Vierstra, Richard D.; Howley, Peter M. (noviembre de 1993). "El complejo E6 y E6-AP de HPV-16 funciona como una proteína ligasa de ubiquitina en la ubiquitinación de p53". Cell . 75 (3): 495–505. doi :10.1016/0092-8674(93)90384-3. PMID 8221889. S2CID 27437768.
- ^ Zanier, Katia; Charbonnier, Sebastián; Sidi, Abdellahi Ould M'hamed Ould; McEwen, Alastair G.; Ferrario, María Giovanna; Poussin-Courmontagne, Pierre; Cura, Vicente; Brimer, Nicole; Babah, Khaled Ould; Ansari, Tina; Muller, Isabelle (8 de febrero de 2013). "Base estructural para el secuestro de motivos celulares LxxLL por oncoproteínas del virus del papiloma E6". Ciencia . 339 (6120): 694–698. Código Bib : 2013 Ciencia... 339..694Z. doi : 10.1126/ciencia.1229934. ISSN 1095-9203. PMC 3899395 . PMID 23393263.
- ^ Hafner, Antonina; Bulyk, Martha L.; Jambhekar, Ashwini; Lahav, Galit (abril de 2019). "Los múltiples mecanismos que regulan la actividad de p53 y el destino celular". Nature Reviews. Biología celular molecular . 20 (4): 199–210. doi :10.1038/s41580-019-0110-x. ISSN 1471-0080. PMID 30824861. S2CID 71143679.
- ^ Hanahan, Douglas; Weinberg, Robert A. (7 de enero de 2000). "Las características del cáncer". Cell . 100 (1): 57–70. doi : 10.1016/S0092-8674(00)81683-9 . ISSN 0092-8674. PMID 10647931. S2CID 1478778.
- ^ Tungteakkhun, Sandy S.; Duerksen-Hughes, Penelope J. (2008). "Socios de unión celular de la proteína E6 del virus del papiloma humano". Archivos de Virología . 153 (3): 397–408. doi :10.1007/s00705-007-0022-5. ISSN 0304-8608. PMC 2249614 . PMID 18172569.
- ^ Karagas MR, Waterboer T, Li Z, Nelson HH, Michael KM, Bavinck JN, et al. (julio de 2010). "Virus del papiloma humano del género beta e incidencia de carcinomas de células basales y de células escamosas de la piel: estudio de casos y controles basado en la población". BMJ . 341 : c2986. doi :10.1136/bmj.c2986. PMC 2900549 . PMID 20616098.
- ^ Cohen J (abril de 2005). "Salud pública. Grandes esperanzas y dilemas para una vacuna contra el cáncer de cuello uterino". Science . 308 (5722): 618–21. doi :10.1126/science.308.5722.618. PMID 15860602. S2CID 31712160.
- ^ abc Ault KA (2006). "Epidemiología e historia natural de las infecciones por el virus del papiloma humano en el tracto genital femenino". Enfermedades infecciosas en obstetricia y ginecología . 2006 Suppl: 40470. doi : 10.1155/IDOG/2006/40470 . PMC 1581465. PMID 16967912 .
- ^ Kreimer AR, Clifford GM, Boyle P, Franceschi S (febrero de 2005). "Tipos de virus del papiloma humano en carcinomas de células escamosas de cabeza y cuello en todo el mundo: una revisión sistemática". Epidemiología del cáncer, biomarcadores y prevención . 14 (2): 467–75. doi : 10.1158/1055-9965.EPI-04-0551 . PMID 15734974. S2CID 6643303.
- ^ Arbyn, Tommasino, Depuydt, Dillner (15 de agosto de 2014). "¿Hay 20 tipos de virus del papiloma humano que causan cáncer de cuello uterino?". The Journal of Pathology . 234 (4): 431–435. doi : 10.1002/path.4424 . PMID 25124771. S2CID 7775411.
- ^ Berrington de González A, Green J, et al. (Colaboración Internacional de Estudios Epidemiológicos del Cáncer Cervical) (febrero de 2007). "Comparación de los factores de riesgo para el carcinoma de células escamosas invasivo y el adenocarcinoma de cuello uterino: reanálisis colaborativo de datos individuales sobre 8.097 mujeres con carcinoma de células escamosas y 1.374 mujeres con adenocarcinoma de 12 estudios epidemiológicos". Revista Internacional del Cáncer . 120 (4): 885–91. doi : 10.1002/ijc.22357 . PMID 17131323. S2CID 33495556.
- ^ Denny LA, Franceschi S, de Sanjosé S, Heard I, Moscicki AB, Palefsky J (noviembre de 2012). «Virus del papiloma humano, virus de inmunodeficiencia humana e inmunosupresión». Vacuna . 30 (Supl 5): F168-74. doi :10.1016/j.vaccine.2012.06.045. PMID 23199960. Archivado desde el original el 8 de noviembre de 2019 . Consultado el 28 de noviembre de 2019 .
- ^ Dugué PA, Rebolj M, Garred P, Lynge E (enero de 2013). "Inmunosupresión y riesgo de cáncer de cuello uterino". Revisión experta de terapias contra el cáncer . 13 (1): 29–42. doi :10.1586/era.12.159. PMID 23259425. S2CID 26312718.
- ^ Willemsen, Anouk; Bravo, Ignacio G. (27 de septiembre de 2018). "Origen y evolución de los (onco)genes y genomas del virus del papiloma". Philosophical Transactions of the Royal Society of London. Serie B, Ciencias Biológicas . 374 (1773). bioRxiv 10.1101/428912 . doi :10.1098/rstb.2018.0303. PMC 6501903 . PMID 30955499.
- ^ Doorbar, John; Quint, Wim; Banks, Lawrence; Bravo, Ignacio G.; Stoler, Mark; Broker, Tom R.; Stanley, Margaret A. (noviembre de 2012). "La biología y el ciclo de vida de los virus del papiloma humano". Vacuna . 30 : F55–F70. doi : 10.1016/j.vaccine.2012.06.083 . ISSN 0264-410X. PMID 23199966.
- ^ Gagliardi, Alessia; Porter, Vanessa L.; Zong, Zusheng; Bowlby, Reanne; Titmuss, Emma; Namirembe, Constance; Griner, Nicholas B.; Petrello, Hilary; Bowen, Jay; Chan, Simon K.; Culibrk, Luka (agosto de 2020). "El análisis de carcinomas cervicales de Uganda identifica paisajes epigenómicos y transcriptómicos específicos del clado del virus del papiloma humano". Nature Genetics . 52 (8): 800–810. doi :10.1038/s41588-020-0673-7. ISSN 1061-4036. PMC 7498180 . PMID 32747824.
- ^ Greenblatt RJ (2005). "Virus del papiloma humano: enfermedades, diagnóstico y una posible vacuna". Boletín de microbiología clínica . 27 (18): 139–145. doi :10.1016/j.clinmicnews.2005.09.001.
- ^ Abudula, Abulizi; Rouzi, Nuermanguli; Xu, Lixiu; Yang, Yun; Hasimu, Axiangu (2019). "La metabolómica basada en tejidos revela posibles biomarcadores para el carcinoma cervical y la infección por VPH". Revista bosnia de ciencias médicas básicas . 20 (1): 78–87. doi : 10.17305/bjbms.2019.4359 . PMC 7029203 . PMID 31465717.
- ^ Freitas LB, Chen Z, Muqui EF, Boldrini NA, Miranda AE, Spano LC, Burk RD (1 de julio de 2014). "Las variantes no europeas del virus del papiloma humano 16 se asocian preferentemente con lesiones cervicales de alto grado". PLOS ONE . 9 (7): e100746. Bibcode :2014PLoSO...9j0746F. doi : 10.1371/journal.pone.0100746 . PMC 4077691 . PMID 24983739.
- ^ abcde Burd EM, Dean CL (agosto de 2016). Hayden RT, Wolk DM, Carroll KC, Tang YC (eds.). "Virus del papiloma humano". Microbiology Spectrum . Microbiología diagnóstica del huésped inmunocomprometido. 4 (4) (Segunda ed.). Sociedad Estadounidense de Microbiología: 177–195. doi : 10.1128/microbiolspec.dmih2-0001-2015 . ISBN 978-1-55581-903-3Número de identificación personal 27726787 .
- ^ Chin-Hong PV, Vittinghoff E, Cranston RD, Browne L, Buchbinder S, Colfax G, et al. (junio de 2005). "Prevalencia relacionada con la edad de precursores de cáncer anal en hombres homosexuales: el estudio EXPLORE". Revista del Instituto Nacional del Cáncer . 97 (12): 896–905. doi : 10.1093/jnci/dji163 . PMID 15956651.
- ^ "Exclusivas web de AIDSmeds: ¿Pruebas de Papanicolaou para el cáncer anal? — por David Evans". AIDSmeds.com. 10 de junio de 2008. Archivado desde el original el 7 de julio de 2011. Consultado el 29 de agosto de 2010 .
- ^ Goldie SJ, Kuntz KM, Weinstein MC, Freedberg KA, Palefsky JM (junio de 2000). "Relación coste-efectividad de la detección de lesiones intraepiteliales escamosas anales y cáncer anal en hombres homosexuales y bisexuales negativos al virus de la inmunodeficiencia humana". The American Journal of Medicine . 108 (8): 634–41. doi :10.1016/S0002-9343(00)00349-1. PMID 10856411.
- ^ ab Elizabeth A. Van Dyne; S. Jane Henley; Mona Saraiya; Cheryll C. Thomas; Lauri E. Markowitz; Vicki B. Benard (24 de agosto de 2018). "Tendencias en los cánceres asociados al virus del papiloma humano: Estados Unidos, 1999-2015" (PDF) . Informe semanal de morbilidad y mortalidad . Vol. 67, núm. 33.
- ^ ab D'Souza G, Kreimer AR, Viscidi R, Pawlita M, Fakhry C, Koch WM, et al. (mayo de 2007). "Estudio de casos y controles del virus del papiloma humano y cáncer de orofaringe". La Revista de Medicina de Nueva Inglaterra . 356 (19): 1944–56. doi : 10.1056/NEJMoa065497 . PMID 17494927. S2CID 18819678.
- ^ ab Ridge JA, Glisson BS, Lango MN, et al. "Head and Neck Tumors" Archivado el 20 de julio de 2009 en Wayback Machine en Pazdur R, Wagman LD, Camphausen KA, Hoskins WJ (Eds) Cancer Management: A Multidisciplinary Approach Archivado el 4 de octubre de 2013 en Wayback Machine . 11.ª ed. 2008.
- ^ Gillison ML, Koch WM, Capone RB, Spafford M, Westra WH, Wu L, et al. (mayo de 2000). "Evidencia de una asociación causal entre el virus del papiloma humano y un subconjunto de cánceres de cabeza y cuello". Revista del Instituto Nacional del Cáncer . 92 (9): 709–20. doi : 10.1093/jnci/92.9.709 . PMID 10793107.
- ^ Gillison ML (diciembre de 2006). "Virus del papiloma humano y pronóstico del carcinoma de células escamosas orofaríngeo: implicaciones para la investigación clínica en cánceres de cabeza y cuello". Journal of Clinical Oncology . 24 (36): 5623–5. doi : 10.1200/JCO.2006.07.1829 . PMID 17179099. S2CID 32491893.
- ^ Saraiya M, Unger ER, Thompson TD, Lynch CF, Hernandez BY, Lyu CW, et al. (junio de 2015). "Evaluación estadounidense de los tipos de VPH en cánceres: implicaciones para las vacunas contra el VPH actuales y nonavalentes". Journal of the National Cancer Institute . 107 (6): djv086. doi :10.1093/jnci/djv086. PMC 4838063 . PMID 25925419.
- ^ Anantharaman D, Abedi-Ardekani B, Beachler DC, Gheit T, Olshan AF, Wisniewski K, et al. (mayo de 2017). "Heterogeneidad geográfica en la prevalencia del virus del papiloma humano en el cáncer de cabeza y cuello". Revista internacional del cáncer . 140 (9): 1968–1975. doi :10.1002/ijc.30608. hdl : 2318/1634649 . PMC 8969079 . PMID 28108990. S2CID 34198821.
- ^ Chaturvedi AK, Engels EA, Pfeiffer RM, Hernandez BY, Xiao W, Kim E, et al. (noviembre de 2011). "Virus del papiloma humano y aumento de la incidencia del cáncer orofaríngeo en los Estados Unidos". Journal of Clinical Oncology . 29 (32): 4294–301. doi :10.1200/JCO.2011.36.4596. PMC 3221528 . PMID 21969503.
- ^ Drake, Virginia; Fakhry, Carole; Windon, Melina J.; Stewart, C. Matthew; Akst, Lee; Hillel, Alexander; Chien, Wade; Ha, Patrick; Miles, Brett; Gourin, Christine G.; Mandal, Rajarsi; Mydlarz, Wojciech K.; Rooper, Lisa; Troy, Tanya; Yavvari, Siddhartha (11 de enero de 2021). "Tiempo, número y tipo de parejas sexuales asociadas con el riesgo de cáncer orofaríngeo". Cáncer . 127 (7): 1029–1038. doi :10.1002/cncr.33346. ISSN 0008-543X. PMC 8035131 . PMID 33426652.
- ^ Ernster JA, Sciotto CG, O'Brien MM, Finch JL, Robinson LJ, Willson T, Mathews M (diciembre de 2007). "Aumento de la incidencia del cáncer orofaríngeo y el papel del virus del papiloma humano oncogénico". The Laryngoscope . 117 (12): 2115–28. doi :10.1097/MLG.0b013e31813e5fbb. PMID 17891052. S2CID 38017888.
- ^ Lechner M, Frampton GM, Fenton T, Feber A, Palmer G, Jay A, et al. (2013). "La secuenciación de próxima generación dirigida del carcinoma de células escamosas de cabeza y cuello identifica nuevas alteraciones genéticas en tumores HPV+ y HPV-". Genome Medicine . 5 (5): 49. doi : 10.1186/gm453 . PMC 4064312 . PMID 23718828.
- ^ "El riesgo de cáncer de pulmón aumenta en presencia de anticuerpos contra el VPH". Archivado desde el original el 27 de abril de 2012.
- ^ "Los pacientes con cáncer de pulmón tienen más probabilidades de contraer el virus del papiloma humano de alto riesgo". NPIN . Archivado desde el original el 27 de julio de 2012.
- ^ Syrjänen K, Syrjänen S, Kellokoski J, Kärjä J, Mäntyjärvi R (1989). "Secuencias de ADN del virus del papiloma humano (VPH) tipo 6 y 16 en carcinomas de células escamosas bronquiales demostradas mediante hibridación de ADN in situ". Pulmón . 167 (1): 33–42. doi :10.1007/BF02714928. PMID 2537916. S2CID 2094038.
- ^ Carpagnano GE, Koutelou A, Natalicchio MI, Martinelli D, Ruggieri C, Di Taranto A, et al. (octubre de 2011). "VPH en el condensado del aliento exhalado de pacientes con cáncer de pulmón". Revista británica de cáncer . 105 (8): 1183–90. doi :10.1038/bjc.2011.354. PMC 3208494 . PMID 21952627.
- ^ Klein F, Amin Kotb WF, Petersen I (julio de 2009). "Incidencia del virus del papiloma humano en el cáncer de pulmón". Cáncer de pulmón . 65 (1): 13–8. doi :10.1016/j.lungcan.2008.10.003. PMID 19019488.
- ^ Moore M (12 de noviembre de 2007). "El hombre-árbol 'que echó raíces' puede curarse". The Daily Telegraph . Londres. Archivado desde el original el 13 de noviembre de 2007.
- ^ ab Patel T, Morrison LK, Rady P, Tyring S (2010). "Epidermodisplasia verruciforme y susceptibilidad al VPH". Marcadores de enfermedades . 29 (3–4): 199–206. doi : 10.1155/2010/345436 . PMC 3835378 . PMID 21178278.
- ^ "HPV y cáncer". Instituto Nacional del Cáncer . 15 de mayo de 2015. Archivado desde el original el 18 de abril de 2017. Consultado el 18 de abril de 2017 .
- ^ ab Miyague AH, Mauad FM, de Paula Martins W, Benedetti AC, Ferreira AE, Mauad-Filho F (5 de febrero de 2019). "La ecografía como fuente potencial de infección nosocomial y cruzada: una revisión de la literatura". Radiología Brasileira . 48 (5): 319–23. doi :10.1590/0100-3984.2014.0002. PMC 4633077 . PMID 26543284.
- ^ Hoyle, Alice; McGeeney, Ester (2019). Relaciones maravillosas y educación sexual. Taylor y Francis. ISBN 978-1-35118-825-8. Recuperado el 11 de julio de 2023 .
- ^ ab Heymann MD (2015). Manual de control de enfermedades transmisibles (20.ª edición). Washington DC: Apha Press. pp. 299–300. ISBN 978-0-87553-018-5.
- ^ ab Burchell AN, Winer RL, de Sanjosé S, Franco EL (agosto de 2006). "Capítulo 6: Epidemiología y dinámica de transmisión de la infección genital por VPH". Vaccine . 24 (Supl 3): S3/52–61. doi :10.1016/j.vaccine.2006.05.031. PMID 16950018.
- ^ Schmitt M, Depuydt C, Benoy I, Bogers J, Antoine J, Arbyn M, Pawlita M (mayo de 2013). "Prevalencia y carga viral de 51 tipos de virus del papiloma humano genital y tres subtipos". Revista internacional del cáncer . 132 (10): 2395–403. doi : 10.1002/ijc.27891 . PMID 23034864. S2CID 1316857.
- ^ Egendorf, Laura. Enfermedades de transmisión sexual (serie At Issue). Nueva York: Greenhaven Press, 2007.
- ^ ab Hernandez BY, Wilkens LR, Zhu X, Thompson P, McDuffie K, Shvetsov YB, et al. (junio de 2008). "Transmisión del virus del papiloma humano en parejas heterosexuales". Enfermedades infecciosas emergentes . 14 (6): 888–94. doi :10.3201/eid1406.070616. PMC 2600292. PMID 18507898 .
- ^ Hernandez BY, Wilkens LR, Zhu X, Thompson P, McDuffie K, Shvetsov YB, et al. (junio de 2008). "Transmisión del virus del papiloma humano en parejas heterosexuales". Enfermedades infecciosas emergentes . 14 (6): 888–94. doi :10.3201/eid1406.070616. PMC 2600292 . PMID 18507898.
- ^ ab Giuliano AR, Nielson CM, Flores R, Dunne EF, Abrahamsen M, Papenfuss MR, et al. (octubre de 2007). "Los sitios anatómicos óptimos para el muestreo de hombres heterosexuales para la detección del virus del papiloma humano (VPH): el estudio de detección del VPH en hombres". The Journal of Infectious Diseases . 196 (8): 1146–52. doi :10.1086/521629. PMC 3904649 . PMID 17955432.
- ^ abcd Winer RL, Hughes JP, Feng Q, Xi LF, Cherne S, O'Reilly S, et al. (julio de 2010). "Detección de tipos de VPH genital en muestras de yemas de dedos de estudiantes universitarias sexualmente activas recientemente". Epidemiología del cáncer, biomarcadores y prevención . 19 (7): 1682–5. doi :10.1158/1055-9965.EPI-10-0226. PMC 2901391 . PMID 20570905.
- ^ Winer RL, Lee SK, Hughes JP, Adam DE, Kiviat NB, Koutsky LA (febrero de 2003). "Infección genital por virus del papiloma humano: incidencia y factores de riesgo en una cohorte de estudiantes universitarias". American Journal of Epidemiology . 157 (3): 218–26. doi : 10.1093/aje/kwf180 . PMID 12543621.
- ^ Tay SK (julio de 1995). "Infección oncogénica genital por virus del papiloma humano: una breve revisión sobre el modo de transmisión" (Texto completo gratuito) . Anales de la Academia de Medicina, Singapur . 24 (4): 598–601. PMID 8849195. Archivado desde el original el 27 de julio de 2012.
- ^ Pao CC, Tsai PL, Chang YL, Hsieh TT, Jin JY (marzo de 1993). "Posible transmisión no sexual de infecciones genitales por virus del papiloma humano en mujeres jóvenes". Revista Europea de Microbiología Clínica y Enfermedades Infecciosas . 12 (3): 221–2. doi :10.1007/BF01967118. PMID 8389707. S2CID 11548979.
- ^ Tay SK, Ho TH, Lim-Tan SK (agosto de 1990). "¿La infección genital por el virus del papiloma humano siempre se transmite sexualmente?" (Texto completo gratuito) . The Australian & New Zealand Journal of Obstetrics & Gynaecology . 30 (3): 240–2. doi :10.1111/j.1479-828X.1990.tb03223.x. PMID 2256864. S2CID 72353975. Archivado desde el original el 6 de abril de 2016.
- ^ ab Sonnex C, Strauss S, Gray JJ (octubre de 1999). "Detección de ADN del virus del papiloma humano en los dedos de pacientes con verrugas genitales". Infecciones de transmisión sexual . 75 (5): 317–9. doi :10.1136/sti.75.5.317. PMC 1758241. PMID 10616355 .
- ^ de Hans Krueger; Gavin Stuart; Richard Gallagher; Dan Williams, Jon Kerner (12 de abril de 2010). VPH y otros agentes infecciosos en el cáncer: oportunidades para la prevención y la salud pública: Oportunidades para la prevención y la salud pública. Oxford University Press. pág. 34. ISBN 978-0-19-973291-3Archivado desde el original el 9 de junio de 2013 . Consultado el 24 de diciembre de 2012 .
- ^ Bodaghi S, Wood LV, Roby G, Ryder C, Steinberg SM, Zheng ZM (noviembre de 2005). "¿Podrían los virus del papiloma humano transmitirse a través de la sangre?". Journal of Clinical Microbiology . 43 (11): 5428–34. doi :10.1128/JCM.43.11.5428-5434.2005. PMC 1287818 . PMID 16272465.
- ^ Chen AC, Keleher A, Kedda MA, Spurdle AB, McMillan NA, Antonsson A (octubre de 2009). "ADN del virus del papiloma humano detectado en muestras de sangre periférica de donantes de sangre masculinos australianos sanos" (PDF) . Revista de Virología Médica . 81 (10): 1792–6. doi :10.1002/jmv.21592. hdl : 10072/44445 . PMID 19697401. S2CID 22918855.
- ^ "Criterios de elegibilidad por tema - Cruz Roja Americana". Archivado desde el original el 1 de enero de 2017.
- ^ abc Watson RA (2005). "Virus del papiloma humano: cómo afrontar la epidemia: la perspectiva de un urólogo". Reseñas en Urología . 7 (3): 135–44. PMC 1477576 . PMID 16985824.
- ^ Guan J, Bywaters SM, Brendle SA, Ashley RE, Makhov AM, Conway JF, et al. (febrero de 2017). "Los mapas de microscopía crioelectrónica del virus del papiloma humano 16 revelan densidades de L2 y el sitio de unión de la heparina". Estructura . 25 (2): 253–263. doi : 10.1016/j.str.2016.12.001 . PMID 28065506.
- ^ abc Schiller JT, Day PM, Kines RC (junio de 2010). "Conocimiento actual del mecanismo de la infección por VPH". Oncología ginecológica . 118 (1 Suppl): S12–7. doi :10.1016/j.ygyno.2010.04.004. PMC 3493113 . PMID 20494219.
- ^ ab Scheurer ME, Tortolero-Luna G, Adler-Storthz K (2005). "Infección por virus del papiloma humano: biología, epidemiología y prevención". Revista internacional de cáncer ginecológico . 15 (5): 727–46. doi :10.1111/j.1525-1438.2005.00246.x. PMID 16174218. S2CID 23849159.
- ^ Woodham AW, Da Silva DM, Skeate JG, Raff AB, Ambroso MR, Brand HE, et al. (2012). "La subunidad S100A10 del heterotetrámero de anexina A2 facilita la infección por virus del papiloma humano mediada por L2". PLOS ONE . 7 (8): e43519. Bibcode :2012PLoSO...743519W. doi : 10.1371/journal.pone.0043519 . PMC 3425544 . PMID 22927980.
- ^ Raff AB, Woodham AW, Raff LM, Skeate JG, Yan L, Da Silva DM y col. (junio de 2013). "El campo en evolución de la investigación del receptor del virus del papiloma humano: una revisión de la unión y la entrada". Revista de Virología . 87 (11): 6062–72. doi :10.1128/JVI.00330-13. PMC 3648114 . PMID 23536685.
- ^ Chen Z, Schiffman M, Herrero R, Desalle R, Anastos K, Segondy M, et al. (2011). "Evolución y clasificación taxonómica de los genomas variantes relacionados con el virus del papiloma humano 16 (HPV16): HPV31, HPV33, HPV35, HPV52, HPV58 y HPV67". PLOS ONE . 6 (5): e20183. Bibcode :2011PLoSO...620183C. doi : 10.1371/journal.pone.0020183 . PMC 3103539 . PMID 21673791.
- ^ Zuna RE, Tuller E, Wentzensen N, Mathews C, Allen RA, Shanesmith R, et al. (octubre de 2011). "Linaje de la variante HPV16, estadio clínico y supervivencia en mujeres con cáncer cervical invasivo". Agentes infecciosos y cáncer . 6 : 19. doi : 10.1186/1750-9378-6-19 . PMC 3226431. PMID 22035468 .
- ^ ab Mirabello, Lisa; Clarke, Megan; Nelson, Chase; Dean, Michael; Wentzensen, Nicolas; Yeager, Meredith; Cullen, Michael; Boland, Joseph; Taller sobre VPH del NCI; Schiffman, Mark; Burk, Robert (13 de febrero de 2018). "La intersección de la epidemiología, la genómica y los estudios mecanísticos de la carcinogénesis mediada por VPH". Viruses . 10 (2): 80. doi : 10.3390/v10020080 . ISSN 1999-4915. PMC 5850387 . PMID 29438321.
- ^ abcde Nikolaidis, Marios; Tsakogiannis, Dimitris; Bletsa, Garyfalia; Mossialos, Dimitris; Kottaridi, Christine; Iliopoulos, Ioannis; Markoulatos, Panayotis; Amoutzias, Grigoris D. (14 de octubre de 2021). "HPV16-Genotyper: una herramienta computacional para la evaluación de riesgos, la genotipificación de linaje y la detección de recombinación en secuencias de HPV16, basada en un análisis evolutivo a gran escala". Diversidad . 13 (10): 497. doi : 10.3390/d13100497 . ISSN 1424-2818.
- ^ Mirabello, Lisa; Yeager, Meredith; Cullen, Michael; Boland, Joseph F.; Chen, Zigui; Wentzensen, Nicolas; Zhang, Xijun; Yu, Kai; Yang, Qi; Mitchell, Jason; Roberson, David (septiembre de 2016). "Asociaciones del sublinaje HPV16 con riesgo de cáncer específico de la histología utilizando secuencias del genoma completo del HPV en 3200 mujeres". Revista del Instituto Nacional del Cáncer . 108 (9): djw100. doi :10.1093/jnci/djw100. ISSN 0027-8874. PMC 5939630 . PMID 27130930.
- ^ Jiang, Mingjun; Xi, Long Fu; Edelstein, Zoe R.; Galloway, Denise A.; Olsem, Gary J.; Lin, William Chun-Che; Kiviat, Nancy B. (noviembre de 2009). "Identificación de variantes recombinantes del virus del papiloma humano tipo 16". Virología . 394 (1): 8–11. doi :10.1016/j.virol.2009.08.040. PMC 2769496 . PMID 19758676.
- ^ Zanier K, Charbonnier S, Sidi AO, McEwen AG, Ferrario MG, Poussin-Courmontagne P, et al. (febrero de 2013). "Base estructural del secuestro de motivos LxxLL celulares por oncoproteínas E6 del virus del papiloma". Science . 339 (6120): 694–8. Bibcode :2013Sci...339..694Z. doi :10.1126/science.1229934. PMC 3899395 . PMID 23393263.
- ^ Ganguly N, Parihar SP (marzo de 2009). "Oncoproteínas E6 y E7 del virus del papiloma humano como factores de riesgo para la tumorigénesis". Journal of Biosciences . 34 (1): 113–23. doi :10.1007/s12038-009-0013-7. PMID 19430123. S2CID 8770549.
- ^ Zheng ZM, Baker CC (septiembre de 2006). "Estructura, expresión y regulación postranscripcional del genoma del virus del papiloma". Frontiers in Bioscience . 11 : 2286–302. doi :10.2741/1971. PMC 1472295 . PMID 16720315.
- ^ Tang S, Tao M, McCoy JP, Zheng ZM (mayo de 2006). "La oncoproteína E7 se traduce a partir de transcripciones E6*I empalmadas en líneas celulares de cáncer de cuello uterino positivas para el virus del papiloma humano de alto riesgo tipo 16 o tipo 18 mediante la reiniciación de la traducción". Journal of Virology . 80 (9): 4249–63. doi :10.1128/JVI.80.9.4249-4263.2006. PMC 1472016 . PMID 16611884.
- ^ Alison A. McBride (18 de marzo de 2017). "Mecanismos y estrategias de replicación del virus del papiloma". Química biológica . 398 (8): 919–927. doi :10.1515/HSZ-2017-0113. ISSN 1431-6730. PMID 28315855. Wikidata Q39186071.
- ^ ab Chaturvedi A, Gillison ML (4 de marzo de 2010). "Virus del papiloma humano y cáncer de cabeza y cuello". En Andrew F. Olshan (ed.). Epidemiología, patogénesis y prevención del cáncer de cabeza y cuello (1.ª ed.). Nueva York: Springer. págs. 87-116. doi :10.1007/978-1-4419-1472-9_5. ISBN 978-1-4419-1471-2.
- ^ Münger K, Howley PM (noviembre de 2002). "Funciones de inmortalización y transformación del virus del papiloma humano". Virus Research . 89 (2): 213–28. doi :10.1016/S0168-1702(02)00190-9. PMID 12445661.
- ^ Conway MJ, Alam S, Ryndock EJ, Cruz L, Christensen ND, Roden RB, Meyers C (octubre de 2009). "Ensamblaje dependiente del gradiente redox que abarca el tejido de viriones nativos del virus del papiloma humano tipo 16". Journal of Virology . 83 (20): 10515–26. doi :10.1128/JVI.00731-09. PMC 2753102 . PMID 19656879.
- ^ Bryan JT, Brown DR (marzo de 2001). "Transmisión de la infección por el virus del papiloma humano tipo 11 por células cornificadas descamadas". Virología . 281 (1): 35–42. doi : 10.1006/viro.2000.0777 . PMID 11222093.
- ^ Rampias T, Boutati E, Pectasides E, Sasaki C, Kountourakis P, Weinberger P, Psyrri A (marzo de 2010). "Activación de la vía de señalización de Wnt por los oncogenes E6 y E7 del virus del papiloma humano en células de carcinoma escamoso orofaríngeo positivas para HPV16". Investigación molecular sobre el cáncer . 8 (3): 433–43. doi : 10.1158/1541-7786.MCR-09-0345 . PMID: 20215420. S2CID : 19411033.
- ^ Giuliano AR, Lu B, Nielson CM, Flores R, Papenfuss MR, Lee JH, et al. (septiembre de 2008). "Prevalencia, incidencia y duración específicas por edad de las infecciones por el virus del papiloma humano en una cohorte de 290 hombres estadounidenses". The Journal of Infectious Diseases . 198 (6): 827–35. doi : 10.1086/591095 . PMID 18657037.
- ^ EHPV, archivado desde el original el 17 de diciembre de 2014
- ^ Schiffman M, Castle PE (agosto de 2003). «Virus del papiloma humano: epidemiología y salud pública» [1 de enero de 2017]. Archives of Pathology & Laboratory Medicine . 127 (8): 930–4. doi :10.5858/2003-127-930-HPEAPH. PMID 12873163. Archivado desde el original el 14 de abril de 2013.
- ^ "HPV | Virus del papiloma humano | Prueba de Papanicolaou | MedlinePlus" . Consultado el 7 de noviembre de 2018 .
- ^ Saslow, D; Solomon, D; Lawson, HW; Killackey, M; Kulasingam, SL; Cain, J; Garcia, FA; Moriarty, AT; Waxman, AG; Wilbur, DC; Wentzensen, N; Downs LS, Jr; Spitzer, M; Moscicki, AB; Franco, EL; Stoler, MH; Schiffman, M; Castle, PE; Myers, ER; Comité de Directrices para el Cáncer Cervical de la ACS-ASCCP-ASCP (mayo de 2012). "Directrices de detección de la Sociedad Estadounidense del Cáncer, la Sociedad Estadounidense de Colposcopia y Patología Cervical y la Sociedad Estadounidense de Patología Clínica para la prevención y detección temprana del cáncer cervical". CA: A Cancer Journal for Clinicians . 62 (3): 147–72. doi :10.3322/caac.21139. PMC 3801360 . PMID 22422631.
- ^ Smith RA, Andrews KS, Brooks D, Fedewa SA, Manassaram-Baptiste D, Saslow D, et al. (marzo de 2017). "Detección del cáncer en los Estados Unidos, 2017: una revisión de las directrices actuales de la Sociedad Estadounidense del Cáncer y los problemas actuales en la detección del cáncer". CA: A Cancer Journal for Clinicians . 67 (2): 100–121. doi : 10.3322/caac.21392 . PMID 28170086. S2CID 37359995.
- ^ "Hoja informativa del Instituto Nacional del Cáncer: VPH y cáncer". Cancer.gov. Archivado desde el original el 31 de octubre de 2013. Consultado el 23 de octubre de 2013 .
- ^ Pan C, Issaeva N, Yarbrough WG (2018). "Cáncer orofaríngeo inducido por VPH: conocimiento actual de la biología molecular y mecanismos de carcinogénesis". Cánceres de cabeza y cuello . 3 : 12. doi : 10.1186/s41199-018-0039-3 . PMC 6460765. PMID 31093365 .
- ^ abcde Dunne EF, Nielson CM, Stone KM, Markowitz LE, Giuliano AR (octubre de 2006). "Prevalencia de la infección por VPH entre los hombres: una revisión sistemática de la literatura". The Journal of Infectious Diseases . 194 (8): 1044–57. doi : 10.1086/507432 . PMID 16991079.
- ^ Burchell AN, Richardson H, Mahmud SM, Trottier H, Tellier PP, Hanley J, et al. (marzo de 2006). "Modelado de la transmisibilidad sexual de la infección por el virus del papiloma humano mediante simulación estocástica por computadora y datos empíricos de un estudio de cohorte de mujeres jóvenes en Montreal, Canadá". American Journal of Epidemiology . 163 (6): 534–43. doi : 10.1093/aje/kwj077 . PMID 16421235.
- ^ Kim JJ (octubre de 2007). "Los análisis de políticas de vacunación pueden beneficiarse de los estudios de la historia natural del virus del papiloma humano en hombres". The Journal of Infectious Diseases . 196 (8): 1117–9. doi : 10.1086/521199 . PMID 17955427.
- ^ "Preguntas frecuentes para hombres". thehpvtest.com . Archivado desde el original el 5 de septiembre de 2012. Consultado el 24 de agosto de 2012 .
- ^ ab Nicolau SM, Camargo CG, Stávale JN, Castelo A, Dôres GB, Lörincz A, de Lima GR (febrero de 2005). "Detección de ADN del virus del papiloma humano en parejas sexuales masculinas de mujeres con infección genital por el virus del papiloma humano". Urología . 65 (2): 251–5. doi :10.1016/j.urology.2004.09.031. PMID 15708032.
- ^ abc Aguilar LV, Lazcano-Ponce E, Vaccarella S, Cruz A, Hernández P, Smith JS, et al. (febrero de 2006). "Virus del papiloma humano en hombres: comparación de diferentes sitios genitales". Infecciones de transmisión sexual . 82 (1): 31–3. doi :10.1136/sti.2005.015131. PMC 2563819. PMID 16461598 .
- ^ abc Weaver BA, Feng Q, Holmes KK, Kiviat N, Lee SK, Meyer C, et al. (febrero de 2004). "Evaluación de los sitios genitales y técnicas de muestreo para la detección de ADN del virus del papiloma humano en hombres". The Journal of Infectious Diseases . 189 (4): 677–85. doi : 10.1086/381395 . PMID 14767822.
- ^ Hernandez BY, McDuffie K, Goodman MT, Wilkens LR, Thompson P, Zhu X, et al. (febrero de 2006). "Comparación de muestras genitales recolectadas por médicos y por el propio paciente para la detección del virus del papiloma humano en hombres". Journal of Clinical Microbiology . 44 (2): 513–7. doi :10.1128/JCM.44.2.513-517.2006. PMC 1392697 . PMID 16455906.
- ^ Ogilvie GS, Taylor DL, Achen M, Cook D, Krajden M (junio de 2009). "Autorrecolección de muestras genitales del virus del papiloma humano en hombres heterosexuales". Infecciones de transmisión sexual . 85 (3): 221–5. doi : 10.1136/sti.2008.033068 . PMID 19066196. S2CID 24410167.
- ^ Petignat P, Faltin DL, Bruchim I, Tramèr MR, Franco EL, Coutlée F (mayo de 2007). "¿Son comparables las muestras recogidas por las propias pacientes a las muestras cervicales recogidas por médicos para la prueba de ADN del virus del papiloma humano? Una revisión sistemática y un metanálisis". Oncología ginecológica . 105 (2): 530–5. doi :10.1016/j.ygyno.2007.01.023. PMID 17335880.
- ^ Partridge JM, Hughes JP, Feng Q, Winer RL, Weaver BA, Xi LF, et al. (octubre de 2007). "Infección genital por virus del papiloma humano en hombres: incidencia y factores de riesgo en una cohorte de estudiantes universitarios". The Journal of Infectious Diseases . 196 (8): 1128–36. doi : 10.1086/521192 . PMID 17955430.
- ^ "El VPH y los hombres: hoja informativa de los CDC". Centros para el Control y la Prevención de Enfermedades . Centros para el Control y la Prevención de Enfermedades (CDC). 3 de abril de 2008. Archivado desde el original el 17 de octubre de 2009. Consultado el 13 de noviembre de 2009 .
- ^ "El virus del papiloma humano (VPH) y los hombres: preguntas y respuestas". 2007. Archivado desde el original el 14 de septiembre de 2008. Consultado el 10 de septiembre de 2008.
Actualmente, en Canadá existe una prueba de ADN del VPH aprobada para mujeres, pero no para hombres.
- ^ "Lo que los hombres necesitan saber sobre el VPH". 2006. Archivado desde el original el 7 de abril de 2007. Consultado el 4 de abril de 2007. Actualmente no existe ninguna prueba aprobada por la FDA para detectar el VPH en los hombres. Esto se debe a que aún no se ha desarrollado una forma eficaz y confiable de recolectar una muestra de células de la piel genital masculina ,
que permita detectar el VPH.
- ^ Storey R, Joh J, Kwon A, Jenson AB, Ghim SJ, Kloecker GH (2013). "Detección de inmunoglobulina G contra E7 del virus del papiloma humano en el cáncer de pulmón de células no pequeñas". Journal of Oncology . 2013 : 240164. doi : 10.1155/2013/240164 . PMC 3603668 . PMID 23533408.
- ^ Rocha-Zavaleta L, Ambrosio JP, de Lourdes Mora-Garcia M, Cruz-Talonia F, Hernandez-Montes J, Weiss-Steider B, et al. (septiembre de 2004). "Detección de anticuerpos contra un péptido del virus del papiloma humano (VPH) tipo 16 que diferencian las lesiones intraepiteliales escamosas de bajo grado asociadas al VPH de alto riesgo de las de bajo riesgo". The Journal of General Virology . 85 (Pt 9): 2643–50. doi : 10.1099/vir.0.80077-0 . PMID 15302958.
- ^ Bolhassani A, Zahedifard F, Taslimi Y, Taghikhani M, Nahavandian B, Rafati S (noviembre de 2009). "Detección de anticuerpos contra fragmentos E7 y GP96 de HPV16 como biomarcadores en pacientes con cáncer de cuello uterino" (PDF) . The Indian Journal of Medical Research . 130 (5): 533–41. PMID 20090101. Archivado desde el original (PDF) el 16 de diciembre de 2010 . Consultado el 18 de marzo de 2014 .
- ^ Fitzgerald K (18 de junio de 2013). "Blood Test May Detect Sexually Transmitted Throat Cancer" (Una prueba de sangre puede detectar cáncer de garganta transmitido sexualmente). Medical News Today . Archivado desde el original el 7 de abril de 2014. Consultado el 18 de marzo de 2014 .
- ^ "Diagnóstico y pruebas del virus del papiloma humano (VPH)". Cleveland Clinic . 18 de septiembre de 2018. Archivado desde el original el 1 de agosto de 2020. Consultado el 8 de febrero de 2019 .
- ^ "La FDA aprueba Gardasil 9 para la prevención de ciertos cánceres causados por cinco tipos adicionales de VPH". Administración de Alimentos y Medicamentos . 10 de diciembre de 2014. Archivado desde el original el 10 de enero de 2015. Consultado el 8 de marzo de 2015 .
- ^ "Epidemiología del virus del papiloma humano y prevención de enfermedades prevenibles mediante vacunación". CDC . Archivado desde el original el 3 de febrero de 2014 . Consultado el 30 de enero de 2014 .
- ^ "Vacunas contra el virus del papiloma humano. Documento de posición de la OMS" (PDF) . Relevé Epidémiologique Hebdomadaire . 84 (15): 118–31. Abril de 2009. PMID 19360985. Archivado (PDF) desde el original el 24 de diciembre de 2010.
- ^ abc Koliopoulos G, Nyaga VN, Santesso N, Bryant A, Martin-Hirsch PP, Mustafa RA, et al. (agosto de 2017). "Citología versus prueba de VPH para la detección del cáncer de cuello uterino en la población general". Base de datos Cochrane de revisiones sistemáticas . 8 (7): CD008587. doi :10.1002/14651858.CD008587.pub2. PMC 6483676. PMID 28796882 .
- ^ "Los CDC recomiendan solo dos dosis de la vacuna contra el VPH para los adolescentes más jóvenes". Centros para el Control y la Prevención de Enfermedades . 20 de octubre de 2016. Archivado desde el original el 23 de marzo de 2017. Consultado el 24 de marzo de 2017 .
- ^ ab Markowitz LE, Dunne EF, Saraiya M, Lawson HW, Chesson H, Unger ER (marzo de 2007). "Vacuna tetravalente contra el virus del papiloma humano: recomendaciones del Comité Asesor sobre Prácticas de Inmunización (ACIP)". MMWR. Recomendaciones e informes . 56 (RR-2): 1–24. PMID 17380109. Archivado desde el original el 20 de mayo de 2017.
- ^ Dobson SR, McNeil S, Dionne M, Dawar M, Ogilvie G, Krajden M, et al. (mayo de 2013). "Inmunogenicidad de 2 dosis de la vacuna contra el VPH en adolescentes más jóvenes frente a 3 dosis en mujeres jóvenes: un ensayo clínico aleatorizado". JAMA . 309 (17): 1793–802. doi : 10.1001/jama.2013.1625 . PMID 23632723.
- ^ "Información sobre la vacuna contra el VPH para mujeres jóvenes". Centros para el Control y la Prevención de Enfermedades . 3 de enero de 2017. Archivado desde el original el 25 de marzo de 2017. Consultado el 24 de marzo de 2017 .
- ^ "Virus HPV: información sobre el virus del papiloma humano". WebMD . Archivado desde el original el 8 de marzo de 2008.
- ^ "Folleto informativo para pacientes de Gardasil" (PDF) . Abril de 2015. Consultado el 11 de julio de 2018 .
- ^ Deleré Y, Wichmann O, Klug SJ, van der Sande M, Terhardt M, Zepp F, Harder T (septiembre de 2014). "La eficacia y duración de la protección de la vacuna contra el virus del papiloma humano: una revisión sistemática y un metanálisis". Deutsches Ärzteblatt International . 111 (35–36): 584–91. doi :10.3238/arztebl.2014.0584. PMC 4174682 . PMID 25249360.
- ^ "La FDA aprueba Gardasil 9 para la prevención de ciertos cánceres causados por cinco tipos adicionales de VPH". Administración de Alimentos y Medicamentos (nota de prensa). 10 de diciembre de 2014. Archivado desde el original el 10 de enero de 2015. Consultado el 28 de febrero de 2015 .
- ^ "CDC — Eficacia de los preservativos — Los preservativos de látex masculinos y las enfermedades de transmisión sexual". Centros para el Control y la Prevención de Enfermedades (CDC). 22 de octubre de 2009. Archivado desde el original el 17 de octubre de 2009. Consultado el 23 de octubre de 2009 .
- ^ ab Meyers J, Ryndock E, Conway MJ, Meyers C, Robison R (junio de 2014). "Susceptibilidad del virus del papiloma humano de alto riesgo tipo 16 a los desinfectantes clínicos". The Journal of Antimicrobial Chemotherapy . 69 (6): 1546–50. doi :10.1093/jac/dku006. PMC 4019329 . PMID 24500190.
- ^ Liu Z, Rashid T, Nyitray AG (febrero de 2016). "No se requieren penes: una revisión sistemática del potencial de transmisión horizontal del virus del papiloma humano que no es sexual o no incluye la penetración del pene". Salud sexual . 13 (1): 10–21. doi :10.1071/sh15089. PMID 26433493. S2CID 20937073.
- ^ Sabeena S, Bhat P, Kamath V, Arunkumar G (marzo de 2017). "Posibles modos no sexuales de transmisión del virus del papiloma humano". The Journal of Obstetrics and Gynaecology Research . 43 (3): 429–435. doi : 10.1111/jog.13248 . PMID 28165175. S2CID 39387099.
- ^ División de Mejora de la Calidad de HSE — Programa de Seguridad de Descontaminación (enero de 2017). Guía del Servicio Ejecutivo de Salud para la Descontaminación de Sondas Ultrasónicas Semicríticas; Sondas Ultrasónicas Semiinvasivas y No Invasivas (PDF) (Informe). Departamento de Salud del Reino Unido. QPSD-GL-028-1. Archivado desde el original (PDF) el 1 de agosto de 2020. Consultado el 8 de febrero de 2019 .
- ^ "Recomendaciones para la limpieza y desinfección en ecografías médicas para prevenir la transmisión del virus del papiloma humano (VPH)" (PDF) . Red Provincial de Control de Infecciones de Columbia Británica . 2 de junio de 2016.
- ^ "Requisitos de reprocesamiento para sondas de ultrasonido" (PDF) . Colegio de Médicos y Cirujanos de Columbia Británica . Diciembre de 2017.
- ^ ab "Hoja informativa sobre la infección genital por VPH". Centros para el Control y la Prevención de Enfermedades (CDC). 10 de abril de 2008. Archivado desde el original el 11 de septiembre de 2012. Consultado el 13 de noviembre de 2009 .
- ^ "Información sobre la vacuna contra el VPH para mujeres jóvenes". Centros para el Control y la Prevención de Enfermedades (CDC). 26 de junio de 2008. Archivado desde el original el 26 de octubre de 2009. Consultado el 13 de noviembre de 2009 .
- ^ Sociedad Estadounidense del Cáncer. "¿Cuáles son los factores de riesgo del cáncer de cuello uterino?". Archivado desde el original el 19 de febrero de 2008. Consultado el 21 de febrero de 2008 .
- ^ "Cura para el VPH". Webmd.com. Archivado desde el original el 18 de agosto de 2010. Consultado el 29 de agosto de 2010 .
- ^ Gilbert LK, Alexander L, Grosshans JF, Jolley L (marzo de 2003). "Respuestas a preguntas frecuentes sobre el VPH". Enfermedades de transmisión sexual . 30 (3): 193–4. doi : 10.1097/00007435-200303000-00002 . PMID 12616133.
- ^ "Directrices actualizadas del Servicio de Salud Pública de los Estados Unidos para el manejo de la exposición ocupacional al VIH y recomendaciones para la profilaxis posterior a la exposición". Centros para el Control y la Prevención de Enfermedades. Archivado desde el original el 16 de noviembre de 2015. Consultado el 23 de octubre de 2015 .
- ^ Desai M, Woodhall SC, Nardone A, Burns F, Mercey D, Gilson R (agosto de 2015). "Recordatorio activo para aumentar las pruebas de VIH y ETS: una revisión sistemática". Infecciones de transmisión sexual . 91 (5): 314–23. doi : 10.1136/sextrans-2014-051930 . PMID 25759476. S2CID 663971.
- ^ van der Heijden E, Lopes AD, Bryant A, Bekkers R, Galaal K (enero de 2015). "Estrategias de seguimiento después del tratamiento (escisión en asa grande de la zona de transformación (LLETZ)) para la neoplasia intraepitelial cervical (CIN): impacto de la prueba del virus del papiloma humano (HPV)". Base de Datos Cochrane de Revisiones Sistemáticas . 1 (1): CD010757. doi :10.1002/14651858.cd010757.pub2. PMC 6457759 . PMID 25562623.
- ^ abc Chan CK, Aimagambetova G, Ukybassova T, Kongrtay K, Azizan A (10 de octubre de 2019). "Infección por virus del papiloma humano y cáncer de cuello uterino: epidemiología, detección y vacunación: revisión de las perspectivas actuales". Journal of Oncology . 2019 : 3257939. doi : 10.1155/2019/3257939 . PMC 6811952 . PMID 31687023.
- ^ ab Serrano B, Brotons M, Bosch FX, Bruni L (febrero de 2018). "Epidemiología y carga de la enfermedad relacionada con el VPH". Mejores prácticas e investigación. Obstetricia y ginecología clínica . Virus del papiloma humano en ginecología. 47 : 14–26. doi :10.1016/j.bpobgyn.2017.08.006. PMID 29037457.
- ^ Forman D, de Martel C, Lacey CJ, Soerjomataram I, Lortet-Tieulent J, Bruni L, et al. (noviembre de 2012). "Carga mundial del virus del papiloma humano y enfermedades relacionadas". Vacuna . Control integral de las infecciones por VPH y enfermedades relacionadas. 30 (Supl. 5): F12-23. doi :10.1016/j.vaccine.2012.07.055. PMID 23199955. S2CID 30694437.
- ^ abcde Dunne EF, Unger ER, Sternberg M, McQuillan G, Swan DC, Patel SS, Markowitz LE (febrero de 2007). "Prevalencia de la infección por VPH entre mujeres en los Estados Unidos". JAMA . 297 (8): 813–9. doi : 10.1001/jama.297.8.813 . PMID 17327523.
- ^ "American Social Health Association — HPV Resource Center". Archivado desde el original el 18 de julio de 2007. Consultado el 17 de agosto de 2007 .
- ^ "Asociación Estadounidense de Salud Social — Centro Nacional de Recursos para la Prevención del VPH y el Cáncer Cervical". Archivado desde el original el 19 de junio de 2008. Consultado el 1 de julio de 2008 .
- ^ "Informe sobre la vacuna contra el VPH", ETS, VIH , Planned Parenthood, archivado desde el original el 25 de abril de 2009 , consultado el 12 de febrero de 2009.
De hecho, el riesgo de contraer VPH a lo largo de la vida es de al menos el 50 por ciento para todas las mujeres y hombres sexualmente activos y se estima que, a la edad de 50 años, al menos el 80 por ciento de las mujeres habrán adquirido VPH de transmisión sexual (CDC, 2004; CDC, 2006).
- ^ ab Weinstock H, Berman S, Cates W (enero-febrero de 2004). "Enfermedades de transmisión sexual entre los jóvenes estadounidenses: estimaciones de incidencia y prevalencia, 2000". Perspectivas sobre la salud sexual y reproductiva . 36 (1): 6–10. doi : 10.1363/3600604 . PMID 14982671. Archivado desde el original el 4 de julio de 2008.
- ^ Koutsky L (mayo de 1997). "Epidemiología de la infección genital por el virus del papiloma humano". The American Journal of Medicine . 102 (5A): 3–8. doi :10.1016/s0002-9343(97)00177-0. PMID 9217656.
- ^ Revzina NV, Diclemente RJ (agosto de 2005). "Prevalencia e incidencia de la infección por el virus del papiloma humano en mujeres de los EE. UU.: una revisión sistemática". Revista internacional de ETS y SIDA . 16 (8): 528–37. doi :10.1258/0956462054679214. PMID 16105186. S2CID 23728417.
La prevalencia del VPH informada en los estudios evaluados varió del 14 % a más del 90 %.
- ^ McCullough, Marie (28 de febrero de 2007). «Las cepas del virus del cáncer son más raras de lo que se había estimado inicialmente». The Philadelphia Inquirer . Archivado desde el original el 10 de marzo de 2007. Consultado el 2 de marzo de 2007 .
- ^ Brown, David (28 de febrero de 2007) [The Washington Post , "Más mujeres estadounidenses tienen VPH de lo que se pensaba"]. "Un estudio descubre que más mujeres de lo esperado tienen VPH". San Francisco Chronicle . Archivado desde el original el 9 de noviembre de 2007. Consultado el 2 de marzo de 2007 .
- ^ Tanner, Lindsey (11 de marzo de 2008). «Estudio descubre que 1 de cada 4 adolescentes estadounidenses tiene una ETS». Newsvine . Associated Press . Archivado desde el original el 16 de marzo de 2008 . Consultado el 17 de marzo de 2008 .
- ^ "MMWR: Resumen de enfermedades de declaración obligatoria". Informe semanal de morbilidad y mortalidad . CDC. Archivado desde el original el 17 de agosto de 2014. Consultado el 18 de agosto de 2014 .
- ^ Enfermedades de declaración obligatoria Archivado el 12 de abril de 2016 en Wayback Machine , desde MedlinePlus , un servicio de la Biblioteca Nacional de Medicina de los Estados Unidos, de los Institutos Nacionales de Salud. Actualización: 19 de mayo de 2013 por Jatin M. Vyas. También revisado por David Zieve.
- ^ abc "Autoridad de Calidad de la Información Sanitaria (HIQA)" (PDF) .
- ^ "Directrices de vacunación del HSE" (PDF) .
- ^ "Estadísticas de ITS – VIH en Irlanda" . Consultado el 11 de enero de 2019 .
- ^ ab "Verrugas anogenitales en Irlanda, 2017" (PDF) . Informe epidemiológico anual . Centro de vigilancia de la protección de la salud del HSE. Octubre de 2018. Archivado desde el original (PDF) el 11 de enero de 2019. Consultado el 11 de enero de 2019 .
- ^ Shanaka KA, Wilathgamuwa S, Gunawardene YI, Dassanayake RS (marzo de 2018). "Prevalencia del virus del papiloma humano y sus genotipos de alto riesgo en mujeres de Sri Lanka". Virusdisease . 29 (1): 27–31. doi :10.1007/s13337-018-0419-7. PMC 5877853 . PMID 29607355.
- ^ Wang X, Ji Y, Li J, Dong H, Zhu B, Zhou Y, Wang J, Zhou X, Wang Y, Peppelenbosch MP, Pan Q, Ji X, Liu D (enero de 2018). "Prevalencia de la infección por el virus del papiloma humano en mujeres de la Región Autónoma de Mongolia Interior: un estudio poblacional de una minoría étnica china". J Med Virol . 90 (1): 148–156. doi :10.1002/jmv.24888. PMID 28661048. S2CID 24613222.
- ^ Virus del papiloma humano . Organización Mundial de la Salud, Centro Internacional de Investigaciones sobre el Cáncer. 2007. p. 36. ISBN 978-92-832-1290-4. Recuperado el 7 de septiembre de 2020 .
- ^ "HPV — el virus tímido" (programa de radio). Copia sonora. 6 de diciembre de 2008. Archivado desde el original el 28 de marzo de 2009 . Consultado el 6 de diciembre de 2008 .
- ^ Picken RN, Yang HL (diciembre de 1987). "La integración del HPV-18 en las células HeLa ha implicado la duplicación de parte del genoma viral, así como de las secuencias flanqueantes del ADN humano". Nucleic Acids Research . 15 (23): 10068. doi :10.1093/nar/15.23.10068. PMC 306572 . PMID 2827110.
- ^ Franco, E.; Villa, L.; Rohan, T.; Ferenczy, A.; Petzl-Erler, M .; Matlashewski, G. (1999). "Diseño y métodos del estudio longitudinal Ludwig-McGill de la historia natural de la infección por virus del papiloma humano y neoplasia cervical en Brasil. Grupo de estudio Ludwig-McGill - PubMed". Revista Panamericana de Salud Pública . 6 (4): 223–233. doi : 10.1590/s1020-49891999000900001 . PMID 10572472.
Véase también
Enlaces externos
- Infección por el virus del papiloma humano en Curlie
- Centro de información sobre el VPH y el cáncer – ICO
- Hojas informativas sobre el VPH en los Centros para el Control y la Prevención de Enfermedades
- "Vacunas contra el virus del papiloma humano (VPH)", hoja informativa del Instituto Nacional del Cáncer , Institutos Nacionales de Salud de EE. UU., 25 de mayo de 2021.
