Esclerosis múltiple
This article needs more reliable medical references for verification or relies too heavily on primary sources, specifically: references that do not meet Wikipedia's guidelines for medical content, or are excessively dated, are contained in this article. (July 2022) |
| Esclerosis múltiple | |
|---|---|
| Otros nombres | Esclerosis cerebral múltiple, esclerosis cerebroespinal múltiple, esclerosis diseminada, encefalomielitis diseminada |
 | |
| El tejido teñido con CD68 muestra varios macrófagos en el área de una lesión desmielinizada causada por EM. | |
| Especialidad | Neurología |
| Síntomas | Variable, incluye casi cualquier síntoma o signo neurológico, siendo los problemas autonómicos , visuales, motores y sensoriales los más comunes. [1] |
| Inicio habitual | Edad 20-50 [2] |
| Duración | A largo plazo [3] |
| Causas | Desconocido [4] |
| Método de diagnóstico | Basado en síntomas y pruebas médicas [5] |
| Tratamiento |
|
| Frecuencia | 0,032% ( mundial ) |
La esclerosis múltiple ( EM ) es una enfermedad autoinmune en la que se dañan las cubiertas aislantes de las células nerviosas del cerebro y la médula espinal . [3] Al ser una enfermedad desmielinizante , la EM altera la capacidad de partes del sistema nervioso para transmitir señales , lo que da lugar a una variedad de signos y síntomas , incluidos problemas físicos, mentales y, a veces, psiquiátricos. [1] [8] [9] Los síntomas incluyen visión doble , pérdida de la visión, dolor ocular, debilidad muscular y pérdida de sensibilidad o coordinación. [3] [10] [11] La EM adopta varias formas, y los síntomas nuevos aparecen en ataques aislados (formas recurrentes) o se acumulan con el tiempo (formas progresivas). [12] [13] En las formas recurrentes de EM, entre los ataques, los síntomas pueden desaparecer por completo, aunque a menudo quedan algunos problemas neurológicos permanentes, especialmente a medida que avanza la enfermedad. [13] En las formas progresivas de EM, la función corporal se deteriora lentamente una vez que se manifiestan los síntomas y empeorará de forma constante si no se trata. [14]
Si bien su causa no está clara, se cree que el mecanismo subyacente es la destrucción por parte del sistema inmunológico o la falla de las células productoras de mielina. [4] Las causas propuestas para esto incluyen la desregulación inmunológica, la genética y los factores ambientales, como las infecciones virales . [15] [16] [8] [17] La EM generalmente se diagnostica según los signos y síntomas que se presentan y los resultados de las pruebas médicas de respaldo. [5]
No se conoce ninguna cura para la esclerosis múltiple. [18] Los tratamientos actuales están dirigidos a mitigar la inflamación y los síntomas resultantes de los brotes agudos y la prevención de nuevos ataques con medicamentos modificadores de la enfermedad. [8] [19] La fisioterapia [7] y la terapia ocupacional , [20] junto con el manejo de los síntomas centrado en el paciente, pueden ayudar a mejorar la capacidad de las personas para funcionar. El resultado a largo plazo es difícil de predecir; los mejores resultados se observan con mayor frecuencia en mujeres, quienes desarrollan la enfermedad temprano en la vida, aquellos con un curso recurrente y aquellos que inicialmente experimentaron pocos ataques. [21]
La esclerosis múltiple es el trastorno inmunomediado más común que afecta al sistema nervioso central . [22] Casi un millón de personas en los Estados Unidos tenían EM en 2022, [23] y en 2020, alrededor de 2,8 millones de personas se vieron afectadas a nivel mundial, con tasas que varían ampliamente en diferentes regiones y entre diferentes poblaciones. [24] La enfermedad generalmente comienza entre los 20 y los 50 años y es dos veces más común en mujeres que en hombres. [2] La EM fue descrita por primera vez en 1868 por el neurólogo francés Jean-Martin Charcot . [25]
El nombre " esclerosis múltiple " es la abreviatura de esclerosis cerebroespinal múltiple , que se refiere a las numerosas cicatrices gliales (o escleróticas, esencialmente placas o lesiones) que se desarrollan en la sustancia blanca del cerebro y la médula espinal. [25]
Signos y síntomas
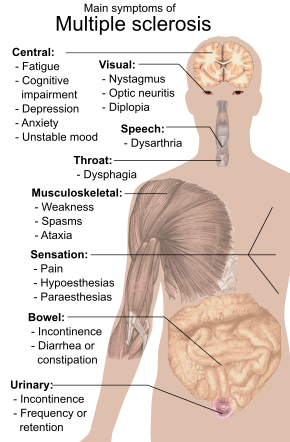
Como las lesiones de esclerosis múltiple (EM) pueden afectar cualquier parte del sistema nervioso central , una persona con EM puede tener casi cualquier síntoma o signo neurológico atribuible al sistema nervioso central.
La fatiga es uno de los síntomas más comunes de la EM. [26] [27] Alrededor del 65% de las personas con EM experimentan sintomatología de fatiga y, de estas, entre el 15 y el 40% informan que la fatiga es su síntoma de EM más incapacitante. [28]
Los problemas autonómicos , visuales, motores y sensoriales también se encuentran entre los síntomas más comunes. [1]
Los síntomas específicos están determinados por la ubicación de las lesiones dentro del sistema nervioso, y pueden incluir pérdida focal de sensibilidad o cambios en la sensibilidad en las extremidades, como sensación de hormigueo, alfileres y agujas, o entumecimiento; debilidad/dolor motor en las extremidades, visión borrosa , [29] reflejos pronunciados , espasmos musculares , dificultad para caminar, dificultades con la coordinación y el equilibrio ( ataxia ); problemas con el habla [30] o la deglución , problemas visuales ( neuritis óptica que se manifiesta como dolor ocular y pérdida de la visión, [31] o nistagmo que se manifiesta como visión doble ), fatiga y dificultades de vejiga e intestino (como incontinencia o retención urinaria o fecal), entre otros. [1] Cuando la esclerosis múltiple está más avanzada, pueden ocurrir dificultades para caminar y aumenta el riesgo de caídas. [32] [19] [33]
También son comunes las dificultades para pensar y los problemas emocionales, como la depresión o el estado de ánimo inestable . [1] [34] El principal déficit en la función cognitiva que experimentan las personas con EM es la disminución de la velocidad de procesamiento de la información, y la memoria también suele verse afectada, y la función ejecutiva con menos frecuencia. La inteligencia, el lenguaje y la memoria semántica suelen estar conservados, y el nivel de deterioro cognitivo varía considerablemente entre las personas con EM. [35] [36] [37]
El fenómeno de Uhthoff , un empeoramiento de los síntomas debido a la exposición a temperaturas más altas de lo habitual, y el signo de Lhermitte , una sensación eléctrica que recorre la espalda al doblar el cuello, son particularmente característicos de la EM, aunque pueden no estar siempre presentes. [1] Otra manifestación de presentación que es rara pero altamente sugestiva de un proceso desmielinizante como la EM es la oftalmoplejía internuclear bilateral, donde el paciente experimenta visión doble cuando intenta mover la mirada hacia la derecha y la izquierda. [38]
Alrededor del 60% o más de los pacientes con EM descubren que sus síntomas, en particular la fatiga, [39] se ven afectados por los cambios en la temperatura corporal. [40] [41] [42]
Medidas de discapacidad
La principal medida de discapacidad y gravedad es la escala ampliada del estado de discapacidad (EDSS), y otras medidas, como la escala compuesta funcional de la esclerosis múltiple, se utilizan cada vez más en la investigación. [43] [44] [45] La EDSS también se correlaciona con las caídas en personas con EM. [10] Si bien es una medida popular, la EDSS ha sido criticada por algunas de sus limitaciones, como depender demasiado de la caminata. [46] [10]
Curso de la enfermedad
Fase prodrómica
La EM puede tener una fase prodrómica en los años previos a su manifestación, caracterizada por problemas psiquiátricos, deterioro cognitivo y mayor uso de la atención médica. [47] [48]
Comienzo
La afección comienza en el 85% de los casos como un síndrome clínicamente aislado (CIS) durante varios días; el 45% presenta problemas motores o sensoriales, el 20% presenta neuritis óptica [31] y el 10% presenta síntomas relacionados con la disfunción del tronco encefálico , mientras que el 25% restante presenta más de una de las dificultades anteriores. [5] Con respecto a la neuritis óptica como el síntoma de presentación más común, las personas con EM notan una pérdida subaguda de la visión, a menudo asociada con un empeoramiento del dolor con el movimiento ocular y una visión reducida del color. El diagnóstico temprano de la neuritis óptica asociada a la EM ayuda a iniciar oportunamente los tratamientos específicos. Sin embargo, es crucial adherirse a los criterios de diagnóstico establecidos cuando se trata la neuritis óptica debido a la amplia gama de causas alternativas, como el trastorno del espectro de la neuromielitis óptica (NMOSD) y otras afecciones autoinmunes o infecciosas. El curso de los síntomas se presenta inicialmente en dos patrones principales: ya sea como episodios de empeoramiento repentino que duran unos días o meses (llamados recaídas , exacerbaciones, ataques o brotes) seguidos de mejoría (85% de los casos) o como un empeoramiento gradual con el tiempo sin períodos de recuperación (10-15% de los casos). [2] También puede ocurrir una combinación de estos dos patrones [13] o las personas pueden comenzar en un curso de recaídas y remisiones que luego se vuelve progresivo más adelante. [2]
Recaídas
Las recaídas suelen ser impredecibles y ocurren sin previo aviso. [1] Las exacerbaciones rara vez ocurren con una frecuencia mayor a dos veces al año. [1] Sin embargo, algunas recaídas están precedidas por desencadenantes comunes y ocurren con mayor frecuencia durante la primavera y el verano. [49] De manera similar, las infecciones virales como el resfriado común , la gripe o la gastroenteritis aumentan su riesgo. [1] El estrés también puede desencadenar un ataque. [50]
Se ha descubierto que muchos eventos no afectan las tasas de recaída que requieren hospitalización, entre ellos la vacunación , [51] [52] la lactancia materna , [1] el trauma físico, [53] y el fenómeno de Uhthoff . [49]
Embarazo
Muchas mujeres con EM que quedan embarazadas experimentan menos síntomas [54] [55] [56] Durante los primeros meses después del parto, el riesgo aumenta. [1] En general, el embarazo no parece influir en la discapacidad a largo plazo. [1]
Causas
La esclerosis múltiple es una enfermedad autoinmune que se origina por una combinación de causas genéticas y ambientales. Tanto las células T como las células B están implicadas, aunque a menudo se considera que las células T son la fuerza impulsora de la enfermedad. Las causas de la enfermedad no se comprenden por completo. Se ha demostrado que el virus de Epstein-Barr (VEB) está directamente presente en el cerebro de la mayoría de los casos de EM y el virus es transcripcionalmente activo en las células infectadas. [57] [58] Se cree que los antígenos nucleares del VEB están involucrados en la patogénesis de la esclerosis múltiple, pero no todas las personas con EM presentan signos de infección por VEB. [15] Se han identificado docenas de péptidos humanos en diferentes casos de la enfermedad, y aunque algunos tienen vínculos plausibles con organismos infecciosos o factores ambientales conocidos, otros no. [59]
Desregulación inmunológica
El fracaso de la eliminación de células inmunes autorreactivas tanto del sistema nervioso central como periférico está implicado en el desarrollo de la EM. [15] El timo es responsable de la tolerancia central del sistema inmunológico, donde las células T autorreactivas son destruidas sin ser liberadas a la circulación. A través de un mecanismo similar, las células B autorreactivas en la médula ósea son destruidas. Algunas células T y B autorreactivas pueden escapar a estos mecanismos de defensa, que es donde las defensas de tolerancia inmune periférica entran en acción al evitar que causen enfermedades. Sin embargo, estas líneas de defensa adicionales aún pueden fallar. [15] [19] Se proporcionan más detalles sobre la contribución de la desregulación inmunológica al riesgo de EM en la sección de fisiopatología de este artículo, así como en el artículo independiente sobre la fisiopatología de la EM .
Agentes infecciosos
Las primeras evidencias sugirieron la asociación entre varios virus con la encefalomielitis desmielinizante humana y la aparición de desmielinización en animales causada por algunas infecciones virales. [60] Uno de estos virus, el virus de Epstein-Barr (VEB), puede causar mononucleosis infecciosa e infecta a aproximadamente el 95% de los adultos, aunque solo una pequeña proporción de los infectados desarrollan posteriormente EM. [61] [16] [62] [58] Un estudio de más de 10 millones de miembros militares de EE. UU. comparó a 801 personas que desarrollaron EM con 1566 controles emparejados que no desarrollaron EM. El estudio encontró un riesgo 32 veces mayor de desarrollar EM después de la infección con VEB. No encontró un mayor riesgo después de la infección con otros virus, incluido el citomegalovirus similar . Estos hallazgos sugieren firmemente que el VEB desempeña un papel en la aparición de la EM, aunque el VEB por sí solo puede ser insuficiente para causarla. [16] [62]
El antígeno nuclear del virus de Epstein-Barr (VEB) , que es el marcador más consistente de la infección por VEB en todas las cepas, [63] ha sido identificado como una fuente directa de autorreactividad en el cuerpo humano. Estos antígenos parecen tener más probabilidades de promover respuestas autoinmunes en una persona que también tiene una deficiencia de vitamina D. La naturaleza exacta de esta relación es poco conocida. [64] [15]
Genética

La EM no se considera una enfermedad hereditaria , pero se ha demostrado que varias variaciones genéticas aumentan su riesgo. [65] Algunos de estos genes parecen tener niveles de expresión más altos en las células microgliales de lo esperado por casualidad. [66] La probabilidad de desarrollar EM es mayor en los familiares de una persona afectada, con un mayor riesgo entre aquellos más estrechamente relacionados. [8] Un gemelo idéntico de un individuo afectado tiene un 30% de posibilidades de desarrollar EM, un 5% para un gemelo no idéntico, un 2,5% para un hermano y una probabilidad aún menor para un medio hermano. [1] [8] [67] Si ambos padres están afectados, el riesgo en sus hijos es 10 veces mayor que el de la población general. [2] La EM también es más común en algunos grupos étnicos que en otros. [68]
Los genes específicos que se han vinculado con la EM incluyen diferencias en el sistema del antígeno leucocitario humano (HLA), un grupo de genes en el cromosoma 6 que sirve como complejo mayor de histocompatibilidad (MHC). [1] La contribución de las variantes de HLA a la susceptibilidad a la EM se conoce desde la década de 1980, [69] y esta misma región también se ha visto implicada en el desarrollo de otras enfermedades autoinmunes, como la diabetes tipo 1 y el lupus eritematoso sistémico . [69] El hallazgo más consistente es la asociación entre un mayor riesgo de desarrollar esclerosis múltiple y el alelo MHC DR15 , que está presente en el 30% de la población de EE. UU. y el norte de Europa. [15] [1] Otros loci exhiben un efecto protector, como HLA-C554 y HLA-DRB1 *11 . [1] Las diferencias de HLA representan un estimado del 20 al 60% de la predisposición genética . [69] Los estudios de asociación del genoma completo han revelado al menos 200 variantes fuera del locus HLA que afectan el riesgo de EM. [70]
Geografía

La prevalencia de la EM desde un punto de vista geográfico se asemeja a un gradiente, siendo más común en personas que viven más lejos del ecuador (por ejemplo, quienes viven en regiones del norte del mundo), aunque existen excepciones. La causa de este patrón geográfico no está clara, aunque se han propuesto como posibles explicaciones la exposición a la radiación ultravioleta B (UVB) y los niveles de vitamina D. [71] [15] Por lo tanto, se cree que quienes viven en regiones del norte del mundo tienen una menor exposición a la radiación UVB y, por lo tanto, niveles más bajos de vitamina D, que es un factor de riesgo conocido para desarrollar EM. [15] Inversamente, quienes viven en áreas de exposición solar relativamente mayor y, por lo tanto, mayor radiación UVB tienen un menor riesgo de desarrollar EM. [15] A partir de 2019, el gradiente de incidencia norte-sur todavía está presente y está aumentando. [72]
La EM es más común en regiones con poblaciones del norte de Europa, [1] por lo que la variación geográfica puede simplemente reflejar la distribución global de estas poblaciones de alto riesgo. [2]
Una relación entre la estación de nacimiento y la EM respalda esta idea: menos personas nacidas en el hemisferio norte en noviembre en comparación con mayo se ven afectadas más tarde en la vida. [73]
Los factores ambientales pueden desempeñar un papel durante la infancia; varios estudios han demostrado que las personas que se mudan a otra región del mundo antes de los 15 años adquieren el riesgo de padecer EM de la nueva región. Si la migración se produce después de los 15 años, las personas conservan el riesgo de su país de origen. [1] [74] Algunas pruebas indican que el efecto de la mudanza puede seguir aplicándose a las personas mayores de 15 años. [1]
Existen algunas excepciones al patrón geográfico mencionado anteriormente, entre ellas los grupos étnicos que tienen un riesgo bajo y que viven lejos del ecuador, como los samis , los amerindios , los huteritas canadienses , los maoríes de Nueva Zelanda [75] y los inuit de Canadá [71] , así como los grupos que tienen un riesgo relativamente alto y que viven más cerca del ecuador, como los sardos [71] , los sicilianos del interior [76] , los palestinos y los parsis [75] .
Impacto de la temperatura
Los síntomas de EM pueden aumentar si la temperatura corporal está desregulada. [77] [78] [79] La fatiga se ve particularmente afectada. [39] [40] [41] [42] [80] [81] [82] [83]
Otro
El tabaquismo puede ser un factor de riesgo independiente para la EM. [84] El estrés también puede ser un factor de riesgo, aunque la evidencia que lo apoya es débil. [74] Se ha evaluado la asociación con exposiciones ocupacionales y toxinas —principalmente disolventes orgánicos [85] —, pero no se han llegado a conclusiones claras. [74] Se estudiaron las vacunas como factores causales; sin embargo, la mayoría de los estudios no muestran asociación. [74] [86] Se han evaluado otros posibles factores de riesgo, como la dieta y la ingesta de hormonas , pero la evidencia sobre su relación con la enfermedad es "escasa y poco convincente". [84] La gota se presenta con menos frecuencia de lo que se esperaría y se han encontrado niveles más bajos de ácido úrico en personas con EM. Esto ha llevado a la teoría de que el ácido úrico es protector, aunque su importancia exacta sigue siendo desconocida. [87] La obesidad durante la adolescencia y la adultez temprana es un factor de riesgo para la EM. [88]
Fisiopatología

La esclerosis múltiple es una enfermedad autoinmune, mediada principalmente por células T. [15] Las tres características principales de la EM son la formación de lesiones en el sistema nervioso central (también llamadas placas), la inflamación y la destrucción de las vainas de mielina de las neuronas . Estas características interactúan de una manera compleja y aún no completamente comprendida para producir la degradación del tejido nervioso y, a su vez, los signos y síntomas de la enfermedad. [1] Se cree que el daño es causado, al menos en parte, por el ataque al sistema nervioso por parte del propio sistema inmunológico de una persona. [1]
Desregulación inmunológica
Como se detalla brevemente en la sección de causas de este artículo, actualmente se cree que la EM se origina de una falla del sistema inmunológico del cuerpo para matar las células T y B autorreactivas. [15] Actualmente, las subpoblaciones de células T que se cree que impulsan el desarrollo de la EM son las células T CD8+ autorreactivas, las células T auxiliares CD4+ y las células TH 17. Estas células T autorreactivas producen sustancias llamadas citocinas que inducen una respuesta inmune inflamatoria en el SNC, lo que conduce al desarrollo de la enfermedad. [15] Más recientemente, sin embargo, se ha dilucidado el papel de las células B autorreactivas. La evidencia de su contribución al desarrollo de la EM está implicada a través de la presencia de bandas de IgG oligoclonales (anticuerpos producidos por células B) en el LCR de pacientes con EM. [15] [19] La presencia de estas bandas oligoclonales se ha utilizado como evidencia de apoyo para confirmar un diagnóstico de EM. [89] Como se describió anteriormente, las células B también pueden producir citocinas que inducen una respuesta inmune inflamatoria a través de la activación de células T autorreactivas. [15] [90] Como tal, los niveles más altos de estas células B autorreactivas se asocian con un mayor número de lesiones y neurodegeneración, así como con una peor discapacidad. [15]
Otra población celular que está cada vez más implicada en la EM es la microglia . Estas células residen en el SNC y lo vigilan, respondiendo a los patógenos cambiando entre estados proinflamatorios y antiinflamatorios. Se ha demostrado que la microglia está involucrada en la formación de lesiones de EM y en otras enfermedades que afectan principalmente a la materia blanca del SNC. Aunque, debido a su capacidad para cambiar entre estados proinflamatorios y antiinflamatorios, también se ha demostrado que la microglia puede ayudar en la remielinización y la posterior reparación neuronal. [15] Como tal, se cree que la microglia participa tanto en las lesiones agudas como crónicas de la EM, y que el 40% de las células fagocíticas en las lesiones de EM activas tempranas son microglia proinflamatoria. [15]
Lesiones

El nombre esclerosis múltiple hace referencia a las cicatrices (escleróticas, más conocidas como placas o lesiones) que se forman en el sistema nervioso. Estas lesiones afectan con mayor frecuencia la materia blanca del nervio óptico , el tronco encefálico , los ganglios basales y la médula espinal , o los tractos de materia blanca cercanos a los ventrículos laterales . [1] La función de las células de la materia blanca es transportar señales entre las áreas de materia gris , donde se realiza el procesamiento, y el resto del cuerpo. El sistema nervioso periférico rara vez se ve afectado. [8]
.jpg/440px-MRI_machine_with_patient_(23423505123).jpg)
Para ser más específicos, la EM implica la pérdida de oligodendrocitos , las células responsables de crear y mantener una capa grasa, conocida como vaina de mielina , que ayuda a las neuronas a transportar señales eléctricas (potenciales de acción). [1] Esto da como resultado un adelgazamiento o pérdida completa de la mielina y, a medida que avanza la enfermedad, la degradación de los axones de las neuronas. Cuando se pierde la mielina, una neurona ya no puede conducir señales eléctricas de manera efectiva. [8] Un proceso de reparación, llamado remielinización , tiene lugar en las primeras fases de la enfermedad, pero los oligodendrocitos no pueden reconstruir completamente la vaina de mielina de la célula. [91] Los ataques repetidos conducen a remielinizaciones sucesivamente menos efectivas, hasta que se acumula una placa similar a una cicatriz alrededor de los axones dañados. [91] Estas cicatrices son el origen de los síntomas y durante un ataque, la resonancia magnética (IRM) a menudo muestra más de 10 placas nuevas. [1] Esto podría indicar que existe un cierto número de lesiones, por debajo de las cuales el cerebro es capaz de repararse a sí mismo sin producir consecuencias notables. [1] Otro proceso involucrado en la creación de lesiones es un aumento anormal en el número de astrocitos debido a la destrucción de neuronas cercanas. [1] Se han descrito varios patrones de lesiones . [92]
Inflamación
Además de la desmielinización, el otro signo de la enfermedad es la inflamación . Según una explicación inmunológica , el proceso inflamatorio es causado por las células T , un tipo de linfocitos que desempeñan un papel importante en las defensas del cuerpo. [8] Las células T entran en el cerebro como resultado de alteraciones en la barrera hematoencefálica . Las células T reconocen la mielina como extraña y la atacan, lo que explica por qué estas células también se denominan "linfocitos autorreactivos". [1]
El ataque a la mielina desencadena procesos inflamatorios que desencadenan la activación de otras células inmunitarias y la liberación de factores solubles como las citocinas y los anticuerpos . Una mayor ruptura de la barrera hematoencefálica, a su vez, provoca una serie de otros efectos perjudiciales, como la hinchazón , la activación de los macrófagos y una mayor activación de las citocinas y otras proteínas destructivas. [8] La inflamación puede reducir potencialmente la transmisión de información entre neuronas de al menos tres maneras. [1] Los factores solubles liberados podrían detener la neurotransmisión por neuronas intactas. Estos factores podrían provocar o potenciar la pérdida de mielina, o pueden hacer que el axón se descomponga por completo. [1]
Barrera hematoencefálica
La barrera hematoencefálica (BHE) es una parte del sistema capilar que impide la entrada de células T al sistema nervioso central. Puede volverse permeable a este tipo de células como consecuencia de una infección por un virus o bacteria. Después de repararse, generalmente una vez que la infección ha desaparecido, las células T pueden quedar atrapadas dentro del cerebro. [8] [93] El gadolinio no puede atravesar una BHE normal, por lo que se utiliza una resonancia magnética con gadolinio para mostrar las rupturas de la BHE. [94]
Fatiga por EM
La fisiopatología y los mecanismos que causan la fatiga en la EM no se comprenden bien. [95] [96] [97] La fatiga en la EM puede verse afectada por el calor corporal, [77] [79] y esto puede diferenciar la fatiga en la EM de otras formas de fatiga primaria. [39] [40] [83] La fatigabilidad (pérdida de fuerza) puede aumentar la percepción de fatiga, pero ambas medidas justifican una evaluación independiente en estudios clínicos. [98]
Diagnóstico


La esclerosis múltiple se diagnostica generalmente en función de los signos y síntomas que se presentan, junto con pruebas de laboratorio e imágenes médicas de apoyo. [5] Puede ser difícil de confirmar, especialmente al principio, ya que los signos y síntomas pueden ser similares a los de otros problemas médicos. [1] [99]
Criterios de McDonald
Los criterios de McDonald , que se centran en la evidencia clínica, de laboratorio y radiológica de lesiones en diferentes momentos y en diferentes áreas, son el método de diagnóstico más comúnmente utilizado [100] y los criterios de Schumacher y Poser tienen una importancia principalmente histórica. [101] Los criterios de McDonald establecen que los pacientes con esclerosis múltiple deben tener lesiones diseminadas en el tiempo (DIT) y diseminadas en el espacio (DIS), es decir, lesiones que han aparecido en diferentes áreas del cerebro y en diferentes momentos. [89] A continuación, se presenta un esquema abreviado de los Criterios de McDonald de 2017 para el diagnóstico de EM.
- Al menos 2 ataques clínicos con resonancia magnética que muestren 2 o más lesiones características de la EM. [89]
- Al menos 2 ataques clínicos con resonancia magnética que muestra 1 lesión característica de EM con evidencia histórica clara de un ataque previo que involucra una lesión en una ubicación distinta en el SNC. [89]
- Al menos 2 ataques clínicos con resonancia magnética que muestra 1 lesión característica de EM, con DIT establecida por un ataque clínico adicional en un sitio del SNC distinto o por resonancia magnética que muestra una lesión antigua de EM. [89]
- 1 ataque clínico con RMN que muestre al menos 2 lesiones características de EM, con DIT establecida por un ataque adicional, por RMN que muestre lesiones antiguas de EM o presencia de bandas oligoclonales en el LCR. [89]
- 1 ataque clínico con RMN que muestra 1 lesión característica de EM, con DIS establecida por un ataque adicional en un sitio diferente del SNC o por RMN que muestra lesiones antiguas de EM, y DIT establecida por un ataque adicional, por RMN que muestra lesiones antiguas de EM, o presencia de bandas oligoclonales en el LCR. [89]
A partir de 2017 [update], ninguna prueba por sí sola (incluida la biopsia) puede proporcionar un diagnóstico definitivo. [102]
Resonancia magnética
La resonancia magnética del cerebro y la columna vertebral puede mostrar áreas de desmielinización (lesiones o placas). El gadolinio puede administrarse por vía intravenosa como medio de contraste para resaltar las placas activas y, por eliminación, demostrar la existencia de lesiones históricas no asociadas a síntomas en el momento de la evaluación. [103] [104]
Se ha propuesto que los signos de las venas centrales (SVC) son un buen indicador de EM en comparación con otras afecciones que causan lesiones blancas. [105] [106] [107] [108] Un estudio pequeño encontró menos SVC en personas mayores e hipertensas. [109] Se están realizando más investigaciones sobre los SVC como biomarcador de EM. [110]
Visibilidad de la lesión in vivo y postoperatoria en exploraciones de resonancia magnética
Sólo la resonancia magnética post mortem permite la visualización de lesiones submilimétricas en las capas corticales y en la corteza cerebelosa. [111]
Líquido cefalorraquídeo (punción lumbar)
El análisis del líquido cefalorraquídeo obtenido a partir de una punción lumbar puede proporcionar evidencia de inflamación crónica en el sistema nervioso central. El líquido cefalorraquídeo se analiza en busca de bandas oligoclonales de IgG en la electroforesis , que son marcadores de inflamación que se encuentran en el 75-85% de las personas con EM. [103] [112]
Diagnóstico diferencial
Varias enfermedades se presentan de manera similar a la EM. [113] [114] Los profesionales médicos utilizan la presentación específica del paciente, la historia clínica y los hallazgos del examen para hacer un diagnóstico diferencial individualizado . Las señales de alerta son hallazgos que sugieren un diagnóstico alternativo, aunque no descartan la EM. Las señales de alerta incluyen un paciente menor de 15 años o mayor de 60, menos de 24 horas de síntomas, afectación de múltiples nervios craneales , afectación de órganos fuera del sistema nervioso y hallazgos atípicos en los exámenes y el laboratorio. [113] [114]
En un contexto de emergencia, es importante descartar un accidente cerebrovascular o sangrado en el cerebro. [114] Los vómitos intratables, la neuritis óptica grave [31] o la neuritis óptica bilateral [31] aumentan la sospecha de un trastorno del espectro de la neuromielitis óptica (NMOSD). [115] Las enfermedades infecciosas que pueden parecerse a la esclerosis múltiple incluyen el VIH, la enfermedad de Lyme y la sífilis . Las enfermedades autoinmunes incluyen la neurosarcoidosis , el lupus , el síndrome de Guillain-Barré , la encefalomielitis diseminada aguda y la enfermedad de Behçet . Las afecciones psiquiátricas como la ansiedad o el trastorno de conversión también pueden presentarse de manera similar. Otras enfermedades raras en el diagnóstico diferencial incluyen el linfoma del SNC , las leucodistrofias congénitas y la mielitis asociada a anti-MOG . [113] [114]
Tipos y variantes

Se han descrito varios fenotipos (comúnmente denominados "tipos") o patrones de progresión. Los fenotipos utilizan la evolución anterior de la enfermedad para intentar predecir la evolución futura. Son importantes no sólo para el pronóstico, sino también para las decisiones de tratamiento.
El Comité Asesor Internacional sobre Ensayos Clínicos de EM describe cuatro tipos de EM (revisados en 2013) en lo que se conoce como la clasificación de Lublin : [116] [117]
- Síndrome clínicamente aislado (CIS)
- Esclerosis múltiple remitente-recurrente (EMRR)
- Esclerosis múltiple progresiva primaria (EMPP)
- Esclerosis múltiple progresiva secundaria (EMSP)
El síndrome de CIS puede caracterizarse como una lesión única observada en la resonancia magnética que se asocia con signos o síntomas encontrados en la EM. Debido a los criterios de McDonald, no cumple completamente los criterios para ser diagnosticado como EM, por lo que se lo denomina "síndrome clínicamente aislado". El síndrome de CIS puede verse como el primer episodio de desmielinización en el sistema nervioso central. Para clasificarse como síndrome de CIS, el ataque debe durar al menos 24 horas y debe ser causado por inflamación o desmielinización del sistema nervioso central . [1] [118] Los pacientes que sufren de síndrome de CIS pueden o no desarrollar EM, pero entre el 30 y el 70 % de las personas que experimentan síndrome de CIS desarrollarán EM más adelante. [119]
La EM RR se caracteriza por recaídas impredecibles seguidas de períodos de meses a años de relativa calma ( remisión ) sin nuevos signos de actividad de la enfermedad. Los déficits que ocurren durante los ataques pueden resolverse o dejar problemas , esto último en alrededor del 40% de los ataques y siendo más común cuanto más tiempo una persona ha tenido la enfermedad. [1] [5] Esto describe el curso inicial del 80% de las personas con EM. [1]
La EMPP se presenta en aproximadamente el 10-20% de las personas con la enfermedad, sin remisión después de los síntomas iniciales. [5] [120] Se caracteriza por la progresión de la discapacidad desde el inicio, sin remisiones y mejoras o solo ocasionales y menores. [13] La edad habitual de aparición del subtipo progresivo primario es posterior a la del subtipo remitente-recurrente. Es similar a la edad en la que suele comenzar la progresiva secundaria en la EMRR, alrededor de los 40 años de edad. [1]
La EMSP se presenta en alrededor del 65% de las personas con EMRR inicial, quienes eventualmente presentan un deterioro neurológico progresivo entre ataques agudos sin períodos definidos de remisión. [1] [13] Pueden aparecer recaídas ocasionales y remisiones menores. [13] El período de tiempo más común entre el inicio de la enfermedad y la conversión de EMRR a EMSP es de 19 años. [121]
Cursos especiales
Independientemente de los tipos publicados por las asociaciones de EM, las agencias reguladoras como la FDA a menudo consideran cursos especiales, tratando de reflejar algunos resultados de ensayos clínicos en sus documentos de aprobación. Algunos ejemplos podrían ser "EM altamente activa" (HAMS), [122] "EM secundaria activa" (similar a la antigua EM progresiva-recidivante) [123] y "EMPP de rápida progresión". [124]
Además, a los déficits que siempre se resuelven entre ataques a veces se los denomina EM "benigna", [125] aunque las personas aún acumulan cierto grado de discapacidad a largo plazo. [1] Por otro lado, el término esclerosis múltiple maligna se utiliza para describir a las personas con EM que han alcanzado un nivel significativo de discapacidad en un período corto. [126]
Un panel internacional ha publicado una definición estandarizada para el curso HAMS. [122]
Variantes
Se han descrito variantes atípicas de la EM, entre ellas la esclerosis múltiple tumefactiva , la esclerosis concéntrica de Balo , la esclerosis difusa de Schilder y la esclerosis múltiple de Marburgo . Aún se debate si son variantes de la EM o enfermedades diferentes. [127] Algunas enfermedades que antes se consideraban variantes de la EM, como la enfermedad de Devic , ahora se consideran fuera del espectro de la EM. [128]
Gestión
Aunque no se ha encontrado una cura para la esclerosis múltiple, varias terapias han demostrado ser útiles. Varios tratamientos eficaces pueden reducir la cantidad de ataques y la velocidad de progresión. [23] Los objetivos principales de la terapia son recuperar la función después de un ataque, prevenir nuevos ataques y prevenir la discapacidad. Generalmente se recomienda comenzar a tomar medicamentos en personas después del primer ataque cuando se observan más de dos lesiones en la resonancia magnética. [129]
Los primeros medicamentos aprobados para tratar la EM fueron moderadamente eficaces, aunque eran mal tolerados y tenían muchos efectos adversos. [3] Se han introducido varias opciones de tratamiento con mejores perfiles de seguridad y tolerabilidad, [23] mejorando el pronóstico de la EM.
Al igual que con cualquier tratamiento médico, los medicamentos utilizados para el tratamiento de la EM tienen varios efectos adversos . Algunas personas recurren a tratamientos alternativos , a pesar de la falta de evidencia que respalde su eficacia.
Manejo inicial del brote agudo
Durante los ataques sintomáticos, la administración de dosis altas de corticosteroides intravenosos , como la metilprednisolona , es la terapia habitual, [1] y los corticosteroides orales parecen tener un perfil de eficacia y seguridad similar. [130] Aunque son eficaces a corto plazo para aliviar los síntomas, los tratamientos con corticosteroides no parecen tener un impacto significativo en la recuperación a largo plazo. [131] [132] El beneficio a largo plazo no está claro en la neuritis óptica a partir de 2020. [133] [31] Las consecuencias de los ataques graves que no responden a los corticosteroides podrían ser tratables mediante plasmaféresis . [1]
Manejo crónico
Esclerosis múltiple remitente-recurrente
Las agencias reguladoras aprobaron múltiples medicamentos modificadores de la enfermedad para la EM RR; son moderadamente eficaces para reducir la cantidad de ataques. [134] Los interferones [135] y el acetato de glatiramer son tratamientos de primera línea [5] y son aproximadamente equivalentes, reduciendo las recaídas en aproximadamente un 30%. [136] La terapia a largo plazo iniciada tempranamente es segura y mejora los resultados. [137] [138]
El tratamiento del CIS con interferones disminuye la probabilidad de progresar a EM clínica. [1] [139] [140] Se ha estimado que la eficacia de los interferones y el acetato de glatiramer en niños es aproximadamente equivalente a la de los adultos. [141] El papel de algunos agentes más nuevos como fingolimod , [142] teriflunomida y dimetilfumarato , [143] aún no está completamente claro. [144] Sacar conclusiones firmes sobre el mejor tratamiento es difícil, especialmente con respecto al beneficio y la seguridad a largo plazo del tratamiento temprano, dada la falta de estudios que comparen directamente las terapias modificadoras de la enfermedad o el seguimiento a largo plazo de los resultados de los pacientes. [145]
La efectividad relativa de los diferentes tratamientos no está clara, ya que la mayoría solo se ha comparado con placebo o un pequeño número de otras terapias. [146] Las comparaciones directas de interferones y acetato de glatiramer indican efectos similares o solo pequeñas diferencias en los efectos sobre la tasa de recaídas, la progresión de la enfermedad y las mediciones de MRI. [147] Existe una alta confianza en que natalizumab, cladribina o alemtuzumab están disminuyendo las recaídas durante un período de dos años para las personas con EMRR. [148] Natalizumab e interferón beta-1a ( Rebif ) pueden reducir las recaídas en comparación con placebo e interferón beta-1a (Avonex), mientras que interferón beta-1b ( Betaseron ), acetato de glatiramer y mitoxantrona también pueden prevenir las recaídas. [ 146] La evidencia sobre la efectividad relativa en la reducción de la progresión de la discapacidad no está clara. [146] Existe una confianza moderada en que un tratamiento de dos años con natalizumab retrasa la progresión de la discapacidad para las personas con EMRR. [148] Todos los medicamentos están asociados con efectos adversos que pueden influir en sus perfiles de riesgo-beneficio. [146] [148]
El ublituximab fue aprobado para uso médico en los Estados Unidos en diciembre de 2022. [149]
Medicamentos
Descripción general de los medicamentos disponibles para la EM. [150]
| Medicamento | Compuesto | Productor | Usar | Eficacia (tasa anualizada de reducción de recaídas) | Tasa de recaída anualizada (ARR) |
|---|---|---|---|---|---|
| Avonex | Interferón beta-1a | Biogen | Intramuscular | 30% | 0,25 |
| Rebif | Interferón beta-1a | Merck Serono | Subcutáneo | 30% | 0,256 |
| Extavia | Interferón beta-1b | Bayer Schering | Subcutáneo | 30% | 0,256 |
| Copaxona | Acetato de glatiramer | Productos farmacéuticos Teva | Subcutáneo | 30% | 0.3 |
| Aubagio | Teriflunomida | Genzima | Oral | 30% | 0,35 |
| Plegridia | Interferón beta-1a | Biogen | Subcutáneo | 30% | 0,12 |
| Tecfidera | Fumarato de dimetilo | Biogen | Oral | 50% | 0,15 |
| Vumeridad | Fumarato de diroximel | Biogen | Oral | 50% | 0,11-0,15 |
| Gilenya | Fingolimod | Oral | 50% | 0,22-0,25 | |
| Ceposia | Ozanimod | [ Se necesita una mejor fuente ] | Oral | 0,18-0,24 | |
| Sensación | Ofatumumab | Subcutáneo | 70% | 0,09-0,14 | |
| Mavenvestido | Cladribina | Oral | 70% | 0,1-0,14 | |
| Lemtrada | Alemtuzumab | Intravenoso | 70% | 0,08 | |
| Ocrevus | Ocrelizumab | Intravenoso | 70% | 0,09 | |
| Ocrevus Zunovo | Ocrelizumab/hialuronidasa | Subcutáneo |
Esclerosis múltiple progresiva
En 2011, la mitoxantrona fue el primer medicamento aprobado para la EM progresiva secundaria. [151] En esta población, la evidencia provisional apoya que la mitoxantrona desacelera moderadamente la progresión de la enfermedad y disminuye las tasas de recaídas en un período de dos años. [152] [153]
Siguen apareciendo nuevos medicamentos aprobados. En marzo de 2017, la FDA aprobó el ocrelizumab como tratamiento para la EM progresiva primaria en adultos, el primer fármaco en obtener esa aprobación, [154] [155] [156] con requisitos para varios ensayos clínicos de fase IV . [157] También se utiliza para el tratamiento de formas recurrentes de esclerosis múltiple, que incluyen el síndrome clínicamente aislado, la enfermedad recurrente-remitente y la enfermedad progresiva secundaria activa en adultos. [156] Según una revisión Cochrane de 2021 , el ocrelizumab puede reducir el empeoramiento de los síntomas de la EM progresiva primaria y probablemente aumenta los efectos no deseados, pero hace poca o ninguna diferencia en el número de efectos no deseados graves. [158]
En 2019, el siponimod y la cladribina fueron aprobados en los Estados Unidos para el tratamiento de la esclerosis múltiple progresiva secundaria (EMSP). [154] Posteriormente, el ozanimod fue aprobado en 2020 y el ponesimod fue aprobado en 2021, ambos aprobados para el tratamiento del CIS, la EM recurrente y la EMSP en los EE. UU., y la EMRR en Europa. [159]
El ocrelizumab/hialuronidasa fue aprobado para uso médico en los Estados Unidos en septiembre de 2024. [160] [161]
Efectos adversos

Los tratamientos modificadores de la enfermedad tienen varios efectos adversos. Uno de los más comunes es la irritación en el lugar de la inyección del acetato de glatiramer y los interferones (hasta el 90% con inyecciones subcutáneas y el 33% con inyecciones intramusculares). [135] [162] Con el tiempo, puede desarrollarse una abolladura visible en el lugar de la inyección, debido a la destrucción local del tejido graso, conocida como lipoatrofia . [162] Los interferones pueden producir síntomas similares a los de la gripe ; [163] algunas personas que toman glatiramer experimentan una reacción posterior a la inyección con enrojecimiento, opresión en el pecho, palpitaciones cardíacas y ansiedad, que generalmente dura menos de treinta minutos. [164] Más peligrosos pero mucho menos comunes son el daño hepático por interferones, [165] la disfunción sistólica (12%), la infertilidad y la leucemia mieloide aguda (0,8%) por mitoxantrona, [152] [166] y la leucoencefalopatía multifocal progresiva que ocurre con natalizumab (que ocurre en 1 de cada 600 personas tratadas). [5] [167]
El fingolimod puede provocar hipertensión y frecuencia cardíaca lenta , edema macular , enzimas hepáticas elevadas o una reducción en los niveles de linfocitos . [142] [144] La evidencia tentativa apoya la seguridad a corto plazo de la teriflunomida, con efectos secundarios comunes que incluyen: dolores de cabeza, fatiga, náuseas, pérdida de cabello y dolor en las extremidades. [134] También ha habido informes de insuficiencia hepática y leucoencefalopatía multifocal progresiva con su uso y es peligroso para el desarrollo fetal . [144] Los efectos secundarios más comunes del dimetilfumarato son sofocos y problemas gastrointestinales. [143] [168] [144] Si bien el dimetilfumarato puede provocar una reducción en el recuento de glóbulos blancos, no se informaron casos de infecciones oportunistas durante los ensayos. [169]
Síntomas asociados
Se ha demostrado que tanto los medicamentos como la neurorrehabilitación mejoran algunos síntomas, aunque ninguno cambia el curso de la enfermedad. [170] Algunos síntomas tienen una buena respuesta a la medicación, como la espasticidad de la vejiga , mientras que otros cambian poco. [1] Los equipos como los catéteres para la disfunción de la vejiga neurogénica o las ayudas para la movilidad pueden ser útiles para mejorar el estado funcional.
Un enfoque multidisciplinario es importante para mejorar la calidad de vida; sin embargo, es difícil especificar un "equipo central" ya que pueden necesitarse muchos servicios de salud en diferentes momentos. [1] Los programas de rehabilitación multidisciplinarios aumentan la actividad y la participación de las personas con EM, pero no influyen en el nivel de deterioro. [171] Los estudios que investigan la provisión de información en apoyo de la comprensión y participación del paciente sugieren que, si bien las intervenciones (información escrita, ayudas para la toma de decisiones, entrenamiento, programas educativos) pueden aumentar el conocimiento, la evidencia de un efecto en la toma de decisiones y la calidad de vida es mixta y de baja certeza. [172] Existe evidencia limitada de la eficacia general de las disciplinas terapéuticas individuales, [173] [174] aunque hay buena evidencia de que enfoques específicos, como el ejercicio, [175] [176] [177] [178] y las terapias psicológicas son efectivas. [179] El entrenamiento cognitivo, solo o combinado con otras intervenciones neuropsicológicas, puede mostrar efectos positivos para la memoria y la atención, aunque no es posible sacar conclusiones firmes dado el pequeño número de muestras, la metodología variable, las intervenciones y las medidas de resultados. [180] La eficacia de los enfoques paliativos además de la atención estándar es incierta, debido a la falta de evidencia. [181] La eficacia de las intervenciones, incluido el ejercicio, específicamente para la prevención de caídas en personas con EM es incierta, mientras que hay cierta evidencia de un efecto sobre la función del equilibrio y la movilidad. [182] La terapia cognitivo-conductual ha demostrado ser moderadamente eficaz para reducir la fatiga de la EM. [183] La evidencia de la eficacia de las intervenciones no farmacológicas para el dolor crónico es insuficiente para recomendar dichas intervenciones por sí solas, sin embargo, su uso en combinación con medicamentos puede ser razonable. [184]
No farmacéutico
Existe cierta evidencia de que la terapia acuática es una intervención beneficiosa. [185]
La espasticidad asociada con la EM puede ser difícil de controlar debido al curso progresivo y fluctuante de la enfermedad. [186] Aunque no hay una conclusión firme sobre la eficacia para reducir la espasticidad, las intervenciones de fisioterapia pueden ser una opción segura y beneficiosa para los pacientes con esclerosis múltiple. La fisioterapia, que incluye intervenciones de vibración, estimulación eléctrica, terapia de ejercicios, terapia de pie y terapia de ondas de choque radiales (RSWT), resultó beneficiosa para limitar la espasticidad, ayudar a limitar la excitabilidad o aumentar el rango de movimiento. [187]
Tratamientos alternativos
Más del 50% de las personas con EM pueden utilizar medicina complementaria y alternativa , aunque los porcentajes varían dependiendo de cómo se defina la medicina alternativa. [188] En cuanto a las características de los usuarios, son más frecuentemente mujeres, han tenido EM durante más tiempo, tienden a ser más discapacitados y tienen menores niveles de satisfacción con la atención médica convencional. [188] La evidencia de la efectividad de tales tratamientos en la mayoría de los casos es débil o nula. [188] [189] Los tratamientos de beneficio no probado utilizados por personas con EM incluyen suplementos dietéticos y regímenes, [188] [190] [191] vitamina D , [192] técnicas de relajación como el yoga , [188] medicina herbal (incluido el cannabis medicinal ), [188] [193] [194] terapia de oxígeno hiperbárico , [195] autoinfección con anquilostomas , reflexología , acupuntura , [188] [196] y mindfulness . [197] La evidencia sugiere que la suplementación con vitamina D, independientemente de la forma y la dosis, no proporciona ningún beneficio para las personas con EM; esto incluye medidas como la recurrencia de la recaída, la discapacidad y las lesiones de la resonancia magnética, mientras que los efectos sobre la calidad de vida relacionada con la salud y la fatiga no están claros. [198] No hay evidencia suficiente que respalde la biotina en dosis altas [199] [200] [201] y alguna evidencia de una mayor actividad de la enfermedad y un mayor riesgo de recaída con su uso. [202] Una revisión reciente de la efectividad del cannabis y los cannabinoides (2022) encontró que, en comparación con el placebo, los nabiximols probablemente reducen la gravedad de la espasticidad a corto plazo. [203]
Pronóstico
La disponibilidad de tratamientos que modifican el curso de la esclerosis múltiple a partir de la década de 1990, conocidos como terapias modificadoras de la enfermedad (TME), ha mejorado el pronóstico. Estos tratamientos pueden reducir las recaídas y retardar la progresión, pero no existe cura. [23] [204]
El pronóstico de la EM depende del subtipo de la enfermedad y existe una considerable variación individual en la progresión de la enfermedad. [205] En la EM recurrente, el subtipo más común, un estudio de cohorte de 2016 encontró que después de una mediana de 16,8 años desde el inicio, uno de cada diez necesitaba una ayuda para caminar y casi dos de cada diez pasaban a la EM progresiva secundaria, una forma caracterizada por un deterioro más progresivo. [23] Con los tratamientos disponibles en la década de 2020, las recaídas se pueden eliminar o reducir sustancialmente. Sin embargo, todavía se produce una "progresión silenciosa" de la enfermedad. [204] [206]
Además de la EM progresiva secundaria (EMSP), una pequeña proporción de personas con EM (10-15%) experimenta un deterioro progresivo desde el inicio, conocido como EM progresiva primaria (EMPP). La mayoría de los tratamientos han sido aprobados para su uso en la EM recurrente; hay menos tratamientos con menor eficacia para las formas progresivas de EM. [207] [204] [23] El pronóstico para la EM progresiva es peor, con una acumulación más rápida de discapacidad, aunque con una variación individual considerable. [207] En la EMPP no tratada, el tiempo medio desde el inicio hasta la necesidad de una ayuda para caminar se estima en siete años. [23] En la EMSP, un estudio de cohorte de 2014 informó que las personas necesitaban una ayuda para caminar después de un promedio de cinco años desde el inicio de la EMSP, y estaban confinadas a una silla o cama después de un promedio de quince años. [208]
Después del diagnóstico de EM, las características que predicen un peor curso son el sexo masculino, la edad avanzada y una mayor discapacidad en el momento del diagnóstico; el sexo femenino se asocia con una mayor tasa de recaídas. [209] Actualmente, ningún biomarcador puede predecir con precisión la progresión de la enfermedad en cada paciente. [205] Las lesiones de la médula espinal, las anomalías en la resonancia magnética y una mayor atrofia cerebral predicen un peor curso, aunque la atrofia cerebral como predictor del curso de la enfermedad es experimental y no se utiliza en la práctica clínica. [209] El tratamiento temprano conduce a un mejor pronóstico, pero una mayor frecuencia de recaídas cuando se trata con DMT se asocia con un peor pronóstico. [205] [209] Un estudio poblacional longitudinal de 60 años realizado en Noruega encontró que aquellos con EM tenían una expectativa de vida siete años menor que la población general. La expectativa de vida media para los pacientes con EM RR fue de 77,8 años y 71,4 años para EM PP, en comparación con 81,8 años para la población general. La expectativa de vida para los hombres fue cinco años menor que para las mujeres. [210]
Epidemiología
This section needs to be updated. (July 2022) |

La EM es el trastorno autoinmune más común del sistema nervioso central. [22] La última estimación del número total de personas con EM fue de 2,8 millones a nivel mundial, con una prevalencia de 36 por cada 100.000 personas. Además, la prevalencia varía ampliamente en diferentes regiones del mundo. [24] En África, hay cinco personas por cada 100.000 diagnosticadas con EM, en comparación con el Sudeste Asiático, donde la prevalencia es de nueve por cada 100.000, 112 por cada 100.000 en las Américas y 133 por cada 100.000 en Europa. [211]
El aumento de las tasas de EM puede explicarse simplemente por un mejor diagnóstico. [2] Los estudios sobre patrones poblacionales y geográficos han sido comunes [212] y han dado lugar a varias teorías sobre la causa. [17] [74] [84]
La EM suele aparecer en adultos de entre veinte y treinta años o de treinta y pocos, pero rara vez puede comenzar en la infancia y después de los 50 años. [2] [100] El subtipo progresivo primario es más común en personas de cincuenta años. [120] De manera similar a muchos trastornos autoinmunes, la enfermedad es más común en mujeres y la tendencia puede estar aumentando. [1] [213] A partir de 2020, a nivel mundial es aproximadamente dos veces más común en mujeres que en hombres, y la proporción de mujeres a hombres con EM es tan alta como 4:1 en algunos países. [214] [ cita médica necesaria ] En los niños, es incluso más común en mujeres que en hombres, [1] mientras que en personas mayores de cincuenta, afecta a hombres y mujeres casi por igual. [120]
Historia
Descubrimiento médico

Robert Carswell (1793-1857), profesor británico de patología , y Jean Cruveilhier (1791-1873), profesor francés de anatomía patológica, describieron e ilustraron muchos de los detalles clínicos de la enfermedad, pero no la identificaron como una enfermedad separada. [215] En concreto, Carswell describió las lesiones que encontró como "una lesión notable de la médula espinal acompañada de atrofia". [1] Bajo el microscopio, el patólogo suizo Georg Eduard Rindfleisch (1836-1908) observó en 1863 que las lesiones asociadas a la inflamación se distribuían alrededor de los vasos sanguíneos. [216] [217]
El neurólogo francés Jean-Martin Charcot (1825-1893) fue la primera persona en reconocer la esclerosis múltiple como una enfermedad distinta en 1868. [215] Resumiendo informes anteriores y añadiendo sus propias observaciones clínicas y patológicas, Charcot llamó a la enfermedad esclerosis en placas .
Historial de diagnóstico
El primer intento de establecer un conjunto de criterios diagnósticos se debió también a Charcot en 1868. Publicó lo que hoy se conoce como la " Tríada de Charcot ", que consiste en nistagmo, temblor intencional y habla telegráfica (habla de exploración). [218] Charcot también observó cambios cognitivos, describiendo a sus pacientes como portadores de un "marcado debilitamiento de la memoria" y "conceptos que se formaban lentamente". [25]
El diagnóstico se basaba en la tríada de Charcot y la observación clínica hasta que Schumacher hizo el primer intento de estandarizar los criterios en 1965 introduciendo algunos requisitos fundamentales: la diseminación de las lesiones en el tiempo (DIT) y el espacio (DIS), y que "los signos y síntomas no pueden explicarse mejor por otro proceso patológico". [218] El requisito de DIT y DIS fue heredado posteriormente por los criterios de Poser y McDonald, cuya revisión de 2017 está en uso. [218] [205]
Durante el siglo XX se desarrollaron teorías sobre la causa y la patogenia y en la década de 1990 comenzaron a aparecer tratamientos eficaces. [1] Desde principios del siglo XXI se han producido mejoras en los conceptos. La revisión de 2010 de los criterios de McDonald permitió el diagnóstico de EM con una sola lesión comprobada (CIS). [219]
En 1996, la Sociedad Nacional de Esclerosis Múltiple de Estados Unidos (NMSS) (Comité Asesor de Ensayos Clínicos) definió la primera versión de los fenotipos clínicos que se utilizan actualmente. En esta primera versión, se proporcionaron definiciones estandarizadas para cuatro cursos clínicos de EM: recurrente-remitente (RR), progresiva secundaria (SP), progresiva primaria (PP) y progresiva recurrente (PR). En 2010, se eliminó la PR y se incorporó el CIS. [219] Tres años después, la revisión de 2013 de los "fenotipos para el curso de la enfermedad" se vio obligada a considerar el CIS como uno de los fenotipos de la EM, lo que hizo obsoletas algunas expresiones como "conversión de CIS a EM". [220] Otras organizaciones han propuesto posteriormente nuevos fenotipos clínicos, como HAMS (EM altamente activa). [221]
Casos históricos
.jpg/440px-Animal_locomotion._Plate_541_(Boston_Public_Library).jpg)
Hay varios relatos históricos de personas que probablemente tuvieron EM y vivieron antes o poco después de que Charcot describiera la enfermedad.
Una joven llamada Halldora, que vivió en Islandia alrededor del año 1200, perdió repentinamente la visión y la movilidad, pero las recuperó siete días después. Santa Liduvina de Schiedam (1380-1433), una monja holandesa , puede ser una de las primeras personas claramente identificables con EM. Desde los 16 años hasta su muerte a los 53, tuvo dolor intermitente, debilidad en las piernas y pérdida de visión: síntomas típicos de la EM. [222] Ambos casos han llevado a la propuesta de una hipótesis del "gen vikingo" para la difusión de la enfermedad. [223]
Augustus Frederick d'Este (1794-1848), hijo del príncipe Augustus Frederick, duque de Sussex y lady Augusta Murray y nieto de Jorge III del Reino Unido , casi con certeza tenía EM. D'Este dejó un diario detallado que describe sus 22 años viviendo con la enfermedad. Su diario comenzó en 1822 y terminó en 1846, aunque permaneció desconocido hasta 1948. Sus síntomas comenzaron a los 28 años con una pérdida visual repentina y transitoria ( amaurosis fugaz ) después del funeral de un amigo. Durante su enfermedad, desarrolló debilidad en las piernas, torpeza en las manos, entumecimiento, mareos, alteración de la vejiga y disfunción eréctil . En 1844, comenzó a usar una silla de ruedas. A pesar de su enfermedad, mantuvo una visión optimista de la vida. [224] [225] Otro relato temprano de EM fue llevado por el diarista británico WNP Barbellion , seudónimo de Bruce Frederick Cummings (1889-1919), quien mantuvo un registro detallado de su diagnóstico y lucha. [225] Su diario fue publicado en 1919 como The Journal of a Disappointed Man . [226] Charles Dickens , un observador agudo, describió una posible neuritis óptica bilateral con visión de contraste reducida y el fenómeno de Uhthoff en el personaje femenino principal de Bleak House (1852-1853), Esther Summerville. [227]
Investigación
Virus de Epstein-Barr
A partir de 2022, se investiga activamente la patogenia de la EM en relación con el virus de Epstein-Barr (VEB) , al igual que las terapias modificadoras de la enfermedad; se busca comprender cómo los factores de riesgo se combinan con el VEB para iniciar la EM. Se podría entender mejor si el VEB es la única causa de la EM si se desarrolla una vacuna contra el VEB y se demuestra que también previene la EM. [16]
Aunque una variedad de estudios han demostrado la conexión entre una infección por VEB y un desarrollo posterior de esclerosis múltiple, los mecanismos detrás de esta correlación no están completamente claros y se han propuesto varias teorías para explicar la relación entre las dos enfermedades. Se cree que la participación de las células B infectadas por VEB (linfocitos B) [228] y la participación de los anticuerpos anti- EBNA , que parecen ser significativamente mayores en pacientes con esclerosis múltiple, juegan un papel crucial en el desarrollo de la enfermedad. [229] Esto está respaldado por el hecho de que el tratamiento contra las células B, por ejemplo, ocrelizumab , reduce los síntomas de la esclerosis múltiple: las recaídas anuales aparecen con menos frecuencia y la progresión de la discapacidad es más lenta. [230] Un estudio de la Universidad de Stanford de 2022 ha demostrado que durante una infección por VEB, puede ocurrir un mimetismo molecular, donde el sistema inmunológico producirá anticuerpos contra la proteína EBNA 1, que al mismo tiempo es capaz de unirse a GlialCAM en la mielina. Además, observaron un fenómeno poco común en individuos sanos, pero que se detecta a menudo en pacientes con esclerosis múltiple: las células B se desplazan al cerebro y la médula espinal, donde producen bandas de anticuerpos oligoclonales. La mayoría de estas bandas oligoclonales tienen afinidad con la proteína viral EBNA1, que es reactiva de forma cruzada con GlialCAM. Estos anticuerpos son abundantes en aproximadamente el 20-25% de los pacientes con esclerosis múltiple y empeoran la desmielinización autoinmune, lo que conduce en consecuencia a una exacerbación fisiopatológica de la enfermedad. Además, la expansión oligoclonal intratecal con una hipermutación somática constante es única en la esclerosis múltiple en comparación con otras enfermedades neuroinflamatorias. En el estudio también se midió la abundancia de anticuerpos con genes IGHV 3-7, que parece estar relacionada con la progresión de la enfermedad. Los anticuerpos basados en IGHV3-7 se unen con una alta afinidad a EBNA1 y GlialCAM. Este proceso está impulsando activamente la desmielinización. Es probable que las células B que expresan los genes IGHV 3–7 ingresaran al LCR y experimentaran una maduración por afinidad después de enfrentarse a GlialCAM, lo que condujo en consecuencia a la producción de anticuerpos anti-GlialCAM de alta afinidad. Esto también se demostró en el modelo de ratón de EAE, donde la inmunización con EBNA1 condujo a una fuerte respuesta de células B contra GlialCAM, lo que empeoró la EAE. [231]
Retrovirus endógenos humanos
Dos miembros de la familia de retrovirus endógenos humanos-W ( HERV -W), a saber, ERVWE1 y el retrovirus asociado a la EM (MSRV), pueden ser cofactores en la inmunopatogénesis de la EM. Los HERV constituyen hasta el 8% del genoma humano; la mayoría son epigenéticamente silenciosos, pero pueden ser reactivados por virus exógenos, condiciones proinflamatorias o estrés oxidativo. [232] [233] [234]
Medicamentos
Se están investigando los medicamentos que influyen en los canales de iones de sodio dependientes del voltaje como una posible estrategia neuroprotectora debido al papel hipotético del sodio en el proceso patológico que conduce a la lesión axonal y la discapacidad acumulada. No hay evidencia suficiente de un efecto de los bloqueadores de los canales de sodio en las personas con EM. [235]
Patogenesia
La EM es una entidad clínicamente definida con varias presentaciones atípicas. Se han encontrado algunos autoanticuerpos en casos atípicos de EM, lo que ha dado origen a familias de enfermedades independientes y ha restringido el concepto anterior más amplio de EM.
Se encontraron autoanticuerpos anti-AQP4 en la neuromielitis óptica (NMO), que anteriormente se consideraba una variante de la EM. Se ha aceptado un espectro de enfermedades denominadas NMOSD (enfermedades del espectro NMO) o enfermedades anti-AQP4. [236] Algunos casos de EM presentaban autoanticuerpos anti-MOG , que se superponían principalmente con la variante de Marburgo. Se encontró que los autoanticuerpos anti-MOG también estaban presentes en la ADEM, y se está considerando un segundo espectro de enfermedades separadas. Este espectro se nombra de manera inconsistente entre diferentes autores, pero normalmente es algo similar a las enfermedades desmielinizantes anti-MOG . [236]
Se acepta un tercer tipo de autoanticuerpos. Se trata de varios autoanticuerpos antineurofascina que dañan los nódulos de Ranvier de las neuronas. Estos anticuerpos están más relacionados con la desmielinización nerviosa periférica, pero también se encontraron en la EM progresiva progresiva crónica y en la desmielinización central y periférica combinada (CCPD, que se considera otra presentación atípica de EM). [237]
Además de la importancia de los autoanticuerpos en la EM, se han descrito cuatro patrones diferentes de desmielinización, lo que abre la puerta a considerar la EM como una enfermedad heterogénea . [238]
Biomarcadores
Dado que la progresión de la enfermedad es el resultado de la degeneración de las neuronas, se están investigando los roles de las proteínas que muestran pérdida de tejido nervioso, como los neurofilamentos , la tau y el N-acetilaspartato . [240] [241]
Las mejoras en las técnicas de neuroimagen, como la tomografía por emisión de positrones (PET) o la resonancia magnética, son prometedoras para mejorar el diagnóstico y las predicciones del pronóstico. En cuanto a la resonancia magnética, hay varias técnicas que ya han demostrado cierta utilidad en entornos de investigación y podrían introducirse en la práctica clínica, como las secuencias de recuperación de doble inversión, la transferencia de magnetización , el tensor de difusión y la resonancia magnética funcional . [242] Estas técnicas son más específicas para la enfermedad que las existentes, pero aún carecen de cierta estandarización de los protocolos de adquisición y la creación de valores normativos. [242] Este es particularmente el caso de la espectroscopia de resonancia magnética de protones , para la que una serie de variaciones metodológicas observadas en la literatura pueden ser la base de las continuas inconsistencias en las anomalías metabólicas del sistema nervioso central, en particular en N-acetil aspartato , mioinositol , colina , glutamato , GABA y GSH , observadas en la esclerosis múltiple y sus subtipos. [243] Hay otras técnicas en desarrollo que incluyen agentes de contraste capaces de medir niveles de macrófagos periféricos , inflamación o disfunción neuronal, [242] y técnicas que miden la deposición de hierro que podrían servir para determinar el papel de esta característica en la EM, o el de la perfusión cerebral. [242]
COVID-19
Se encontró que la tasa de hospitalización era mayor entre las personas con EM e infección por COVID-19, en un 10%, mientras que la tasa de infección agrupada se estima en un 4%. La prevalencia agrupada de muerte en personas hospitalizadas con EM se estima en un 4%. [244]
Metformina
Un estudio de 2019 en ratas y un estudio de 2024 en ratones mostraron que un medicamento de primera línea para el tratamiento de la diabetes tipo 2 , la metformina , podría promover la remielinización . [245] [246] El prometedor fármaco se está investigando actualmente en humanos en los ensayos Octopus, un ensayo de múltiples brazos y etapas, centrado en probar medicamentos existentes para otras afecciones en pacientes con EM. [247] Actualmente, se están realizando ensayos clínicos en humanos en Bélgica , para pacientes con EM progresiva no activa, [248] en el Reino Unido , en combinación con clemastina para el tratamiento de la EM remitente recurrente, [249] y Canadá , para pacientes con EM de hasta 25 años. [250] [251]
Otras teorías emergentes
Una hipótesis emergente, conocida como la hipótesis de la higiene, sugiere que la exposición temprana a agentes infecciosos ayuda a desarrollar el sistema inmunológico y reduce la susceptibilidad a las alergias y los trastornos autoinmunes. La hipótesis de la higiene se ha vinculado con las hipótesis de la esclerosis múltiple y del microbioma . [252]
También se ha propuesto que ciertas bacterias que se encuentran en el intestino utilizan mimetismo molecular para infiltrarse en el cerebro a través del eje intestino-cerebro , iniciando una respuesta inflamatoria y aumentando la permeabilidad de la barrera hematoencefálica. Los niveles de vitamina D también se han correlacionado con la EM; los niveles más bajos de vitamina D corresponden a un mayor riesgo de EM, lo que sugiere una prevalencia reducida en los trópicos (un área con más luz solar rica en vitamina D), lo que refuerza el impacto de la ubicación geográfica en el desarrollo de la EM. [253] Los mecanismos de la EM comienzan cuando las células T CD4+ efectoras autorreactivas periféricas se activan y se mueven hacia el SNC. Las células presentadoras de antígenos localizan la reactivación de las células T CD4-E efectoras autorreactivas una vez que han ingresado al SNC, atrayendo más células T y macrófagos para formar la lesión inflamatoria. [254] [ cita médica necesaria ] En los pacientes con EM, los macrófagos y la microglía se reúnen en lugares donde la desmielinización y la neurodegeneración están ocurriendo activamente, y la activación de la microglía es más evidente en la materia blanca de apariencia normal de los pacientes con EM. [255] Los astrocitos generan sustancias químicas neurotóxicas como el óxido nítrico y el TNFα , atraen monocitos inflamatorios neurotóxicos al SNC y son responsables de la astrogliosis , la cicatrización que impide la propagación de la neuroinflamación y mata las neuronas dentro del área cicatrizada. [256] [ se necesita una mejor fuente ]
En 2024, los científicos compartieron investigaciones sobre sus hallazgos sobre la migración antigua al norte de Europa desde el área cultural Yamnaya , [257] rastreando variantes genéticas de riesgo de EM que datan de alrededor de 5000 años. [258] [259] Las variantes genéticas de riesgo de EM protegieron a los antiguos pastores de ganado de las enfermedades animales, [260] pero los estilos de vida modernos, las dietas y una mejor higiene han permitido que el gen se desarrolle, lo que resulta en el mayor riesgo de EM en la actualidad. [261]
Véase también
Referencias
- ^ abcdefghijklmnopqrstu vwxyz aa ab ac ad ae af ag ah ai aj ak al am an ao ap aq ar as Compston A , Coles A (octubre de 2008). "Esclerosis múltiple". Lancet . 372 (9648): 1502–1517. doi :10.1016/S0140-6736(08)61620-7. PMID 18970977. S2CID 195686659.
- ^ abcdefgh Milo R, Kahana E (marzo de 2010). "Esclerosis múltiple: geoepidemiología, genética y medio ambiente". Autoimmunity Reviews . 9 (5): A387-94. doi :10.1016/j.autrev.2009.11.010. PMID 19932200.
- ^ abcd «Página de información sobre esclerosis múltiple del NINDS». Instituto Nacional de Trastornos Neurológicos y Accidentes Cerebrovasculares . 19 de noviembre de 2015. Archivado desde el original el 13 de febrero de 2016. Consultado el 6 de marzo de 2016 .
- ^ ab Nakahara J, Maeda M, Aiso S, Suzuki N (febrero de 2012). "Conceptos actuales en esclerosis múltiple: autoinmunidad versus oligodendrogliopatía". Clinical Reviews in Allergy & Immunology . 42 (1): 26–34. doi :10.1007/s12016-011-8287-6. PMID 22189514. S2CID 21058811.
- ^ abcdefgh Tsang BK, Macdonell R (diciembre de 2011). "Esclerosis múltiple: diagnóstico, tratamiento y pronóstico". Australian Family Physician . 40 (12): 948–955. PMID 22146321.
- ^ Liu Z, Liao Q, Wen H, Zhang Y (junio de 2021). "Terapias modificadoras de la enfermedad en la esclerosis múltiple recurrente-remitente: una revisión sistemática y un metanálisis en red". Autoimmunity Reviews . 20 (6): 102826. doi :10.1016/j.autrev.2021.102826. PMID 33878488. S2CID 233325057.
- ^ abc Alphonsus KB, Su Y, D'Arcy C (abril de 2019). "El efecto del ejercicio, el yoga y la fisioterapia en la calidad de vida de las personas con esclerosis múltiple: revisión sistemática y metanálisis". Terapias complementarias en medicina . 43 : 188–195. doi :10.1016/j.ctim.2019.02.010. PMID 30935529. S2CID 86669723.
- ^ abcdefghij Compston A, Coles A (abril de 2002). "Esclerosis múltiple". Lancet . 359 (9313): 1221–1231. doi :10.1016/S0140-6736(02)08220-X. PMID 11955556. S2CID 14207583.
- ^ Murray ED, Buttner EA, Price BH (2012). "Depresión y psicosis en la práctica neurológica". En Daroff R, Fenichel G, Jankovic J, Mazziotta J (eds.). Neurología de Bradley en la práctica clínica (6.ª ed.). Filadelfia, PA: Elsevier/Saunders. ISBN 978-1-4377-0434-1.
- ^ abc Piryonesi SM, Rostampour S, Piryonesi SA (abril de 2021). "Predicción de caídas y lesiones en personas con esclerosis múltiple mediante algoritmos de aprendizaje automático". Esclerosis múltiple y trastornos relacionados . 49 : 102740. doi :10.1016/j.msard.2021.102740. PMID 33450500. S2CID 231624230.
- ^ Mazumder R, Murchison C, Bourdette D, Cameron M (25 de septiembre de 2014). "Caídas en personas con esclerosis múltiple en comparación con caídas en controles sanos". PLOS ONE . 9 (9): e107620. Bibcode :2014PLoSO...9j7620M. doi : 10.1371/journal.pone.0107620 . PMC 4177842 . PMID 25254633.
- ^ Baecher-Allan C, Kaskow BJ, Weiner HL (febrero de 2018). "Esclerosis múltiple: mecanismos e inmunoterapia". Neuron . 97 (4): 742–768. doi : 10.1016/j.neuron.2018.01.021 . PMID 29470968. S2CID 3499974.
- ^ abcdef [ cita médica necesaria ] Lublin FD , Reingold SC (abril de 1996). "Definición del curso clínico de la esclerosis múltiple: resultados de una encuesta internacional. Comité asesor de ensayos clínicos de nuevos agentes en la esclerosis múltiple de la Sociedad Nacional de Esclerosis Múltiple (EE. UU.)". Neurología . 46 (4): 907–911. doi :10.1212/WNL.46.4.907. PMID 8780061. S2CID 40213123.
- ^ Loma I, Heyman R (septiembre de 2011). "Esclerosis múltiple: patogénesis y tratamiento". Neurofarmacología actual . 9 (3): 409–416. doi :10.2174/157015911796557911. PMC 3151595. PMID 22379455 .
- ^ abcdefghijklmnopq Ward M, Goldman MD (agosto de 2022). "Epidemiología y fisiopatología de la esclerosis múltiple". Continuum . 28 (4): 988–1005. doi :10.1212/CON.0000000000001136. PMID 35938654. S2CID 251375096.
- ^ abcd Aloisi F, Cross AH (octubre de 2022). "MINI-revisión de la participación del virus de Epstein-Barr en la etiología y patogénesis de la esclerosis múltiple". Revista de neuroinmunología . 371 : 577935. doi :10.1016/j.jneuroim.2022.577935. PMID 35931008. S2CID 251152784.
- ^ ab Ascherio A, Munger KL (abril de 2007). "Factores de riesgo ambientales para la esclerosis múltiple. Parte I: el papel de la infección". Anales de neurología . 61 (4): 288–299. doi : 10.1002/ana.21117 . PMID 17444504. S2CID 7682774.
- ^ "Página de información sobre esclerosis múltiple del NINDS". Instituto Nacional de Trastornos Neurológicos y Accidentes Cerebrovasculares . 19 de noviembre de 2015. Archivado desde el original el 13 de febrero de 2016. Consultado el 6 de marzo de 2016 .
- ^ abcd McGinley MP, Goldschmidt CH, Rae-Grant AD (febrero de 2021). "Diagnóstico y tratamiento de la esclerosis múltiple: una revisión". JAMA . 325 (8): 765–779. doi :10.1001/jama.2020.26858. PMID 33620411. S2CID 232019589.
- ^ Quinn É, Hynes SM (julio de 2021). "Intervenciones de terapia ocupacional para la esclerosis múltiple: una revisión exploratoria". Revista escandinava de terapia ocupacional . 28 (5): 399–414. doi :10.1080/11038128.2020.1786160. hdl : 10379/16066 . PMID: 32643486. S2CID : 220436640.
- ^ Weinshenker BG (1994). "Historia natural de la esclerosis múltiple". Anales de neurología . 36 (Supl.): S6-11. doi :10.1002/ana.410360704. PMID 8017890. S2CID 7140070.
- ^ ab Berer K, Krishnamoorthy G (noviembre de 2014). "Visión microbiana de la autoinmunidad del sistema nervioso central". FEBS Letters . 588 (22): 4207–13. Bibcode :2014FEBSL.588.4207B. doi :10.1016/j.febslet.2014.04.007. PMID 24746689. S2CID 2772656.
- ^ abcdefg McGinley MP, Goldschmidt CH, Rae-Grant AD (febrero de 2021). "Diagnóstico y tratamiento de la esclerosis múltiple: una revisión". JAMA . 325 (8): 765–779. doi :10.1001/jama.2020.26858. PMID 33620411. S2CID 232019589.
- ^ ab Lane J, Ng HS, Poyser C, Lucas RM, Tremlett H (julio de 2022). "Incidencia de esclerosis múltiple: una revisión sistemática del cambio a lo largo del tiempo por región geográfica". Mult Scler Relat Disord . 63 : 103932. doi : 10.1016/j.msard.2022.103932 . PMID: 35667315. S2CID : 249188137.
- ^ abc Clanet M (junio de 2008). "Jean-Martin Charcot. 1825 a 1893". Revista Internacional de Esclerosis Múltiple . 15 (2): 59–61. PMID 18782501.
* Charcot J (1868). "Histología de la esclerosa en placas". Gaceta de los Hopitaux, París . 41 : 554–5. - ^ "Fatiga". Letchworth Garden City, Reino Unido: Multiple Sclerosis Trust.
- ^ Moore H, Nair KP, Baster K, Middleton R, Paling D, Sharrack B (agosto de 2022). "Fatiga en la esclerosis múltiple: un estudio basado en el registro de EM del Reino Unido". Esclerosis múltiple y trastornos relacionados . 64 : 103954. doi :10.1016/j.msard.2022.103954. PMID 35716477.
- ^ Bakalidou D, Giannopapas V, Giannopoulos S (julio de 2023). "Reflexiones sobre la fatiga en pacientes con esclerosis múltiple". Cureus . 15 (7): e42146. doi : 10.7759/cureus.42146 . PMC 10438195 . PMID 37602098.
- ^ "Signos de EM". Webmd . Archivado desde el original el 30 de septiembre de 2016. Consultado el 7 de octubre de 2016 .
- ^ Plotas P, Nanousi V, Kantanis A, Tsiamaki E, Papadopoulos A, Tsapara A, et al. (julio de 2023). "Déficits del habla en la esclerosis múltiple: una revisión narrativa de la literatura existente". Revista Europea de Investigación Médica . 28 (1): 252. doi : 10.1186/s40001-023-01230-3 . PMC 10364432 . PMID 37488623.
- ^ abcde Petzold A, Fraser CL, Abegg M, Alroughani R, Alshowaeir D, Alvarenga R, et al. (diciembre de 2022). "Diagnóstico y clasificación de la neuritis óptica". La lanceta. Neurología . 21 (12): 1120-1134. doi : 10.1016/s1474-4422(22)00200-9 . PMID 36179757.
- ^ Cameron MH, Nilsagard Y (2018). "Equilibrio, marcha y caídas en la esclerosis múltiple". En Day BL, Lord SR (eds.). Equilibrio, marcha y caídas . Manual de neurología clínica. Vol. 159. págs. 237–250. doi :10.1016/b978-0-444-63916-5.00015-x. ISBN 978-0-444-63916-5. Número de identificación personal 30482317.
- ^ Ghasemi N, Razavi S, Nikzad E (enero de 2017). "Esclerosis múltiple: patogénesis, síntomas, diagnósticos y terapia basada en células". Cell Journal . 19 (1): 1–10. doi :10.22074/cellj.2016.4867. PMC 5241505 . PMID 28367411.
- ^ Chen MH, Wylie GR, Sandroff BM, Dacosta-Aguayo R, DeLuca J, Genova HM (agosto de 2020). "Mecanismos neuronales que subyacen a la fatiga mental en la esclerosis múltiple: un estudio piloto". Journal of Neurology . 267 (8): 2372–2382. doi :10.1007/s00415-020-09853-w. PMID 32350648.
- ^ Oreja-Guevara C, Ayuso Blanco T, Brieva Ruiz L, Hernández Pérez MÁ, Meca-Lallana V, Ramió-Torrentà L (2019). "Disfunciones cognitivas y evaluaciones en la esclerosis múltiple". Fronteras en Neurología . 10 : 581. doi : 10.3389/fneur.2019.00581 . PMC 6558141 . PMID 31214113.
- ^ Kalb R, Beier M, Benedict RH, Charvet L, Costello K, Feinstein A, et al. (noviembre de 2018). "Recomendaciones para la detección y el tratamiento cognitivos en la atención de la esclerosis múltiple". Esclerosis múltiple . 24 (13): 1665–1680. doi :10.1177/1352458518803785. PMC 6238181 . PMID 30303036.
- ^ Benedict RH, Amato MP, DeLuca J, Geurts JJ (octubre de 2020). "Deterioro cognitivo en la esclerosis múltiple: tratamiento clínico, resonancia magnética y vías terapéuticas". The Lancet. Neurología . 19 (10): 860–871. doi :10.1016/S1474-4422(20)30277-5. PMC 10011205 . PMID 32949546. S2CID 221744328.
- ^ Zainal Abidin N, Tuan Jaffar TN, Ahmad Tajudin LS (marzo de 2023). "Oftalmoplejía internuclear bilateral con ojos bizcos como presentación temprana de esclerosis múltiple". Cureus . 15 (3): e36835. doi : 10.7759/cureus.36835 . PMC 10147486 . PMID 37123672.
- ^ abc "Calor y molestias: cómo el calor empeora los síntomas de la EM". Letchworth Garden City, Reino Unido: Multiple Sclerosis Trust.
- ^ abc Christogianni A, Bibb R, Davis SL, Jay O, Barnett M, Evangelou N, et al. (17 de enero de 2018). "Sensibilidad a la temperatura en la esclerosis múltiple: una descripción general de su impacto en los síntomas sensoriales y cognitivos". Temperatura . 5 (3): 208–223. doi :10.1080/23328940.2018.1475831. PMC 6205043 . PMID 30377640.
- ^ ab "Sensibilidad al calor".
- ^ ab "Sensibilidad a la temperatura". Letchworth Garden City, Reino Unido: Multiple Sclerosis Trust.
- ^ Kurtzke JF (noviembre de 1983). "Evaluación del deterioro neurológico en la esclerosis múltiple: una escala ampliada del estado de discapacidad (EDSS)". Neurología . 33 (11): 1444–52. doi : 10.1212/WNL.33.11.1444 . PMID 6685237.
- ^ Amato MP, Ponziani G (agosto de 1999). "Cuantificación del deterioro en la EM: discusión de las escalas en uso". Esclerosis Múltiple . 5 (4): 216–9. doi :10.1177/135245859900500404. PMID 10467378. S2CID 6763447.
- ^ Rudick RA, Cutter G, Reingold S (octubre de 2002). "El compuesto funcional de la esclerosis múltiple: una nueva medida de resultados clínicos para ensayos de esclerosis múltiple". Esclerosis múltiple . 8 (5): 359–65. doi :10.1191/1352458502ms845oa. PMID 12356200. S2CID 31529508.
- ^ van Munster CE, Uitdehaag BM (marzo de 2017). "Medidas de resultados en ensayos clínicos para esclerosis múltiple". Fármacos para el sistema nervioso central . 31 (3): 217–236. doi :10.1007/s40263-017-0412-5. PMC 5336539 . PMID 28185158.
- ^ Makhani N, Tremlett H (agosto de 2021). "El pródromo de la esclerosis múltiple". Nature Reviews. Neurología . 17 (8): 515–521. doi :10.1038/s41582-021-00519-3. PMC 8324569 . PMID 34155379.
- ^ Marrie RA (diciembre de 2019). "Cada vez hay más pruebas de un pródromo de esclerosis múltiple". Nature Reviews. Neurology . 15 (12): 689–690. doi :10.1038/s41582-019-0283-0. PMID 31654040. S2CID 204887642.
- ^ ab Tataru N, Vidal C, Decavel P, Berger E, Rumbach L (2006). "Impacto limitado de la ola de calor del verano en Francia (2003) en las admisiones hospitalarias y las recaídas de la esclerosis múltiple". Neuroepidemiología . 27 (1): 28–32. doi :10.1159/000094233. PMID 16804331. S2CID 20870484.
- ^ Heesen C, Mohr DC, Huitinga I, Bergh FT, Gaab J, Otte C, et al. (marzo de 2007). "Regulación del estrés en la esclerosis múltiple: cuestiones y conceptos actuales". Esclerosis múltiple . 13 (2): 143–148. doi :10.1177/1352458506070772. PMID 17439878. S2CID 8262595.
- ^ Confavreux C, Suissa S, Saddier P, Bourdès V, Vukusic S (febrero de 2001). "Vacunas y riesgo de recaída en la esclerosis múltiple. Grupo de estudio sobre vacunas en la esclerosis múltiple". The New England Journal of Medicine . 344 (5): 319–326. doi : 10.1056/NEJM200102013440501 . PMID 11172162.
- ^ Grimaldi L, Papeix C, Hamon Y, Buchard A, Moride Y, Benichou J, et al. (octubre de 2023). "Vacunas y riesgo de hospitalización por brotes de esclerosis múltiple". JAMA Neurology . 80 (10): 1098–1104. doi :10.1001/jamaneurol.2023.2968. PMC 10481324 . PMID 37669073.
- ^ Martinelli V (2000). "Trauma, estrés y esclerosis múltiple". Neurological Sciences . 21 (4 Suppl 2): S849–S852. doi :10.1007/s100720070024. PMID 11205361. S2CID 2376078.
- ^ Dobson R, Dassan P, Roberts M, Giovannoni G, Nelson-Piercy C, Brex PA (abril de 2019). "Consenso del Reino Unido sobre el embarazo en la esclerosis múltiple: directrices de la 'Asociación de neurólogos británicos'". Neurología práctica . 19 (2): 106–114. doi :10.1136/practneurol-2018-002060. PMID 30612100.
- ^ Varytė G, Zakarevičienė J, Ramašauskaitė D, Laužikienė D, Arlauskienė A (enero de 2020). "Embarazo y esclerosis múltiple: una actualización de la estrategia de tratamiento modificador de la enfermedad y una revisión del impacto del embarazo en la actividad de la enfermedad". Medicina . 56 (2): 49. doi : 10.3390/medicina56020049 . PMC 7074401 . PMID 31973138.
- ^ "Embarazo, parto, lactancia materna y EM". Multiple Sclerosis Society .
- ^ Serafini B, Rosicarelli B, Franciotta D, Magliozzi R, Reynolds R, Cinque P, et al. (noviembre de 2007). "Infección por el virus de Epstein-Barr desregulada en el cerebro con esclerosis múltiple". The Journal of Experimental Medicine . 204 (12): 2899–2912. doi :10.1084/jem.20071030. PMC 2118531 . PMID 17984305.
- ^ ab Hassani A, Corboy JR, Al-Salam S, Khan G (2018). "El virus de Epstein-Barr está presente en el cerebro de la mayoría de los casos de esclerosis múltiple y puede afectar a más células que las B". PLOS ONE . 13 (2): e0192109. Bibcode :2018PLoSO..1392109H. doi : 10.1371/journal.pone.0192109 . PMC 5796799 . PMID 29394264.
- ^ Lutterotti A, Hayward-Koennecke H, Sospedra M, Martin R (2021). "Tolerancia inmunitaria específica de antígeno en la esclerosis múltiple: enfoques prometedores y cómo llevarlos a los pacientes". Frontiers in Immunology . 12 : 640935. doi : 10.3389/fimmu.2021.640935 . PMC 8019937 . PMID 33828551.
- ^ Gilden DH (marzo de 2005). "Causas infecciosas de la esclerosis múltiple". The Lancet. Neurology . 4 (3): 195–202. doi :10.1016/S1474-4422(05)01017-3. PMC 7129502 . PMID 15721830.
- ^ Soldan SS, Lieberman PM (enero de 2023). "Virus de Epstein-Barr y esclerosis múltiple". Nature Reviews. Microbiología . 21 (1): 51–64. doi :10.1038/s41579-022-00770-5. PMC 9362539 . PMID 35931816.
- ^ ab Bjornevik K, Cortese M, Healy BC, Kuhle J, Mina MJ, Leng Y, et al. (enero de 2022). "El análisis longitudinal revela una alta prevalencia del virus de Epstein-Barr asociado con la esclerosis múltiple". Science . 375 (6578): 296–301. Bibcode :2022Sci...375..296B. doi :10.1126/science.abj8222. PMID 35025605. S2CID 245983763.Véase el resumen para legos: Gallagher J (13 de abril de 2022). "¿Un virus que todos tenemos causa la esclerosis múltiple?". BBC .
- ^ Münz C (mayo de 2004). "Antígeno nuclear 1 del virus de Epstein-Barr: de inmunológicamente invisible a un prometedor objetivo para las células T". The Journal of Experimental Medicine . 199 (10): 1301–1304. doi :10.1084/jem.20040730. PMC 2211815 . PMID 15148332.
- ^ Miclea A, Bagnoud M, Chan A, Hoepner R (6 de mayo de 2020). "Una breve revisión de los efectos de la vitamina D en la esclerosis múltiple". Frontiers in Immunology . 11 : 781. doi : 10.3389/fimmu.2020.00781 . PMC 7218089 . PMID 32435244.
- ^ Dyment DA, Ebers GC, Sadovnick AD (febrero de 2004). "Genética de la esclerosis múltiple". The Lancet. Neurología . 3 (2): 104–10. CiteSeerX 10.1.1.334.1312 . doi :10.1016/S1474-4422(03)00663-X. PMID 14747002. S2CID 16707321.
- ^ Skene NG, Grant SG (2016). "Identificación de tipos de células vulnerables en trastornos cerebrales importantes mediante transcriptomas de células individuales y enriquecimiento de tipos de células ponderado por expresión". Frontiers in Neuroscience . 10 : 16. doi : 10.3389/fnins.2016.00016 . PMC 4730103 . PMID 26858593.
- ^ Hassan-Smith G, Douglas MR (octubre de 2011). "Epidemiología y diagnóstico de la esclerosis múltiple". British Journal of Hospital Medicine . 72 (10): M146-51. doi :10.12968/hmed.2011.72.Sup10.M146. PMID 22041658.
- ^ Rosati G (abril de 2001). "La prevalencia de la esclerosis múltiple en el mundo: una actualización". Neurological Sciences . 22 (2): 117–39. doi :10.1007/s100720170011. PMID 11603614. S2CID 207051545.
- ^ abc Baranzini SE (junio de 2011). "Revelando la base genética de la esclerosis múltiple: ¿hemos llegado ya?". Current Opinion in Genetics & Development . 21 (3): 317–24. doi :10.1016/j.gde.2010.12.006. PMC 3105160 . PMID 21247752.
- ^ Consorcio Internacional de Genética de Esclerosis Múltiple (2019). "El mapa genómico de la esclerosis múltiple implica a las células inmunes periféricas y a la microglía en la susceptibilidad". Science . 365 (6460). doi :10.1126/science.aav7188. PMC 7241648 . PMID 31604244.
- ^ abc Milo R, Kahana E (marzo de 2010). "Esclerosis múltiple: geoepidemiología, genética y medio ambiente". Autoimmunity Reviews . 9 (5): A387-94. doi :10.1016/j.autrev.2009.11.010. PMID 19932200.
- ^ Simpson S, Wang W, Otahal P, Blizzard L, van der Mei IA, Taylor BV (noviembre de 2019). "La latitud sigue estando significativamente asociada con la prevalencia de la esclerosis múltiple: un metanálisis actualizado". Revista de neurología, neurocirugía y psiquiatría . 90 (11): 1193–1200. doi :10.1136/jnnp-2018-320189. PMID 31217172.
- ^ Kulie T, Groff A, Redmer J, Hounshell J, Schrager S (2009). "Vitamina D: una revisión basada en evidencia". Revista de la Junta Estadounidense de Medicina Familiar . 22 (6): 698–706. doi : 10.3122/jabfm.2009.06.090037 . PMID 19897699.
- ^ abcde Marrie RA (diciembre de 2004). "Factores de riesgo ambientales en la etiología de la esclerosis múltiple". The Lancet. Neurology . 3 (12): 709–18. doi :10.1016/S1474-4422(04)00933-0. PMID 15556803. S2CID 175786.
- ^ ab Pugliatti M, Sotgiu S, Rosati G (julio de 2002). "La prevalencia mundial de la esclerosis múltiple". Neurología clínica y neurocirugía . 104 (3): 182–91. doi :10.1016/S0303-8467(02)00036-7. PMID 12127652. S2CID 862001.
- ^ Grimaldi LM, Salemi G, Grimaldi G, Rizzo A, Marziolo R, Lo Presti C, et al. (noviembre de 2001). "Alta incidencia y creciente prevalencia de EM en Enna (Sicilia), sur de Italia". Neurología . 57 (10): 1891–3. doi :10.1212/wnl.57.10.1891. PMID 11723283. S2CID 34895995.
- ^ ab "Sensibilidad al calor y al frío en la esclerosis múltiple: una perspectiva centrada en el paciente sobre los desencadenantes, los síntomas y las prácticas de resiliencia térmica - Esclerosis múltiple y trastornos relacionados".
- ^ Davis SL, Wilson TE, White AT, Frohman EM (noviembre de 2010). "Termorregulación en la esclerosis múltiple". Revista de fisiología aplicada . 109 (5): 1531–1537. doi :10.1152/japplphysiol.00460.2010. PMC 2980380 . PMID 20671034.
- ^ ab Davis SL, Jay O, Wilson TE (2018). "Disfunción termorreguladora en la esclerosis múltiple". En Romanovsky AA (ed.). Termorregulación: de la neurociencia básica a la neurología clínica, parte II . Manual de neurología clínica. Vol. 157. págs. 701–714. doi :10.1016/B978-0-444-64074-1.00042-2. ISBN 978-0-444-64074-1. Número de identificación personal 30459034.
- ^ Staff B (11 de agosto de 2014). "Una temperatura corporal más elevada en pacientes con EM RR podría provocar un aumento de la fatiga". multiplesclerosisnewstoday.com .
- ^ Sumowski JF, Leavitt VM (julio de 2014). "La temperatura corporal se eleva y se relaciona con la fatiga en la esclerosis múltiple recurrente-remitente, incluso sin exposición al calor". Archivos de Medicina Física y Rehabilitación . 95 (7): 1298–1302. doi :10.1016/j.apmr.2014.02.004. PMC 4071126 . PMID 24561056.
- ^ Leavitt VM, De Meo E, Riccitelli G, Rocca MA, Comi G, Filippi M, et al. (noviembre de 2015). "La temperatura corporal elevada está relacionada con la fatiga en una muestra italiana de pacientes con esclerosis múltiple recurrente-remitente". Journal of Neurology . 262 (11): 2440–2442. doi :10.1007/s00415-015-7863-8. PMID 26223805.
- ^ ab Christogianni A, O'Garro J, Bibb R, Filtness A, Filingeri D (noviembre de 2022). "Sensibilidad al calor y al frío en la esclerosis múltiple: una perspectiva centrada en el paciente sobre los desencadenantes, los síntomas y las prácticas de resiliencia térmica". Esclerosis múltiple y trastornos relacionados . 67 : 104075. doi :10.1016/j.msard.2022.104075. PMID 35963205.
- ^ abc Ascherio A, Munger KL (junio de 2007). "Factores de riesgo ambientales para la esclerosis múltiple. Parte II: Factores no infecciosos". Anales de neurología . 61 (6): 504–13. doi : 10.1002/ana.21141 . PMID 17492755. S2CID 36999504.
- ^ Hedström A, Hössjer O, Katsoulis M (septiembre de 2018). "Disolventes orgánicos y susceptibilidad a la EM: interacción con los genes HLA de riesgo de EM". Neurología . 91 (5): 455–462. doi :10.1212/WNL.0000000000005906. PMC 6093765 . PMID 29970406.
- ^ Stowe J, Andrews N, Miller E (enero de 2020). "¿Las vacunas desencadenan enfermedades neurológicas? Evaluación epidemiológica de la vacunación y las enfermedades neurológicas utilizando ejemplos de esclerosis múltiple, síndrome de Guillain-Barré y narcolepsia". CNS Drugs . 34 (1): 1–8. doi :10.1007/s40263-019-00670-y. PMC 7224038 . PMID 31576507.
- ^ Spitsin S, Koprowski H (2008). "El papel del ácido úrico en la esclerosis múltiple". En Rodríguez M (ed.). Avances en esclerosis múltiple y enfermedades desmielinizantes experimentales . Temas actuales en microbiología e inmunología. Vol. 318. págs. 325–342. doi :10.1007/978-3-540-73677-6_13. ISBN 978-3-540-73676-9. Número de identificación personal 18219824.
- ^ Nourbakhsh B, Mowry EM (junio de 2019). "Factores de riesgo y patogenia de la esclerosis múltiple". Continuum . 25 (3): 596–610. doi :10.1212/CON.0000000000000725. PMID 31162307. S2CID 174806511.
- ^ abcdefg Thompson AJ, Banwell BL, Barkhof F, Carroll WM, Coetzee T, Comi G, et al. (febrero de 2018). "Diagnóstico de esclerosis múltiple: revisiones de 2017 de los criterios de McDonald". La lanceta. Neurología . 17 (2): 162-173. doi :10.1016/s1474-4422(17)30470-2. PMID 29275977.
- ^ Hassani A, Reguraman N, Shehab S, Khan G (2021). "La infección periférica primaria por el virus de Epstein-Barr puede provocar una infección del sistema nervioso central y neuroinflamación en un modelo de conejo: implicaciones para la patogénesis de la esclerosis múltiple". Frontiers in Immunology . 12 : 764937. doi : 10.3389/fimmu.2021.764937 . PMC 8656284 . PMID 34899715.
- ^ ab Chari DM (2007). "Remielinización en la esclerosis múltiple". En Minagar A (ed.). La neurobiología de la esclerosis múltiple . Revista internacional de neurobiología. Vol. 79. págs. 589–620. doi :10.1016/S0074-7742(07)79026-8. ISBN 978-0-12-373736-6. PMC 7112255 . PMID 17531860.
- ^ Pittock SJ, Lucchinetti CF (marzo de 2007). "La patología de la EM: nuevos conocimientos y posibles aplicaciones clínicas". The Neurologist . 13 (2): 45–56. doi :10.1097/01.nrl.0000253065.31662.37. PMID 17351524. S2CID 2993523.
- ^ Huang X, Hussain B, Chang J (enero de 2021). "Inflamación periférica y alteración de la barrera hematoencefálica: efectos y mecanismos". Neurociencia y terapéutica del sistema nervioso central . 27 (1): 36–47. doi :10.1111/cns.13569. PMC 7804893 . PMID 33381913.
- ^ Ferré JC, Shiroishi MS, Law M (noviembre de 2012). "Técnicas avanzadas con medios de contraste en neuroimagen". Clínicas de imágenes por resonancia magnética de Norteamérica . 20 (4): 699–713. doi :10.1016/j.mric.2012.07.007. PMC 3479680. PMID 23088946 .
- ^ Manjaly ZM, Harrison NA, Critchley HD, Do CT, Stefanics G, Wenderoth N, et al. (junio de 2019). "Mecanismos fisiopatológicos y cognitivos de la fatiga en la esclerosis múltiple". Revista de neurología, neurocirugía y psiquiatría . 90 (6): 642–651. doi :10.1136/jnnp-2018-320050. PMC 6581095 . PMID 30683707.
- ^ Ellison PM, Goodall S, Kennedy N, Dawes H, Clark A, Pomeroy V, et al. (septiembre de 2022). "Correlaciones neuroestructurales y neurofisiológicas de la fatiga física en la esclerosis múltiple: revisión sistemática y metaanálisis de estudios transversales". Neuropsychology Review . 32 (3): 506–519. doi :10.1007/s11065-021-09508-1. PMC 9381450 . PMID 33961198.
- ^ Newland P, Starkweather A, Sorenson M (2016). "Fatiga central en la esclerosis múltiple: una revisión de la literatura". Revista de Medicina de la Médula Espinal . 39 (4): 386–399. doi :10.1080/10790268.2016.1168587. PMC 5102292 . PMID 27146427.
- ^ Loy BD, Taylor RL, Fling BW, Horak FB (septiembre de 2017). "Relación entre la fatiga percibida y la fatigabilidad por rendimiento en personas con esclerosis múltiple: una revisión sistemática y un metanálisis". Journal of Psychosomatic Research . 100 : 1–7. doi :10.1016/j.jpsychores.2017.06.017. PMC 5875709 . PMID 28789787.
- ^ Trojano M, Paolicelli D (noviembre de 2001). "El diagnóstico diferencial de la esclerosis múltiple: clasificación y características clínicas de los síndromes neurológicos progresivos y recurrentes". Neurological Sciences . 22 (Supl 2): S98-102. doi :10.1007/s100720100044. PMID 11794488. S2CID 3057096.
- ^ ab Organización Mundial de la Salud (2008). Atlas: Multiple Sclerosis Resources in the World 2008. Ginebra: Organización Mundial de la Salud. pp. 15–16. hdl : 10665/43968 . ISBN 978-92-4-156375-8.
- ^ Poser CM, Brinar VV (junio de 2004). "Criterios diagnósticos de esclerosis múltiple: una revisión histórica". Neurología clínica y neurocirugía . 106 (3): 147–58. doi :10.1016/j.clineuro.2004.02.004. PMID 15177763. S2CID 23452341.
- ^ Rovira À (noviembre de 2017). "Diagnóstico de la esclerosis múltiple". Revista de la Sociedad Belga de Radiología . 101 (S1): 12. doi : 10.5334/jbr-btr.1426 .
- ^ ab McDonald WI , Compston A, Edan G, Goodkin D, Hartung HP, Lublin FD, et al. (julio de 2001). "Criterios de diagnóstico recomendados para la esclerosis múltiple: directrices del Panel internacional sobre el diagnóstico de la esclerosis múltiple". Anales de neurología . 50 (1): 121–7. doi : 10.1002/ana.1032 . PMID: 11456302. S2CID : 13870943.
- ^ Rashid W, Miller DH (febrero de 2008). "Avances recientes en neuroimagenología de la esclerosis múltiple". Seminarios en neurología . 28 (1): 46–55. doi :10.1055/s-2007-1019127. PMID 18256986. S2CID 260317568.
- ^ Sinnecker T, Clarke MA, Meier D, Enzinger C, Calabrese M, De Stefano N, et al. (Grupo de estudio MAGNIMS) (diciembre de 2019). "Evaluación del signo de la vena central como biomarcador de diagnóstico por imágenes en la esclerosis múltiple". JAMA Neurology . 76 (12): 1446–1456. doi :10.1001/jamaneurol.2019.2478. PMC 6704746 . PMID 31424490.
- ^ Bernitsas E (febrero de 2020). "El signo de la vena central". Neurología práctica . Archivado desde el original el 5 de octubre de 2021. Consultado el 5 de octubre de 2021 .
- ^ Castellaro M, Tamanti A, Pisani AI, Pizzini FB, Crescenzo F, Calabrese M (noviembre de 2020). "El uso del signo de la vena central en el diagnóstico de la esclerosis múltiple: una revisión sistemática y un metanálisis". Diagnóstico . 10 (12): 1025. doi : 10.3390/diagnostics10121025 . PMC 7760678 . PMID 33260401.
- ^ Al-Zandi SH, Fayadh NA, Al-Waely NK (1 de marzo de 2018). "Signo de la vena central detectado por SWI en resonancia magnética de 3 T como discriminador entre esclerosis múltiple y leucoaraiosis". Revista Egipcia de Radiología y Medicina Nuclear . 49 (1): 158–164. doi : 10.1016/j.ejrnm.2017.09.003 .
- ^ Guisset F, Lolli V, Bugli C, Perrotta G, Absil J, Dachy B, et al. (junio de 2021). "El signo de la vena central en pacientes con esclerosis múltiple con comorbilidades vasculares". Esclerosis Múltiple . 27 (7): 1057–1065. doi :10.1177/1352458520943785. hdl : 2078.1/239849 . PMID 32749948.
- ^ Chapman M (16 de junio de 2020). "Subvención de 7,2 millones de dólares del NIH apoya el estudio de un biomarcador de diagnóstico de la EM". BioNews Services. Archivado desde el original el 5 de octubre de 2021 . Consultado el 5 de octubre de 2021 .
- ^ Weigel M, Dechent P, Galbusera R, Bahn E, Nair G, Lu PJ, et al. (julio de 2021). "Obtención de imágenes de la patología de la esclerosis múltiple con una resolución isotrópica de 160 μm mediante resonancia magnética ex vivo de todo el cerebro humano a 3 T". Scientific Reports . 11 (1): 15491. doi :10.1038/s41598-021-94891-1. PMC 8322069 . PMID 34326420.
- ^ Link H, Huang YM (noviembre de 2006). "Bandas oligoclonales en el líquido cefalorraquídeo de pacientes con esclerosis múltiple: una actualización sobre la metodología y la utilidad clínica". Journal of Neuroimmunology . 180 (1–2): 17–28. doi :10.1016/j.jneuroim.2006.07.006. PMID 16945427. S2CID 22724352.
- ^ abc Hauser SL (2022). "Capítulo 442: Enfermedades de la médula espinal". En Loscalzo J, Fauci AS, Kasper DL, Hauser SL, Longo DL, Jameson JL (eds.). Principios de medicina interna de Harrison (21.ª ed.). Nueva York: McGraw-Hill. pág. 3466. ISBN 978-1-264-26849-8.OCLC 1282172709 .
- ^ abcd Saguil A, Farnell IV EA, Jordan TS (agosto de 2022). "Esclerosis múltiple: una perspectiva de atención primaria". Médico de familia estadounidense . 106 (2): 173–183. PMID 35977131.
- ^ Solomon AJ (junio de 2019). "Diagnóstico, diagnóstico diferencial y diagnóstico erróneo de la esclerosis múltiple". Continuum . 25 (3): 611–635. doi :10.1212/CON.0000000000000728. PMID 31162308. S2CID 173991777.
- ^ Lublin FD, et al. (15 de julio de 2014). "Definición del curso clínico de la esclerosis múltiple, revisiones de 2013". Neurología . 83 (3): 278–286. doi :10.1212/WNL.0000000000000560. PMC 4117366 . PMID 24871874.
- ^ Lublin FD, Coetzee T, Cohen JA, Marrie RA, Thompson AJ (junio de 2020). "Descriptores del curso clínico de 2013 para la esclerosis múltiple: una aclaración". Neurología . 94 (24): 1088–1092. doi :10.1212/WNL.0000000000009636. PMC 7455332 . PMID 32471886.
- ^ "Síndrome clínicamente aislado (CIS)". Sociedad Nacional de Esclerosis Múltiple . Archivado desde el original el 30 de septiembre de 2023. Consultado el 4 de octubre de 2023 .
- ^ Miller D, Barkhof F, Montalban X, Thompson A, Filippi M (mayo de 2005). "Síndromes clínicamente aislados sugestivos de esclerosis múltiple, parte I: historia natural, patogénesis, diagnóstico y pronóstico". The Lancet. Neurología . 4 (5): 281–8. doi :10.1016/S1474-4422(05)70071-5. PMID 15847841. S2CID 36401666.
- ^ abc Miller DH, Leary SM (octubre de 2007). "Esclerosis múltiple primaria progresiva". The Lancet. Neurología . 6 (10): 903–12. doi :10.1016/S1474-4422(07)70243-0. hdl : 1871/24666 . PMID 17884680. S2CID 31389841.
- ^ Rovaris M, Confavreux C, Furlan R, Kappos L, Comi G, Filippi M (abril de 2006). "Esclerosis múltiple progresiva secundaria: conocimiento actual y desafíos futuros". The Lancet. Neurología . 5 (4): 343–54. doi :10.1016/S1474-4422(06)70410-0. PMID 16545751. S2CID 39503553.
- ^ ab Sørensen PS, Centonze D, Giovannoni G, et al. (2020). "Opinión de expertos sobre el uso de comprimidos de cladribina en la práctica clínica". Ther Adv Neurol Disord (Revisión). 13 : 1756286420935019. doi :10.1177/1756286420935019. PMC 7318823. PMID 32636933 .
- ^ "Novartis recibe la aprobación de la FDA para Mayzent® (siponimod), el primer fármaco oral para tratar la esclerosis múltiple progresiva secundaria con enfermedad activa". Novartis.com . Archivado desde el original el 20 de noviembre de 2020 . Consultado el 12 de noviembre de 2021 .
- ^ Saida T (noviembre de 2004). "多発性硬化症:再燃時の治療と再発予防" [Esclerosis múltiple: tratamiento y prevención de las recaídas y progresión de la esclerosis múltiple].臨床神経学[ Rinsho Shinkeigaku ] (Revisión) (en japonés). 44 (11): 796–8. PMID 15651294.
- ^ Pittock SJ, Rodriguez M (2008). "Esclerosis múltiple benigna: una entidad clínica distinta con implicaciones terapéuticas". En Rodriguez M (ed.). Avances en esclerosis múltiple y enfermedades desmielinizantes experimentales . Temas actuales en microbiología e inmunología. Vol. 318. págs. 1–17. doi :10.1007/978-3-540-73677-6_1. ISBN 978-3-540-73676-9. Número de identificación personal 18219812.
- ^ Feinstein A (2007). "Capítulo 1 - Esclerosis múltiple: diagnóstico y definiciones". Neuropsiquiatría clínica de la esclerosis múltiple . pp. 1–27. doi :10.1017/CBO9780511543760. ISBN . 978-0-521-85234-0.
- ^ Stadelmann C, Brück W (noviembre de 2004). "Lecciones de la neuropatología de formas atípicas de esclerosis múltiple". Neurological Sciences . 25 (Supl 4): S319–S322. doi :10.1007/s10072-004-0333-1. PMID 15727225. S2CID 21212935.
- ^ Fujihara K (junio de 2019). "Trastornos del espectro de la neuromielitis óptica: en constante evolución y ampliación". Current Opinion in Neurology (Revisión). 32 (3): 385–394. doi :10.1097/WCO.0000000000000694. PMC 6522202 . PMID 30893099.
- ^ Rae-Grant A, Day GS, Marrie RA, Rabinstein A, Cree BA, Gronseth GS, et al. (abril de 2018). "Resumen de recomendaciones de las guías de práctica: Terapias modificadoras de la enfermedad para adultos con esclerosis múltiple: Informe del Subcomité de Desarrollo, Difusión e Implementación de Guías de la Academia Estadounidense de Neurología". Neurología . 90 (17): 777–788. doi : 10.1212/WNL.0000000000005347 . PMID 29686116.
- ^ Burton JM, O'Connor PW, Hohol M, Beyene J (diciembre de 2012). "Esteroides orales versus intravenosos para el tratamiento de las recaídas en la esclerosis múltiple". Base de datos Cochrane de revisiones sistemáticas . 12 : CD006921. doi :10.1002/14651858.CD006921.pub3. PMID 23235634.
- ^ Filippini G, Brusaferri F, Sibley WA, et al. (2000). "Corticosteroides o ACTH para las exacerbaciones agudas en la esclerosis múltiple". Cochrane Database Syst Rev. 2013 ( 4): CD001331. doi :10.1002/14651858.CD001331. PMC 11391333. PMID 11034713 .
- ^ Centro Nacional de Colaboración para Enfermedades Crónicas (2004). "Tratamiento de episodios agudos". Esclerosis múltiple: guía clínica nacional para el diagnóstico y el tratamiento en atención primaria y secundaria. Londres: Royal College of Physicians. págs. 54-58. ISBN 1-86016-182-0. PMID 21290636. Archivado desde el original el 10 de febrero de 2023 . Consultado el 5 de octubre de 2021 .
- ^ Petzold A, Braithwaite T, van Oosten BW (enero de 2020). "Caso para un nuevo ensayo de tratamiento con corticosteroides en la neuritis óptica: revisión de la evidencia actualizada". J. Neurol. Neurosurg. Psychiatry (Revisión). 91 (1): 9–14. doi :10.1136/jnnp-2019-321653. PMC 6952848. PMID 31740484 .
- ^ ab He D, Zhang C, Zhao X, Zhang Y, Dai Q, Li Y, et al. (marzo de 2016). "Teriflunomida para la esclerosis múltiple". Base de datos Cochrane de revisiones sistemáticas . 2016 (3): CD009882. doi :10.1002/14651858.CD009882.pub3. PMC 10493042. PMID 27003123 .
- ^ ab Rice GP, Incorvaia B, Munari L, et al. (2001). "Interferón en la esclerosis múltiple recurrente-remitente". Cochrane Database Syst Rev. 2001 ( 4): CD002002. doi :10.1002/14651858.CD002002. PMC 7017973. PMID 11687131 .
- ^ Hassan-Smith G, Douglas MR (noviembre de 2011). "Manejo y pronóstico de la esclerosis múltiple". British Journal of Hospital Medicine . 72 (11): M174-6. doi :10.12968/hmed.2011.72.Sup11.M174. PMID 22082979.
- ^ Freedman MS (enero de 2011). "Seguimiento a largo plazo de ensayos clínicos de terapias para la esclerosis múltiple". Neurología . 76 (1 Suppl 1): S26-34. doi :10.1212/WNL.0b013e318205051d. PMID 21205679. S2CID 16929304.
- ^ Qizilbash N, Mendez I, Sanchez-de la Rosa R (enero de 2012). "Análisis de riesgo-beneficio del acetato de glatiramer para la esclerosis múltiple con síndrome clínico aislado y recurrente-remitente". Clinical Therapeutics . 34 (1): 159–176.e5. doi :10.1016/j.clinthera.2011.12.006. PMID 22284996.
- ^ Bates D (enero de 2011). "Efectos del tratamiento con terapias inmunomoduladoras en diferentes etapas de la esclerosis múltiple en ensayos a corto plazo". Neurology . 76 (1 Suppl 1): S14-25. doi :10.1212/WNL.0b013e3182050388. PMID 21205678. S2CID 362182.
- ^ Clerico M, Faggiano F, Palace J, et al. (abril de 2008). "Interferón beta recombinante o acetato de glatiramer para retrasar la conversión del primer evento desmielinizante en esclerosis múltiple". Cochrane Database Syst Rev (2): CD005278. doi :10.1002/14651858.CD005278.pub3. PMID 18425915.
- ^ Johnston J, So TY (junio de 2012). "Terapias modificadoras de la enfermedad de primera línea en la esclerosis múltiple pediátrica: una descripción general completa". Drugs . 72 (9): 1195–211. doi :10.2165/11634010-000000000-00000. PMID 22642799. S2CID 20323687.
- ^ ab La Mantia L, Tramacere I, Firwana B, et al. (abril de 2016). "Fingolimod para la esclerosis múltiple recurrente-remitente". Cochrane Database Syst Rev. 2016 ( 4): CD009371. doi : 10.1002 /14651858.CD009371.pub2. PMC 10401910. PMID 27091121.
- ^ ab Xu Z, Zhang F, Sun F, et al. (abril de 2015). "Dimetilfumarato para la esclerosis múltiple". Cochrane Database Syst Rev. 2015 ( 4): CD011076. doi :10.1002/14651858.CD011076.pub2. PMC 10663978. PMID 25900414 .
- ^ abcd Killestein J, Rudick RA, Polman CH (noviembre de 2011). "Tratamiento oral para la esclerosis múltiple". The Lancet. Neurology . 10 (11): 1026–34. doi :10.1016/S1474-4422(11)70228-9. PMID 22014437. S2CID 206160178.
- ^ Filippini G, Del Giovane C, Clerico M, et al. (abril de 2017). "Tratamiento con fármacos modificadores de la enfermedad para personas con un primer ataque clínico sugestivo de esclerosis múltiple". Cochrane Database Syst Rev. 2017 ( 4): CD012200. doi :10.1002/14651858.CD012200.pub2. PMC 6478290. PMID 28440858 .
- ^ abcd Filippini G, Del Giovane C, Vacchi L, et al. (junio de 2013). "Inmunomoduladores e inmunosupresores para la esclerosis múltiple: un metanálisis en red". Cochrane Database Syst Rev (6): CD008933. doi :10.1002/14651858.CD008933.pub2. PMID 23744561.
- ^ La Mantia L, Di Pietrantonj C, Rovaris M, et al. (noviembre de 2016). "Interferones beta versus acetato de glatiramer para la esclerosis múltiple recurrente-remitente". Cochrane Database Syst Rev. 2016 ( 11): CD009333. doi :10.1002/14651858.CD009333.pub3. PMC 6464642. PMID 27880972 .
- ^ abc Gonzalez-Lorenzo M, Ridley B, Minozzi S, Del Giovane C, Peryer G, Piggott T, et al. (enero de 2024). "Inmunomoduladores e inmunosupresores para la esclerosis múltiple recurrente-remitente: un metanálisis en red". Cochrane Database Syst Rev. 2024 ( 1): CD011381. doi :10.1002/14651858.CD011381.pub3. PMC 10765473. PMID 38174776 .
- ^ "TG Therapeutics anuncia la aprobación por parte de la FDA de Briumvi (ublituximab-xiiy)" (Comunicado de prensa). TG Therapeutics. 28 de diciembre de 2022. Archivado desde el original el 28 de diciembre de 2022. Consultado el 29 de diciembre de 2022 a través de GlobeNewswire.
- ^ "Ayuda para la toma de decisiones en pacientes con EM". Letchworth Garden City, Reino Unido: Multiple Sclerosis Trust. 3 de diciembre de 2023. Consultado el 3 de diciembre de 2023 .
- ^ Keegan BM (22 de diciembre de 2011). "Esclerosis múltiple". En Bope ET, Kellerman RD (eds.). Conn's Current Therapy 2012: Expert Consult – Online and Print . Elsevier Health Sciences. pág. 626. ISBN 978-1-4557-0738-6.
- ^ ab Martinelli Boneschi F, Vacchi L, Rovaris M, Capra R, Comi G (mayo de 2013). "Mitoxantrona para la esclerosis múltiple". Base de Datos Cochrane de Revisiones Sistemáticas . 5 (5): CD002127. doi :10.1002/14651858.CD002127.pub3. hdl : 2434/533488 . PMID: 23728638.
- ^ Marriott JJ, Miyasaki JM, Gronseth G, O'Connor PW (mayo de 2010). "Informe de evidencia: eficacia y seguridad de la mitoxantrona (Novantrone) en el tratamiento de la esclerosis múltiple: Informe del Subcomité de Evaluación de Tecnología y Terapéutica de la Academia Estadounidense de Neurología". Neurología . 74 (18): 1463–70. doi :10.1212/WNL.0b013e3181dc1ae0. PMC 2871006 . PMID 20439849.
- ^ ab Faissner S, Gold R (2019). "Esclerosis múltiple progresiva: últimos avances terapéuticos y direcciones futuras". Avances terapéuticos en trastornos neurológicos . 12 : 1756286419878323. doi : 10.1177/1756286419878323 . PMC 6764045. PMID 31598138 .
- ^ Winslow R (28 de marzo de 2017). "Tras 40 años de odisea, el primer fármaco para la esclerosis múltiple agresiva obtiene la aprobación de la FDA". STAT. Archivado desde el original el 1 de abril de 2017.
- ^ ab "Ocrevus- inyección de ocrelizumab". DailyMed . 13 de diciembre de 2019. Archivado desde el original el 27 de junio de 2020 . Consultado el 26 de marzo de 2020 .
- ^ "Carta de aprobación de la BLA" (PDF) . FDA. 28 de marzo de 2017. Archivado (PDF) del original el 2 de abril de 2017.
- ^ Lin M, Zhang J, Zhang Y, Luo J, Shi S, et al. (Grupo Cochrane de Esclerosis Múltiple y Enfermedades Raras del Sistema Nervioso Central) (mayo de 2022). "Ocrelizumab para la esclerosis múltiple". Base de Datos Cochrane de Revisiones Sistemáticas . 2022 (5): CD013247. doi :10.1002/14651858.CD013247.pub2. PMC 9115862. PMID 35583174 .
- ^ Penner IK, Schreiber H (2023). "Inmunoterapias modificadoras de la enfermedad y fatiga". En Penner IK (ed.). Fatiga en la esclerosis múltiple . Springer, Cham. págs. 161–177. ISBN 978-3-031-13498-2.
- ^ "La FDA aprueba Ocrevus Zunovo como la primera y única inyección subcutánea de 10 minutos que se administra dos veces al año para personas con esclerosis múltiple recurrente y progresiva". Genentech (nota de prensa). 13 de septiembre de 2024. Archivado desde el original el 14 de septiembre de 2024 . Consultado el 13 de septiembre de 2024 .
- ^ "Halozyme anuncia la aprobación por parte de la FDA de Ocrevus Zunovo subcutáneo de Roche con Enhanze para personas con esclerosis múltiple progresiva primaria y recurrente" (Comunicado de prensa). Halozyme Therapeutics. 13 de septiembre de 2024. Archivado desde el original el 14 de septiembre de 2024. Consultado el 13 de septiembre de 2024 a través de PR Newswire.
- ^ ab Balak DM, Hengstman GJ, Çakmak A, Thio HB (diciembre de 2012). "Eventos adversos cutáneos asociados con el tratamiento modificador de la enfermedad en la esclerosis múltiple: una revisión sistemática". Esclerosis múltiple . 18 (12): 1705–17. doi :10.1177/1352458512438239. hdl : 1765/73097 . PMID 22371220.
- ^ Sládková T, Kostolanský F (2006). "El papel de las citoquinas en la respuesta inmune a la infección por el virus de la influenza A". Acta Virológica . 50 (3): 151–62. PMID 17131933.
- ^ La Mantia L, Munari LM, Lovati R (mayo de 2010). "Acetato de glatiramer para la esclerosis múltiple". Base de datos Cochrane de revisiones sistemáticas (5): CD004678. doi :10.1002/14651858.CD004678.pub2. PMID 20464733.
- ^ Tremlett H, Oger J (noviembre de 2004). "Lesión hepática, monitorización hepática y los interferones beta para la esclerosis múltiple". Journal of Neurology . 251 (11): 1297–303. doi :10.1007/s00415-004-0619-5. PMID 15592724. S2CID 12529733.
- ^ Comi G (octubre de 2009). "Tratamiento de la esclerosis múltiple: papel del natalizumab". Neurological Sciences . 30. 30 (S2): S155-8. doi :10.1007/s10072-009-0147-2. PMID 19882365. S2CID 25910077.
- ^ Hunt D, Giovannoni G (febrero de 2012). "Leucoencefalopatía multifocal progresiva asociada al natalizumab: un enfoque práctico para la elaboración de perfiles de riesgo y su seguimiento". Neurología práctica . 12 (1): 25–35. doi :10.1136/practneurol-2011-000092. PMID 22258169. S2CID 46326042.
- ^ "TECFIDERA™ (dimetilfumarato) de Biogen Idec aprobado en EE. UU. como tratamiento oral de primera línea para la esclerosis múltiple" (nota de prensa). Biogen Idec. 27 de marzo de 2013. Archivado desde el original el 12 de mayo de 2013. Consultado el 4 de junio de 2013 .
- ^ "NDA 204063 – Texto de etiquetado aprobado por la FDA" (PDF) . Agencia de Alimentos y Medicamentos de los Estados Unidos. 27 de marzo de 2013. Archivado (PDF) desde el original el 4 de octubre de 2013 . Consultado el 5 de abril de 2013 .
"Aprobación NDA" (PDF) . Agencia de Alimentos y Medicamentos de Estados Unidos. 27 de marzo de 2013. Archivado (PDF) del original el 4 de octubre de 2013 . Consultado el 5 de abril de 2013 . - ^ Kesselring J, Beer S (octubre de 2005). "Terapia sintomática y neurorrehabilitación en la esclerosis múltiple". The Lancet. Neurology . 4 (10): 643–52. doi :10.1016/S1474-4422(05)70193-9. PMID 16168933. S2CID 28253186.
- ^ Khan F, Turner-Stokes L, Ng L, Kilpatrick T (abril de 2007). Khan F (ed.). "Rehabilitación multidisciplinaria para adultos con esclerosis múltiple". Base de datos Cochrane de revisiones sistemáticas . 2011 (2): CD006036. doi : 10.1002 /14651858.CD006036.pub2. PMC 8992048. PMID 17443610.
- ^ Köpke S, Solari A, Rahn A, Khan F, Heesen C, Giordano A (octubre de 2018). "Provisión de información para personas con esclerosis múltiple". Base de datos Cochrane de revisiones sistemáticas . 2018 (10): CD008757. doi :10.1002/14651858.CD008757.pub3. PMC 6517040. PMID 30317542 .
- ^ Steultjens EM, Dekker J, Bouter LM, Leemrijse CJ, van den Ende CH (mayo de 2005). "Evidencia de la eficacia de la terapia ocupacional en diferentes condiciones: una descripción general de las revisiones sistemáticas". Rehabilitación clínica . 19 (3): 247–54. doi :10.1191/0269215505cr870oa. hdl :1871/26505. PMID 15859525.
- ^ Steultjens EM, Dekker J, Bouter LM, Cardol M, Van de Nes JC, Van den Ende CH (2003). Steultjens EE (ed.). "Terapia ocupacional para la esclerosis múltiple". Base de Datos Cochrane de Revisiones Sistemáticas . 2010 (3): CD003608. doi :10.1002/14651858.CD003608. PMC 9022193. PMID 12917976 .
- ^ Amatya B, Khan F, Galea M (enero de 2019). "Rehabilitación para personas con esclerosis múltiple: una descripción general de las revisiones Cochrane". Base de datos Cochrane de revisiones sistemáticas . 1 ( 1): CD012732. doi :10.1002/14651858.CD012732.pub2. PMC 6353175. PMID 30637728.
- ^ Heine M, van de Port I, Rietberg MB, van Wegen EE, Kwakkel G (septiembre de 2015). "Terapia con ejercicios para la fatiga en la esclerosis múltiple". Base de datos Cochrane de revisiones sistemáticas . 2015 (9): CD009956. doi :10.1002/14651858.CD009956.pub2. PMC 9554249. PMID 26358158 .
- ^ Gallien P, Nicolas B, Robineau S, Pétrilli S, Houedakor J, Durufle A (julio de 2007). "Entrenamiento físico y esclerosis múltiple". Annales de Réadaptation et de Médecine Physique . 50 (6): 373–6, 369–72. doi :10.1016/j.annrmp.2007.04.004. PMID 17482708.
- ^ Rietberg MB, Brooks D, Uitdehaag BM, Kwakkel G (enero de 2005). Kwakkel G (ed.). "Terapia de ejercicios para la esclerosis múltiple". Base de datos Cochrane de revisiones sistemáticas . 2005 (1): CD003980. doi :10.1002/14651858.CD003980.pub2. PMC 6485797. PMID 15674920 .
- ^ Thomas PW, Thomas S, Hillier C, Galvin K, Baker R (enero de 2006). Thomas PW (ed.). "Intervenciones psicológicas para la esclerosis múltiple". Base de datos Cochrane de revisiones sistemáticas . 2010 (1): CD004431. doi :10.1002/14651858.CD004431.pub2. PMC 8406851. PMID 16437487 .
- ^ Rosti-Otajärvi EM, Hämäläinen PI (febrero de 2014). "Rehabilitación neuropsicológica para la esclerosis múltiple". Base de datos Cochrane de revisiones sistemáticas . 2014 (2): CD009131. doi :10.1002/14651858.CD009131.pub3. PMC 10966661. PMID 24515630 .
- ^ Latorraca CO, Martimbianco AL, Pachito DV, Torloni MR, Pacheco RL, Pereira JG, et al. (octubre de 2019). "Intervenciones de cuidados paliativos para personas con esclerosis múltiple". Base de datos Cochrane de revisiones sistemáticas . 2019 (10): CD012936. doi : 10.1002 /14651858.CD012936.pub2. PMC 6803560. PMID 31637711.
- ^ Hayes S, Galvin R, Kennedy C, Finlayson M, McGuigan C, Walsh CD, et al. (noviembre de 2019). "Intervenciones para prevenir caídas en personas con esclerosis múltiple". Base de datos Cochrane de revisiones sistemáticas . 2019 (11): CD012475. doi :10.1002/14651858.CD012475.pub2. PMC 6953359. PMID 31778221 .
- ^ van den Akker LE, Beckerman H, Collette EH, Eijssen IC, Dekker J, de Groot V (noviembre de 2016). "Efectividad de la terapia cognitivo-conductual para el tratamiento de la fatiga en pacientes con esclerosis múltiple: una revisión sistemática y un metanálisis". Journal of Psychosomatic Research . 90 : 33–42. doi :10.1016/j.jpsychores.2016.09.002. PMID 27772557.
- ^ Amatya B, Young J, Khan F (diciembre de 2018). "Intervenciones no farmacológicas para el dolor crónico en la esclerosis múltiple". Base de Datos Cochrane de Revisiones Sistemáticas . 12 (12): CD012622. doi : 10.1002/14651858.CD012622.pub2 . PMC 6516893 . PMID 30567012.
- ^ Corvillo I, Varela E, Armijo F, Alvarez-Badillo A, Armijo O, Maraver F (diciembre de 2017). "Eficacia de la terapia acuática para la esclerosis múltiple: una revisión sistemática". Eur J Phys Rehabil Med (Revisión). 53 (6): 944–952. doi :10.23736/S1973-9087.17.04570-1. PMID 28215060.
- ^ Khan F, Amatya B, Bensmail D, Yelnik A (julio de 2019). "Intervenciones no farmacológicas para la espasticidad en adultos: una descripción general de las revisiones sistemáticas". Ann Phys Rehabil Med . 62 (4): 265–273. doi : 10.1016/j.rehab.2017.10.001 . PMID: 29042299. S2CID : 207497395.
- ^ Etoom M, Khraiwesh Y, Lena F, et al. (noviembre de 2018). "Efectividad de las intervenciones de fisioterapia sobre la espasticidad en personas con esclerosis múltiple: una revisión sistemática y un metanálisis". Am J Phys Med Rehabil . 97 (11): 793–807. doi :10.1097/PHM.0000000000000970. PMID 29794531. S2CID 44156766.
- ^ abcdefg Huntley A (enero de 2006). "Una revisión de la evidencia de la eficacia de las medicinas complementarias y alternativas en la EM". Revista Internacional de EM . 13 (1): 5–12, 4. PMID 16420779.
- ^ Olsen SA (2009). "Una revisión de la medicina complementaria y alternativa (MCA) por parte de personas con esclerosis múltiple". Occupational Therapy International . 16 (1): 57–70. doi :10.1002/oti.266. PMID 19222053.
- ^ Parks NE, Jackson-Tarlton CS, Vacchi L, Merdad R, Johnston BC (mayo de 2020). "Intervenciones dietéticas para los resultados relacionados con la esclerosis múltiple". Base de datos Cochrane de revisiones sistemáticas . 2020 (5): CD004192. doi :10.1002/14651858.CD004192.pub4. PMC 7388136. PMID 32428983 .
- ^ Grigorian A, Araujo L, Naidu NN, Place DJ, Choudhury B, Demetriou M (noviembre de 2011). "La N-acetilglucosamina inhibe las respuestas de las células T-helper 1 (Th1)/T-helper 17 (Th17) y trata la encefalomielitis autoinmune experimental". The Journal of Biological Chemistry . 286 (46): 40133–41. doi : 10.1074/jbc.M111.277814 . PMC 3220534 . PMID 21965673.
- ^ Pozuelo-Moyano B, Benito-León J, Mitchell AJ, Hernández-Gallego J (2013). "A systematic review of randomized, double-blind, placebo-controlled trials examination the clinical effectiveness of vitamin D in multiple sclerosis". Neuroepidemiology (Systematic review). 40 (3): 147–53. doi :10.1159/000345122. PMC 3649517 . PMID 23257784.
la evidencia disponible no corrobora ni un beneficio clínicamente significativo ni un daño de la vitamina D en el tratamiento de pacientes con EM
- ^ Chong MS, Wolff K, Wise K, Tanton C, Winstock A, Silber E (octubre de 2006). "Uso de cannabis en pacientes con esclerosis múltiple". Esclerosis múltiple . 12 (5): 646–51. doi :10.1177/1352458506070947. PMID 17086912. S2CID 34692470.
- ^ Torres-Moreno MC, Papaseit E, Torrens M, Farré M (octubre de 2018). "Evaluación de la eficacia y la tolerabilidad de los cannabinoides medicinales en pacientes con esclerosis múltiple: una revisión sistemática y un metanálisis". JAMA Network Open . 1 (6): e183485. doi :10.1001/jamanetworkopen.2018.3485. PMC 6324456 . PMID 30646241.
- ^ Bennett M, Heard R (2004). Bennett MH (ed.). "Terapia con oxígeno hiperbárico para la esclerosis múltiple". Base de Datos Cochrane de Revisiones Sistemáticas . 2011 (1): CD003057. doi :10.1002/14651858.CD003057.pub2. PMC 8407327. PMID 14974004 .
- ^ Adams T (23 de mayo de 2010). "Instinto intestinal: el milagro del anquilostoma parásito". The Observer . Archivado desde el original el 24 de octubre de 2014.
- ^ Simpson R, Booth J, Lawrence M, Byrne S, Mair F, Mercer S (enero de 2014). "Intervenciones basadas en la atención plena en la esclerosis múltiple: una revisión sistemática". BMC Neurology . 14 : 15. doi : 10.1186/1471-2377-14-15 . PMC 3900731 . PMID 24438384.
- ^ Jagannath VA, Filippini G, Di Pietrantonj C, Asokan GV, Robak EW, Whamond L, et al. (septiembre de 2018). "Vitamina D para el tratamiento de la esclerosis múltiple". Base de datos Cochrane de revisiones sistemáticas . 9 (9): CD008422. doi :10.1002/14651858.CD008422.pub3. PMC 6513642. PMID 30246874 .
- ^ Motte J, Gold R (diciembre de 2020). "Biotina en dosis altas en la esclerosis múltiple: el final del camino". Lancet Neurol . 19 (12): 965–966. doi :10.1016/S1474-4422(20)30353-7. PMID 33222766. S2CID 225049079.
- ^ Tryfonos C, Mantzorou M, Fotiou D, Vrizas M, Vadikolias K, Pavlidou E, et al. (septiembre de 2019). "Suplementos dietéticos para controlar los síntomas y las recaídas de la esclerosis múltiple: evidencia clínica actual y perspectivas futuras". Medicinas . 6 (3): 95. doi : 10.3390/medicines6030095 . PMC 6789617 . PMID 31547410.
- ^ Sedel F, Bernard D, Mock DM, Tourbah A (noviembre de 2016). "Tratamiento de la desmielinización y la hipoxia virtual con biotina en dosis altas como tratamiento para la esclerosis múltiple progresiva". Neurofarmacología . 110 (Pt B): 644–653. doi : 10.1016/j.neuropharm.2015.08.028 . PMID 26327679.
- ^ Goldschmidt CH, Cohen JA (julio de 2020). "El ascenso y la caída de la biotina en dosis altas para tratar la esclerosis múltiple progresiva". Neurotherapeutics . 17 (3): 968–970. doi : 10.1007/s13311-020-00907-5 . PMC 7609671 . PMID 32761325.
- ^ Filippini G, Minozzi S, Borrelli F, Cinquini M, Dwan K (mayo de 2022). "Cannabis y cannabinoides para el tratamiento sintomático de personas con esclerosis múltiple". Base de Datos Cochrane de Revisiones Sistemáticas . 5 (5): CD013444. doi :10.1002/14651858.CD013444.pub2. PMC 9069991 . PMID 35510826.
- ^ abc Cree BA, Hartung HP, Barnett M (junio de 2022). "Nuevos fármacos para la esclerosis múltiple: nuevos algoritmos de tratamiento". Curr Opin Neurol . 35 (3): 262–270. doi : 10.1097/WCO.0000000000001063 . PMID 35674067. S2CID 249438715.
- ^ abcd Oh J, Vidal-Jordana A, Montalban X (diciembre de 2018). "Esclerosis múltiple: aspectos clínicos". Curr Opin Neurol . 31 (6): 752–759. doi :10.1097/WCO.0000000000000622. PMID 30300239.
- ^ Hauser SL, Cree BA (diciembre de 2020). "Tratamiento de la esclerosis múltiple: una revisión". Am J Med . 133 (12): 1380–1390.e2. doi :10.1016/j.amjmed.2020.05.049. PMC 7704606 . PMID 32682869.
- ^ ab Ontaneda D (junio de 2019). "Esclerosis múltiple progresiva". Continuum . 25 (3): 736–752. doi :10.1212/CON.0000000000000727. PMID 31162314. S2CID 174808956.
- ^ Inojosa H, Proschmann U, Akgün K, Ziemssen T (abril de 2021). "Un enfoque en la esclerosis múltiple progresiva secundaria (EMSP): desafíos en el diagnóstico y la definición". J Neurol . 268 (4): 1210–1221. doi :10.1007/s00415-019-09489-5. PMID 31363847. S2CID 198999832. La Escala ampliada del estado de discapacidad (EDSS) de 6,0 equivale a requerir un dispositivo de ayuda para caminar, y la EDSS de 8,0 equivale a estar postrado en una silla o en cama.
- ^ abc Thompson AJ, Baranzini SE, Geurts J, Hemmer B, Ciccarelli O (abril de 2018). "Esclerosis múltiple". Lanceta . 391 (10130): 1622–1636. doi :10.1016/S0140-6736(18)30481-1. PMID 29576504. S2CID 4313310.
- ^ Lunde HM, Assmus J, Myhr KM, Bø L, Grytten N (agosto de 2017). "Supervivencia y causa de muerte en la esclerosis múltiple: un estudio poblacional longitudinal de 60 años". Revista de neurología, neurocirugía y psiquiatría . 88 (8): 621–625. doi :10.1136/jnnp-2016-315238. PMC 5537547 . PMID 28365589.
- ^ "Atlas de EM" (PDF) . Federación Internacional de Esclerosis Múltiple . Septiembre de 2020.
- ^ Kurtzke JF (octubre de 1993). "Evidencia epidemiológica de la esclerosis múltiple como infección". Clinical Microbiology Reviews . 6 (4): 382–427. doi :10.1128/CMR.6.4.382. PMC 358295 . PMID 8269393.
- ^ Alonso A, Hernán MA (julio 2008). "Tendencias temporales en la incidencia de la esclerosis múltiple: una revisión sistemática". Neurología . 71 (2): 129–135. doi :10.1212/01.wnl.0000316802.35974.34. PMC 4109189 . PMID 18606967.
- ^ Walton C, King R, Rechtman L, Kaye W, Leray E, Marrie RA, et al. (diciembre de 2020). "Aumento de la prevalencia de la esclerosis múltiple en todo el mundo: perspectivas del Atlas de EM, tercera edición". Esclerosis múltiple . 26 (14): 1816–1821. doi :10.1177/1352458520970841. PMC 7720355 . PMID 33174475.
- ^ ab Compston A (octubre de 1988). "El 150 aniversario de la primera representación de las lesiones de la esclerosis múltiple". Revista de neurología, neurocirugía y psiquiatría . 51 (10): 1249–52. doi :10.1136/jnnp.51.10.1249. PMC 1032909 . PMID 3066846.
- ^ Lassmann H (octubre de 1999). "La patología de la esclerosis múltiple y su evolución". Philosophical Transactions of the Royal Society of London. Serie B, Ciencias Biológicas . 354 (1390): 1635–40. doi :10.1098/rstb.1999.0508. PMC 1692680. PMID 10603616 .
- ^ Lassmann H (julio de 2005). "Patología de la esclerosis múltiple: evolución de los conceptos patogénicos". Patología cerebral . 15 (3): 217–22. doi :10.1111/j.1750-3639.2005.tb00523.x. PMC 8095927 . PMID 16196388. S2CID 8342303.
- ^ abc Milo R, Miller A (abril de 2014). "Criterios de diagnóstico revisados de la esclerosis múltiple". Autoimmunity Reviews . 13 (4–5): 518–524. doi :10.1016/j.autrev.2014.01.012. PMID 24424194.
- ^ ab Polman CH, Reingold SC, Banwell B, Clanet M, Cohen JA, Filippi M, et al. (febrero de 2011). "Criterios diagnósticos para la esclerosis múltiple: revisiones de 2010 de los criterios de McDonald". Anales de neurología . 69 (2): 292–302. doi :10.1002/ana.22366. PMC 3084507 . PMID 21387374.
- ^ Lublin FD, Reingold SC, Cohen JA, Cutter GR, Sørensen PS, Thompson AJ, et al. (julio de 2014). "Definición del curso clínico de la esclerosis múltiple: revisiones de 2013". Neurología . 83 (3): 278–86. doi :10.1212/WNL.0000000000000560. PMC 4117366 . PMID 24871874.
- ^ Sørensen PS, Centonze D, Giovannoni G, Montalban X, Selchen D, Vermersch P, et al. (24 de junio de 2020). "Opinión de expertos sobre el uso de comprimidos de cladribina en la práctica clínica". Avances terapéuticos en trastornos neurológicos . 13 : 1756286420935019. doi : 10.1177/1756286420935019 . PMC 7318823. PMID 32636933 .
- ^ Medaer R (septiembre de 1979). "¿Se remonta la historia de la esclerosis múltiple al siglo XIV?". Acta Neurologica Scandinavica . 60 (3): 189–92. doi :10.1111/j.1600-0447.1979.tb08970.x. PMID 390966. S2CID 221422840.
- ^ Holmøy T (2006). "Una contribución nórdica a la historia de las enfermedades neurológicas". Neurología europea . 55 (1): 57–8. doi : 10.1159/000091431 . PMID 16479124.
- ^ Firth D (1948). El caso de August D'Esté . Cambridge: Cambridge University Press.
- ^ ab Pearce JM (2005). "Descripciones históricas de la esclerosis múltiple". Neurología europea . 54 (1): 49–53. doi : 10.1159/000087387 . PMID 16103678.
- ^ Barbellion WN (1919). El diario de un hombre desilusionado. Nueva York: George H. Doran. ISBN 0-7012-1906-8.
- ^ Petzold A (2013). "Neuritis óptica: otro diagnóstico dickensiano". Neuro-Oftalmología . 37 (6): 247–250. doi :10.3109/01658107.2013.830313. PMC 5291069 . PMID 28167994.
- ^ Bar-Or A, Pender MP, Khanna R, Steinman L, Hartung HP, Maniar T, et al. (marzo de 2020). "Virus de Epstein-Barr en esclerosis múltiple: teoría e inmunoterapias emergentes". Tendencias en medicina molecular . 26 (3): 296–310. doi :10.1016/j.molmed.2019.11.003. PMC 7106557 . PMID 31862243.
- ^ DeLorenze GN, Munger KL, Lennette ET, Orentreich N, Vogelman JH, Ascherio A (junio de 2006). "Virus de Epstein-Barr y esclerosis múltiple: evidencia de asociación a partir de un estudio prospectivo con seguimiento a largo plazo". Archivos de Neurología . 63 (6): 839–844. doi : 10.1001/archneur.63.6.noc50328 . PMID 16606758.
- ^ Hauser SL, Bar-Or A, Comi G, Giovannoni G, Hartung HP, Hemmer B, et al. (enero de 2017). "Ocrelizumab versus interferón beta-1a en esclerosis múltiple recurrente". The New England Journal of Medicine . 376 (3): 221–234. doi :10.1056/NEJMoa1601277. hdl : 2445/178507 . PMID 28002679. S2CID 205099904.
- ^ Lanz TV, Brewer RC, Ho PP, Moon JS, Jude KM, Fernandez D, et al. (marzo de 2022). "Las células B expandidas clonalmente en la esclerosis múltiple se unen a EBV EBNA1 y GlialCAM". Nature . 603 (7900): 321–327. Bibcode :2022Natur.603..321L. doi :10.1038/s41586-022-04432-7. PMC 9382663 . PMID 35073561.
- ^ Morandi E, Tanasescu R, Tarlinton RE, Constantinescu CS, Zhang W, Tench C, et al. (16 de febrero de 2017). Ruprecht K (ed.). "La asociación entre los retrovirus endógenos humanos y la esclerosis múltiple: una revisión sistemática y un metanálisis". PLOS ONE . 12 (2): e0172415. Bibcode :2017PLoSO..1272415M. doi : 10.1371/journal.pone.0172415 . PMC 5313176 . PMID 28207850.
- ^ Li Y, Fan T, Cui J (marzo de 2022). "Retrovirus endógenos humanos en enfermedades virales y terapia". Descubrimiento clínico y traslacional . 2 (1). doi : 10.1002/ctd2.38 . S2CID 247750447.
- ^ Rangel SC, da Silva MD, da Silva AL, Dos Santos JM, Neves LM, Pedrosa A, et al. (23 de noviembre de 2022). "Retrovirus endógenos humanos y la respuesta inflamatoria: un círculo vicioso asociado con la salud y la enfermedad". Frontiers in Immunology . 13 : 1057791. doi : 10.3389/fimmu.2022.1057791 . PMC 9744114 . PMID 36518758.
- ^ Yang C, Hao Z, Zhang L, Zeng L, Wen J (octubre de 2015). "Bloqueadores de los canales de sodio para la neuroprotección en la esclerosis múltiple". Base de datos Cochrane de revisiones sistemáticas . 2015 (10): CD010422. doi :10.1002/14651858.CD010422.pub2. PMC 9242538. PMID 26486929 .
- ^ ab Misu T, Fujihara K (febrero de 2019). "Espectro de la neuromielitis óptica y encefalomielitis diseminada relacionada con anticuerpos anti-glicoproteína de oligodendrocitos de mielina". Neuroinmunología clínica y experimental . 10 (1): 9–17. doi : 10.1111/cen3.12491 .
- ^ Kira JI, Yamasaki R, Ogata H (2019). "Autoanticuerpo anti-neurofascina y desmielinización". Neuroquímica Internacional . 130 : 104360. doi : 10.1016/j.neuint.2018.12.011 . PMID 30582947.
- ^ Popescu BF, Pirko I, Lucchinetti CF (agosto de 2013). "Patología de la esclerosis múltiple: ¿dónde nos encontramos?". Continuum . 19 (4 Multiple Sclerosis): 901–21. doi :10.1212/01.CON.0000433291.23091.65. PMC 3915566 . PMID 23917093.
- ^ Mehta V, Pei W, Yang G, Li S, Swamy E, Boster A, et al. (2013). "El hierro es un biomarcador sensible de la inflamación en las lesiones de esclerosis múltiple". PLOS ONE . 8 (3): e57573. Bibcode :2013PLoSO...857573M. doi : 10.1371/journal.pone.0057573 . PMC 3597727 . PMID 23516409.
- ^ Khalil M, Teunissen CE, Otto M, Piehl F, Sormani MP, Gattringer T, et al. (octubre de 2018). "Neurofilamentos como biomarcadores en trastornos neurológicos". Nature Reviews. Neurología . 14 (10): 577–589. doi :10.1038/s41582-018-0058-z. PMID 30171200.
- ^ Petzold A (junio de 2005). "Fosfoformas de neurofilamentos: marcadores sustitutos de lesión, degeneración y pérdida axonal". Revista de ciencias neurológicas . 233 (1–2): 183–98. doi :10.1016/j.jns.2005.03.015. PMID 15896809.
- ^ abcd Filippi M, Rocca MA, De Stefano N, Enzinger C, Fisher E, Horsfield MA, et al. (diciembre de 2011). "Técnicas de resonancia magnética en la esclerosis múltiple: el presente y el futuro". Archivos de Neurología . 68 (12): 1514–20. doi : 10.1001/archneurol.2011.914 . PMID 22159052.
- ^ Swanberg KM, Landheer K, Pitt D, Juchem C (2019). "Cuantificación de la firma metabólica de la esclerosis múltiple mediante espectroscopia de resonancia magnética de protones in vivo: desafíos actuales y perspectivas futuras en la traducción de la señal de protones a biomarcador de diagnóstico". Frontiers in Neurology . 10 : 1173. doi : 10.3389/fneur.2019.01173 . PMC 6876616 . PMID 31803127.
- ^ Moghadasi AN, Mirmosayyeb O, Barzegar M, Sahraian MA, Ghajarzadeh M (agosto de 2021). "La prevalencia de la infección por COVID-19 en pacientes con esclerosis múltiple (EM): una revisión sistemática y un metanálisis". Neurol Sci . 42 (8): 3093–3099. doi :10.1007/s10072-021-05373-1. PMC 8184129 . PMID 34100130.
- ^ Neumann B, Baror R, Zhao C, Segel M, Dietmann S, Rawji KS, et al. (octubre de 2019). "La metformina restaura la capacidad de remielinización del sistema nervioso central rejuveneciendo las células madre envejecidas". Cell Stem Cell . 25 (4): 473–485.e8. doi :10.1016/j.stem.2019.08.015. PMC 6863391 . PMID 31585093.
- ^ Gilbert EA, Livingston J, Flores EG, Khan M, Kandavel H, Morshead CM (enero de 2024). "El tratamiento con metformina reduce la inflamación, la desmielinización y la gravedad de la enfermedad en un modelo murino de esclerosis múltiple y encefalomielitis autoinmune experimental". Brain Research . 1822 : 148648. doi : 10.1016/j.brainres.2023.148648 . PMID 37890574.
- ^ "Nueva esperanza de tratamiento con el primer megaensayo mundial sobre EM que abre un centro en Irlanda del Norte". www.qub.ac.uk . 6 de junio de 2023 . Consultado el 30 de julio de 2024 .
- ^ De Keersmaecker AV, Van Doninck E, Popescu V, Willem L, Cambron M, Laureys G, et al. (21 de febrero de 2024). "Un estudio clínico de adición de metformina en esclerosis múltiple para evaluar la remielinización cerebral y la neurodegeneración (MACSiMiSE-BRAIN): protocolo de estudio para un ensayo clínico aleatorizado, controlado con placebo y multicéntrico". Frontiers in Immunology . 15 : 1362629. doi : 10.3389/fimmu.2024.1362629 . PMC 11046490 . PMID 38680485.
- ^ "¿Pueden la metformina y la clemastina reparar la mielina en personas con EM?". Sociedad de EM del Reino Unido . Consultado el 30 de julio de 2024 .
- ^ "Resultados visuales y neurocognitivos". Programa de Trastornos Neuroinflamatorios Pediátricos . Consultado el 30 de julio de 2024 .
- ^ "Metformina". Sociedad de Esclerosis Múltiple .
- ^ Wasko NJ, Nichols F, Clark RB (enero de 2020). "Esclerosis múltiple, el microbioma, TLR2 y la hipótesis de la higiene". Autoimmunity Reviews . 19 (1): 102430. doi : 10.1016/j.autrev.2019.102430 . PMID 31734400.
- ^ Aranow C (agosto de 2011). "Vitamina D y el sistema inmunológico". Revista de Medicina Investigativa . 59 (6): 881–886. doi :10.2310/jim.0b013e31821b8755. PMC 3166406 . PMID 21527855.
- ^ Tada T, Takemori T, Okumura K, Nonaka M, Tokuhisa T (febrero de 1978). "Dos tipos distintos de células T colaboradoras implicadas en la respuesta de anticuerpos secundarios: efectos independientes y sinérgicos de las células T colaboradoras Ia- e Ia+". The Journal of Experimental Medicine . 147 (2): 446–458. doi :10.1084/jem.147.2.446. PMC 2184496 . PMID 415110.
- ^ Lassmann H (marzo de 2018). "Patología de la esclerosis múltiple". Cold Spring Harbor Perspectives in Medicine . 8 (3): a028936. doi :10.1101/cshperspect.a028936. PMC 5830904 . PMID 29358320.
- ^ Minagar A, Shapshak P, Alexander JS (28 de diciembre de 2004). "Patogénesis de la demencia asociada al VIH y la esclerosis múltiple: papel de la microglia y los astrocitos". En Aschner M, Costa LG (eds.). El papel de la glía en la neurotoxicidad (2.ª ed.). CRC Press. págs. 283–298. doi :10.1201/9781420039740-21. ISBN 978-0-429-12860-8.
- ^ Allentoft ME, Sikora M, Refoyo-Martínez A, Irving-Pease EK, Fischer A, Barrie W, et al. (11 de enero de 2024). "Genómica de poblaciones de Eurasia occidental postglacial". Nature . 625 (7994): 301–311. Bibcode :2024Natur.625..301A. doi : 10.1038/s41586-023-06865-0 . PMC 10781627 . PMID 38200295.
- ^ Johnson CY (10 de enero de 2024). «El ADN antiguo ayuda a rastrear los orígenes de la esclerosis múltiple en los descendientes europeos». Washington Post . Consultado el 11 de enero de 2024 .
- ^ Roxby P (10 de enero de 2024). "Los científicos descifran el misterio de cómo se propaga el gen de la esclerosis múltiple". BBC News . Consultado el 11 de enero de 2024 .
- ^ Barrie W, Yang Y, Irving-Pease E, Attfield KE, Scorrano G, Jensen LT, et al. (6 de octubre de 2023). "El riesgo genético elevado de esclerosis múltiple se originó en poblaciones de pastores esteparios". bioRxiv 10.1101/2023.10.06.561165 .
Nuestros hallazgos también respaldan la interpretación de una mayor presión patógena como impulsor de la selección positiva de variantes inmunogenéticas asociadas con el riesgo de esclerosis múltiple, una enfermedad autoinmune, en poblaciones esteparias hace unos 5000 años[59]
- ^ "Un nuevo estudio sugiere que la esclerosis múltiple llegó al norte de Europa hace 5000 años". Sociedad Nacional de Esclerosis Múltiple . 10 de enero de 2024.




