GJA1
| GJA1 | |||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| Identificadores | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Alias | GJA1 , AVSD3, CMDR, CX43, EKVP, GJAL, HLHS1, HSS, ODDD, PPKCA, proteína de unión estrecha alfa 1, EKVP3 | ||||||||||||||||||||||||||||||||||||||||||||||||||
| Identificaciones externas | OMIM : 121014; MGI : 95713; HomoloGene : 136; Tarjetas genéticas : GJA1; OMA :GJA1 - ortólogos | ||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| Wikidatos | |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| Conexina43 | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 dominio carboxilo terminal de la conexina 43 | |||||||||
| Identificadores | |||||||||
| Símbolo | Conexina43 | ||||||||
| Pfam | PF03508 | ||||||||
| Interprofesional | IPR013124 | ||||||||
| Base de datos de datos termodinámica | 1.A.24 | ||||||||
| |||||||||
La proteína de unión en hendidura alfa-1 ( GJA1 ), también conocida como conexina 43 ( Cx43 ), es una proteína que en los humanos está codificada por el gen GJA1 en el cromosoma 6. [5] [6] [7] Como conexina , GJA1 es un componente de las uniones en hendidura , que permiten la comunicación intercelular de unión en hendidura (GJIC) entre células para regular la muerte celular , la proliferación y la diferenciación . [8] Como resultado de su función, GJA1 está implicada en muchos procesos biológicos, incluida la contracción muscular , el desarrollo embrionario , la inflamación y la espermatogénesis , así como en enfermedades , incluida la displasia oculodentodigital (ODDD), malformaciones cardíacas y cánceres . [7] [9] [10]
Estructura
GJA1 es una proteína de 43,0 kDa compuesta por 382 aminoácidos . [11] GJA1 contiene una larga cola C-terminal , un dominio N-terminal y múltiples dominios transmembrana . La proteína pasa a través de la bicapa de fosfolípidos cuatro veces, dejando sus terminales C y N expuestas al citoplasma . [12] La cola C-terminal está compuesta por 50 aminoácidos e incluye sitios de modificación postraduccional , así como sitios de unión para factores de transcripción , elementos del citoesqueleto y otras proteínas. [12] [13] Como resultado, la cola C-terminal es fundamental para funciones como la regulación de la compuerta de pH y el ensamblaje del canal. En particular, la región de ADN del gen GJA1 que codifica esta cola está altamente conservada, lo que indica que es resistente a las mutaciones o se vuelve letal cuando muta. Mientras tanto, el dominio N-terminal está involucrado en la compuerta y oligomerización del canal y, por lo tanto, puede controlar el cambio entre los estados abierto y cerrado del canal. Los dominios transmembrana forman el canal de unión en hendidura, mientras que los bucles extracelulares facilitan el acoplamiento adecuado del canal. Además, dos bucles extracelulares forman enlaces disulfuro que interactúan con dos hexámeros para formar un canal de unión en hendidura completo. [12]
El sitio de entrada interna al ribosoma de la conexina-43 es un elemento del ARN presente en el extremo 5' UTR del ARNm de GJA1. Este sitio de entrada interna al ribosoma (IRES) permite la traducción independiente de la tapa durante condiciones como el choque térmico y el estrés. [14]
| Sitio de entrada interna al ribosoma (IRES) de la conexina-43 | |
|---|---|
 Estructura secundaria prevista y conservación de secuencia de IRES_Cx43 | |
| Identificadores | |
| Símbolo | IRES_Cx43 |
| RFAM | RF00487 |
| Otros datos | |
| Tipo de ARN | Cis-reg ; IRES |
| Dominio(s) | Eucariota |
| IR | IR:0043022 |
| ENTONCES | SO:0000243 |
| Estructuras del PDB | PDBe |
Función
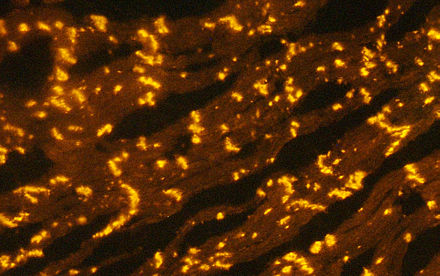
Como miembro de la familia de las conexinas , GJA1 es un componente de las uniones estrechas , que son canales intercelulares que conectan células adyacentes para permitir el intercambio de moléculas de bajo peso molecular, como iones pequeños y mensajeros secundarios , para mantener la homeostasis . [7] [12] [15]
GJA1 es la conexina expresada de forma más ubicua y se detecta en la mayoría de los tipos de células. [7] [9] [12] Es la proteína principal en las uniones estrechas del corazón y se supone que desempeña un papel crucial en la contracción sincronizada del corazón. [7] A pesar de su papel clave en el corazón y otros órganos vitales, GJA1 tiene una vida media corta (solo dos a cuatro horas), lo que indica que la proteína sufre una renovación diaria en el corazón y puede ser muy abundante o compensarse con otras conexinas. [12] GJA1 también está muy involucrado en el desarrollo embrionario . [7] [8] Por ejemplo, se observó que el factor de crecimiento transformante beta 1 (TGF-β1) induce la expresión de GJA1 a través de las vías de señalización Smad y ERK1 /2 , lo que resulta en la diferenciación de células del trofoblasto en la placenta . [8]
Además, GJA1 se expresa en muchas células inmunes , como los eosinófilos y las células T , donde su función de unión en hendidura promueve la maduración y activación de estas células y, por extensión, la comunicación cruzada necesaria para generar una respuesta inflamatoria . [10] También se ha demostrado que los macrófagos uterinos se acoplan físicamente directamente con los miocitos uterinos a través de GJA1, transfiriendo Ca²⁺ , para promover la contracción y excitación del músculo uterino durante el inicio del parto humano . [16]
Además, GJA1 se puede encontrar en las células de Leydig y los túbulos seminíferos entre las células de Sertoli y las espermatogonias o espermatocitos primarios , donde desempeña un papel clave en la espermatogénesis y el desarrollo de los testículos a través del control de las proteínas de unión estrecha en la barrera hemato-testicular .
Si bien es una proteína de canal, GJA1 también puede realizar funciones independientes del canal. En el citoplasma , la proteína regula la red de microtúbulos y, por extensión, la migración y polaridad celular . [9] [13] Esta función se ha observado en el desarrollo del cerebro y el corazón, así como en la cicatrización de heridas en las células endoteliales . [13] También se ha observado que GJA1 se localiza en las mitocondrias, donde promueve la supervivencia celular al regular a la baja la vía apoptótica intrínseca durante condiciones de estrés oxidativo. [15]
Importancia clínica
Las mutaciones en este gen se han asociado con ODDD ; displasia craneometafisaria ; síndrome de muerte súbita del lactante , que está vinculado a arritmia cardíaca ; síndrome de Hallermann-Streiff ; y malformaciones cardíacas, como heterotaxia víscero-atrial . [7] [9] [12] [17] También ha habido algunos casos de pérdida auditiva y trastornos de la piel no relacionados con ODDD. [12] En última instancia, GJA1 tiene baja tolerancia a las desviaciones de su secuencia original, con mutaciones que resultan en pérdida o ganancia de la función del canal que conducen a fenotipos de enfermedad. [12] Sin embargo, es paradójico que los pacientes con una variedad de mutaciones somáticas en GJA1 con mayor frecuencia no presenten arritmias cardíacas , a pesar de que la conexina-43 es la proteína más abundante que forma poros de unión en hendidura en los cardiomiocitos y es esencial para la propagación normal del potencial de acción . [18]
En particular, la expresión de GJA1 se ha asociado con una amplia variedad de cánceres, incluidos el carcinoma nasofaríngeo , el meningioma , el hemangiopericitoma , el tumor de hígado , el cáncer de colon , el cáncer de esófago , el cáncer de mama , el mesotelioma , el glioblastoma , el cáncer de pulmón , los tumores adrenocorticales , el cáncer de células renales , el carcinoma de cuello uterino , el carcinoma de ovario , el carcinoma de endometrio , el cáncer de próstata , el carcinoma de tiroides y el cáncer testicular . [9] Se pensaba que su papel en el control de la motilidad y la polaridad celular contribuía al desarrollo del cáncer y la metástasis , aunque su papel como proteína de unión en hendidura también puede estar involucrado. [9] [15] Además, los efectos citoprotectores de esta proteína pueden promover la supervivencia de las células tumorales en los tratamientos de radioterapia , mientras que silenciar su gen aumenta la radiosensibilidad. Como resultado, GJA1 puede servir como objetivo para mejorar el éxito del tratamiento radioterapéutico del cáncer. [15] Como biomarcador, GJA1 también podría utilizarse para evaluar el riesgo de cáncer de testículo en varones jóvenes. [9]
La hormona tiroidea triyodotironina (T3) regula a la baja la expresión de GJA1. Se supone que este es un mecanismo clave por el que la velocidad de conducción en el tejido miocárdico se reduce en la tirotoxicosis , lo que promueve la arritmia cardíaca . [19]
Actualmente, solo el rotigaptide , un fármaco basado en péptidos antiarrítmicos, y sus derivados , como el danegaptide, han llegado a ensayos clínicos para tratar patologías cardíacas mediante la mejora de la expresión de GJA1. Alternativamente, los fármacos podrían dirigirse a las conexinas complementarias, como Cx40 , que funcionan de manera similar a GJA1. Sin embargo, ambos enfoques aún requieren un sistema para dirigirse al tejido enfermo para evitar inducir anomalías del desarrollo en otras partes. [12] Por lo tanto, un enfoque más eficaz implica diseñar un miRNA a través de oligonucleótidos antisentido , transfección o infección para inhibir solo el ARNm de GJA1 mutante, permitiendo así la expresión de GJA1 de tipo salvaje y conservando el fenotipo normal . [9] [12]
Interacciones
Se ha demostrado que la proteína de unión estrecha alfa 1 interactúa con:
- Cx37 , [12]
- Cx40 , [12]
- Cx45 , [12]
- MAPK7 , [20]
- Caveolina 1 , [21]
- Proteína de unión estrecha 1 [22]
- CSNK1D , [23] y
- PTPmu ( PTPRM ). [24]
Véase también
Referencias
- ^ abc GRCh38: Lanzamiento de Ensembl 89: ENSG00000152661 – Ensembl , mayo de 2017
- ^ abc GRCm38: Lanzamiento de Ensembl 89: ENSMUSG00000050953 – Ensembl , mayo de 2017
- ^ "Referencia de PubMed humana:". Centro Nacional de Información Biotecnológica, Biblioteca Nacional de Medicina de EE. UU .
- ^ "Referencia PubMed de ratón:". Centro Nacional de Información Biotecnológica, Biblioteca Nacional de Medicina de EE. UU . .
- ^ Boyadjiev SA, Jabs EW, LaBuda M, Jamal JE, Torbergsen T, Ptácek LJ, Rogers RC, Nyberg-Hansen R, Opjordsmoen S, Zeller CB, Stine OC, Stalker HJ, Zori RT, Shapiro RE (mayo de 1999). "El análisis de ligamiento limita la región crítica para la displasia oculodentodigital al cromosoma 6q22-q23". Genómica . 58 (1): 34–40. doi :10.1006/geno.1999.5814. PMID 10331943.
- ^ Fishman GI, Eddy RL, Shows TB, Rosenthal L, Leinwand LA (mayo de 1991). "La familia de genes de conexina humana de proteínas de unión en hendidura: ubicaciones cromosómicas distintas pero estructuras similares". Genomics . 10 (1): 250–256. doi :10.1016/0888-7543(91)90507-B. PMID 1646158.
- ^ abcdefg "Entrez Gene: proteína de unión gap GJA1, alfa 1, 43 kDa".
- ^ abc Cheng JC, Chang HM, Fang L, Sun YP, Leung PC (julio de 2015). "TGF-β1 regula positivamente la expresión de conexina 43: un mecanismo potencial para la diferenciación de células del trofoblasto humano". Journal of Cellular Physiology . 230 (7): 1558–1566. doi :10.1002/jcp.24902. PMID 25560303. S2CID 28968035.
- ^ abcdefgh Chevallier D, Carette D, Segretain D, Gilleron J, Pointis G (abril de 2013). "Conexina 43, un componente de punto de control de la proliferación celular implicado en una amplia gama de enfermedades de los testículos humanos". Ciencias de la vida celular y molecular . 70 (7): 1207–1220. doi :10.1007/s00018-012-1121-3. PMC 11113700 . PMID 22918484. S2CID 11855947.
- ^ ab Vliagoftis H, Ebeling C, Ilarraza R, Mahmudi-Azer S, Abel M, Adamko D, Befus AD, Moqbel R (2014). "Expresión de conexina 43 en eosinófilos de sangre periférica: papel de las uniones en hendidura en la migración transendotelial". BioMed Research International . 2014 : 803257. doi : 10.1155/2014/803257 . PMC 4109672 . PMID 25110696.
- ^ "Secuencia de proteína de GJA1 humana (Uniprot ID: P17302)". Base de conocimiento del Atlas de proteínas organelares cardíacas (COPaKB) . Archivado desde el original el 5 de octubre de 2015. Consultado el 18 de septiembre de 2015 .
- ^ abcdefghijklmn Laird DW (abril de 2014). "Mutaciones sindrómicas y no sindrómicas de Cx43 vinculadas a enfermedades". FEBS Letters . 588 (8): 1339–1348. doi : 10.1016/j.febslet.2013.12.022 . PMID 24434540. S2CID 20651016.
- ^ abc Kameritsch P, Pogoda K, Pohl U (agosto de 2012). "Influencia independiente del canal de la conexina 43 en la migración celular". Biochimica et Biophysica Acta (BBA) - Biomembranas . 1818 (8): 1993–2001. doi : 10.1016/j.bbamem.2011.11.016 . PMID 22155212.
- ^ Schiavi A, Hudder A, Werner R (diciembre de 1999). "El ARNm de conexina 43 contiene un sitio de entrada interno funcional al ribosoma". FEBS Letters . 464 (3): 118–122. doi : 10.1016/S0014-5793(99)01699-3 . PMID 10618489. S2CID 26020820.
- ^ abcd Ghosh S, Kumar A, Chandna S (julio de 2015). "La regulación negativa de la conexina-43 en las células tumorales enriquecidas en la fase G2/M provoca una hiperradiosensibilidad (HRS) extensa a dosis bajas asociada con eventos apoptóticos mitocondriales". Cancer Letters . 363 (1): 46–59. doi :10.1016/j.canlet.2015.03.046. PMID 25843295.
- ^ Boros-Rausch, A., Shynlova, O. y Lye, SJ (2021). "Un inhibidor de quimiocinas de amplio espectro bloquea la comunicación entre miocitos y macrófagos del miometrio inducida por la inflamación y la contracción del miometrio". Cells . 11 (1): 128. doi: 10.3390/cells11010128 PMID 35011690
- ^ Pizzuti A, Flex E, Mingarelli R, Salpietro C, Zelante L, Dallapiccola B (marzo de 2004). "Una mutación homocigótica del gen GJA1 provoca un fenotipo del espectro Hallermann-Streiff/ODDD". Mutación humana . 23 (3): 286. doi : 10.1002/humu.9220 . PMID 14974090. S2CID 13345970.
- ^ Delmar M, Makita N (mayo de 2012). "Conexinas cardíacas, mutaciones y arritmias". Current Opinion in Cardiology . 27 (3): 236–241. doi :10.1097/HCO.0b013e328352220e. PMID 22382502. S2CID 205620477.
- ^ Müller P, Leow MK, Dietrich JW (2022). "Pequeñas perturbaciones de la homeostasis tiroidea y principales criterios de valoración cardiovasculares: mecanismos fisiológicos y evidencia clínica". Frontiers in Cardiovascular Medicine . 9 : 942971. doi : 10.3389/fcvm.2022.942971 . PMC 9420854 . PMID 36046184.
- ^ Cameron SJ, Malik S, Akaike M, Lerner-Marmarosh N, Yan C, Lee JD, Abe J, Yang J (mayo de 2003). "Regulación de la comunicación de la unión gap de la conexina 43 inducida por el factor de crecimiento epidérmico por la proteína quinasa 1/ERK5 activada por mitógenos grandes pero no por la activación de la quinasa ERK1/2". The Journal of Biological Chemistry . 278 (20): 18682–18688. doi : 10.1074/jbc.M213283200 . PMID 12637502.
- ^ Schubert AL, Schubert W, Spray DC, Lisanti MP (mayo de 2002). "Los miembros de la familia de las conexinas se dirigen a los dominios de las balsas lipídicas e interactúan con la caveolina-1". Biochemistry . 41 (18): 5754–5764. doi :10.1021/bi0121656. PMID 11980479.
- ^ Giepmans BN, Moolenaar WH (1998). "La proteína de unión en hendidura conexina43 interactúa con el segundo dominio PDZ de la proteína de la zona occludens-1". Current Biology . 8 (16): 931–934. Bibcode :1998CBio....8..931G. doi : 10.1016/S0960-9822(07)00375-2 . PMID 9707407. S2CID 6434044.
- ^ Cooper CD, Lampe PD (noviembre de 2002). "La caseína quinasa 1 regula el ensamblaje de la unión gap de la conexina-43". The Journal of Biological Chemistry . 277 (47): 44962–44968. doi : 10.1074/jbc.M209427200 . PMID 12270943.
- ^ Giepmans BN, Feiken E, Gebbink MF, Moolenaar WH (2003). "Asociación de la conexina 43 con un receptor de proteína tirosina fosfatasa". Comunicación celular y adhesión . 10 (4–6): 201–205. doi : 10.1080/cac.10.4-6.201.205 . PMID 14681016.
Lectura adicional
- Harris AL, Locke D (2009). Conexinas, una guía. Nueva York: Springer. pág. 574. ISBN 978-1-934115-46-6.
- Saffitz JE, Laing JG, Yamada KA (abril de 2000). "Expresión y recambio de conexinas: implicaciones para la excitabilidad cardíaca". Circulation Research . 86 (7): 723–728. doi : 10.1161/01.res.86.7.723 . PMID 10764404.
Enlaces externos
- Página del sitio de entrada interna al ribosoma (IRES) de la conexina-43 en Rfam






