Fosfato de amonio
 | |
 | |
| Nombres | |
|---|---|
| Nombre IUPAC fosfato de amonio | |
| Otros nombres fosfato de triamonio | |
| Identificadores | |
Modelo 3D ( JSmol ) |
|
| Araña química | |
| Tarjeta informativa de la ECHA | 100.030.709 |
| Número CE |
|
Identificador de centro de PubChem |
|
| UNIVERSIDAD | |
Panel de control CompTox ( EPA ) |
|
| |
| |
| Propiedades | |
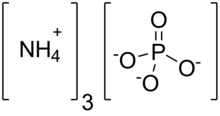
| ( NH4 ) 3PO4 | |
| Masa molar | 149,09 g/mol |
| Apariencia | Cristales tetraédricos blancos. |
| 58,0 g/100 ml (25 °C) | |
| Solubilidad | Insoluble en acetona [2] |
| Peligros | |
| Etiquetado SGA : | |
 | |
| Advertencia | |
| H302 , H319 | |
| P264 , P270 , P280 , P301+P312 , P305+P351+P338 , P330 , P337+P313 , P501 | |
| NFPA 704 (rombo cortafuegos) | |
| Termoquímica | |
Entalpía estándar de formación (Δ f H ⦵ 298 ) | −1671,9 kJ/mol |
| Compuestos relacionados | |
Otros cationes | Fosfato trisódico Fosfato tripotásico |
Compuestos relacionados | Fosfato diamónico Fosfato monoamónico |
Salvo que se indique lo contrario, los datos se proporcionan para los materiales en su estado estándar (a 25 °C [77 °F], 100 kPa). | |
El fosfato de amonio es un compuesto inorgánico con la fórmula (NH 4 ) 3 PO 4 . Es la sal de amonio del ácido ortofosfórico. Una "sal doble" relacionada, (NH 4 ) 3 PO 4 . (NH 4 ) 2 HPO 4 también se reconoce, pero su uso es poco práctico. Ambas sales de triamonio liberan amoníaco. En contraste con la naturaleza inestable de las sales de triamonio, el fosfato de diamonio (NH 4 ) 2 HPO 4 y la sal monoamónica (NH 4 )H 2 PO 4 son materiales estables que se utilizan comúnmente como fertilizantes para proporcionar a las plantas nitrógeno y fósforo fijos. [3]
Preparación de fosfato de triamonio
El fosfato de triamonio se puede preparar en el laboratorio tratando ácido fosfórico al 85% con solución de amoníaco al 30%: [ cita requerida ]
- H 3 PO 4 + 3 NH 3 → (NH 4 ) 3 PO 4
El (NH 4 ) 3 PO 4 es un sólido cristalino incoloro. El sólido, que tiene olor a amoníaco, es fácilmente soluble en agua. La sal se convierte en fosfato de hidrógeno diamónico (NH 4 ) 2 HPO 4 .
Véase también
Referencias
- ^ Lide, David R. (1998). Manual de química y física (87.ª ed.). Boca Raton, Florida: CRC Press. pp. 4–42, 5–19. ISBN 978-0-8493-0594-8.
- ^ John Rumble (18 de junio de 2018). Manual de química y física del CRC (99.ª edición). CRC Press. págs. 4–41. ISBN 978-1138561632.
- ^ Schrödter, Klaus; Bettermann, Gerhard; Staffel, Thomas; Wahl, Friedrich; Klein, Thomas; Hofmann, Thomas (2008). "Ácido fosfórico y fosfatos". Enciclopedia de química industrial de Ullmann . Weinheim: Wiley-VCH. doi :10.1002/14356007.a19_465.pub3. ISBN 978-3527306732.




